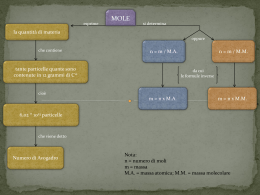
Facoltà di Ingegneria – Università degli Studi di Siena Laurea Magistrale in “Ingegneria Gestionale” Corso di Gestione dei Servizi e delle Tecnologie Ambientali (GS&TA) Parte 14 – Metodi di trattamento delle correnti gassose. Rimozione delle particelle solide e degli inquinanti gassosi Prof. Ing. Andrea Corti ([email protected]) Metodi di rimozione del particolato Geometria delle particelle Aerosol e polveri si trovano in atmosfera sia per effetti naturali che per effetto delle attività antropiche. Le caratteristiche che principalmente ne identificano il comportamento e l’effetto sulla salute sono: . la composizione . la forma . la concentrazione . la densità . la composizione granulometrica . la corrosività . la reattività . la tossicità In particolare, la composizione granulometrica è di importanza fondamentale per due motivi: - le particelle in grado di penetrare nelle parti più interne dell’apparato respiratorio – e quindi di causare i maggiori danni clinici – sono contenute nel range dimensionale 0,5-2 µm (diametro equivalente) - i fenomeni che sovrintendono al moto delle particelle in flusso gassoso sono fortemente influenzati dalla dimensione delle stesse e pertanto sia le trattazioni teoriche che le tecniche di depurazione utilizzate dipenderanno direttamente dal diametro equivalente delle particelle E’ fondamentale perciò conoscere la distribuzione dimensionale delle particelle, cioè la frazione percentuale relativa ad ogni intervallo dimensionale (curva granulometrica cumulata) 2 Caratteristiche delle particelle 3 Metodi di rimozione del particolato Geometria delle particelle – Diametro equivalente Il Diametro equivalente è definito per mezzo della sfera di volume pari alla particella: V= π 6 1/ 3 D 3 s 6V D = π s Il Diametro Medio DM è quello per il quale il 50% di particelle ha diametro minore di DM. Fattore di sfericità: λ = A/As As = πDs2 λ =1 part. Sferiche λ>1 in genere 4 Metodi di rimozione del particolato Rappresentazione della granulometria Esempio: curva cumulata di distribuzione delle dimensioni di particelle solide 120% 100% 80% 60% 40% 20% 0% 0 20 40 60 80 100 120 140 -20% µm Altre definizioni di diametro medio Il Diametro Medio di Sauter è molto più utilizzato: DaS = 1/(Σ Σixi/Di) Dove xi é la frazione in massa di particelle di diametro Di. Il Diametro Medio aritmetico è Dam = ΣD/N. Più che d una distribuzione normale, si fa spesso riferimento alla log-normale che esclude le particelle di dimensione negativa. 5 Efficienza di rimozione del particolato M& i − M& e L&i − L&e η= = M& i L& i M& i = portata particolato in ingresso M& e = portata particolato in uscita L& = concentrazione particolato in ingresso i L&e = concentrazione particolato in uscita Quando l’efficienza di rimozione è data in funzione della dimensione delle particelle, l’efficienza complessiva di rimozione del particolato è data da: η = ∑η j m j η j = efficienza di rimozione per il range dimensionale j − esimo m j = frazione in massa delle paerticelle nel range dimensionale j − esimo 6 Metodi di rimozione del particolato - Efficienza L’efficienza di raccolta di un dispositivo di rimozione del particolato è pari a: massa particelle rimosse ep = = 50 ÷ 99% massa di particelle originariamente presenti Semplici dispositivi meccanici Precipitatori elettrostatici o filtri a manica 7 Dispositivi di separazione meccanica I metodi meccanici che consentono la raccolta del particolato si fondano su uno o più dei seguenti effetti: - rallentamento brusco - brusco cambio di direzione ep < 75% - urto su piatti o lamelle - forza centrifuga Spesso impiegati nei generatori di vapore a combustibile solido 8 Cicloni E’ possibile sottoporre il gas ad un moto circolare. Tale meccanismo si realizza nei cicloni, che sono dispositivi inerziali di separazione che sono dotati di un campo centrifugo generato da una velocità tangenziale ut impressa in ingresso al gas. Le particelle, in virtù del moto tangenziale, assumono una componente radiale di deposizione ur che dipende dal diametro delle particelle e dalla loro densità. ρ − ρ 2 s D p ut = u r 18 µ r 2 9 Cicloni Le particelle grandi migrano rapidamente verso raggi elevati; impattano sulle superfici laterali e perdendo la loro energia cinetica cadono sul fondo per gravità. r2 r1 Le particelle piccole migrano + lentamente, e non é detto che nel tempo di residenza all’interno del ciclone raggiungano le pareti laterali; in tali condizioni possono essere facilmente catturate dal flusso secondario e trascinate dalla corrente gassosa. In particolare esiste un diametro critico – determinato dalla dimensione r2 della bocca di uscita - al di sotto del quale praticamente le particelle restano nella corrente di gas in uscita. 10 uz2 Cicloni PERDITE DI PRESSIONE r r1 L ut1 I cicloni presentano una perdita di carico complessiva rilevante: ∆p = ½ ρut12(r1/r2- ½) + ½ ρuz22 11 Cicloni I separatori a ciclone hanno più alte efficienze (ep ≈ 85%) Sono apparecchi molto semplici, senza alcun organo in movimento e costruibili con qualunque materiale. Sono costituiti da un corpo cilindrico con fondo tronco-conico che funge da tramoggia. Un cilindro di diametro minore esce dall’alto del ciclone, con la funzione di estrarre il gas depolverato. Il gas viene alimentato tangenzialmente nella parte superiore del ciclone, ad una velocità superiore ai 15 m/s. Le particelle solide sono spinte radialmente sulla parete del cilindro esterno dalla forza centrifuga, perdono la loro energia cinetica e cadono sul fondo per gravità, dove sono scaricate in una tramoggia. Questi cicloni sono noti come cicloni a grande diametro e presentano efficienze accettabili solo su particelle maggiori di 10 µm. 12 Cicloni L’efficienza di separazione dipende da diversi parametri, in particolare l’efficienza aumenta quando: - aumenta la dimensione delle particelle - aumenta la velocità del gas - aumenta la densità delle particelle - aumenta la portata di solido - diminuisce la viscosità dell’aria - diminuisce la superficie specifica delle particelle 13 Cicloni I cicloni, basando la loro efficienza sulla velocità di rotazione dei gas, risentono notevolmente delle variazioni della portata e dovrebbero essere installati solo su flussi a portata del gas costante. Per far fronte a questo inconveniente e mantenere costante la velocità di ingresso del gas nel ciclone, si ricorre al montaggio di deflettori a farfalla che variano la sezione di ingresso e di conseguenza regolano la velocità del gas. Per aumentare l’efficienza di separazione (90%), soprattutto su particelle fini, è possibile utilizzare i cicloni con spruzzatori di acqua all’interno. La dimensione delle gocce è una variabile che influenza l’efficienza della depolverazione. Svantaggi: raffreddamento gas, perdite di carico, corrosione 14 Cicloni Nei cicloni a piccolo diametro l’introduzione del gas viene fatta assialmente ed il moto circolare viene impresso da un gruppo di palette disposte nella parte superiore. Il diametro di questi cicloni è solitamente inferiore ai 250 mm e l’efficienza risulta un poco superiore a quella del ciclone semplice a grande diametro. Il vantaggio di questo ciclone è di poter facilmente essere assemblato in batterie che contengono molte unità (multicicloni) 15 Cicloni Diametro Ciclone particelle convenzionale (µ m) <5 <50 5-20 50-80 15-50 80-95 >40 95-99 Ciclone alta efficienza 50-80 80-95 95-99 95-99 16 Precipitatori elettrostatici Un precipitatore elettrostatico (Electrostatic Precipitator ESP) è costituito da fili ad alta tensione (30-60 kV) sospesi nel canale di scarico dei gas, tra piatti metallici paralleli posti a massa. Nel processo di elettrofiltrazione le particelle di polvere vengono dapprima caricate elettricamente (positive) per collisione da ioni prodotti da un elettrodo ad alta tensione (filo sospeso) e successivamente attratte dall’elettrodo passivo (negativo) sul quale si depositano (piatto). Dall’elettrodo passivo il deposito è rimosso, per mezzo di un raschiatore metallico, con frequenza prefissata e raccolto nella tramoggia di fondo. Il sistema presenta un’elevata efficienza di raccolta anche su particelle fini (ep> 99%). 17 Precipitatori elettrostatici VANTAGGI: - elevata efficienza di rimozione anche su particelle fini (> 99%) - ridotta perdita di carico del gas: la velocità di attraversamento del gas nel precipitatore è infatti molto ridotta (sempre < 5 m/s) e le perdite di carico aggiuntive sono trascurabili. - passaggio di corrente (quindi l’energia spesa nel trattamento) è circa proporzionale al flusso di solido separato e non alla portata di gas: quindi è un sistema adatto al trattamento di grosse portate di gas - possibilità di operare con temperature relativamente elevate (fino a circa 650 °C) PROBLEMI: - necessità assoluta di prevenzione della possibilità di presenza nei fumi di composti incombusti (archi elettrici si verificano normalmente nei precipitatori) - scarsa efficienza se usati con combustibili a basso tenore di zolfo, che producono ceneri ad alta resistività elettrica (>1010 ohm·cm.). Iniezione SO3 (10 ÷ 20 ppm) nei gas di scarico, con recupero quasi totale nell’ESP. - costo elevato La velocità di migrazione delle particelle verso i piatti raccolta aumenta proporzionalmente alla potenza elettrica applicata, perciò l’efficienza aumenta come mostrati in figura. Anche l’incremento della differenza di potenziale (DDP) agli elettrodi porta ad un incremento dell’efficienza di rimozione. 18 Precipitatori elettrostatici – Elementi di dimensionamento η = 1− e ( − wA / Q ) η = efficienza di cattura dimensionale A = area di cattura complessiva [m 2 ] Q = portata volumetrica di gas [m 3 / min] w = velocità di drift (velocità terminale in direzione y) [m/min] VELOCITA’ DI DRIFT La velocità di drift può essere calcolata in modo simile alla velocità di deposizione in un campo gravitazionale. Comunque si possono ottenere espressioni per la velocità di drift che sono accurate per casi di particelle sferiche, soggette a portate di gas costanti e campo elettrico costante. L’effetto di particelle con forme diverse, le variazioni nel campo elettrico, la non uniformità di distribuzione della portata di gas, e la risospensione fanno sì che la velocità di drift calcolata teoricamente non sia affidabile per il dimensionamento degli ESP. Nella pratica quindi la velocità di drift viene valutata per mezzo di studi pilota o da precedenti esperienze. L’espressione della efficienza di rimozione riportata può essere utlizzata per un primo dimensionamento, anche se i produttori di ESP hanno modelli proprietari più dettagliati per il dimensionamento finale. 19 Precipitatori elettrostatici – Resistività delle particelle Le particelle che arrivano sulla superficie dei piatti vi rimangono grazie alle forze adesiva, coesiva ed elettrica, che devono essere tali da prevenire la risospensione delle particelle nella corrente gassosa. La proprietà che risulta estremamente importante per il funzionamento del precipitatore elettrostatico è la resistività elettrica dello strato di polvere depositato sui piatti, proprio al fine di evitare la risospensione delle particelle. La resistività delle polveri comunemente rimosse in processi industriali può variare, a causa della varietà dei processi stessi, da 10-3 a 1014 ohm·cm. Quando la resistività è inferiore a 104 ohm·cm si ha un rapido movimento di carica dalla polvere al piatto di raccolta, lasciando le particelle depositate sul piatto con una bassa carica, insufficiente a mantenerle insieme ed ad impedire la risospensione. Questo può portare ad una sensibile riduzione dell’efficienza di rimozione. Dall’altro lato, una resistività superiore a 1010 ohm·cm, può creare problemi legati all’effetto di isolamento che lo strato di polvere ad alta resistività sul piatto di raccolta può provocare, riducendo la differenza di potenziale che si instaura e quindi l’efficienza di rimozione. Il range di resistività per le polveri che possono essere efficacemente raccolte da un ESP si trova quindi fra 104 a 1010 ohm·cm, quindi è spesso necessario modificare la resistività delle particelle a monte del trattamento. Temperatura ed umidità possono influenzare largamente la resistività. Un altro modo per modificare la resistività è l’aggiunta di agenti esterni, come SO3 o NH3, che adsorbiti sulle particelle, ne riducono la resistività. Effetto di temperatura ed umidità sulla resistività di polveri dell’industria del cemento: in generale ad aumentare dell’umidità la resistività diminuisce, mostrando un valore massimo rispetto alla 20 temperatura Precipitatori elettrostatici – Resistività delle particelle Effetto del condizionamento di fly ash per iniezione di H2SO4 (a) e SO3 (b) nei gas di scarico. Variazione della resistività di fly ash rispetto al contenuto di zolfo del carbone. L’aggiunta o la presenza di zolfo riduce effettivamente la resistività delle particelle. E’ pratica comune quindi aggiungere SO3 per ridurre la resistività di certe polveri ed aumentarne l’efficienza di rimozione. Le emissioni di SOx non ne risentono, in quanto l’SO3 viene adsorbito sulle particelle solide e con esse rimosso. 21 Precipitatori elettrostatici Attualmente si tende ad adottare soluzioni con ampie distanze tra i piatti (dai 20-30 iniziali ai 50-60 cm odierni) e basse velocità di attraversamento (< 1-2 m/s). Parametro fondamentale è la SCA (Specific Collection Area), che vale circa 130 m2/(m3/s) per contenuti di ceneri di circa 80 mg/Nm3. Metodi di alimentazione impulsiva, sovrapposta alla tensione continua, al fine di migliorare la ionizzazione delle particelle. Sistemi per ionizzare le ceneri a monte del precipitatore. Sistemi a film di liquido discendente per gravità sulle piastre per migliorare la rimozione delle particelle. Tecnicamente sono possibili due soluzioni per la disposizione dei fili: - fili sospesi con contrappesi: problema rottura per fatica (diametro circa 2,5 mm, lunghezza max circa 15 m) - fili tesi su telai rigidi: più diffusa La figura mostra la misura dell’efficienza di rimozione nel caso di un ESP, sui fumi di scarico di una caldaia a carbone, operato a diverse SCA, evidenziando come l’efficienza di rimozione aumenti per particelle submicroniche. Per particelle >1 µm, si ha una saturazione della carica, che porta ad una diminuzione dell’efficienza di rimozione. Per particelle <0,4 µm la carica aumenta (si instaurano diversi fenomeni di carica al decrescere delle dimensioni delle particelle), portando un incremento dell’efficienza di rimozione. ESP adatti a rimuovere particelle molto fini. 22 Filtri a manica I filtri a maniche sono veri e propri filtri di tessuto in forma di una superficie cilindrica attraverso i quali passa il gas da depurare. La filtrazione avviene per effetto combinato di tre meccanismi: - impatto inerziale: le particelle solide trascinate dal gas, a causa della loro massa, non seguono la traiettoria del gas quando questo curva trovando un ostacolo e vanno ad impattare sull’ostacolo stesso (prevalente per particelle > 1 µm); - intercettazione: le particelle solide seguendo la traiettoria del gas intorno all’ostacolo si trovano a distanze inferiori al loro raggio rispetto all’ostacolo e vengono intercettate da esso (prevalente per particelle 0,2-1 µm); - le particelle, a causa del proprio moto browniano, urtano con le altre molecole del gas deviando dalla loro traiettoria e possono urtare l’ostacolo (diffusione) (prevalente per particelle < 0,2 µm). 23 Filtri a manica Da un punto di vista impiantistico i filtri a maniche sono costituiti da camere parallelepipede entro le quali sono disposte verticalmente numerose maniche cilindriche, attaccate sul fondo. Il gas attraversa le maniche dall’esterno verso l’interno (captazione esterna – nel caso di passaggio dall’interno verso l’esterno si ha captazione interna) con una velocità dell’ordine di 1,5 m/s e viene aspirato dal ventilatore posto a valle del depolveratore. Il numero delle maniche installate dipende dalla portata di gas da trattare. Le dimensioni sono standardizzate dai costruttori e comprese tra: Diametro Lunghezza min 12 cm min 1,5 m max 90 cm max 6 m • Il sistema presenta un’elevata efficienza di raccolta fino al 99% • Adatto a particelle fini • Possibilità di trattamenti di adsorbimento sul “cake” (es. Carboni attivi). La deposizione di materiale sul filtro aumenta l’efficienza di filtrazione. La deposizione di materiale carbonioso garantisce un fenomeno di adsorbimento di metalli pesanti, composti organoclorurati e gas acidi. Questo fenomeno è spesso favorito mediante l’immissione a monte del filtro di additivi adsorbenti come carbone attivo (AC). 24 Filtri a manica - Pulizia La perdita di carico attraverso la superficie filtrante aumenta con il depositarsi del solido trattenuto e quando raggiunge un valore limite il flusso di gas viene sospeso e a manica viene pulita recuperando il solido nella tramoggia di fondo. Per evitare di fermare il flusso del gas da trattare durante la fase di pulizia, il filtro è realizzato solitamente a settori, ognuno dei quali subisce la fase di pulizia a rotazione mentre gli altri sono in fase di funzionamento. La pulizia del filtro può avvenire per tre meccanismi: Meccanico:per scuotimento o vibrazione delle maniche. Si utilizza solo con filtri a captazione interna, ma sollecita molto le fibre. Corrente inversa: si fa passare gas depolverato in senso inverso a quello di marcia. Isolamento della manica. Pulse-Jet: è utilizzabile solo con maniche a captazione esterna. Non richiede l’esclusione della manica dal flusso e non è traumatico per i tessuti. All’interno di ciascuna manica viene sparato periodicamente un getto di aria a 6-7 bar, il quale genera un’onda di pressione che la fa bruscamente espandere e causa il 25 distacco del deposito. Filtri a manica - Pulizia 26 Filtri a manica – Il materiale filtrante Dal punto di vista del materiale filtrante si possono distinguere due tipi di materiali: il tessuto, costituito da fili (fibre di vetro) perpendicolari intrecciati regolarmente, con apertura a maglia quadrata il teflon (feltro pressato), che è un insieme di piccole fibre disposte casualmente La maggiore differenza fra i due è nel meccanismo della filtrazione: il tessuto trattiene in superficie le particelle relativamente grandi formando uno strato di solido che funge anch’esso da filtro; il teflon, oltre ad un’azione di superficie, esegue il trattenimento delle particelle soprattutto all’interno dello strato filtrante, risultando efficiente anche su particelle fini Il teflon presenta una pulizia più difficoltosa ed una perdita di carico superiore, ma risulta più efficiente. Il tessuto perde, dopo la pulizia, parte della polvere aderente alla trama e, per un breve periodo dopo la pulizia, cala l’efficienza. I vari materiali filtranti si caratteristiche fondamentali: distinguono per altre Maniche in feltro o in tessuto? - la dimensione delle fibre - la resistenza temperature) meccanica delle - la resistenza chimica delle fibre - la resistenza al passaggio dell’aria - la carica elettrostatica Pulibilità della manica in funzione del tipo di filtro: fibre (a diverse Le maniche in feltro si impiegano generalmente su filtri con pulizia a lavaggio pneumatico: quelli dove le maniche sono, a brevi intervalli, pulite da un soffio di aria compressa in controcorrente al flusso di aria polverosa da depurare. I pesi vanno da 500 a 600 gr/mq e le permeabilità da 10 a 20 mc/min/mq a 200 Pa. Le maniche in tessuto si impiegano nei filtri statici (senza sistema di pulizia) o a pulizia meccanica, dove un vibratore meccanico o pneumatico scuote le maniche alla fine del ciclo di lavoro. Maniche in tessuto o in feltro leggero si impiegano sui filtri con pulizia a inversione di flusso. 27 Filtri a manica – Il materiale filtrante LE FIBRE E I LORO CAMPI DI IMPIEGO PRINCIPALI POLIESTERE: miniere - cave cementifici industrie siderurgiche - fonderie ceramiche - industrie del legno - industrie dell' amianto industrie della plastica impianti di verniciaturaproduzione di vernici in polvere. Impieghi in condizioni di bassa umidità con temperature sotto i 150°C. POLIACRILONITRILE : impianti per emulsioni bituminose - essiccatoi - industria del gesso e della calce. Impieghi in condizioni di alta umidità fino a 120°centigradi . POLIPROPILENE: industrie alimentari - produzione di detersivi. Impieghi che richiedono buona inerzia chimica fino a 90°centigradi. POLIAMIDE AROMATICA (NOMEX): impianti per emulsioni bituminose - cementifici - fonderie di metalli ferrosi e non ferrosi - ceramiche. Impieghi ad alta temperatura fino a 200 ° centigradi in condizioni di bassa aggressività chimica. POLIFENILSOLFURO (RYTON): caldaie a carbone - industrie chimiche. Impieghi fino a 180 °centigradi anche in condizioni gravose dal punto di vista chimico. PTFE (Teflon): Inceneritori. Massima inerzia chimica fino a 250°C. 28 Filtri a manica Anche i filtri a manica hanno un costo piuttosto elevato, soprattutto per le maniche che rappresentano oltre il 20% del costo del sistema di filtraggio ed hanno durate teoriche dai 18 ai 36 mesi. Il vantaggio fondamentale dei filtri a manica rispetto ai precipitatori elettrostatici è che l’efficienza di raccolta è sostanzialmente indipendente dal contenuto di zolfo. Problemi dei filtri a manica sono: - scarsa resistenza a temperature superiori a 150-170 °C; - scarsa resistenza a ceneri acide o bagnante; La superficie richiesta é di almeno 8 m2/MWe (2500 m2 per una centrale da 320 MWe), ed i volumi necessari, con attraversamento a bassa velocità per contenere le perdite di carico, sono elevati. - sensibile perdita di carico e necessità di maggiore potenza dei ventilatori; - necessità assoluta di operare il filtro al di sopra della temperatura di rugiada: se la temperatura scende sotto il dew-point l'acqua in fase vapore contenuta nel gas condensa: le gocce di acqua in fase liquida non solo inumidiscono lo strato di polvere depositato sulle maniche aumentandone così la resistenza al passaggio dell'aria (e quindi la ∆P del filtro), ma disciolgono anche eventuali composti acidi causa di corrosione su maniche, cestelli portamaniche e carpenteria del filtro ; - alti costi di manutenzione. Lo strato di polvere depositato sul tessuto aumenta l’efficienza del dispositivo. La figura mostra come in condizioni pulite l’efficienza per particelle di dimensioni a 1 µm si riduca notevolmente. Avvicinandosi alle condizioni di sporcamento, l’efficienza di rimozione è superiore al 95% per particelle inferiori a 1 µm e addirittura superiore al 99,6% per particelle superiori a µm. In generale i filtri a maniche avranno efficienze dell’ordine del 90% appena dopo la pulizia, mentre l’efficienza di rimozione supera mediamente il 29 99%. Applicabilità generale dei sistemi di controllo del particolato 30 Tabella comparativa fra i diversi sistemi 31 Metodologie fisico/chimiche di rimozione degli inquinanti gassosi 1. Condensazione: la temperatura della miscela gassosa viene ridotta al di sotto della temperatura di condensazione dell’inquinante da rimuovere 2. Assorbimento: rimozione dell’inquinante gassoso per mezzo di un solvente liquido 3. Adsorbimento: rimozione dell’inquinante gassoso per passaggio sulla superficie di un solido 4. Ossidazione catalitica e non catalitica: l’inquinante gassoso viene ossidato e trasformato in un altro composto chimico Efficienza di rimozione E.R.: inquinante rimosso E.R.= X 100 inquinante originariamente presente 32 1. Condensazione La condensazione è un metodo fisico importante per la rimozione di inquinanti che si presentano sotto forma di gas o vapori. Range applicazione: c > 5000 ppm. Efficienza 50-90% (per c >10.000ppm) Il metodo è particolarmente efficace per i composti che presentano una curva della tensione di vapore psi(T) molto ripida: in questo modo, refrigerando, la pressione di saturazione cala rapidamente; la condensazione inizia quando la pressione parziale del gas nella miscela risulta superiore alla tensione di vapore. Riducendo la temperatura, è possibile abbassare psi e, di conseguenza, innescare la condensazione della specie. La funzione p(T) è descritta in forma differenziale dall’Equazione di Clapeyron: è più pratico fare riferimento all’ Equazione di Antoine (sperimentale): log(psi) = A - B/(Ts+C) dove psi è la tensione di vapore della specie i-esima; A, B, C sono costanti caratteristiche della specie che possono essere determinate su basi di similitudine delle molecole e di variabili termodinamiche ridotte. 33 1. Condensazione 34 1. Condensazione Per la condensazione è necessario un circuito refrigerante. I costi di esercizio della refrigerazione sono elevati, ma questa operazione può permettere il recupero del componente condensato puro che, se commerciabile, consente un recupero economico. Inoltre esiste il problema della presenza simultanea di altre specie. Se nei gas da trattare è presente vapore d'acqua, questo condensa a temperature relativamente elevate; al di sotto di 0°C congela ed il ghiaccio va a depositarsi sulle superfici ostacolando la trasmissione del calore. Una soluzione è deumidificare preventivamente il gas da trattare, anche tramite la condensazione del vapore d'acqua. Si installano quindi due condensatori in serie: il primo, che raffredda fino a T> 0°C, fa condensare la maggior parte del vapore d'acqua senza formare ghiaccio; il secondo - di tipo criogenico - raffredda al di sotto di 0°C il gas ormai deumidificato. 40°C 1°C Acqua -10°C Emiss. 35 1. Condensazione In alternativa si possono utilizzare due condensatori in che vengono parallelo, periodicamente esclusi con rimozione del ghiaccio formatosi (ad esempio facendoli lambire dai gas caldi). Od anche, si può far lambire la superficie dal condensato non acquoso in modo da rimuovere il ghiaccio (soluzione applicabile solo in caso di solubilità tra acqua e condensato non acquoso, che deve presentare un punto di congelamento minore della temperatura di parete). Defrost 30°C Operate 40°C -10°C -20°C Refrigerante Condensato 36 1. Condensazione Le principali applicazioni riguardano ovviamente sostanze che a basse temperature hanno basse tensioni di vapore Applicazioni comuni: alcools, chetoni, nitrili (solventi) La condensazione conviene in genere quando la concentrazione delle emissioni da rimuovere è abbastanza elevata (è necessario comunque raffreddare tutta la portata dell’effluente). Minimizzazione del rapporto [costo energetico/massa di inquinante condensato] 37 2. Assorbimento E’ il processo con il quale la sostanza da rimuovere viene trasferita dalla fase gassosa a quella liquida, nella quale si trova dissolta in un opportuno sorbente (o solvente). Esempi di applicazioni: - rimozione e recupero di ammoniaca in processi di produzione di fertilizzanti - rimozione di HF dai fumi delle fornaci per il vetro - controllo degli ossidi di zolfo dalla combustione - recupero di solventi solubili in acqua (acetone e alcool metilici) - controllo gas odorigeni Solventi fisici: il gas viene disciolto in una soluzione liquida non reattiva e non volatile. Procedimento indicato per concentrazioni volumetriche del gas nella corrente gassosa superiori al 10% Solventi chimici: il gas viene legato alla fase liquida da una reazione chimica veloce e reversibile. Procedimento indicato per concentrazioni volumetriche del gas nella corrente gassosa tra 1% e 10% I processi di assorbimento chimico: - assorbimento di gas acidi in soluzioni alcaline (SO2) - assorbimento di gas odorigeni in soluzioni ossidanti Metodologie di rimozione di inquinanti - assorbimento di CO2 o H2Sgassosi in soluzioni di ammine 38 2. Assorbimento Rigenerazione del solvente (Desorbimento): a) Per via termica (es. “Stripping” con vapore o per riscaldamento) b) Per diminuzione di pressione (“Flash” o “Pressure-Swing” Absorption/Desorption). Sistema comune per solventi fisici. c) Per via elettrochimica (es. formazione di sali in soluzione) d) Per adsorbimento (es. su carbone attivo; stadio finale per rigenerazione del solvente con elevata purezza) Esempio: Rimozione dell’ H2S: 1. Concentrazioni elevate: assorbimento fisico in glicole etilenico, carbonato di propilene o soluzioni acquose di alchilammine. 2. Concentrazioni intermedie: assorbimento chimico su MonoEtanolAmmina (MEA: H2-N-CH2CH2OH), reversibile con calore. 3. Concentrazioni basse: assorbimento chimico con base forte, Soda Idrata NaOH, con produzione di cristalli di NaHS che devono essere rimossi e smaltiti (non reversibile) 39 2. Assorbimento chimico – Relazione di Equilibrio La relazione di equilibrio chimico per un sistema gas-liquido può scriversi: y, x concentrazioni volumetriche nella Pv = y* P = ps x fv,s fase gassosa e liquida ovvero ps pressione di saturazione y* = m x fv,s coefficiente di attività del componente gassoso nel solvente pv è la pressione parziale del componente nella fase vapore, Pv = P y* fv,s risulta diverso dall'unità quando il componente v è capace di stabilire legami chimici (deboli o forti) con il solvente; nei liquidi, i fenomeni di interferenza molecolare non sono - come avviene per i gas - trascurabili. Assorbimento fisico fv,s ≅ 1 Assorbimento fisico fv,s < 1 40 2. Assorbimento – Torri di lavaggio La resistenza principale per il passaggio di un gas in soluzione in fase liquida è costituita dal passaggio attraverso la superficie di interfaccia. Per questo motivo i processi industriali tendono a moltiplicare (per unità di volume) la superficie di interfaccia ed a garantire flussi omogenei e controllati di gas e di liquido Le Torri di Lavaggio, con flusso di liquido discendente per gravità e di gas da purificare ascendente, sono la soluzione più diffusa. Pro: semplicità, affidabilità, flessibilità per variazione di portata e concentrazione del gas Contro: Ingombro, raffreddamento del gas 41 2. Assorbimento – Torri di lavaggio – Riempimenti I molti vassoi della torre di lavaggio sono occupati da riempimenti (“Packing”) che possono essere ordinati (griglie, reti,…) o disordinati, che hanno la funzione di moltiplicare il film liquido e di rinnovarlo con frequenza in modo da facilitare lo scambio di massa gas-solvente. I riempimenti ordinati sono più efficienti ma hanno costo superiore. Ogni 5-6 vassoi si dispone un redistributore per evitare il “channelling” delle due correnti. 42 2. Assorbimento – Torri di lavaggio – Channeling Le torri (numero, diametro ed altezza) sono progettate in base alla portata di gas da trattare. Il diametro di una torre di lavaggio difficilmente supera 1,5 m, per le difficoltà inerenti alla distribuzione uniforme del solvente su sezioni elevate. L’altezza risulta tra i 4 e gli 8 m, in modo da contenere la perdita di carico per il gas ma da consentire un numero elevato di vassoi. Per portate di liquido ridotte, è possibile il channeling: il liquido non bagna uniformemente il riempimento, ma cala preferenzialmente nella parte centrale della torre dove incontra minore resistenza. Il gas sale lateralmente e la torre è inefficiente GAS LIQUIDO 43 2. Assorbimento – Torri di lavaggio – Flooding (Portata liquido costante) Per portate di gas elevate, è possibile il flooding: il liquido non riesce a colare lungo il riempimento, ed allaga il vassoio. LIQUIDO Il gas riesce a passare gorgogliando, con elevata intermittenza e fortissima perdita di carico. Buona parte del solvente non è interessato al flusso di gas. GAS 44 2. Assorbimento – Torri di lavaggio – Flooding Nelle condizioni di allagamento si hanno fenomeni di trascinamento di liquido e formazione di canali di by-pass del gas, di tipo non stazionario, che impediscono di fatto l'esercizio dell'assorbitore. Di conseguenza, operativamente la velocità del gas viene limitata a circa il 50 - 75% della velocità di flooding. Quest'ultima può essere stimata con opportune correlazioni per riempimenti disordinati od ordinati. Il liquido viene distribuito al di sopra del riempimento, con soluzioni a gravità od in pressione (con possibile atomizzazione). La perdita di carico in fase liquida può essere rilevante per tali ultimi sistemi, ma comporta una spesa energetica contenuta per il pompaggio del solvente. 45 2. Assorbimento – Torri di lavaggio – Flooding Per basse portate di gas la curva pressione-portata risulta di tipo quadratico, con coefficiente di perdita superiore per la colonna bagnata rispetto al riempimento secco. Oltre una certa velocità del gas il liquido incontra forti difficoltà a scendere per gravità lungo la colonna, ed aumenta di conseguenza la sua ritenzione all'interno della colonna ("Hold-up“od ingorgamento). Aumentando ancora la velocità del gas, il gas si trova ad attraversare zone completamente allagate (punto di allagamento o "flooding" della colonna). 46 2. Assorbimento – Cicloni Scrubber Negli Scrubber Ciclone, che hanno la forma rudimentale di un ciclone (separatore di polveri), la corrente gassosa entra con vorticità opposta a quella generata da uno spruzzatore rotante del solvente liquido. Le particelle liquide atomizzate interagiscono con forte turbolenza con il gas, ed il solvente parzialmente esausto viene centrifugato alle pareti e raccolto sul fondo, mentre il gas lavato fuoriesce dalla sommità del ciclone. 47 2. Assorbimento – Ciclone Scrubber Pro: adatti per la rimozione simultanea di particelle ed emissioni gassose (con assorbimento); Contro: •il sistema non è indicato se le particelle solide presentano attività chimica che disturba la reazione di assorbimento; •il liquido raccolto al fondo deve andare ad un processo di separazione della parte solida prima di essere riciclato; •i gas escono sensibilmente raffreddati (l’evaporazione del liquido sottrae molto calore alla corrente gassosa); • i gas incontrano nel ciclone umido una forte perdita di carico. Queste caratteristiche rendono i cicloni scrubber poco adatti alla depolverazione e purificazione delle emissioni gassose in sistemi di combustione. 48 2. Assorbimento – Scrubber Venturi Un solvente liquido viene atomizzato a forte pressione, ottenendo gocce di piccolo diametro ed un efficace effetto di moltiplicazione della superficie di interfaccia. Il gas viene iniettato trasversalmente nella gola di un con una tubo di venturi, configurazione geometrica (miscelazione a flussi incrociati) che favorisce elevati coefficienti di scambio di materia. Sistema molto utilizzato per la rimozione di polveri; consente anche di realizzare sistemi ad assorbimento di tipo estremamente compatto. 49 2. Assorbimento – Scrubber Venturi Pro: Sistema estremamente compatto Contro: •Per piccole portate di solvente ed elevate portate di gas (caso frequente), è necessario energizzare adeguatamente il gas mediante un opportuno compressore o soffiante; se invece la portata di liquido è elevata, il sistema funziona come pompa a getto e non è necessaria energia per il pompaggio lato gas. •La potenza necessaria per accelerare il flusso di gas (anche fino a 120 m/s) è rilevante; i gas incontrano nello scrubber venturi una forte perdita di carico. •Il sistema è poco adatto per portata di gas da trattare variabile Lo Scrubber Venturi si applica favorevolmente nei casi in cui la tensione di vapore dell'inquinante è molto bassa, e la quantità dello stesso elevata (ad esempio, assorbimento in soluzioni alcaline di gas acidi) 50 3. Adsorbimento E' il fenomeno di cattura dell'inquinante gassoso su di una superficie solida porosa. Con un solido adsorbente appropriato ed un tempo di contatto molto lungo è possibile raggiungere elevate efficienze di rimozione. Eventualmente è possibile il recupero del composto adsorbito. L’adsorbimento è usato per applicazioni industriali quali: - controllo degli odori - recupero di solventi volatili come benzene, etanolo, freon, etc. - essiccamento di correnti gassose Comunque una delle principali applicazioni è la cattura di composti organici volatili (VOC) 51 3. Adsorbimento La molecola gassosa adsorbita sulla superficie si comporta come una molecola condensante, ed è trattenuta sulla superficie stessa da forze di attrazione assimilabili alla tensione superficiale (forza di Van der Waals); esistono anche sistemi a chemioadsorbimento in cui si stabiliscono effettivamente legami chimici tra molecola gassosa ed adsorbitore. Generalmente la capacità di un adsorbente di adsorbire un determinato composto è direttamente proporzionale al peso molecolare ed inversamente proporzionale alla tensione di vapore. Isoterma di Langmuir Q ⋅ KL ⋅ c q° = (1 + K L ⋅ c ) q°=frazione adsorbita c = concentrazione in fase gas Q = valore massimo asintotico della frazione adsorbita KL= costante di equilibrio grammi adsorbiti grammi solido adsorbente L’emissione viene catturata efficacemente già a basse concentrazioni Isoterma favorevole Isoterma sfavorevole Le isoterme di adsorbimento riportano la frazione adsorbita nel solido in funzione della concentrazione nella fase gas, e sono riferite alle condizioni di equilibrio L’emissione dovrebbe raggiungere concentrazioni elevate per essere catturata efficacemente Fraz. molare emissione da adsorbire in fase gassosa Determinazione sperimentale delle isoterme di adsorbimento 52 3. Adsorbimento Il comportamento all'equilibrio non è sufficiente a descrivere le reali prestazioni, in quanto i sistemi effettivi operano in condizioni dinamiche con tempi di contatto limitati tra gas e solido. La cinetica del fenomeno presenta tre fasi: 1. 2. 3. la diffusione della sostanza i in fase gas, che obbedisce a leggi del tutto simili a quelle dell'assorbimento in fase liquida, una volta definita una opportuna pressione parziale del gas all'interfaccia la penetrazione delle particelle di gas all'interno della superficie porosa dell'adsorbitore, che risulta influenzata dalla diffusività all'interno dei pori su scala molecolare la formazione del legame tra solido e particella della specie i, che, essendo più rapida rispetto alle fasi (a) e (b), non influenza di fatto il flusso adsorbito. 53 3. Adsorbimento L'adsorbimento é un fenomeno superficiale; la capacità adsorbente aumenta con il crescere della superficie di contatto gas - solido. Si utilizzano perciò solidi molto porosi: carbone attivo, allumina, gel di silice. Tali sostanze hanno capacità di stabilire legami chimici (chemioadsorbimento) con le molecole polari presenti nel gas: ad esempio gli atomi di ossigeno presenti nel solido adsorbitore formano legami con l'idrogeno delle sostanze inquinanti (idrocarburi). La cattura delle molecole sul solido comporta la perdita del grado di libertà della molecola gassosa, con rilascio di energia sotto forma termica. Per adsorbimento fisico tale energia corrisponde al calore di condensazione; per chemioadsorbimento, si ha il rilascio di energia di reazione, che può essere molto più rilevante (da 20 a 400 kJ/gmole). Il fenomeno è influenzato dalla temperatura (cfr. isoterme di adsorbimento); è quindi necessario rimuovere calore per garantire il mantenimento di temperature basse sulla superficie solida. Il riscaldamento del solido adsorbitore può realizzare il desorbimento per cambiamento dell’isoterma di funzionamento. In tal modo si ha la rigenerazione del solido adsorbente e si realizza il recupero dell'inquinante in concentrazioni elevate. 54 3. Adsorbimento Sono di tre tipi: 1. Carboni attivi: adatti per molecole non polari, es. Idrocarburi 2. Sostanze Inorganiche: Allumina attivata; Gel di Silice; argille; Zeoliti 3. Polimeri sintetici; polimeri a scambio ionico negativo (stirene/divinilbenzene) o positivo (gruppi alkilamminici), polimeri a base di esteri acrilici. Per molecole polari complesse, spesso per il trattamento delle acque (resine a scambio ionico) Materiale Area [mq/g] Carbone attivo 500-1500 Gel di silice 200-600 Allumina attiva 175 Volume dei pori [cmc/g] 0,6-0,8 circa 0,4 0,39 Diametro medio dei pori [Α] 20-40 30-200 90 55 3. Adsorbimento Carbone attivo In generale è un ottimo adsorbente per sostanze organiche non polari. La capacità adsorbente aumenta all’aumentare del peso molecolare della molecola e della temperatura di ebollizione. I parametri basilari che determinano la prestazione del carbone sono la superficie specifica e la dimensione media dei pori. Il carbone attivo viene di norma prodotto dalla carbonizzazione di legno, carbone, noccioli di frutta o noci di cocco; l'attivazione – che rende disponibili atomi di ossigeno per il legame - è realizzata mediante trattamento con aria calda o vapore. Il carbone attivo si impiega normalmente per la depurazione dell'aria o di altri flussi gassosi da solventi e sostanze organiche, oltre che per la rimozione dell'odore. La capacità adsorbente del carbone attivo é notevolmente diminuita dalla presenza di umidità nel gas in percentuali prossime alla saturazione, od anche dalla presenza di inquinanti inorganici capaci di formare legami chimici con il carbone. Per ridurre il primo effetto, può risultare conveniente la rimozione dell'umidità mediante condensazione. 56 3. Adsorbimento Gas Out Gas Out Ciclone Soluzioni realizzative: Ricircolo solido Colonna di adsorbimento Adsorbente depositato sulla parete interna Piccole portate, applicazioni di misura (gascromatografia) Rigenerazione solido Ricircolo solido Gas In Gas In Letto Compattato Adsorbente in grani porosi Portate medio/elevate, applicazioni industriali, Disposizione in parallelo con adsorbimento/desorbimento (rigenerazione) Letto Fluidizzato Adsorbente in grani porosi Portate elevate, applicazioni industriali, Possibilità di estrazione continua del solido dal ciclone rigenerazione per desorbimento 57 3. Adsorbimento Concentratore rotativo Uscita gas arricchiti (al processo di trattamento) L’Adsorbimento/ Desorbimento – ad es. su zeoliti – può essere un buon sistema per arricchire le concentrazioni prima di un successivo processo di trattamento (assorbimento, incenerimento) Ingresso gas concentrazione dell’emissione con bassa 58 4 . Ossidazione E’ una tecnica molto utilizzata per l'eliminazione di sostanze inquinanti ossidabili (idrocarburi; VOC, CO; etc.). Il problema dell’ossidazione è la possibilità di ottenere altre specie indesiderate: SO2, HCl, NOx, etc. Soluzioni realizzative: a) Torcia atmosferica (fiamma libera) b) Camera di combustione con possibile recupero termico Gas In Combustibile Il recuperatore (preriscaldatore rigenerativo gas/fumi) consente di raggiungere temperature elevate di combustione con consumi ridotti di combustibile 59 4 . Ossidazione Con riferimento alle sostanze organiche, a seconda che la concentrazione complessiva nella miscela sia o meno sufficiente per l'infiammabilità della miscela, si deve provvedere: A) se la concentrazione é al di sotto del limite di infiammabilità, all'utilizzo di un combustibile ausiliario (gas naturale) B) se la concentrazione è prossima (in tal caso per motivi di sicurezza) o superiore al limite di infiammabilità, alla diluizione della miscela con aria, con soluzioni impiantistiche atte a prevenire ed impedire ritorni di fiamma ed infiltrazioni da e verso il gas combustibile. La temperatura risulta tipicamente di 700-800°C. Ciò risulta da un compromesso tra le condizioni di equilibrio chimico, la necessità di favorire la cinetica delle reazioni, e l'economicità del processo. 60 4 . Ossidazione La catalisi é un aumento della velocità con cui una reazione chimica raggiunge il proprio equilibrio ad opera di una sostanza (catalizzatore) che, nonostante modifichi il processo reattivo, non subisce alcun coinvolgimento nella trasformazione. Il catalizzatore viene coinvolto nel meccanismo chimico di reazione generando un percorso alternativo a bassa energia di attivazione che semplifica il passaggio da reagenti a prodotti: esso permette l’abbassamento dell’energia dello stato transitorio, o complesso attivato, della reazione, mantenendo inalterata l’energia di prodotti e reagenti. L’abbassamento dell’energia di attivazione comporta un’accelerazione della velocità di reazione in ugual modo per le reazioni dirette e per le reazioni inverse, quindi la presenza del catalizzatore non modifica la condizione complessiva di equilibrio del sistema Nel caso in cui la reazione abbia luogo in una sola fase si parla di catalisi omogenea: quando invece la reazione avviene all’interfaccia tra diversi stati di aggregazione si parla di catalisi eterogenea. 61 4 . Ossidazione La combustione catalitica consente di utilizzare temperature e condizioni di composizione al di fuori dei limiti normali di infiammabilità, e riduce i tempi di permanenza. In particolare interessa garantire le reazioni di combustione in ambiente fortemente ossidante; a causa della forte diluizione in aria, le temperature di combustione possono scendere fino a 250-400 °C, pur garantendo una elevata cinetica delle reazioni di ossidazione. Sostanze con attività catalitica: metalli nobili (platino, palladio; dispersi su supporto di allumina od altro materiale ceramico). Ossidi metallici attivi (aallumina ed altri), gli ossidi di rame e manganese (Hopcalite); e gli Ossidi metallici su supporto metallico; tali materiali (meno costosi) si applicano con successo alla rimozione degli idrocarburi. Fasi: a) b) c) d) e) Diffusione in fase gassosa Diffusione all’interfaccia Adsorbimento Diffusione all’interno dei pori Reazione chimica di trasformazione (con catalizzatore) Processo inverso di desorbimento dei prodotti 62 4 . Ossidazione Una delle attrattive della combustione catalitica è la possibilità di minimizzare od eliminare l'utilizzo di combustibile supplementare, rispetto ad un’ossidazione nelle camere di combustione. Il processo si applica favorevolmente alla rimozione di solventi (toluolo, metiletilchetone, xilolo, alcohols,etc.); di monossido di carbonio, etilene, ossido di etilene, e propilene. Un problema della combustione catalitica è l'avvelenamento del catalizzatore da parte di contaminanti specifici: ferro, piombo, silice e fosforo diminuiscano drasticamente la vita di molti catalizzatori. La temperatura del processo deve essere attentamente controllata, in quanto molti catalizzatori presentano un limite operativo attorno agli 850 °C. 63 4 . Ossidazione La presenza di un recuperatore per preriscaldare in ingresso il gas da trattare può ulteriormente abbassare i consumi di combustibile. Clean air In molti casi il gas da trattare deve essere preventivamente depolverato, in quanto il particolato ostruisce i pori della superficie supporto per il catalizzatore, diminuendone l'efficacia. Fan Polluted air 64 Riduzione delle emissioni di ossidi di zolfo I due approcci nella riduzione delle emissioni degli ossidi di zolfo consistono: 1) Rimuovere S dal combustibile prima della combustione 2) Rimuovere SO2 dai gas combusti 65 Riduzione delle emissioni di ossidi di zolfo Desolforazione del combustibile Il processo di raffinazione del petrolio (alcuni tipi di petrolio contengono 1-3% di S) prevede la desolforazione, cioè la rimozione dei composti organici a base di zolfo per mezzo di una reazione catalitica con l’idrogeno R-S + H2 H2S + R L’H2S prodotto da questi processi viene di solito utilizzato per la produzione di S elementare attraverso il processo Clauss, in presenza di un catalizzatore: H2S + 3/2 O2 H2O + SO2 (ossidazione) 2H2S + SO2 2H2O + 3S (riduzione) Tale processo può essere applicato direttamente a combustibili (gas naturale) che contengono H2S 66 Rimozione degli ossidi di zolfo I processi di desolforazione sono solitamente classificati come: -non rigenerativi - rigenerativi A seconda che la soluzione di lavaggio di rigenerata e lo zolfo rimosso sia recuperato o meno oppure -a umido - a secco A seconda della fase in cui avvengono le reazioni I più impiegati sono applicati ai gas combusti e richiedono in genere un processo di rimozione meccanica ad umido o a semi-secco (“Wet scrubbing” o “spry absorber”) In tali processi l’anidride solforica o solforosa interagisce con composti di calcio (calce spenta CaO; calcare CaCO3; gesso; argilla), dando luogo a fanghi acidi di zolfo. Sono anche possibili processi rigenerativi, a ciclo praticamente chiuso ma di costo elevato, in cui si recupera il solvente per il suo riciclaggio (prodotto finale H2SO4 o S). Nella maggior parte dei processi è prevista la discarica controllata di dei fanghi (prodotto finale CaSO4) o delle polveri. 67 Desolforazione Reagenti: calce o calcare (umido-semisecco.-secco) Il processo prevede che il gas attraversi un separatore ad umido (scrubber) in cui viene in contatto con una miscela acquosa di calce (CaO) e calcare (CaCO3). L’SO2 presente nei gas reagisce e forma a sua volta CaSO3 e CaSO4. Reagente: bicarbonato di sodio (umido-semisecco-secco) Il processo porta alla formazione di solfato di sodio (Na2SO4) che precipita in forma solida. 68 Desolforazione a umido (assorbimento) La miscela viene spruzzata nella torre di reazione in controcorrente ai gas, aspirati da ventilatore di aspirazione alla base del camino. Nel processo i gas si raffreddano sensibilmente e può essere necessario un modesto riscaldamento per garantire il tiraggio. Il problema principale dei sistemi di desolforazione ad umido è la possibilità di formazioni di incrostazioni e di ostruzione degli ugelli nella torre di reazione. Infatti la solubilità di CaSO3 e CaSO4 nell’acqua è limitata al 30% ed occorre perciò garantire una diluizione sufficiente con H2O, a seconda del contenuto di SO2 nei fumi. Inoltre la precipitazione della fase solida richiede un certo tempo, quindi la miscela deve essere lasciata decantare in un apposito serbatoio prima del riciclaggio: se il tempo non è sufficiente, si corre il rischio di iniettare miscele soprasature e di avere incrostazioni ed occlusioni. Un accorgimento adottato è quello di utilizzare cristalli di CaSO3 e CaSO4 precipitati, che favoriscono l’addensamento di tali componenti nelle loro vicinanze. La miscela da smaltire viene fatta prima sedimentare, in modo da ricircolare parte dell’acqua con i sorbenti freschi, e di ottenere fanghi densi. Il sistema comporta rischi di inquinamento del suolo e richiede ampie superfici di stoccaggio. 69 Desolforazione a umido L’efficienza di rimozione può raggiungere il 95% E’ un sistema molto diffuso commercialmente 70 Desolforazione a semi-secco (assorbimento) Anche in questo processo si utilizza calce CaO, che viene atomizzata e spruzzata per formare CaSO3 e CaSO4. A differenza del sistema ad umido, l’atomizzazione è spinta fino alla produzione di particelle estremamente piccole e la quantità di liquido iniettato è limitata al di sotto del valore che satura i gas di scarico alla temperatura di iniezione. In tal modo non si ha mai condensazione: le particelle iniettate solidificano come CaSO3 e CaSO4 e sono rimosse mediante un sistema di rimozione del particolato (in genere filtri a manica). Le particelle raccolte nel filtro sono in parte riciclate, dopo l’aggiunta di rigeneranti alcalini. Il materiale di scarto è allo stato secco di polvere ed è perciò più facilmente smaltibile rispetto al residuo fangoso dei sistemi ad umido. L’efficienza di desolforazione è però inferiore rispetto al sistema ad umido. Desolforazione a secco (adsorbimento) La calce viene iniettata sotto forma di polvere, senza acqua. Avviene quindi una reazione sulla superficie solida e le particelle vengono rimosse da un FF dove un’ulteriore rimozione ha luogo. Efficienza inferiore 71 Desolforazione a semi-secco L’efficienza di rimozione può raggiungere l’85% E’ un sistema molto diffuso commercialmente 72 Confronto sistemi rimozione gas acidi dei di dei 73 Rimozione degli ossidi di azoto Per il controllo degli ossidi di azoto si applicano innanzitutto misure preventive volte alla riduzione della temperatura di fiamma ed alla eliminazione di “punti caldi” nella camera di combustione. Inoltre si tende a ridurre il rapporto aria/combustibile fino a rapporti prossimi allo stechiometrico e si utilizza la ricircolazione dei gas di scarico in caldaia. Se è comunque necessario provvedere alla rimozione degli ossidi di azoto dai fumi, sono disponibili due sistemi di denitrificazione: Selective Catalitic Reduction (SCR) Non Selective Catalitic Reduction (NSCR) NOx Termici - Catena di Zeldovich La catena di Zeldovich presuppone la formazione di ossigeno monoatomico, con reazione che avviene ad alta temperatura (T> 2200K) : O2 2O Dopodiché l’azoto (dell’aria comburente) viene facilmente ossidato: O + N2 NO + N N + O2 NO + O 74 Rimozione degli ossidi di azoto - SCR Selective Catalitic Reduction (SCR) - Riduzione Selettiva Catalitica (SCR). Consente la rimozione di un'alta percentuale degli ossidi di azoto dai gas (dal 70 al 90%), ed é fondata sull'iniezione nei gas di un agente riducente (ammoniaca NH3, urea od altri composti ad alto tenore di azoto) in presenza di un catalizzatore ed a temperature nella fascia 350 - 400 °C – in un generatore di vapore immediatament e a monte dello scambiatore rigenerativo gas/aria. I costi del processo sono elevati a causa dei catalizzatori, che devono essere periodicamente rinnovati. 75 Rimozione degli ossidi di azoto - SCR Iniezione di NH3 od Urea in zona a 300 – 400°C, con catalizzatore (metallo nobi le, ossidi metallici, zeoliti): 4NH3 + 4 NO + O2 4 N2 + 6 H2O 8NH3 + 6 NO2 7 N2 + 12 H2O Tali reazioni di riduzione in questa fascia di temperatura, grazie alla presenza del catalizzatore, prevalgono su quelle di ossidazione: 4NH3 + 5 O2 4 NO + 6 H2O E’ essenziale evitare che la polvere possa occludere i pori della matrice ceramica del catalizzatore (filtraggio ESP a caldo; matrici con pori di grandi dimensioni;...) ed assicurare una miscelazione omogenea tra NH3 e flusso da trattare (turbolenza elevata). Un sistema di controllo degli NOx provvede al dosaggio dell’ammoniaca. L’efficienza di rimozione raggiunge il 90%, con perdite di carico di 5-7 mbar, con velocità spaziali vs tra 2500 e 7000 hr-1 . (vs = (m3/h) di gas / m3 di catalizzatore) 76 Rimozione degli ossidi di azoto - SCR 77 Rimozione degli ossidi di azoto - NSCR Riduzione Selettiva Non Catalitica. I reagenti sono gli stessi, ma è assente il catalizzatore e la temperatura deve essere compresa tra 870 e 1200 °C (mediante l'aggiunta di additivi chimici si può arri vare fino a 540°C). L’efficacia dipende largamente dall'ottimizzazione dell’ iniezione e dalla soluzione di problemi di corrosione e/o formazione di pennacchi allo scarico. La riduzione conseguibile negli ossidi di azoto é dell'ordine del 40 - 70 %. Non Selective Catalitic Reduction (NSCR) - Iniezione di NH3 od Urea nella zona a 850-1000°C, senza alcun catalizzatore : 4NH3 + 4 NO + O2 4 N2 + 6 H2O L’efficienza di rimozione si situa tra il 40 % ed il 70%, con rapporti molari N/NO (consumo di reagenti) anche doppi rispetto allo stechiometrico N/NO=1). 78
Scaricare