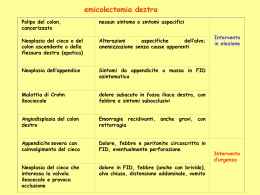
IF Alberto Arezzo Mauro Verra Mario Morino Colorectal leaks and fistulas are severe post-surgical complications. Over-thescope clip (OTSC) application represents an innovative technique to seal the visceral wall. Endoscopic closure with OTSC is a safe technique that accomplishes a high success rate in both acute and chronic cases, including rectovaginal, rectovesical, and colocutaneous fistulas. Overall success rate is higher than 70%, as reported in the literature. No OTSC-related complications have been described in the lower gastrointestinal tract so far. Introduzione Key words: colorectal surgery, postoperative complications, anastomotic leak, endoscopic clips, Over-The-Scope Clip Dipartimento di Scienze Chirurgiche Università di Torino La deiscenza anastomotica è una complicanza relativamente frequente della chirurgia colorettale, causa di elevata morbilità e aumentata mortalità. La sua frequenza è riportata nei dati di letteratura, dall’1 al 39%, per quanto deiscenze clinicamente significative sembrano essere meno frequenti, con frequenza variabile dal 3 al 6% (1-6), potendo molti casi essere clinicamente asintomatici. Diversi sono i fattori di rischio significativamente associati allo sviluppo di una deiscenza anastomotica (malnutrizione, uso di steroidi, disturbi cardiovascolari; la distanza dell’anastomosi dal margine anale, la concomitante presenza di occlusione intestinale, la vascolarizzazione dei monconi colici, la necessità di trasfusioni nel periodo perioperatorio e la presenza di uno stato settico) (1-3,7). La presenza di un’ileostomia di protezione è stato dimostrato ridurre invece l’incidenza di deiscenze sintomatiche (8). La gestione clinica dipende da diversi fattori quali la sede e le caratteristiche della perforazione e la stabilità clinica del paziente. Il trattamento chirurgico tradizionale richiede solitamente una laparotomia esplorativa ed, in almeno l’80% dei casi, il confezionamento di una stomia derivativa. La gestione chirurgica riduce la mortalità, Giorn Ital End Dig 2014;37:43-47 Le deiscenze anastomotiche e le fistole post-chirurgiche sono una complicanza della chirurgia colorettale gravata di una relativamente alta morbilità e mortalità. L’applicazione endoscopica della clip OTSC rappresenta una tecnica innovativa che permette la chiusura per prima intenzione del difetto parietale. L’OTSC si è dimostrata essere una tecnica sicura, con un’alta percentuale di successo (maggiore del 70%) sia in caso di fistole acute sia croniche, senza che siano state descritte complicanze correlate alla manovra. Parole chiave: chirurgia colorettale, complicanze postoperatorie, deiscenze anastomotiche, llips endoscopiche, Over-The-Scope Clip Iniziative Formative > Tecniche endoscopiche Efficacia del trattamento endoscopico di deiscenze post-chirurgiche e fistole colorettali 43 IF Iniziative Formative > Tecniche endoscopiche Alberto Arezzo et al > Efficacia del trattamento endoscopico post-chirurgico 44 ma è gravata da una elevata morbilità (fino al 30%) ed una percentuale di riconversione della stomia inferiore al 50% (9-11). Attualmente il trattamento endoscopico delle deiscenze e delle perforazioni gastrointestinali è dimostrato essere, in casi selezionati, un’alternativa sicura ed efficace al trattamento chirurgico, con una conseguente riduzione della morbilità post-operatoria. La presenza di peritonite generalizzata, instabilità emodinamica e perforazione intraperitoneale rappresentano un'indicazione assoluta all’intervento chirurgico. Negli altri casi l’approccio endoscopico può essere una valida alternativa (12). In genere la diagnosi precoce è un fattore prognostico importante per il successo della terapia endoscopica perché la percentuale di successo è significativamente maggiore quando viene trattato un tessuto vitale, non fibrotico. Il tipo di trattamento endoscopico dipende poi dalle caratteristiche della perforazione: la sede, le dimensioni e la concomitante presenza di un’infezione. Ad esempio in presenza di ampie deiscenze o perforazioni viscerali, che interessano più del 30% della circonferenza, e in presenza di una cavità ascessuale extraviscerale, si può utilizzare la tecnica Endo-VAC (BBraun Melsungen AG, Melsungen, Germany). Questa situazione si presenta soprattutto in sede extra-peritoneale; l’Endo-VAC permette al tempo stesso il drenaggio della cavità extra-luminale, la granulazione tissutale e la successiva chiusura della soluzione di continuo per seconda intenzione evitando la contaminazione da parte del contenuto gastrointestinale (13-15). Stent endoscopici parzialmente o totalmente ricoperti possono essere utilizzati e periodicamente sostituiti in caso di perforazioni o deiscenze anastomotiche con una concomitante stenosi viscerale. Il principio è quello di escludere la contaminazione dei tessuti extra-luminali da parte del contenuto gastrointestinale durante la chiusura della soluzione di continuo. È importante in questo caso l’assenza di infezione a livello dei tessuti extra-intestinali o che la cavità sia adeguatamente drenata (16). In presenza di piccole soluzioni di continuo può essere indicato l’utilizzo di mezzi di sintesi di sutura diretta, tra i quali quelli più frequentemente utilizzati sono le clip endoscopiche. Queste hanno una relativamente alta percentuale di successo in casi selezionati (descritta in letteratura tra il 60 e il 100%) (17). In particolare il posizionamento di clip endoscopiche è efficace in caso di piccole perforazioni iatrogene; il loro utilizzo in caso di deiscenza anastomotica, dove i tessuti sono spesso fibrotici anche nelle fasi precoci, è invece spesso inefficace. Un nuovo mezzo di sintesi, la Over-The-Scope Clip (OTSC, Ovesco GmbH, Tuebingen, Germany), è disponibile dal 2007. Il sistema è costituito da una clip in nitinolo con una forma tipo "tagliola" o "trappola per orso’", che viene caricata in un cappuccio posto all’estremità dell’endoscopio e che permette di includere tra le sue branche una più ampia quantità di tessuto. La prima casistica di utilizzo di OTSC è stata presentata da Kirschniak (18). In un lavoro più recente dello stesso gruppo sono stati presentati 8 casi di fistola gastrointestinale e 11 casi di perforazione con una percentuale di successo del 100% e una percentuale di recidiva del 26% (19). In un recente studio (20) Weiland ha condotto un revisione sistematica sull’uso dell’OTSC in caso di perforazione gastrointestinale. È stata riportata una percentuale di successo procedurale compresa tra l’80 e il 100%, con una percentuale di successo clinico compresa tra il 57 e il 100% in assenza di complicanze maggiori legate alla procedura, concludendo che l’utilizzo dell’OTSC può ridurre la necessità di intervento chirurgico. La casistica del nostro centro include 24 casi consecutivi (età media 62 anni; range 38-76 anni) trattati tra aprile 2011 e ottobre 2013 per deiscenza anastomotica o fistola del colon o del retto (tabella 1). La percentuale di successo procedurale è stata del 92% (22/24), ma a 2 mesi dal trattamento solo il 71% (17/24) risultava trattata con successo. In 8 dei 9 pazienti trattati entro i 2 mesi dalla comparsa della complicanza il trattamento è risultato efficace (89%), non differente rispetto al gruppo trattato oltre ai 2 mesi dalla comparsa della complicanza (P=0.1). In 11 dei 13 pazienti trattati dopo radioterapia neoadiuvante il trattamento è risultato efficace (85%), non differente rispetto al gruppo trattato senza radioterapia neoadiuvante (P=0.1). Di seguito sono presentate alcune indicazioni e impressioni sviluppate nel corso della nostra esperienza per quanto riguarda il trattamento endoscopico con OTSC delle deiscenze, delle fistole e delle perforazioni colorettali. Procedura endoscopica È ormai dimostrato che la preparazione intestinale non è più necessaria prima di un intervento sul colon, ma è dai più considerata tuttora indicata prima di una resezione del retto. Ciò dipende dal fatto che le resezioni del retto sono caratterizzate da un più alto rischio di deiscenza rispetto a quelle coliche. La preparazione non influisce sulla incidenza di deiscenza ma sulla gravità delle sue conseguenze e sulla possibilità di trattarle in maniera conservativa. Nel caso la complicanza perforativa avvenga su un intestino non preparato, occorrerebbe un esteso lavaggio del tratto intestinale, con il rischio di disseminazione del contenuto gastrointestinale negli spazi extraviscerali. Come alternativa è possibile eseguire un clisma attraverso la stomia di protezione, se presente. Il primo tempo della procedura è l’esplorazione chirur- IF Iniziative Formative > Tecniche endoscopiche tabella 1: caratteristiche dei pazienti con deiscenza anastomotica o fistola colorettale (casistica personale) Tempo dopo Diametro/margini chirurgia Età Sede Eziologia OTSC mm Successo Follow-up 73 Retto Deiscenza anastomosi colorettale Post Radioterapia 24 mesi 10 Fibrotico 12 Sì Successo primario 58 Retto Deiscenza anastomosi colorettale Post Radioterapia 21 mesi 8/5 Fibrotico 12 No Difetto persistente 76 Retto Deiscenza anastomosi colorettale Post Radioterapia 13 giorni 10 Fibrotico 12 Sì Successo primario 41 Retto Deiscenza anastomosi colorettale Post Radioterapia 16 mesi 6 Fibrotico 12 Sì Successo primario 59 Retto Fistola rettovaginale Post Radioterapia 25 giorni 5 Fibrotico 12 Sì Successo primario 65 Retto Fistola rettovaginale 6 giorni 10 Soffice 12 Sì Difetto persistente 73 Retto Deiscenza anastomosi colorettale Post Radioterapia 15 giorni 10 Fibrotico 12 Sì Successo primario 56 Retto Deiscenza anastomosi colorettale Post Radioterapia 20 giorni 10 Fibrotico 12 Sì Successo primario 74 Retto Deiscenza anastomosi colorettale Post Radioterapia 21 mesi 12 Fibrotico 12 Sì Successo primario 66 Retto Deiscenza anastomosi colorettale Post Radioterapia 13 giorni 8 Fibrotico 12 Sì Successo primario 69 Retto Deiscenza anastomosi colorettale 25 giorni 9 Fibrotico 12 Sì Successo primario 76 Retto Deiscenza anastomosi colorettale 16 giorni 12 Fibrotico 12 Sì Successo primario 68 Colon Fistola colocutanea 6 mesi 5 Fibrotico 12 Sì Successo primario 82 Colon Fistola colocutanea 6 mesi 2 Fibrotico 12 Sì Difetto persistente 38 Retto Fistola rettovescicale Traumatica 120 mesi 5 Fibrotico 14 Sì Successo primario 63 Retto Deiscenza anastomosi colorettale Post Radioterapia 4 mesi 15 Fibrotico 12 Sì Successo primario 57 Retto Fistola rettocutanea 3 mesi 10 Fibrotico 12 Sì Successo primario 74 Retto Deiscenza anastomosi colorettale 13 giorni 12 Soffice 14 Sì Successo primario 74 Retto Fistola rettovescicale Perforazione chirurgica 8 mesi 10 Fibrotico 12 Sì Difetto persistente 52 Retto Fistola rettovescicale Pouchite 21 mesi 3 Fibrotico 12 Sì Difetto persistente 75 Retto Fistola rettovescicale PPH* 72 mesi 5 Fibrotico 12 Sì Difetto persistente 78 Retto Fistola rettovescicale Post Radioterapia 6 mesi 5 Fibrotico 12 Sì Successo primario 62 Retto Fistola rettocutanea Post Radioterapia 6 mesi 8 Fibrotico 12 Sì Successo primario 47 Retto Fistola rettovaginale Post Radioterapia 12 mesi 5 Fibrotico 12 No Difetto persistente *PPH= Procedura per prolasso e emorroidi Giorn Ital End Dig 2014;37:43-47 45 IF Iniziative Formative > Tecniche endoscopiche Alberto Arezzo et al > Efficacia del trattamento endoscopico post-chirurgico 46 gica del sito utilizzando un endoscopio standard. L’indicazione all’applicazione dell’OTSC è la presenza di una deiscenza anastomotica, una fistola o una perforazione con un difetto di parete minore di 20 mm di diametro massimo in assenza di una cavità extraluminale, dal momento che la sua presenza costituirebbe un fattore di rischio per la formazione di un ascesso. Se esiste una piccola cavità o una fistola, è sufficiente lavare con soluzione di iodopovidone. Una volta che l’indicazione è stata confermata, l’endoscopio viene retratto e si monta il cappuccio dedicato sull’estremità distale dell’endoscopio. Il rilascio della clip avviene con un sistema analogo a quello del legatore elastico di varici. È importante accertarsi che, durante il montaggio, il cappuccio sia ruotato sulla punta dell’endoscopio in modo che il filo sia teso dal canale operativo al cappuccio senza che la visione endoscopica sia ostacolata. Prima della reintroduzione dello strumento è importante ricordarsi di ruotare la manopola del sistema di rilascio di un mezzo giro, in modo da allentare la tensione del filo ed evitare il rilascio indesiderato della clip durante l’introduzione. Per le applicazioni transanali è opportuno, per evitare il dolore durante l’introduzione dello strumento attraverso il canale anale, l’utilizzo di un anoscopio standard come introduttore, che viene poi retratto e resta lungo lo strumento durante la procedura. Se il tessuto dei margini della soluzione di continuo è soffice (come accade in caso di trattamento precoce), la manipolazione del tessuto può non essere necessaria, e può essere sufficiente la semplice aspirazione del tessuto all’interno del cappuccio. Se il difetto di parete è ampio, è preferibile l’utilizzo di una pinza a 3 branche, detta Twin Grasper (Ovesco GmbH, Tuebingen, Germany), che consiste in una singola pinza dotata di 2 branche che si aprono indipendentemente, in modo da poter retrarre entrambi i margini del difetto parietale utilizzando uno strumento con un unico canale operativo. Nel caso in cui i margini del difetto siano fibrotici, la retrazione del tessuto sclerotico richiede una forza particolare che può essere ottenuta, per orifizi relativamente piccoli (fino a 5 mm di diametro), utilizzando un retrattore ad ancora, detto Anchor, che viene aperta direttamente all’interno dell’orifizio. Occorre prestare attenzione a non rilasciare la clip sulla pinza, per cui è necessario retrarla finche non la si vede comparire fuori dall’orifizio. Un ulteriore accorgimento, importante per la corretta applicazione dell’OTSC, è far aderire l’intera circonferenza del cappuccio ai margini del difetto di parete; è quindi necessario posizionare il cappuccio e di conseguenza la punta dell’endoscopio, perpendicolare alla parete intestinale. Questo non è sempre facile, soprattutto nei tratti più stretti dell’intestino. In questi casi il posizionamento di una pinza o di un retrattore dedicato all’interno dell’orifizio può essere utile per mantenere la lesione al centro dell’angolo di visione e l’endoscopio perpendicolare alla parete. Se non controindicato, dovrebbe sempre essere applicato il modello più ‘’traumatico’’ della clip che ha delle punte sulle branche per un migliore ancoraggio ai tessuti. Il rilasciamento della clip è una procedura eseguita a 4 mani. Una vota che l’endoscopista ha affrontato il difetto ed eventualmente lo ha ancorato con una pinza o un retrattore, l’assistente tiene lo strumento in posizione mentre l’endoscopista ruota la manopola finchè la clip non viene rilasciata dal cappuccio. Nel caso la clip non sia stata rilasciata in maniera appropriata sull’obiettivo e c’è il sospetto che l’orifizio fistoloso sia ancora presente, si può iniettare mezzo di contrasto idrosolubile per verificarlo. Nel caso poi che l’OTSC non sia correttamente posizionata, questa può essere rimossa. In ogni caso, però, la forza sviluppata dalla clip è elevata e la sua rimozione non è così semplice come per le altre clip endoscopiche. Si consiglia di raffreddarla irrigandola con acqua fredda (può essere opportuno tenerne sempre un certa quantità in frigo in previsione della procedura). Dopo qualche minuto dall’irrigazione la clip perde parte della sua forza e può essere portata via dal tessuto con una normale pinza da corpo estraneo così da lasciare il tessuto libero per l’applicazione di una nuova clip. Corrispondenza Alberto Arezzo Dipartimento di Scienze Chirurgiche Università di Torino Corso Dogliotti, 14 - 10126 Torino Tel. + 39 335 8378243 Fax + 39 011 6336641 e-mail: [email protected] Bibliografia 1.Law WI, Chu KW, Ho JW, Chan CW. Risk factors for anastomotic leakage after low anterior resection with total mesorectal excision. Am J Surg 2000;179:92-6. 2.Rullier E, Laurent C, Garrelon JL et al. Risk factors for anastomotic leakage after resection of rectal cancer. Br J Surg 1998;85:355-58. 3.Alves A, Panis Y, Trancart D et al. Factors associated with clinically significant anastomotic leakage after large bowel resection: multivariate analysis of 707 patients. World J Surg 2002;26:499-502. 4.Lipska MA, Bissett IP, Parry BR, Merrie AE. Anastomotic leakage after lower gastrointestinal anastomosis: men are at a higher risk. ANZ J Surg 2006;76:579-85. 5.Biondo S, Pares D, Kreisler E et al. Anastomotic dehiscence after resection and primary anastomosis in left-sided colonic emergencies. Dis Colon Rectum 2005;48:2272-280. 6.Platell C, Barwood N, Dorfmann G, Makin G. The incidence of anastomotic leaks in patients undergoing colorectal surgery. Colorectal Dis 2007;9:71-79. IF Iniziative Formative > Tecniche endoscopiche 14. Weidenhagen R, Gruetzner KU, Wiecken T, Spelsberg F, Jauch KW. Endoluminal vacuum therapy for the treatment of anastomotic leakage after anterior rectal resection. Rozhl Chir. 2008 Aug;87(8):397-402. 15. Mees ST, Palmes D, Mennigen R, Senninger N, Haier J, Bruewer M. Endo-vacuum assisted closure treatment for rectal anastomotic insufficiency. Dis Colon Rectum. 2008 Apr;51(4):404-10. 16.Bonin EA, Baron TH Update on the indications and use of colonic stents. Curr Gastroenterol Rep 201012:374-382 Grupka MJ, Benson J Endoscopic clipping. J Dig Dis. 2008 May;9(2):72-8. 17.Trecca A, Gaj F, Gagliardi G. Our experience with endoscopic repair of large colonoscopic perforations and review of the literature. Tech Coloproctol. 2008 Dec;12(4):315-21; discussion 322. 18. Kirschniak A, Kratt T, Stüker D, Braun A, Schurr MO, Königsrainer A. A new endoscopic over-the-scope clip system for treatment of lesions and bleeding in the GI tract: first clinical experiences. Gastrointest Endosc. 2007 Jul;66(1):162-7. 19. Kirschniak A, Subotova N, Zieker D, Königsrainer A, Kratt T. The Over-The-Scope Clip (OTSC) for the treatment of gastrointestinal bleeding, perforations, and fistulas. Surg Endosc. 2011 Sep;25(9):2901-5. 20.Weiland T, Fehlker M, Gottwald T, Schurr MO. Performance of the OTSC System in the endoscopic closure of iatrogenic gastrointestinal perforations: a systematic review. Surg Endosc 2013 Jul;27(7):2258-74. Giorn Ital End Dig 2014;37:43-47 7. Choi HK, Law WL, Ho JW. Leakage after resection and intraperitoneal anastomosis for colorectal malignancy: analysis of risk factors. Dis Colon Rectum 2006;49:1719-725. 8.Matthiessen P, Hallböök O, Rutegård J, Simert G, Sjödahl R. Defunctioning stoma reduces symptomatic anastomotic leakage after low anterior resection of the rectum for cancer: a randomized multicenter trial. Ann Surg. 2007 Aug;246(2):207-14. 9.Gastinger I, Marusch F, Steinert R, Wolff S, Koeckerling F, Lippert H. Protective defunctioning stoma in low anterior resection for rectal carcinoma. Br J Surg 2005;92:1137-42. 10.Khan AA, Wheeler JM, Cunningham C, George B, Kettlewell M, Mortensen NJ. The management and outcome of anastomotic leaks in colorectal surgery. Colorectal Dis 2007;10:587-92. 11.Mala T, Nesbakken A. Morbidity related to the use of a protective stoma in anterior resection for rectal cancer. Colorectal Dis 2008;10:785-8. 12.Chopra SS, Mrak K, Hünerbein M. The effect of endoscopic treatment on healing of anastomotic leaks after anterior resection of rectal cancer. Surgery. 2009 Feb;145(2):182-8.doi:10.1016/j. surg.2008.09.012. Epub 2008 Dec 23. 13.van Koperen PJ, van Berge Henegouwen MI, Rosman C, Bakker CM, Heres P, Slors JF, Bemelman WA. The Dutch multicenter experience of the endo-sponge treatment for anastomotic leakage after colorectal surgery. Surg Endosc. 2009 Jun;23(6):1379-83. 47
Scaricare