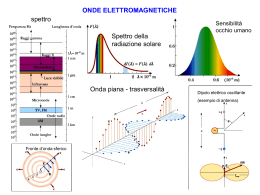
Spettroscopia e spettrometria molecolare UV-visibile Francesco Nobili Assorbimento di radiazione nella reg ione UV-Vis corrispondente al range di lunghezze d’onda 100-800 nm 10 -10 10 -8 Vacuum-UV UV-vis 10 -6 10 21 10 19 10 15 Elettroni esterni Vibrazioni 10 -4 Onde radio (NMR) Elettroni interni 10 17 Infrarosso Micro-onde ν/Hz molecole Raggi X 10 -12 atomi λ/m 10 13 10 -2 10 11 10 0 10 9 Rotazioni Spin nucleari 10 2 10 7 I livelli energetici coinvolti sono i L I V E L L I E L E T T R O N I C I D I A T O M I E M O L E C O L E che abbiano o rbita li es terni a bba s ta nza vic ini da dare transizioni a questi valori di energia come: -m eta lli di tra ns izioni (elettro ni d o f) -m o lec o le org a nic he (leg a m i m ultipli, elettro ni π , σ , n) -c o m ples s i m eta llo -org a nic i 3 FO R M A Z I O N E D E G L I OR B ITA LI M OLE C OLA R I P er combinazione lineare deg li orbitali atomici s or p atomic orbital non-bonding orbital σ or π molecular orbital Energy σ* or π* molecular orbital 4 2 orbitali σ da 2 orbitali s 5 2 o rbita li π da 2 o rbita li p y o p z o rbita li σ da 2 o rbita li p x 6 G li orbitali molecolari n di non legame si formano invece a partire dagli orbitali atomici popolati dagli elettroni che non partecipano alla formazione di legami 7 •Le trans izioni che richiedono minore energia coinvolgono l’Highes t O ccupied M olecular O rbital (H O M O ) e il Lowest Unoccupied M olecular O rbital (L U M O ) e s ono per ques to motivo le più importanti. •Alcune trans izioni NO N s ono pos s ibili (trans izioni proibite) a caus a di precise regole di s elezione; in effetti le trans izioni proibite s ono oss ervate, ma hanno un’intens ità molto bas s a. 8 Trans izioni che riguardano alcuni leg ami chimici: σ σ* alcani σ π * carbonili π π *alcheni, carbonili, alchini, azomposti n σ* oss igeno, azoto, zolfo, alogeni n π * carbonili 9 T ra ns izio ni elettro nic he m o lec o la ri Le transizioni elettroniche più comuni sono illustrare nella figura sottostante. E sse si verificano se nel campione s ono presenti molecole aventi cromofori, cioè gruppi funzionali in grado di as sorbire la radiazioni UV-sis ibile, come il gruppo – NO 2 (nitro), -N 2- (azo) S olo le trans izioni di elettroni n e π hanno energ ie nel rang e 200-800 nm, quindi rivelabili con l’UV-visibile 10 G ruppi cromofori Alcuni esempi di g ruppi c rom o fori con i relativi coefficienti di estinzione molare o ass orbività molare (ε) Transizione λmax, nm Cromoforo Esempio ε Solvente C=C Etene π → π* 171 15,000 esano C≡C 1-Esino π → π* 180 10,000 esano C=O Etanale n → π* π → π* 290 180 15 10,000 esano N=O Nitrometano n → π* π → π* 275 200 17 5,000 etanolo C-X X=Br X=I Metil bromuro o ioduro n → σ* n → σ* 205 255 200 360 esano 11 Le transizioni elettroniche promosse dalla radiazione UV-Vis-NIR coinvolgono anche i vari livelli vibrazionali. P er questo motivo lo s pettro è a ba nde Q ues ta caratteristica complica notevolmente il riconoscimento e la quantificazione di composti in miscela E sempio di spettro UV-visibile di un’aldeide insatura. La banda a 395 nm rende conto del fatto che il compos to è colorato in a ra nc io , colore complementare rispetto al violetto che corris ponde alla regione spettrale interes sata (~ 400 nm) Le bande di assorbimento in UV-Vis-NIR sono in numero minore rispetto all’IR , tuttavia è possibile utilizzarle per effettuare determinazioni quantitative secondo la 12 legge di Lambert-B eer Il massimo di assorbimento (λmax) di un cromoforo può essere influenzato da: -s truttura della molecola di cui fa parte -a m biente (s olvente) di cui fa parte E sempio (A) benzene (vapore) (B ) nitrobenzene (vapore) (C ) benzene (in acqua) 13 Le molecole organiche presentano spesso gruppi cromofori dovuti alla presenza di s is tem i I N S A T U R I L’energia (frequenza lunghezza d’onda) della radiazione assorbita dipende dalla differenza energ etic a Δ E tra l’o rbita le H O M O e l’o rbita le L U M O In generale, la C O N I U G A Z I O N E D I LE G AM I INS ATUR I provoca una diminuzione del ΔE e un A U M E N T O DE LLA ε 14 15 FA T T O R I C H E I N FL U E N Z A N O L ’I N T E N S I T A ’ D I U N A B A N D A Il valore del c oeffic iente di es tinzione m ola re ε di un cromoforo dipende da quattro fattori 1. pro ba bilità della tra ns izione elettronica 2. va ria zione del m om ento di dipolo elettric o ass ociata alla trans izione 1. natura del s o lvente 2. tipo di s o s tituenti 16 1. P ro ba bilità della tra ns izio ne G eneralmente, le tra ns izioni π π * s ono più pro ba bili delle nπ * :O : Ad es empio, l’acetone ha due ass orbimenti ππ* λmax = 188nm ε = 10000 nπ* λmax = 279nm ε = 14.8 2. V a ria zio ne del m o m ento di dipo lo elettric o Nella trans izione nπ* lo s tato eccitato coinvolge solo l’atomo di oss igeno, mentre nella tra ns izione π π * il pa s s a g g io a llo s ta to ec c ita to c orris ponde a lla form a zione di una s truttura a s epa ra zione di c a ric a aumento di ε 17 3. na tura del s olvente Il s olvente es ercita un’a zione a bba s ta nza lim ita ta s ulla ε Ad es empio, la banda a 279 nm dell’acetone in n-es ano ha ε = 14.8 In acqua s i s pos ta a 264.5 nm ed ha ε = 17.4 4. tipo di s o s tituenti I s ostituenti pres enti pos s ono modificare l’as s etto elettronico influendo direttamente s ui fattori 1 e 2 (probabilità, s eparazione di carica) Q ua ndo a um enta no la ε s i pa rla di effetto iperc rom o Q ua ndo dim inuis c ono la ε s i pa rla di effetto ipoc rom o 18 FA T T O R I C H E I N FL U E N Z A N O LA POS IZ ION E DI U N A B AN DA La posizione di una banda di ass orbimento nell’UV è influenzata da: - sos tituenti pres enti nella molecola - ambiente (solvente) in cui la molecola si trova S i possono avere vari tipi di effetto 1. effetto ba toc rom o – R E D S H I FT 1. effetto ips oc rom o – B L U S H I FT 1. effetto a ux oc rom o 1. effetto s o lvente 1. effetti s teric i 19 1. E FFE T T O B A T O C R O M O (R E D S H I FT ) S postamento a lunghezze d’onda maggiori (verso il rosso, energie inferiori) della λmax. D ovuto a sistemi coniugati insaturi e sostituenti alchilici su anello benzenico 20 E s em pio: effetto della c oniug a zione L’aumento della coniugazione (e della delocalizzazione degli elettroni) porta ad una progres s iva diminuzione della ΔE tra l’orbitale HO M O (s tato fondamentale) e l’orbitale LUM O (s tato eccitato) Ad es empio, per i P O L I E N I H3C CH3 H3C CH3 ecc. H3C n CH3 21 Un analogo andamento si ha per gli A N E L L I A R O M A T I C I C ON DE N S A TI 22 2. E FFE T T O I P S O C R O M O (B L U E S H I FT ) E ’ dovuto ad un sostituente (ipsocromo) che s posta l’assorbimento del cromoforo a λ più ba s s e (energie coinvolte maggiori) E sempio: a nilina in ambiente acido in s o luzione a c quos a leg g erm ente a c ida per HC l in n-pro pa nolo in s o luzione netta m ente a c ida 23 3. E FFE T T O A U X O C R O M O E ’ dovuto ad un gruppo funzionale (auxocromo) s aturo (senza elettroni π) che quando è legato ad un cromoforo determina una variazione, in genere un a um ento , s ia della λ c he della ε Q ues to effetto è dovuto alla presenza di do ppietti liberi di no n leg a m e (come nei gruppi – O H, -NH 2, -C l, ecc.) che di per sé non assorbono nella regione UV-Vis, ma po s s o no P A R T E C I P A R E A L L A C O N I U G A Z I O N E degli elettroni contenuti nei cromofori 24 4. E FFE T T O S O L V E N T E Il solvente può variare i livelli energetici in una molecola. Le proprietà determinanti a questo proposito sono la po la rità e la c a pa c ità di fo rm a re leg a m i idro g eno Il solvente influisce stabilizzando o destabilizzando lo stato fondamentale o lo stato eccitato. Lo s ta to ec c ita to è uno s ta to a s epa ra zio ne di c a ric a , quindi l’effetto della polarità è nell’a bba s s a re l’energ ia dello s ta to ec c ita to e quindi fa vo rire una tra ns izio ne π π * (red s hift) In generale, qua ls ia s i intera zio ne dipo la re (c om e il leg a m e idro g eno ) pro vo c a una s ta bilizza zio ne dello s ta to ec c ita to Inoltre, l’instaurarsi di interazioni tra un solvente polare e un soluto aromatico può portare ad a ltera zio ni del s is tem a a ro m a tic o (visibili ad esempio con la scomparsa della “struttura fine” dei segnali generati dagli anelli benzenici) 25 spettri di assorbimento del feno lo in n-penta no λmax = 271 nm struttura fine in a c qua λmax = 271 nm perdita della struttura fine in N a O H 0.5 N λmax = 285 nm red-shift 26 Q uando si parla di solvente, ovviamente dobbiamo tenere in considerazione anche la T R A S P A R E N Z A del solvente nell’intervallo di λ in es ame 27 5. E FFE T T I S T E R I C I Anche le interazioni dovute all’ingombro sterico dei gruppi funzionali possono influenzare i livelli energetici delle transizioni elettroniche S e la c o pla na rità dei s is tem i π viene perturba ta da lla pres enza di g ruppi di g ra ndi dim ens io ni, λm a x viene s po s ta to vers o lung hezze d’o nda più c o rte in seguito a diminuzione della delocalizzazione (e diminuisce anche ε perché diminuisce la probabilità della transizione) R R' λmax = 246 nm εmax = 20000 λmax = 250 nm εmax = 2000 28 C L A S S I FI C A Z I O N E D E L L E PR IN C IPA LI TR A N S IZ ION I E LE TTR ON IC H E T ra ns izio ni R trans izioni n σ * e n π * di S I N G O L I G R U P P I C R O M O FO R I (ra dic a lic he) come il carbonile o il nitro gruppo. S ono trans+Oizioni Oproibite dalle regole di selezione bassa assorbività N molare O T ra ns izio ni K (di c o niug a zione) trans izioni π π * di S I S T E M I C O N I U G A T I (es. butadiene). Appaiono anche negli spettri di molecole aromatiche con sostituenti c romofori. Non sono influenzate dalla polarità del solvente T ra ns izio ni B trans izioni π π * caratteristiche di molecole A R O M A T I C H E ed (ba nde benzenoidi) eteroaromatiche. Il benzene ha ad esempio una banda nel vicino UV tra 230 e 270 nm. P resentano s truttura fine dovuta all’interazione dei sottolivelli vibrazionali T ra ns izio ni E trans izioni π π * caratteristiche di molecole A R O M A T I C H E . Nel (ba nde etilenic he) benzene tra 180 e 200 nm. E teroatomi con doppietti 29 elettronici spostano la λmax a valori più alti T ra ns izio ni σ σ * S ono quelle che richiedono le energie più elevate perché corrispondono alla ro ttura di leg a m i σ . S ono caratteristiche di molecole come gli a lc a ni s a turi che contengono solo legami C -C o C -H. D anno assorbimenti nella zona dell’UV lontano, detto anche U V s o tto vuo to (l’O 2 dell’aria assorbirebbe nella stessa regione) T ra ns izio ni do vute a tra s ferim ento di c a ric a S ono le più intense dello spettro. Nell’intervallo 220-370 nm a ro m a tic i s o s tituti Nel vis ibile c o m po s ti di c o ordina zio ne 30 31 A S S OR B IM E N TO DA S PE C IE IN OR G A N IC H E M olti metalli di trans izione liberi, s otto forma di ioni o c o m ples s i, as s orbono nella regione vis ibile dello s pettro 32 tribuzione della dens ità elettro nic a neg li o rbita li d che caratterizzano i metalli ransizione Q uando lo ione è “nudo”, i 5 orbitali d sono D E G E NE R I: hanno tutti la stessa energia indipendentemente dall’orientamento spaziale I n pres enza di leg a nti, a seconda della geometria (ottaedrica, tetraedrica, planare quadrata) s i c rea una differenzia zio ne tra le energ ie deg li o rbita li d. La radiazione UV-Vis può essere assorbita per promuovere transizioni di elettroni tra questi orbitali 33 34 35 D ifferenti leg a nti c a us a no differenti s plitting Δ E per le tra ns izio ni d-d I-<B r-<C l-<F -<H 2O <NH 3<etilen diammina<C N C olori dei complessi del C o2+ : c o n C l -1 (blue) Δ E m a g g io re c o n B r-1 (blue/verde) Δ E m o dera to c o n I -1 (g reen/yello w ) Δ E m ino re 36 S TR U M E N TA Z ION E - A PPLIC A Z ION I S pettrofotometri a singolo o doppio raggio possono essere utilizzati per misurare l’assorbanza o la trasmittanza dei campioni S i può operare a lunghezza d’onda fissa o in funzione della lunghezza d’onda, si possono effettuare a na lis i qua lita tive (s truttura li) o qua ntita tive 37 R I C E R C A D E I C R O M O FO R I E D E L L A S TR U TTU R A M OLE C OLA R E D a un punto di vis ta Q U A L I T A T I V O , l’a na lis i in a s s o rbim ento U V -V is è in grado di fornire indicazioni (tramite la λmax e la ε) solo sulla presenza di alcuni gruppi funzionali ma no n può po rta re a ll’identific a zio ne di una m o lec o la Alcuni punti da tenere presenti: -assorbimenti molto forti nell’intervallo 200-300 nm : sistemi di almeno due c ro m o fo ri c o niug a ti -assorbimenti piuttosto forti nella zona 270-370 nm : sistemi a ro m a tic i c o n s o s tituenti po la ri -assorbimenti deboli o di media forza nell’intervallo 210-300 nm : sistemi a ro m a tic i c o n s o s tituenti a lc hilic i, ma anche transizioni nσ * di a to m i c he po s s iedo no do ppietti di no n leg a m e -assorbimenti molto deboli nella zona 200-300 nm : transizioni nπ * a carico dei gruppi N =O , C =O , N =N , C =S , ecc. -assorbimenti molto forti verso il vis ibile: bande di tra s ferim ento di c a ric a intermolecolari o intramolecolari -l’unic a info rm a zio ne dec is iva è il da to N E G A T I V O : se queste bande 38 sono assenti, si può escludere la presenza nella molecola dei corrispondenti 39 40 C A R A T T E R I Z Z A Z I O N E E D I D E N T I FI C A Z I O N E In linea di massima lo spettro elettronico non è abbastanza selettivo per caratterizzare una molecola; per distinguere tra sostanze molto simili si possono comunque utilizzare due accorgimenti per a um enta re la “qua lità ” dell’info rm a zio ne fornita : (1) Q uo zienti di a s s o rba nza (2) S pettri in deriva ta QU OZ IE N TI DI A S S OR B A N Z A S i misura il ra ppo rto tra l’a s s o rba nza a d una lung hezza d’o nda nell’into rno del punto di m a s s im o e l’a s s orba nza a lung hezze d’o nda vic ino a i punti a m età a ltezza (in sostanza si misura la FO R M A del picco) I valori ottenuti sono valori TAB ULATI e C AR ATTE R IS TIC I P E R O G NI S P E C IE C HIM IC A 41 S PE TTR I IN DE R IV A TA S e il rumore di fondo è abbastanza basso, registrando le derivate del segnale (solitamente la derivata seconda) si possono ottenere dei vantaggi: -a um ento della ris o luzio ne: picchi parzialmente sovrapposti pos sono essere separati -dis c rim ina zio ne vers o la la rg hezza della ba nda : bande più s trette presenteranno derivate più pronunciate si esalta la differenza tra bande strette e bande larghe 42 A N A LIS I QU A N TITA TIV A S i basa sulla legge di Lambert-B eer: A = εlc La specie chimica deve essere in grado di assorbire la radiazione UV-Vis, quindi: -deve contenere un c ro m o fo ro oppure -deve essere opportunamente tra tta ta per contenere un cromoforo eliminazione interferenti regolazione pH (tamponi) stabilizzazione specie chimica aggiunta reattivo per formazione cromoforo 43 S C E L T A D E L L A L U N G H E Z Z A D ’O N D A Il monocromatore non lascia mai passare una singola lunghezza d’onda, ma un range di lunghezze d’onda A seconda della zona dello spettro, allo stesso range Δλ possono corrispondere diversi errori nell’assorbanza ΔA Le zone migliori (Δ A m inim o ) sono s ui m a s s im i o s ui m inim i meglio il massimo perché A è maggiore Inoltre, è preferibile scegliere una λ tale che l’assorbimento da parte di interferenti (matrice) sia minimo Q uindi B è meglio di R 1 spettro di ass orbimento della s ostanza 2 spettro di ass orbimento della matrice 44 DE V IA Z ION I DA LLA LE G G E DI B E E R S ono deviazioni apparenti e possono es sere: - s trum enta li : derivano dalla larghezza di banda del monocromatore la radiazione non è mai puramente monocromatica, e l’assorbività è variabile. A s econda della pos izione sul picco, questa deviazione dipenderà in mis ura maggiore o minore dalla larghezza di banda. In assoluto, comunque, è il rapporto tra la larghezza di banda e la larghezza del picco ad influire s ulla deviazione In questa zona l’assorbanza media non dipende dalla larghezza di banda In questa zona l’assorbanza media dipende dalla larghezza di banda, ma le variazioni in assoluto sono minori 45 -c him ic he: sono dovute allo spostamento di un equilibrio che coinvolge una specie assorbente E sempio: 2C rO 42- + 2H + 2HC rO 4- C r2O 72- + H 2O Lo ione bicromato assorbe a 450 nm D iluendo la soluzione, l’equilibrio si sposta verso sinistra All’aumentare del pH l’equilibrio si sposta verso sinistra: aggiungendo KO H 0.05 M tutto il cromo è convertito a cromato Il controllo del pH è necessario O ppure, se sono presenti complessi, dobbiamo ess ere certi che la formazione del complesso sia quantitativa: legante libero in un eccesso di circa 100 volte rispetto all’analita in esame 46 A N A LIS I A L PU N TO IS OS B E S TIC O R osso fenolo: Forma acida gialla massimo a 433 nm Forma basica rossa massimo a 558 nm P unti is o s bes tic i a 338, 367, 480 nm ( 480 480 A480 = ε HIn b [ HIn ] + ε In480- b In - = ε HIn b [ HIn ] + In - ) A l punto is o s bes tic o l’a s s orbività m o la re no n dipende da lla c o nc entra zio ne rela tiva delle s pec ie c o invo lte m a S O L O DA LLA LOR O C ON C E N TR A Z ION E TOTA LE L’esistenza di un punto isos bestico durante una reazione chimica costituisce una buona prova del fatto che sono presenti due specie principali 47 M E TODI DI A N A LIS I 1. M E T O D O D E G L I S T A N D A R D E S T E R N I 2. M E T O D O D E L L E A G G I U N T E D I S T A N D A R D (1) (2) 48 T I T O L A Z I O N I FO T O M E T R I C H E Il cambiamento dell’assorbanza di una soluzione durante una titolazione può ess ere utilizzato per seguirne il decorso. L’assorbanza (additiva) di ogni specie chimica coinvolta (analita, titolante, prodotto) è direttamente proporzionale alla sua concentrazione La curva A vs V di titolante fornirà il punto equiva lente a ll’inters ezio ne di due tra tti rettilinei (a) S olo il titolante as sorbe: titolazione di As(II) con bromato-bromuro (b) Il prodotto di reazione assorbe: titolazione di C u(II) con E D TA (c) L’analita (assorbente) è convertito in un prodotto che non as sorbe: titolazione di ptoluidina in butanolo con HC lO 4 a 290 nm (e) L’analita colorato è convertito in un prodotto incolore da un titolante colorato (d)-(f) Il legante aggiunto forma due complessi successivi a differenti as sorbività L’assorbanza va corretta per il FA T T O R E D I D I L U Z I O N E : A corr=A obs ·(V+v)/V 49 S P E T T R O FO T O M E T R I A D I FL U O R E S C E N Z A E FO S FO R E S C E N Z A Q ues to tipo di spettrofotometria sfrutta i pro c es s i di fo to lum ines c enza : -fluo res c enza riemessa una radiazione a lunghezza d’onda maggiore ris petto a quella as sorbita, senza transizioni di spin -fo s fo res c enza riemessa una radiazione a lunghezza d’onda maggiore rispetto a quella as sorbita, C O N TR ANS IZIO NI D I S P IN tempi più lunghi 50 A s s o rbim ento passaggio dal livello vibrazionale fondamentale del livello elettronico fondamentale ad un livello vibrazionale eccitato del livello elettronico eccitato E m is s io ne pass aggio dal livello vibrazionale fondamentale del livello elettronico eccitato ad un livello vibrazionale eccitato del livello elettronico fondamentale picchi simmetrici che riflettono la spaziatura simile, nei due livelli elettronici, dei livelli vibrazionali 51 T em po di vita di uno stato di s ing o letto ec c ita to : 10-8 - 10 -4 s tempo di vita della fluo res c enza T em po di vita di uno stato di tripletto ec c ita to : 10 -4 - 10 2 s tempo di vita della fo s fo res c enza : è una transizione proibita. Altri processi possono verificarsi più velocemente resa molto bassa La radiazione di fotoluminescenza è sempre a lunghezza d’onda maggiore (energia minore) della radiazione incidente Nel caso della fosforescenza, la lunghezza d’onda è ancora maggiore perché lo stato di tripletto deve trovarsi ad energia minore rispetto al primo stato di singoletto eccitato affinché si verifichi l’intersytem crossing 52 C a ra tteris tic he delle s pettro s c o pia di fluores c enza : - A lta s ens ibilità misurata rispetto ad un background pari a circa zero - A lta s pec ific ità doppia selettività in eccitazione ed emissione possibilità di misurare il tempo di vita della fluorescenza possibilità di monitorare una radiazione di fluorescenza sopra ad un background non fluores cente P rocedura comunemente seguita per misurare gli spettri di eccitazione e di emissione: 1) C i si posiziona, tramite il monocromatore di ec c ita zio ne, ad una qualsiasi lunghezza d’onda di eccitazione capace di provocare fluorescenza 2) S i effettua una s cansione con il m o no c ro m a to re di em is s io ne e si registra uno s pettro di em is s ione 53 1) C i si posiziona con il m o no c ro m a to re di em is s io ne alla lunghezza d’onda per cui l’intensità di fluorescenza è mas sima 2) S i effettua una s cansione con il m o noc ro m a to re di ec c ita zio ne registrando lo s pettro di ec c ita zio ne 3) C i si posiziona con il m o no c ro m a to re di ec c ita zio ne alla lunghezza d’onda per cui l’a s s o rbim ento è m a s s im o 4) S i effettua una s cansione con il m o noc ro m a to re di em is s io ne registrando lo s pettro di 54 R E L A Z I O N E C O N C E N T R A Z I O N E -I N T E N S I T A ’ D I FO T O L U M I N E S C E N Z A La P O T E N Z A E M E S S A in fluorescenza o fosforescenza è direttamente proporzionale alla potenza as sorbita (Φ F = resa di fluorescenza) PF = Φ F ( P٠ − P ) P er valori di assorbanza molto piccoli (A<0.07), si arriva ad una relazione di proporzionalità diretta tra potenza di fluores cenza e concentrazione PF = Φ F P٠ε bc All’aumentare della concentrazione oltre certi limiti si ha autoassorbimento e la curva cambia pendenza, finché tutta la radiazione incidente viene as sorbita, ed una frazione viene riemes sa indipendentemente dalla concentrazione della soluzione PF = Φ F P٠ε bc PF = Φ F P٠ Range di linearità piuttosto stretto 55 In pratica il segnale registrato dal detector è ridotto di altri contributi, dovuti all’A N G O L O S O L I D O visto dal detector e dall’E FFI C I E N Z A del detector (funzione della lunghezza d’onda) F = P٠ f ( Φ ) g( λ ) Φ F ε bc L’intensità di fluorescenza registrata sarà data dal prodotto dei tre fattori (potenza emessa, angolo solido, efficienza del detector) Nell’equazione di Lambert-B eer che descrive l’assorbimento il termine geometrico b non si riferisce al cammino ottico del raggio incidente, ma al vo lum e s o lido interc etta to da lle fenditure in ing res s o ed in us c ita , che definiscono la parte di soluzione direttamente coinvolta nei processi di assorbimento-emissionerilevazione del segnale 56 S TR U M E N TA Z ION E P revede il detector posizionato fuori asse rispetto al raggio incidente (di solito a 90°) ed un doppio monocromatore per garantire la doppia selettività in eccitazione ed in emissione 57 S P E T T R O FL U O R I M E T R I S elezionano le lunghezze d’onda di eccitazione e di fluorescenza mediante monocromatori a reticolo nel range UV-vis 200-800nm Il monocromatore in eccitazione di solito è centrato a lunghezze d’onda più bas se rispetto a quello in emis sione. E s.: 300 vs 500nm 58 Negli s pettro fluo rim etri a s ing o lo ra g g io gli spettri di eccitazione e di emissione saranno una combinazione degli spettri “veri”, della distribuzione spettrale dell’emissione della lampada, dell’efficienza dei monocromatori, e della distribuzione spettrale della risposta del detector Nel “ra tio m o de”, una parte della luce di eccitazione è inviata al detector correzione relativa all’emissione della lampada Nella s pettro fluo rim etria differenzia le si opera analogamente agli spettrofotometri a doppio raggio: correzione per tutti gli elementi (lampada, monocromatori, detector) limite della velocità del chopper 59 S PE TTR OC OPIA DI LU M IN E S C E N Z A TOTA LE S i registra l’intens ità in funzio ne di T U T T E le lung hezze d’o nda di ec c ita zio ne di em is s io ne spettri bidimens ionali che permettono di correlare direttamente i risultati e di osservare simmetrie ed anomalie impronta digitale del campione dovuta alla DOPPIA S E LE TTIV ITA ’ 60 S TR U M E N TA Z ION E PE R M IS U R E DI FO S FO R E S C E N Z A S i utilizzano celle che possono essere refrigerate basse temperature per registrare la fosforescenza: la molecola eccitata ha più tempo prima di tornare allo stato fondamentale ed aumenta così la probabilità che si verifichi la transizione di inter-system crossing D elay tra l’eccitazione e la registrazione del segnale di fosforescenza per tagliare la radiazione di fluorescenza (che è più rapida) P er ottenere il delay si può rotare la cella (a) o lo shutter (b) 61
Scaricare