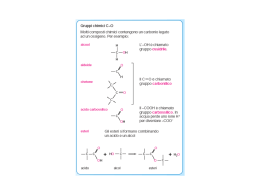
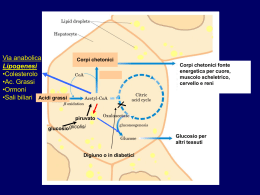
IL TESSUTO ADIPOSO vLa funzione del tessuto adiposo, che è costituito da adipociti, è quella di garantire all’organismo animale una riserva di energia, prontamente disponibile quando l’organismo ne ha bisogno. Detta riserva è costituita da trigliceridi che vengono immagazzinati negli adipociti come goccioline di grasso. ØI Lipidi sono apolari (idrofobici), solubili in solventi organici ed insolubili in acqua ØGli acidi grassi sono costituiti da catene idrocarburiche che terminano con un gruppo carbossilico ØUn acido grasso con 16-C: Ø CH3(CH2)14-COOnonnon-polare polare ØNegli acidi grassi insaturi, i doppi legami hanno in genere una configurazione cis ØLa maggior parte degli acidi grassi naturali hanno un numero pari di atomi di carbonio Un acido grasso C-16 con un doppio legame cis tra gli atomi di C 9-10 viene rappresentato come 16:1 cis ∆9. 14:0 16:0 18:0 18:1 18:2 18:3 20:4 20:5 acido miristic acido palmitico acido stearico cis∆ cis∆9 acido oleico cis∆ cis∆9,12 acido linoleico cis∆ cis∆9,12,15 acido α-linonenico cis∆ cis∆5,8,11,14 acido arachidonico cis∆ cis∆5,8,11,14,17 acido eicosapentaenoico (un omegaomega-3) Un trigliceride IL TESSUTO ADIPOSO La funzione del tessuto adiposo è quella di garantire all’organismo animale una riserva di energia, prontamente disponibile quando ne ha bisogno. Detta riserva è costituita da trigliceridi che vengono immagazzinati negli adipociti come goccioline di grasso. La secrezione nel sangue di ormoni come il glucagone (o l’adrenalina) stimola gli adipociti a trasformare i trigliceridi immagazzinati in glicerolo e acidi grassi liberi che vengono rilasciati nel sangue. Questi ormoni, agendo su un recettore di membrana, stimolano la produzione dell’AMP ciclico (2° messaggero) il quale va ad attivare la lipasi degli adipociti (lipasi ormono-sensibile). Tale enzima catalizza l’idrolisi completa dei trigliceridi. La reazione catalizzata dalla lipasi degli adipociti (ormono-sensibile) : 3 molecole di acqua attaccano i 3 legami di estere contenuti nei trigliceridi rompendoli per idrolisi. I prodotti della reazione sono 3 molecole di acidi grassi liberi e una molecola di glicerolo Gli acidi grassi liberi ed il glicerolo vengono rilasciati nel sangue. Mentra il glicerolo viene recuperato e metabolizzato dal fegato, gli acidi grassi si legano all’albumina del sangue (l’albumina è il trasportatore ematico deli acidi grassi nonesterificati), che li trasporta fino alle reti capillari dei tessuti utilizzatori (cuore, muscolo, …). Gli acidi grassi liberi (non esterificati) passano attraverso la membrana plasmatica delle cellule ed entrano nel citoplasma dove vengono attivati dalla acil-CoA sintetasi per prepararli al successivo metabolismo (vedi ad esempio la β-ossidazione). CATABOLISMO DEGLI ACIDI GRASSI Il catabolismo degli acidi grassi consiste nella parziale ossidazione che avviene con la β-ossidazione e che trasforma l’acido grasso in molte molecole di acetilCoA. Quindi l’acetil-CoA entra nel ciclo di Krebs dove viene completamente ossidato producendo molecole dei coenzimi ridotti NADH e FADH2. Questi coenzimi, che vengono prodotti anche ad ogni ciclo diella βossidazione, trasportano elettroni alla catena respiratoria che è accoppiata alla fosforilazione ossidativa, il processo mitocondriale che produce la massima parte dell’ATP cellulare in molti tessuti. Gli acidi grassi, utilizzati nel metabolismo ossidativo, vengono forniti alle cellule come acidi grassi liberi (non esterificati) con due modalità distinte: Ø dai complessi acidi grassi liberi-albumina; Ø dalle lipoproteine plasmatiche (VLDL o chilomicroni): in questo caso i trigliceridi contenuti nelle lipoproteine vengono prima idrolizzati da una lipoproteina lipasi tissutale, aderente agli endoteli delle reti capillari, che si lega alle lipoproteine plasmatiche via l’apo-C2 e produce acidi grassi liberi e glicerolo. Solo gli acidi grassi vengono assunti dai tessuti. Il glicerolo viene assorbito dal fegato che è l’unico organo capace di metabolizzarlo, trasformandolo in molecole di glucosio o producendo energia. Schema della struttura di una lipoproteina plasmatica Esteri del colesterolo fosfolipidi colesterolo trigliceridi Apoproteina Densità e composizione delle lipoproteine plasmatiche Le lipoproteine plasmatiche (chilomicroni, VLDL, LDL, HDL) trasportano lipidi nel sangue. I chilomicroni e le VLDL sono da considerare trasportatori di trigliceridi: i chilomicroni quelli di origine esogena (alimenti) e le VLDL quelli di origine endogena (neosintesi degli acidi grassi da carboidrati e amino acidi nel fegato) Attivazione degli acidi grassi nel citoplasma e trasporto dell’acile nella matrice mitocondriale. Gli acidi grassi vengono prima attivati nel citoplasma da un enzima detto acil-coenzima-A-sintetasi, consumando ATP: CH3-(CH2)n-COOH + ATP + HSCoA (acido grasso) P∼Pi + H2 O CH3-CH2)n-CO-SCoA + P∼Pi + AMP (acil-cenzima-A) 2 Pi (pirofosfato) (nella reazione viene prodotto anche pirofosfato P∼Pi, che viene subito idrolizzato a Pi da una pirofosfatasi inorganica) Successivamente gli acili vengono trasferiti nel mitocondrio con un complesso processo di trasporto trans-membrana che richiede: Øcarnitina ((CH3)3-N+-CH2-CHOH-CH2-COOH, una piccola molecola organica Øun trasportatore di membrana (translocasi) Ødue enzimi (carnitina acil-transferasi-I e carnitina aciltransferasi-II) localizzati sui due lati della membrana mitocondriale interna. Inizialmente la carnitina aciltransferasi-I, che è localizzata sulla faccia esterna della membrana mitocondriale interna, catalizza il reasferimento dell’acile dall’acil-CoA alla carnitina producendo acil-carnitina. Questa viene traslocata nella matrice da un trasportatore di membrana, detto traslocasi, che contemporaneamente esporta carnitina dal mitocondrio. Infine, la carnitina aciltransferasi-II, che è localizzata sulla faccia interna della membrana mitocondriale interna, catalizza il trasferimento dell’acile dalla acil-carnitina al CoA mitocondriale formando acil-CoA nel mitocondrio. Questo subisce poi la β-ossidazione. BETA-OSSIDAZIONE DEGLI ACIDI GRASSI La β-ossidazione degli acidi grassi è una via metabolica localizzata nella matrice del mitocondrio. La sua funzione è quella di demolire ossidativamente gli acidi grassi trasformandoli in acetil-CoA (cioè frammentando le lunghe molecole di acidi grassi nel radicale dell’acido acetico (CH3CO), un composto con solo 2 atomi di carbonio, riducendo contemporaneamente molecole di FAD e NAD a FADH2 e NADH + H+. Reazioni della β-ossidazione Il primo enzima della β-ossidazione è una deidrogenasi flavinica che trasforma l’acil-CoA in un composto insaturo (∆2-enoil-CoA) trasferendo 2 dei suoi idrogeni sul FAD formando FADH2. Il secondo enzima addiziona una molecola di acqua al ∆2-enoil-CoA formando il βidrossi-acil-CoA. Il terzo enzima (una deidrogenasi piridinica) toglie 2 idrogeni a quest’ultimo metabolita, trasformadolo nel β-cheto-acil-CoA, formando anche NADH. L’ultimo enzima della via metabolica βossidazione è una tiolasi che, utilizzando una molecola di HSCoA, rompe il legame tra il secondo ed il terzo atomo di carbonio dell’acido grasso formando un frammento bicarbonioso (acetil-CoA) ed un nuovo acil-S-CoA accorciato di 2 atomi di carbonio. Questo viene ancora attaccato dal primo e poi dal secondo, terzo e quanto enzima che lo accorciano di nuovo finché tutta la molecola di acido grasso viene demolita ad acetil-CoA. Bisogna notare che ad ogni ciclo della β-ossidazione, oltre ad 1 molecola di acetil-CoA, si formano anche 1 molecola di FADH2 ed 1 di NADH. Come vi è noto, questi coenzimi trasportano gli elettroni alla catena respiratoria e per ogni molecola di NADH si formano 2,5 molecole di ATP, mentre per ogni molecola di FADH2 si formano 1,5 molecole di ATP. Questo significa che ad ogni ciclo di degradazione della β-ossidazione si formano 4 molecole di ATP, perché la β-ossidazione è accoppiata con il processo della fosforilazione ossidativa. Quindi per un acido grasso con 16 atomi di carbonio la β-ossidazione produce: CH3-(CH2)14-COOH =8 molecole di CH3-CO-S-CoA 7 molecole di FADH2 7 molecole di NADH Totale 80 molecole di ATP 10,5 molecole di ATP 17,5 molecole di ATP 108 molecole di ATP Da notare che, ossidando ogni molecola di CH3-CO-S-CoA vengono prodotte 10 molecole di ATP (vedi Ciclo di Krebs) e che nell’attivazione dell’acido grasso viene consumata 1 molecola di ATP trasformandola in AMP. Dato che per ricostruire l’ATP dall’AMP servono due fosforilazioni successive, il consumo cellulare di ATP nell’attivazione dell’acido grasso è di 2 molecole di ATP. Se sottraiamo queste 2 molecole di ATP spese per attivare l’acido grasso, la resa energetica globale che la cellula ricava dalla ossidazione completa (cioè a CO2 ed H2O) di una molecola di acido grasso con 16 atomi di carbonio (acido palmitico) è di 108 - 2 = 106 molecole di ATP. CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-COCO-SCoA) (punti di rottura della catena carboniosa degli acidi grassi) 8 molecole di CH3COCO-SCoA + 7 FADH2 + 7 NADH + 7 H+ Il numero di molecole di acetil-CoA, di FADH2 e NADH dipende dalla lunghezza della catena carboniosa dell’acido grasso. Degradazione degli acidi grassi a catena dispari: conversione del propionil-CoA in succinil-CoA
Scaricare