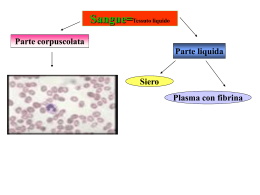
Dossier scientifico Quali marcatori utilizzare per valutare l’efficacia dell’immunoterapia specifica? La ricerca nel campo dei marcatori biologici per valutare l’efficacia della desensibilizzazione ha suscitato l’attenzione di numerosi team scientifici. Così come l’efficacia è stata dimostrata dai punteggi clinici e di consumo dei farmaci, dalla funzionalità respiratoria e dai punteggi di qualità della vita, la dimostrazione di variazioni significative dei marcatori biologici aiuterebbe a comprendere meglio la fisiopatologia della desensibilizzazione. L’effetto di desensibilizzazione sulle immunoglobuline dei livelli di IgG4. Tuttavia, la correlazione con l’efficacia clinica dell’aumento di anticorpi IgG durante la desensibilizzazione è ancora oggetto di discussione [1]. egli ultimi 20 anni, l’attenzione degli scienziati si è concentrata dapprima sulle conseguenze della desensibilizzazione sull’immunità umorale rivelate dai test cutanei, dagli anticorpi IgE, dagli anticorpi specifici circolanti IgG e dal rilascio di istamina da parte dei basofili nel sangue. L’aumento naturale degli anticorpi IgE specifici osservato durante la stagione dei pollini di graminacee in pazienti allergici si è rivelato significativamente più contenuto dopo la desensibilizzazione [1]. Un nuovo elemento nella desensibilizzazione sublinguale riguarda gli anticorpi IgA. Durante la desensibilizzazione sublinguale con i pollini di graminacee, si è notato infatti un aumento degli anticorpi sierici IgA. Per quanto riguarda la desensibilizzazione sublinguale con gli acari della polvere, si è rilevato un discreto aumento delle IgA sieriche, che presentano un livello inferiore nei soggetti sensibilizzati, che ha raggiunto all’incirca lo stesso livello di quello registrato in soggetti sani dopo la desensibilizzazione [2]. Diversi studi hanno dimostrato come i progressi clinici ottenuto dopo la desensibilizzazione sublinguale e iniettiva erano accompagnati da un aumento L’effetto della desensibilizzazione sui linfociti T e sul rilascio dei loro mediatori N Nel corso degli anni ’90, dopo l’applicazione del concetto di Th1 e Th2 all’allergologia, si è dimostrato come la desensibilizzazione, in particolare durante l’immunoterapia al veleno di imenotteri e ai pollini di graminacee, portasse in alcuni casi al riorientamento del profilo del linfocita Th2 verso un profilo Th1. A livello sistemico, la rilevazione dei marcatori dell’infiammazione cellulare ha dimostrato un reclutamento inferiore di neutrofili e eosinofili, un’espressione ridotta delle risposte di Th2 (riduzione di IL-4, IL-5, IL-13) e un ••• GLI ANTICORPI IGG E IGA SEMBRANO AGIRE SECONDO DIVERSI MECCANISMI NON ESCLUSIVI: • legandosi competitivamente all’allergene in modo da bloccare i legami delle IgE e quindi la degranulazione dei basofili e dei mastociti, o presentazione di recettori (FCεR1 e CD23) dell’allergene ai linfociti T; • agendo come anticorpi bloccanti, in modo da stimolare il recettore FCgRII che porta a una riduzione del rilascio di fattori proinfiammatori, secondari all’attivazione delle cellule da parte dei recettori FCγRII. I livelli di IgG4 erano significativamente maggiori durante la desensibilizzazione iniettabile 7 Dossier scientifico Quali marcatori utilizzare ... ••• aumento delle citochine Th1 (interferone gamma, IL-12). Più di recente, si è evidenziato il ruolo dei linfociti T regolatori – linfociti Treg (vedi diagramma nella pagina di fronte). EFFETTI DELLA DESENSIBILIZZAZIONE SULLE CELLULE Linfociti T periferici: aumento di IL-10 con pneumoallergeni L’attività allergenica degli allergeni ricombinanti può essere ridotta La desensibilizzazione stimola questi linfociti regolatori? A livello periferico, durante i protocolli per la desensibilizzazione sottocutanea al veleno di imenotteri e anche negli apicoltori che sono naturalmente desensibilizzati rispetto alle punture di api, si è notato un aumento dei linfociti T che producono IL-10 e una riduzione delle citochine rilasciate dai linfociti T [1]. Il lavoro svolto da Francis e coll. [3], con un numero ridotto di pazienti, ha dimostrato un aumento di IL-10 nel sangue di pazienti desensibilizzati rispetto ai pazienti atopici non desensibilizzati e di controllo. 12 soggetti atopici desensibilizzati, 11 soggetti atopici non desensibilizzati e 10 soggetti normali (controlli) Almeno 1 anno e mezzo di desensibilizzazione all’erba codolina Desensibilizzazione clinicamente efficace I globuli bianchi periferici sono stimolati dall’erba codolina per 6 giorni IL-10 misurato nel sangue: • in pazienti desensibilizzati: 116 ± 21 pg/ ml • in pazienti atopici non desensibilizzati: 30 ± 5 pg / ml • nei soggetti di controllo: 10 pg / ml Rilevazione di linfociti T CD4+ CD 25 che producono IL-10: • desensibilizzati: 20.5 ± 1.5% • atopici non desensibilizzati: 2.6 ± 1.0% • nei soggetti di controllo: 1.3 ± 0.3% Si è scoperto che i linfociti T regolatori (CD4+, CD5+) producono IL10 nei pazienti desensibilizzati. Questa ricerca ha dimostrato una maggiore presenza di IL-10 e di linfociti regolatori in pazienti atopici non desensibilizzati. Nella mucosa nasale, 2 anni dopo la desensibilizzazione ai pollini di graminacee, Wachholtz e coll. [4] hanno rilevato un aumento significativo di RNA messaggero per l’ interferone gamma dalle biopsie nasali. Il miglioramento clinico è accompagnato inoltre da una crescita nel rapporto IFNγ/ IL5 nelle cellule della mucosa nasale. Nella mucosa nasale dopo la desensibilizzazione, Klimek e coll. [5] hanno rilevato inoltre un aumento di RNA messaggero per interferone gamma e una riduzione dei RNA messaggero per IL-4 e IL-5. Per quanto riguarda la desensibilizzazione sublinguale, vi sono diverse argomentazioni a favore della stimolazione dei linfociti T regolatori, in particolare in modelli animali. D’altro lato, negli esseri umani dopo la desensibilizzazione sublinguale non vi sono ancora forti evidenze a favore della produzione di linfociti T regolatori [1]. Tuttavia, i dati ottenuti di recente da Ciprandi e al. [6] hanno dimostrato che IL-10 è significativamente più elevato in pazienti che hanno ricevuto la 8 Francis et al. JACI, 2003 desensibilizzazione sublinguale agli acari della polvere rispetto a soggetti atopici non desensibilizzati o normali. L’effetto della desensibilizzazione a seconda dell’allergene La desensibilizzazione si sta evolvendo velocemente. Dopo la nuova via di somministrazione, si stanno prospettando ora le prime applicazioni cliniche di allergeni ricombinanti, clonati per la prima volta nel 1989 (acari della polvere). La desensibilizzazione sottocutanea ha rivelato una stimolazione di IL-10 e di linfociti T regolatori. Tuttavia, la correlazione con un’eventuale efficacia clinica resta ancora da dimostrare. Indipendentemente dai marcatori come gli anticorpi IgE e IgG4, restano ancora da esaminare le risposte dei linfociti T CD4+, poiché lo sviluppo di allergeni ricombinanti aumenta la possibilità di ottenere risultati sostanziali. Siccome gli allergeni ricombinanti sono più specifici, dovrebbe manifestarsi una risposta maggiore di linfociti T regolatori, il che spiega l’interesse per gli allergeni per via sublinguale. È inoltre possibile ridurre l’attività allergenica degli allergeni ricombinanti. Esistono degli isoallergeni che non vengono riconosciuti dagli anticorpi IgE. Queste proteine possono anche essere modificate eliminando gli epitopi IgE dipendenti, in modo da consentire di aumentare le concentrazioni per la desensibilizzazione sottocutanea. Tuttavia, è ancora difficile dire se queste modifiche porteranno a progressi clinici. Infine, favorendo la comparsa di anticorpi IgG bloccanti, gli allergeni modificati dovrebbero portare inoltre ad aumenti significativi delle loro dosi. MECCANISMI IMMUNOLOGICI DELLA SLIT [1] Basato sulla presentazione di F. de Blay (French Language Pneumology Congress, Nizza 2006) Conclusione Durante la desensibilizzazione per via sottocutanea o sublinguale, si sono osservati cambiamenti nell’immunità umorale nel corso di studi clinici. Tuttavia, anche se questi cambiamenti sono significativi, la loro entità resta modesta e solo raramente è stato dimostrato un diretto collegamento con gli aspetti clinici. Dopo 20 anni di ricerche sui cambiamenti dei marcatori biologici durante la desensibilizzazione, sembra doveroso intraprendere ricerche molto più estese rispetto a quelle effettuate fino ad ora, per analizzare sia l’immunità umorale che quella cellulare. L’impiego di molecole allergeniche più specifiche come gli allergeni ricombinanti potrebbe aumentare le possibilità di ottenere cambiamenti significativi. 1 - Moingeon P, Batard T, Fadel R et al. Immune mechanisms of allergen-specific sublingual immunotherapy. Allergy. 2006; 61: 151-65. 2 - Bahceciler NN et coll. Impact of sublingual immunotherapy on specific antibody levels in asthmatic children allergic to house dust mites. Int Arch Allergy Immunol. 2005;136: 287-94. 3 - Francis JN et al. J Allergy Clin Immunol 2003; 111: 1255-61. 4 - Wachholz PA et al. Grass pollen immunotherapy for hayfever is associated with increases in local nasal but not peripheral Th1 : Th2 cytokine ratios. Immunology 2002; 105: 56-62. 5 - Klimek et al Short-term preseasonal birch pollen allergoid immunotherapy influences symptoms, specific nasal provocation and cytokine levels in nasal secretions, but not peripheral T-cell responses, in patients with allergic rhinitis. Clin Exp All 1999; 29:1326-35. 6 - Ciprandi et al . Induction of interleukin 10 by sublingual immunotherapy for house dust mites: a preliminary report. Ann Allergy, Asthma & Immunol, 2005; 95: 38-44. 9
Scaricare