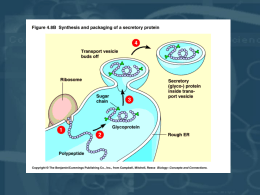
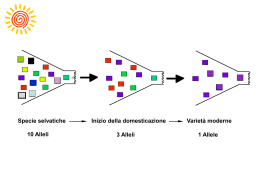
Regolazione dell’espressione genica 1 Eucarioti pluricellulari -un singolo organismo, utilizzando un unico genoma, deve produrre centinaia di tipi cellulari differenti e specializzati. -le cellule differenziate sono prodotte da popolazioni di cellule immature, non specializzate, dette cellule staminali, attraverso un processo noto come differenziamento cellulare. 2 I meccanismi di controllo usati per regolare l’espressione dei geni umani a differenza di quelli dei procarioti, devono riuscire a gestire quantità molto superiori di DNA, “impacchettati” in strutture apparentemente inaccessibili. 3 •Regolazione trascrizionale •Regolazione post-trascrizionale •Meccanismi epigenetici e controllo dell’espressione genica a lunga distanza 4 Cellula umana contiene circa 24000 geni RNA genes (rRNA, tRNA, miRNA o MIR) Geni per proteine Ogni cellula in un determinato momento esprime solo una piccola parte di questo potenziale (˜ 5000 geni) Geni housekeeping metabolismo biosintesi membrane cellulari istoni RNA ribosomiali Geni tessuto - specifici DIFFERENZIAMENTO CELLULARE 5 Esistono molteplici livelli di regolazione dell’espressione genica negli eucarioti NUCLEO Meccanismi epigenetici: controllo a lungo raggio DNA mediante rimodellamento della struttura della cromatina controllo trascrizionale: legame di fattori trascrizionali tessuto specifici, legame diretto di ormoni, fattori di crescita o elementi Trascritto primario intermedi a elementi responsivi di geni (precursore) inducibili controllo post-trascrizionale: splicing alternativo, polyA alternativo, RNA editing tessuto-specifico mRNA CITOPLASMA controllo del trasporto mRNA controllo traduzionale traduzione controllo della stabilità degradazione PROTEINA controllo post-traduzionale PROTEINA attiva o inattiva 6 Controllo Genomico Decondensazione della cromatina e espressione genica 7 Se si procede all’estrazione della cromatina dalle cellule, la si tratta con endonucleasi aspecifiche e si procede quindi all’estrazione del DNA, si nota, dopo corsa elettroforetica, che la maggior parte del DNA viene rotto in frammenti di 200 bp o in multipli di tale lunghezza. Il DNA cromosomico è protetto dall’azione delle nucleasi perché associato alle proteine istoniche. 8 Negli eucarioti superiori i geni inattivi da un punto di vista trascrizionale hanno una struttura cromatinica meno accessibile BamHI 4,6 kb Globina DNAseI Eritroblasto embrionale di 14 giorni BamHI BamHI 4,6 kb BamHI Globina DNAseI Cellule non differenziate MSB Isolamento dei nuclei e digestione con quantità crescente di DnasiI. Estrazione DNA digestione con BamHI Analisi mediante Southern Blot Ibridazione con globina 9 Geni attivi da un punto trascrizionale sono più suscettibili di quelli inattivi alla digestione con DNAsiI Sono in una conformazione cromatinica particolare che li rende più accessibili a DNAsiI Il DNA trascrizionalmente inattivo assume una conformazione cromatinica più condensata che protegge il gene globinico dalla digestione con DNAsiI DNA da Eritroblasti di 14 giorni DnaseI (µg/ml) 0 0,01 0,05 0,1 0,5 1 1,5 DNA da cellule MBS 1,5 4,6kb 10 Esistono anche siti di ipersensibilità alla DnasiI, evidenziabili con trattamenti più blandi. Sono siti probabilmente localizzati al 5’ dei geni nelle regioni regolatorie dei geni e sono considerate regioni in cui i nucleosomi sono stati rimossi e quindi più accesibili alle proteine regolatorie 11 Gene Expression La regolazione dell’espressione genica può avvenire ad ogni passaggio Per la maggior parte dei geni avviene a livello dell’inizio della trascrizione. Esso coinvolge cambiamenti della struttura della cromatina al promotore, accompagnati dal legame del apparato basale di trascrizione (inclusa RNA polymerase II) al promotore. Eventi successivi possono modificare il tipo di proteina che viene espressa. 12 La decondensazione della cromatina rappresenta un prerequisito dell’attivazione trascrizionale 13 CROMATINA •EUCROMATINA -> TRASCRIZIONE POTENZIALE a) geni housekeeping b) geni tessuto-specifici •ETEROCROMATINA FACOLTATIVA -> inattiva quando condensata. Fornisce un meccanismo di compensazione: rapporto geni autosomici/geni X-linked •ETEROCROMATINA COSTITUTIVA -> sempre inattiva; Localizzata nelle regioni peri - e centromeriche 14 I meccanismi epigenetici Fattori che vengono trasmessi alla progenie, ma che non sono direttamente attribuibili alla sequenza del DNA. I geni mappano tutti in regioni le cui caratteristiche generali possono essere definite inizialmente eucromatiche. In questa regioni, ancora una volta, agiscono i meccanismi epigenetici per tenerle più o meno aperte e quindi più o meno disponibili ad interagire con i meccanismi di controllo trascrizionale. Durante il differenziamento alcune di queste regioni possono eterocromatizzare definitivamente. 15 L’INATTIVAZIONE DEL CROMOSOMA X È UN PROCESSO EPIGENETICO 16 L’inattivazione del cromosoma X è un processo epigenetico, cioè un processo che influenza l’espressione di geni specifici ed è ereditato dalle cellule figlie senza che avvenga alcuna variazione nella sequenza del DNA. L’attività dei geni del cromosoma X nelle femmine dei mammiferi è controllata da strutture cromatiniche piuttosto che dalla sequenza nucleotidica del DNA che forma il cromosoma. Il cromosoma X inattivato (sia esso Xmaterno o Xpaterno) è mantenuto nello stato di cromosoma inattivo nella progenie che deriva dalle future divisioni cellulari poiché gli istoni, modificati in modo da determinare repressione trascrizionale, sono fedelmente ereditati in questo stato ad ogni divisione della cellula. 17 I meccanismi epigenetici •Metilazione del DNA Nelle cellule eucariotiche la metilazione è a carico della Citosina. Solo il 3% delle Citosine sono metilate ed in genere è bersaglio della metilazione la Citosina della doppietta CpG (dinucleotide citosina-guanina). •Modificazioni degli istoni Acetilazioni, fosforilazioni e metilazioni, cambiamenti conformazionali della cromatina. responsabili di 18 Meccanismi epigenetici: Metilazione del DNA La metilazione del DNA è un processo post-replicativo. L’estensione delle modificazioni riguardanti la metilazione del DNA è fondamentalmente decisa durante lo sviluppo. La metilazione del DNA è quindi uno dei meccanismi correlati con il differenziamento cellulare, tramite l’inibizione dell’espressione genica a livello trascrizionale. 19 CpG islands sono bersagli di regolazione • CpG islands circondano i promotori di geni espressi costitutivamente e sono non-metilate. • Si trovano anche ai promotori di qualche gene tessuto-regolato. • Ci sono ~29,000 CpG islands nel genoma umano. • La metilazione di una CpG island impedisce la attivazione di un promotore. • La repressione è causata da proteine che si legano alle doppietta CpG metilate. 20 Quali regioni sono bersaglio della metilazione? •Nel genoma umano il 56% dei geni sono associati a isole CpG: tutti i geni housekeeping ed il 40% dei geni con espressione tessuto-specifica •I geni tessuto-specifici sono metilati in CpG nei tessuti dove non sono espressi in quanto i geni metilati sono silenti. (B) 21 Cambiamenti dello stato di metilazione del DNA durante lo sviluppo dei mammiferi Durante la segmentazione si ha subito una fase di demetilazione, seguita da una metilazione “de novo” dispersa su tutto il genoma, dopo l’impianto. La metilazione de novo è rara dopo la gastrulazione, ma è stata vista frequentemente durante la stabilizzazione di colture in vitro e nei tumori. 22 Metilazione del DNA e divisione cellulare La metilazione del DNA è mantenuta durante la replicazione 23 espressione genica è associata alla demetilazione • Demetilazione al 5 ′ del gene è necessaria per la trascrizione. 24 Meccanismi epigenetici: Modificazioni degli Istoni I residui amminoacidici all’N-terminale di ciascun istone (20-60 residui) si estendono al di fuori della superficie del nucleosoma. Queste regioni sono particolarmente ricche in lisina (K) che può essere reversibilmente modificata mediante acetilazione, fosforilazione e metilazione. 25 26 Modificazioni degli istoni H3 e H4 La lisina 9 di H3 può essere sia acetilata che metilata. L’acetilazione è associata alla cromatina trascrizionalmente attiva, ma se la regione cromatinica viene metilata a livello del DNA (CpG). Le proteine che si legano al DNA metilato richiamano le deacetilasi istoniche, che rimuovono i gruppi acetile e le metil transferasi istoniche, legate alle CpG binding protein, metilano gli istoni. Il risultato è la condensazione della cromatina. 27 L’acetilazione degli istoni è associata al controllo dell’espressione genica. Il grado di acetilazione degli istoni regola l’espressione genica. Gli istoni acetilati hanno un’affinità ridotta per il DNA, quindi la cromatina è più aperta. La repressione delle sequenze CpG metilate nei promotori è legata a due proteine che si legano a CpG metilati ed attivano la deacetilazione degli istoni. MeCP1 e MeCP2 (methylated Cpg-binding proteins 1 and 2) 28 L’acetilazione degli istoni è associata al controllo dell’espressione genica MeCP2 acts as a trascriptional repressor and recruits a corepressor complex consisting of the tracription factor repressor mSin3A and histone deacetylase. MeCP2 è essenziale per lo sviluppo embrionale e si comporta come repressore funzionale. MeCP2 silenzia l’espressione di geni mediante il reclutamento dell’attività di HDAC (histone deacetylase) che causa il rimodellamento della cromatina. La rimozione del gruppo acetile dell’istone 3 lisina 9 (H3-K9) è seguita dalla metilazione che rappresenta il segnale per proteine quali HP1 che causa la condensazione della cromatina 29 Nelle cellule umane, la proteina HP1 si lega alle code dell’istone H3, metilato a livello della lisina 9 HP1 Me 9 Me 9 30 Silenziamento del telomero • I telomeri (e centromeri) sono generalmente nell’eterocromatina. I geni sono silenziati • Nel telomeri agisce la prot Rap1 che recluta SIR. Sir2 è una deacetilasi, Sir3 e 4 reclutano altri SIR ed espandono il silenziamento • SIR = Silent Information Regulator 31 Le modificazioni delle code istoniche sono importanti per il successivo assemblamento di fattori di eterocromatinizzazione. In lievito, le proteine SIR si legano alla coda di H4 non acetilata Me 9 Me 9 32 Le proteine eterocromatiniche condensano la fibra di 30nm in una struttura maggiormente impaccata 33 Le modificazioni delle code istoniche controllano la condensazione e la funzione della Cromatina Le code istoniche sono necessarie affinchè la cromatina possa condensarsi da una struttura a filo di perle ad una fibra di 30nm. Recenti esperimenti indicano che le estrmità N-terminali dell’istone H4, in particolare la lisina 16, sono elementi cruciali per la formazione della fibra da 30 nm. Le code istoniche sono soggette a modificazioni post-trduzionali multiple, quali acetilazione, metilazione, fosforilazioe, e ubiquitinazione. Una proteina istonica non ha mai tutte queste modificazioni simultaneamente, ma gli istoni di un singolo nucleosoma possono contenere diversi tipi di modificazioni. 34 Attivazione per alterazione della struttura della cromatina L’attivatore recluta: – Istone acetilasi o chromatin remodeling complexes – Facilita il reclutamento di proteine con bromodomini (es. TFIID) 35 Legame cooperativo degli attivatori • Gli attivatori agiscono in modo sinergico. • Ciò può avvenire in diversi modi, e con legami cooperativi 36 Modificazioni covalenti delle code degli istoni alterano l’accessibilità della cromatina. Lisine: acetilate o metilate Serine: fosforilate Acetilazione: trascrizione attiva Deacetilazione: trascrizione repressa Metilazione: sia attivazione che repressione Proteine con bromodominio riconoscono code istoniche acetilate Proteine con cromodominio riconoscono code istoniche metilate 37 Il cromodominio HP1 lega la coda N-terminale dell’ istone H3 solo quando la lisina 9 è trimetilata. HP1 contiene un secondo dominio, chiamato dominio cromo-ombra, che si trova frequentemente in proteine che contengono cromo domini. Il dominio cromo-ombra, lega altri domini cromo-ombra ed è per questo che la cromatina con la lisina 9 di H3 trimetilata tende a condensarsi per mezzo di HP1. Oltre a legare se stesso il dominio cromo –ombra lega l’enzima che metila la lisina 9 di H3, noto come meliltrasferasi istonica H3K9 (HMTH3K9). 38 Gli attivatori alterano la cromatina • Acetilazione degli istoni e rimodellament o dei nucleosmi sono indotti dagli attivatori 39 Acetilazione degli istoni • L’attivatore lega HAT la cui attività chiama altri attivatori • Il bromodomain di TFIID riconosce alcune lisine acetilate della coda di H4, che sono associate a regioni della cromatina attive nella trascrizione 40 CARATTERISTICHE DELLA CROMATINA Caratteristica Cromatina attiva Cromatina inattiva Conformazione Estesa, aperta Condensata della cromatina Metilazione del Pocometilata Metilata DNA specialmente nelle regioni del promotore Acetilazione Istoni acetilati Istoni non degli istoni acetilati 41 Controllo Trascrizionale Il metodo principale col quale avviene il controllo dell’espressione genica negli eucarioti è una trascrizione selettiva, che si ottiene grazie a specifiche “DNA binding proteins”. 42 REGOLAZIONE GENICA A LIVELLO TRASCRIZIONALE LA REGOLAZIONE GENICA A LIVELLO TRASCRIZIONALE AVVIENE ATTRAVERSO IL LEGAME DI FATTORI PROTEICI A SEQUENZE NUCLEOTIDICHE DI REGOLAZIONE. I FATTORI PROTEICI IMPEGNATI A REGOLARE L’ESPRESSIONE GENICA AGISCONO IN TRANS LEGANDOSI ALLE SEQUENZE DI DNA CHE SONO IN PROSSIMITA’ DEL GENE (IN CIS) 43 Fattori coinvolti in gene expression • I fattori basali insieme alla RNA polymerase, si legano allo startpoint e TATA box • Gli Attivatori sono fattori di trascrizione che riconoscono specifici elementi di corte sequenze consenso. • Si legano a siti nel promotore o negli enhancers. • Le sequenze che legano vengano chiamate response elements. • I Coattivatori danno un collegamento tra gli attivatori e l’apparato basale. • Non legano il DNA • Alcuni regolatori inducono cambiamenti nella cromatina 44 Sinergia nella trascrizione • Gli attivatori agiscono su molti passaggi diversi e la loro azione è sinergica 45 Attivatori hanno domini di legano il DNAbinding e di attivazione Le attività DNA-binding e di attivazione della trascrizione sono in domini indipendenti di un attivatore. Il ruolo del dominio DNA-binding è di portare il dominio di attivazione della trascrizione vicino al promotore. Gal4 regola la trascrizione del gene del galattosio in S. cerevisiae. Si lega a un sito di 17 bp. Ci sono 4 siti, ciascuno lega un dimero di Gal4, che formano la UASG (Upstream Activating Sequence di Gal) 46 Come fa un attivatore a stimolare la trascrizione Due modelli generali : • Il modello di reclutamento implica che il solo effetto è di aumentare il legame della RNA polimerase al promotore. • Un modello alternativo è che esso induca dei cambiamenti conformazionali nel complesso trascrizionale, che ne aumenta l’efficienza. 47 Attivazione per reclutamento • L’attivatore può legare il mediatore che è associato alla pol-II o a fattori di trascrizione (TFII-D) 48 • I coattivatori sono fattori di trascrizione la cui specificità è data dalla capacità di legare DNA-binding transcription factors invece di legare direttamente il DNA. • Quando un attivatore funziona tramite un coattivatore la connessione prevede legami non covalenti tra le due proteine I contatti con l’apparato basale possono essere fatti con ognuno dei vari fattori basali, tipicamente TFIID, TFIIB, or TFIIA. 49 • Tutti i componenti necessari per una trascrizione efficiente: • basal factors, • RNA polymerase, • activators, • coactivators formano un apparato molto grande, di >40 proteine. • Alcuni attivatori, coattivatori, e fattori basali possono assemblarsi uno dopo l’altro al promotore, ma poi possono unirsi ad un complesso molto grande fatto dalla RNA polimerasi preassemblata con altri attivatori e coattivatori. 50 • Una serie di fattori trascrizionali deve legarsi al promotore prima che possa farlo la RNA polimerasi. • Quindi se la RNA polimerasi potrà iniziare la trascrizione dipenderà anche dal legame di proteine regolatorie, attivatori e repressori. Elementi distali Elementi prossimali Promotore basale 51 Il promotore del gene umano dell’insulina Nero: fattori ubiquitari Rossi: fattori specifici delle cellule beta pancreatiche 52 Gli attivatori trascrizionali sono proteine modulari composte da distinti domini funzionali 53 Repressori e attivatori possono dirigere la deacetilazione/acetilazione degli istoni a livello di specifici geni Importanza della struttura modulare e delle interazioni proteina-proteina 54 55 Attività a distanza: anse e isolatori • Gli enhancers agiscono anche a 100 kb dal gene. • Essi possono essere portati sul gene dalla formazione di anse e dalla struttura della cromatina • Gli insulators bloccano l’attivazione promossa dagli enhancers 56 Enhancer Una sequenza enhancer classica contiene al suo interno parecchi elementi di controllo differenti, ognuno dei quali è costituito da una corta sequenza di DNA che funziona da sito di legame per uno specifico fattore di trascrizione regolativo (attivatore). Spesso i siti di legame possono essere gli stessi presenti nelle sequenze prossimali. I silencer sono meno abbondanti, legano fattori in grado di ridurre l’efficienza di trascrizione (repressori). 57 L’enhanceosome dell’interferone beta • IFN-beta è indotto da infezione virale • Questa causa la sintesi di NFkB, IRF e Jun/ATF • Questi si legano ad unsito 1 kb upstream il promotore in un complesso cui partecipa HMG, un fattore strutturale 58 Insulators • Gli insulators delimitano un dominio di espressione • si localizzano preferenzialmente nelle interbande • possono bloccare il passaggio degli effetti attivanti o disattivanti dagli enhancers, silencers, o LCRs. • possono agire da barriera contro la propagazione della heterochromatin 59 Insulators e struttura della cromatina • Forse gli insulators agiscono sulla struttura del DNA • Possono organizzare anse di DNA che limitano le interazioni attivatore-promotore 60 Il cluster dei geni delle betaglobine • L’espressione dei 5 geni cambia con lo sviluppo • Tutti i geni sono sotto il controllo di LCR • LCR controlla la condensazione della cromatina 61 Regioni di controllo: LCR • Il Locus Control Region (LCR) è 30-50 kb a monte dei geni della beta-globina. Regola l’apertura della cromatina per l’accesso dei fattori di regolazione 62 COMPETIZIONE 10_23_2.jpg l’espressione di alcuni geni (geni umani delle globine) è coordinata da una regione di controllo dominante LCR localizzata a monte dei geni delle globine 63 z2e2, Emoglobina Embrionale (espressione nel sacco vitellino) a2g2 HbF Emoglobina fetale (espressione nel fegato e nella milza) a2d2 HbA2 Emoglobina dell’adulto a2b2 HbA Le LCR funzionano da enhancer per la trascrizione dei geni globinici Altri siti ipersensibili nella regione dei promotori dei singoli geni -> specificità dello stadio di sviluppo. Siti ipersensibili a DNAsi I Eritroide-specifici (enhancer) Siti ipersensibili del fegato fetale Siti ipersensibili nel midollo osseo adulto 64 Esempio: beta globina • Proteine regolatorie: • GATA-1 (fattore di trascrizione) è eritroidespecifica • CP1 (fattore di trascrizione) ubiquitaria 65 Alcune proteine che legano il promotore sono repressori. • La repressione solitamente avviene modificando la struttura della cromatina, ma ci sono repressori che agiscono legandosi a promotori specifici. • repressori Eucariotici che bloccano la trascrizione sono relativamente rari. Un esempio è il repressore globale NC2/Dr1/DRAP1, un eterodimero che lega TBP(TATA Box-Binding protein) per impedirne la interazione con altri componenti del apparato basale 66 Repressori 67 SWI/SNF: (proteine che rimodellano la cromatina) HAT: (histon acetiltransferasi) Gli attivatori interagiscono con i coattivatori e stimolano il rimodellamento della cromatina e l’acetilazione degli istoni Un grosso complesso multiproteico, detto mediatore funge da ponte, legando sia le proteine attivatrici, associate all’enhancer, sia la RNA pol., in modo da connettere gli enhancer con i componenti coinvolti nell’inizio della trascrizione genica. 68 Ciascun elemento presente in un promotore possiede una specifica sequenza consenso che lega i fattori di attivazione ubiquitari della trascrizione. Il legame dei fattori trascrizionali avviene nel sito consenso che include un numero variabile di nucleotidi a seconda del promotore. CTF è un membro di una famiglia proteica di fattori trascrizionali NF-1 è un fattore nucleare-1 SP-1 è un fattore trascrizionale ubiquitario 69 Regolazione della trascrizione da glucocorticoidi Gli ormoni lipofili diffondono attraverso la membrana plasmatica, ma solo nelle cellule bersaglio trovano il loro recettore specifico ad elevata affinità, con cui si associano. Il complesso ormone-recettore va incontro ad una “reazione di attivazione” temperatura e concentrazione salina dipendente, che ne determina un cambiamento delle dimensioni, della conformazione e della carica superficiale che lo rendono capace di legarsi alla cromatina. In alcuni casi, come nel caso del recettore per i glucocorticoidi, l’attivazione provoca la dissociazione del recettore da un’altra proteina come la proteina 90 da shock termico (HSP 90). 70 HSP90 maschera il sito legante il DNA dei Recettori per gli steroidi DNA SR hsp90 Elementi di Fisiologia – A.A. 2004-2005 Attivazione della trascrizione genica operata da recettori nucleari per gli ormoni steroidei (ER) E2 hsp50 ER hsp70 hsp90 hsp50 hsp70 ER hsp90 ER ER hsp90 hsp90 hsp50 hsp70 hsp50 HAT Histone-Acetyl-Transferase ER ER TATA Elementi di Fisiologia – A.A. 2004-2005 hsp70 Il complessso recettore-ormone si lega a specifici regioni del DNA (dette elementi di risposta dell’ormone) determinando l’attivazione oppure l’inattivazione di specifici geni. Si ha cosi una selettiva modulazione della trascrizione di particolari geni e della produzione delle corrispondenti molecole di mRNA, in questo modo gli ormoni riescono a controllare la sintesi di specifiche proteine e a influenzare i processi metabolici della cellula. 73 L’HRE deve associarsi con altri elementi per agire in modo ottimale. Questi complessi di DNA sono detti unita’ di risposta all’ormone (HRU) . Quindi una HRU è costituita da una o più HRE e uno o più elementi di DNA asssociati con fattori accessori. La comunicazione tra un HRU e l’apparato trascrizionale di base è resa possibile dall’intervento di una o piu’ molecole appartenenti a una classe di coregolatori. La prima di queste molecole ad essere stata descritta è la proteina legante CREB (la proteina legante l’elemento di risposta al cAMP) detta CBP. 74 CBP attraverso un dominio amminoterminale, lega il residuo fosforilato di serina 137 di CREB mediante la transattivazione in risposta al cAMP. CBP e un’altra proteina strettamente correlata, la P300, interagiscono con diverse molecole segnalatrici tra cui la proteina attivatrice-1 (AP-1), trasduttori del segnale, attivatori della trascrizione (STAT), recettori nucleari e CREB. E’ importante notare che il complesso CBP/P300 presenta anche un’attivita’ intrinseca istone acetil-transferasica (HAT). 75 Regolazione della trascrizione da ormoni steroidi In molti geni regolati dagli ormoni steroidei è stato individuato un secondo elemento di risposta (HRE) che si trova all’estremita’ 5’ rispetto all’elemento promotore. L’HRE presumibilmente modula la frequenza di inizio della trascrizione e dipende in misura minore dalla posizione e dall’orientamento. Sembra che sia simile agli elementi amplificatori della trascrizione presenti in altri geni. 76 Diversi elementi hanno effetti diversi sul livello di trascrizione, alcuni con effetti maggiori di altri, e alcuni possono anche attivare la risposta tessuto specifica. Il legame dei fattori trascrizionali all’elemento di risposta per gli steroidi, modula la frequenza di trascrizione del messaggero. MyoD è un fattore specifico delle cellule muscolari GRE è l’elemento di risposta ai glucocorticoidi 77 Somiglianza fra i diversi recettori steroidei Nei recettori steroidei, le regioni di legame per il DNA e quelle di legame per gli ormoni condividono un alto grado di omologia. Il recettore per gli estrogeni è meno simile al recettore dei glucocorticoidi di quanto non lo siano gli altri recettori steroidei. AR=recettore degli androgeni; ER=recettore per gli estrogeni; GR=recettore per i glucocorticoidi; MR=recettore per i mineralcorticoidi; PR=recettore per il progesterone. I numeri indicano il grado di omologia 78 Come avviene l’interazione DNAproteine? Le proteine con DNA binding domains hanno dei motivi particolari: A) Motivo helix-turn-helix (elicagiro-elica), consiste di due a eliche separate da un ripiegamento della catena polipeptidica. Il motivo è sempre lo stesso: una a elica di riconoscimento, che con le catene laterali dei suoi residui amminoacidici riconosce specifiche sequenze di DNA (posizionate nel solco maggiore della doppia elica) alle quali si lega (leg. idrogeno). La seconda a elica stabilizza la conformazione generale. C) Motivo Zinc finger (a dita di zinco), è constituito da una a elica e da due segmenti a foglietti b, tenuti insieme da residui di cisteina o istidina, posti in modo preciso, con un atomo di zinco . Il numero di zinc finger varia tra un fattore di trascrizione e un altro. Le strutture zinc finger protrudono dalla superficie della proteina e servono da punto di contatto con specifiche sequenze di DNA posizionate nel solco maggiore della doppia elica. 79 Le dita di zinco sono sequenze molto comuni che permettono alla proteina di legare il DNA a doppio filamento. X= qualsiasi amminoacido 80 D) Motivo leucine zipper (a cerniera di leucine), è formato dall’interazione di due catene polipeptidiche, ognuna contenente una α elica con residui di leucina (a.a. idrofobico) regolarmente spaziati. Le leucine, interagendo tra di loro, provocano un attorcigliamento delle due eliche. Il motivo è utilizzato per unire due polipeptidi uguali o diversi. Il legame al DNA è reso possibile dalla presenza di due ulteriori regioni ad α elica che interagiscono con le sequenze del solco maggiore. E) Motivo helix-loop-helix (elicaansa-elica), consiste di due α eliche una più piccola e una più grande, separate da un’ansa. I motivi helix-loop-helix contengono regioni idrofobiche che permettono di connettere due polipeptidi uguali o diversi. La formazione di un fascio di 4 α eliche provoca la giustapposizione dell’elica di riconoscimento di un polipeptide con quella dell’altro, creando così un dominio di legame al DNA bipartito. 81 Il legame dei fattori trascrizionali al DNA coinvolge una piccola porzione di proteina, la quale entra in contatto con il solco maggiore e/o solco minore della doppia elica del DNA che deve essere trascritto. Le cerniere di leucina possiedono sempre dei residui idrofobici di leucina da un lato dell’elica, che permettono a due cerniere di leucina d’interagire tra loro attraverso legami idrofobici. HTL= elica-ansa-elica; HTH= elica-giro-elica 82 Controllo post-trascrizionale 83 L’uso di promotori alternativi, di splicing alternativi, di poliadenilazioni alternative e di editing, può dare luogo a isoforme diverse con proprietà differenti quali : •Isoforme tessuto-specifiche. Gene DMD (gene mutato nella distrofia muscolare di Duchenne) presenta otto promotori diversi a seconda del tessuto, che danno origine a 8 diverse proteine •Isoforme stadio di sviluppo specifiche •Isoforme transmembrana o solubili •Diversa localizzazione cellulare •Funzione cambiata -> isoforme di fattori trascrizionali che agiscono da attivatori o repressori a seconda dei domini contenuti Lo splicing alternativo è controllato da proteine che si legano alle molecole di premRNA e fanno in modo che alcuni siti di splicing non vengano utilizzati e altri siano invece attivati. 84 L’editing ( modifica ) dell’RNA del gene APOB nell’uomo genera trascritti tessuto-specifici Nell’intestino tenue, l’editing del nucleotide 6666 del mRNA di ApoB, cambia una citosina in uracile, converte un codone per la glutammina nel mRNA per ApoB 100 in un codone stop prematuro e quindi produce la proteina troncata ApoB 48. 85 Il legame di proteine specifiche all’elemento di risposta per il ferro (IRE) dell’mRNA di un gene che risponde alle variazioni delle concentrazioni di ferro, può alterare in diversi modi la traduzione dell’mRNA in proteine funzionali. Quando si manifesta una carenza di ferro, la proteina che lega l’elemento di risposta al ferro (IRE-BP) è attiva e può legarsi all’estremità 3’ dell’mRNA per il recettore della trasferrina. Questo evento previene la degradazione dell’mRNA e quindi aumenta la quantità di recettore per la trasferrina che può essere sintetizzata (parte sinistra della figura) aumentando di conseguenza la quantità di ferro che il recettore può inviare alla cellula. La IRE-BP lega anche l’estremità 5’ dell’mRNA per la ferritina e blocca la traduzione. La ferritina è una proteina che sequestra e immagazzina nel citoplasma il ferro e risulta meno richiesta in condizione di carenza di ferro. 86 I cromosomi sessuali sono di due tipi, X e Y, con l’X sostanzialmente più grande dell’Y. Le femmine possiedono due cromosomi X, mentre i maschi hanno un cromosoma X e uno Y. Una regione del cromosoma Y è identica a una regione del cromosoma X, ma il cromosoma X contiene anche geni che non sono presenti sul cromosoma Y, per esempio SRY un gene determinante il sesso. Questi geni sono monoallelici e non hanno alcuna possibilità di scelta per quale allele verrà scelto. Nell’uomo, i geni sono stati identificati come biallelici, ma solo un allele, materno o paterno, è espresso prevalentemente, nonostante entrambi gli alleli siano perfettamente normali e identici. 87 Il risultato è che il 50% dei prodotti genici viene sintetizzato, ma il prodotto è funzionalmente attivo. Quindi, in ogni caso , nelle femmine uno dei due cromosomi X è inattivato durante una fase precoce dell’embriogenesi. Il cromosoma X-inattivato può ancora esprimere alcuni geni, incluso l’XIST ( trascritto specifico dell’X inattivato ) il quale codifica per un RNA che gioca un ruolo fondamentale nella inattivazione dell’X. Il cromosoma X-inattivato viene riattivato nelle femmine durante l’ovogenesi. 88 Controllo della traduzione La sintesi della globina nei reticolociti ( globuli rossi immaturi ) procede rapidamente, ma solo se è disponobile eme. L’inibizione della sintesi della globina avviene a livello dell’inizio della traduzione. In assenza di eme i reticolociti accumulano una proteina detta inibitore regolato dall’eme ( HRI). 89 L’ HRI è una chinasi che fosforila un residuo di Ser 51 della subunità α del fattore eIF2 ( il fattore d’inizio che trasporta GTP e Met-tRNAimet sul ribosoma). Il fattore eIF2 fosforilato può partecipare all’inizio della traduzione così come il fattore eIF2 non fosforilato, ma non è rigenerato. Dopo aver completato il processo d’inizio, il fattore IF2 non modificato scambia il GDP legato con il GTP, in una reazione innescata da un altro fattore di inizio “eIF2B” . 90 L’IF2 fosforilato forma un complesso molto più stabile con il fattore “eIF2B” rispetto a quello formato con il fattore IF2 non foforilato. Ciò determina il sequestro di “eIF2B” che è presente in quantità inferiori rispetto a eIF2, e impedisce la rigenerazione del complesso eIF2GTP necessario per la traduzione. In presenza di eme, i siti di legame dell’eme su HRI sono occupati e la chinasi è inattiva. Le molecole di eIF2 già fosforilate sono riattivate dalla eIF2 fosfatasi, che non è influenzata dall’eme. Il reticolocita coordina quindi la sua sintesi di globina e di eme. 91 Le chinasi ciclina dipendenti regolano la crescita cellulare Le cicline presenti in molti eucarioti, si combinano con una proteina con una massa di 34 kD e formano una proteina chinasi Ser/Thr attiva detta proteina chinasi ciclina-dipendente (CDK) che per essere attiva può richiedere una sua fosforilazione. Il cico cellulare dell’uomo è governato da diverse CDK. Esse fosforilano numerose proteine nucleari, tra cui l’istone H1, diverse proteine oncogeniche e proteine coinvolte nell’organizzazione del citoscheletro e nella disgregazione del nucleo. CDK2 nell’uomo è stata determinata in diverse condizioni conformazionali: (1) legata all’ATP (2) legata all’ATP e al frammento C-terminale della ciclina A (3) legata all’ATPγS ( un analogo dell’ATP che si idrolizza molto lentamente) e al frammento C-terminale della ciclina A, e con il residuo Thr 160 della CDK2 fosforilato. 92 93 Fattori di trascrizione 94 Fattori di trascrizione La trascrizione del gene è iniziata e regolata da numerose e diverse proteine che legano il DNA in maniera sequenza specifica, conosciute col nome di fattori di trascrizione. Questi fattori si legano a specifiche sequenze nucleotidiche e producono la differente espressione del gene, non solo durante lo sviluppo, ma anche all’interno dei tessuti e dell’organo adulto. Molti fattori trascrizionali agiscono in maniera positiva, promuovendo la trascrizione, mentre altri agiscono in maniera negativa promuovendo la repressione. I fattori di trascrizione qualche volta vengono chiamati fattori trans-agenti, per enfatizzare che, come proteine solubili, essi possono diffondere all’interno del nucleo e agire su più geni diversi localizzati su cromosomi diversi. 95 Modello d’azione dei fattori di trascrizione T1, T2, T3, T4, si legano alle loro sequenze di DNA bersaglio e contemporaneamente in gruppi di due mediante interazioni relativamente non specifiche al complesso di pre-inizio (PIC). L’interazione fattore di trascrizione-PIC inizialmente debole, si rafforza consentendo alla RNA polimerasi di attaccarsi al PIC e di iniziare la trascrizione. 96 Struttura a raggi X del complesso CDK2ciclina A-ATPγγS, in cui la CDK2 è fosforilata a livello del residuo di Thr 160 Il ciclo cellulare degli eucarioti La progressione delle cellule nel ciclo è determinata da modificazioni covalenti quali aggiunta o eliminazioni di gruppi fosfato. 97 Alcune forme di cancro derivano dalla soppressione dei repressori dei tumori Uno dei bersagli delle CDK è la proteina del retinoblastoma (Rb), che inibisce la crescita cellulare bloccando la funzione del fattore di trascrizione E2F. Questo fattore attiva i geni che innescano la proliferazione cellulare, compresi quelle delle cicline. La fosforilazione della proteina Rb da parte di CDK blocca l’attività antiproliferativa di Rb . La proteina Rb è nota come soppressore di tumori, in quanto la sua assenza può portare al retinoblastoma ( un cancro della retina) e altri tipi di tumori. L’attività di E2F è anch‘essa inibita dalla fosforilazione catalizzata da alcune forme di CDK. Il fattore di trascrizione e soppressore di tumori p53 viene attivato, a differenza di E2F, dalla fosforilazione catalizata da CDK. La proteina p53 fosforilata si lega a specifici geni e agisce come un potente fattore di trascrizione. Nel 50% di tipi di cancro dell’uomo sono presenti mutazioni della proteina p53. 98 Alcune forme di cancro derivano dalla soppressione dei repressori di tumori Struttura ai raggi X del dominio che lega il DNA della proteina p53 dell’uomo unita al suo DNA bersaglio 99 FINE 100
Scaricare