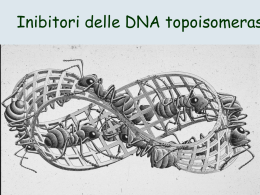
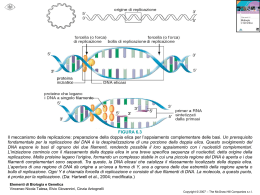
INIBITORI DELLA SINTESI DEGLI ACIDI NUCLEICI Nicasio Mancini 04/12/2008 1 Topoisomerasi IV 2 E. coli ~ 2 μm Cromosoma ~ 2 mm 3 4 5 Il superavvolgimento (supercoiling) del DNA non è solo indotto dalla necessità di compattarsi all’interno della cellula ma è una proprietà intrinseca del DNA stesso Fondamentale importanza dei fattori che regolano il superavvolgimento del DNA nei meccanismi di trascrizione, replicazione, trasposizione: TOPOISOMERASI 6 7 REPLICAZIONE DEL DNA 8 REPLICAZIONE DEL DNA ( t (catena veloce) l ) Topoisomerasi IV 9 REPLICAZIONE DEL DNA ( t (catena lenta) l t ) 10 TRASCRIZIONE DEL DNA 11 RICOMBINAZIONE DEL DNA 12 I CHINOLONI 13 CARATTERISTICHE GENERALI • Farmaci di SINTESI la cui attività antibatterica fu evidenziata casualmente nei processi di produzione della clorochina • Sviluppo per migliorarne le caratteristiche farmacocinetiche e lo spettro d’azione – 1a generazione (metà anni ‘60) 60) – 2a generazione (metà anni ’80) – 3a generazione (fine anni ‘90) • Piccole molecole idrofiliche o anfotere a seconda del pH 14 2a generazione (migliore farmacocinetica ed ampliamento dello spettro d’azione anche ai gram-positivi) FLUOROCHINOLONI 3a generazione (maggiore attività su anaerobi e patogeni atipici) 15 MECCANISMO DI INGRESSO • GRAM-POSITIVI Meccanismi non saturabili energia-indipendenti Peptidoglycan-teichoic acid Lipoteichoic acid • • Diffusione passiva attraverso i rivestimenti esterni (OmpF nei gram-negativa) Cytoplasmic membrane Cytoplasm Capacità di attraversare le membrane (rapida diffusione passiva anche attraverso la membrana citoplasmatica interna) Buona penetrazione all’interno delle cellule eucariotiche GRAM-NEGATIVI Porin Outer Membrane Perip plasmic space • Lipopolysaccharide Braun lipoprotein Inner (cytoplasmic) membrane Cytoplasm 16 MECCANISMO D’AZIONE • Doppio target: – DNA girasi (topoisomerasi II): soprattutto nei gram-negativi – Topoisomerasi IV: soprattutto nei gram-positivi • Dettagli molecolari ancora non ben compresi • Possibile formazione di complessi enzima-DNA-farmaco p che bloccano la replicazione degli acidi nucleici (MODELLO COOPERATIVO) • Altri possibili fattori (proteine ?) intervengono in questa fase • Potente ATTIVITÀ BATTERICIDA 17 Morrissey I et al., AAC, 40: 1775-1784, 1996 18 MECCANISMI DI RESISTENZA • SINTESI DI UN TARGET ALTERATO • PROTEZIONE DEL TARGET • EFFLUSSO DELL’ANTIBIOTICO 19 MECCANISMI DI RESISTENZA (1) – SINTESI DI UN TARGET ALTERATO • RESISTENZA CROMOSOMICA • Mutazioni puntiformi in regioni precise di ciascuna delle due subunità dei due enzimi (QRDR: quinoloneresistance-determining region) • Mutazioni successive • Efetto più importante per mutazioni di subunità GyrA (gram-negativi) e ParC (gram-positivi) 20 MUTAZIONI GENI GyrA y E ParC 21 MUTAZIONI GENI GyrB y E ParE 22 MECCANISMI DI RESISTENZA (2) – PROTEZIONE DEL TARGET • RESISTENZA PLASMIDICA • Mediata da diverse classi di geni Qnr che codificano per una proteina di circa 220 aa • La proteina QnrA previene il legame dei chinoloni alle topoisomerasi di tipo II • Franca resistenza ai chinoloni e ridotta sensibilità chinoloni, ai fluorochinoloni 23 MECCANISMI DI RESISTENZA (3) – EFFLUSSO DELL DELL’ANTIBIOTICO ANTIBIOTICO • Mediata da trasportatori attivi di membrana • Iperespressione di pompe multiantibiotico: – – – – NorA (S. aureus) PmrA (S. (S pneumoniae) MexD (P. aeruginosa) MexF (P. aeruginosa) • RESISTENZA CROMOSOMICA • Possibile associazione con meccanismi di downregulation di porine per i gram-negativi 24 POMPE MDR 25 LA RIFAMPICINA 26 CARATTERISTICHE GENERALI • Antibiotico semisintetico che inibisce la subunità β della RNApolimerasi DNA-dipendente batterica • Meccanismo di resistenza associato a mutazioni concentrate in una regione di 69 bp del gene rpoB (RRDR: rifampin-resistancedetermining region) • Utilità clinica in casi di micobatteriosi • Utilizzato sempre in associazione con altri farmaci per limitare l’isorgenza di resistenze 27 RRDR 28 IL SINERGISMO TRIMETHOPRIM - SULFAMIDICI 29 CARATTERISTICHE GENERALI • Molecole semisintetiche che agiscono su fasi successive della sintesi dell’acido tetraidrofolico • Le cellule eucariotiche NON sono in grado di sintetizzare il THF dal PABA ma devono utilizzare di tt direttamente t l’l’acido id ffolico li • SULFAMIDICI: inibitori competitivi p dell’enzima DHPS a seguito di omologie strutturali con il vero ( ) substrato (PABA) • TRIMETHOPRIM: inibitore p dell’enzima DHFR a competitivo seguito di omologie strutturali con il vero substrato (DHF) 30 VIA BIOSINTETICA DEL THFA DHPS DHFR 31 RUOLO DEL THFA 32 MECCANISMI DI RESISTENZA • EFFLUSSO O DIMINUITA PENETRAZIONE DELL ANTIBIOTICO DELL’ANTIBIOTICO • SINTESI DI UN TARGET ALTERATO O IPERPRODUZIONE DEL TARGET 33 IL METRONIDAZOLO 34 CARATTERISTICHE GENERALI • Farmaco molto attivo sui batteri anaerobi • Attivazione della molecola a seguito della riduzione in posizione 5’ • Molecola attivata solo da batteri con un basso potenziale redox interno (anaerobi) • La molecola attivata agisce sottraendo elettroni dalla doppia elica di DNA destabilizzandola • Meccanismi di resistenza legati a problemi di uptake 35 BREVI CONSIDERAZIONI CONCLUSIVE 36 NEL 1988 IN UK PRIMO ISOLATO DI ENTEROCOCCO VANCOMICINO RESISTENTE VANCOMICINO-RESISTENTE (VRE) EMERGENZA DELLA RESISTENZA Anni per Anni per osservare 25% osservare resistenza di resistenza in ospedale Antibiotico Anno di introduzione Penicillina 1941 0-2 Meticillina 1961 1 6 25-30 Anni per osservare 25% di resistenza in comunità 15-20 DISTRIBUZIONE DIVERSA DELLE RESISTENZE IN COMUNITÀ FRA EUROPA E USA 40 Oggi fino al 60-70% degli stafilococchi ospedalieri è resistente alla meticillina 34 14 VRSA 34 37 35 L’EMERGENZA L EMERGENZA DI ISOLATI MULTIRESISTENTI RENDE ASSOLUTAMENTE NECESSARIO L’AMPLIAMENTO DELL’ARMAMENTARIO ANTIBATTERICO A NOSTRA DISPOSIZIONE 38 POSSIBILI STRATEGIE • SINTESI DI MOLECOLE CON MIGLIORI CARATTERISTICHE DI SPETTRO D’AZIONE E FARMACOCINETICA IN CLASSI GIÀ ESISTENTI • IDENTIFICAZIONE DI NUOVE MOLECOLE DIRETTE CONTRO NUOVI TARGET • APPROCCI ALTERNATIVI 39 STATO DELL DELL’ARTE ARTE • Storicamente tre importanti funzioni della cellula batterica hanno rappresentato il bersaglio dell’antibioticoterapia: – SINTESI DELLA PARETE – SINTESI PROTEICA – METABOLISMO DEGLI ACIDI NUCLEICI • Processi complessi determinati da reazioni enzimatiche successive • SOLO UNA PICCOLA PARTE DELLE REAZIONI COINVOLTE IN UN DATO PROCESSO SONO OGGI IL BERSAGLIO DI MOLECOLE ANTIBIOTICHE 40 IDENTIFICAZIONE DI NUOVI TARGET (1) • IDENTIFICARE NUOVI BERSAGLI IN VIE BIOSINTETICHE GIÀ SFRUTTATE IN ANTIBIOTICOTERAPIA 41 IDENTIFICAZIONE DI NUOVI TARGET (2) 2) IDENTIFICARE NUOVI BERSAGLI A SEGUITO DELLA MIGLIORE COMPRENSIONE DI ALCUNI ASPETTI DELLA FISIOLOGIA DEL BATTERIO 42 IDENTIFICAZIONE DI NUOVI TARGET (3) 3) SVILUPPO DI MOLECOLE DI NUOVA CONCEZIONE 43 NUOVE MOLECOLE MOLECOLE: DAPTOMICINA 44 Cellular membrane 45 DAPTOMICINA (1) • Membro di una nuova classe di antibiotici già approvata negli USA • Lipopeptide ciclico naturalmente prodotto da Streptomyces reoseosporus • Peculiare meccanismo d’azione • Attivo A i suii b batterii grampositivi (compresi MRSA; VRE e S. pneumoniae multiresistenti) lti i t ti) 46 DAPTOMICINA (2) • Attività calcio-dipendente • Modifiche strutturali che ne permettono l’oligomerizzazione all’interno della membrana • Alterazione dei flussi osmotici e probabili successivi altri effetti intracellulari • Selettività d d’azione azione assicurata dalla diversità delle cariche elettrostatiche di membrana tra cellula procariotica e cellula eucariotica 47 48
Scaricare