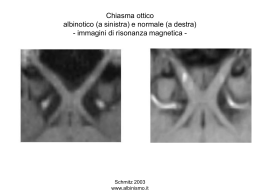
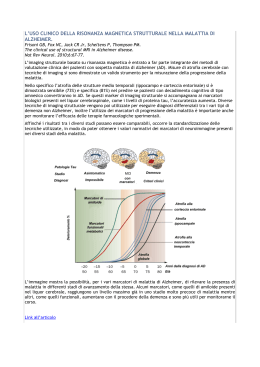
D OTTORATO DI R ICERCA IN N EUROSCIENZE C LINICO -S PERIMENTALI P SICHIATRIA E V ALUTAZIONE DEI F ENOMENI N EURODEGENERATIVI C EREBRALI NELLA M ALATTIA DI A LZHEIMER ATTRAVERSO M ETODICHE C OMBINATE DI R ISONANZA M AGNETICA N ON C ONVENZIONALE R ELATORE D OTTORANDO CHIAR.MO PROF. FRANCO GIUBILEI D O TT . G I U S E P P E B O M B OI M AT R . N . 936783 A NNO A CCADEMICO 2011 - 2012 A Letizia e alla mia famiglia La vita non è quella che si è vissuta, ma quella che si ricorda e come la si ricorda per raccontarla. Gabriel García Márquez L'uomo di scienza non è nient'altro che un misero filosofo. Albert Einstein Il ricordo è poesia, e la poesia non è se non ricordo. Giovanni Pascoli … Come la cosmologia si chiede quale sia la struttura dell'universo, le neuroscienze cognitive si domandano quale sia la struttura della mente. Eric Kandel Che cosa fanno i bambini tutto il giorno? Fabbricano ricordi. Dino Risi Meglio aggiungere vita ai giorni che non giorni alla vita. Rita Levi Montalcini “Alcuni esseri umani credono che l’ani ma viva dopo la morte del corpo; altri credono, invece, che muoia con esso... Altri ancora pensano che, in alcuni casi, l’anima muoia pri ma del corpo: e questo chiamano demenza”. Jay Ringraziamenti Questo studio rappresenta un ulteriore gradino di quella scala che ho iniziato a salire nel 2001 quando, poco più che ventenne, ho deciso di occuparmi degli uomini “senza memoria”, cioè dei pazienti affetti da malattia di Alzheimer e da altre forme di demenza. E, dopo avergli dedicato la quasi totalità delle mie ricerche e tutte le mie tesi universitarie, dedico loro anche questo lavoro come uomo e come medico. Già, perché questo studio vorrebbe essere un altro piccolo “pezzo di luce” nelle tenebre che avvolgono le circonvoluzioni cerebrali di chi è affetto da un processo neurodegenerativo. In questa ricerca ci sono momenti trascorsi a Roma dentro un vecchio policlinico e momenti passati dentro uno stretto e più moderno ospedale, momenti trascorsi ad ovest, dalla parte americana dell’oceano, momenti spesi ad est, dentro un laboratorio ungherese e, infine, momenti passati in reparti ed ambulatori della regione Lazio e nella mia casa. E nei miei sogni. Questo studio è la sintesi della mia esperienza clinica e della mia ricerca scientifica, tratti che hanno profondamente segnato la mia esistenza dai vent’anni al “mezzo del cammin di nostra vita”: nell’arco di questo tempo spero di essere “cresciuto”, di aver sempre prestato fede al Giuramento d’Ippocrate, di aver meritato il recente titolo di Neurologo e di meritare adesso il titolo di Dottore di Ricerca in Neuroscienze. Questo lavoro è stato realizzato grazie a persone che soffrono e che non smetterò mai di ringraziare. Un grazie particolare va al Prof. Franco Giubilei perché mi ha accompagnato nel corso di tutti questi anni. Ringrazio sentitamente il Prof. Francesco Orzi soprattutto perché, due anni circa or sono, mi consigliò di partecipare al Department to Department Programme realizzato dalle European Federation of Neurological Societies. Mi sono così ritrovato alla "corte" del Professor László Vécsei, nella Neurológiai Klinika dell’Albert Szent-Györgyi Medical and Pharmaceutical Center Faculty of General Medicine della University of Szeged, dove, grazie alla collaborazione con il Dr. Zsigmond Tamás Kincses e con i ragazzi della Sezione di Neuroimmagini, soprattutto quella della Dr. Nikoletta Szabó, ho appreso metodiche fondamentali per analizzare immagini di Risonanza Magnetica. Questa esperienza, sommata a quella maturata, durante un periodo del mio percorso di specializzazione in Neurologia, presso i National Institutes of Health di Bethesda, negli Stati Uniti d’America, nel gruppo del Dr. Henry McFarland, mi ha permesso di conoscere varie interessanti metodiche di analisi di neuroimmagini cerebrali. Tutto questo ha portato alla realizzazione del protocollo base di questo progetto, già premiato nel 2010 dal Prof. Cesare Fieschi con il Premio Aleth Barbot Patrassi per le Neuroscienze. Ringrazio, quindi, più di tutti la Dott.ssa Elisabetta Giugni, il Prof. Stefano Bastianello, il Dott. Giacomo Luccichenti e il Dott. Stefano Galletti della Fondazione Biomedica Europea, la Dott.ssa Francesca Romana Pezzella dell’Azienda Ospedaliera San Camillo Forlanini, la Dott.ssa Rita Vadalà dell’IRCCS Fondazione Santa Lucia e la Dott.ssa Orietta Picconi di Opera S.r.l. Genova per aver attivamente collaborato con me alla realizzazione di questo lavoro. Ringrazio anche i colleghi del “Centro Demenze” dell’Ospedale Sant’Andrea, con cui ha trascorso costruttivi momenti di lavoro e sono molto riconoscente al Prof. Cesare Fieschi che, nel 2001, mi ha accolto nel Dipartimento di Scienze Neurologiche. Sono poi immensamente grato alle strutture del San Raffaele Pisana di Roma, dell’Istituto Santo Volto e dell'Unità Operativa di Geriatria e Medicina di Montefiascone (AUSL Viterbo) presso cui ho lavorato nel corso di questi ultimi anni e dell’Ars Medica di Santa Marinella e della Unità Operativa di Medicina Generale di Tarquinia (AUSL Viterbo) presso cui lavoro attualmente poiché mi hanno permesso di mantenermi economicamente durante questo percorso di Dottorato di Ricerca senza borsa. E voglio ringraziare tutto il personale di tutte queste strutture. Un grazie particolare va a tutti i miei grandi amici, soprattutto a Marco, Stefano, Daniele, Beto, Francesco, Diego, Antonella e Alina perché mi sono sempre rimasti vicini anche quando la distanza sembrava un problema e i capelli iniziavano a cadere o a farsi bianchi. Sono molto riconoscente alla mia famiglia che mi ha insegnato a non mollare mai e a non perdere mai la speranza. Infine, un immenso ringraziamento è per Letizia con cui ho condiviso tutte le difficoltà e tutti i successi di questi anni perché mi ha supportato e sopportato con la sua tenacia, la sua comprensione ed il suo amore. INDICE INTRODUZIONE ................................................................................... 1 VALUTAZIONE NEUROANATOMICA E NEUROMETABOLICA DEI DISTURBI COGNITIVI..................... 3 I disturbi cognitivi.................................................................................................. 3 I marcatori anatomici e metabolici nelle neuroscienze cognitive ...................... 7 LA MALATTIA DI ALZHEIMER ....................................................... 9 Epidemiologia ....................................................................................................... 11 Ipotesi eziopatogenetiche ..................................................................................... 15 Problematiche diagnostiche e terapeutiche ....................................................... 21 LA RISONANZA MAGNETICA NON CONVENZIONALE ......... 25 Le tecniche di RM non convenzionale utilizzate in questo studio ................... 30 Analisi postprocessamento di immagini di RM in diffusione ........................... 30 Analisi postprocessamento di immagini di RM strutturale ............................... 49 Analisi postprocessamento di immagini di spettroscopia in RM ...................... 60 IL NOSTRO STUDIO .......................................................................... 66 Disegno dello studio ............................................................................................. 66 Popolazione ........................................................................................................... 67 Metodi ................................................................................................................... 69 Visita neurologica .............................................................................................. 70 Valutazione Neuropsicologica ........................................................................... 71 Risonanza Magnetica ......................................................................................... 72 Analisi statistica ................................................................................................. 79 Risultati ................................................................................................................. 81 Discussione............................................................................................................ 86 BIBLIOGRAFIA ................................................................................XCI Introduzione INTRODUZIONE Negli ultimi anni, in conseguenza dell'aumento dell'aspettativa di vita media, particolarmente in Italia, si sta assistendo ad una crescita esponenziale di tutte le patologie croniche e correlate all’età. Tra queste patologie, le demenze stanno acquisendo, sempre di più, un ruolo di primo piano. La Malattia di Alzheimer (MA), in particolare, rappresentando la causa più comune di demenza, è diventata un vero e proprio problema di sanità pubblica con risvolti socio-economici dall’impatto devastante. Nonostante le recenti scoperte sui meccanismi fisiopatogenetici, la diagnosi di MA resta un problema di notevole rilevanza pratica: attualmente, infatti, le metodiche diagnostiche a disposizione non permettono di arrivare ad una diagnosi di certezza, con conseguenti ed inevitabili problemi di scelta terapeutica per il neurologo. Il ruolo delle neuroimmagini è stato, fino ad oggi, principalmente rivolto ad escludere altre patologie che, clinicamente, entrano nella diagnosi differenziale con la MA. Infatti, le tecniche di Risonanza Magnetica (RM) convenzionale non permettono di distinguere, in base ai soli dati morfologici, le differenti malattie neurodegenerative primitive, se non in rari casi, e non forniscono informazioni quantitative sui processi degenerativi. 1 Introduzione Lo scopo del presente studio è stato quello di individuare tecniche valide ed efficaci per la quantificazione della degenerazione neuronale mediante metodiche non convenzionali di RM e attraverso aggregati di valori derivati da queste stesse metodiche per permettere di ottenere indici maggiormente sensibili nell’individuazione della degenerazione precoce con importanti risvolti terapeutici. 2 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi VALUTAZIONE NEUROANATOMICA E NEUROMETABOLICA DEI DISTURBI COGNITIVI I disturbi cognitivi “Se il cervello umano fosse così semplice da permetterci di sondarlo, allora saremmo noi gli stupidi a non capirci nulla lo stesso.” In questa frase dello scrittore e filosofo contemporaneo Jostein Gaarder1 viene espressa con un paradosso la complessità della cognizione umana. Il termine “cognizione” (dal greco e dal latino cognoscere, “conoscere”, “sapere”) è utilizzato in diverse accezioni da differenti discipline ed è, generalmente, accettato con riferimento al pensiero ed al modo con cui si raggiunge la consapevolezza. Nelle neuroscienze, il vocabolo viene usato per riferirsi alla capacità, caratteristica degli organismi viventi avanzati e, in particolare dell’uomo, di possedere processi mentali coinvolti nella conoscenza e nella comprensione. Tali processi o funzioni cognitive includono il pensiero astratto, il sapere, il linguaggio, la memoria, il giudizio e la capacità di risolvere i problemi. 3 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi "Come dalla materia inanimata si è pervenuti alla materia organica e da questa alla formazione di quello stupendo congegno che è il cervello dell'Homo sapiens?" Questa è la domanda posta da Rita Levi Montalcini in una sua opera recente e a cui le neuroscienze stanno cercando da anni di dare risposte in senso evoluzionistico2. Eric Kandel considera la mente umana la sfida della biologia del terzo millennio sostenendo che "come la cosmologia si chiede quale sia la struttura dell'universo, le neuroscienze cognitive si domandano quale sia la struttura della mente3." Nel corso dei secoli, è stato dimostrato, sempre in maniera più evidente che i fenomeni fisici che sono alla base dei processi cognitivi sono sostenuti da reti neurali localizzate all’interno del sistema nervoso. In molti casi, dal punto di vista anatomico, è stato possibile localizzare in determinate aree cerebrali alcuni domini cognitivi responsabili di funzioni neuropsicologiche. Attualmente lo sviluppo della tecnologia ha radicalmente modificato il modo di analizzare la mente umana. Così, per poter indagare il cervello umano "si è passati dal tavolo anatomico allo schermo del computer", con risvolti pratici sempre più importanti in ambito scientifico e clinico. 4 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi In un articolo di fondamentale valore scientifico, pubblicato sulla rivista Brain, nel 1998, Mesulam, ipotizza l’organizzazione delle reti neurali responsabili dei processi cognitivi4 (Fig. 1). Fig. 1. Rappresentazione generale di una larga scala di reti. Le linee senza punte di freccia rappresentano connessioni reciproche. Le connessioni corticali allo striato non sono reciproche. Le linee tratteggiate illustrano le proiezioni talamiche. Le aree A e B rappresentano due epicentri della rete A, B. Le aree 1AB, 2AB e 3AB rappresentano tre componenti crticali additive della rete. AB, XA e BY rappresentano I nuclei subtalamici. Immagine comparsa su Annals of Neurology (Mesulam, 1990). Tuttavia, i sistemi cognitivi sono suscettibili di alterazione. Con la dizione di “disturbo cognitivo” ci si riferisce a quella condizione patologica in cui un individuo presenta disturbi o deficit in una delle funzioni neuropsicologiche, come la memoria, il linguaggio o altre funzioni, tali da poter essere osservati da altri individui o da poter essere messi in evidenza con test mirati. I disturbi cognitivi possono essere congeniti cioè presenti alla nascita o acquisiti: in questo ultimo caso, oggetto di questa tesi, il soggetto va incontro alla perdita o all’alterazione di una funzione cognitiva che possedeva in precedenza. 5 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi Quando i disturbi cognitivi acquisiti interessano più funzioni e divengono tali da interferire con le attività della vita quotidiana, si utilizza, per descriverli, il termine "demenza". Pertanto, con il termine demenza, si intende un disturbo mentale, acquisito, caratterizzato dalla perdita di funzioni che il soggetto possedeva nel passato. Temporanee alterazioni delle funzioni cognitive possono essere comunemente individuate in alcuni stati dismetabolici o in alcune patologie psichiatriche come l’ansia o la depressione. In alcuni casi queste alterazioni possono essere così rilevanti da configurare un quadro che viene definito di “pseudo-demenza”. In altre patologie, invece, una volta instauratosi, il danno cognitivo diviene irreversibile, configurando un quadro di demenza che, in determinati casi, tende a progredire. La presenza dei disturbi cognitivi nelle malattie neurologiche è molto elevata: disturbi cognitivi possono, infatti, essere individuati in tutte le malattie che possono colpire l’encefalo. Patologie neurologiche ritenute fino a poco tempo fa “fisiche”, cioè responsabili di danno nelle funzioni motorie o sensitive, come la Sclerosi Multipla (SM), la Sclerosi Laterale Amiotrofica (SLA) e le patologie cerebrovascolari, possono essere associate ad alterazioni cognitive. Solo nelle demenze degenerative, tuttavia, si assiste ad un’alterazione di queste funzioni in maniera primitiva e primaria. La valutazione del loro correlato anatomico-strutturale e metabolico sarà l’oggetto principale di questa tesi. 6 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi I marcatori anatomici e metabolici nelle neuroscienze cognitive La descrizione del caso di Tan da parte di Pierre Paul Broca, nel 18615, può essere considerata una delle prime dimostrazioni scientifiche del fatto che le funzioni cognitive possiedano un correlato neuroanatomico. È negli ultimi anni, tuttavia, che l’avvento delle neuroimmagini ha permesso la visualizzazione in vivo del substrato anatomico che si ritiene responsabile dei processi cognitivi. Il supporto di strumenti diagnostici sempre più evoluti fornisce attualmente informazioni sia funzionali che anatomiche sul sistema nervoso. In particolare, l’invenzione della Risonanza Magnetica Nucleare6 7 e la sua applicazione in vivo8 ha rappresentato una svolta nello studio delle malattie neurologiche, soprattutto grazie alla possibilità di utilizzare quelle che vengono definite metodiche non convenzionali, come il tensore di diffusione, il magnetization transfer ratio, la spettroscopia in RM o l’acquisizione di sequenze strutturali tridimensionali9. Personalmente ho avuto l’opportunità di apprendere alcune di queste metodiche di analisi post-processamento di immagini, durante la mia esperienza di "Specializzazione in Neurologia all'estero" presso il National Institute of 7 Valutazione neuroanatomica e neurometabolica dei disturbi cognitivi Neurological Disorders and Stroke (NINDS) dei National Institutes of Health (NIH) di Bethesda, in Maryland, negli Stati Uniti d’America nel 2007. Durante quel periodo ho preso parte ad un grande progetto, condotto dal Dr. McFarland e dalla Dr. Bagnato, volto ad esplorare il ruolo che le alterazioni cerebrali macroscopiche e microscopiche causate dalla SM hanno nella genesi dei disturbi cognitivi10. Successivamente ho avuto occasione di apprendere altre metodiche durante la mia esperienza di "Dottorato di Ricerca in Neuroscienze all'estero" presso la University of Szeged in Ungheria nel 2010. Infatti, ho collaborato ad un progetto volto ad indagare le alterazioni microstrutturali che avvengono nei pazienti affetti da emicrania11. L’applicazione delle metodiche di analisi post-processamento delle neuroimmagini ai pazienti affetti da MA ed il successivo confronto con la performance cognitiva degli stessi pazienti, obiettivo di questo studio, potrebbe fornire importanti informazioni in ambito clinico e biologico e aprire nuove porte in ambito diagnostico. 8 La Malattia di Alzheimer LA MALATTIA DI ALZHEIMER Nel 1906, a Tübingen, in Germania, il Dott. Alois Alzheimer (Fig. 2) di Monaco descrisse il caso di Auguste D.12 (Fig.3). Si tratta della prima descrizione scientifica di un caso di demenza degenerativa. Oggi la MA rappresenta la più comune forma di demenza e una delle principali cause di morte e disabilità Fig. 2. Alois Alzheimer. della nostra era. Si tratta di un quadro drammatico, non solo sotto il punto di vista personale dell’individuo affetto, ma anche sotto il punto di vista socio-affettivo, perché interessa da vicino anche le persone che vivono e conoscono la persona malata. Nel corso della patologia si assiste, infatti, alla progressiva perdita dei ricordi e, quindi, dell’essenza stessa dell’identità, accompagnata da deficit del pensiero astratto, delle capacità di giudizio critico, delle funzioni corticali Fig. 3. Auguste D., il primo caso descritto di "demenza degenerativa". superiori (fasie, modificazioni prassie, della gnosie) personalità, e, in spesso, da assenza di compromissione dello stato di coscienza. A causa dell'aumento dell'aspettativa di vita media, negli ultimi decenni si sta assistendo ad una crescita esponenziale di tutte le patologie croniche età correlate, 9 La Malattia di Alzheimer prime fra tutte le demenze. L'interesse scientifico rivolto a queste patologie ha portato al rapido sviluppo di tecniche di biologia molecolare volte all'identificazione dei processi patogenetici che le sottendono e alla realizzazione di nuove strategie terapeutiche. A fronte di questi progressi scientifici, la diagnosi di demenza presenta ancora delle difficoltà. Le metodiche diagnostiche fino ad oggi a disposizione, infatti, non permettono di arrivare ad una diagnosi di certezza, fatto che può generare problemi di scelta terapeutica per il clinico. La diagnosi è, infatti, principalmente basata sulla valutazione neuropsicologica ed è tuttora fondamentale il ruolo del MiniMental State Examination (MMSE) 13 nella valutazione iniziale di un disturbo dementigeno. Le difficoltà divengono ancora maggiori in campo di diagnostica differenziale: nonostante, infatti, la MA sia la più comune forma di demenza degenerativa, è piuttosto difficile distinguerla da altre forme di demenza degenerativa. 10 La Malattia di Alzheimer Epidemiologia Secondo vari studi effettuati in Occidente, l’età avanzata rappresenta il fattore di rischio più importante per il possibile sviluppo di demenza: tra i 60 ed i 64 anni l’1% degli individui viene colpito dalla malattia, mentre dopo i 95 anni ne viene colpito oltre il 35%. È stato evidenziato, da stime nordeuropee, che il tasso di prevalenza tende a raddoppiare ogni 5 anni di età, a partire dai 60 fino ad arrivare ai 95 anni14. Questo è un dato allarmante soprattutto se si considera che il numero delle persone anziane nella popolazione è in continua crescita: nel 1995, nel mondo, gli ultra sessantacinquenni erano 371 milioni di persone, cioè il 6% della popolazione mondiale. Molti di loro vivono oggi il dramma della demenza che colpisce 18 milioni di individui nel mondo, quasi tutti anziani, la metà dei quali vive in Nord America ed in Europa. In Italia la situazione è ancora più preoccupante: nel 1995, nel nostro paese, gli ultrasessantacinquenni erano 9.5 milioni, cioè il 16% della popolazione. Secondo stime dell’Istat nel 2025 un italiano su quattro avrà più di 65 anni di età ed uno su nove più di 75 anni. Complessivamente, oltre il 41% della popolazione avrà più di 55 anni di età. Il nostro paese, comunque, come altri paesi sviluppati, ha già calcolato le proiezioni per valutare l’aumento di incidenza delle demenze. Se si parte dall’assunto 11 La Malattia di Alzheimer che i tassi di incidenza età-specifici non cambieranno nei prossimi anni, nel nostro paese si prevedono 213.000 nuovi casi di demenza ogni anno a partire dal 2020 contro i 150.000 rilevati Fig. 4. In Italia si prevedono 213.000 nuovi casi di demenza ogni anno a partire dal 2020 contro i 150.000 rilevati nel 2000. Fig. 3. Proiezioni dei casi di demenza nei prossimi 20 anni nel 2000 (Fig. 4). L’ILSA (Italian Longitudinal Study On 300000 200000 Aging), un altro grande studio prevalenza italiano 100000 di 0 2000 2020 sesso- specifica, ha evidenziato che la demenza interessa il 5.3% degli uomini ed il 7.2% delle donne sopra i 65 anni di età15 16. Al momento attuale quasi un milione di famiglie italiane sono toccate dal problema della demenza ed in sostanza abbandonate, dimenticate nella loro penosa situazione di bisogno17. I dati emersi dallo studio Censis sottolineano il carattere familiare delle demenze. Questo in un duplice senso: da una parte è risultato totale il coinvolgimento dei familiari nella cura, nell’assistenza, nel sostegno psicologico e nella tutela del proprio congiunto e dall’altra parte è risultata grave la carenza dei servizi sanitari e socio-assistenziali di supporto ai bisogni di assistenza, con implicita e totale delega alla famiglia che si trova a doversi occupare da sola dei suoi cari affetti dalla malattia. Ecco perché le demenze sono delle vere e proprie “malattie familiari”. 12 La Malattia di Alzheimer Nel 1998, negli USA, i costi delle demenze sono stati superiori a quelli del cancro, cioè i più elevati in campo sanitario, soprattutto se si calcola che, nello stesso anno, la malattia colpiva 4 milioni di anziani. I costi per singolo paziente sono elevatissimi, cioè oltre 25.000 dollari l’anno soprattutto se confrontati con quelli di altre patologie: per il cancro e la schizofrenia vengono spesi 15.000 dollari l’anno per paziente. In Italia non è facilmente stimabile il peso economico della malattia, da un lato perché mancano registri sanitari, che sono invece utilizzati da anni in paesi come gli USA, il Canada (Quebec) e la Svezia, dall’altro perché è molto difficile valutare l’entità dei costi diretti e soprattutto indiretti. Appare, in effetti, arduo calcolare quanto costi la cura e l’assistenza dei malati non tanto a livello sanitario, ma soprattutto a livello sociale, considerata l’impossibilità di valutare la perdita economica arrecata al sistema statale da un individuo, spesso un parente che sottrae ore lavorative alla sua attività per prendersi cura dell’ammalato. Questa persona, spesso il coniuge o un parente, definita caregiver (Fig. 5) che si occupa direttamente Fig. 5. Colui che si occupa del paziente con demenza è, generalmente, il coniuge o un parente. del paziente colpito da demenza, è sottoposto a due tipi di carico assistenziale: un carico oggettivo ed uno soggettivo. Il carico oggettivo nasce da problemi pratici legati alle modificazioni del comportamento e delle abitudini di vita dell’individuo affetto da demenza. Il carico soggettivo è legato, invece, alla sfera emotiva ed alla sofferenza prodotta in un individuo, costretto ad assistere, inerte, al lento ed 13 La Malattia di Alzheimer inesorabile declino di una persona cara. Il carico soggettivo del caregiver è solo parzialmente correlato alla gravità del deficit cognitivo e funzionale del paziente: molto più importanti sembrano essere la qualità della relazione esistente fra paziente ed assistente, il supporto sociale disponibile ed il modo di porsi davanti al decadimento di qualcuno che si ama18. 14 La Malattia di Alzheimer Ipotesi eziopatogenetiche Le ricerche nel campo della genetica e della biologia molecolare hanno prodotto alcune interessanti scoperte nel campo della MA19, anche se i meccanismi patogenetici della malattia restano poco chiari. I principali aspetti clinici di questa Fig. 6. A sinistra immagine di corteccia cerebrale normale. A destra atrofia corticale. malattia neurodegenerativa sono, in genere, la perdita della memoria ed il successivo declino cognitivo, che rappresentano l’espressione di un’importante e progressiva rarefazione neuronale di varie aree cerebrali, che si esprime macroscopicamente con l’atrofia cerebrale 20 (Fig. 6). Studi neuropatologici post mortem21 permettono di individuare i glomeruli neurofibrillari e le placche senili, ovvero le alterazioni microscopiche descritte per primo da Alois Alzheimer 22 23. I glomeruli neurofibrillari (Fig. 7) sono alterazioni citoscheletriche derivanti dall’accumulo di proteina τ, iperfosforilata in maniera abnorme e aggregata in classi di neuroni suscettibili. Nelle cellule nervose sane, la proteina τ stabilizza le 15 La Malattia di Alzheimer componenti microtubulari del citoscheletro che sono coinvolte nel trasporto di molecole da un compartimento cellulare e l’altro. La destabilizzazione micro tubulare e l’ostacolo al trasporto assonale, secondari alla formazione di proteina τ iperfosforilata, causa un inappropriato metabolismo proteico, un malfunzionamento sinaptico e un danno alla trasmissione dei segnali legata al trasporto retrogrado dei fattori neurotrofici. La perdita di queste funzioni potrebbe significativamente Fig.7. Glomeruli neuro fibrillare: colorazione argentica contribuire alla morte neuronale. Il prodotto iniziale della fosforilazione patologica è una proteina τ solubile non-argirofila. L’altro aspetto microscopico neuropatologico della malattia, la placca senile (Fig. 8) è, invece, causato principalmente dall’accumulo della proteina β amiloide (Aβ), un peptide derivato dal più grande Precursore della Proteina β Amiloide (APP) cioè da una glicoproteina transmembrana espressa in maniera ubiquitaria 24. L’ipotesi della “cascata dell’amiloide”25, la più accreditata ipotesi patogenetica formulata negli ultimi venti anni, prevede che il peptide Aβ sia una proteina spazzatura che autoaggrega spontaneamente in fibrille amiloidee neurotossiche in grado di instaurare il processo dementigeno. La più lunga forma della proteina Aβ (Aβ 1-42) è la più strettamente correlata al processo Fig. 8. Placca senile patogenetico perché è stato dimostrato che sia sovraespressa in soggetti con una mutazione genetica familiare e che, in vitro, tenda più facilmente ad autoaggregare rispetto alle forme più corte, come la Aβ 1-4026 27. 16 La Malattia di Alzheimer Nonostante questa ipotesi sia molto accreditata, rimane piuttosto incompleta: non spiega, infatti, in alcun modo, che relazione vi sia tra il processo amiloidogenetico extracellulare ed il deposito di glomeruli neurofibrillari all’interno dei neuroni, né quale siano i ruoli fisiologici dell’APP e dei suoi derivati 28 . In particolare, l’ipotesi dell’autoaggregazione delle due componenti microscopiche della patologia lascia senza risposta alcuna importanti domande sulla biologia della MA. Non è noto, infatti, perché una proteina ubiquitaria, come la Aβ, dovrebbe aggregare solo nella neocortex o perchè altre specie di mammiferi non sviluppino una patologia legata alla Aβ durante l’invecchiamento 29 . L’ipotesi non spiega, inoltre, perché l’età senile ed il sesso femminile rappresentino i maggiori fattori di rischio. Gli elementi chimici potrebbero essere la risposta chiave per molte di queste domande 30 31 32 . Recentemente, infatti, studi neurochimici avrebbero individuato un ruolo dei metalli nelle malattie neurodegenerative come la MA 33 34 . È noto, infatti, che i metalli rivestono un ruolo catalitico nello smaltimento di radicali liberi 35 . Evidenze sempre più consistenti dimostrano oggi che l’alterazione dell’omeostasi dell’attività redox catalizzata dai biometalli e il conseguente incremento dello stress ossidativo contribuiscano alla patogenesi della MA 36 37 È stato, infatti, osservato che i metalli possano interagire direttamente con il peptide Aβ 38 . Il legame dei metalli ad Aβ modula alcune proprietà fisiochimiche di Aβ, ritenute fondamentali nei processi patogenetici indotti dal peptide 39 : studiando le proprietà chimiche dei metalli, Bush ha formulato un modello di MA in grado di 17 La Malattia di Alzheimer fornire spiegazioni a molti dei quesiti generati dall’ipotesi della cascata dell’amiloide40. Secondo Bush et al., lo ione zinco rivestirebbe un ruolo chiave nell’aggregazione dell’ Aβ in presenza di condizioni acide interstiziali 41 . Anche il rame ed il ferro prenderebbero parte ai processi neuropatologici. A dimostrazione del loro ruolo, tutti questi metalli sono stati trovati a concentrazioni elevate nelle regioni neocorticali più suscettibili all’insulto primario della MA. In queste regioni, infatti, questi elementi svolgerebbero un ruolo fisiologico. Il rame e lo zinco, ad esempio, vengono rilasciati durante i processi di neurotrasmissione. Lo zinco, in particolare, depositato durante la neurotrasmissione, è in grado di indurre l’accumulo della β-amiloide in modelli murini geneticamente modificati per sviluppare la MA 42 . Poco è noto sul ruolo del rame extracellulare nell’encefalo, ma studi in vitro evidenziano che la deporalizzazione delle cellule nervose cerebrali causa liberazione di rame a concentrazioni micromolari 43 . Inoltre, molti lavori indicano un ruolo cruciale del rame e del ferro nell’aggregazione della Aβ 44. Proprio l’interazione del rame e del ferro con l’Aβ, sarebbe responsabile della tossicità del peptide in studi effettuati su colture cellulari. Infatti, la Aβ catalizza la produzione di perossido di idrogeno tramite riduzione di rame e ferro in un processo in cui si utilizza ossigeno e come substrati agenti biologici riduttivi come il colesterolo, la vitamina C e le catecolamine. In accordo con queste evidenze, Bush et al. hanno ipotizzato che la Aβ e la APP vengano alterate nelle loro funzioni biochimiche principali: la partecipazione all’omeostasi metallo ionica ed il controllo dei processi ossidativi metallo-mediati 45. 18 La Malattia di Alzheimer L’APP possiede, infatti, siti di legame per il rame e lo zinco nel suo ectodominio Nterminale, con i quali modula l’adesività delle proteine ed il trasferimento del rame 46 . L’eccezionale affinità dell’Aβ per il rame e la selettività dei siti di legame per il rame e lo zinco giustificano il suo fisiologico ruolo nel metabolismo degli ioni metallici. L’Aβ e la APP prenderebbero, quindi, anche parte ai normali processi di omeostasi dei metalli 47. Un incremento inevitabile di rame e ferro, età correlato, a livello cerebrale, ipermetallerebbe il peptide Aβ, causando il processo catalitico di genesi del perossido di idrogeno, responsabile della tossicità per autoossidazione dell’ Aβ. In questo senso, la più elevata incidenza della patologia nel sesso femminile, potrebbe essere giustificata dal fatto che in questo sesso è costitutivamente più elevata l’attività del trasportatore sinaptico dello zinco. Recentemente, nel corso delle nostre indagini, anche noi abbiamo dimostrato come la concentrazione anche a livello periferico (nel siero e nel plasma) dei metalli pesanti correli con alcune caratteristiche cliniche della MA 48 e con le alterazioni neuropsicologiche49. Ciò potrebbe costituire l’evidenza che la MA sia un processo amiloidogenetico del sistema nervoso centrale (SNC) con ripercussioni sistemiche. Sulla base di queste recenti evidenze si stanno indirizzando le nuove strategie terapeutiche con obiettivi patogenetici e non solo sintomatici. Infatti, attualmente gli unici farmaci disponibili sul mercato per la MA sono rappresentati da prodotti come la memantina e gli inibitori delle colinesterasi, in grado di migliorare in alcuni casi i sintomi della MA per tempi breve, ma non in grado di influenzare l’inesorabile decorso naturale della malattia. 19 La Malattia di Alzheimer I nuovi farmaci, in corso di studio clinico, che vengono progettati sulla base dell’ipotesi metallo biologica della MA, includono composti, generalmente chelanti, che interdicono il legame della Aβ agli ioni metallici, riducendo, in tal modo, l’aggregazione amiloidea. Tuttavia, l’ipotesi della cascata della β-amiloide non è universalmente riconosciuta e, quindi, neanche la sua spiegazione metallo biologica. Un importante problema, inoltre, è dovuto al fatto che non è possibile formulare una diagnosi di certezza di MA, con gravi conseguenze sul piano terapeutico. 20 La Malattia di Alzheimer Problematiche diagnostiche e terapeutiche Attualmente sono in fase di revisione50 gli attuali criteri diagnostici redatti per la diagnosi di MA, cioè i National Institute of Neurological and Comunicative Disorders and Stroke-Alzheimer’s Disease and Related Disorders Association (NINCDS-ADRDA) Work Group criteria51 e quelli proposti nel Diagnostic and Statistical Manual of Mental Disorders, 4th edition (DSM-IV)52 in considerazione dei loro notevoli limiti dovuti non solo alla mutevolezza della presentazione clinica della malattia, ma soprattutto all’incerto inquadramento patogenetico della patologia. Anche in conseguenza di ciò, e non solo per motivi meramente tecnici, le metodiche diagnostiche, fino ad oggi a disposizione, non permettono di arrivare ad una diagnosi di certezza, fatto che può generare problemi di scelta terapeutica per il clinico. La diagnosi è, infatti, principalmente basata sulla valutazione neuropsicologica ed è tuttora fondamentale il ruolo del MMSE, strumento utilizzato da quasi quaranta anni. Le difficoltà divengono ancora maggiori in campo di diagnostica differenziale non solo con le altre forme di demenza degenerativa, come la demenza frontotemporale (DFT) o la demenza a corpi di Lewy (DCL)53, ma anche con varie forme di demenza secondaria, soprattutto la demenza vascolare. 21 La Malattia di Alzheimer La condivisione dei fattori di rischio, i quadri di neuroimmagini e altre problematiche cliniche e fisiopatologiche rendono, infatti, la MA difficilmente distinguibile dalla demenza vascolare54. Un altro problema che contribuisce a creare difficoltà diagnostiche è la presenza di quadri clinici non classificabili né come normali né come patologici: si tratta dei soggetti con un danno cognitivo isolato o Mild Cognitive Impairment (MCI). Il concetto di MCI è divenuto, dunque, cruciale in questo campo di patologie. I primi criteri diagnostici per il MCI formulati da Petersen55 descrivevano la presenza di un disturbo di memoria isolato in assenza di compromissione delle attività funzionali. Successivamente, il MCI è stato classificato in quattro sottotipi sulla base dei deficit cognitivi presenti: amnestic-MCI/not amnestic-MCI e single/multiple domain56. Questa classificazione non è puramente aneddotica, ma è importante ai fini di una diagnosi precoce di una condizione dementigena. Infatti, il MCI è spesso il primo stadio clinico verso la trasformazione in demenza conclamata con un tasso di conversione annuo del 12%57. Studi più recenti, inoltre, suggeriscono che la conversione vari sia in base alla gravità che al tipo di deficit cognitivo. Il disturbo della memoria episodica, quindi l'amnestic MCI, sembra rappresentare una condizione di maggiore probabilità di progressione a MA. Di contro i restanti sottotipi clinici che enfatizzano la presenza di deficit in domini cognitivi diversi dalla memoria, come ad esempio linguaggio, funzioni esecutive ed abilità visuo-spaziali, hanno una maggiore probabilità di progredire verso forme di demenza diverse dalla MA, come ad esempio la DFT e la DCL. 22 La Malattia di Alzheimer Un grosso contributo in senso diagnostico è stato l’individuazione di marker liquorali specifici che possono essere usati per distinguere diversi tipi di demenza. Si basa sulla ricerca delle due proteine alterate nella MA: la beta amiloide e la proteina . Sfortunatamente la metodica invasiva di prelievo e la non assoluta specificità dell’esame, lo rendono piuttosto scomodo da utilizzare soprattutto in una popolazione prevalentemente anziana. Come già detto, però, il miglioramento delle metodiche diagnostiche sarebbe, senza dubbio, un ausilio importante per lo sviluppo di nuove terapie per la MA. Attualmente, infatti, sono proprio le incertezze patogenetiche e le difficoltà diagnostiche a limitare la ricerca di nuovi farmaci. Le ripercussioni sono enormi: si ribadisce che, ad oggi, gli inibitori delle colinesterasi e la memantina, farmaci esclusivamente sintomatici, rappresentano ancora l’unica arma contro questa forma di demenza. La RM non convenzionale si pone attualmente come la metodica d’avanguardia per l’attuazione del miglioramento diagnostico. Studi effettuati negli ultimi anni, tramite RM non convenzionale, hanno permesso lo studio dei disturbi cognitivi in pazienti affetti da patologie neurologiche diverse dalla malattia di Alzheimer9. Recentissimi studi di correlazione tra dati morfologico-strutturali cerebrali di RM e dati di analisi delle connessioni con trattografia58 hanno dimostrato che le due metodiche combinate possono contribuire al miglioramento della diagnosi. 23 La Malattia di Alzheimer Infatti, le tecniche di trattografia sono state recentemente utilizzate con ottimi risultati per differenziare la AD dal MCI 59 , mentre le metodiche di misurazione dello spessore corticale regionale per differenziare la AD da altre forme di demenza 60 . Non sono invece state utilizzate tecniche non convenzionali combinate di analisi morfologico-strutturale, spettroscopica e di dati ottenuti da metodiche di diffusione. 24 La Risonanza Magnetica Non Convenzionale LA RISONANZA MAGNETICA NON CONVENZIONALE Il ruolo della diagnostica per immagini nello studio delle demenze è sempre più determinante sia grazie alla sua sempre maggiore rilevanza in ambito di diagnostica differenziale sia grazie allo sviluppo di tecniche non convenzionali di RM, quali studi morfometrici, di spettroscopia, di perfusione e di RM funzionale, in grado di quantificare la connettività cerebrale e l’evoluzione della malattia. Nello studio delle demenze, infatti, le tecniche di neuroimmagini, oltre al loro noto ruolo nella diagnosi differenziale, si pongono i seguenti obbiettivi: 1. diagnosi precoce o preclinica; 2. quantificazione della progressione di malattia e dell’efficacia terapeutica. Come noto, la diagnosi differenziale tra demenza primitiva e secondaria, può essere raggiunta mediante le tecniche convenzionali. Queste tecniche di neuroimaging non permettono tuttavia di distinguere, in base ai soli dati morfologici, le differenti malattie neurodegenerative primitive a causa della scarsa specificità. Gli obbiettivi indicati ai suddetti punti, inoltre, non sono stati ancora raggiunti per insufficiente sensibilità delle tecniche diagnostiche. Infatti, la diagnostica per immagini ha fornito risultati incoraggianti, ma ancora insufficienti per ciò che concerne la diagnosi preclinica. La quantificazione della progressione della malattia 25 La Risonanza Magnetica Non Convenzionale e dell’efficacia terapeutica rappresenta poi un obbiettivo ambizioso e anch’esso ben lontano dall’essere raggiunto. Le principali tecniche di neuroimmagini attualmente utilizzate per lo studio del paziente con demenza sono: la tomografia computerizzata, che fornisce una stima dell’entità dell’atrofia cerebrale e l’eventuale presenza di una patologia vascolare, tumorale o idrocefalica. L’utilizzo del mezzo di contrasto non è necessario, salvo il riscontro di altre patologie che lo richiedano, e in questo ultimo caso, a meno di una controindicazione specifica, risulta indicato l’esame di RM; la RM, con tecniche convenzionali o con tecniche non convenzionali, mediante la quale sono possibili, oltre alla valutazione dell’atrofia cerebrale e la presenza di altre patologie, anche la quantificazione di alcuni indicatori microstrutturale metabolici e funzionali dell’attività cerebrale. La RM è attualmente considerata l’esame di riferimento per lo studio del sistema nervoso. Ciascuna tecnica di diagnostica per immagini permette di valutare, con sensibilità e specificità differenti, gli aspetti morfologici, microstrutturali, metabolici e funzionali del SNC. 26 La Risonanza Magnetica Non Convenzionale La RM rappresenta il sistema di neuroimaging gold standard per lo studio del SNC e delle demenze. Le tecniche di RM trovano la loro indicazione a seconda del particolare aspetto patologico che si vuole studiare. È possibile distinguere le tecniche di RM in convenzionali, per lo studio morfologico dell’encefalo, e non convenzionali, che richiedono elaborazioni successive e comunemente non effettuate nella routine clinica. Tra le tecniche non convenzionali si annoverano: la tecnica di diffusione, basata sull’abbattimento, nelle sequenze eco planari, del segnale provocato dalla migrazione delle molecole di acqua, che spostandosi da un punto ad un altro dello spazio, portano in esse la magnetizzazione e la fase acquisite. La diffusione è rallentata dalle strutture anatomiche microscopiche normali ed è alterata in molti processi patologici, in particolare in occasione di alterazioni infiammatorie, di insorgenza di edema citotossico e vasogenico, o di variazioni della cellularità o dell’ampiezza dell’interstizio del parenchima encefalico; la tecnica dell’imaging del tensore di diffusione: l’anatomia microscopica del SNC comporta una prevalenza della diffusione lungo la direzione di decorso dei fasci di fibre nervose. Con la tecnica dell’imaging del tensore della diffusione è possibile rappresentare l’anisotropia della diffusione delle molecole di acqua, dalla quale è possibile desumere il decorso delle fibre nervose. Il decorso delle fibre nervose può essere stimato con tecniche locali deterministiche o con più sofisticate tecniche probabilistiche che permettono 27 La Risonanza Magnetica Non Convenzionale di stimare la probabilità della connessione tra due aree cerebrali anche a partire dalla sostanza grigia; la perfusione con RM, basata sulla stima dell’apporto ematico nel parenchima encefalico mediante la misurazione del segnale durante il passaggio di un bolo di mezzo di contrasto o di sangue con particolare magnetizzazione; la spettroscopia in RM (MRS. acronimo inglese per Magnetic Resonance Spectroscopy) che permette di documentare i livelli di alcuni metaboliti presenti nel SNC. Essa si fonda sulla minima differenza nella frequenza di precessione dei protoni dei metaboliti (chemical shift), dovuta alla reciproca influenza dei gruppi chimici in essi presenti; la RM funzionale che permette di documentare l’attivazione corticale a seguito di uno stimolo o di un esercizio codificato. La tecnica maggiormente utilizzata consiste nel monitorare i cambiamenti nel livello di ossigenazione del sangue, assumendo che durante l’attività neuronale vi sia un aumentato apporto di ossigeno ossiemoglobina, che ed una presenta conseguente proprietà maggiore amagnetiche, presenza rispetto di alla desossiemoglobina dalle proprietà paramagnetiche; la valutazione degli spessori, dei volumi e delle superfici cerebrali tramite analisi post-processamento di immagini di RM strutturale, utilizzando programmi informatici (http://surfer.nmr.mgh.harvard.edu/)61 62 63. 28 quali FreeSurfer La Risonanza Magnetica Non Convenzionale I vantaggi delle tecniche non convenzionali di RM nello studio della AD possono essere: valutare i segni precoci della degenerazione neuronale osservando le alterazioni precoci, biochimiche e microstrutturali, mediante analisi metaboliche e del tensore; verificare le variazioni della connettività delle aree corticali; quantificare la degenerazione corticale e sottocorticale mediante tecniche combinate di imaging postprocessing; valutare l’effetto di trattamenti farmacologici sui parametri di RM, con correlazione della risposta clinica e quantificazione di questi effetti. 29 La Risonanza Magnetica Non Convenzionale Le tecniche di RM non convenzionale utilizzate in questo studio Analisi postprocessamento di immagini di RM in diffusione La diffusione è un parametro utilizzato in risonanza magnetica per produrre immagini basate sui movimenti microscopici delle molecole di acqua. Le immagini pesate in diffusione (o DWI, acronimo inglese per diffusion weighted imaging) evidenziano le variazioni della mobilità dei protoni dell'acqua in un tessuto biologico. L’imaging di diffusione con Risonanza Magnetica (RM) rappresenta l’unica modalità di studio in cui il contrasto dipende dal movimento di diffusione delle molecole. Esistono due modalità di diffusione: isotropica e anisotropica. La diffusione isotropica è quella non dipendente dalla direzione nello spazio, quindi casuale, mentre la diffusione anisotropica è tipica dei tessuti biologici perché la presenza di cellule impedisce il movimento casuale delle molecole costringendole lungo direzioni particolari. La diffusione anisotropica, dipendendo anche dalla presenza delle guaine mieliniche, fornisce informazioni circa l’orientamento, le dimensioni e la geometria delle strutture encefaliche. In generale, già in condizioni normali la componente cellulare del SNC “costringe” il movimento delle molecole d’acqua determinando in tal modo una riduzione del coefficiente di diffusione apparente (Apparent Diffusion Coefficient o ADC). Di contro le varie patologie del 30 La Risonanza Magnetica Non Convenzionale SNC che modificano l’integrità tissutale, rimuovendo alcune di queste “barriere” cellulari, sono responsabili di un’alterazione dei valori di ADC, che incrementano, ma soprattutto della diffusione anisotropica che è sicuramente più sensibile alla microstruttura tissutale. La diffusione è la migrazione di molecole o piccole particelle dovuta al moto causato dall'energia termica. Normalmente ci si riferisce alla diffusione di un soluto in un solvente (ad es. acqua in zucchero) in presenza di un gradiente di concentrazione del soluto. Per descrivere il fenomeno della diffusione vengono utilizzate generalmente le leggi di Fick. Secondo la prima legge di Fick, il flusso del soluto in una particolare direzione è direttamente proporzionale al gradiente di concentrazione attraverso una costante di proporzionalità D, detta coefficiente di diffusione. D dipende dalla temperatura, dalla viscosità del mezzo e dal peso molecolare della molecola diffondente. Dalla prima legge di Fick consegue che quando il soluto è uniformemente distribuito (gradiente di concentrazione = 0) il flusso netto è nullo. Questo accade anche in caso di solvente puro: le molecole del solvente sono distribuite uniformemente e appaiono macroscopicamente in stasi. Ciò non vuol dire che le singole molecole siano immobili ma semplicemente che, in media, la somma vettoriale dei loro spostamenti è uguale a zero. In altre parole la diffusione è un fenomeno che avviene anche in assenza di gradienti di concentrazione. Per visualizzare questo processo di “auto diffusione”, possiamo pensare ad un volume d’acqua pure al quale aggiungiamo in un punto specifico una piccola quantità di 31 La Risonanza Magnetica Non Convenzionale acqua marcata con trizio,un isotopo radioattivo dell’idrogeno. Col passare del tempo la radioattività non sarà più concentrata nel punto di inoculo ma si sarà distribuita nell’intero volume. In pratica, le molecole di acqua triziata si saranno mosse all’interno del fluido senza alcuno spostamento macroscopico del fluido stesso. Questo è esattamente quello che accade all’acqua nei tessuti biologici. Per studiare questo fenomeno di diffusione, in assenza di gradienti di concentrazione, le leggi di Fick non sono applicabili e quindi conviene ricavare il valore di D con un approccio di tipo probabilistico. La distribuzione statistica degli spostamenti delle molecole, per effetto della diffusione, in un intervallo di tempo t, ha un profilo gaussiano con media uguale a zero e varianza data dalla seguente relazione (equazione di Einstein): (1a)<r²> = 2Dt in una dimensione (1b)<r²> = 6Dt in tre dimensioni Ovvero: (2a) |r| = <r²> ½= (2Dt)½ in una dimensione (2b) |r| = <r²>½= (6Dt)½ in tre dimensioni dove |r| è la deviazione standard della distanza percorsa dalle molecole. Questa relazione permette di dire che per molecole libere di diffondere, la distanza percorsa è una funzione lineare della radice quadrata del tempo di diffusione e che la costante 32 La Risonanza Magnetica Non Convenzionale di proporzionalità che mette in relazione queste due grandezze è una funzione di D. Ne consegue che, se siamo in grado di conoscere r per un determinato tempo di diffusione, possiamo calcolare D. Questa è la relazione fondamentale che permette di misurare il coefficiente di diffusione dell’acqua nei tessuti biologici. Nel 1954, Carr e Purcell notarono per la prima volta che il segnale RM poteva essere influenzato dalla diffusione delle molecole64. Questa scoperta è in qualche modo sorprendente perché i metodi per misurare la diffusione si basano sull’utilizzo di gradienti di campo magnetico (G), prodotti dalle bobine che non erano presenti nei magneti usati da Carr e Purcell. Di fatto, Carr e Purcell avevano un magnete così inomogeneo da avere un gradiente di campo magnetico costante di circa 1 Gauss/cm. Se il loro magnete fosse stato di migliore qualità, forse questi pionieri della RM non avrebbero avuto gli elementi necessari per giungere a questa scoperta. Per comprendere come sia possibile misurare la diffusione attraverso l’uso di gradienti di campo magnetico occorre valutare la modificazione di fase degli spin in presenza di gradienti. La frequenza di precessione degli spin è direttamente proporzionale all’intensità del campo, per cui, se il campo magnetico è uniforme, tutti gli spin avranno la stessa frequenza di precessione. Applicando un gradiente di campo magnetico in una certa direzione d si ottiene una variazione nello spazio del campo che produce una diversa frequenza di precessione degli spin in diverse posizioni x (d) lungo la direzione di applicazione del gradiente. La fase Φ accumulata dagli spin in seguito all’applicazione di un gradiente di intensità costante G e di durata δ è una funzione della posizione x ed è data dalla relazione: 33 La Risonanza Magnetica Non Convenzionale (3) x) = γ G δ x assumendo Φ(x = 0)=0 dove γ è la costante giromagnetica del protone. Se applichiamo due gradienti di uguale intensità e durata ma di segno opposto separati da un intervallo di tempo ∆, la fase accumulata dagli spin originariamente in posizione x al momento dell’applicazione del primo gradiente e, spostati dalla posizione x, al momento dell’applicazione del secondo gradiente sarà: (4) Φ = γ G δ ( xi – xf ) Vediamo quindi che la fase dipenderà dallo spostamento (xi – xf) degli spin nell’intervallo di tempo ∆. Per spin statici l’applicazione dei due gradienti non ha alcun effetto, infatti se xi = xf dalla (4) risulta che Φ =0. Se gli spin si sono spostati dalla medesima distanza in modo coerente, come avviene quando abbiamo un flusso ordinato, vi è una identica variazione di fase per tutti gli spin con mantenimento della coerenza di fase e nessuna perdita di segnale. Su questa variazione di fase in presenza di movimento coerente si basa una delle tecniche di angiografia in RM. Infine, se lo spostamento avviene in maniera casuale e disordinata, come nel caso del moto associato alla diffusione, le variazioni di fase sono diverse per i vari spin, vi è perdita di coerenza di fase e conseguente diminuzione del segnale. È importante sottolineare che la perdita di segnale è tanto maggiore quanto maggiore è lo spostamento nell’intervallo di tempo ∆ e poiché la (2) ci dice che lo spostamento in un dato intervallo di tempo dipende da D, possiamo concludere che la perdita di 34 La Risonanza Magnetica Non Convenzionale segnale sarà influenzata dal valore di D e solamente dal valore di D. In particolare si può dimostrare che la perdita di segnale è una funzione esponenziale di D: (5) S(b)=S(b=0)e-bD Dove S(b) è il segnale in presenza dei gradienti sensibilizzati alla diffusione, S (b=0) è il segnale in assenza di gradienti sensibilizzati alla diffusione e b è un fattore che dipende dallo schema di applicazione dei gradienti usato in una particolare sequenza. Nella figura 9 (a) è mostrato lo schema originariamente proposto da Stejskal e Tanner65 per una sequenza spin-echo in cui due gradienti identici sono applicati ai lati dell’impulso a 180°. Figura 9 (a): Schema originariamente proposto da Stejskal e Tanner per sensibilizzare alla diffusione il segnale di una sequenza spin-echo. Due gradienti di elevata intensità sono applicati ai lati dell’impulso a 180°. Figura 9 (a): Figura 9 (b): Utilizzando una sequenza STEAM (STimulated Echo Acquisition Mode) è possibile intercettare il tempo di diffusione mantenendo un TE ragionevolmente breve. 35 La Risonanza Magnetica Non Convenzionale In questo caso b risulta essere: (6) b = γ² G² δ² (Δ - δ/3) La dipendenza del fattore b dal quadrato dell’intensità del gradiente fa capire che il poter disporre di un apparecchio RM che sia in grado di fornire gradienti di elevata intensità sia un requisito fondamentale per acquisire immagini pesate in diffusione. Fino a non molto tempo fa la massima intensità di gradienti in apparecchi per uso clinico era di 1 Gauss/cm. Magneti con gradienti così deboli, non riuscivano a fornire immagini con un soddisfacente livello di sensibilizzazione alla diffusione anche se erano dotati di una sequenza per l’acquisizione di immagini pesate in diffusione. Dalla (6) vediamo che, se si dispone di gradienti di debole intensità, si può tentare di aumentare b incrementando sia la durata del gradiente δ sia la durata dell’intervallo Δ. Il problema è che ogni incremento di δ o Δ comporta un allungamento del TE, e quindi il fattore limitante diventa il rilassamento T2. E' facilmente prevedibile che, se siamo costretti a lavorare con TE di 150-200 ms al fine di ottenere un adeguato peso in diffusione, le immagini prodotte saranno di scarsa qualità. In pratica, per ovviare a questo inconveniente, tutti i centri che hanno attuato la diffusion imaging con magneti con gradienti deboli hanno utilizzato una sequenza STEAM (STtimulated Echo Aquisisition Mode) che è schematizzata nella figura 9 (b). La sequenza STEAM differisce da una sequenza spin-echo (SE) per il fatto che l’impulso a 180° è costituito da 2 impulsi a 90°. Questo comporta che nel periodo fra il secondo e terzo impulso, metà della magnetizzazione è immagazzinata come magnetizzazione longitudinale che quindi decade con una costante di tempo T1. Poiché nei tessuti T1 36 La Risonanza Magnetica Non Convenzionale è molto più lungo di T2, è possibile ottenere Δ molto più lunghi senza eccessivo decadimento del segnale. Il prezzo che si paga è che solo la metà della magnetizzazione è utilizzabile per produrre l’eco, e quindi il rapporto segnale/rumore è esattamente metà di quello che avremmo con una sequenza spin-echo con uguale TE. Abbiamo visto precedentemente che, per molecole libere di diffondere, il coefficiente D è indipendente dal tempo di diffusione Δ ma dipende solamente dalla temperatura e dal peso molecolare. Il coefficiente di diffusione dell’acqua “libera” a 37°C è = 3,2* 10 ³ mm²/sec, ed il suo valore, è inoltre “isotropico”, cioè indipendente dalla direzione in cui si effettua la misura. Considerando molecole d’acqua in tessuti biologici occorre valutare altri fattori che possono modificarne la diffusione. Uno di questi è la presenza di macromolecole che tendono a legare debolmente una certa percentuale dell’acqua tissutale riducendone la mobilità. Dalla conseguente diminuzione di D si potrebbe in teoria stimare la concentrazione di macromolecole nel tessuto ed avere informazioni sulle loro dimensioni. Un altro fattore rilevante è la presenza di barriere biologiche (membrane cellulari, mitocondriali, guaine mieliniche ecc.) che limitano la possibilità di libera diffusione. Studiando lo spostamento delle molecole per distanze sia molto brevi che più lunghe delle dimensioni cellulari, si possono ottenere informazioni sulla mobilità dell’acqua intracellulare e sulla permeabilità delle membrane. Questo si può ottenere con la RM acquisendo dati con differenti intervalli di diffusione Δ. Infatti, per Δ di breve durata (inferiori a 1-2 ms), poche molecole si saranno spostate abbastanza da venire in contatto con la membrana limitante della cellula ed il valore di D sarà quello proprio 37 La Risonanza Magnetica Non Convenzionale dei compartimenti intra ed extracellulare nella assunzione di libera diffusione. Al contrario, per tempi di diffusione lunghi, la maggior parte delle molecole avrà dovuto attraversare la membrana cellulare e il valore di D ci apparirà ridotto (diffusione “ristretta”) in funzione della permeabilità di membrana. E da notare inoltre che la distanza associata alla transizione fra regime di libera diffusione a quello di diffusione “ristretta” ci fornisce informazioni sulle dimensioni cellulari. La valutazione del grado di “restrizione” alla libera diffusione esercitato dalle membrane delle cellule in vivo è però di difficile realizzazione usando comuni apparecchi di RM, perché per le misurazioni di D con tempi di diffusione molto corti occorrono gradienti molto elevati come osservabile nell'eq. (6). Un altro effetto dovuto alla presenza di membrane è che il valore di D per particolari strutture, quali le fibre nervose e muscolari, risulta “anisotropico”, cioè dipendente dalla direzione in cui esso viene misurato. Ad esempio, il coefficiente di diffusione dell’acqua misurato nella sostanza bianca in direzione parallela alle fibre è 1.2 * 10 ³ mm²/sec; 3 volte più alto di quello che si rileva con misurazioni effettuate in direzione perpendicolare alle fibre. Si è ipotizzato che la guaina mielinica fosse primariamente responsabile di questo fenomeno, ma altre ipotesi potrebbero essere valide alla luce di recenti dati dimostranti un discreto grado di anisotropia anche in fibre amieliniche66. In conclusione, la diffusione dell’acqua nei tessuti è influenzata non solo dalla temperatura ma anche da altri fattori quali: — permeabilità delle membrane; — compartimentalizzazione dell’acqua (extracellulare - intracellulare); — dimensioni cellulari; 38 La Risonanza Magnetica Non Convenzionale — caratteristiche ultrastrutturali (ricchezza di organelli e altre strutture dotate di membrane); — grado di anisotropia in strutture quali fibre nervose, muscolari e tessuto connettivale ricco di macromolecole orientate; — orientamento spaziale delle strutture anisotropiche; —composizione fisico-chimica del tessuto (quantità e dimensione delle macromolecole)67. E’ evidente che tutti questi fattori hanno una notevole rilevanza biologica e possono fornire preziose informazioni sulla fisiopatologia del tessuto: la RM è l’unica tecnica oggi disponibile per ottenerle in vivo ed in maniera non invasiva. Può essere utile aggiungere una nota sulla terminologia in uso: la possibilità che l’acqua nei tessuti abbia una diffusione “ristretta” e quindi un coefficiente di diffusione “apparentemente” inferiore a quello che ci si potrebbe aspettare in un mezzo privo di membrane, ha reso di uso comune il termine ADC. Sia per semplicità, sia perché questa terminologia non è condivisa da tutti, anche in riferimento a misurazioni fatte in tessuti biologici, continueremo ad usare il termine coefficiente di diffusione (D). Gli effetti del fenomeno della diffusione degli spin sul segnale RM sono noti da molto tempo68, tuttavia l’applicazione di queste conoscenze al campo delle immagini è piuttosto recente. La realizzazione delle prime immagini di RM sensibilizzate alla diffusione sono state realizzate attorno alla metà degli anni Ottanta69 70. 39 La Risonanza Magnetica Non Convenzionale L’approccio alla “diffusion imaging” può essere affrontato con tre differenti livelli di complessità: 1- immagini pesate in diffusione; 2- mappe del coefficiente di diffusione; 3- tensore di diffusione (diffusion tensor magnetic resonance imaging, DT-MRI)71. Immagini pesate in diffusione L’acquisizione di immagini pesate in diffusione è il punto di partenza per ottenere sia le mappe del coefficiente di diffusione sia le mappe gli elementi del tensore di diffusione; le differenze riguardano il modo in cui i dati vengono processati. Abbiamo visto che utilizzando opportuni gradienti di campo magnetico, una normale sequenza (spin-echo, gradient-echo, STEAM ecc.) può essere modificata in modo da ottenere immagini in cui il contrasto risulta influenzato dallo spostamento delle molecole dovuto alla diffusione nella direzione del gradiente applicato. Mappe del coefficiente di diffusione Acquisendo un insieme di immagini (almeno 2) con diverso grado di sensibilizzazione alla diffusione, è possibile, sfruttando l’equazione (5), elaborare un’immagine calcolata in cui in ogni voxel si ottiene il valore medio di D nella direzione di applicazione del gradiente senza più alcun influsso da parte dei tempi di rilassamento T1 e T2. A queste immagini calcolate diamo il nome di mappe del coefficiente di diffusione. Il contrasto delle mappe del coefficiente di diffusione 40 La Risonanza Magnetica Non Convenzionale fornisce un’informazione diretta del valore di D. Il calcolo di mappe del coefficiente di diffusione richiede una elaborazione dell’immagine al computer ed è quindi un poco più complicato da eseguire rispetto alla semplice acquisizione di immagini pesate in diffusione. Inoltre, per calcolare la mappa di D sono necessarie almeno 2 immagini pesate in diffusione, per cui la durata dell’esame di RM è maggiore. Il vantaggio è che la rimozione dell’influsso di T1, T2 e densità protonica facilita l’interpretazione di eventuali reperti patologici in cui questi parametri sono alterati. Quando questo avviene è infatti impossibile attribuire univocamente ad una variazione di D il cambiamento di segnale nelle immagini pesate in diffusione. Tensore di diffusione Le mappe del coefficiente di diffusione, pur rappresentando un importante passo avanti rispetto alle immagini pesate in diffusione, soffrono comunque di un importante limite, dovuto al fatto che i valori di D ottenuti dipendono dall’orientamento dei gradienti rispetto alla struttura studiata; in pratica dalla posizione del soggetto all’interno del magnete. Questo difetto viene eliminato dall’uso di mappe ottenute con il tensore di diffusione. L’uso di un tensore è un modo matematicamente corretto per descrivere la diffusione in strutture non isotropiche di cui non si conosca a priori l’orientamento nello spazio. Il tensore di diffusione consiste di tre elementi diagonali (Dxx, Dyy e Dzz), e di tre elementi nondiagonali (Dxy, Dxz e Dyz). Dxx, Dyy e Dzz sono dimensionalmente dei coefficienti di diffusione per cui possono essere solo positivi, mentre Dxy, Dxz e Dyz ci informano sul grado di correlazione dei coefficienti di diffusione nei tre assi. Poiché 41 La Risonanza Magnetica Non Convenzionale la correlazione può essere positiva o negativa, Dxy, Dxz e Dyz possono assumere sia valori positivi che negativi. Per calcolare il tensore di diffusione sono necessarie almeno sei immagini pesate in diffusione acquisite con gradienti orientati in direzioni diverse più un’immagine acquisita senza sensibilizzazione alla diffusione. Tramite l’uso del tensore di diffusione siamo in grado di costruire, per ogni voxel, un sistema di coordinate “locali” determinato solamente dalle caratteristiche di diffusività dell’acqua nel tessuto e che risulta indipendente dall’orientamento del soggetto all’interno del magnete. Questo sistema di coordinate è rappresentato da tre direzioni mutualmente perpendicolari (auto-vettori) a cui sono associati tre valori di diffusività (autovalori) che indichiamo, in ordine di grandezza decrescente, come 1, 2, 3 (Fig. 10). Questi tre valori rappresentano i semiassi di un ellissoide la cui superficie è data dall’insieme delle distanze di diffusione ad uguale probabilità per quel particolare tempo di diffusione Δ . Da tali elementi si ricava l’indice di anisotropia (“Lattice index”). Fig. 10. Principali parametri utilizzati in diffusione. 42 La Risonanza Magnetica Non Convenzionale Le regioni in cui la diffusione è isotropica (l =2 = 3) appaiono scure in queste immagini, mentre regioni in cui la diffusione è anisotropica, cioè diversa in differenti direzioni, appaiono chiare. Le strutture anisotropiche appaiono tanto più chiare quanto maggiore è il loro grado di anisotropia. Tipicamente la sostanza bianca è più anisotropica del liquor o della sostanza grigia. E’ importante notare, tuttavia, che vi è un alto grado di variabilità nell’anisotropia della sostanza bianca. L’anisotropia è alta in regioni, dove le fibre sono arrangiate in fasci paralleli, come nel corpo calloso, mentre l’anisotropia è molto più bassa in regioni dove le fibre sono orientate in modo incoerente all’interno del voxel, come nelle zone sottocorticali o nel centro semiovale. Questa dipendenza dell’anisotropia dalla “architettura” della sostanza bianca è una scoperta relativamente recente 72 , che è stata possibile in seguito all’uso del tensore di diffusione nello studio della sostanza bianca. Un’altra utile quantità scalare derivata dagli autovalori è la traccia del tensore di diffusione che si può ottenere sommando i tre autovalori (traccia = 1 + 2 + 3). Nel cervello normale, la traccia ha valori molto omogenei in tutto il parenchima cerebrale. La traccia è utile per identificare piccole variazioni della diffusività del parenchima che passerebbero inosservate nelle mappe del coefficiente di diffusione. E’ utile sottolineare che sia indici di anisotropia calcolati a partire dagli autovalori del tensore di diffusione sia la traccia sono indipendenti dall’orientamento dei gradienti rispetto alla struttura studiata e quindi sono indicativi di proprietà intrinseche del tessuto indipendenti dalla posizione del soggetto all’interno del magnete. La traccia del tensore e gli indici di anisotropia sono grandezze scalari che contengono essenzialmente informazioni derivate dagli autovalori del tensore. Altre informazioni 43 La Risonanza Magnetica Non Convenzionale importanti sono però contenute negli autovettori del tensore. In conclusione abbiamo visto come uno studio in diffusione ci può fornire informazioni sulla struttura ed architettura del sistema nervoso che non potremmo ottenere con nessuna altra tecnica in modo non invasivo. Nei pazienti con MA c’è un considerevole danno microscopico a carico della sostanza bianca non riconosciuto dalle sequenze RM convenzionali, ma dimostrato dalla RM con il calcolo del Tensore di Diffusione e in particolare dallo studio della Anisotropia Frazionaria (FA), indice di integrità delle fibre assonali. Nei pazienti con AD, le fibre di sostanza bianca che connettono le aree associative presentano valori ridotti di FA e aumentati di diffusione dovuti verosimilmente alla degenerazione walleriana degli assoni conseguente all’atrofia della corteccia associativa. Dalla teoria alla pratica: analisi delle immagini tramite FSL Per l'analisi di immagine di RM in diffusione ci si può avvalere dell'aiuto delle invenzioni del Functional Magnetic Resonance Imaging of the Brain (FMRIB) di Oxford e, in particolare del FMRIB Software Library (FSL). FSL consiste in una serie di programmi che contengono strumenti per l'analisi delle immagini e programmi di statistica per l'analisi dei dati provenienti da immagini di risonanza magnetica funzionale, strutturale e di risonanza magnetica a tensore di diffusione (fig. 11). Il programma FSL è disponibile sia come file binario pre-compilato che come codice sorgente disponibile sia per Mac OS X che per i PC (Linux, Windows Vista e XP). Viene concesso gratuitamente per l'utilizzo non commerciale. 44 La Risonanza Magnetica Non Convenzionale Dopo aver convertito in formato nii.gz i dati acquisiti nel formato standard .dicom, deve essere effettuata l'estrazione cerebrale e la rimozione del cranio tramite l'applicazione Bet. I dati di diffusione vengono, quindi, corretti per la presenza di "correnti parassite" e di artefatti di movimento per effettuare una registrazione lineare ad un'immagine di riferimento pesata non in diffusione per 12 gradi libertà 73. Le direzioni dei gradienti di diffusione vengono riorientate secondo i risultati delle correzioni delle "correnti parassite" 74. I tensori di diffusione per ogni voxel sono adattati secondo un algoritmo incluso nel "Toolbox di diffusione del FMRIB (FDT)" di FSL (v. 4.0, www.fmrib.ox.ac.uk/fsl75). Fig. 11. FSL è un insieme di applicazioni per l'analisi di neuroimmagini di RM strutturale, funzionale e in diffusione. A questo punto è possibile correlare i dati, per esempio di FA e di diffusività media (MD) con i test neuropsicologi utilizzando vari metodi, di cui uno dei più affidabili è il metodo Tract-Based Spatial Statistics o TBSS76. Questo metodo riduce la comparsa di possibili errori dovuti al disallineamento delle immagini. 45 La Risonanza Magnetica Non Convenzionale E', infatti, obbiettivo dei neuroscienziati utilizzare immagini di diffusione tramite metodiche di analisi statistica per voxel. Tale metodo permette di localizzare modificazioni cerebrali correlate a processi di sviluppo o di degenerazione. Tuttavia, un’analisi ottimale è invariabilmente compromessa dall’uso degli algoritmi standard di registratura. Fino a pochi anni fa, non era stata data alcuna soluzione soddisfacente al problema di come allineare le immagini di diffusione di diversi soggetti in maniera tale da permettere un’analisi statistica per singoli voxel. Oggi il metodo TBSS cerca di risolvere questo problema tramite un’attenta registratura non lineare e la proiezione in una rappresentazione di tratti che non varia con l’allineamento (mean FA skeleton). In questa maniera TBSS ha migliorato la sensibilità, l’oggettività e l’interpretabilità dell’analisi di RM in diffusione di più soggetti. I dati di FA di tutti i soggetti devono essere allineati in uno spazio comune derivato da immagini di FA di 58 soggetti sani, utilizzando un applicazione di registratura non lineare del FMRIB nota come FNIRT 77 (Fig. 12). 46 La Risonanza Magnetica Non Convenzionale Fig. 12. La registratura e la sommazione di molteplici esposizioni della stessa scena migliorano il rapporto segnale/rumore, consentendo così di vedere oggetti o condizioni invisibili oppure quasi inapparenti. Questa applicazione utilizza una rappresentazione b-spline della registrazione del campo di ripiegatura o warp-field 78 . I cervelli umani normali, infatti, variano molto in dimensione e forma e le loro immagini di risonanza devono necessariamente subire un processo di normalizzazione spaziale, cioè di deformazione, in modo che un'area anatomica presentata dalla scansione del cervello del soggetto corrisponda alla localizzazione corrispondente nella scansione di un altro soggetto. Nell'elaborazione informatica delle immagini neurologiche, la normalizzazione spaziale è un passo dell'elaborazione digitale delle immagini, più 47 La Risonanza Magnetica Non Convenzionale specificamente un metodo di registratura delle immagini. Esistono due passi inerenti al processo di normalizzazione spaziale: la stima del warp-field l'applicazione del warp-field con ricampionamento La stima del warp-field (o campo di ripiegatura) può essere eseguita in una modalità di RM e può essere applicata ad un'altra modalità di imaging se le due immagini sono state coregistrate. La normalizzazione spaziale utilizza tipicamente un modello di trasformazione non rigida tridimensionale, o "campo di ripiegatura" per la procedura di "warping" nell'analisi delle immagini di una scansione cerebrale rispetto a un template di riferimento. Il warp-field può essere parametrizzato da funzioni base come il coseno e i polinomi. Esiste un certo numero di programmi che implementa sia la stima che l'applicazione di un campo "warp". E' stata, quindi, realizzata un'immagine con media FA e limitata ad un valore di FA pari a 0.2, che deriva da un"'immagine modello medio" di FA che rappresenta i centri di tutti i tratti comuni al nostro campione. I dati di FA di ogni soggetto sono stati allineati e poi proiettati su questo modello e i risultati ottenuti sono stati introdotti in un modello statistico multivoxel dei vari soggetti. L'inferenza statistica basata su un modello standard lineare è stata eseguita utilizzando un'analisi basata su permutazioni (5000 permutazioni) secondo un modello già presente in FSL. 48 79 , La Risonanza Magnetica Non Convenzionale L'analisi statistica è stata effettuata secondo una soglia predefinita (t = 2.3) e corretta per comparazioni multiple (spaziali) all'interno di un insieme di permutazioni comprese tra un'ipotesi nulla e un valore massimo per ogni permutazione (P < 0.05). Analisi postprocessamento di immagini di RM strutturale Le immagini di RM strutturale forniscono dettagli particolareggiati dell’anatomia cerebrale. La RM strutturale è diventata ormai un sussidio importante per la gestione clinica dei pazienti neurologici e viene sempre più utilizzata nell’ambito degli studi clinici per valutare la risposta terapeutica. Per esempio, la RM strutturale è attualmente utilizzata come misura di endpoint secondario nei trial clinici che vedono coinvolti pazienti affetti da SM, perché permette di quantificare in maniera rapida e riproducibile le lesioni tipiche della malattia80. Inoltre, anche nel campo dell’invecchiamento, la RM strutturale sta divenendo uno strumento sempre più importante per caratterizzare le modificazioni corticali associate all’invecchiamento fisiologico, come ben sottolineato da Raz81. Nel campo delle demenze, solo da pochi anni, le ricerche cliniche hanno iniziato a considerare il ruolo di alcuni parametri di RM strutturale, ma sono state prese primariamente in considerazione solo valutazioni generali dell’atrofia globale cerebrale82 83 84 e le misure manuali dell’ippocampo85 86. Inoltre, l’applicazione della RM strutturale alla ricerca e agli studi clinici è stata limitata dal fatto che non era possibile ricavare informazioni da specifiche 49 La Risonanza Magnetica Non Convenzionale regioni di interesse (RI) anatomico. Quando poi, sono stati sviluppati metodi di quantificazione automatica di determinate RI, solo raramente queste metodiche sono state utilizzate negli studi clinici87. Ciò è derivato dal fatto di non sapere quali RI andare a considerare e dalla difficile collocazione anatomica delle RI che variavano di dimensioni e collocazioni a seconda dell’operatore. Così, per anni, alcuni di questi metodi si sono focalizzati su una singola RI, come l’ippocampo88 89 , il giro del cingolo90 o alcune RI sottocorticali91, poiché non esisteva il modo di valutare, per esempio, tutte le aree della corteccia cerebrale, dato che sarebbe stato fondamentale nella valutazione di una patologia diffusa come la MA. Lo sviluppo di procedure semiautomatiche per la quantificazione delle RI corticali è stato ancora più complesso a causa della sostanziale variabilità interindividuale degli spetti topografici della corteccia92 93. Gli sforzi iniziali per misurare RI corticali tramite RM richiedevano un totale coinvolgimento dell’operatore94 95. Metodiche più recenti e più automatiche hanno impiegato una varietà di approcci ai sistemi di indagine dei dati corticali, inclusi gli approcci basati su modelli, in cui si stabilisce una corrispondenza tra un atlante di riferimento e le neuroimmagini di un soggetto in esame96 97 o approcci basati sull’estrazione dei solchi corticali98 o ancora su tecniche basate sui grafici che rappresentano i solchi come vertici di un grafico99 100. Solo dieci anni fa, però, si è giunti ad una svolta. 50 La Risonanza Magnetica Non Convenzionale Nel 1999 un gruppo di lavoro guidato da Fishl, Sereno e Dale ha realizzato dei sofisticati studi algoritmici probabilistici, recentemente pubblicati 101, che sono stati applicati a due diversi sistemi di definizione delle RI corticali65 102. Da questi studi algoritmici è nato FreeSurfer103 ((http://surfer.nmr.mgh.harvard.edu/), un programma sviluppato presso i laboratori dell’Athinoula A. Martinos Center per Biomedical Imaging del Massachusett General Hospital, con il supporto dei CorTechs Labs, Inc, La Jolla, CA. e la collaborazione con il Mental Illness and Neuroscience Discovery (MIND) Institute, parte del National Alliance for Medical Image Computing (NA-MIC) fondato dai National Institutes of Health attraverso il NIH Roadmap for Medical Research e con il National Center for Research Resources del NINDS. In accordo con gli studi di Fischl et al.104, Dale et al.74, e Fischl e Dale105, la ricostruzione tridimensionale della superficie corticale viene effettuata sulla base delle immagini pesate in T1 magnetization-prepared rapid gradient echo (MPRAGE) di RM. Il programma, infatti, permette di misurare lo spessore corticale dalle immagini di RM, usando una ricostruzione automatica della superficie tramite procedure di allineamento e trasformazione ad alta risoluzione. Il processo consiste nella segmentazione della sostanza bianca cerebrale, nella delimitazione del confine tra sostanza bianca e grigia e nella correzione semiautomatica dei difetti topologici risultanti dall'analisi del software. Questi risultati consentono di analizzare la superficie delle aree di sostanza bianca, grigia e la superficie piale con precisione submillimetrica. 51 La Risonanza Magnetica Non Convenzionale La metodica utilizza informazioni di intensità e continuità derivanti dal processo di deformazione della superficie con interpolazione delle aree di superficie in cui l'immagine è ambigua. Lo spessore corticale viene analizzato mediante una griglia con 1 mm di spazio tra i due emisferi. Lo spessore corticale è, infatti, definito come la più breve distanza tra i modelli di superficie piale, di sostanza bianca e di grigia76 con possibilità di stimare anche differenze submillimetriche. Le misure di spessore corticale vengono mappate sull'immagine tridimensionale ottenuta dalla ricostruzione dell'encefalo di ogni soggetto: in questo modo è possibile visualizzare i dati inerenti l'intera superficie corticale. Tutte le immagini vengono comparate con una superficie di riferimento usando una tecnica di averaging ad alta risoluzione basata sulla superficie. Le RI ricavate da un modello standardizzato di encefalo vengono mappate sulle immagini relative al soggetto di interesse usando una procedura morfologica ad alta dimensione sferica per individuare le regioni omologhe in diversi soggetti. Infine, il volume e lo spessore medio corticale della sostanza grigia è analizzato in ciascuna RI. Lo spessore corticale è, quindi, approssimato nell'ordine di 1 mm di grandezza per ridurre l'effetto derivante da variazioni locali. Ciò permette di avere informazioni sullo spessore corticale che fino a poco tempo fa era possibile ottenere solo all’esame autoptico. Oltre ai dati di spessore, il programma fornisce informazioni di volume e superficie delle stesse RI. FreeSurfer è un programma di mappatura cerebrale e di misurazione in vivo dello spessore corticale che include dei tool per la ricostruzione di modelli 52 La Risonanza Magnetica Non Convenzionale topologicamente corretti e geometricamente accurati della superficie grigia, bianca e piale a partire dai dati di RM strutturale per misurare lo spessore corticale e le aree di superficie anche nelle circonvoluzioni. Il programma include la possibilità di valutare automaticamente 34 regioni corticali e le regioni non corticali. Anche FreeSurfer utilizza FSL. L’attivazione funzionale si ottiene usando sia FreeSurfer Functional Analysis Stream (FS-FAST) sia applicazioni di FSL che permettono di creare ricostruzioni cerebrali per insuflazione, sfericizzazione o appiattimento della superficie. FreeSurfer utilizza anche il toolkit di MNI MINC, VXL, Tcl/Tk/Tix/BLT e Qt, già inclusi nel pacchetto. Differenti programmi di elaborazione immagini, come Caret e 3D Slicer, possono, poi, importare dati ottenuti con FreeSurfer. I tool di FreeSurfer permettono di trattare due tipi di dati: di volume (volumi dei voxel); di superficie (poligoni che compongono una superficie). Usando FreeSurfer è possibile: eseguire ricostruzioni delle superfici; generare segmentazioni delle strutture sottocorticali; correggere errori riscontrati durante la generazione dei dati di volume e superficie. 53 La Risonanza Magnetica Non Convenzionale FreeSurfer può essere installato gratuitamente da Internet su sistemi operativi MacOS o Linux. Il supporto tecnico viene fornito in rete da un equipe di tecnici alla comunità di fruitori tramite la FreeSurfer mailing list. In questa sezione, si cercherà di fornire brevemente, delle informazioni sul programma. Il comando chiave dei processi è noto come recon-all che, nel suo primo processo, autorecon1, trasforma le immagini di RM encefalo di un singolo soggetto dal formato grezzo (generalmente .hdr .dicom) in immagini dal formato facilmente utilizzabile (.mgz) per l’analisi morfometrica e funzionale con il pacchetto FsFast. Nel caso si possiedano multiple acquisizioni di un singolo soggetto, FreeSurfer è in grado di creare un’immagine media in cui la rappresentazione sarà necessariamente più accurata. In questo processo, la prima scansione viene considerata dal programma come modello su cui le immagini successive vengono registrate. Viene applicato anche un filtro di correzione degli artefatti da movimento. Alla fine si otterrà un’immagine di Fig. 13. La rimozione del cranio, uno dei primi processi attuati da FreeSurfer. media delle varie scansioni in formato .mgz. Il volume dell’immagine viene conformato automaticamente al volume standard di 2563 in cui ogni voxel rappresenta un’area pari ad 1 mm3. 54 La Risonanza Magnetica Non Convenzionale Recon-all utilizza un tool di FreeSurfer detto mri_motion_correct.fsl, che lavora in maniera molto simile a FLIRT, un programma del toolset di FSL. Le fasi di processamento del volume consistono nella correzione Fig. 14. La finestra con i comandi di modiofica e visualizzazione di Tkmedit e Tksurfer. degli artefatti di movimento, nella correzione dell’intensità dell’immagine e nella normalizzazione, cioè la trasformazione in uno spazio Talairach. Per correggere l’intensità il volume T1 subisce una modificazione che elimina il cranio (Fig. 13) ed i rumori di fondo, generando il brainmask volume, privo della teca cranica e conformato ad un’immagine di riferimento. Tkmedit and Tksurfer (Fig. 14) costituiscono i comandi di visualizzazione Fig. 15 Segmentazioni cerebrali attuate con FreeSurfer. grafica e di modifica dei dati e sono inclusi nel pacchetto di FreeSurfer. È già in fase di realizzazione un nuovo sistema di comandi di visualizzazione grafica, Scuba, che rimpiazzerà Tkmedit e Tksurfer, una volta completato. Generato il brainmask, si procede con l’autorecon2, la seconda fase, che include l’imponente lavoro di segmentazione delle superfici cerebrali (Fig. 15). 55 La Risonanza Magnetica Non Convenzionale Purtroppo il processo di ricostruzione non è infallibile: è, quindi, necessario controllare sempre il processo di segmentazione ad ogni fase ed eventualmente correggerlo manualmente. Il processo di segmentazione può fallire per molte ragioni, ma principalmente per bassa qualità di scansione o differente anatomia interindividuale. La correzione viene effettuata utilizzando i tool di modifica di Tkmedit. In particolare Tkmedit è in grado di creare un’interfaccia per visualizzare e modificare i voxels presenti nelle singole slices bidimensionali delle scansioni di risonanza. Oltre alla segmentazione, il programma è in grado anche di parcellare i volumi corticali e sottocorticali (Fig. 16) in RI standard, sviluppate dal Center for Morphometric Analysis. Nel pacchetto sono inclusi molti sistemi che permettono di valutare, come già detto, lo spessore corticale e consentono anche altri tipi di analisi, inclusa la retinotopia. L’ultimo processo, autorecon3, sostanzialmente essenziale ai quantificazione dell’analisi fini e è della per la Fig. 16. Parcellazioni cerebrali attuate con FreeSurfer. visualizzazione tridimensionale completa del lavoro con Tksurfer. Per la misurazione dello spessore corticale regionale il programma suddivide l’encefalo in 34 regioni corticali, attribuibili a 5 lobi cerebrali, che ricordano le aree di K. Brodmann del 1909 106. 56 La Risonanza Magnetica Non Convenzionale Le aree cerebrali sono state recentemente descritte da Desikan et al.57 e vengono elencate di seguito: a) Lobo frontale 1 - Circonvoluzione frontale superiore 2 – Porzione anteriore della circonvoluzione frontale media 3 – Porzione posteriore della circonvoluzione frontale media 4 – Porzione triangolare della circonvoluzione frontale inferiore 5 - Porzione opercolare della circonvoluzione frontale inferiore 6 – Porzione orbitale della circonvoluzione frontale inferiore 7 - Porzione mediale della corteccia orbitofrontale 8 - Porzione laterale della corteccia orbitofrontale 9 - Polo frontale. 10 - Giro precentrale o prerolandico 11 - Lobulo paracentrale b) Lobo temporale Lobo temporale mediale 12 - Corteccia entorinale 13 - Circonvoluzione paraippocampica 14 - Polo temporale 15 - Giro fusiforme Lobo temporale laterale 16 - Giro temporale superiore 17 - Giro temporale medio 57 La Risonanza Magnetica Non Convenzionale 18 - Giro temporale inferiore 19 - Corteccia temporale trasversa 20 - Porzione posteriore del solco temporale superiore c) Lobo parietale 21 - Giro postcentrale o postrolandico 22 - Giro sopramarginale 23 - Corteccia parietale superiore 24 - Corteccia parietale inferiore 25 - Precuneo d) Lobo occipitale 26 - Circonvoluzione linguale 27 - Corteccia pericalcarina 28 - Cuneo 29 - Corteccia occipitale laterale e) Corteccia del Cingolo Porzione antero-rostrale Porzione antero-caudale Porzione posteriore Istmo Corpo calloso 58 La Risonanza Magnetica Non Convenzionale Per una rappresentazione grafica delle mappe, si può osservare la figura 17. Fig. 17. Rappresentazioni corticali piale (a sinistra) e “gonfiata” (a destra) delle RI in un emisfero. Le immagini nella riga in alto illustrano la proiezione laterale dell’emisfero, mentre quelle nella riga in basso quella mediale. L’asterisco bianco sulla superficie piale di sinistra indica la corteccia inclusa all’interno della scissura rolandica non visibile. Gli asterischi gialli sulla superficie “gonfiata” di destra indicano la stessa corteccia, visibile dopo il rigonfiamento. 59 La Risonanza Magnetica Non Convenzionale Analisi postprocessamento di immagini di spettroscopia in RM La MRS è una tecnica analitica strumentale che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame. Viene utilizzata per effettuare studi in vivo sull’uomo sin dagli anni Ottanta107 108 , ma solo recentemente, grazie al progresso tecnologico avvenuto nella costruzione di magneti superconduttivi (ad elevata intensità di campo ed elevata omogeneità su ampi volumi), al progresso elettronico e al progresso informatico (implementazione delle tecniche di trasformata di Fourier e di ricostruzione bidimensionale), ha acquisito un'enorme valenza scientifica e diagnostica. In sintesi, il principio su cui si basa la MRS è il seguente: quando nel corpo immerso nel campo magnetico B sono presenti delle molecole, i nuclei di queste, a causa del parziale schermaggio della nuvola elettronica che circonda le molecole stesse, non "vedono" il campo magnetico esterno B ma un campo effettivo B'=B(1-s) dove s è una costante che tiene conto dell'effetto di schermo della nuvola elettronica; da questo segue allora che, a seconda del tipo di molecola a cui appartengono, gli spin nucleari avranno frequenze di precessione diverse, e precisamente frequenze f'=1/(2) g B(1-s) dove g è il rapporto giromagnetico del nucleo in questione. Dallo spettro del segnale acquisito possono allora essere estratte informazioni riguardanti l'identità e la quantità delle diverse molecole presenti nel campione 60 La Risonanza Magnetica Non Convenzionale analizzando le posizioni e le ampiezze dei picchi presenti. Gli spostamenti di frequenza (chemical shift) sono tanto maggiori, e quindi danno luogo a picchi ben definiti, quanto più è maggiore B; da qui la necessità di avere campi magnetici elevati (≥1,5 Tesla). E’ utile, inoltre, sottolineare che per ottenere uno spettro di buona qualità è essenziale che l'uniformità spaziale del campo magnetico B sia elevata (dell'ordine di 0,1 ppm), per evitare che disuniformità del campo "mascherino" eventuali chemical shift. Il nucleo di fondamentale importanza nell'imaging RM, ma anche molto importante nella spettroscopia, è quello dell'idrogeno ed è quindi della spettroscopia basata su tale nucleo (1H-MRS) che ci occuperemo principalmente nel seguito. La 1H-MRS deve la sua diffusione anche al fatto che per il suo utilizzo non sono necessarie bobine dedicate e catene RF aggiuntive rispetto a quelle usate per il “normale” imaging RM, non gravando quindi con spese aggiuntive sul costo dell’hardware del sistema RM. Oltre alla spettroscopia single-voxel (SV-MRS: Single Voxel MRS) che consente di ottenere uno spettro da un volume di interesse specifico, molto diffusa è anche la tecnica dell'imaging spettroscopico, che attraverso l'introduzione di una opportuna codifica di fase, permette la suddivisione della regione da esaminare in più "voxel" (8x8, 16x16, 32x32, ecc...) e l'elaborazione contemporanea di uno spettro da ogni voxel, consentendo così di ottenere informazioni sulla distribuzione spaziale dei metaboliti, anche se a scapito di una minor qualità degli spettri e di tempi di acquisizione maggiori. 61 La Risonanza Magnetica Non Convenzionale In entrambe le tecniche sopra descritte, l'acquisizione spettroscopica viene in genere preceduta da una sessione di imaging che consente la localizzazione del voxel di interesse, e poi eseguita tramite opportune sequenze quali (per l'1H-MRS) la STEAM (STimulated Echo Acquisition Mode) o la PRESS (Point RESolved Spectroscopy). Nella spettroscopia protonica, buona parte delle applicazioni cliniche riguardano le patologie del cervello umano. Le principali ragioni sono da ricercarsi nel fatto che: nella maggior parte degli organi i lipidi non sono così nettamente separati dal tessuto di interesse come nel cervello e, pertanto, la soppressione del segnale dei lipidi, molto intenso, può diventare un problema; gli organi interni sono interessati dai movimenti cardiaci e respiratori che possono portare ad artefatti e a spettri di scarsa qualità; il cervello è meno facilmente accessibile per le biopsie che la maggior parte degli altri organi109. Spettro dell'idrogeno I principali metaboliti visualizzabili nello spettro dell’idrogeno acquisito a livello cerebrale sono: N-Acetyilaspartato (NAA), un composto localizzato all’interno dei neuroni e per questo motivo utilizzato come marker neuronale, utile per 62 La Risonanza Magnetica Non Convenzionale indagare sul numero e sulla funzionalità dei neuroni contenuti all’interno del voxel di interesse selezionato; Creatina (Cr), che comprende sia creatina che fosfocreatina e che fornisce informazioni sul metabolismo energetico del tessuto; Colina (Cho), comprendente principalmente fosfocolina e glicerofosforilcolina, e legata ai processi di costruzione e di degradazione delle membrane cellulari; myo-Inositolo (myo-Ins), utilizzato comunemente come marker della glia. In spettri patologici possono comparire anche le risonanze del Lattato (Lac), indice di una alterata glicolisi anaerobia, e quello degli acidi grassi, legato alla degradazione delle membrane cellulari. Numerosi studi hanno mostrato come la 1HMRS sia di estrema utilità nello studio di svariate patologie (tumori, sclerosi multipla, demenze etc.)110. In particolare, nello studio dei tumori, la MRS trova un suo importante spazio come supporto alla diagnosi (finding tipici : riduzione del NAA e notevole incremento della Cho) e nella distinzione tra tessuto normale, recidiva e necrosi. In ambito neurologico generale, la MRS mostra lo stato metabolico dei tessuti e i cambiamenti del metabolismo negli stati patologici e permette il monitoraggio della terapia e la ricerca di nuove vie metaboliche in vivo e nella ricerca biochimica. I parametri comunemente utilizzati in MRS (Fig. 18) sono: lo spettro, cioè la rappresentazione del segnale RM in funzione della "frequenza di risonanza"; 63 La Risonanza Magnetica Non Convenzionale i picchi ovvero la rappresentazione grafica del segnale emesso dai vari metaboliti; l'unità di misura in Parti per Milione (PPM) per poter confrontare spettri a c. magnetico diverso; la posizione, cioè la struttura chimica; l'intensità (area) cioè la concentrazione. Fig. 18. Parametri utilizzati in MRS (vedi testo). Le caratteristiche di acquisizione di risonanza prevedono sequenze a TE breve (10-30 msec), TE breve (130-140 msec) e TE lungo (150-276 msec). Successivamente è prevista un'analisi 64 qualitativa volta al semplice La Risonanza Magnetica Non Convenzionale riconoscimento visivo dei picchi e quantitativa o ratio, volta ad indagare i rapporti tra i vari metaboliti in esame. 65 IL NOSTRO STUDIO Disegno dello studio Questo studio è nato nel 2010 dalla collaborazione tra la Facoltà di Medicina e Psicologia della “Sapienza” Università di Roma – Azienda Ospedaliera Sant’Andrea, la Fondazione Biomedica Europea, l'Azienda Ospedaliera San Camillo - Forlanini e la Fondazione Santa Lucia. Per la realizzazione dello studio è stata fondamentale la supervisione dei colleghi del Neuroimaging Section della University of Szeged. Lo studio è stato suddiviso in varie fasi. Al momento dell’arruolamento, durante una visita neurologica, i pazienti sono stati sottoposti ad esame neurologico comprensivo di MMSE, successivamente sono stati sottoposti ad una valutazione neuropsicologica e, poi, ad un esame di RM dell’encefalo sia con sequenze convenzionali, senza somministrazione di contrasto, che con sequenze non convenzionali. Successivamente le sequenze di RM sono state analizzate con metodiche di postprocessamento e si è proceduto all’analisi statistica dei dati. Per questo studio tutte le neuroimmagini sono state analizzate presso la Fondazione Biomedica Europea di Roma. Tutti i partecipanti hanno firmato un consenso informato prima dell'inizio dello studio. Ad ogni soggetto è stato assegnato un numero progressivo identificativo in conformità con la legge sulla privacy. 66 Popolazione Abbiamo arruolato in serie continua 19 soggetti (9 maschi e 10 femmine, con età media di 74 ± 8 anni e con range tra i 52 ed i 86 anni) affetti da probabile MA. Per una visione globale delle caratteristiche del campione, si può osservare la tab. 1. I soggetti hanno fornito consenso informato alla partecipazione allo studio. Criteri di inclusione Pazienti affetti da probabile MA, secondo i criteri NINDS-ADRDA Età compresa tra 50 e i 90 anni Criteri di esclusione Presenza di gravi deficit neurosensoriali Scolarità inferiore a 3 anni Presenza di gravi patologie internistiche Scarsa compliance che non garantisca la completa adesione alle richieste del protocollo per tutta la durata dello studio Storia di abuso di sostanze Presenza di fattori che controindichino l'esecuzione di un esame di RM 67 Presenza di quadri neuroradiologici di importante sofferenza cerebrovascolare o di pregresse lesioni ischemiche/emorragiche Mancato consenso informato alla partecipazione allo studio Pazienti (n=19) Età (anni) 74±8 Sesso (maschi/femmine) 9/10 Livello di istruzione (anni) Punteggio al MMSE Mesi di malattia 9.5±5.6 20±6 43.1±7.7 Tab. 1. Caratteristiche demografiche e cliniche della nostra coorte. I dati sono espressi in media±deviazione standard, tranne che nei casi diversamente indicati 68 Metodi Le seguenti procedure sono state effettuate durante lo studio: visita neurologica valutazione neuropsicologica esame di RM dell’encefalo con metodiche non convenzionali analisi post-processamento di immagini analisi statistica 69 Visita neurologica Per il reclutamento in serie continua, tutti i pazienti giunti all’osservazione, dopo una vista neurologica, comprensiva di anamnesi ed esame obbiettivo neurologico, sono stati registrati progressivamente e valutati secondo i criteri di inclusione ed esclusione. I soggetti che hanno presentato i requisiti per l’arruolamento allo studio e hanno fornito il loro consenso informato sono stati sottoposti all’esame neuropsicologico e di RM encefalo. I loro i dati clinici sono stati raccolti su una cartella clinica informatizzata. 70 Valutazione Neuropsicologica La valutazione ha incluso test neuropsicologici molto dettagliati e standardizzati nella popolazione italiana. Oltre ad una valutazione cognitiva globale tramite il MMSE e più approfondita per mezzo del Milan Overoll Dementia Assessment (MODA)111, sono state indagate in maniera specifica diverse aree cognitive quali l'attenzione selettiva (test delle matrici attentive o Visual Search and Attention Test o VSAT112) e l'attenzione continua (trail making test o TMT113 A e B), la memoria a breve e a lungo termine uditivo-verbale (test di Lista di Rey o RAVLT114 nelle modalità immediata e differita e test della memoria di prosa115), la memoria immediata (Test Digit Span Avanti ed Indietro116), le abilità logico-deduttive (Test delle matrici di Raven117), il linguaggio (Test di fluenza fonemica e semantica118) e le capacità prassiche (test di aprassia costruttiva 59). I punteggi ottenuti sono stati normalizzati per età e scolarità. 71 Risonanza Magnetica Acquisizione ed archivio delle immagini di RM L’esame di RM è stato eseguito tramite un’apparecchiatura con intensità di campo magnetico di 1.5 Tesla. I parametri di scansione sono stati i seguenti: FOV: 250 mm Matrice di acquisizione: 256 x 256 Spessore di strato : 3 mm Distanza tra le immagini: 0 Modalità di acquisizione interlacciata Numero di sezioni: 44-48 Al fine di velocizzare l’acquisizione, si è utilizzato un FOV rettangolare con una lunghezza dell’asse della codifica di fase = ¾ FOV Per ridurre il tempo di acquisizione, la lunghezza del treno di echi (fast turbo factor) è stata ottimizzata. I tomogrammi sul piano assiale sono stati posizionati paralleli alla linea passante dal margine superiore della commessura anteriore e dal margine inferiore della commessura posteriore (linea CA-CP, o bicommissurale). Il volume di acquisizione si è esteso oltre la corteccia a coprire tutto l’encefalo. Le sezioni sono state acquisite perpendicolarmente al piano sagittale definito come il piano passante 72 lungo il seno sagittale superiore, la falce cerebrale, le strutture della linea mediana lungo la sutura fronto-nasale (nasion). Sono state effettuate le seguenti acquisizioni: 0. Localizer 1. Assiale T1 pesata 2. Assiale DP-T2-T2 (tripla echo) 3. Assiale DWI - DTI 4. Assiale 3D Magnetization prepared Fast Low Angle Shot (MP-RAGE) 5. Magnetic resonance spectroscopy 6. Acquisizione con tecnica Chemical Shift Imaging (CSI) SE con TE=30ms con soppressione del segnale dell’acqua in corrispondenza degli ippocampi e dei centri semiovali. Prima dell'inizio dello studio è stato effettuato un test di prova (dummy run) con un volontario sano. La copia elettronica degli esami di RM è stata archiviata presso la Fondazione Biomedica Europea di Roma. I dati informatici delle immagini di RM, in formato DICOM, sono stati trasferiti presso una work-station presente presso la stessa Fondazione. L'intero lavoro di post-processamento delle neuroimmagini, descritto nei prossimi paragrafi, è stato svolto presso la Fondazione Biomedica Europea, in collaborazione con il Neuroimaging Section della Neurológiai Klinika dell’Albert Szent-Györgyi Medical and Pharmaceutical Center Faculty of General Medicine della University of Szeged per quanto concerne le analisi delle immagini in 73 diffusione. E' stata utilizzata la stessa work-station precedentemente menzionata con un sistema operativo Linux Ubuntu (http://www.ubuntu.com/) per l'intero processo analitico. Analisi qualitativa delle immagini di RM L’analisi delle immagini è stata effettuata indipendentemente da operatori esperti, all’oscuro sia della storia clinica che dei risultati delle analisi quantitative. I risultati sono stati registrati su appositi moduli. Si sono valutate le seguenti caratteristiche: il “rumore” del segnale delle immagini su una scala a tre punti; gli artefatti da movimento su una scala a tre punti; altri artefatti, che sono stati descritti e quantificati su una scala a tre punti; la qualità dell’immagine su una scala a cinque punti Queste altre caratteristiche delle immagini sono state valutate separatamente per ogni esame di RM: la visibilità di lesioni iperintense in T2 su una scala a tre punti; la stima visiva del quadro radiologico dell’atrofia per entità e per sedi. Analisi post-processamento delle immagini in diffusione di RM Dopo aver convertito in formato nii.gz i dati acquisiti nel formato standard .dicom, è stata effettuata l'estrazione cerebrale e la rimozione del cranio tramite l'applicazione Bet. I dati di diffusione sono stati corretti per la presenza di "correnti 74 parassite" e di artefatti di movimento per effettuare una registrazione lineare ad un'immagine di riferimento pesata non in diffusione per 12 gradi libertà72. Le direzioni dei gradienti di diffusione sono state riorientate secondo i risultati delle correzioni delle "correnti parassite"73. I tensori di diffusione per ogni voxel sono stati adattati secondo un algoritmo incluso nel "Toolbox di diffusione del FMRIB (FDT)" di FSL. La FA e la MD sono state calcolate per tutto l'encefalo e correlate con i test neuropsicologi (fig.19). Abbiamo utilizzato il metodo Tract-Based Spatial Statistics o TBSS74 in maniera tale da ridurre la comparsa di possibili errori dovuti al disallineamento delle immagini. Fig. 19. Immagini ottenute grazie all'uso del metodo TBSS e visualizzate tramite FSL view. In questa fase è stata fondamentale la supervisione da parte del Neuroimaging Section della University of Szeged. 75 I dati di FA di tutti i soggetti sono stati allineati in uno spazio comune derivato da immagini di FA di 58 soggetti sani, utilizzando un applicazione di registratura non lineare del FMRIB nota come FNIRT 69. Questa applicazione, come sopra illustrato, utilizza una rappresentazione b-spline della registrazione del campo di ripiegatura o warp-field 119 (comando tbss_1_preproc *nii.gz). E' stata, quindi, realizzata un'immagine con media FA e limitata ad un valore di FA pari a 0.2, che deriva da un"'immagine modello medio" di FA che rappresenta i centri di tutti i tratti comuni al nostro campione (comando tbss_2_reg -T, poi comando tbss_3_postreg -S e, infine, comando tbss_4_prestats 0.2, con controllo visivo di ogni operazione tramite fslview). I dati di FA di ogni soggetto sono stati allineati e poi proiettati su questo modello e i risultati ottenuti sono stati introdotti in un modello statistico multivoxel dei vari soggetti (applicazione Glm). L'inferenza statistica basata su un modello standard lineare è stata eseguita utilizzando un'analisi basata su permutazioni (5000 permutazioni), secondo un modello già presente in FSL (comando randomise -i). L'analisi statistica è stata effettuata secondo una soglia predefinita (t = 2.3) e corretta per comparazioni multiple (spaziali) all'interno di un insieme di permutazioni comprese tra un'ipotesi nulla e un valore massimo per ogni permutazione (P < 0.05). 76 Analisi post-processamento delle immagini strutturali di RM La ricostruzione tridimensionale della superficie corticale è stata effettuata sulla base delle immagini MPRAGE usando il software FreeSurfer. La procedura, già descritta nel precedente capitolo, è consistita nella segmentazione della sostanza bianca cerebrale, nella delimitazione del confine tra sostanza bianca e grigia e nella correzione semi-automatica dei difetti topologici risultanti dall'analisi del software (Fig. 18). Questo risultato è stato poi utilizzato come punto di partenza per analizzare la superficie delle aree di sostanza bianca, grigia e la superficie piale con precisione sub millimetrica. Sono state ottenute anche le parcellazioni delle varie RI (Fig. 19). Per ogni soggetto, lo spessore corticale è stato Fig. 20. Segmentazione cerebrale attuata su un soggetto del nostro studio analizzato con una griglia con 1 mm di spazio tra i due emisferi. Le misure di spessore corticale sono state mappate sull'immagine tridimensionale ottenuta dalla ricostruzione dell'encefalo di ogni soggetto (Fig. 20). Tutte le immagini sono state comparate con una superficie di riferimento usando una tecnica di averaging ad alta risoluzione basata sulla superficie. Le Fig. 21. Parcellazione cerebrale attuata su un soggetto del nostro studio 77 RI ricavate da un cervello standard sono state mappate sulle immagini relative ad ogni partecipante, usando una procedura morfologica ad alta dimensione sferica per trovare le regioni omologhe nei vari soggetti. Infine, il volume e lo spessore medio corticale della sostanza grigia sono stati analizzati in ciascuna Fig. 22. Visualizzazione delle aree corticali cerebrali di un soggetto del nostro studio RI. Lo corticale spessore è stato, quindi, arrotondato nell'ordine di 1 mm di grandezza per ridurre l'effetto derivante da variazioni locali. Si sono, così, ottenute informazioni di volume, superficie e spessore corticale regionale dalla nostra coorte di pazienti. Analisi post-processamento delle immagini in spettroscopia di RM L'indagine di RM in spettroscopia è stata condotta per i lobi temporali, parietali e frontali. I metaboliti presi in considerazione sono stati l'N-acetilaspartato (NAA), la colina (Cho) e la creatina (Cr). 78 Fig. 23. Analisi di immagini in Spettroscopia. Analisi statistica I dati di DTI, come precedentemente descritto, avevano già parzialmente subito il processo di analisi statistica nel corso della loro analisi grazie al metodo TBSS. I dati clinici, neuropsicologici e di analisi post-processamento delle neuroimmagini sono stati sottoposti ad analisi statistica utilizzando SPSS 15.0 per Windows, versione 15.0.1 (SPSS Inc. 2006). E' stato utilizzato il modello di regressione lineare per stimare i coefficienti dei diversi parametri considerati nella determinazione del valore dei test cognitivi (se il coefficiente è positivo la relazione è diretta, se invece è negativo la relazione è inversa). E' stata, quindi, effettuata un'analisi di correlazione calcolando i coefficienti di correlazione di Spearman (rho). In questo studio sono stati calcolati i valori di rho per valutare la correlazione esistente tra: 79 le dimensioni di ogni scala neuropsicologica; le caratteristiche demografiche dei pazienti; i parametri ottenuti dalle indagini di RM non convenzionale. Per ciascuna correlazione è stata valutata la significatività statistica per p<0.05. Quando il valore di rho è compreso tra 0 e +1,00 significa che una variabile aumenta con l’aumentare dell’altra; quando rho è compreso tra 0 e –1,00 significa che una variabile aumenta col diminuire dell’altra: se rho = +/-1,00 significa che una variabile spiega completamente l’altra. Se rho = 0.00-0.40 la correlazione tra le variabili è scarsa; se rho = 0.40-0.60 è discreta; se rho = 0.60-0.80 è buona; se rho = 0.80-1.00 è forte. 80 Risultati Non abbiamo ottenuto alcuna correlazione statisticamente significativa tra i valori di MD e i punteggi di tutti i test neuropsicologici. Dall’analisi statistica è emersa, invece, una correlazione selettiva tra i valori di FA misurati nel corpo calloso e i punteggi ottenuti ai test MMSE, TMT-B, fluenza fonemica e RAVLT (in modalità differita) ed una correlazione tra i valori di FA delle regioni fronto-parieto-temporali destre ed il RAVLT (in modalità differita). Come già spiegato precedentemente, è stato direttamente possibile visualizzare i risultati statistici con l'interfaccia grafica fslview come osservabile nelle figure 24 (a, b, c, d). Abbiamo ottenuto questi risultati per il MMSE (Fig. 24 a). Fig. 24 (a). Correlazione tra punteggio del MMSE e dati di FA. La Tract-Based Spatial Statistic (TBSS) indica una riduzione dei valori di anisotropia frazionaria (FA) nel segmento postero-parietale di sinistra del corpo calloso nei pazienti affetti da MA. I valori medi di FA sono rappresentati in colore rosso. 81 Abbiamo ottenuto questi risultati per il TMT-B (Fig. 24 b). Fig. 24 (b). Correlazione tramite TBSS tra punteggio del TMT-B e dati di FA. La TractBased Spatial Statistic (TBSS) indica una riduzione dei valori di anisotropia frazionaria (FA) nel segmento postero-parietale di destra del corpo calloso nei pazienti affetti da MA. I valori medi di FA sono rappresentati in colore rosso. Sono emersi questi risultati per il test della fluenza fonemica (Fig. 24 c). Fig. 24 (c). Correlazione tramite TBSS tra punteggio del test della fluenza fonemica e dati di FA. La Tract-Based Spatial Statistic (TBSS) indica una riduzione dei valori di anisotropia frazionaria (FA) in tutte le porzioni del corpo calloso nei pazienti affetti da MA. I valori medi di FA sono rappresentati in colore rosso. 82 E, quindi, abbiamo osservato questi risultati per il RAVLT. Fig. 24 (e). Correlazione tramite TBSS tra punteggio del RAVLT (in modalità differita) e dati di FA. La Tract-Based Spatial Statistic (TBSS) indica una riduzione dei valori di anisotropia frazionaria (FA) nel segmento antero-frontale bilaterale, postero-frontale destro del corpo calloso nei pazienti affetti da MA. I valori medi di FA sono rappresentati in colore rosso. Terminata l'analisi dei dati di diffusione, abbiamo effettuato un'analisi dei dati ottenuti tramite la valutazione degli spessori e dei volumi regionali cerebrali utilizzando FreeSurfer ed i punteggi ottenuti dai soggetti affetti da MA ai test neuropsicologici. Per effettuare tale correlazione abbiamo utilizzato il coefficiente di correlazione di Spearman. Abbiamo osservato varie correlazioni significative tra il RAVLT (in modalità immediata e differita) ed il test delle matrici progressive di Raven e lo spessore di varie aree corticali sinistre. 83 Tuttavia, il dato più rilevante è stato la diretta correlazione tra il punteggio ottenuto al MMSE e lo spessore della corteccia entorinale destra, lo spessore dell'area fusiforme e lo spessore del polo temporale infero-superiore (P>0.01) come visibile in figura 25. Fig. 25.Il MMSE appariva direttamente correlato con lo spessore della corteccia entorinale destra, con l'area fusiforme e con il polo temporale infero-superiore (P>0.01).Il codice di colori per il valori di P è espresso da una scala logaritmica da 1 a 5. I colori più caldi rappresentano le regioni in cui la severità del disturbo cognitivo correlava maggiormente con la riduzione di spessore corticale. Sempre utilizzando il coefficiente di correlazione di Spearman abbiamo ottenuto delle correlazioni tra il rapporto NAA/Cr e il rapporto Cho/Cr valutati nei lobi temporali, parietali e frontali e i punteggi ottenuti ai test neuropsicologici dai soggetti affetti da MA. 84 E' emerso, in particolare, che esiste un'elevata e significativa correlazione tra alcuni test neuropsicologici e il rapporto NAA/Cr della sostanza bianca frontale destra e della sostanza grigia frontale sinistra. Inoltre, la stessa analisi ha dimostrato una correlazione significativa tra i test neuropsicologici e il rapporto Cho/Cr della sostanza grigia mesiale occipitale (Tab. 2). Tab. 2. L'analisi di correlazione tramite i coefficienti di correlazione di Spearman (Rho) del rapporto NAA/Cr ha mostrato che esiste un'elevata e significativa correlazione tra alcuni test neuropsicologici e la sostanza bianca frontale destra e la sostanza grigia frontale sinistra. Inoltre, la stessa analisi ha dimostrato una correlazione significativa tra i test neuropsicologici e il rapporto Cho/Cr della sostanza grigia mesiale occipitale. Il risultato più importante è stato, infine, ottenuto utilizzando l'analisi multimodale d'immagine: abbiamo, infatti, osservato, in questa maniera, una relazione combinata tra valore di FA del corpo calloso, il suo volume ed il punteggio del MMSE. 85 Discussione Nel nostro studio abbiamo osservato interessanti evidenze. Innanzitutto, le microstrutture della sostanza bianca valutate con il metodo TBSS appaiono significativamente alterate nei paziente affetti da MA. In particolare, il dato più rilevante appare la degenerazione delle fibre del corpo calloso nella patogenesi dei disturbi cognitivi dei soggetti affetti da MA, come dimostrato dalla relazione tra i test neuropsicologici alterati e i ridotti valori di FA del corpo calloso dei paziente affetti da MA. Questo dato viene integrato anche dall'evidenza anatomica di riduzione di volume globale del corpo calloso valutata tramite FreeSurfer. Tale "danno" appare intimamente correlato soprattutto ai disturbi mnesici, verbali e attentivi presenti nella MA. Il corpo calloso rappresenta la più ampia via di connessione di fibre di sostanza bianca nel nostro cervello e la conoscenza dei suoi cambiamenti correlati all'età e alle patologie è uno degli aspetti chiave per comprendere il suo ruolo nei processi cognitivi. A partire dal 2005120 sono stati effettuati molti studi trattografia volti ad analizzare il ruolo del corpo calloso nei processi cognitivi. Nel 2010, proprio utilizzando tecniche trattografiche, un gruppo di ricercatori canadesi ha realizzato un "atlante probabilistico" in cui sono virtualmente ricostruiti 86 ben definiti segmenti del corpo calloso sulla base della loro area corticale di connessione121. Su queste basi, il corpo calloso viene ormai comunemente distinto in sette distinti segmenti sulla base delle aree corticali bersaglio: orbito-frontale (OF), anterofrontale (AF), supero-frontale (SF), supero-parietale (SP), postero-parietale (PP), temporale (Temp) ed occipitale (Occ). Fig. 26. Segmentazione del corpo calloso tramite trattografia. Corpus callosum parcellation by tractography. Il corpo calloso viene convenzionalmente diviso in sette segmenti separati: orbito-frontale (OF), antero- frontale (AF), supero-frontale (SF), supero-parietale (SP), postero-parietale (PP), temporale (Temp) e occipitale (Occ). La segmentazione del corpo calloso in sette porzioni, invece della classica divisione anatomo-patologica in quattro porzioni (rostro, genio, corpo e splenio) permette una più dettagliata localizzazione delle alterazioni dovute ai processi patologici. 87 Sulla base di queste recenti evidenze, noi abbiamo evidenziato una correlazione tra le prestazioni attentive e cognitive globali e la degenerazione del segmento postero-parietale del corpo calloso e una correlazione tra la degenerazione globale di questa struttura e le funzioni fonemiche. Da un punto di vista fisiopatologico questi risultati confermano che differenti pattern di alterazione della sostanza bianca del corpo calloso siano associati alla MA122. Ciò supporta l’ipotesi che le “disconnessioni cerebrali” svolgano un ruolo fondamentale nella patogenesi della MA, contribuendo ai disturbi cognitivi soprattutto mnesici ed attentivi nella fase iniziale-moderata della MA (ricordiamo, a tal proposito, che il nostro campione aveva un punteggio medio di MMSE di circa 20). Al dato ultrastrutturale ottenuto con i dati di RM in diffusione occorre aggiungere la correlazione anatomica tra il volume del corpo calloso ed il punteggio del MMSE. Tuttavia dal nostro studio sono emersi anche altri interessanti dati anatomici, analizzando la relazione tra la gravità dei disturbi cognitivi ed il volume e lo spessore corticale di alcune strutture cerebrali primariamente interessate dal processo neurodegenerativo della MA. Il dato più rilevante è la correlazione tra il test MMSE e lo spessore della corteccia entorinale, del giro fusiforme e del polo temporale. Il dato dimostra, infatti, da un lato, l'importanza del ruolo del MMSE come test di screening globale dei 88 disturbi cognitivi, considerata la sua importante correlazione con l'atrofia delle strutture primariamente interessate dalla MA e, dall'altro lato, il valore diagnostico della valutazione dello spessore corticale nella MA, proprio in considerazione della sua correlazione con il punteggio del MMSE. Oltre a questi risultati relativi al MMSE, lo studio ha mostrato che le funzioni cognitive che più correlano con il processo atrofico appaiono essere la memoria e le abilità logico-deduttive. Al danno anatomico delle strutture corticali temporo-mesiali, occorre aggiungere l'evidenza di danno di natura metabolica individuato dai nostri studi spettroscopici. Il rapporto NAA/Cr nella sostanza bianca frontale destra correla con i test indicanti i disturbi di memoria e linguaggio e anche con il MMSE, indice di declino cognitivo globale. Lo stesso rapporto nella corteccia frontale sinistra è apparso correlato con i disturbi della memoria di prosa e con il declino cognitivo globale, mentre il rapporto Cho/Cr nella sostanza occipitale mesiale destra correlava con i disturbi attentivi. Come noto, nella MA è presente proprio una diminuzione caratteristica e consistente di NAA parieto-occipitale123 e proprio il rapporto NAA/Cr ratio nella corteccia del lobo occipitale sinistro ha una sensibilita del 78% e una specificita del 69% nel predire lo sviluppo di demenza in soggetti affetti da MCI124. Occorre aggiungere che le misurazioni ottenuti dall’elaborazione dei dati di RM appaiono in linea con quanto evidenziato anche dagli studi neuropatologici nella diagnosi differenziale tra soggetti sani e soggetti affetti da MA125 126 e contribuiscono 89 in maniera sostanziale al miglioramento della diagnosi, rispetto all’uso dei soli test neuropsicologici. Prima di giungere alle conclusioni occorre sottolineare il fatto che questo studio presenta alcuni limiti ovvero la ridotta dimensione del campione di popolazione in esame, l’assenza di un campione di controllo e, ovviamente, l’assenza di una conferma neuropatologica della diagnosi. Dobbiamo tuttavia sottolineare che si tratta di risultati preliminari ottenuti su un piccolo gruppo di pazienti. Ulteriori studi saranno necessari per confermare i nostri dati. Possiamo, pertanto, concludere che, analizzando insieme dati di diffusione con i dati strutturali, il nostro studio ha permesso di evidenziare una correlazione in vivo tra parametri anatomici e ultrastrutturali e parametri cognitivi. La combinazione di metodiche differenti di risonanza magnetica non convenzionale che valutino la morfometria, la spettroscopia la MD e la FA fornisce un nuovo utile approccio per la valutazione anatomica, metabolica ed ultrastrutturale dei processi neurodegenerativi alla base della MA. 90 Bibliografia BIBLIOGRAFIA 1 Gaarder J. L’enigma del solitario (1996). Baldini e Castoldi Editore. 2 Levi Montalcini R. La Galassia Mente (1999). TEA Edizioni. 3 Kandel E. I misteri della mente. A cura di Bruno Levy ed Emile Servan-Schreiber, (1998) Le Scienze. 4 Mesulam MM. From sensation to cognition. Brain (1998) 121, 1013–1052. 5 Broca P. Perte de la parole, ramollissement chronique et destruction partielle du lobe antérieur gauche. Bulletin de la Société d"Anthropologie (1861) 2, 235–38. 6 Bloch F, Hansen WW, Packard ME. Nuclear induction. Phys Rev (1946) 69, 127. 7 Purcell EM, Torrey HC, Pound RV. Resonance absorption by nuclear magnetic moments in a solid. Phys Rev (1946) 69, 37-38. 8 Damadian R, Goldsmith M, Minkoff L. NMR in cancer. XVI. FONAR image of the live human body. Physiol Chem Phys (1977) 9, 97–100. 9 Bagnato F, Frank JA. The role of nonconventional magnetic resonance imaging techniques in demyelinating disorders. Curr Neurol Neurosci Rep (2003) 3, 238-45. 10 Bomboi G, Ikonomidou VN, Pellegrini S, Stern SK, Gallo A, Auh S, Evangelou IE, Agarwal J, Pellicano C, Ohayon JM, Cantor FK, Ehrmantraut M, McFarland HF, Kane RL, XCI Bibliografia Bagnato F. Quality and quantity of diffuse and focal white matter disease and cognitive disability of patients with multiple sclerosis. J Neuroimaging (2011) 21, 57-63. 11 Szabó N, Kincses ZT, Párdutz A, Tajti J, Szok D, Tuka B, Király A, Babos M, Vörös E, Bomboi G, Orzi F, Vécsei L. White matter microstructural alterations in migraine: a diffusion-weighted MRI study. Pain (2012) 153, 651-6. 12 Alzheimer A. Über einen eigenartigen schweren Erkrankungsprozeß der Hirnrinde. Neurologisches Centralblatt (1906) 23, 1129–36. 13 Folstein MF, Folstein SE, McHugh PR. "Mini-mental state". A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res (1975) 12, 189-98. 14 Jorm AF, Korten AE, Henderson AS. The prevalence of Dementia: a Quantitative Integration of the Literature, Acta Psychiatrica Scandinavica (1987) 76, 465-479. 15 Amaducci L. Italian Longitudinal Study on Ageing: incidence study of dementia. Neuroepidemiology (1992) Suppl. 1, 119-122. 16 Pinessi L, Rainero I, Asteggiano G et al. Primary Dementias: Epidemiological and Sociomediacal Aspects. The Italian Journal of Neurological Sciences (1984) V, 51-55. 17 Frisanco R. The quality of psychiatric care since the reform law: the “Censis”survey. Int J Soc Psychiatry (1989) 35, 81-89. 18 Teunisse S, Derix MMA, Van Crevel H et al. Assessing the severity of dementia. Patient and caregiver. Arch Neurol (1991) 48, 274-277. 19 Games D, Adams D, Alessandrini R, Barbour R, Berthelette P, Blackwell C, Carr T, Clemens J, Donaldson T, Gillespie F, et al. Alzheimer-type neuropathology in transgenic mice overexpressing V717F beta-amyloid precursor protein. Nature (1995) 373, 523-7. XCII Bibliografia 20 Terry RD, Masliah E, Salmon DP, Butters N, De Teresa R, Hill R, Hansen LA, Katman R. Physical basis of cognitive alterations in Alzheimer’s disease: synapse loss in the major correlate of cognitive impairment. Ann Neurol (1991) 30, 572-80. 21 Braak H, Braak E. Staging of Alzheimer’s disease-related neurofibrillary changes. Neurobiol Aging (1995) 16, 271–8. 22 Masliah E, Ellisman M, Carragher B, Mallory M, Young S, Hansen L, DeTeresa R, Terry RD. Three-dimensional analysis of the relationship between synaptic pathology and neuropil threads in Alzheimer disease. J Neuropathol Exp Neurol (1992) 51, 404-14. 23 Joachim CL, Selkoe DJ. The seminal role of beta-amyloid in the pathogenesis of Alzheimer disease. Alz Dis Assoc Dis (1992) 6, 7-34. 24 Selkoe DJ. Cell biology of the beta-amyloid precursor protein and the genetics of Alzheimer’s disease. Cold Spring Harb Symp Quant Biol (1996) 61, 587-96. 25 Hardy JA, Higgins GA. Alzheimer's disease: the amyloid cascade hypothesis. Science. (1992) 256, 184-5. 26 Atwood CS, Huang X, Moir RD, Tanzi RE, Bush AI. Role of free radicals and metal ions in the pathogenesis of Alzheimer’s disease. Met Ions Biol Syst (1999) 36, 309-64. 27 Cuajungco MP, Faget KY, Huang X, Tanzi RE, Bush AI. Metal chelation as a potential therapy for Alzheimer’s disease. Ann NY Acad Sci (2000) 920, 292-304. 28 Tanzi RE, Bertram L. Twenty years of the Alzheimer’s disease amyloid hypothesis: a genetic perspective. Cell (2005) 120, 545-55. 29 Perry G, Sayre LM, Atwood CS, Castellani RJ, Cash AD, Rottkamp CA, Smith MA. The role of iron and copper in the aetiology of neurodegenerative disorders: therapeutic implications. CNS Drugs (2002) 16, 339-52. XCIII Bibliografia 30 Rottkamp CA, Nunomura A, Raina AK, Sayre LM, Perry G, Smith MA. Oxidative stress, antioxidants, and Alzheimer disease. Alz Dis Assoc Dis (2000) 1, 62-6. 31 Smith MA, Nunomura A, Zhu X, Takeda A, Perry G. Metabolic, metallic, and mitotic sources of oxidative stress in Alzheimer disease. Antioxid Redox Signal (2000) 2, 413-20. 32 Forte G, Bocca B, Senofonte O, Petrucci F, Brusa L, Stanzione P, Zannino S, Violante N, Alimonti A, Sancesario G. Trace and major elements in whole blood, serum, cerebrospinal fluid and urine of patients with Parkinson’s disease. J Neural Transm (2004) 111, 1031-40. 33 Bush AI. Copper, zinc, and the metallobiology of Alzheimer disease. Alz Dis Assoc Dis (2003) 17, 147-50. 34 Giubilei F, Marchione F, Forte G, Bocca B, Sepe-Monti M, Bomboi G, Alimonti A. Trace and major elements in whole blood and serum of patients with Alzheimer’s disease. Neurobiol Aging (2004) 25, 353. 35 Christen Y. Oxidative stress and Alzheimer disease. Am J Clin Nutr (2000) 71, 621-9. 36 Behl C. Amyloid beta-protein toxicity and oxidative stress in Alzheimer’s disease. Cell Tissue Res (1997) 290, 471-80. 37 Hartman D. Free radical theory of aging: Alzheimer’s disease pathogenesis. Age (1995) 18, 97-119. 38 Lovell MA, Robertson JD, Teesdale WJ, Campbell JL, Markesbery WR. Copper, iron and zinc in Alzheimer’s disease senile plaques. J Neurol Sci (1998) 158, 47-52. 39 Huang X, Moir RD, Tanzi RE, Bush AI, Rogers JT. Redoxactive metals, oxidative stress, and Alzheimer’s disease pathology. Ann NY Acad Sci (2004) 1012, 153-63. 40 Bush AI. The metallobiology of Alzheimer’s disease. Trends Neurosci (2003) 26, 207-14. XCIV Bibliografia 41 Bush AI, Pettingell WH, Multhaup G, d Paradis M, Vonsattel JP, Gusella JF, Beyreuther K, Masters CL, Tanzi RE. Rapid induction of Alzheimer A beta amyloid formation by zinc. Science (1994) 265, 1464-7. 42 Lee JY, Cole TB, Palmiter RD, Suh SW, Koh JY. Contribution by synaptic zinc to the gender-disparate plaque formation in human Swedish mutant APP transgenic mice. Proc Natl Acad Sci USA (2002) 99, 7705-10. 43 Hartter DE, Barnea A. Evidence for release of copper in the brain: depolarization-induced release of newly taken-up 67copper. Synapse (1988) 2, 412-5. 44 Atwood CS, Moir RD, Huang X, Scarpa RC, Bacarra NM, Romano DM, Hartshorn MA, Tanzi RE, Bush AI. Dramatic aggregation of Alzheimer ABeta by Cu(II) is induced by conditions representing physiological acidosis. J Biol Chem (1998) 273, 12817-26. 45 Bush AI, Multhaup G, Moir RD, Williamson TG, Small DH, Rumble B, Pollwein P, Beyreuther K, Masters CL. A novel zinc (II) binding site modulates the function of the beta A4 amyloid protein precursor of Alzheimer’s disease. J Biol Chem (1993) 268, 16109-12. 46 Simons A, Ruppert T, Schmidt C, Schlicksupp A, Pipkorn R, Reed J, Masters CL, White AR, Cappai R, Beyreuther K, Bayer TA, Multhaup G. Evidence for a copper-binding superfamily of the amyloid precursor protein. Biochemistry (2002) 41, 9310-20. 47 White AR, Reyes R, Mercer JF, Camakaris J, Zheng H, Bush AI, Multhaup G, Beyreuther K, Masters CL, Cappai R. Copper levels are increased in the cerebral cortex and liver of APP and APLP2 knockout mice. Brain Res (1999) 842, 439-44. 48 Bomboi G, Marchione F, Sepe-Monti M, De Carolis A, Bianchi V, Medda E, Pino A, Bocca B, Forte G, D’Ippolito C, Giubilei F. Correlation between metal ions and clinical findings in subjects affected by Alzheimer's disease. Ann Ist Super Sanita (2005) 41, 205212. XCV Bibliografia 49 Bomboi G, Prosperini L, Guidoni SV, Sepe-Monti M, De-Carolis A, Bocca B, Pino A, Alimonti A, Giubilei F. Cognitive performance and clinical status of patients with Alzheimr’s disease can be influenced by haematic concentration of metals. 19th World Congress of Neurology (2009). 50 Dubois B, Feldman HH, Jacova C, Dekosky ST, Barberger-Gateau P, Cummings J, Delacourte A, Galasko D, Gauthier S, Jicha G, Meguro K, O'brien J, Pasquier F, Robert P, Rossor M, Salloway S, Stern Y, Visser PJ, Scheltens P. Research criteria for the diagnosis of Alzheimer's disease: revising the NINCDS—ADRDA criteria. The Lancet Neurology (2007) 6, 734–746. 51 McKhann G, Drachman D, Folstein M, Katzman R, Price D, Stadlan EM. Clinical diagnosis of Alzheimer’s disease: Report of the NINCDS-ADRDA Work Group under the auspices of Department of Health Services Task Force on Alzheimer’s disease. Neurology (1984) 34, 359-364. 52 American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders Text Revision, 4th edn. Washington, D. C.: American Psychiatric Association (1994). 53 Ricci M, Guidoni SV, Sepe-Monti M, Bomboi G, Antonini G, Blundo C, Giubilei F. Clinical findings, functional abilities and caregiver di stress in the early stage of dementia with Lewy bodies (DLB) and Alzheimer’s disease (AD). Arch Gerontol Geriatr. (2009) 49, e101-4. 54 Bomboi G, Castello L, Cosentino F, Giubilei F, Orzi F, and Volpe M. Alzheimer’s disease and endothelial dysfunction. Neurological Sciences (2010) 31, 1-8. 55 Petersen RC, Stevens JC, Ganguli M, Tangalos EG, Cummings JL, DeKosky ST. Practice parameter: early detection of dementia: mild cognitive impairment (an evidence-based XCVI Bibliografia review). Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology (2001) 56, 1133-42. 56 Winblad B, Palmer K, Kivipelto M, Jelic V, Fratiglioni L, et al. Mild cognitive impairment—Beyond controversies, towards a consensus: Report of the International Working Group on Mild Cognitive Impairment. J Intern Med (2004) 256, 240–246. 57 Petersen RC. Mild cognitive impairment as a diagnostic entity J Intern Med (2004) 256, 183-94. 58 Zarei M, Patenaude B, Damoiseaux J, Morgese C, Smith S, Matthews PM, Barkhof F, Rombouts S, Sanz-Arigita E, Jenkinson M. Combining shape and connectivity analysis: an MRI study of thalamic degeneration in Alzheimer’s disease. Neuroimage (2009) 49, 1-8. 59 Pievani M, Agosta F, Pagani E, Canu E, Sala S, Absinta M, Geroldi C, Ganzala R, Frisoni GB, Filippi M. Assessment of white matter tract damage in mild cognitive impairment and Alzheimer’s disease. Hum Brain Mapp (2010) 31, 1862-75. 60 Du AT, Schuff N, Kramer JH, Rosen HJ, Gorno-Tempini ML, Rankin K, Miller BL, Weiner MW. Different regional patterns of cortical thinning in Alzheimer's disease and frontotemporal dementia. Brain (2007) 130, 1159-66. 61 Dale AM, Fischl B, Sereno MI. Cortical surface-based analysis: I. Segmentation and surface reconstruction. NeuroImage (1999) 9, 179– 194. 62 Fischl B, Sereno MI, Dale AM. Cortical surface-based analysis. II: inflation, flattening, and a surface-based coordinate system. Neuro-Image (1999) 9, 195–207. 63 Fischl B, Dale AM. Measuring the thickness of the human cerebral cortex from magnetic resonance images. Proc. Natl. Acad. Sci. U. S. A. (2000) 97, 11050–11055. 64 Carr HY, Purcell EM. Effect of diffusion on free precession in nuclear magnetic resonance experiments. Phys rev (1954) 94, 630-638. XCVII Bibliografia 65 Taylor DG, Bushell MC. The spatial mapping of translation diffusion coefficients by the NMR imaging technique. Phys Med Biol (1985) 30, 345-349. 66 Beaulieu C, Allen PS. Water diffusion in the giant axon of the squid: implications for diffusion-weighted MRI of the nervous system. Magn Reson Med (1994) 32, 579-583. 67 Damion RA, Vennart W, Summers IR, Ellis RE. Water diffusion coefficient measurements in the finger by magnetic resonance imaging. Magn Reson Imaging (1994) 12, 873-879. 68 Torrey HC: Bloch equation with diffusion terms. Phys Rev (1956) 104, 563-565. 69 Merboldt KD, Hanicke W, Frahm J. Self-diffusion NMR imaging using stimulated echoes. J Magn Resons (1985) 64, 479-486. 70 Stejskal EO, Tanner JE. Spin diffusion measurements: spin echoes in the presence of time- dependent field gradient. Journal of Chemical Physics (1965) 42, 288-292. 71 Campanile AP, Terlizzi R, Miscio G. Studio di diffusione con tomografo RM ad alto campo: indagine sperimentale nelle malattie degenerative. (2011) Università di Foggia. 72 Pierpaoli C, Basser PJ. Toward a quantitative assessment of diffusion anisotropy. Magn Reson Med (1996) 6, 893-906. 73 Jenkinson M, Smith S. A global optimisation method for robust affine registration of brain images. Med Image Anal (2001) 5, 143–56. 74 Leemans A, Jones DK. The B-matrix must be rotated when correcting for subject motion in DTI data. Magn Reson Med (2009) 61, 1336–49. 75 Smith SM, Jenkinson M, Woolrich MW, Beckmann CF, Behrens TE, Johansen-Berg H, Bannister PR, De Luca M, Drobnjak I, Flitney DE, Niazy RK, Saunders J, Vickers J, Zhang Y, De Stefano N, Brady JM, Matthews PM. Advances in functional and structural MR image analysis and implementation as FSL. Neuroimage (2004) 23, 208–19. XCVIII Bibliografia 76 Smith SM, Jenkinson M, Johansen-Berg H, Rueckert D, Nichols TE, Mackay CE, Watkins KE, Ciccarelli O, Cader MZ, Matthews PM, Behrens TE. Tract-based spatial statistics: voxelwise analysis of multi-subject diffusion data. Neuroimage (2006) 31,1487–505. 77 Andersson JLR, Jenkinson M, Smith S. Non-linear optimisation: FMRIB technical report. (2007) Oxford, UK: FMRIB. 78 Rueckert D, Sonoda LI, Hayes C, Hill DL, Leach MO, Hawkes DJ. Nonrigid registration using free-form deformations: application to breast MR images. IEEE Trans Med Imaging (1999) 18,712–21. 79 Nichols TE, Holmes AP. Nonparametric permutation tests for functional neuroimaging: a primer with examples. Hum Brain Mapp (2002) 15,1–25. 80 Bakshi R, Minagar A, Jaisani Z, Wolinsky JS. Imaging of multiple sclerosis: role in neurotherapeutics. NeuroRx (2005) 2, 277–303. 81 Raz N. The aging brain: Structural changes and their implications for cognitive aging. In: Dixon, R., Ba¨ckman, L., Nilsson, L.-G. (Eds.), New Frontiers in Cognitive Aging. Oxford (2004) Univ. Press, pp. 115–134. 82 Freeborough, PA, Fox NC. MR image texture analysis applied to the diagnosis and tracking of Alzheimer’s disease. IEEE Trans. Med Imaging (1998) 17, 475–479. 83 Fox NC, Warrington EK, Rossor MN. Serial magnetic resonance imaging of cerebral atrophy in preclinical Alzheimer’s disease Lancet (1999) 353, 2125. 84 Fox NC, Crum WR, Scahill RI, Stevens JM, Janssen JC, Rossor MN. Imaging of onset and progression of Alzheimer’s disease with voxel-compression mapping of serial magnetic resonance images. Lancet (2001) 358, 201–205. XCIX Bibliografia 85 Jack CRJ, Theodore WH, Cook M, McCarthy G. MRI-based hippocampal volumetrics: data acquisition, normal ranges, and optimal protocol. Magn Reson Imaging (1995) 13, 1057–1064. 86 Jack CRJ, Petersen RC, Xu YC, Waring SC, O’Brien PC, Tangalos EG, Smith GE, Ivnik RJ, Kokmen E. Medial temporal atrophy on MRI in normal aging and very mild Alzheimer’s disease. Neurology (1997) 49, 786–794. 87 Desikan RS, Ségonne F, Fischl B, Quinn BT, Dickerson BC, Blacker D, Buckner RL, Dale AM, Maguire RP, Hyman BT, Albert MS, Killiany RJ. An automated labeling system for subdividing the human cerebral cortex on MRI scans into gyral based regions of interest. Neuroimage (2006) 31, 968-80. 88 Hsu YY, Schuff N, Du AT, Mark K, Zhu X, Hardin D, Weiner MW. Comparison of automated and manual MRI volumetry of hippocampus in normal aging and dementia. J Magn Reson Imaging (2002) 16, 305–310. 89 Csernansky, JG, Wang L, Swank J, Miller JP, Gado M, McKeel D, Miller MI, Morris JC. Preclinical detection of Alzheimer’s disease: hippocampal shape and volume predict dementia onset in the elderly. NeuroImage (2005) 25, 783– 792. 90 Miller MI, Hosakere M, Barker AR, Priebe CE, Lee N, Ratnanather JT, Wang L, Gado M., Morris JC, Csernansky JG. Labeled cortical mantle distance maps of the cingulate quantify differences between dementia of the Alzheimer type and healthy aging. Proc. Natl. Acad. Sci. U. S. A. (2003) 100, 15172–15177. 91 Fischl B, Salat DH, Busa E, Albert M, Dieterich M, Haselgrove C, van der Kouwe A, Killiany R, Kennedy D, Klaveness S, Montillo A, Makris N, Rosen B, Dale AM. Whole brain segmentation: automated labeling of neuroanatomical structures in the human brain. Neuron (2002) 33, 341– 355. C Bibliografia 92 Zilles K, Armstrong E, Schleicher A, Kretschmann HJ. The human pattern of gyrification in the cerebral cortex. Anat. Embryol, Berl (1988) 179, 173– 179. 93 Kennedy DN, Lange N, Makris N, Bates J, Meyer J, Caviness VSJ. Gyri of the human neocortex: an MRI-based analysis of volume and variance. Cereb Cortex (1998) 8, 372– 384. 94 Damasio H, Damasio AR. Lesion Analysis in Neuropsychology. Oxford Univ (1989) Press, Oxford. 95 Rademacher J, Galaburda AM, Kennedy DN, Filipek PA, Caviness VSJ. Human cerebral cortex: localization, parcellation and morphometry with magnetic resonance imaging. J. Cogn Neurosci (1992) 4, 352–374. 96 Thompson PM, Schwartz C, Toga AW. High-resolution random mesh algorithms for creating a probabilistic 3D surface atlas of the human brain. NeuroImage (1996) 3, 19–34. 97 Sandor S, Leahy R. Surface-based labeling of cortical anatomy using a deformable atlas. IEEE Trans. Med. Imaging (1997) 16, 41–54. 98 Lohmann G. Extracting line representations of sulcal and gyral patterns in MR images of the human brain. IEEE Trans Med Imaging (1998) 17, 1040–1048. 99 Mangin JF, Frouin V, Bloch J, Regis J, Lopez-Krahe J. From 3-D magnetic resonance images to structured representations of the cortex topography using topology preserving deformations. J Math Imaging Vis (1995) 5, 297–318. 100 Le Goualher G, Procyk E, Collins DL, Venugopal R, Barillot C, Evans AC. Automated extraction and variability analysis of sulcal neuroanatomy. IEEE Trans Med Imaging (1999) 18, 206–217. 101 Fischl B, van der Kouwe A, Destrieux C, Halgren E, Segonne F, Salat DH, Busa E, Seidman LJ, Goldstein J, Kennedy D, Caviness V, Makris N, Rosen B, Dale AM. Automatically parcellating the human cerebral cortex. Cereb Cortex (2004) 14, 11–22. CI Bibliografia 102 Destrieux C, Halgren E, Dale AM, Fischl B, Sereno MI. Variability of the human brain studied on the flattened cortical surface. Abstr Soc Neurosci (1998) 24, 1164. 103 Dale AM, Fischl B, Sereno MI. Cortical surface-based analysis: I. Segmentation and surface reconstruction. NeuroImage (1999) 9, 179– 194. 104 Fischl B, Sereno MI, Dale AM. Cortical surface-based analysis. II: inflation, flattening, and a surface-based coordinate system. Neuro-Image (1999) 9, 195–207. 105 Fischl B, Dale AM. Measuring the thickness of the human cerebral cortex from magnetic resonance images. Proc. Natl. Acad. Sci. U. S. A. (2000) 97, 11050–11055. 106 von Economo C, Koskinas GN. Die Cytoarchitektonik der Hirnrinde des erwachsenen Menschen. Vienna and Berlin (1925) Julius Springer. 107 Ross BD, Radda GK, Gadian DG, Rocker G, Esiri M, Falconer-Smith J. Examination of a case of suspected McArdle's syndrome by 31P nuclear magnetic resonance. N Eng J Med (1981) 304, 1338-1342. 108 Bottomley PA, Hart HR, Edelstein WA, Schenck JF, Smith LS, Leue WM, Mueller OM, Redington RW. NMR imaging/spectroscopy system to study both anatomy and metabolism. Lancet (1983) 2, 273–274. 109 Presciutti O. Tecniche di Spettroscopia ed imaging funzionale mediante RM. SC di Fisica Sanitaria, Azienda Ospedaliera di Perugia. (2003) AIFM. 110 Pirzkall A, Tracy R, Mcknight TR, Graves E, et al. MR-Spectroscopy guided target delineation for high-grade gliomas. Int J Radiation Oncology Biol Phys (2001) 50, 915–928. 111 M Brazzelli, E Capitani, S Della Sala, H Spinnler, and M Zuffi. A neuropsychological instrument adding to the description of patients with suspected cortical dementia: the Milan overall dementia assessment. J Neurol Neurosurg Psychiatry (1994) 57, 1510–1517. 112 Trenerry MR. Visual Search and Attention Test (1990). CII Bibliografia 113 Reitan R. M. Validity of the Trail Making test as an indicator of organic brain damage. Percept. Mot Skills (1958) 8, 271-276. 114 115 Rey A. Rey Auditory Verbal Learning Test (RAVLT) (1958). Spinnler H, Tognoni G. Standardizzazione e taratura italiana di testneuropsicologici. Italian Journal of Neuroscience (1987) 6, 8. 116 Wechsler DA, Digit Span Backward from WAIS–R (1981). 117 Raven J, Raven JC, Court JH. Raven Manual, Section 1(General overview) and Section 2 (Coloured Progressive Matrices) (1998) Oxford Psychologist Press, Oxford, UK. 118 Borkowski J G, Benton A L, Spreen O. Word fluency and brain damage. Neuropsychologia (1967) 5, 135-140. 119 Rueckert D, Sonoda LI, Hayes C, Hill DL, Leach MO, Hawkes DJ. Nonrigid registration using free-form deformations: application to breast MR images. IEEE Trans Med Imaging (1999) 18, 712–21. 120 Huang H, Zhang J, Jiang H, Wakana S, Poetscher L, Miller MI, van Zijl PC, Hillis AE, Wytik R, Mori S. DTI tractography based parcellation of white matter: application to the mid-sagittal morphology of corpus callosum. Neuroimage (2005) 26, 195-205. 121 Lebel C, Caverhill-Godkewitsch S, Beaulieu C. Age-related regional variations of the corpus callosum identified by diffusion tensor tractography. Neuroimage (2010) 52: 20–31. 122 Preti MG, Baglio F, Laganà MM, Griffanti L, Nemni R, Clerici M, Bozzali M, Baselli G. Assessing corpus callosum changes in Alzheimer's disease: comparison between tract-based spatial statistics and atlas-based tractography. Assessing corpus callosum changes in Alzheimer's disease: comparison between tract-based spatial statistics and atlas-based tractography. PLoS One (2012) 7, e35856 CIII Bibliografia 123 Jones RS, Waldman AD. 1HMRS evaluation of metabolism in Alzheimer's disease and vascular dementia. Neurol Res (2004) 26, 48895. 124 Fayed N, Davila J et al. Utility of different mr modalities in mild cognitive impairment and its use as a predictor of conversion to probable dementia. Acad Radiol (2008) 15, 108998. 125 Braak H, Braak E. Staging of Alzheimer’s disease-related neurofibrillary changes. Neurobiol Aging (1995) 16, 271–8. 126 Lerch JP, Pruessner JC, Zijdenbos A, Hampel H, Teipel SJ, Evans AC. Focal decline of cortical thickness in Alzheimer’s disease identified by Computational neuroanatomy. Cereb Cortex (2005) 15, 995–1001. CIV
Scaricare