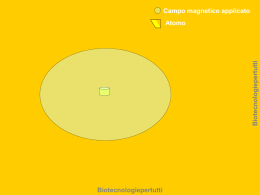
ATOMO DI IDROGENO Le coordinate e l’equazione di Schrödinger Non è necessario dilungarsi sull’importanza dell’atomo idrogenoide come base per lo studio della struttura di tutti gli atomi. Il sistema è illustrato in figura 1 con la scelta delle coordinate rilevanti. Il sistema rassomiglia evidentemente al sistema di due particelle studiato nel caso del rotatore rigido. Riportiamo di seguito alcune relazioni e definizioni utili che abbiamo già visto nel caso del rotatore rigido. mM = massa ridotta m+M ma = M b −→ def inizione centro di massa m a b= M M b a= m m+M m+M r =a+b= a= b M m M µ a= r= r m+M m m µ b= r= r m+M M µ= (1) Per descrivere il sistema sono necessarie 6 coordinate indipendenti e cioè 3 coordinate cartesiane per il nucleo e 3 per l’elettrone (ci sono 6 gradi di libertà). Come al solito sarebbe importante trattare separatamente ognuna delle coordinate in modo da trasformare un’equazione di Schrödinger in 6 incognite in 6 equazioni ad una sola variabile. Questa separazione non sarebbe realizzabile se si usassero le sei coordinate cartesiane nelle quali l’Hamiltoniano classico avrebbe la forma · 2 · 2 · 2 · 2 · 2 · 2 1 1 H = M (X 1 + Y 1 + Z 1 ) + m(X 2 + Y 2 + Z 2 ) + V (r) 2 2 o in termini dei momenti H= 1 1 2 (Px2 + Py2 + Pz2 ) + (p + p2y + p2z ) + V (r) 2M 2m x 1 (2) (3) e l’operatore Hamiltoniano assumerebbe la forma ~2 H =− 2M −p ∂2 ∂2 ∂2 + + ∂X12 ∂Y12 ∂Z12 e2 ~2 − 2m ∂2 ∂2 ∂2 + + ∂X22 ∂Y22 ∂Z22 − (4) (X2 − X1 )2 + (Y2 − Y1 )2 + (Z1 − Z2 )2 L’impossibilità di separare le variabili dipende dalla forma dell’energia potenziale di interazione nucleo elettrone che mescola irrimediabilmente le coordinate del nucleo e dell’elettrone. È allora di fondamentale importanza scegliere il sistema di coordinate più opportuno per realizzare la separazione delle variabili. Notiamo a questo proposito che possiamo immaginare di scomporre il moto globale dell’atomo di idrogeno in uno spostamento globale rispetto ad assi fissi nel laboratorio: ciò corrisponde a traslazioni globali lungo le direzioni X, Y e Z (equivalenti a tre gradi di libertà). Oltre a questo possiamo pensare ad una rotazione dell’elettrone intorno al nucleo (che può essere caratterizzata da due coordinate angolari come longitudine e latitudine) ed infine dobbiamo pensare ad un moto di variazione della distanza nucleo-elettrone. Scegliamo allora un sistema di coordinate cartesiane fisso nel laboratorio X, Y , Z ed un sistema di coordinate sferiche fisso nel baricentro dell’atomo come indicato in figura 1. Allora invece di usare le sei coordinate cartesiane, tre per il nucleo e tre per l’elettrone, usiamo le tre coordinate cartesiane del centro di massa X, Y , Z e le tre coordinate polari r, θ, ϕ. Le relazioni tra le coordinate cartesiane e le nuove coordinate sono µ r sin θ cos ϕ M µ Y1 = Y − y1 = Y − r sin θ sin ϕ M µ Z1 = Z − z1 = Z − r cos θ M (5) µ X2 = X + x2 = X + r sin θ cos ϕ m µ Y2 = Y + y2 = Y + r sin θ sin ϕ m µ Z2 = Z + z2 = Z + r cos θ m che sono essenzialmente le stesse relazioni già viste per i momenti angolari e per il rotatore rigido, con la sola importante differenza che ora dobbiamo X1 = X − x1 = X − 2 tenere conto che anche r può variare. Usando questo nuovo sistema di coordinate l’Hamiltoniano del sistema può essere riscritto come · 2 · 2 · 2 1 H = (m + M )(X + Y + Z )+ 2 1 1 ·2 ·2 ·2 ·2 ·2 ·2 + M (x1 + y 1 + z 1 ) + m(x2 + y 2 + z 2 ) + V (r) 2 2 (6) dove è stata sfruttata la relazione che definisce il centro di massa ed annulla i termini in croce. Il primo termine descrive l’energia cinetica di traslazione di un corpo di massa uguale alla massa totale dell’atomo e quindi serve a definire la posizione assoluta dell’atomo nello spazio: questo termine contiene coordinate (del centro di massa) che non compaiono nell’energia potenziale e quindi questo è un movimento che si può separare dal moto interno (rotazione dell’elettrone intorno al nucleo e movimento di allontanamento o avvicinamenmto dell’elettrone al nucleo). Poiché il nostro interesse è sulla struttura interna dell’atomo possiamo lasciar perdere il primo termine (la traslazione dell’atomo potrà sempre essere trattata come nel problema della particella libera). L’energia cinetica allora assume la forma 1 1 ·2 ·2 ·2 ·2 ·2 ·2 T = M (x1 + y 1 + z 1 ) + m(x2 + y 2 + z 2 ) (7) 2 2 e ha la stessa espressione che abbiamo visto per le due particelle del rotatore rigido. Come visto in quel caso possiamo trasformare questa espressione nell’operatore relativo e trasformare poi l’operatore nelle coordinate polari ottenendo ~2 2 ∇ +V = 2µ (8) ~2 1 ∂ 2 ∂ 1 ∂ ∂ 1 ∂2 =− r + sin θ + + V (r) 2µ r2 ∂r ∂r r2 sin θ ∂θ ∂θ r2 sin2 θ ∂θ2 H =− Ricordando la forma già vista dell’operatore per il momento angolare 1 ∂ ∂ 1 ∂2 2 2 L = −~ sin θ + sin θ ∂θ ∂θ sin2 θ ∂θ2 possiamo scrivere 3 (9) 1 2 1 ∂ 2∂ r + L 2 r ∂r ∂r 2µr2 e quindi otteniamo l’Hamiltoniano nella forma ∇2 = (10) ~2 1 ∂ 2 ∂ 1 2 r + L + V (r) 2 2 2µr r ∂r ∂r 2µr2 (11) H=− È evidente che l’Hamiltoniano commuta con il momento angolare e con le sue componenti e quindi H, L2 ed Lz avranno autofunzioni comuni e quindi possiamo scrivere le nostre equazioni agli autovalori come Hψ = Eψ (12) L2 ψ = ~2 l(l + 1)ψ (13) Lz ψ = ~mψ (14) e cerchiamo soluzioni della forma ψ(r, θ, ϕ) = R(r)Ylm (θ, ϕ) (15) con l = 0, 1, 2, 3, ... e m = −l, −l + 1, ..., 0, ..., l − 1, l Abbiamo quindi chiaramente sfruttato il fatto che abbiamo già risolto il problema del momento angolare e ne conosciamo autovalori ed autofunzioni. Possiamo ora riscrivere l’equazione di Schrödinger come − ~2 ∂ 2 ψ 2 ∂ψ 1 2 ( 2 + )+( L + V (r))ψ = Eψ 2µ ∂r r ∂r 2µr2 ~2 ∂ 2 ψ 2 ∂ψ 1 2 − ( 2 + )+( ~ l(l + 1) + V (r))ψ = Eψ 2µ ∂r r ∂r 2µr2 Introducendo ora la forma scelta per la funzione d’onda otteniamo ~2 ∂ 2 R 2 ∂R 1 2 ( 2 + )+( ~ l(l + 1) + V (r))R = ER 2µ ∂r r ∂r 2µr2 che possiamo riscrivere − ∂ 2 R 2 ∂R 1 2µ Ze2 2µ + + (− l(l + 1) + )R = − 2 ER 2 2 2 ∂r r ∂r r ~ r ~ 4 (16) (17) (18) (19) A questo punto vediamo quindi che cercando una separazione tra variabili angolari θ, ϕ ed r la equazione si separa in due parti, e cioè la parte angolare che è identica, a parte una costante, a quella che abbiamo risolto per il momento angolare ed in una equazione per la parte radiale R(r). Resta allora da risolvere solo questa ultima parte. Definiamo la costante a= ~2 µe2 (20) e riscriviamo l’equazione da risolvere come 2Z l(l + 1) 2E ∂ 2 R 2 ∂R + + ( − + 2 )R = 0 (21) ∂r2 r ∂r ar r2 ae Come al solito vogliamo procedere in modo da cercare di ridurre questa equazione ad una equazione differenziale nota e già risolta. Possiamo preliminarmente cercare una soluzione asintotica per r tendente ad infinito. In questo limite i termini con r al denominatore diventano trascurabili ed abbiamo ∂2R 2E ' − 2R 2 ∂r ae (22) Se E ≥ 0 abbiamo soluzioni √ 2 R(r) ' e±i 2E/ae ·r (23) in cui tutti i valori di E positivi sono possibili: abbiamo un continuo di stati non legati. Queste soluzioni sono del tutto simili a quelle viste per la particella libera: infatti sostituendo l’espressione di a si ottiene i R = e± ~ √ 2mE·r (24) che è identica con la soluzione per la particella libera. Queste soluzioni del continuo corrispondono a stati in cui l’elettrone si dissocia dal nucleo e si muove liberamente senza sentire più l’attrazione coulombiana. Ora dobbiamo cercare soluzioni per E < 0. Per questo definiamo la costante r 2E c= − 2 (25) ae avremo per 5 r→∞ R ' e−cr (26) mentre la soluzione generale sarà della forma R(r) = K(r)e−cr (27) Sostituendo nella equazione per R si otterrà una equazione per K(r) la cui soluzione richiede numerosi passaggi algebrici che omettiamo. Al termine si ottiene per l’energia µe4 Z 2 (28) 2~2 n2 e per la parte radiale della autofunzione una soluzione con una parte polinomiale En = − l − Zr na Rnl (r) = r e n−l−1 X bj r j (29) j Le autofunzioni per l’atomo di idrogeno saranno infine, includendo la parte angolare che già conosciamo, 1 ψnlm (r, θ, ϕ) = Rnl (r)Ylm (θ, ϕ) = Rnl (r)Slm (θ) √ eimϕ 2π (30) con n = 1, 2, 3, 4, ..., l = 0, 1, 2, 3, ..., (n − 1) e m = −l, ..., +l. Le soluzioni: autovalori ed autofunzioni Le soluzioni per l’energia sono riportate in Figura 2 e 3 nelle quali è mostrato anche l’andamento della energia potenziale in funzione di r. Nella figura 2 è mostrato anche, in tratteggio, il continuo delle energie positive. L’energia dipende esclusivamente dal numero quantico principale n, mentre le autofunzioni dipendono anche dai numeri quantici angolare l e magnetico m. Pertanto gli stati come rappresentati nelle due figure sono degeneri. La degenerazione dei livelli, per ogni valore di n, si trova subito tenendo conto dei valori possibili dei numeri quantici riportati sopra e sarà 6 n−1 X (2l + 1) = 2 0 n−1 X l+ n−1 X 0 1 = n(n − 1) + n = n2 (31) 0 e quindi specificamente n degenerazione 1 2 3 4 . . 1 4 9 16 . . Abbiamo già detto qualcosa della forma della parte angolare delle autofunzioni (armoniche sferiche). Esaminiamo ora piú in dettaglio le autofunzioni iniziando dalla parte radiale. R diventa zero per r = 0 e per r = ∞. Inoltre la funzione potrà avere altri nodi corrispondenti agli zeri del polinomio di grado n − l − 1 che compare nella autofunzione radiale: il numero di nodi addizionali sarà n l n. nodi addizionali 1 2 2 3 3 3 0 0 1 0 1 2 0 1 0 2 1 0 Esaminiamo le funzioni più in dettaglio. Stato fondamentale: n =1 l= 0 m = 0 La parte radiale sarà Z R10 (r) = b0 e− a r (32) nella quale bisogna calcolare il valore della costante b0 : ciò può essere fatto in base alla condizione di normalizzazione ottenendo Z Z (33) R10 (r) = 2( )3/2 e− a r a Ricordando poi che per la parte angolare Y00 = √14π si ottiene per la funzione totale Z 1 Z Ψ100 = √ ( )3/2 e− a r π a 7 (34) Per l’energia otteniamo Z 2 e2 Z 2 µe4 = − (35) 2~2 2a e nel caso dell’idrogeno con Z = 1 si ottiene E0 = 13.598 eV (1 eV = 1.6022 1012 erg) mentre per la costante a si ottiene il valore E0 = − a= ~2 = 0.5292 =⇒ raggio di Bohr µe2 (36) Procedendo in modo analogo possiamo trovare la forma esplicita di tutte le altre autofunzioni. Ad esempio per n = 2 avremo le funzioni Ψ200 , Ψ210 , Ψ211 , Ψ21−1 . Nel caso della prima avremo per la parte radiale Z R200 (r) = (b0 + b1 ) e− 2a r (37) ed in questo caso dobbiamo determinare i valori di due costanti: per fare questo sfruttiamo le due relazioni di normalizzazione ed ortogonalità < R10 | R20 >= 0 (38) < R20 | R20 >= 1 (39) Nelle tabelle che seguono sono riportate esplicitamente le espressioni per la parte radiale e per le autofunzioni totali dell’atomo idrogenoide. Nella figura 4 gli andamenti delle funzioni radiali sono rappresentati graficamente in una direzione: si vede come cambia il numero di nodi con il variare dei numeri quantici secondo quanto riportato sopra. Possiamo avere una diversa rappresentazione delle stesse funzioni se decidiamo di riportare in grafico la probabilità che un elettrone abbia coordinata comprese tra r ed r + dr e cioè se riportiamo Z 2 2 | Ψ(r) | dr =| Rnl (r) | Ylm (θ, ϕ) sin θdθdϕ r2 dr (40) Poiché le Y sono normalizzate si avrà | Ψ(r) |2 dr =| Rnl (r) |2 r2 dr (41) Questa viene detta funzione di distribuzione radiale: questa rappresentazione è riportata nella figura 5a e figura 5b. 8 Le funzioni con numeri quantici 211 e 21-1 sono funzioni complesse: infatti come si vede dalle tabelle esse contengono rispettivamente il termine eiϕ (42) e−iϕ (43) e Se vogliamo usare funzioni reali sceglieremo le combinazioni lineari eiϕ + e−iϕ = cos ϕ 2 eiϕ − e−iϕ = sin ϕ 2i =⇒ x (44) =⇒ y per cui le parti angolari diventeranno Ψ210 =⇒ p2z =⇒ cos θ =⇒ z Ψ2px =⇒ sin θ cos ϕ =⇒ x Ψ2py =⇒ sin θ cos ϕ =⇒ y (45) Queste nuove funzioni saranno ancora autofunzioni di H e di L2 ma non sono più autofunzioni di Lz . Per quanto riguarda la rappresentazione grafica della parte angolare possiamo procedere rappresentandola in un sistema di coordinate polari. Ad esempio una funzione di tipo s (l = 0) che non contiene dipendenza dagli angoli sarà isotropa cioè identica in tutte le direzioni dello spazio e quindi sarà rappresentata da una sfera. Una funzione con l = 1 ed m = 0 che ha parte angolare cosθ possiamo rappresentarla riportando in ogni direzione, corrispondente ad un valore dell’angolo, il valore di cosθ. In questo modo in un piano si ottengono due circonferenze tangenti disposte lungo l’asse z. Oppure in una rappresentazione spaziale due sfere tangenti. In modo analogo si hanno rappresentazioni grafiche delle altre funzioni, come sono riportate nelle figure 6a, 6b e 6c. Una rappresentazione grafica alternativa e di riportare delle superficie sulle quali la probabilità sia costante oppure una unica superficie che racchiuda al suo interno il 90% della probabilità. Queste rappresentazioni grafiche sono riportate nella figura 7. 9 Infine non abbiamo detto nulla della simbologia in uso per identificare le varie autofunzioni atomiche in quanto queste sono già note: comunque la notazione viene riassunta qui di seguito l 0 notazione s 1 p 2 d 3 f 4 g 5 6 h i Effetto Zeeman Abbiamo visto che livelli con diverso numero quantico m (ma con n ed l uguali) sono degeneri. Questa degenerazione si perde se l’atomo è immerso in una campo magnetico. Infatti ad un elettrone che ruota è associato un momento magnetico e la interazione tra il momento magnetico ed il campo magnetico applicato separa gli stati con diverso m. Per vedere come questo avvenga consideriamo la situazione illustrata in figura 8 e calcoliamo il momento magnetico associato con l’elettrone ruotante. Abbiamo circonf erenza : tempo di rivoluzione : intensità di corrente : area spira 2πr 2πr v q qv I= = t 2πr A = πr2 (46) Il momento magnetico associato all’elettrone ruotante sarà IA qv πr2 qvr qrp = = = (47) c 2πr c 2c 2mc Se consideriamo il momento come un vettore scriveremo più precisamente µ= q q r×p= L (48) 2mc 2mc con una espressione analoga per i relativi operatori. Nel caso specifico dell’elettrone avremo µ= µ=− e L 2mc L=~ e quindi 10 p l(l + 1) (49) | µ |= e~ p l(l + 1) 2mc (50) e~ 2mc (51) e definendo il magnetone di Bohr βe = possiamo scrivere | µ |= βe p l(l + 1) (52) Se applichiamo un campo magnetico B ci sarà un’energia di interazione con il momento magnetico dell’elettrone data da e L·B 2mc Se il campo magnetico è applicato nella direzione z avremo E = −µ · B = e βe Lz B = Lz B 2mc ~ In questa situazione avremo nell’Hamiltoniano un nuovo termine E= (53) (54) βe Lz B ~ (55) HT = H + HB (56) HB = per cui l’Hamiltoniano totale sarà e la nuova equazione di Schrödinger in presenza del campo magnetico sarà βe Lz BRnl (r)Ylm (θϕ) = ~ (57) Ze2 = (− + βe Bm)Rnl (r)Ylm (ϕ) 2an2 (H + HB )Rnl (r)Ylm (ϕ) = HRnl (r)Ylm (θϕ) + Si vede quindi che in presenza del campo magnetico stati con diverso m hanno energia diversa. È chiara anche da questo il nome di numero quantico magnetico per m. Bisogna notare però che in questa trattazione abbiamo trascurato lo spin dell’elettrone che del resto non abbiamo ancora introdotto. 11 Orbitali di Slater Abbiamo visto la forma degli orbitali per atomi idrogenoidi, cioè gli orbitali che descrivono un elettrone sotto l’azione del solo campo di interazione con il nucleo −Ze2 /r. È evidente che questi orbitali non saranno adatti per descrivere un elettrone in un atomo polielettronico dove oltre alla attrazione con il nucleo è presente anche la interazione con gli altri elettroni. Tuttavia è sempre valido o comunque si può sempre giustificare il modello di un elettrone che si muove in un campo centrale ”efficace” che è la risultante della attrazione nucleare e della repulsione interelettronica. Naturalmente in questo caso il campo non è più coulombiano e gli orbitali non saranno più come quelli idrogenoidi per la parte radiale. Si possono descrivere questi orbitali come combinazioni di orbitali di Slater che hanno la forma Ψ = Rnl (r)Ylm (θϕ) (58) con parte radiale r Rnl (r) = cn rn−1 e−ζ ao (59) dove p 2ζ/ao cn = p (2n)! (60) e dove ζ viene detto esponente orbitale e, dalla sua definizione, è in sostanza una carica nucleare efficace schermata (s = fattore di schermo). A livello approssimato l’esponente orbitale può essere definito come ζ = Z−s dove s n è un fattore di schermo dovuto agli altri elettroni. In pratica l’esponente orbitale viene considerato come un parametro aggiustabile per ogni atomo; in ogni modo ci sono modi di stimare gli esponenti orbitali in vari atomi ed alcuni esponenti orbitali sono riportati nella tabella che segue. Poiché l’esponente orbitale contiene l’effetto di schermo dovuto agli altri elettroni e quindi dipende dalla distribuzione elettronica è chiaro che potrà dipendere sia da n che da l. Gli orbitali di Slater soddisfano la equazione radiale con un potenziale della forma U (r) = − ζn n(n − 1) + r r2 12 (61) e quindi una equazione di Schrödinger radiale con una energia potenziale efficace ζn n(n − 1) − l(l + 1) + (62) r r2 e quindi diversa da un potenziale puramente coulombiano. Nel limite di r grande il potenziale efficace si approssima ad un potenziale coulombiano con Zef f = ζn, mentre nel caso in cui l = n−1 l’orbitale di Slater diventa identico ad un orbitale idrogenoide. Vef f = − 13
Scaricare