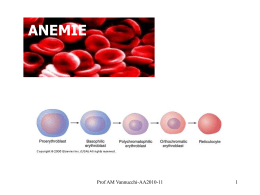
ANEMIE 1 ERITROPOIESI - Cellule staminali commissionate (BFU-E, CFU-E) - Precursori eritroidi - Proeritroblasti, eritroblasti basofili e policromatofili proliferano e maturano (sintesi HB) -Eritroblasti ortocromatici “perdono” il nucleo e continuano a sintetizzare HB - Reticolociti: si completa la sintesi dell’HB - Eritrociti - Eritropoietina PROGENITORI PRECURSORI ERITROIDI BFU-E CFU-E ERITROBLASTI 1,100 <100 EPO-R c-Kit Epo- DIPENDENTE •Commissionamento •Proliferazione •Maturazione •Apoptosi 3 ERITROPOIETINA L’eritropoietina e’ prodotta da cellule del sistema monocito-macrofagico posizionate intorno ai tubuli prossimali nella corticale del rene (cellule interstiziali renali). Il consumo di O2 nella corticale del rene è pressochè costante, quindi la pO2 dipende dalla quantita’ di O2 trasportata dagli eritrociti. Le cellule peritubulari “sentono” la pO2 attraverso un sistema di proteine la cui configurazione ossi/desossi regola la sintesi di un fattore di trascrizione (hypoxia inducible factor, hif) che regola la sintesi di eritropoietina. 5 SINTESI EPO EMOPOIESI IPOSSIA EPO Fe DEPOSITI MARZIALI EMOCATERESI 6 Anemia • Valore di Hb <14 g/dL nell’uomo e <13 g/dL nella donna • Ampia variabilità fisiologica in rapporto all’età, altitudine, etnia, etc • Non è una diagnosi, ma solo l’inizio di un iter diagnostico che deve portare alla caratterizzazione dell’anemia • Astenia, facile affaticabilità, tachicardia, dispnea da sforzo, difficoltà di cencentrazione, pallore. La tolleranza dipende dalla velocità con cui l’anemia si determina, dalla durata, dall’età del soggetto, dalle condizioni generali, dalla causa stessa della anemia. 7 Emocromo Emoglobina (Hb) Numero dei globuli rossi (GRC) Ematocrito (Hct) MCV=volume corpuscolare medio RDW= red cell distribution width o distribuzione dei volumi delle emazie Formula leucocitaria Forma dei globuli rossi, schistociti Morfologia leucociti e piastrine 8 INDICATORI DI ERITROPOIESI - I • CONTA RETICOLOCITI Valutano la funzionalità dell’ERITRONE, cioè dell’unità funzionale costituita da eritrociti circolanti e loro precursori • Colorazione sopravitale blu di metilene (1-1.5%) Indice reticolocitario = %reticolociti x Hct paziente x ½ * Hct normale(45) * Fattore correzione per il rilascio prematuro • Analisi citofluorimetrica (60x109/L; L, H, M fractions) • FERROCINETICA (turnover plasmatico del 59Fe; curve di sopravvivenza) sideremia, recettore solubile per la transferrina, ferritina. 9 INDICATORI DI ERITROPOIESI - II • ERITROPOIETINA SIERICA • RECETTORI SOLUBILI PER LA TRANSFERRINA (TfR) Golgi FERRITINA EME ERITROBLASTO Hb •TfR presente su tutte le cellule •>80% si trova sugli eritroblasti •Equilibrio tra forma di membrana e quella solubile •Correlato con i livelli di Fe: quando la cellula necessita di ferro, l’espressione del TfR aumenta per favorirne la captazione GLOBINE 10 CLASSIFICAZIONE FUNZIONALE DELLE ANEMIE ANEMIA reticolociti IPORIGENERATIVA VCM •Normocitica •Microcitica •Macrocitica IPOPROLIFERAZIONE ALTERATA MATURAZIONE * •Alterata sintesi Hb •Alterata sintesi DNA IPERRIGENERATIVA Post emorragica Da sequestro splenico emolitica 11 * Eritropoiesi inefficace ANEMIE-PATOGENESI ANEMIE DA ALTERATA PRODUZIONE (IPOPROLIFERATIVE) •PER INFILTRAZIONE MIDOLLARE •ANEMIA APLASTICA E APLASIA •DA ALTERATA PROLIFERAZIONE E MATURAZIONE •Anemia malattie croniche, disordini endocrini •Sindromi mielodisplastiche •DA ALTERATA SINTESI DEL DNA •Da carenza di folati, vit B12 •Difetti congeniti •DA ALTERATA SINTESI DELL’HB •Anemia sideropenica •Talassemie •Emoglobinopatie (HbS, Hb instabili, metemoglobinemia) 12 ANEMIE DA ALTERATA DISTRUZIONE (IPERPROLIFERATIVE) •DA DIFETTO INTRAGLOBULARE •Difetto di membrana •Sferocitosi ereditaria •Ellissocitosi ereditaria •Da carenza enzimatica (G6PDH, PK) •DA DIFETTO EXTRAGLOBULARE •Da autoanticorpi •Stress meccanico (microangiopatie, protesi valvolari, emoglobinuria da marcia) •Chimici/fisici (piombo, aresenico, rame, ustioni, veleni) 13 INQUADRAMENTO FUNZIONALE Anemia DELLE ANEMIE Recettore solubile per la Transferrina Reticolociti EPO Ipoproliferativa , * Eritropoiesi inefficace Emolisi * in caso di produzione inappropriata 14 Altri test utili per l’inquadramento di una anemia • • • • • • • • • • • Esame morfologico dello striscio Test di Coombs Diretto e Indiretto Dosaggio vitamina B12, acido folico Autoanticorpi anti-Fattore Intrinseco Dosaggio sideremia, ferritina, transferrina Elettroforesi/HPLC della Hb Dosaggi enzimatici eritrocitari (G6PDH, PK) Test delle resistenze osmotiche globulari Test del siero acidificato (di Ham) & FACS CD59/55 Valutazione striscio midollare e BOM Test genetici 15 ANEMIE IPORIGENERATIVE MICROCITICA NORMOCITICA MACROCITICA sideropenica In malattie croniche Carenza di vit. B12 talassemie Insufficienza renale Carenza di folati Anemia aplastica Mielodisplasie Invasione midollare 16 Anemia sideropenica-I • Assorbimento Poco efficiente – Normale: <10% – In caso di deficit di Fe: 30% • Fabbisogno: – 1 mg/die per soggetti sani e normali – 3 mg/die per donne con ciclo mestruale – 3-6 mg/die durante gravidanza e allattamento 17 • Escrezione Via primaria di escrezione: perdita di cellule – Epidermide – Mucosa intestinale, 1 mg/die – Sangue: mestruazioni (0.5-1 g/die) emorragie, versamenti etc Anemia sideropenica-II Ridotto introito malassorbimento Stillicidio cronico: •Menorragie o fibromi uterini •Ulcera gastrica •Neoplasie gastro-enteriche •Diverticolosi •emorroidi Ferro (sideremia) Transferrina Ferritina 18 Anemia microcitica ipocromica I globuli rossi sono più piccoli e più pallidi del normale. E’ presente anche anisopoichilocitosi (eterogeneità di dimensione e forma) Talassemie “Patologie in cui si ha riduzione più o meno grave della sintesi di catene dell’emoglobina” Hb fisiologiche EMOGLOBINE ADULTE: – A 2 β2 96-98% – A2 2,2 2-3.5% – F 2 2 <1% EMOGLOBINE EMBRIONALI: – Gower 1 2 2 – Portland 2 2 – Gower 2 2 2 20 Talassemia 2 geni di globina per ogni cromosoma 16:meccanismo è la DELEZIONE -/ --/, -/- --/- --/-- silente tratto talassemico: lieve anemia, riduzione MCV anemia moderata, riduzione MCV, splenomegalia idrope fetale b Talassemia 1 gene di globina b per ogni cromosoma 11:meccanismo è la MUTAZIONE 1 solo allele mutato : talassemia minor (anemia lieve, riduzione MCV, aumento numero dei globuli rossi, aumento RDW) Entrambi gli alleli mutati: talassemia major o intermedia (anemia grave con necessità di trasfusioni, riduzione MCV, aumento numero dei globuli rossi, aumento RDW , aumento HbF, lesioni ossee, ittero, epatosplenomegalia) 21 Modalità di trasmissione della talassemia Quali sono le conseguenze della Talassemia? Inadeguata produzione delle catene globiniche-->ipocromia e microcitosi accumulo non bilanciato di altre catene globiniche-->precipitati negli eritroblasti eritropoiesi inefficace ridotto numero di eritrociti maturi distruzione periferica con anemia emolitica Talassemia major Classificazione clinica • Portatore sano (tratto talassemico) • Talassemia intermedia • Talassemia major Anemie normocitiche Secondaria a neoplasie o stati infiammatori cronici Meccanismi: produzione di citochine che deprimono l’eritropoiesi, favoriscono l’accumulo di ferro nei depositi (ferritina); riduzione della vita dei globuli rossi. Alterazioni: ferritina Sideremia e transferrina Insufficienza renale: ridotta secrezione EPO Aplasia midollare/invasione midollare 25 Anemie macrocitiche Deficit di acido folico Deficit di vitamina B12 Carenza alimentare Deficit di assorbimento Defict nella sintesi del DNA 26 Anemia megaloblastica • Carenza da acido folico o vitamina B12 = necessari alla sintesi del DNA • Sintomi neurologici da carenza di B12: demielinizzazione • Coinvolge anche le altre cellule mieloidi • Dieta • Anemia perniciosa – Anticorpi contro le cellule parietali – Carenza di fattore intrinseco, necessario per l’assorbimento intestinale della B12 ANEMIE IPERRIGENERATIVE Post emorragica Da sequestro splenico Emolitica Da cause globulari Da cause extraglobulari CONGENITE (difetti di membrana, emoglobinopatie, enzimopatie) MECCANICA (protesi valvolari, microangiopatie) ACQUISITE (Emoglobinuria parossistica notturna) INFETTIVA (es. malaria) IMMUNE 28 INDICATORI DI • • • • • EMOLISI LDH Bilirubina Indiretta Aptoglobina Reticolociti Emosiderinuria 29 ANEMIE EMOLITICHE DA DIFETTO CONGENITO DI MEMBRANA SFEROCITOSI EREDITARIA Disordine congenito Sferociti nello striscio periferico: hanno perso il caratteristico pallore nella zona centrale: sono sfere e non dischi biconcavi. 30 ETIOLOGIA Difetto congenito qualitativo o quantitativo di una proteina della membrana del GR ANCHIRINA (chr 8) – SPECTRINA (chr 1) b - SPECTRINA (chr 14) PROTEINA DI BANDA 3 (chr 17) PROTEINA 4.2 (chr 15) Sono state descritte a carico di tali geni: Mutazioni puntiformi Difetti di “mRNA processing” Delezioni geniche 31 PATOGENESI L’ aumentata fragilità di membrana provoca una riduzione dell’area di superficie e la formazione di eritrociti di forma sferica scarsamente deformabili che vengono distrutti a livello splenico. Le condizioni del microcircolo splenico (pH basso; bassi livelli di Glu e ATP; alti livelli di radicali liberi) favoriscono il danno di membrana. 2/3 dei casi ereditarietà AD (soprattutto per difetti a carico dell’anchirina, seguita per frequenza dalla banda 3 e dalla b-spectrina). 1/3 dei casi ereditarietà AR (difetti sia a carico dell’ - spectrina che della proteina 4.2). 32 DIAGNOSI Anamnesi familiare ed E.O. Striscio di sangue periferico. MCHC (concentrazione emoglobinica corpuscolare media, Hb/Hct) aumentato nel 50% dei pazienti a causa della disidratazione cellulare. Indici di emolisi: aumento LDH; bilirubina totale e indiretta; riduzione aptoglobina; reticolocitosi. 33 TEST DI HAM: misura in vitro la lisi di globuli rossi sospesi in soluzioni di osmolarità decrescente. Gli sferociti emolizzano più dei GR normali se sospesi in una soluzione ipotonica di NaCl. 34 CLINICA Il grado di emolisi è variabile, da pazienti asintomatici a pazienti trasfusione-dipendenti. FORMA CLASSICA: la maggior parte dei pazienti è asintomatica. Anemia con reticolocitosi, ittero, calcolosi biliare (50%), splenomegalia. FORMA SEVERA: emolisi scarsamente compensata ed anemia severa, ritardi di crescita, ritardo della maturazione sessuale, emopoiesi extramidollare (pseudotumori), ulcere cutanee. COMPLICAZIONI: coliche biliari, colecistiti e colangiti; crisi emolitiche, aplastiche (coinfezione da Parvovirus B19) e megaloblastiche (deficit di folati, soprattutto in gravidanza e negli anziani); emocromatosi secondaria a supporto trasfusionale. 35 Terapia: Splenectomia 36 DEFICIT DI G6PDH Mutazioni a carico del gene dell’enzima glucosio 6-fosfato deidrogenasi, sul cromosoma X donne portatrici, maschi affetti Le mutazioni riducono in misura variabile l’attività del gene In occasione di condizioni di stress ossidativo (farmaci, alimenti, infezioni) ossidazione delle globine danno della membrana emolisi 3 forme: 1. Emolisi cronica 2. Emolisi acuta intermittente (mediterraneo) 3. Nessuna riduzione della vita del globulo rosso 37 EMOGLOBINOPATIE ANEMIA FALCIFORME mutazione puntiforme del gene della b globina:HbS Nella forme deossigenata polimerizza e precipita, rendendo rigida la membrana dell’eritrocita Clinica: sintomi da occlusione del microcircolo: crisi dolorose, infarti, emolisi cronica Dg: striscio di sangue periferico, elettroforesi dell’Hb 38 AUTOIMMUNI Da isoanticorpi: anticorpi responsabili di reazioni trasfusionali in caso di incompatibilita •post-trasfusionale, •emolitica del neonato Da autoanticorpi: •caldi (si formano e reagiscono a 37°C) •freddi (crioagglutinine, reagiscono a T<37°C) •bifasici (ab si attivano con l’esposizione al freddo, ma attivano il complemento a 37°C) 39 MALATTIE EMOLITICHE AUTOIMMUNI La diagnosi - Anemia, ittero, urine ipercromiche, feci ipercromiche - (Splenomegalia) - Anemia di grado variabile, con reticolocitosi - Aptoglobina, bilirubina, LDH - Test di coombs IL TEST DI COOMBS Diretto – eritrociti paziente + siero di coombs. Se agli eritrociti sono adesi anticorpi (Ig), il siero di coombs fa agglutinare - rivela anticorpi adesi agli eritrociti Indiretto – eritrociti normali + siero paziente + siero di coombs. Se il siero del paziente contiene anticorpi antieritrociti, questi si agglutinano. Rivela anticorpi nel siero. EMOGLOBINURIA PAROSSISTICA NOTTURNA Patologia clonale della cellula staminale ematopoietica che rende i globuli rossi più sensibili alla lisi mediata da complemento Deficit di proteine transmembrana (PIG) Frequentemente associata ad anemia aplastica Dg: espressione di CD55/59 aberrante , valutata all’immunofenotipo Emolisi cronica intravascolare, particolarmente frequente durante la notte, probabilmente per variazioni del pH Aumentato rischio trombotico 42 PNH: un difetto del gene PIG-A (chr Xp22.1) Codifica per la proteina richiesta per il trasferimento di N-acetilglucosammina a fosfatidilinositolo: Difetto di ancoraggio alla membrana eritrocitaria di alcune proteine che “proteggono” dalla lisi complementare (CD55, CD59) Luzzatto L, 2003 EMOGLOBINURIA PAROSSISTICA NOTTURNA Triade: • anemia emolitica (da difetto intrinseco) • pancitopenia (aplasia midollare) • trombosi venose (specialmente del sistema epato-portale, ma anche mesenteriche, spleniche, cerebrali) 3 forme cliniche: • Forma classica • In corso di disordini midollari (aplasia midollare, MDS, PMF) • Forma subclinica Diagnosi: • “Consistente” sospetto clinico • Dimostrazione citofluorimetrica di cellule carenti in GPI (“PNH cells”) • Valutazione indici di emolisi e valutazione midollare (per i sottotipi clinici) TROMBOSI & PNH Le trombosi rappresentano la causa principale di mortalità Sedi di trombosi più rappresentate: Vene epatiche (S. di B-C) Vene mesenteriche Vena porta Vene cerebrali Vene derma La frequenza di trombosi è correlata alle dimensioni del pool PNH (odds ratio 1.64 per ogni 10% incremento del pool) La incidenza di trombosi è associata a fattori razziali I pazienti di razza bianca e afro-americani con >50% di cellule GPI-AP deficienti, e che non abbiano controindicazioni, sono candidati alla terapia profilattica con warfarin [INR 2.0-3.0] I pazienti che abbiano presentato eventi trombotici dovrebbero ricevere terapia anticoagulante indefinitamente [INR 3.0-4.0] International PNH Interest Group, Blood 2005:106:3699 PNH LABORATORIO: - CD55, CD59 su eritrociti e leucociti - test dell’emolisi acida (test di ham) Ctrl PNH Meccanismi della trombosi • Piastrine: rilascio di micro-particelle procoagulanti • Granulociti: carenza del recettore dell’attivatore del plasminogeno • Eritrociti: in conseguenza della emolisi Hugel B, Blood 1999; 93:3451 APLASIA significa “carenza di elementi figurati del sangue” con riduzione delle cellule progenitrici e dei precursori midollari Si manifesta con i segni e sintomi • Infettivi • Emorragici • Necessità di supporto trasfusionale per la anemia e/o piastrinopenia 48 Aplasie midollari • Congenite – Anemia di Fanconi, Anemia familiare, S. Schwachmann Diamond, Discheratosi congenita • Acquisite – Idiopatica – Da farmaci • Dose dipendente • idiosincrasica – – – – Da tossici chimici Infezioni Timoma In corso di altre malattie ematologiche (S. mielodisplastiche, EPN) 49 Reperti di laboratorio Conta del sangue periferico (vari gradi di pancitopenia): - anemia sempre presente (normocromica-normocitica, reticolociti bassi) - granulocitopenia, monocitopenia, riduzione linfociti T helper e suppressor - trombocitopenia di grado variabile 50 Midollo osseo nell’anemia aplastica Midollo osseo (ridotta ematopoiesi): - “puntio sicca” all’aspirato - la biopsia mostra ipocellularità con predominanza di cellule adipose, linfociti e plasmacellule con residui mieloidi, eritroidi e maegacariociti. Midollo normale: Ematopoiesi occupante 30-70% dello spazio, Restante parte adipociti Anemia Aplastica: Assenza di ematopoiesi identificabile 51 Reperti di laboratorio Altri test diagnostici: - coagulazione nella norma - metabolismo del ferro normale ma, a causa della ridotta utilizzazione, aumento o normalità della sideremia. Eventuale riduzione del ferro compartimentalizzato in caso di perdite ematiche - eritropoietina serica elevata (a seconda dell’anemia) 52 Terapia 1. Terapia di supporto - profilassi per il rischio infettivo - Supporto trasfusionale 2. Terapia immunosoppresiva 3. Trapianto di midollo 53 Aplasia eritroide pura Definizione: danno della cellula progenitrice ERITROIDE a. forma congenita cronica: : anemia di DiamondBlackfan b. forma acquisita acuta: associata a infezione da Parvovirus B19, gravidanza, farmaci, agenti tossici c. forma acquisita cronica: mediata da anticorpi anti-eritroblesti o anti eritropoietina (es. Timoma, malattie autoimmuni) 54
Scaricare