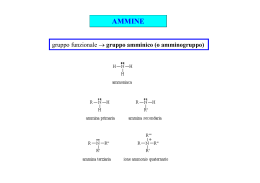
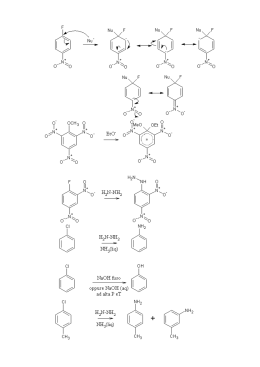
SAGGI DI RICONOSCIMENTO DI AMMINE ALIFATICHE ED AROMATICHE Composto CH3CH3 CH3OH CH3NH2 CH3CH2CH3 CH3CH2OH CH3CH2NH2 Mol.Wt. 30 32 31 44 46 45 Punto Eboll. ºC -88.6º 65º -6.0º -42º 78.5º 16.6º BASICITA’ DI AMMINE DI USO COMUNE Base pKa CH3C≡N NH3 11.0 10.7 10.7 9.3 5.2 4.6 1.0 pKa + pKb = 14 Più elevato è il pKa più forte è la base 0.0 -1.0 -10.0 GRUPPO GUANIDINICO Guanidina (pKa = 13.6). AMMINE SAGGI DI RICONOSCIMENTO: 1- Saggio di HINSBERG 2- Saggio con Acido Nitroso 3- Saggio delle Carbilammine 4- Saggio con Ioni Rameici 5- Saggio di Rimini 6- Saggio degli Acidi ditiocarbammici 7- Saggio della Lignina Amine Saggio di Hinsberg La metodica di questo saggio può essere utilizzata sia ai fini qualitativi, per stabilire se l'ammina in esame é I°, II° o III°, sia per il frazionamento di miscele di ammine a diverso grado di sostituzione sull'azoto amminico. R1 NH2 R1 R2 VALIDO PER AMMINE AROMATICHE NH R1 R2 N R3 Tecnica di esecuzione del saggio qualitativo: A 0,1 g di ammina posti in una provetta, si aggiungono 0,2 g di benzen- o di ptoluensolfonilcloruro e dopo qualche minuto 5 ml di NaOH al 10%. Si tappa accuratamente la provetta e si agita energicamente il suo contenuto per circa 5 minuti. Si rimuove il tappo, si scalda su bagnomaria per qualche secondo e quindi si agita la provetta, nuovamente tappata, per alcuni ulteriori minuti o comunque fino a completa scomparsa del reagente, verificando che l'ambiente sia rimasto alcalino L'acido nitroso reagisce con le ammine in maniera differente a seconda che siano I°, II° o III°, alifatiche o aromatiche. Tecnica di esecuzione: Circa 50 mg di ammina vengono disciolti in provetta in 2-3 ml di HCl diluito e la soluzione é raffreddata in ghiaccio (soluzione 1). In una seconda provetta viene preparata una soluzione contenente 0,2-0,4 g di NaNO2 in 2-3 ml di H2O (soluzione 2), mentre in una terza provetta vengono disciolti 30-50 mg di β-naftolo in 5-6 ml di NaOH al 5% (soluzione 3); anche queste ultime due soluzioni devono essere raffreddata in ghiaccio. Alla soluzione dell'ammina (Soluzione 1) viene aggiunta la soluzione di nitrito sodico (Soluzione 2), goccia a goccia, fino ad avere un leggero eccesso di acido nitroso, e cioè fino al viraggio al blu di una cartina imbevuta di soluzione acquosa di KI e di salda d’amido, osservando il comportamento della soluzione. Si possono verificare le situazioni descritte ai seguenti punti a)-e), che nei casi b) e c) possono suggerire ulteriori reazioni: a) Se la soluzione rimane limpida con sviluppo di un gas incolore (N2) sotto forma di bollicine che si generano in tutta la soluzione, l'ammina é probabilmente primaria alifatica. b) Se la soluzione rimane limpida e incolore senza che si sviluppi alcun gas, l'ammina dovrebbe essere primaria aromatica e il sale di diazonio formatosi dovrebbe essere sufficientemente stabile da poter copulare con il β-naftolo. c) Se si separa un olio o un solido giallastro, l'ammina è probabilmente secondaria. Si libera HNO2 d) Se la soluzione rimane limpida ma compare una evidente colorazione generalmente verde, significa che si e formato il nitrosoderivato di un'ammina terziaria alifatico-aromatica tipo N,Ndialchilanilina, che per alcalinizzazione con NaOH diluito precipita come un solido giallo-verdastro. e) Se non si verifica nessuno dei casi precedenti la sostanza è probabilmente un'ammina terziaria alifatica. RIEPILOGO Ammine Primarie Ammine Secondarie Il saggio é valido per le ammine primarie sia alifatiche (R-NH2) che aromatiche (Ar-NH2). Il saggio si effettua sciogliendo 20-30 mg del composto in 0,5 ml di etanolo e aggiungendo alla soluzione 0,5 ml di cloroformio e quindi una pasticca di KOH. La miscela é scaldata all'ebollizione. La reazione risulta positiva se si ha la liberazione di un odore molto sgradevole, caratteristico, dovuto alla formazione di carbilamine (isonitrili). Il saggio, valido per ammine a basso peso molecolare, solubili in acqua, si basa sulla formazione di complessi tetracoordinati con lo ione rameico. ESECUZIONE: Il saggio si esegue addizionando alcuni mg dell'ammina ad 1-2 ml di soluzione acquosa di CuSO4 al 10%. In caso di saggio positivo (interferisce l'ammoniaca) si forma una colorazione o un precipitato da blu a verde. Il saggio può anche essere eseguito su carta da filtro. Questo saggio è generalmente valido per ammine I° alifatiche solubili in H2O. Ad una soluzione acquosa dell'ammina si addiziona goccia a goccia una soluzione di sodio nitroprussiato all'1%. Si ottiene entro 2 minuti una colorazione rosso-violetta. Il saggio è specifico per le ammine II° alifatiche o alicicliche che reagiscono facilmente con CS2 per dare dialchilditiocarbammati. Questi ultimi sono capaci di dare precipitati salini con vari ioni di metalli pesanti. La lignina contenuta nella comune carta di giornale da con le ammine primarie e secondarie alifatiche ed aromatiche, composti colorati in giallo-arancione di struttura non definita. Il saggio è abbastanza specifico e può essere usato per differenziare le ammine terziarie dalle primarie e dalle secondarie: inoltre poiché il saggio risulta positivo per le ammine alifatiche primarie e secondarie solo se viene eseguito a caldo, possono essere anche distinte con questo metodo le ammine aromatiche dalle alifatiche. Esecuzione pratica: 10 mg del composto in esame + 3-4 gocce di etanolo; bagnare con la soluzione ottenuta un pezzetto di carta di giornale; + 2 gocce di HCl 6N sulla carta così bagnata; in presenza di ammine aromatiche primarie o secondarie immediata formazione di una colorazione gialla o arancione. Se il test condotto come descritto è negativo, ripeterlo una soluzione calda dell'ammina e una soluzione calda di acido cloridrico: in queste condizioni il saggio è positivo anche per le ammine primarie e secondarie alifatiche.
Scaricare