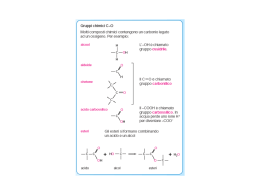
Oli e grassi.
Oli e grassi sono materiali familiari poiché formano un'importante parte della normale
dieta umana. Oltre il loro uso come cibo essi sono stati utilizzati fin dall'antichità come
combustibili da illuminazione, come base per profumi, come pomata per scopi medici e
cosmetici. Materiali per pratiche rituali avrebbero spesso compreso materie grasse e,
come conseguenza del loro utilizzo, essi sono stati spesso incontrati in contesti
archeologici come residui nel vasellame. Il sottogruppo formato da olii siccativi è di
importanza basilare nella tecnologia dei rivestimenti in generale e in particolar modo nei
dipinti. La chimica dei grassi, benché semplice come sostanza, diventa più complicata e
meno precisa quando è subentrata la domanda sulla siccatività o polimerizzazione.
Composizione
Non c'è una differenza essenziale tra oli e grassi tranne che il primo è generalmente
liquido, il secondo solido a temperatura ambiente. Occorrerebbe ricordare che i grassi
animali, che noi pensiamo come solidi, sono liquidi alla temperatura corporea
dell'animale. Clinicamente, i grassi sono definiti come miscele di trigliceridi misti, che
sono esteri dell'alcool glicerolo triossidrilico, con una gamma di possibili acidi grassi a
lunga catena. I grassi formano il principale sottogruppo della più larga classe di esteri di
acidi grassi conosciuti come lipidi, la definizione dei quali qualche volta si estende a
includere altri composti grassi solubili. Le proprietà fisiche e chimiche dei singoli grassi
sono determinanti dai tipi e dalle proporzioni di acidi grassi che entrano nella
composizione del triglicerde.
Definizione:
I lipidi sono sostanze organiche ternarie insolubili in acqua e solubili in solventi apolari come
etere e benzene.
Dal punto di vista chimico si dividono in:
SAPONIFICABILI O COMPLESSI: possono essere scissi, mediante idrolisi, in acidi grassi e
molecole portanti uno o più gruppi alcolici (gliceridi, fosfolipidi, glicolipidi, cere, steridi);
NON SAPONIFICABILI O SEMPLICI: non contengono acidi grassi nella loro struttura (terpeni,
steroidi, prostaglandine).
1
Acidi grassi.
Mentre l'intervallo degli acidi grassi che può essere trovato nei grassi è ampio, la
maggior parte dei trigliceridi sono fatti da relativamente pochi di essi, più
specificatamente gli acidi grassi a catena lineare con 18 atomi di carbonio.
2
I principali Acidi Grassi Saturi
N°
di C
Composizione
Denominazione
comune
Denomin. IUPAC Notazione Punto
abbreviata di
fusione
(°C)
Fonti in natura
4
CH3(CH2)2COOH
Butirrico
Butanoico
C4:0
-5
6
CH3(CH2)4COOH
Caprinico
Esanoico
C6:0
-2
8
CH3(CH2)6COOH
Caprilico
Ottanoico
C8:0
17
Grasso del latte, olio
di cocco
10
CH3(CH2)8COOH
Caprico
Decanoico
C10:0
32
Grasso del latte, olio
di cocco
12
CH3(CH2)10COOH
Laurico
Dodecanoico
C12:0
44
Grasso del latte, olio
di cocco, semi di
olmo (50% degli
acidi grassi)
14
CH3(CH2)12COOH
Miristico
Tetradecanoico
C14:0
58
Semi di Lauraceae,
oli di cocco
62
Presente in tutti gli
oli e grassi vegetali
ed animali, latte (812%), cocco (1530%), noce moscata
70-80%
72
Presente in tutti gli
oli grassi animali e
vegetali,sego e
strutto(25-30%).
palma (30-50%),
cacao (25%)
78
Presente in tutti gli
oli e grassi animali e
vegetali,
sego(20%), strutto
(10%), cacao
(35%), oli vegetali
(1-5%)
80
Presente in tutti gli
oli e grassi animali
in quantità
limitate,solo nell’olio
di arachide 1-2%
16
18
20
22
24
CH3(CH2)14COOH
CH3(CH2)16COOH
CH3(CH2)18COOH
CH3(CH2)20COOH
CH3(CH2)22COOH
Palmitico
Stearico
Arachio
Beenico
Lignocerico
Esadecanoico
Ottadecanoico
Eicosanoico
Docosanoico
Tetracosanoico
C16:0
C18:0
C22:0
C22:0
C24:0
Presente in tutti gli
oli e grassi animali
in quantità
limitate,solo nell’olio
di arachide 1-2%
Presente in tutti gli
oli e grassi animali
in quantità limitate,
solo nell’olio di
arachide 1-2%
3
Ac. Laurico (12:0)
Ac. Miristico (14:0)
Ac. Palmitico (16:0)
Ac. Stearico (18:0)
4
I principali acidi grassi monoinsaturi
n°
Di
C
Composizione
Denominazione Denominazione Notazione Fonti in natura
comune
IUPAC
abbreviata
10
CH2=CH(CH2)7COOH
Caproleico
cis-9decanoico
14
CH3(CH2)3CH=CH(CH2)7COOH
Miristoleico
cis-9C14:1 ω5 Latte
tetradecenoico
16
CH3(CH2)5CH=CH(CH2)7COOH
Palmitoleico
cis-6esadecenoico
C16:1 ω7
18
CH3(CH2)10CH=CH(CH2)4COOH Petroselinico
cis-6ottadecenoico
C18:1 ω6 Latte
18
CH3(CH2)7CH=CH(CH2)7COOH
Oleico
cis-9ottadecenoico
Tutti gli oli ed
grassi, olio di oliva
C18:1 ω9
(56-84%),oli di
semi (38-72%)
18
CH3(CH2)7CH=CH(CH2)7COOH
Elaidinico
trans-9ottadecenoico
C18: ω9
Latte oli e grassi
raffinati, margarine
18
CH3(CH2)5CH=CH(CH2)9COOH
Vaccenico
trans-11ottadecenoico
C18:1
ω11
Latte
18
CH3(CH2)5CH=CH(CH2)9COOH
Vaccenico
cis-11ottadecenoico
C18:1
ω11
Olio di pesce
20
CH3(CH2)9CH=CH(CH2)7COOH
Gadoleico
cis-9eicosenoico
C20:1 ω9 Olio di pesce
20
CH3(CH2)7CH=CH(CH2)9COOH
Gondoico
cis-11eicosenoico
C20:1
ω11
Olio di pesce
22
CH3(CH2)9CH=CH(CH2)9COOH
Cetoleico
cis-11docosenoico
C22:1
ω11
Olio di pesce
24
CH3(CH2)7CH=CH(CH2)13COOH Selacoleico
C10:1
cia-13C24:1
tetracosenocio ω13
26
Ximenico
cis-17esacosenoico
C26:1
ω17
26
Lumechico
cis-21esacosenoico
C22:1 ω1
Latte
Tutti i grassi
vegetali e animali
Cerebrosidi
5
Gli acidi grassi polinsaturi hanno piu di un doppio legame (-C=C-).
n°
di C
Composizione
Denominazione
comune
Denominazione Nota
IUPAC
abbr
Note/Fonti in natura
Grassi essenziali, ω6
(origine vegetale)Oli
C18:2 vegetali, in particolare oli
di semi (girasole, mais
ecc.)
18
CH3(CH2)4CH=CHCH2CH=CH(
Linoleico
CH2)7COOH
cis,cis-9,12octadecadienoi
co
18
CH3CH2(CH=CHCH2)3(C
H2)6COOH
α-Linolenico
cis,cis,cisGrassi essenziali, ω3
9,12,15(origine animale) Oli
C18:3
octadecatrienoi
vegetali, in particolare oli
co
di semi (soia, colza ecc)
γ-Linolenico
cis,cis,cis,6ω6 (origine vegetale) Oli di
9,12,pesce, olio di semi di
C18:3
octadecatrienoi
Borrago officinalis, olilo di
co
semi di Oenotera biennis
Morotico
cis,cis,cis,48,12,15octadecatetrae
noico
18
C17H29COOH
18
C18:4 Oli di pesce
20
Oli vegetali, in particolare
C20:1 oli di semi (soia, colza
ecc.)
20
cis,cis-13,16Oli di pesce olio di semi di
C20:2
docosadienoico
colza
20
CH3(CH2)4(CH=CHCH2)4(CH2
Arachidonico
)2COOH
cis,cis,cis,cis5,8,12,15ω6 (origine animale) Oli di
C20:4
eicosatetraenoi
pesce
co
20
Eicosapentaenoico
(EPA)
22
Docosaesaenoico
(DHA )
C22:6
Nisinico
cis,cis,cis,cis4,8,12,15eicosapentenoi
co
25
26
C23H35COOH
C20:5 Oli di pesce
Oli di pesce
C26:4 Oli di pesce
C26:5
ω3 (origine animale)Oli di
pesce
6
Ac. Oleico (18:1;9)
Ac. Linoleico (18:2;9,12)
Ac. γ-Linolenico (18:3;6,9,12)
Ac. α-Linolenico
(18:3;9,12,15)
Ac. Arachidonico
(20:4;5,8,11,14)
NOTA BENE: l'acido γ-Linolenico non appartiene alla serie omega tre, ma a quella omega 6; per
questo motivo gli integratori a base di acidi grassi essenziali ω3 devono contenere "acido αLinolenico" e non "acido γ-Linolenico"
Le serie di acidi a catena lineare e saturi è mostrata nella tabella 1.3 (1.2.2.3). I più
importanti dei quali sono ripetuti in tabella 3.1 insieme con gli acidi insaturi e gli acidi a
singolo ossidrile, acido ricinoleico, che è il maggiore componente dell'olio di ricino.
Gli atomi di carbonio degli acidi grassi a catena lineare sono numerati partendo dal
gruppo carbossilico il cui carbonio ha il numero uno e con nomi sistematici di acidi
grassi insaturi viene indicata la posizione di ciascuno dei doppi legami all'inizio del
nome dando la numerazione più bassa dei due carboni che contengono il doppio legame.
Quindi l'acido linoleico è 9, 12-octadecanoico e ha struttura 3.1.
7
Si può facilmente vedere che i doppi legami possono avere configurazioni CIS o
TRANS (vedi 1.1.2): nella struttura sopra vengono mostrati come legami CIS, che è la
più frequente, sebbene non invariabile, configurazione trovata negli acidi naturali e
quella che viene assunta se non viene specificato il nome.
Gli acidi grassi insaturi, se in configurazione cis, creano una piega. Le pieghe dei grassi
insaturi impediscono alle molecole di compattarsi saldamente e di solidificare a
temperatura ambiente.
Acidi grassi cis e trans
8
La forma cis abbassa
il punto di fusione
dell'acido grasso e ne
fa
aumentare
la
fluidità.
In natura prevalgono nettamente gli acidi grassi cis rispetto ai trans, che si formano soprattutto
in seguito a determinati trattamenti artificiali. Per esempio, durante il processo di rettifica
necessario per renderli idonei all'alimentazione, gli oli di semi si arricchiscono di acidi grassi
trans. Analogo discorso per la produzione di margarine, che avviene attraverso un processo di
idrogenazione degli oli vegetali (si aggiungono atomi di idrogeno per saturare i carboni impegnati
nel doppio legame, ottenendo così trigliceridi con acidi grassi saturi, quindi solidi, a partire da
lipidi insaturi, quindi liquidi).
Due acidi grassi uguali, ma che hanno un legame in conformazione cis ed uno in conformazione
trans, possiedono nomi diversi. In figura è riportato un acido grasso a diciotto atomi di carbonio,
con insaturazione in posizione nove e conformazione cis (acido oleico, l'acido grasso più
abbondante in natura e presente soprattutto nell'olio di oliva); il suo isomero trans, presente in
percentuali molto basse, assume un nome differente (acido elaidinico).
Importanza della stereo-isomeria del doppio legame
Osserviamo l'immagine sopra: a sinistra è rappresentato un acido grasso saturo, notare la catena
alifatica (coda lipofila) perfettamente lineare.
Alla sua destra vediamo invece lo stesso acido grasso con un legame di tipo trans. La catena
subisce una piccola flessione, ma rimane comunque una struttura lineare, simile a quella
dell'acido grasso saturo.
9
Ancora più a destra possiamo apprezzare il ripiegamento della catena indotto dalla presenza di un
doppio legame cis. Infine, all'estrema destra, è rappresentato il fortissimo ripiegamento associato
alla presenza di due doppi legami insaturi cis. Ecco spiegato come mai il burro, alimento ricco di
acidi grassi saturi, è solido a temperatura ambiente, mentre gli oli, in cui prevalgono gli acidi
grassi insaturi cis, sono liquidi nelle medesime condizioni. In altre parole, la presenza di doppi
legami cis abbassa il punto di fusione del lipide.
Dove si trovano gli acidi grassi trans?
Per dare maggiore consistenza agli oli ed ai grassi insaturi sono stati ideati processi
(idrogenazione) in cui si effettua la rottura artificiale di un doppio legame e l’idrogenazione del
prodotto, ottenendo così alimenti in cui la percentuale della forma trans è elevata.
Come già ricordato, i grassi insaturi naturali si trovano normalmente nella forma cis. Una
piccola quantità di grassi trans è però presente nel cibo, poiché si forma nello stomaco dei
ruminanti a causa dell'azione di determinati batteri. Per questo motivo nel latte, nei prodotti
caseari e nella carne bovina si trovano piccolissime quantità di acidi grassi trans. Gli stessi, si
trovano anche nei semi e nelle foglie di diverse piante, il cui consumo alimentare è però
irrilevante.
I rischi maggiore per la salute derivano quindi dal massiccio utilizzo di oli e grassi idrogenati, che
abbondano soprattutto nelle margarine, negli snack dolci e in molti prodotti spalmabili. Tale
processo avviene attraverso l'utilizzo di specifici catalizzatori che sottopongono la miscela di oli e
grassi animali ad elevate temperature e pressioni, fino ad ottenere acidi grassi chimicamente
alterati. Tale processo fa particolarmente gola alle industrie alimentari poiché permette di
ottenere grassi ad un costo ridotto e con specifici requisiti (spalmabilità, compattezza ecc.).
Inoltre viene considerevolmente prolungato il tempo di conservazione, aspetto fondamentale
anche sotto il punto di vista economico.
Perché gli acidi grassi trans sono pericolosi?
Tutta questa attenzione rivolta agli acidi grassi trans (trans fatty acid) è dovuta alle implicazioni
salutistiche negative che il loro uso comporta. Questi acidi grassi determinano infatti un aumento
del "colesterolo cattivo" (lipoproteine LDL) accompagnato ad una diminuzione della frazione
"buona" (lipoproteine HDL). Un elevato consumo di acidi grassi trans, aumenta quindi il rischio di
sviluppare gravi patologie cardiovascolari (aterosclerosi, trombosi, ictus ecc).
L'introduzione dell'insaturazione nelle molecole abbassa il punto di fusione rispetto
quello delle corrispondente acido grasso saturo . Questa proprietà è trasmessa al
triglicerde e quindi il grasso spesso la assume. Questa è la principale ragione per la
naturali liquida degli oli vegetali se confrontati con i grassi animali: essi contengono
proporzioni più elevate di trigliceridi insaturi. Un indice della quantità totale di
insaturazione dei grassi è il numero di iodio, una misura della quantità di iodio che
reagisce chimicamente con esso per addizione ai doppi legami. Questo è di solito è
ancora un'importante fattore caratterizzante gli oli e grassi in particolar modo gli oli
siccativi.
L''acido linoleico doppiamente insaturo e l'acido linolenico con tre doppi legami sono i
composti principalmente responsabili delle proprietà siccative degli oli siccativi. Si
potrebbe notare che essi non sono rispettivamente di dieni e trieni coniugati (1.1.2) ma
10
essi possono diventarlo facilmente per isomerizzazione. Questo avviene nei primi stadi
del processo di essiccamento, come osservato dallo sviluppo di assorbimento radiazioni
'ultraviolette ad una lunghezza d'onda di 233 nanometri. (diene coniugato) e 268
nanometri (triene coniugato).
La composizione in acidi grassi di un certo numero di oli e grassi sono elencati nella
tabella 3.2.
All'interno di un limitato e arbitrario raggruppamento di grassi, olio commestibile, semi
siccativi, e olio siccativo, le differenze di composizione sono. ampiamente quantitative
piuttosto che qualitative. Soltanto raramente un olio è univocamente distinguibile per la
presenza di particolari tipi di acidi grassi. Un esempio di uno tipico è l'olio di ricino che
contiene grandi quantità di acido idrossioleico, acido ricinoleico.
acido ricinoleico
Il campione nel suo insieme può essere tuttavia particolare come per esempio l'olio di
cocco. Questo potrebbe probabilmente essere confuso solamente con quello del seme di
palma che ha una composizione simile.
11
Non bisognerebbe pensare che la composizione di un particolare olio sia perfettamente
costante essa può variare per un numero di ragion, tra di loro:
tipo e varietà di pianta,
natura del suolo,
stagione della raccolta,
variazioni delle condizioni climatiche.
Ugualmente la determinazione della composizione è soggetta a errore sperimentale ed a
variazioni dovute all'uso di differenti tecniche di misurazione.
I risultati della tabella 3.2. sono tutti basati sulla gascromatografia, ma molti dei grafici
nei testi più vecchi sono state ottenute usando altri metodi meno accurati. Un numero
valido di studi sui semi di lino è servito a mostrare come la composizione varia da tipo a
tipo e con la stagione. Quest'ultima principalmente condiziona il grado di insaturazione,
ma questo a turno influenza il rapporto di acido palmitico e stearico, poiché un aumento
della quantità di acidi C18 insaturi diminuisce la quantità di acido stearico.
Trigliceridi.
Mentre la composizione degli oli e dei grassi è generalmente discussa in termini di
percentuale di singoli acidi grassi che entrano nella loro composizione, questi sono in
verità presenti combinati con il glicerolo per dare esteri noti come trigliceridi della
seguente formula generale:
Molto lavoro è stato fatto e diverse teorie formulate per predire il modo in cui gli acidi
grassi sono distribuiti fra le molecole dei triglicerde.
12
Fu scoperto in un primo momento che essi non erano generalmente presenti come
semplici trigliceridi, trioleina, tripalmitina etc., ma teorie su una pari distribuzione
(ciascun acido grasso distribuito su molte molecole di trigliceridi possibili) o una
distribuzione randomizzata (acidi grassi distribuiti in maniera casuale sui trigliceridi),
sono state ugualmente trovate spesso non corrispondere alle composizioni sperimentali
determinante dei trigliceridi.
Come può essere visto, i gruppi ossidrilici del glicerolo non sono tutti equivalenti ci
sono due primari e uno secondario su ciascuna molecola.
Un'altra teoria sulla distribuzione degli acidi grassi è che gli acidi insaturi si attaccano
preferibilmente alla posizione secondaria e quelli rimanenti, insieme con gli acidi saturi,
sono distribuiti in moto casuale fra le posizioni primarie. Infatti ciò risulta in una
composizione calcolata di trigliceridi non lontana dalla casualità, che però ancora non
concorda con quella realmente trovata per l'olio di lino, per esempio per la quale è stata
presentata una teoria di aggiustamento.
Per i nostri scopi comunque la cosa importante da ricordare è che il numero dei possibili
differenti trigliceridi è molto maggiore del numero degli acidi grassi componenti. Per
esempio con solamente tre acidi grassi possono essere formati 14 differenti trigliceridi
assumendo che i due gruppi ossidrilici primari sono considerati chimicamente
equivalenti. Con più acidi grassi il numero di possibilità cresce rapidamente: con cinque
acidi grassi dell'olio di lino ci possono essere ben 55 differenti trigliceridi. La
complessità risultante significa che l'analisi di un grasso, per la determinazione specifica
della composizione dei trigliceridi, è un compito molto più difficile nell'analisi degli
acidi grassi e che è stata eseguita solo in maniera incompleta per la maggior parte di
essi. Ciò è risultato difficile perché l'alto peso molecolare dei trigliceridi e la loro
conseguente bassa volatilità rende difficile analizzarli mediante gascromatografia.
Dovremmo quindi qui considerare i grassi in generale, solo in termini degli acidi grassi
che li compongono.
Proprietà chimiche dei grassi.
Le proprietà chimiche dei grassi sono determinate dalle loro principali caratteristiche
strutturali, vale a dire dalla presenza della funzione tripla esterea in ciascuna molecola
e dalla possibile presenza di doppi legami reattivi.
La presenza di acidi grassi contenenti due o più doppi legami conferisce alla molecola
l'alta sensibilità all'ossidazione, caratteristica degli oli siccativi, che sarà discussa di
seguito. Al contrario l'assenza di doppi legami si traduce in una relativa stabilità
all'ossidazione e questo è vero in molti grassi animali saturi purificati.
La presenza di gruppi esterei significa che le molecole possono essere rotte a livello del
glicerolo e degli acidi grassi mediante processi di saponificazione e di idrolisi.
13
Il termine saponificazione si riferisce al trattamento del grasso con alcali acquosi, soda
caustica o potassa (per esempio l'idrossido di sodio o l'idrossido di potassio) per portare
ai sali di sodio e potassio degli acidi grassi (saponi) e glicerolo.
L'idrolisi si riferisce alla reazione per mezzo della quale la scissione viene portata avanti
anche con sola acqua, richiede temperature più elevate, la presenza di una certa quantità
di acido minerale come catalizzatore, entrambi i processi portano ad acidi grassi liberi.
La reazione può anche avvenire come risultato dell'azione enzimatica iniziata da batteri
o funghi, e questa sarà discussa nella prossima sezione.
Reazioni dei lipidi:
Saponificazione la reazione consiste nel trattare il trigliceride con idrossido di sodio per la precisione tre molecole, nel
sistema biologico la reazione avviene per mezzo di enzimi quali la lipasi, a bassa temperatura. Il prodotto viene detto
sapone ed è un sale dell’acido carbossilico a catena lunga, liberando glicerina:
Idrogenazione questa reazione comporta la saturazione dei doppi legami e viene sfruttata industrialmente per trasformare gli
oli in grassi. La reazione consiste nell’aggiungere idrogeno con catalizzatori a base di nichel, a differenti temperature. Le
margarine sono grassi alimentari ottenuti per idrogenazione catalitica di un emulsione in acqua di oli vegetali. Il burro
invece e una miscela di trigliceridi in cui sono presenti grassi a catena corta, massimo 16 atomi di carbonio.
14
Idrogenolisi questa reazione comporta la scissione dei legami esterei mediante riduzione operata con idrogeno in presenza
di una miscela di ossidi a base di cromo e rame. Si lavora a temperature dell’ordine di 150°C e a pressioni di 300 atm. I
prodotti che si ottengono sono la glicerina e alcol corrispondente.
Autossidazione meglio conosciuta come irrancidimento, è la reazione che porta alla formazione degli idroperossidi. Si
formano in presenza di traccie di metalli, calore, radiazioni.
15
Cambiamenti nei grassi.
Grassi sepolti.
Materiali grassi sono stati trovati in vasellami sepolti nel terreno e sono stati trovati di
solito completamente convertiti in acidi grassi liberi. Tutto il glicerolo ha subito la
reazione di idrolisi,ed è stato presumibilmente lavato via dall'acqua. Come questa
trasformazione sia avvenuta non è stato ancora chiaramente stabilito. Si può ipotizzare
che l'idrolisi ha avuto effetto solo per azione dell'acqua, avendo avuto un tempo
sufficientemente lungo, ma di fatto sembra che il cambiamento sia avvenuto, molto più
rapidamente, per azione batterica.
I materiali più studiati sono stati quelli derivanti da grassi umani, conosciuti come
adipocere e il materiale qualche volta trovato sepolto nelle paludi Scozzesi e Irlandesi
conosciuto come “burro delle paludi”.
Il cosidetto “burro di palude” fu trovato sepolto all’interno di una sorta di
contenitore di legno. Esso è un idrocarburo di origine animale, conosciuto
anche come butirellite. Fino al 2003 gli scienziati e gli archeologi non
erano affatto sicuri della sua origine. Alcuni scienziati dell’università di
Bristol scoprirono che alcuni campioni del “burro” erano di origine
adiposa/sego, mentre altri di origine lattario/casearia.
Fu proposto che il “burro di palude” sia stato fatto da prodotti alimentari
sepolti allo scopo di refrigerazione arcaica, poiché la torba crea un sigillo
igienico intorno al materiale sepolto
Il “burro delle paludi” ha una composizione con alta percentuale di acidi grassi saturi, la
maggior parte C16 e C18, con una certa quantità di acido C18 mono-insaturo (oleico) in
gran parte riconducibile ai due possibili tipici contendenti il materiale originale, burro e
grasso di montone.
La scomparsa degli acidi insaturi avrebbe potuto essere prevista, ma la cosa meno
spiegabile è un'apparente aumento del rapporto di acido palmitico e acido stearico nel
burro di palude. Esperimenti hanno mostrato che il burro ed il grasso di montone,
incubati nell'acqua contenente piccole quantità di nutrienti chimici e microrganismi del
terreno in un ambiente virtualmente anaerobico (senza ossigeno), piuttosto rapidamente
(1 o 2 anni) inducono i cambiamenti indicati sopra.
L’adipocere si riferisce al prodotto di decomposizione che si forma per la conversione
dopo la morte del tessuto adiposo in una miscela lipidica. Durante il processo di
conversione, i trigliceridi presenti nel tessuto adiposo si trasformano in acidi grassi
mediante idrolisi. Nelle giuste condizioni, l’idrogenazione degli acidi grassi liberi
produrrà adipocere, che è principalmente composto di acidi grassi saturi liberi. Quindi
l’adipocere o cera di tomba o cera mortuaria sono gli acidi grassi insolubili lasciati
16
come residuo dai grassi pre-esistenti provenienti da materiale in decomposizione come
un cadavere umano. Esso è formato per lenta idrolisi in terreno umido e può avvenire
sia in corpi imbalsamati che in corpi non trattati.
L’adipocere inibisce la crescita dei batteri, e in qualche modo può proteggere il
cadavere dalla decomposizione. Esso si incomincia a formare dopo circa un mese
dalla morte e può persistere per secoli. Poiché si forma attraverso l’idrolisi ciò avviene
più facilmente in ambienti umidi o dentro l’acqua. Un corpo esposto all’aria
difficilmente forma depositi di adipocere. Il processo di formazione di adipocere è
anche conosciuto come saponificazione.
Un’ampia serie di esperimenti è stata portata avanti da den Dooren de Jong sulla
conversione dell'olio di oliva ad un materiale simile all'adipocere mediante acqua e
batteri in eventuali (sebbene non inizialmente) condizioni anaerobiche.
Egli dimostrò che la proporzione di acido palmitico nel materiale risultante era
fortemente aumentato e che questo era apparentemente formato da acido oleico, poiché
ciò era risultato da una conversione simile della trioleina pura (trigliceride formato da
glicerolo e acido oleico). Anche una certa quantità di culture pure, vale a dire di
staffilococco spp e Proteus, sono stati capaci di realizzare la trasformazione molto
rapidamente, per esempio in poche settimane.
Come avvenga questa trasformazione dell'acido oleico ad acido palmitico, coinvolgendo
la perdita di due carboni e la saturazione del doppio legame, è lontana da essere ovvia.
Non c'è una semplice strada chimica, ma apparentemente tali reazioni si possono
comunemente incontrare nel metabolismo dei lipidi.
La strada suggerita coinvolge prima
l'idrolisi ad acidi liberi mediante lipasi associata con certi batteri (l'ossigeno
sembra necessario);
poi la deidrogenazione per dare l’ acido -insaturo (il carbonio è quello a cui
il gruppo dell’acido carbossilico è attaccato, mentre il carbonio è il successivo
lungo la catena);
segue la scissione ossidativa di questo doppio legame per dare l'acido con due
atomi di carbonio in meno;
ed infine la idrogenazione del doppio legame originale.
In ogni caso, rimangono dei problemi con questa spiegazione.
1. L'ossidazione nella posizione distante due carboni dal gruppo carbossilico
( ossidazione) è molto ben conosciuta come parte del metabolismo degli
acidi grassi, ma generalmente non si ferma finché tutta la catena non sia
stata degradata.
17
2. Inoltre l'attacco generalmente avviene al doppio legame, qualora sia
presente, come qui, e l’apparente riduzione di questo, qui è senza
spiegazione.
Chiaramente sono richieste ulteriori investigazioni.
The Varrentrapp reaction is an organic reaction involving the chemical
decomposition of an α,β-unsaturated acid into two other acid fragments by action
of molten alkali. This reaction pioneered by F. Varrentrapp in 1840 [1] has been of
some importance in structure elucidation of certain fatty acids but has no
practical synthetic use [2] [3].
The original 1840 Varrentrapp reaction concerned the conversion of oleic acid to
palmitic acid, acetic acid and hydrogen gas:
the reaction conditions are harsh: medium molten potassium hydroxide at
temperatures in the range of 250 to 300 °C. Likewise cinnamic acid is converted
to benzoic acid.
The reaction mechanism for this reaction is outlined below. Although the alkene
group in the fatty acid can be located at more than one position in the chain, this
does not affect the nature of te reaction products. This is because the double
bond always migrates to the position next to the carboxylic acid group prior to
cleavage. The next step is nucleophilic addition of a hydroxyl anion to the double
bond of 1 followed by proton migration to intermediate 3. The next step is
cleavage to enolate 4a and aldehyde 4b. The enolate on acidic workup will form
acetic acid. The aldehyde continues to react with another equivalent of base
forming carboxylate 7 together with hydrogen. The hydride transfer is akin the
Cannizzaro reaction.
18
19
Initiating Step:
For this example, the 16 carbon palmitic acid is being used.
The initial event in the utilization of fat as an energy source is the
hydrolysis of the triglyceride by a lipase in the adipose tissue cell.
Hormones such as epinephrine, norepinephrine, glucagon, and
adrenocorticotrophic hormones, stimulate the adenyl cyclase in
adipose cells. The sequence of reactions is similar to that already
described for glycogenolysis in prior page. Ultimately, lipase is
activated by a phosphorylation reaction.
Before fatty acids can be oxidized, they must first undergo an initiating
or priming step. Fatty acids in the cytoplasm must cross the
mitachondria membrane before the oxidations begin. Simple fatty
acids are unable to cross this membrane unassisted. The overall initiating step is the reaction of the fatty acid with
coenzyme A in a thioester formation. This reaction requires energy and is therefore coupled with the hydrolysis of ATP to
AMP. The activated long chain fatty acid is carried across the mitochondria membrane by an organic compound called
carnitine
The fatty acid-CoA molecule is degraded into acetyl CoA molecules by a recurring cyclic sequence of four reactions. The
end product of each cycle is the fatty acid shortened by 2 carbons and
acetyl CoA.
The series of reactions is also known as the beta-oxidation pathway
because the major reaction site is the beta-carbon or #3 carbon from
the thioester carbon. The complete reaction sequence for one fatty
acid cycle is given as follows.
Actually, the reactions in the fatty acid cycle closely resemble the
last three steps of the citric acid cycle.
Step 1: Oxidation (Dehydrogenation)
The coenzyme FAD, which is directly connected to the electron
transport chain is involved with this reaction. Again it is somewhat
unusual for hydrogens to be removed from an alkane hydrocarbon
chain.
The hydrogens on the #2 and # 3 carbons are removed to form a trans double bond (alkene) type compound. The FAD is
converted
to
FADH2 and carries the two hydrogens and two electrons in the electron transport chain. Because this is the second
enzyme complex, the net yield of ATP is two
Step 2: Hydration Reaction:
This is an easily recognizable hydration reaction of an alkene to make an alcohol where the alcohol is
formed on the # 3 or beta carbon. This is the beginning reaction preparation for the eventual break off
of two carbons at a time.
Step 3: Oxidation Reaction:
Again, this reaction should be readily recognized as an oxidation of an alcohol
by the coenzyme NAD+ to form a ketone on the #3 or beta carbon.
The NAD+ is converted to NADH + H+ which is a direct link to the electron
transport chain. A result of this oxidation reaction is the production of three
ATP molecules.
Step 4: Cleavage by CoA:
The final step is the cleavage of the acetyl CoA from the original fatty acid chain (16 carbons).
At the same time, a new CoA molecule makes a new thioester bond to the # 3 or beta carbon
carbonyl group. Notice that the final fatty acid molecule attached to the new CoA has two
carbons less than when it started (14 carbons).
The 14 carbon-CoA molecule repeats steps 1-4 and finishes as 12 carbon-CoA plus acetyl CoA.
The 12 carbon-CoA repeats steps 1-4 and finishes as 10 carbon-CoA plus acetyl CoA. The
cycles are repeated until the last cycle begins with a 4 carbon-CoA and finishes as two acetyl
CoA molecules. Since the fatty acid cycles have a definite beginning and end, it is better to refer
20
21
Queste trasformazioni dovute a batteri sono dipendenti dalla temperatura e sono lente a
bassa temperatura. Recentemente è stato dimostrato che campioni di grasso di un
migliaio di anni proveniente da un mucchio di letame congelato nell'Yukon non erano
stati sottoposti a grandi cambiamenti nella composizione degli acidi grassi e ancora
presentavano una relativamente grande quantità di acido oleico e altri acidi insaturi. Ciò
nonostante, gli acidi grassi erano quasi interamente liberi, indicando che l’idrolisi del
campione avviene nel tempo in condizioni umide.
L’adipocere di un corpo immerso in una palude irlandese di circa 1570 d.C.. è stato
analizzato con attenzione mediante gas-massa. Esso era completamente idrolizzato, e
consisteva interamente di acidi grassi, la composizione del quale era molto usuale, con
grandi proporzioni di acido palmitico. Gli acidi idrossi-palmitico e stearico erano
ugualmente presenti in piccole quantità.
Alcuni campioni archeologici indicano che non avviene necessariamente la completa
idrolisi. Il contenuto di due bottiglie di vetro romane, che contenevano acqua come
22
anche residui grassi, consistevano di mono e di-gliceridi, come anche di acidi grassi
liberi, e questo risultato simile è stato riportato per l'analisi di un grasso emulsionato in
un'altra bottiglia romana. Una quantità significativa di acido oleico era anche presente
nell’ultimo esempio ed questo era vero anche che i resti di olio di oliva sulle pareti di
anfore ricoperto dal terreno, sebbene qui non è stato determinato quanto l'idrolisi sia
andata avanti. Il contenuto di una giara egiziana rotta (sesto secolo prima di Cristo)
conteneva anche acidi grassi liberi, sebbene in una proporzione con i gliceridi che non è
stata determinata. In questo caso sono stati trovati anche acidi dicarbossilici a catena più
corta come l’acido azelaico (vedi dopo).
Serie omologhe di acidi di carbossilici sono state trovate nei lipidi di una mummia
egiziana di 4000 anni, come anche idrossi e ossiacidi grassi, sebbene non sia chiaro se in
quantità relative significative rispetto agli acidi saturi.
L’analisi gascromatografica degli acidi grassi è usata sempre di più allo scopo di
identificare le origini vegetali o animali dei residui grassi archeologici. E’ necessaria
cautela in relazione ai cambiamenti nelle percentuali degli acidi grassi saturi che
possono avvenire come spiegato sopra.
Grassi in oggetti etnografici e di altro tipo.
Certi oggetti sono stati spesso trattati o ricoperti con oli o grassi sia come trattamento sia
come presunta misura di conservazione. I cambiamenti chimici nei grassi generalmente
hanno conseguenze visibili che è necessario studiare con attenzione e per questo sono
state effettuate un certo numero di analisi.
Sculture in legno e oggetti domestici da Mali nell'Africa occidentale spesso mostrano
una fioritura biancastra sulla superficie come risultato di un trattamento originale con
grassi disponibili localmente come il grasso di noce shea (da Butyrospermum parkii) e
altri. Uno studio di questa fluorescenza su un certo numero di oggetti usando la gas
cromatografia per alcuni e la spettroscopia infrarossa per i rimanenti ha confermato la
sua natura grassa. GLC ha identificato positivamente il grasso di noce shea per un
campione ed olio di palma per un altro, e questa seconda identificazione è servita per
confermare una ri-attribuzione di un oggetto ad una differente tribù e località.
Sfortunatamente non è stato chiaramente stabilito in che proporzione l'essudato
consisteva di acidi grassi liberi piuttosto che trigliceridi. Nel caso di un campione
proveniente da una zona restaurata di una scultura, la spettroscopia infrarossa ha
identificato il materiale come cera di carnauba non originale (4.2.1).
La tapa Hawaiana, stoffa di corteccia, preparata dalla corteccia interna di certe piante è
spesso oliata per renderlo impermeabile e più flessibile. Questo porta ad un notevole
degrado probabilmente dovuto alla natura acida dei prodotti di ossidazione dell'olio.
GLCè stata usata per identificare l'olio, in sei o sette campioni come anche l'olio di noce
kukui da Aleurites molluccana Wild .
23
Uno studio interessante è stato pubblicato sui risultati di un trattamento con grassi '(fatto
da collezionisti e musei) dei bronzi di Benin, come protettivi ipotizzati. Le analisi GLC
hanno mostrato che i grassi sono stati quasi completamente idrolizzati ad acidi grassi
liberi e che questi hanno corroso il bronzo per dare rame e sali di zinco. Tests di studio
hanno mostrato che una copertura di acidi grassi liberi (oleico, palmitico e stearico)
applicati al rame viene convertito per il 50% in sali di rame in soltanto quattro giorni,
dopo due mesi la trasformazione è completa. L'effetto è simile a quello qualche volta
osservato nei dipinti ad olio occidentali su pannelli di rame, dove la preparazione ad olio
ha reagito con il metallo per dare sali di rame verdi.
Florescenze acide sono qualche volta osservate anche su superfici dei dipinti e questo
sarà discusso nella sezione più avanti.
Oli siccativi e processo di essiccamento.
Un olio è capace di seccare, cioè si dice di polimerizzare in una forma semi solida solo
se ha un contenuto sufficiente di acidi grassi di o tri insaturi nella composizione dei suoi
componenti trigliceridi. Devono avere una media di almeno due centri reattivi all'interno
di ciascuna molecola dei trigliceridi, ciò sarebbe ottenuto in un olio teorico che
contenesse 66% di acido linoleico. In pratica sia gli acidi linoleico che linolenico sono
trovati insieme e il tipo di composizione che risulta soddisfacente per un essiccamento
può essere stabilita dalla tabella 3.1.
Il grado con cui l'acido oleico mono-insaturo prende parte alle reazioni di
polimerizzazione non è certa Certamente esso viene ossidato gradualmente, ma
probabilmente non viene incorporato nella rete polimerica tranne forse occasionalmente
come gruppo finale.
Gli oli siccativi che hanno trovato il maggiore uso dei dipinti europei occidentali sono
l'olio di lino, l'olio di noce e l'olio di papavero. Altri che sono stati nominati nelle prime
fonti di letteratura, ma per i quali non c'è una certezza evidente di utilizzo, sono l'olio di
24
canapa (dalla cannabis sativa) ed l'olio di pigna (dai semi commestibili o noci del pino a
ombrello, (pinus pinea) L'evidenza della analisi (12.1.4) suggerì che l'olio di lino fu
usato nel nord Europa dal XIII secolo almeno; sulla sua introduzione in Italia nei dipinti
ad olio del XV secolo sembra principalmente sia stato usato l'olio di noce, ma l'utilizzo
dell'olio di lino divenne più generale nel XVI secolo.
Il periodo in cui gli olii furono usati per la prima volta nei dipinti è abbastanza
sconosciuto. L'olio di lino era ben conosciuto dagli antichi egiziani, poiché il lino veniva
fatto crescere per la sua filatura in tessuto, ma in accordo con Lucas non c'è un'evidenza
che l'olio fosse mai stato usato per dipingere. Ugualmente sebbene gli oli di noce e di
papavero erano conosciuti nell'epoca classica greca e romana , non c'è menzione del
loro utilizzo nella pittura.
Gli scritti di Teofilo del XII secolo, sono il primo riferimento dell'utilizzo dell'olio per
stemperare i colori, ma ancora prima, nel sesto secolo, uno scrittore medico chiamato
Ezio ha menzionato l'olio siccativo come vernice per finire i dipinti. Eastlake ha
focalizzato l'attenzione sui Close Rolls (registri delle spese reali) per l'acquisto di grandi
quantità di olio da pittori doveva essere usato per il lavoro sulla decorazione della
cappella di Santo Stefano, una parte del palazzo di Westminster, nel XIV secolo e i
dipinti infatti si è trovato che sono eseguiti con pitture ad olio. Molti antichi lavori in
arte norvegese, comprese le pale d'altare e le sculture policrome, sono anch'esse dipinti
con olio, probabilmente di lino. Altri oli siccativi sono stati prodotti da alberi e piante
native di altre parti del mondo e alcune hanno una lunga storia di utilizzo locale. Quindi
gli oli di perilla e canapa sono entrambi menzionati in un documento giapponese
dell'883. L'olio di perilla è stato probabilmente il tipo utilizzato nell'antica (VIII secolo)
tecnica di pittura ad olio in Giappone, nella quale veniva incorporato piombo come
essiccante. L'olio di Chia dai semi di salvia hispanica è stato usato come legante di
pittura in Messico durante il periodo coloniale spagnolo.
Alcuni oli esotici come il Tung ( olio dei legno della Cina), perilla e Oiticica sono stati
prodotti su larga scala per un utilizzo commerciale nel XX secolo. Altri oli, come i semi
del tabacco, sono una recente introduzione, come lo è l'utilizzo di oli naturali modificati
come l'olio di ricino disidratato.
Meccanismo di essiccamento.
La graduale conversione di un olio liquido attraverso uno stato di gel morbido ad una
forma solida gommosa avviene come risultato di una reazione a catena di radicali liberi.
Poiché gli oli sono miscele di composti, il loro essiccamento non è spiegabile in termini
di un semplice ed uniforme schema di reazione come può essere la polimerizzazione di
un monomero puro come l'acetato di vinile. Ciò che può essere indicato sono i tipi di
reazioni che possono avvenire e i tipi di legame che si formano; anche le reazioni
competitive di ossidazione che avvengono e che sono in natura degradative e portano
alla produzione di molecole piccole. In pratica esistono anche fattori che influenzano
25
l'andamento della reazione di essiccamento, come l'influenza della luce, la presenza di
differenti ioni metallici dai pigmenti, lo spessore del film e inoltre la disponibilità di
ossigeno, e l'estensione della pre-polimerizzazione dell'olio.
I legami tra carbonio e idrogeno sono molto forti e una elevata energia deve essere
trasmessa alla molecola per poterli rompere. La quantità di energia richiesta, l'energia di
dissociazione del legame, dipende dalla struttura della molecola nel suo insieme, ma in
particolar modo dall'intorno molecolare più vicino del legame in questione. Esso
diminuisce quanto più l’atomo di carbonio che ha un legame con l'idrogeno, possiede
legami con altri atomi di carbonio piuttosto che con altri idrogeni; cioè a dire (vedi
1.1.1) quando l'idrogeno è terziario piuttosto che secondario o primario. Quindi per il
metano, CH3-H, l'energia è di 102 kcal, per gli idrogeni primari come nell'etano
CH3CH2-H è di 98, per gli idrogeni secondari, come nell'isopropano (CH3)2CH-H, è di
94, (CH3)3C-H, è di 90. Queste sono tuttavia energie elevate e ciò significa che la rottura
del legame di questi composti avvengono solo a temperature molto elevate.
In prossimità dei doppi legami risulta anche un abbassamento dell'energia di
dissociazione del legame: scende a 77 kcal per il propilene, CH 2=CHCH2-H. Valori
ancora più bassi si ottengono dagli atomi di idrogeno situati sul gruppo metilenico tra
due doppi legami coniugati, sebbene le cifre esatte sembra non siano disponibili. Questo
è il caso degli acidi grassi insaturi con cui noi abbiamo a che fare, acido linoleico e
linolenico, il primo con uno, il secondo con due gruppi metilenici.
Il primo passo nel processo di essiccamento si pensa generalmente che sia l'estrazione di
un atomo di idrogeno dalla sua posizione per portare a un radicale libero:
Come questa estrazione avvenga inizialmente è ancora una questione aperta; ci sono
molti possibili modi. Comunque come essa continua sembra abbastanza chiaro per i
radicali reattivi che vengono formati e che ne determineranno lo svolgimento, come
vedremo di seguito. Il radicale sopra è stabilizzato dalla delocalizzazione o risonanza,
che si comporta come se fosse una miscela o un ibrido del radicale scritto sopra con due
radicali riarrangiati con i doppi legami coniugati:
e
26
Questi radicali liberi sono molto reattivi e per loro sono possibili diverse possibilità di
reazione. La più favorita è la reazione con l'ossigeno dell'aria, se esso è facilmente
disponibile, per portare a radicali intermedi di perossidi:
Questi a turno possono estrarre un atomo di idrogeno da un'altra molecola di acido
insaturo (propagando così la reazione) per dare gli idroperossidi:
Queste reazioni propagate a catena non risultano però unire insieme le unità dei
trigliceridi. Questo può avvenire in diversi modi. I radicali perossidici possono, invece
di estrarre l'idrogeno, addizionarsi al sistema di doppi legami, specialmente di doppi
legami coniugati:
Per dare un dimero legato attraverso un gruppo perossidico, il nuovo radicale, in grado
di riarrangiare e/o reagire ulteriormente, lo apre in varie modalità possibili. Allo stesso
modo, può avvenire un’addizione simile ai doppi legami con i radicali alcossidici,
prodotti per
27
Omolisi degli idroperossidi e perossidi, per portare al dimero formato da un singolo
ossigeno (etere) che fa da ponte di legame.
Può anche avvenire una polimerizzazione poiché i radicali carbonici, formati, come
spiegato sopra, possono addizionare direttamente i doppi legami nello stesso modo come
alchilperossidi radicale o alchilossi radicale
Il nuovo radicale formato va avanti a reagire nello stesso o in altri modi. Non si creda
che ognuna di queste reazioni di formazione di legami va avanti per produrre catene
polimeri molto lunghe che invece si formano nella regolare polimerizzazione dei
monomeri vinilici, ma non è necessario che essi debbano farlo per la produzione del
polimero tridimensionale a rete, come spieghiamo in seguito. Le reazioni a catena
vengono terminate per formazione di prodotti non radicali, ugualmente per reazione tra
due radicali, come:
oppure occasionalmente, mediante ossidazione dei radicali carbonilici a ioni carbonio
con ioni di metalli di transizione nel film, lo ione quindi perde un protone per riformare
un doppio legame:
Le proporzioni relative dei tre tipi di legami prodotti, carbonio-carbonio, etere e
perossido, non sono conosciute. Esse varieranno con le condizioni e non rimarranno mai
costanti. I legami carbonio-carbonio ed esterei sono probabilmente stabili rispetto ai
28
legami perossidici, che possono convertirsi in due alcossi-radicali e reagire
ulteriormente come spiegato sopra.
Le reazioni sopradescritte sono state discusse in termini di acidi grassi singoli ed è stato
detto che i legami che si sviluppano raramente procedono oltre il punto di formazione di
dimeri o possibilmente trimeri. Chiaramente se fossero coinvolti i singoli acidi essi non
potrebbero infatti mai condurre a una rete con legami incrociati in tre dimensioni: ma
non sono gli acidi singoli ad essere coinvolti, bensì i trigliceridi e ciascun trigliceride ha
due o tre acidi grassi insaturi su ciascuna molecola.
Quindi dopo la formazione di un dimero trigliceride usando una catena di acido grasso
da ciascuna molecola, il dimero manterrà ancora da 2 a 4 catene di acido grasso insaturo
rimanenti per continuare il processo di polimerizzazione.
Se due di questi dimeri quindi si legano insieme per dare un tetramero allora questo avrà
tra 2 e 6 catene di acidi grassi insaturi rimanenti, ed esso, per esempio, sarà almeno
altrettanto bene, o anche meglio attrezzato a continuare il processo di dimerizzazione. E
questo discorso presume solo la dimerizzazione: se le reazioni a catena fossero più
lunghe, procedendo con tre o quattro stadi, allora il risultato sarebbe anche più
favorevole per lo sviluppo di una rete altamente ramificata.
Fattori che influenzano il processo di essiccamento.
La precedente descrizione del meccanismo di essiccamento è semplificata e lascia fuori
molte possibilità per lo più non spiegate, in particolare rimangono incerti i meccanismi
di iniziazione della reazione a catena.
È noto che certi oli come il Tung contengono alte proporzioni di acidi con doppi legami
coniugati, essi seccano molto più rapidamente di quelli come l'olio di lino, in cui i doppi
legami sono inizialmente non coniugati. Le ragioni per questo sono incerte. Può
significare:
che la polimerizzazione può essere iniziata da un diretto attacco dell'ossigeno sui
doppi legami coniugati;
che i radicali liberi sono più facilmente formati da essi, mediati forse da ioni
metallici di transizione;
oppure è possibile che specie attivate siano formate per assorbimento della luce (i
dieni e i trieni coniugati assorbono nel vicino ultravioletto).
Tutte queste cause hanno i loro sostenitori. Esse non possono essere considerate in
dettaglio qui, la questione degli effetti dei pigmenti deve però almeno essere toccata.
Nella storia della pittura fu presto scoperto che gli oli seccavano più rapidamente in
presenza di certi pigmenti piuttosto che di altri. Gli effetti potevano non essere
semplicemente di una maggiore velocità di essiccamento, certi pigmenti base servono a
raccogliere i prodotti di ossidazione acidi a basso peso molecolare, la cui presenza può
altrimenti ammorbidire il film essiccato (un effetto conosciuto come sineresi:
29
separazione spontanea di un liquido da un gel o da una sospensione colloidale dovuta
alla contrazione del gel). L'aumento della velocità di essiccamento si trova
principalmente con composti dei metalli capaci di esistere in più di uno stato di valenza.
Il cobalto, il manganese e il piombo sono considerati essere i più attivi in questo ordine.
I loro composti che sono solubili in olio come il loro naftenati, resinati o i loro sali con
acidi grassi a lunga catena, sono spesso addizionati a pitture ad olio commerciali o
vernici per favorire l'essiccamento. I pigmenti tradizionali degli artisti non sono solubili
in grande quantità nel legante olio naturalmente (con alcune eccezioni), ogni effetto per
favorire l'essiccamento che essi hanno deve presumibilmente partire dall'interfaccia
pigmento legante. Le reazioni che possono avvenire sono semplificate dai seguenti
schemi:
La prima equazione mostra una tipica reazione con idroperossido che avviene facilmente
a temperatura ambiente. Lo ione cobaltico è ridotto a cobaltoso, convertendo
l'idroperossido in idroperossido radicale e un protone. Questo sistema è spesso utilizzato
per favorire la polimerizzazione di certi monomeri, essendo l'idroperossido così
chiamato iniziatore, il cobalto o un il sale di un altro metallo in soluzione, il promotore.
Nella seconda equazione lo ione cobaltoso è ri-ossidato di nuovo a ione cobaltico
dall'ossigeno atmosferico, e viene prodotto un radicale ione ossigeno. A questo punto
facilmente reagisce con lo ione idrogeno, come nella terza equazione, per dare un
radicale libero perossido che può anche iniziare le reazioni a catena. Queste non sono le
sole possibili vie di reazione, lo ione cobaltoso può anche favorire la decomposizione
dell' idroperossido in un modo differente, quindi:
Questa reazione, insieme con la prima delle tre viste sopra, fornisce un meccanismo
redox (riduzione-ossidazione) che favorisce la polimerizzazione di un sistema chiuso
senza l'intervento dell'ossigeno. Un'altra possibilità è la diretta ossidazione dei gruppi
metilenici adiacenti o tra doppi legami come segue:
30
Reazioni come queste hanno grandi vantaggi di requisiti energetici rispetto quelle che
comportano l'omolisi in due radicali.
Alcuni ioni metallici possono agire come terminatori di catena. È stato osservato spesso
che film di pittura contenenti pigmenti verdi di rame, in particolar modo verdigris
(acetato basico di rame, Pb(CH3COO)2.Pb(OH)2), contengono una quantità maggiore di
composti insaturi come per esempio acido oleico rispetto ad altre pellicole pittoriche
dello stesso periodo contenenti altri pigmenti. Il meccanismo di interruzione della catena
in questo caso si crede che sia l'ossidazione del singolo elettrone del carbonio radicale a
ione carbonio, seguito dalla perdita di un protone adiacente alla catena per ridare un
doppio legame:
Allo stesso modo questi composti di rame sembrano non ritardare in alcun modo il
processo di essiccamento. Chiaramente ci sono sottigliezze che qui non sono ancora
state capite.
Il vermiglione pigmento rosso (solfuro di mercurio) ha un effetto di notevole
accelerazione sulla degradazione ossidativa dell'olio essiccato. Questo probabilmente
spiega la maggiore vulnerabilità verso deboli solventi di pulitura spesso notata nelle
zone dipinte a vermiglione nei dipinti antichi.
Antiossidanti ed inibitori.
Non sono solamente i materiali inorganici che possono influenzare il corso o la velocità
di essiccamento. Alcune classi di composti chimici, in particolare fenolici, sono in grado
di reagire con i perossi o alcossi radicali formati nel processo di essiccamento, per dare
arilossi radicali piuttosto stabili che finiscono per dimerizzare o piuttosto essere ossidati
dall'ossigeno a chinoni.
Le reazioni a catena dei radicali liberi che portano all'essiccamento (o ad altre reazioni
di auto ossidazione) sono quindi effettivamente stoppate, almeno finché tutti i fenoli
presenti non vengono utilizzati.
Composti di questo tipo sono conosciuti come inibitori o antiossidanti (discussi più
avanti nella sezione 11.2.1) e sono di grande importanza industriale essendo aggiunti a
molti prodotti per fermare o rallentare la degradazione ossidativa. Vari tipi di fenoli sono
comuni componenti minori di prodotti naturali di cui si servono come naturali
antiossidante. Il periodo di ritardo iniziale nell'inizio dell'essiccamento degli oli
31
siccativi si pensa sia dovuto alla presenza di questi, e in particolare il gruppo di composti
conosciuti come tocoferoli (vitamina E).
I fenoli sono presenti nei catrami, in certi altri materiali che sono prodotti di pirolisi, e
questa è la probabile ragione per la scarsa capacità essiccativa dei film pittorici
contenenti carbone nero come pigmento come anche terre bituminose, come i bruni di
Vandyck.
Processi di ossidazione a che portano a piccole molecole.
Alcune delle reazioni che avvengono durante l'essiccamento non portano a legami
incrociati, ma alla rottura del legame e alla formazione di prodotti di degradazione a
basso peso molecolare.
Il principale modo con cui questo avviene è attraverso un percorso alternativo della
reazione degli intermedi idroperossidici. Alchilossi radicali, prodotti dagli idroperossidi
nei modi descritti, possono rompersi invece di addizionarsi ai doppi legami o estrarre
idrogeno ad altre molecole:
I prodotti sono un'aldeide e un radicale alchilico. Il radicale può andare a reagire con
l'ossigeno o addizionarsi ai doppi legami: l'aldeide generalmente viene ulteriormente
ossidata ad acido carbossilico. Se R rappresenta il gliceroestere finale di una molecola di
acido grasso, allora il risultante acido è ancora attaccato a questa come metà dell'estere
dell'acido carbossilico. Se rappresenta l'idrossicarbonio finale della catena dell'acido
grasso, allora il prodotto è un acido monocarbossilico libero. La lunghezza della catena
di questi possibili prodotti dipende dall'esatta posizione dei gruppi idroperossidici sulla
catena di acido grasso C18. Generalmente è in qualche punto più o meno nel mezzo, e
conseguentemente i maggiori prodotti sono mezzi esteri dell'acido dicarbossilico C9,
acida azelaico e i composti C8 e C10, con anche piccole quantità di composti a catena
più corta.
32
Il più abbondante acido monocarbossilico prodotto è anche il composto C9, sebbene si
siano trovati nei film di oli invecchiati quantità molto minori di questo e di altri acidi
monocarbossilici rispetto agli acidi dicarbossilici.
Ingiallimento delle pellicole ad olio.
Le pellicole pittoriche formate da alcuni oli siccativi ingialliscono più di altre,
specialmente quando tenute al buio ed è noto che gli oli con un alto contenuto di acido
linolenico sono particolarmente soggetti a questo processo. Diverse strutture chimiche
sono state suggerite come i possibili i contributi a questo colore giallo, compresi i
chetoni e i sali di metalli di forme enoliche come queste:
È stato ugualmente focalizzato che questi sono dei gruppi di cromofori abbastanza
deboli (un cromoforo è un gruppo che assorbe nel visibile o dell'ultravioletto) e tali
composti dovrebbero essere presenti in grandi quantità per produrre l'intensità del colore
osservato.
Un suggerimento alternativo fu che l'ingiallimento al buio è una reazione superficiale
che ha bisogno della presenza di tracce di ammoniaca, o forse di altre ammine, presenti
nell'atmosfera dando origine alla formazione di composti contenenti nuclei pirrolici. Il
pirrolo stesso è incolore, ma facilmente dà prodotti scuri di auto-ossidazione di struttura
incerta.
Sono stati suggeriti altri possibili cromofori che possono dare un colore giallo per
esempio strutture chinoidi, che possono derivare dalla condensazione di due molecole di
di-chetone: la reazione di ingiallimento è lenta, mentre il seguente sbiancamento, per riesposizione alla luce, avviene molto rapidamente.
33
Il ciclo di ingiallimento seguito dallo sbiancamento può essere ripetuto un certo numero
di volte. Alcuni studi suggerirono che l'estensione dell'ingiallimento diminuiva ogni
volta, ma un lavoro più recente ha indicato che l'inscurimento e la suscettibilità allo
sbancamento non sono una funzione dell'età della pellicola pittorica e/o della sua storia
di inscurimento e sbancamento. Reazioni di ingiallimento ugualmente sembrano il
risultato dell'interazione delle proteine (attendibilmente danno luogo ad ammine) con oli
siccativi auto-ossidanti, e di conseguenza sono particolarmente responsabili di avvenire
con leganti emulsionati di proteine/olio.
Prepolimerizzati o stand oil.
Gli oli siccativi possono essere trattati in vari modi per produrre materiali nei quali i
legami che legano insieme i trigliceridi sono già parzialmente realizzati prima che l'olio
sia utilizzato.
Il prodotto è naturalmente più viscoso rispetto agli oli grezzi, da cui viene il nome di oli
addensati e olio a corpo. La natura delle reazioni che avvengono dipende se
l'addensamento è portato avanti in presenza o in assenza di aria. Nel primo caso le
reazioni che avvengono sono essenzialmente le stesse di quelle che avvengono
nell'essiccamento di un film di olio, ma quando gli oli sono resi densi per calore in
assenza di aria, che è il metodo usuale per preparare oggi gli stand oil, allora avvengono
altri tipi di reazione.
Da tempo è stato proposto che le reazioni di dimerizzazione che avvengono sono di tipo
Diels-Alder è ciò sembra essere stato confermato recentemente. Una reazione di DielsAlder avviene tra un diene coniugato è un composto con una doppio legame singolo per
dare un composto ciclico:
34
Perché ciò avvenga con l'acido linolenico o linoleico è necessaria prima la reazione di
isomerizzazione dei doppi legami non coniugati per dare un diene coniugato. Questo
avviene semplicemente riscaldando l'olio, ma è un processo lento e probabilmente con
uno stadio che controlla la velocità.
La formazione di prodotti di- e talvolta trimerici aumenta grandemente durante il
periodo di riscaldamento: in alcuni esperimenti sulla formazione di stand Oil riscaldando
olio di lino a 300 gradi in atmosfera di azoto è stato trovato che dopo sei ore l'olio
conteneva circa il 49% di gliceridi polimerici, dopo 6,5 ore il 57% e dopo sette ore
l'84%. Le viscosità corrispondenti erano 33, 73, e 210 pois rispettivamente.
Come può essere visto, il prodotto di dimerizzazione contiene un singolo doppio legame
e quindi potrebbe andare avanti a reagire ulteriormente con un diene per dare un trimero
sebbene di fatto l'evidenza è che poco di questo viene formato. Si sa che in aggiunta alla
formazione del dimero, acidi monomerici ciclici vengono formati riscaldando gli oli
siccativi in vari condizioni.
Mentre la maggior parte del lavoro sperimentale sulla formazione di queste specie è
stata condotta usando condizioni alcaline, che promuovevano l’isomerizzazione, essi
anche sono conosciuti per essere formati con il solo calore. Il precursore dei monomeri
ciclici è un acido trienoico coniugato, e infatti si notò che nell'olio tung riscaldato, è
formato dall'acido elaeostearico coniugato. La reazione avviene mediante una reazione
così chiamata elettrociclica:
Dove X+Y =10. La posizione del gruppo dienico nei prodotti, che può essere
inizialmente come mostrata, può spostarsi. In circa il 55% del prodotto proveniente
dall'olio di lino X è 2 e Y è 8.
Il destino di questi acidi ciclizzati non è stato determinato con precisione, ma quasi
certamente essi vengono incorporati nella rete del polimero, forse prima attraverso la
partecipazione nella reazione di dimerizzazione dì Diels-Alder. Certamente essi non
sembra siano rilevabili, dopo saponificazione, nei film bene essiccati.
Essiccamento degli stand Oil.
Gli stand Oil seccano più lentamente degli oli grezzi e con assorbimento di molto meno
ossigeno. Quindi l'olio di lino grezzo può assorbire circa il 10 o il 12% di ossigeno in
35
peso, in confronto con il 3% per gli oli riscaldati. La predominanza del legame carboniocarbonio rispetto ai legami carbonio-ossigeno nel polimero risultante è probabilmente
responsabile della migliore qualità di durabilità del film formato..
Altri vantaggi degli stand Oil provengono dai minori cambiamenti di volume
nell'essiccamento (risultano così meno raggrinzimenti) e la minore tendenza
all'ingiallimento (dovuta alla riduzione del contenuto di acido linolenico).
Componenti minori negli oli e nei grassi.
In aggiunta ai trigliceridi, gli oli e grassi generalmente contengono una piccola
proporzione, generalmente meno dell'1% dei cosiddetti composti neutri non
saponificabili, che non reagiscono con gli alcali per dare saponi solubili in acqua.
Attenzione particolare è stata data all'identificazione di queste specie in questi ultimi
anni ed esse sono state proposte anche come una possibile chiave di identificazione dei
differenti oli. Comunque, tranne nel caso dei grassi delle uova, essi sono presenti in
quantità così piccola da non avere un particolare significato, sia per influenzare le
proprietà dell'olio, sia come sostanze identificative nelle analisi, almeno nei casi di
piccoli campioni di oli essiccati.
Le sostanze non saponificabili degli oli di semi sono generalmente miscele molto
complesse contenenti alcoli triterpenici (8.3.1), metil steroli e steroli. Immancabilmente
presente, e generalmente in grande quantità è il sitosterolo.
sitosterolo
36
Lo sterolo colesterolo è generalmente trovato soltanto in piccole quantità insignificanti,
per questo è lo sterolo caratteristico degli animali. E' presente in grandi quantità nel
rosso del uovo, che lo rende un interessante oggetto di discussione della composizione di
questo materiale complesso.
colesterolo
La composizione del uovo, in termini generali di gruppi chimici, è mostrata in tabella
3.3.
Le proteine saranno discusse in una parte specifica. I lipidi i sono fatti di trigliceridi
(circa 65%), fosfolipidi (circa 29%) e colesterolo (circa 5.2%). Il colesterolo è quindi
presente in quantità di circa lo 0.5% dell'intera composizione dell'uovo, 1.5% nel rosso
dell'uovo, o ancora come 2.5% dell'intero uovo solido essiccato. E questa è una grande
quantità se confrontata con il contenuto di qualsiasi sterolo in un olio vegetale e la sua
determinazione in pittura indica la presenza dell'uovo.
La natura dei fosfolipidi deve essere brevemente spiegata. Essi sono in effetti trigliceridi
nei quali uno dei gruppi esterei degli acidi grassi è sostituito da un gruppo fosfato, cioè a
dire un'estere con l'acido fosforico. Poiché l'acido fosforico è tribasico, esso può a turno,
essere ulteriormente combinato con vari composti. Quando viene così esterificato un con
la base forte azotata colina, il composto risultante è uno dei composti del gruppo
chiamato lecitine, le forme idratate e disidratate delle lecitine (con un gruppo fosfato
in una posizione primaria del trigliceride ) sono scritte di solito così:
37
Composti come questi sono solo costituenti molto minori della maggior parte degli oli
vegetali e sono in gran parte rimossi durante procedure di lavaggio o di altre lavorazioni.
Una quantità sostanziale nel rosso dell' uovo significa, comunque, che questo ha una
quantità di fosforo significativa, circa 0.5% in peso, equivalente a circa 0.9% dell'intero
uovo disidratato. A causa di ciò, test per il fosforo elementare sono stati alla base per la
determinazione dell' uovo nei leganti pittorici da alcuni ricercatori in passato, ma questo
metodo non è molto affidabile a causa anche delle possibili altre sorgenti dell'elemento
(da pigmenti) La composizione di acido grasso nel rosso dell'uovo (dalla combinazione
con i trigliceridi e fosfati) è inclusa nella tabella 3.2.
38
Prodotti contenenti o derivati dagli acidi grassi e acidi grassi
Vernici.
Fino all'avvento dei materiali sintetici negli anni '40 e negli anni '50, le vernice ad olio
erano il materiale standard per la copertura interna ed esterna di manufatti in legno, ed
anche di oggetti fatti di altri materiali compresi i metalli. Esse furono anche usate come
vernici per i dipinti fino allo sviluppo della distillazione, e la preparazione di olio di
trementina (8.1.1), permise l'introduzione di vernici a spirito contenenti una piccola
quantità o completamente prive di olio.
Sopravvivono pochissime evidenze per l'uso di vernici ad olio nei dipinti antichi, poiché
la maggior parte con il passare del tempo è stata sostituita, durante le pulitura per la
conservazione. In ogni caso, una piccola zona di vernice trovata su un dipinto italiano
del XIV secolo ha mostrato come tale vernice fosse composta da olio bollito e resina di
Sandracca, e molto probabilmente era quella applicata originariamente. L'indicatore
trovato qui di pre-polimerizzazione mediante riscaldamento è stato una percentuale
relativa di acidi suberico e azelaico (per esempio degli acidi dicarbossilici da C8 a C9 )
negli oli essiccati.
Acido suberico
acido azelaico
Proporzioni molto maggiori del primo sono stati trovati per gli oli trattati piuttosto che
per quelli non trattati.
Ricette antiche per le vernici ad olio sono qualche volta così complesse da essere
impraticabili e improbabili. In ogni caso comunque le ricette generalmente prevedevano
una combinazione di resina dura (con cui si intendeva un copale africano o Kauri o un
materiale simile) con olio caldo bollito e disidratato. Il tutto era quindi diluito con olio
di trementina. Le seguenti due ricette dal “Manuale per il pittore dei colori, degli oli e
delle vernici” di Hurst esemplificherà ultima procedura descritta. Le quantità devono
essere convertite in percentuali di peso dalle misure originali in pound e galloni ed
occorre ignorare le possibili perdite in peso per flusso delle resine e per bollitura
dell'olio. Come può essere visto esse contengono un'alta percentuale di olio rispetto alla
resina.
Vernice elastica per carrozze.
Resina ("Animé" o copale) 10%
Olio di lino 29%
Solfato di zinco 0.15%
39
Litargiro (monossido di piombo,) 0.3%
Acetato di piombo 0.15%
Olio di trementina 60%
Vernice chiara di quercia.
Resina 9%
Olio 35%
Solfato ferroso 0.3%
Acetato di piombo 0.3%
Litargiro 0.3%
Oli di trementina 55%
La procedura di fabbricazione della vernice era in primo luogo di fondere, o far fluire la
resina per riscaldamento a circa 330 °C e mantenerla a questa temperatura per mezz'ora
circa. Nel frattempo l'olio veniva separatamente riscaldato a circa 260 gradi centigradi e
quindi aggiunto alla resina fusa con una agitazione vigorosa. Gli essiccanti venivano
quindi aggiunti alla vernice bollita per diverse ore, fino a che diventava fibrosa, cioè
quando una piccola quantità messa tra due dita si allunga a filamento quando le due dita
vengono allontanate tra di loro. Dopo aver permesso il suo raffreddamento in qualche
modo la miscela veniva diluita con trementina.
L'espressione "bollire" si riferisce ad una ebollizione lieve e apparente che in realtà
consisteva nella fuoriuscita di prodotti di decomposizione volatili dall'olio e dalla resina,
prodotti sia per processi di ossidazione che di pirolisi. Dopo la sua preparazione la
vernice veniva fatta riposare, o invecchiare, per il tempo necessario, affinché una certa
parte di materiale insolubile poteva depositarsi sul fondo. Questi materiali
probabilmente includevano alcuni siccativi addizionati, che non venivano sempre
disciolti completamente. Le vernici sopradescritte si dice che fossero molto veloci ad
essiccare: alcune si diceva che seccavano in cinque ore in estate.
Sebbene l'uso di resine dure è stato sempre affermato da autori del XIX secolo e dei
primi anni del XX secolo, come Hurst, che sostenevano fossero necessarie per la
realizzazione di vernici migliori e più durature, essi stessi concedevano che, la resina di
pino, molto più economica (colofonia o pece greca) sarebbe potuta essere stata usata con
un certo successo per vernici cotte per uso interno. Si può però sospettare che, in pratica,
non si resisteva alla tentazione di sostituirla, almeno in parte nelle ricette antiche,
infatti, come in una traduzione di Teofilo, la resina di pino era un ingrediente
comunemente usato.
La diffusione con cui le vernici ad olio furono utilizzate come legante nelle pitture è
ancora materia di dubbio, poiché la determinazione analitica e la stima delle resine, in
particolar modo quelle denominate dure o resine polimerizzate, in una vernice olio
resina essiccata, è un compito difficile, come verrà discusso successivamente nella
sezione 8.3.6 e 12.1.5.
40
Comunque sono stati trovati una certa quantità di tracce di resina di pino all'interno di un
legante pittorico e quando queste sono combinate con l'indicazioni che l'olio
componente è stato pre-polimerizzato mediante riscaldamento (come discusso prima)
allora è ragionevole sospettare un legante olio-vernice.
Inchiostri di stampe.
Il legante per l'inchiostro per stampe è stato tradizionalmente la vernice litografica, che è
in realtà solo un altro nome per indicare olio bollito. L'olio di lino è stato praticamente
l'unico ad essere usato fino a questo secolo. La preparazione spesso comportava la reale
infiammazione dell'olio, che veniva lasciato bruciare per un po' di tempo. Naturalmente
questo dava un prodotto molto scuro, ma questo non aveva conseguenza perché il nero
carbone in qualche forma (generalmente nero fumo di lampada) veniva in ogni caso
addizionando come pigmento. Generalmente veniva anche incorporata qualche resina,
probabilmente resina di pino.
Nel XIX secolo varie peci e catrami cominciarono anche ad essere addizionati agli
inchiostri per applicazioni più economiche, come anche prodotti del petrolio come
diluenti. Attualmente ai giorni nostri gli inchiostri per stampa, che includono inchiostri
colorati, generalmente possiedono componenti dall'intera gamma di resine sintetiche e
semi sintetiche ed altri materiali che sono ora disponibili.
Inchiostri utilizzati per i giornali su carta molto assorbente spesso non seccano, nel senso
di polimerizzare, ma sono semplicemente assorbiti nelle fibre del tessuto di carta e
perdono il solvente per evaporazione.
Linoleum ed altri rivestimenti in olio.
Il materiale di copertura dei pavimenti è chiamato Linoleum e, come dice il nome, è un
prodotto dell'olio di lino. La prima industria di Linoleum fu costruita Inghilterra nel
1864 ed il materiale divenne la copertura flessibile per pavimenti dominante fino a che i
prodotti vinilici non lo sostituirono negli anni ‘50 e ‘60. Essenzialmente esso consiste in
tre componenti: il legante organico; la carica inorganica (pigmenti e preparazione
calcarea); e una carica organica (preparazione di sughero e di farina di legno). Il legante
era fatto da olio bollito seccato lavorato in un certo modo e quindi fatto fluire con circa
un quarto di tonnellata del suo peso di resina, generalmente colofonia, ma qualche volta
resine più costose come la kauri.
I rivestimenti in olio sono di due tipi. In uno il tessuto viene impegnato con olio
siccativo non pigmentato che viene quindi lasciato seccare. Tali materiali sono stati
largamente utilizzati fino a tempi abbastanza recenti per fare cappelli impermeabili,
ombrelli (specialmente in Giappone) e simili. Nel secondo tipo di rivestimenti ad olio un
lato del tessuto è coperto con rivestimento continuo di olio pigmentato, essenzialmente
pittura, per dare una superficie lavabile, e tali materiali sono stati usati come coperture
41
per tavoli, scaffali, eccetera, i rivestimenti dipinti per pavimenti del XVIII e XIX secolo
in Inghilterra e America (i precursori del Linoleum) consistevano in diversi strati di
spessa pittura a olio su forti sostegni di tela (spesso tele per vela) ed erano sia lisce che
modellabili.
Stucco da vetrario e plasilina.
......................................................................................
I saponi.
I saponi sono sali di acidi grassi a lunga catena. Il materiale generalmente conosciuto
come sapore è in particolar modo il sale di sodio o potassio nelle proporzioni in cui essi
sono presenti nel grasso da cui il sapone proviene. Trattamenti di grassi con alcali
acquosi danno saponi solubili e glicerolo:
I saponi, o almeno le soluzioni di saponi, apparentemente erano conosciute sin
dall'antichità, poiché il processo di saponificazione poteva essere eseguito, sebbene
molto lentamente, con carbonato di potassio lisciviato dalle ceneri della lana.
Le lavandaie usavano le ceneri di legni dolci, le mescolavano con acqua, e le filtravano con
tele o sacchi dopo aver fatto decantare le impurezze. Poiché le ceneri sono ricche di
carbonati, silicati, solfati (oltre che di cloruri e fosfati) di metalli alcalini ed alcalinoterrosi le lavandaie eseguendo questa “lisciviazione” non facevano altro che estrarre dalle
ceneri i sali alcalini solubili. L’azione detergente delle acque da loro utilizzate era,
dunque dovuta alla loro “alcalinità” e alla presenza di sostanze che si comportavano
(anche se in modo più blando) come gli additivi che si aggiungono oggi ai
moderni detersivi (ad es. agenti antiridepositanti dello sporco).
L’ origine del sapone vero e proprio non si conosce con precisione anche se la tecnologia
per fabbricarlo era nota fin dall’antichità. Le liscivie alcaline ottenute da cenere di legno
venivano, infatti, utilizzate per la saponificazione di sego o di scarti di grassi animali o di
oli vegetali.
Già nel 600 a.C. i Fenici riuscivano ad ottenere un materiale cagliato bollendo grasso di
capra con estratti di legno di frassino. Gli Egizi invece mescolavano un alcali con un olio
ottenendo una specie di sapone.
I Romani infine usavano liscivie potassiche per ottenere sapone da grassi animali (quali ad
esempio il grasso di capra). Questi precursori dei saponi erano in realtà degli impiastri
42
usati soprattutto come cosmetici.
L’uso del sapone a scopo detersivo, infatti, cominciò a diffondersi soltanto nel
diciottesimo secolo. C’è da notare comunque alla base della loro produzione c’era la stessa
La fabbricazione del sapone raggiunse un elevato grado di sviluppo nel XVIII secolo,
ma non fu prima del primo XIX secolo che il suo uso divenne comune con la produzione
di soda caustica a buon mercato con il processo di LeBlanc.
Chemistry
The Leblanc process was a batch process in which sodium chloride was subjected to a series of
treatments, eventually producing sodium carbonate. In the first step, the sodium chloride was
heated with sulfuric acid to produce sodium sulfate (called the salt cake) and hydrochloric acid
gas according to the chemical equation
2 NaCl + H2SO4 → Na2SO4 + 2 HCl
This chemical reaction had been discovered in 1772 by the Swedish chemist Carl Wilhelm
Scheele. Leblanc's contribution was the second step, in which the salt cake was mixed with
crushed limestone (calcium carbonate) and coal and fired. In the ensuing chemical reaction, the
coal (carbon) was oxidized to carbon dioxide, reducing the sulfate to sulfide and leaving behind a
solid mixture of sodium carbonate and calcium sulfide, called black ash.
Na2SO4 + CaCO3 + 2 C → Na2CO3 + CaS + 2 CO2
Because sodium carbonate is soluble in water, but neither calcium carbonate nor calcium sulfide
is, the soda ash was then separated from the black ash by washing it with water. The wash water
was then evaporated to yield solid sodium carbonate. This extraction process was termed
lixiviation.
Process detail
The sodium chloride is initially mixed with sulfuric acid solution and the mixture exposed to low
heat. Much of the hydrogen chloride gas (and virtually all of the economically recoverable HCl
gas) escapes at this point. This continues until all that is left is a fused mass. This mass still
contains enough chloride to contaminate the later stages of the process. The mass is then
exposed to direct flame, which evaporates nearly all of the remaining chloride. [4]
The coal used in the next step must be low in nitrogen to avoid the formation of cyanide. The
calcium carbonate, in the form of limestone or chalk, should be low in magnesia and silica. The
weight ratio of the charge is 2:2:1 of salt cake, calcium carbonate, and carbon respectively. It is
fired in a reverberatory furnace at about 1000°C.[5]
The black-ash product of firing must be lixiviated right away to prevent oxidation of sulfides back
to sulfate.[5] In the lixiviation process, the black-ash is completely covered in water, again to
prevent oxidation. To optimize the leaching of soluble material, the lixiviation is done in cascaded
stages. That is, pure water is used on the black-ash that has been already been through prior
stages. The liquor from that stage is used to leach an earlier stage of the black-ash, and so on. [5]
The final liquor is treated by blowing carbon dioxide through it. This precipitates dissolved
calcium and other impurities. It also volatilizes the sulfide, which is carried off as H 2S gas. Any
residual sulfide can be subsequently precipitated by adding zinc hydroxide. The liquor is
separated from the precipitate and evaporated using waste heat from the reverberatory furnace.
The resulting ash is then redissolved into concentrated solution in hot water. Solids that fail to
dissolve are separated. The solution is then cooled to recrystallize nearly pure sodium carbonate
decahydrate.[5]
43
Molti saponi metallici, come quelli di calcio e di magnesio, sono insolubili in acqua e
così precipitano quando il sapone viene usato in acqua dura, che contiene sali disciolti di
questi metalli, con conseguente perdita della loro proprietà di detergenti. L'effetto
detergente del sapone, in comune con quello di altri detergenti, ha molti aspetti, ma è
dovuto in pratica al fatto che la molecola è sia idrofobica che idrofilica.
Come tutti sali, i saponi di sodio e di potassio sono ionizzati in soluzione acquosa. Di
conseguenza ad ogni interfaccia tra acqua e materiale non popolare immiscibile le
molecole si orientano esse stesse con lo ione carbossilato nella fase acquosa e la lunga
catena idrocarburica degli acidi grassi dentro o verso il materiale non polare. Questo
forma un legame tra le due fasi che risulta in una facile emulsione o sospensione di uno
nell'altro.
Acidi grassi liberi: stearina
Gli acidi grassi liberi sono stati prodotti in commercio già nei primi anni del XIX secolo,
perché hanno diversi utilizzi. Essi sono formati quando i saponi vengono acidificati, ma
un processo più economico è la diretta idrolisi dei grassi con acqua. Questo può avvenire
a pressione atmosferica in presenza di acido e certi altri catalizzatori (processo di
Twitchell) o, con differenti catalizzatori, ad elevate temperature (260 °C) che può
avvenire sotto pressione. Il prodotto è naturalmente una miscela di acidi nelle
proporzioni in cui essi sono presenti nel grasso. Come citato prima, gli acidi insaturi C18
tendono ad essere liquidi a temperatura ambiente, e per ottenere gli acidi solidi saturi
mischiati (C16 e C18) conosciuti come stearina o cera liquida stearinica
prevalentemente insaturi, gli acidi sono sparati fuori i sotto pressione.
La cera stearinica, in un certo senso, è ancora un importante ingrediente di certi tipi di
candele, particolarmente quelle usate nelle chiese. Essa quindi può esser considerata
come ingrediente delle sculture a cera o dei modelli in cera, sia perché addizionata
volutamente o perché le candele venivano usate come sorgenti della cera.
Essenzialmente identica alla cera stearinica, sebbene in proporzioni differenti di
componenti, sono la adipocere e il burro delle paludi, discussi prima.
Analisi degli oli e dei grassi.
Sufficienti esempi sono già stati dati in questo capitolo per rendere evidente che il
rilevamento e l'identificazione dei materiali grassi fa molto affidamento sull’analisi
qualitativa e quantitativa dei componenti degli acidi grassi, e che l'unica strada
praticabile nel fare ciò, è mediante gascromatografia. L'applicazione di questa a leganti
pittorici risale a 30 anni fa e più recentemente è stata ampiamente discussa e adottata.
44
Essa viene considerata nel suo aspetto pratico in dettaglio nel capitolo 12. GLC è stata
anche un'applicazione per lo studio dei componenti estraibili con solventi delle pellicole
pittoriche ad olio, che consistono di trigliceridi non polimerizzati, acidi grassi liberi e
prodotti di ossidazione a basso peso molecolare. Fioriture deturpanti, analoghe a quelle
incontrate sugli oggetti discussi prima, qualche volta si manifestano su dipinti, in
particolar modo in quelli del XX secolo, e spesso si è trovato che consistono in acidi
grassi liberi. I lavori degli artisti, che hanno mischiato elaborate miscele di leganti
invece di usare direttamente pitture a olio, sono particolarmente soggette a questi difetti.
L'essudato bianco semi cristallino di alcuni dipinti di Mark Rotko è stato trovato
mediante GLC che consisteva in acido palmitico, acido stearico e un plastificante, bis
(2-etilesil)adipato.
Apparentemente l'artista usa un'emulsione ad hoc composta di pittura ad olio, uova,
vernice dammar. Gli acidi grassi chiaramente sono derivati dall'idrolisi dei trigliceridi
saturi dei grassi dell'uovo; il plastificante dal copolimero acrilico che è stato anche
utilizzato come legante nell'impiego.
Un simile fenomeno fu notato con un numero di dipinti di Serge Poliakoff, il legante qui
erano acidi grassi liberi in gran quantità, e in parte saponi di acidi grassi.
Una chiara spiegazione, in termini di composizione originale del legante, non era
disponibile in questo caso. Risultati non pubblicati su un simile caso mostrarono che
questo artista aveva usato un'emulsione di uovo e olio come legante, e questo è stato
supportato da aneddoti che riguardavano il suo modo di dipingere. Queste analisi tutte
hanno comportato la GLC di derivati di acidi grassi che seguivano la saponificazione del
materiale grasso. Potrebbe anche essere che in futuro sarà data più attenzione all'analisi
dei grassi non saponificabili, poiché adesso è possibile separare acidi grassi, mono e digliceridi come anche trigliceridi non carichi tutti insieme, in una sola corsa, ad una
45
opportuna temperatura elevata. Residui grassi archeologici sono stati così analizzati,
gruppi acidi carbossilici ed idroperossidici del campione dopo essere stati prima
trasformati in esteri trimetilsilici (TMS) ed esteri derivati per trattamento con N,Obis(trimetilsilil)trifluoroacetammideammide. Usando colonne capillare al quarzo come
un rivestimento di fase fissa di dimetilepolisilossano (BP-1) programmata fino a 350 °C,
tutti questi gruppi di composti sono stati ben separati, i trigliceridi sono apparsi alla fine
di un periodo a temperatura costante.
46
Scaricare