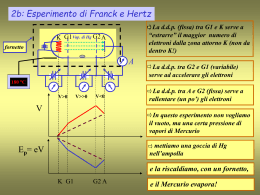
Dalla Fisica Classica alla Fisica Moderna Alla fine del 1800, con le Equazioni Elettromagnetiche Fondamentali, tutti i fenomeni Fisici, anche quelli più complessi (la luce come onda elettromagnetica) sembravano risolti; restavano però alcuni aspetti apparentemente marginali………. 1) Dalla teoria elettromagnetica risulta un valore finito della velocità della luce; cosa succede se un corpo si avvicina o supera quella velocità? 2) Scaldando un gas in una cavità si modifica la distribuzione delle velocità delle particelle ed anche la distribuzione spettrale della luce emessa si modifica; che relazione esiste tra i due fenomeni? 3) Quando un raggio di luce colpisce una superficie metallica si può avere emissione di elettroni; il fenomeno è legato alla frequenza della luce, perché? 4) Il modello dell’atomo con nucleo centrale carico positivamente ed elettroni ruotanti nello spazio circostante è incompatibile con la teoria elettromagnetica; come si può elaborare un diverso modello, compatibile? Relatività ristretta 1) Dalla teoria elettromagnetica risulta un valore finito della velocità della luce; cosa succede se un corpo si avvicina o supera quella velocità? Secondo la fisica classica : dv dt la massa non dipende dalla velocità . F ma m Secondo la teoria della relatività : m(v ) m0 2 , v c2 ove m0 è detta massa a riposo 1 Quando un corpo si muove la sua massa cambia ed aumenta e raggiungerebbe un valore infinito alla velocità della luce. Il lavoro che viene fatto per aumentare la velocità si esprime anche come aumento di massa: esiste una equivalenza massaenergia. E mc 2 Teoria del Corpo nero 2) Scaldando un gas in una cavità si modifica la distribuzione delle velocità delle particelle ed anche la distribuzione spettrale della luce emessa si modifica; esiste una relazione tra i due fenomeni? Intensità T1 T2 T T3 T1 N T2 T3 Frequenza Energia E’ possibile descrivere il fenomeno della cavità radiante utilizzando lo stesso metodo impiegato per la teoria cinetica dei gas? No! Quantizzazione dell’energia Una descrizione coerente della emissione di radiazione elettromagnetica da parte di gas surriscaldato è possibile solo ipotizzando una “Quantizzazione dell’Energia”: L’onda elettromagnetica è costituita da un insieme di “Fotoni” di energia h (Max Plank) il cui numero è proporzionale all’Intensità L’onda elettromagnetica può essere descritta come fenomeno “ondulatorio” o “corpuscolare”. L’Effetto Fotoelettrico 3) Quando un raggio di luce colpisce una superficie metallica si può avere emissione di elettroni; il fenomeno è legato alla frequenza della luce, perché? I I E cin ? V ? fc Frequenza fc Frequenza Risposta di Einstein: Il raggio luminoso è composto di fotoni che interagiscono singolarmente con gli elettroni del materiale; si ha fotoemissione solo se l’energia h del fotone è superiore all’energia di legame dell’elettrone. h è la costante di Plank: 6.63 10-34 J.s In caso di fotoemissione l’energia del fotone non spesa per compensare l’energia di legame è acquisita come energia cinetica dell’elettrone, che quindi aumenta con la frequenza della luce incidente. L’ Atomo La crisi dei modelli dell’atomo (1) 4) Le nuove esperienze mettono in crisi il “modello” atomico Modello atomico (J.J.Thomson) era basto su tre assunti derivanti dalla osservazione empirica. 1) L’atomo è la particella elementare costituente le specie chimiche (tavola periodica); 2) La materia è neutra, ma esistono cariche positive e negative. 3) La materia è compatta Atomo Massa Carica Materia La crisi dei modelli dell’atomo (2) Cosa ci si aspetta facendo collidere particelle α accelerate su una lamina d’oro? Nessuna particella è la può attraversare Conteggi Rivelatore ? Schermo Posizione Esperimento: alcune particelle attraversano la materia senza essere deviate. L’atomo ha una struttura diversa da quella ipotizzata! Modello di atomo con spazi “vuoti” Elettroni Modello di Rutherford Nucleo Problema: gli elettroni ruotanti attorno al nucleo hanno un moto accelerato: secondo le leggi dell’elettromagnetismo dovrebbero irradiare energia, perdere velocità e ricadere sul nucleo! Lo spettro a righe dell’Idrogeno L’atomo più semplice è quello dell’Idrogeno: osservando la radiazione emessa da Idrogeno surriscaldato si vede che sono presenti solo frequenze specifiche: Il nuovo modello atomico deve spiegare anche questo! Intensità Gas H2 Frequenza Il modello atomico proposto da Bohr 1° Postulato: L’atomo ha una struttura con nucleo centrale positivo ed elettroni ruotanti su orbite circolari non radiative (stati stazionari); 2° Postulato: si ha emissione di energia sotto forma di onda elettromagnetica quando un elettrone passa da uno stato stazionario più esterno ad uno più interno; la frequenza dell’onda emessa è proporzionale al dislivello energetico; 3° Postulato: i raggi delle orbite permesse sono tali che il momento angolare dell’elettrone è multiplo intero di h/2 R e- Nell’atomo di H non eccitato: E=-13.6 eV Ei Ef h h mvR n 2 Orbite ellittiche, principio di esclusione e di indeterminazione - La conservazione e la quantizzazione del momento angolare valgono anche per le orbite ellittiche (A. Sommerfeld). - Gli atomi con maggior numero atomico dovrebbero essere più piccoli, perché si ha una maggiore forza sugli elettroni. Questo non avviene perché su ogni stato stazionario possono stare solo due elettroni, con spin opposto (W.Pauli) - Non è possibile conoscere esattamente e simultaneamente la posizione e l’energia dell’elettrone (Principio di indeterminazione di Heisenberg): gli stati stazionari vengono descritti da funzioni matematiche che esprimono la probabilità di trovare l’elettrone in una porzione dello spazio atomico (orbitale). Fenomeni “Atomici” Ora che ne sappiamo di più su come è fatto l’atomo, cerchiamo di spiegare i fenomeni correlati La “Luce” come onda elettromagnetica Radiofrequenze 5 6 7 8 9 10 5.2 5.7 Lontano Vicino IR IR Microonde 12 11 13 UV 14 15 6.4 7.1 x 1014 Hz UV nel vuoto 16 Raggi X, raggi g 17 18 19 105Hz Viola Blu 5800 5300 4700 4200 Verde 6200 Giallo 7000 Arancione l Rosso log 4.8 4.3 Angstrom 20 Assorbimento della luce ( legge di Lambert- Beer) I I 0 e εcd I I0 d I T I0 Trasmittanza ln T c d Assorbanza ln I I0 ε c d =Coeff. Ass. Molare c=Concentrazione d=Cammino ottico (l ) ossiemoglobina emoglobina l L’assorbimento è selettivo e corrisponde ai fotoni con energia pari ad un salto quantico tra livelli energetici: si può determinare la concentrazione di una data sostanza in soluzione. Produzione di fotoni (emissione di luce) n E h E i E f Atomo h Spettro a righe n Molecola h Materia n Banda di conduzione Banda di valenza Spettro continuo h Produzione di fotoni per accelerazione di particelle cariche q F qE Forza Elettrica B h q v F qv B Forza Magnetica Produzione dei Raggi X Rx mA kV Radiazione Caratteristica h Ein E fin n h Radiazione di frenamento h f (r, v, z) n lmin l N() Spettro energetico dei Raggi X Rad. Frenamento Rad. Caratteristica E=h N() Spettro del Fascio Rx Emergente E=h eVmax (keV) Emissione stimolata della luce Livello Eccitato E h=E Livello Base Emissione “Stimolata” Fotoni “Coerenti”: stessa energia, stessa direzione, stessa fase Light Amplification by Stimulated Emission of Radiation Emissione stimolata Pompaggio Inversione di popolazione HV Gas Specchio Raggio LASER Specchio Gli effetti della luce coerente dipendono da intensità e frequenza: per ottenere frequenze che favoriscano effetti particolari (infrarosso per interagire con l’emoglobina e coagulare, ultravioletto per vaporizzare) si usano gas molecolari con molti livelli energetici. In particolare si usano molecole formate da due unità (dimeri) per produrre l’ultravioletto (luce fredda), (laser a dimeri eccitati: “eccimeri”) Impiego del LASER Luce non coerente Luce Coerente I I Il Nucleo Atomico Il nucleo atomico Il modello atomico proposto da Bohr, con le integrazioni di Sommerfeld e Pauli, spiega la maggior parte dei fenomeni che non potevano essere descritti con i metodi della Fisica classica (non quantistica). Restano aperti due problemi: a) Tutta la carica positiva è concentrata nel nucleo; come sono compensate le intense forze di repulsione elettrica? ++++ + + + + - b) Alcuni materiali emettono particelle con carica negativa certamente provenienti dal nucleo; come è possibile che questo avvenga? Il Difetto di Massa La risposta al quesito sulla repulsione elettrica tra le cariche positive del nucleo venne da misure della massa atomica effettuate con lo spettrometro di massa: -le misure dimostrano una “quantizzazione della massa nucleare” -confrontando massa e carica, il nucleo risulta formato da particelle cariche (+) e neutre -La massa del nucleo misurata non corrisponde alla massa calcolata come somma della masse delle particelle costituenti: risulta un “difetto di massa” Difetto di massa (energia di legame) per nucleone MeV + + + 8 7 6 5 4 3 2 1 20 60 A Il difetto di massa può essere giustificato, in base alla teoria relativistica (E=mc2) come energia di legame del nucleo. Ne consegue l’esistenza di forze nucleari. Forza Nucleare Confrontando l’energia nucleare di legame, per nucleone (78 Mev), con l’energia di legame degli elettroni orbitali ( eV keV), si evidenzia la presenza di “Forze Nucleari” di altissima intensità, che compensano la repulsione elettrica e mantengono il nucleo compatto. 10-15 m Dimensioni dell’atomo e del nucleo 10-10 m Se il nucleo avesse le dimensioni di 1 m, l’atomo avrebbe le dimensioni di 100000 m, cioè 100 km. Il Nucleo Atomico Acceleratore di particelle + + + + + + + + I Nuclei Ogni nucleo viene definito dalla propria massa e dalla propria carica: 1. la MASSA consiste nel numero totale di particelle nucleari (n. nucleoni = protoni + neutroni) e indicato come NUMERO DI MASSA A 2. la CARICA consiste nel numero di protoni presenti e indicato come NUMERO ATOMICO Z A Z X Fissione Nucleare 137 52Te n 235 U 95 236 U 95 n Tellurio n 97 40 Zr Zirconio n + frammento di fissione 235 1 U 92 0n 236 92 U 200 MeV n + frammento di fissione 235 grammi di uranio contengono il Numero di Avogadro di atomi; 235 grammi di uranio possono produrre, per fissione, NA·200MeV di energia = = 6.021023 ·200 =12.04·1025 MeV Un grammo di uranio produce 5.12·1023 MeV =8.2·1010 J Una tonnellata di carbone produce 3.0 ·1010 J Un grammo di uranio produce la stessa energia di 2.7 Tonnellate di Carbone !!!!!!!! PROBLEMA DELLA FISSIONE: difficoltà nel controllare il processo e produzione di nuclei radioattivi Fusione Nucleare Unendo nuclei leggeri, si ottiene un nucleo con maggiore numero di massa e maggiore energia di legame per nucleone (più stabile). Nel processo di fusione si ha emissione di energia. 2 1 2 1 H 12H 23H e 01n H 2.014740U .M . A. 3 2 1 0 H e 3.016986U .M . A. n 1.008986U .M . A. Nel processo di fusione dei due nuclei di deuterio, per formare un nucleo di elio si ha la diminuzione di 0.03508 U.M.A. corrispondenti a 3.26 MeV di energia prodotta. Fusione Nucleare 2 2 3 H H 1 1 2 He n 3.26MeV 2 2 3 1 H H H 1 1 1 1 p 4.05MeV 2 3 4 H H 1 1 2 He n 17.58MeV Per fondere, i due nuclei devono avvicinarsi in modo che le forze nucleari compattino i nucleoni in un’unica struttura. Le forze repulsive elettriche si oppongono all’avvicinamento, che può avvenire solo se i due nuclei hanno una elevatissima Energia Cinetica (temperatura di decine di milioni di gradi). Questa reazione può avvenire a (solo!) 40 milioni di gradi Il vantaggio della fusione nucleare è rappresentato dalla assoluta mancanza di isotopi radioattivi a lunga vita. La Radioattività Radioattività Z > 82 n>p 4 2 A Z X Y A 4 Z 2 4 2 Energia cinetica di emissione = 2-5MeV, massa = 4U.M.A., carica =2e- - A Z X Y A Z 1 Neutroni in eccesso: uno di essi si trasforma in protone emettendo un elettrone (-); non tutti i - non hanno la stessa energia (si associa quindi al fenomeno anche la produzione di un antineutrino) p>n + A Z X Z A1Y Protoni in eccesso: uno di essi si trasforma in neutrone emettendo un positrone (+). In questo caso si associa al fenomeno anche la produzione di un neutrino Emissione g g 4 2 A seguito di una emissione o il nucleo può venirsi a trovare in uno stato energetico “eccitato” e si riporta allo stato di base mediante emissione di radiazione elettromagnetica (Radiazione g) N + + + Spettro g g h Ogni elemento radioattivo ha un suo spettro g caratteristico Decadimento radioattivo Mat. Radioattivo N(t) Decadimento Mat. inerte dN (t ) l N (t ) Attività [dis/s= Bequerel)] dt N0 N (t ) N 0 e lt N0/2 Legge del decadimento Radioattivo λ = prob. che un atomo decada in un s = cost. radioattiva dell’elemento T1/2 t T1/2=0.693/λ = emivita Decadimento radioattivo Ogni materiale radioattivo è caratterizzato dal tipo di particella e radiazione che emette, dall’energia della particella o radiazione, dall’attività specifica (attività per unità di massa), dal tempo di dimezzamento (o emivita). Per terapia radiante con fasci esterni si usano: Radio 226 Energia fotoni 0.83 MeV emivita 1622 anni attività 0.98 Ci/gr Cesio 137 Energia fotoni 0.66 MeV emivita 30 anni Cobalto 60 Energia fotoni 1.17 MeV emivita 5.5 anni attività 200 Ci/gr attività 50 Ci/gr Interazione particelle-materia 4 2 Quando interagisce con gli atomi del mezzo c’è attrazione elettrostatica che provoca ionizzazioni a causa dell’elevata carica positiva delle particelle . N P Quando la particella - interagisce con gli elettroni del mezzo subendo forti repulsioni e cambiamenti di direzione e con i nuclei accelerando ed emettendo raggi X. + P N Quando la particella + si trova in vicinanza di un elettrone del mezzo si annichila con questo, cioè trasformano la loro massa in due fotoni di energia 511keV che si muovono nella stessa direzione ma in versi opposti Interazione particelle-materia ed effetto biologico Una ionizzazione 10 eV E = 1 MeV = 100.000 ionizazioni Cellula Azione biochimica Effetto biologico Radiazione Radicali liberi Alterazione funzione g
Scaricare