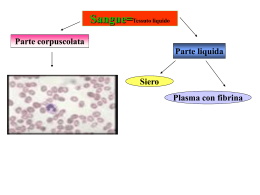
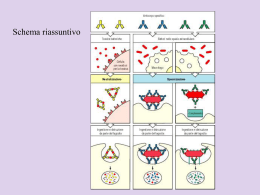
Immunodeficienze e malattie autoimmuni: due mondi contrapposti? Chiara Azzari Dipartimento di Pediatria Università di Firenze Ospedale Pediatrico Universitario A.Meyer Jeffrey Modell Center for Immunodeficiencies FIRENZE BG, femmina, anamnesi ndn per polmonite 11 mesi: Ricovero Non leucocitosi Non neutrofilia BP virale Rx: flogosi interstiziale Sfebbrata, dimessa con tosse sonnolenza, febbre, iporeattiva Mai cessata la tosse Esami: non leucocitosi, non neutrofilia Ricerca su liquor: Enterovirus (positivo in PCR) Recupero neurologico non rapido (7gg) ma completo Durante il ricovero il quadro respiratorio è altalenante, momenti di franco distress respiratorio Esami immunologici I livello Emocromo: Linfociti: Neutrofili: RBC,PLT: Esami immunologici II livello GB 6900 Sottopopolazioni linfocitarie 51% 3519/mm3 CD3 (T) : 52% (vn: 55-80) 40% OK Immunoglobuline: ndn IgG: 1170 mg/dl IgA: 76 mg/dl IgM: 82 mg/dl CD4: CD8: val.ass= 493/mm3 14 % (vn: 30-50) 35% (vn: 14-38) CD19 (B): 39% (vn: 6-25) CD3-16+56+: 8% (vn: 5-25) (NK) Dopo 15 gg: anti MPR positivi, anti-DT negativi anti HBs negativi Troppe cose: CD4 bassi BP a lenta risoluzione Difetto di produzione anticorpale Ulteriori approfondimenti Lavaggio broncoalveolare: Immunoglobuline: Normali come numero, alterata produzione di acp specifici acp anti DT assenti acp anti MPRV presenti Troppi autoanticorpi CD4: Bassi (ma con valore assoluto ancora compatibile con infezione) accertamenti immunologici più approfonditi Terapia come ad immunodepresso (antibiotico, antimicotico, antivirale + Bactrim) I linfociti sono capaci di rispondere agli antigeni? Quanti linfociti vengono “sfornati” dal timo? Transitorio(post-infettivo) o congenito? V V1 V2 V3 V4 D J J1 J2 J3 J4 … TREC V DJ E’ un recettore transmembrana Sta sulla superficie dei T Riconosce gli antigeni presentati all’interno dell’HLA V D V1 V2 V3 V4 50 20 zone Va (Variable) zone Vb (Variable) J J1 J2 J3 J4 … 100 Da (Diversity) 35 Db (Diversity) 50 13 zone Ja (Joint) zone Jb (Joint) V DJ V D V1 V2 V3 V4 J J1 J2 J3 J4 … Step 1: Vengono casualmente eliminati segmenti D; Si forma un legame DJ (ad un J casuale) Step 2: Vengono casualmente eliminati segmenti V e il J non legato; Step 3: Si forma il VDJ completo V DJ Totocalcio: 3 risultati (1-2-X) per 13 partite porta una possibilità 13 di risultati di 3 =1.594.323 Nel TCR con 70 V, oltre 100 D, 33 J abbiamo una probabilità di combinazioni di oltre 109 (un miliardo) La formazione del TCR (ricombinazione VDJ) avviene per caso La probabilità che si formi un TCR specifico per un virus (es.CMV) è la stessa che si formi un TCR specifico per un antigene self (es. tiroide) Dobbiamo quindi eliminare tutti quei linfociti che casualmente hanno un recettore che riconosce il self Il linfocita T immaturo passa nel al timo Il timo è la vera scuola dei linfociti T Nel timo i linfociti imparano a riconoscere tutti gli antigeni self Antigeni espressi nel timo Nel timo sono espressi tutti gli antigeni self del nostro organismo. In quella sede il linfocita T può riconoscerli L’espressione degli atg self nel timo è regolata dalla proteina AIRE I linfociti immaturi che incontrano un antigene nel timo sono indotti all’apoptosi (morte programmata) I linfociti residui possono andare incontro a proliferazione Se il timo funziona bene, la “selezione” alla nascita è già stata fatta Un linfocita con TCR specifico per un antigene self incontra l’antigene nel tessuto linfocita in apoptosi Se non sono presenti segnali di infiammazione provenienti dall’immunità innata il legame linfocitatessuto porta il linfocita all’apoptosi Tolleranza periferica indotta da linfociti T regolatori (alcuni sono CD8,altri CD4 CD25 e Foxp3, altre si differenziano da tipi a funzione suppressor come TR1, Th3,CD8+CD28-, e quelle ristrette per Qa-1 (HLA-E per la specie umana). Vignali, Nature Immunology, 2008 Come il linfocita T, anche il B viene spinto all’apoptosi Al contatto con l’antigene self, il linfocita B esprimerà sulla superficie la molecola CXCR5. Il CXCR5 impedirà per sempre al linfocita di rientrare in un follicolo linfatico, dove avrebbe potuto produrre autoanticorpi Quanto sono rari i difetti congeniti dell’immunità? Patologia Frequenza per 105 Artrite reumatoide 1000 Diabete tipo I 200 Sclerosi multipla 60 LES 40 Immunodeficienza comune variabile Sclerodermia 8 (=1:12.500) 1 S.del22 (1:6000) Helen Chapel, ESID 2008 SM, Femmina, aa. 10 Storia di Broncopolmonite a lenta risoluzione Otiti ricorrenti nell’ultimo anno Anamnesi familiare Genitori viventi. La madre ha uveite la zia materna ha tiroidite Il padre ha m.di Crohn Anamnesi patologica remota Niente di notevole fino a 4 anni. Normale numero di infezioni respiratorie vie aeree superiori A 4 e 5 anni 2 episodi di piastrinopenia diagnosticata come porpora trombocitopenia idiopatica Anamnesi patologica prossima A 10 anni febbre, dolore toracico. Terapia antibiotica domiciliare per sospetta BP. A novembre, cessata la febbre, persiste dolore toracico e tosse produttiva. Fini rantoli base dx Tosse produttiva Esami (IgG, IgA, IgM) Terapia antibiotica: amoxi + clavulanico DH immunologia DH immunologia Emocromo: GB: 8.450/mm3 Neutrofili: 68.2 % Linfociti : 24.4 % Immunoglobuline IgG: 245 mg/dl IgA: < 6 mg/dl IgM: 21 mg/dl vn: 650-1400 mg/dl vn: 70-140 mg/dl vn: 70-120 mg/dl DH immunologia Sottopopolazioni linfocitarie CD19 : 12 % CD3 : 74 % VN:6-25 VN: 55-80 CD4 : 43 % VN: 30-50 CD8 : 27 % VN: 14-38 CD16-56 (NK) : 13 % VN: 5-25 CD4/8 : 1.6 VN: 1.3-2.7 CD40 Ligando: nella norma Diagnosi La ipo–g-globulinemia e il difetto non numerico ma solo funzionale dei linfociti permette di ipotizzare una Immunodeficienza comune variabile Se ha cominciato ad avere infezioni “da grande”…. Soprattutto se nella sua storia c’è “qualcosa di autoimmune” Ed anche se la patologia autoimmune è nella famiglia… Pensiamo ad un difetto immunitario tipo Immunodeficienza comune variabile Caratteristiche cliniche Infezioni ricorrenti sinusali e polmonari (soprattutto polmonite batterica) Anche otiti Mastoiditi Caratteristiche cliniche Malattie autoimmuni Anemia emolitica Trombocitopenia Artrite Malattie gastrointestinali, (malassorbimento) Vitiligine Parotidite (o altre salivari) Le malattie autoimmuni sono più frequenti nei pazienti con CVID e nei loro familiari 20-25% dei CVID alla diagnosi o dopo hanno almeno una manifestazione autoimmune Manifestazioni gastrointestinali nella CVID Sono presenti in oltre il 20% dei pazienti ! ! Malassorbimento con Steatorrea Deficit di vitamina B12 e folati Deficit di Calcio e ferro Intolleranza al lattosio Difetto di disaccaridasi Enteropatia proteino-disperdente Anormalità dell’architettura dei villi MANIFESTAZIONI CLINICHE ASSOCIATE •Tumori Linfoma non Hodgkin (300 volte superiore) Tumori gastroenterici (soprattutto K gastrico) (50 volte superiore) TERAPIA •Terapia sostitutiva con Ig e.v. o mg/Kg/mese sottocute 400 Scopo: mantenere livelli sierici > 500 mg/dl •Fisioterapia respiratoria con PEP mask (maschera a pressione espiratoria positiva) Per evitare l’accumulo di secrezioni e non peggiorare la situazione bronchiectasica •Terapia antibiotica A cicli? Profilassi continua? (solo dopo Pn. Carinii) Nessuna terapia? TERAPIA •Vaccini Non sono indicati i vaccini vivi OK a tutti i vaccini uccisi. Da consigliare in particolare: anti-influenzale, anti-pneumo e anti-meningo La presenza di autoimmunità è più frequente in tutti quelle immunodeficienze dove il difetto principale è dei linfociti T Difetto di linfociti B DifettoBruton, di linfociti B (m.di X-linked) Immunodeficienza comune variabile (B+T) Anticorpi molto bassi o assenti Anticorpi molto bassi o assenti Di solito si manifesta nel primo anno di vita Di solito si manifesta dopo i 10 anni Gravi infezioni Gravi infezioni NON autoimmunità Frequente autoimmunità M.N. 3aa e 5 mm alla nascita intervento per malformazione cardiaca (tetralogia di Fallot) Infezioni recidivanti delle alte e basse vie respiratorie Emocromo: nella norma Ig frazionate: nella norma esegue studio delle sottopopolazioni linfocitarie M.N. 3aa e 5 mm Sottopopolazioni linfocitarie (%) CD3 (T) 40 (VN=55-80) CD4 24 (VN=30-50) CD8 14 CD19 (B) 26 (VN=6-25) CD16-56 31 (VN=5-25) Ipotesi diagnostica: sindrome di Di George (22q11 del) dismorfismi malformazione cardiaca malformzioni scheletriche ipocalcemia ritardo mentale e/o del linguaggio I.D. con ridotti livelli di CD3 e CD4 Conferma genetica:delezione 22q11.2 Facies tipica della sindrome di Di George Ipertelorismo Taglio antimongoloide degli occhi Micrognatia, bocca a carpa Orecchie prominenti con impianto basso Ugula bifida, alterazioni del palato Facies tipica della sindrome di Di George Ipertelorismo Bocca a carpa Micrognatia Taglio antimongoloide degli occhi Disturbi neuropsichiatrici nella 22q11del Difetto di attenzione depressione Stati d’ansia Disturbi psicotici transitori (1/2 dei pazienti) Anormali comportamenti sociali Emozionalità alterata Schizofrenia (doppia dei controlli) Niklasson L, Genet Med 2001; 3 (1): 79-84 Baker KD, Br J Psychiatry 2005; 186, 115-120 Debbane M, Schizophr Res 2006; 84 (2-3): 187-93 Gothelf D, Am J Psychiatry 2007; 164 (4): 663-9 Il rischio di malattie autoimmuni è più elevato nei pazienti con sindrome di Tison BE, JACI 2011 Di George Il rischio di autoimmunità è più elevato in pazienti con minor numero di cellule Tison BE, JACI 2011 CD4 naive M.N. 3aa e 5 mm Terapia: profilassi antibiotica sulla base del numero dei CD4 Terapia chirurgica e farmacologica della cardiopatia Terapia/profilassi per ipocalcemia (calcio + vit.D) Logopedia FT per difetti scheletrici FT respiratoria (cardiopatia, infezioni polmonari) Sostegno scolastico per il ritardo psicomotorio Monitoraggio di patologie autoimmuni ANA: anticorpi anti nucleo Presenti in molte malattie autoimmuni Non specifici per una singola malattia LES Sclerodermia Sjogren Malattia mista del connettivo Polimiosite/Dermatomiosite Artrite reumatoide Cosa sapere degli ANA nella pratica clinica? Un titolo di ANA <1:160 è normalmente aspecifico Un titolo ANA elevato richiede solo attesa se asintomatico. Gli ANA possono manifestarsi molto prima che la malattia dia segno di sé Un’altra informazione: il pattern Gli ANA si leggono in immunofluorescenza al microscopio, il microscopista descrive un “pattern” Un pattern omogeneo è tipico (non esclusivo) del LES o artrite reumatoide Un pattern punteggiato (fine o grossolano) si trova in LES, Sjogren, MCTD, RA, scleroderma Il pattern centromerico è tipico della sindrome CREST C=calcinosi R=raynaud E=ipomotilità esofagea S=sclerodattilia T=telangiectasia Il pattern nucleolare è tipico della sclerodermia e di alcune forme di Raynaud Quali test fare se troviamo gli ANA positivi? 1)il titolo ANA (quasi tutti i laboratori lo fanno spontaneamente 2)anti DNA a doppia elica (dsDNA) (70% dei LES, occasionalmente in AR o Sjogren) 3) ENA (antigeni nucleari estraibili ) Il titolo ANA dil. 1:2 1:160 dil. 1:2 1:320 dil. 1:2 1:640 dil. 1:2 1:1280 1:2560 Il passaggio da una diluizione a quella immediatamente adiacente può essere ininfluente ENA Malattia U1-RNP Malattia mista del connettivo (100% LES (30-40%) Sm LES (20-30%), altamente specifico SSA-Ro Sjogren (60-75%) LES (40-50%) Lupus neonatale (100%) Lupus forme cutanee (100%) SSB-La Sjogren (10-40%) LES (6-15%) Lupus neonatale (90%) Lupus forme cutanee (25-35%) Scl-70 Sclerodermia (forma diffusa: 25%) Jo-1 Polimiosite-dermatomiosite Nato a termine, ndn A 4 mesi: ricovero per grave diarrea acquosa, disidratazione, eczema esteso a volto, tronco ed arti (dermatite?) anemia e piastrinopenia Trattamento: Supporto per disidratazione Eczema (simil atopico) Diarrea grave e protratta Sospetto di IPEX Anemia emolitica Piastrinopenia IgE elevate Immunodisregolazione Poliendocrinopatia Enteropatia X-linked • Malattia genetica autoimmune rara • dovuta a mutazioni del gene FOXP3 • Disregolazione immunologica con poliendocrinopatia autoimmune ed enteropatia, trasmissione legata al cromosoma X • Incidenza non chiara, sottostimata • esordio precoce , elevata mortalità Manifestazioni cliniche principali • Esordio: nascita o prima infanzia (rari casi ad esordio tardivo), maschi • enteropatia (diarrea intrattabile acquosa o con perdite ematiche e mucose) fino a malassorbimento e ritardo di crescita (biopsia intestinale : severa atrofia dei villi con infiltrato linfocitario nella sottomucosa e/o nella lamina propria) • endocrinopatie: DM I ad esordio neonatale, anomalie della tiroide su base autoimmune • malattie cutanee: eczema (eritrodermia, dermatite psoriasiforme, orticaria, pemfigoide nodulare, alopecia) Trattamento • Precocemente aggressivo • Terapia steroidea: d’attacco e associata a immunosoppressore • Terapia immunosoppressiva: spesso multipla ciclosporina o tacrolimus (iniziale remissione, possibile aumento del rischio delle infezioni) • Rapamicina (immunosoppressore con meccanismo con vantaggio selettivo sulle Treg favorendone l’espansione e la sopravvivenza) • Terapia immunosoppressiva e trapianto di cellule staminali ematopoietiche Un caso clinico…. Fabio: 5 anni Storia recente di polmonite grave Il PdF richiede esami GB: nella norma IgG: assenti IgA: assenti IgM: assenti La presenza di autoimmunità è più frequente in tutti quelle immunodeficienze dove il difetto principale è dei linfociti T Difetto di linfociti B DifettoBruton, di linfociti B (m.di X-linked) Immunodeficienza comune variabile (B+T) Anticorpi molto bassi o assenti Anticorpi molto bassi o assenti Di solito si manifesta nel primo anno di vita Di solito si manifesta dopo i 10 anni Gravi infezioni Gravi infezioni NON autoimmunità Frequente autoimmunità Esame obiettivo Peso e altezza: 10° centile (in linea col bersaglio genetico) Sviluppo neuromotorio nella norma Psoriasi ungueale Alopecia completa delle sopracciglia Esami “storici”: IgG < 2 DS già a 12 mesi IgG= 90 mg/dl (VN 480 mg/dl) IgA=assenti IgM=assenti L’associazione immunodeficienza ed autoimmunità è tutt’altro che rara La presenza di autoimmunità è più frequente nelle ID con difetto di linfociti T La patogenesi dell’associazione sta in un difetto della tolleranza centrale (timo) e periferica (cellule T e B regolatorie) IL sospetto clinico è più importante di qualunque esame! c.azzari @meyer.it c.canessa @meyer.it f.lippi @meyer.it Division of Pediatric Immunology University of Florence and A.Meyer Children’s Hospital Jeffrey Modell Center for Immunodeficiencies
Scaricare