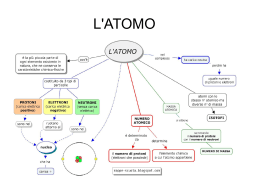
La struttura dell’atomo ed i legami chimici Indice generale sulla struttura dell’atomo A • Cos’è la materia B • La struttura dell’atomo B1 • Un modello su come è fatto l’atomo B2 • Il numero atomico e la tavola periodica degli elementi B3 • I livelli di energia degli elettroni B4 • Isotopi e numero di massa C • Metalli e non metalli; i legami chimici C1 • Metalli e non metalli C2 • Legame ionico C3 • Legame covalente C4 • Legame metallico Che cos’è la materia Cos’è la materia La materia è tutto ciò che ci circonda, che occupa uno spazio ed ha una sua massa Sostanze semplici o elementi Le sostanze di cui la materia è costituita possono essere: Sostanze composte o composti Negli elementi, le molecole sono formate da atomi dello stesso tipo Nei composti, le molecole sono formate da atomi di tipo diverso Qualsiasi elemento è costituito da tante particelle elementari dette atomi Due o più atomi, legandosi tra loro, secondo leggi ben precise, formano le molecole La struttura dell’Atomo • B1 Un modello su come è fatto l’atomo • B2 Il numero atomico e la tavola periodica degli elementi B3 • I livelli di energia degli elettroni • B4 Isotopi e numero di massa Un modello su come è fatto l’atomo In passato gli atomi sono stati considerati le particelle più piccole della materia. Si riteneva che essi non potessero essere divisi in particelle ancora più piccole (la parola atomo significa “Indivisibile”) Oggi sappiamo invece che l’atomo è formato da una parte centrale, il nucleo, circondato da elettroni che ruotano attorno ad esso. Protoni (particelle relativamente grosse che hanno carica elettrica positiva) Oggi si sa che l’atomo è formato dalle seguenti particelle: Elettroni (particelle molto 2000 volte più piccole dei protoni; hanno carica elettrica negativa) + p+ - e- Neutroni (particelle grosse come i protoni; ma che non hanno nessuna carica elettrica) I Protoni ed i neutroni si trovano nel nucleo dell’atomo mentre gli elettroni vi girano attorno - + n L’atomo non presenta normalmente carica elettrica e per questo si definisce neutro. In questo caso il numero di protoni è uguale al numero di elettroni (ricorda le regole della somma algebrica) - - + 1 1 0 + - + 22 0 Vedremo che il numero dei neutroni può essere diverso Gli elettroni ruotano attorno al nucleo in “orbite” fisse - - Nella prima “orbita” ci stanno al massimo 2 elettroni; - nelle altre “orbite” ci stanno al massimo 8 elettroni + - - + - - + + - + + + ++ + + - - Gli elettroni in realtà occupano diversi strati ( o gusci) via via più grandi. Essi si dispongono nello spazio attorno al nucleo partendo dal guscio più interno per poi occupare progressivamente gli altri. La tavola periodica degli elementi Nel 1869 Dmitrij Mendeleev ordinò i 63 elementi noti in base alla massa atomica crescente, e costruì la prima tavola periodica degli elementi. Nella tavola periodica che Mendeleev pubblicò nel 1871, gli elementi erano ordinati in dodici file orizzontali e otto verticali secondo la massa atomica crescente. Non comparivano i gas nobili. Negli anni la tavola periodica è stata aggiornata, inserendo nuovi elementi via via scoperti. Gli elementi sono sistemati, in righe orizzontali, in ordine crescente di numero atomico ( indicato con Z che indica il numero di protoni presenti nell’atomo). Il primo elemento del sistema periodico è l’idrogeno ( 1 protone) Nella Tavola periodica gli elementi sono disposti lungo 7 righe orizzontali dette periodi e in 8 colonne verticali o gruppi , cui vengono aggiunti i cosiddetti elementi di transizione. Le proprietà fisiche e chimiche degli elementi appartenenti a una stessa riga (periodo) variano con gradualità. Gli elementi che hanno proprietà chimiche simili appartengono a una stessa colonna (gruppo). ALCUNE CARATTERISTICHE DELLA TAVOLA PERIODICA 1. Gli elementi della moderna tavola periodica sono 118; 2. la posizione di ciascun elemento sulla tavola dipende dal suo numero atomico (Z); Numero atomico 3. gli elementi che chiudono i periodi sono i gas nobili, così chiamati per la scarsissima reattività dovuta alla loro configurazione elettronica stabile; 5. gli elementi verticali formano i gruppi; 6. fra il gruppo II e il gruppo III si trovano gli elementi di transizione; 7. in fondo alla tavola periodica ci sono due file di 14 elementi metallici costituenti le serie dei lantanidi e degli attinidi. I livelli di energia degli elettroni - - - - ++ +++ + ++ + + ++ + - - - Ricordiamo quindi: •un elemento è diverso da un altro per il numero di protoni e quindi di elettroni presenti nell’atomo •Questo numero si chiama numero atomico •Poiché l’atomo è neutro, il numero di protoni deve essere uguale al numero di elettroni; i neutroni possono essere diversi. •I protoni ed i neutroni stanno nel nucleo, mentre gli elettroni vi girano intorno •Nella prima “orbita” ci stanno al massimo 2 elettroni, mentre nelle altre ci stanno al massimo 8 elettroni - + Le “orbite” degli elettroni vengono chiamati gusci o strati. Essi sono dei livelli energetici posseduti dagli elettroni - - - - ++ +++ + ++ + + ++ + - - - Gli elettroni situati negli strati (“orbite”) più lontani dal nucleo sono più ricchi di energia (si trovano ad un livello energetico superiore); quelli situati negli strati più vicini al nucleo si trovano ad un livello energetico inferiore Quando ad un atomo viene fornita energia, può succedere che gli elettroni saltano negli strati più lontani dal nucleo (strati ad energia più alta) - + Subito dopo, l’elettrone ritorna nello strato iniziale liberando (per esempio sottoforma di luce) l’energia che aveva ricevuto prima Abbiamo detto che quando l’elettrone ritorna al livello inferiore libera l’energia che lo aveva fatto saltare - Questa energia spesso è energia luminosa + Il colore della luce emessa dipende dalla struttura dell’atomo di quel dato elemento chimico Isotopi e numero di massa ISOTOPI Abbiamo detto che un elemento è diverso da un altro per il numero di protoni e quindi di elettroni (numero atomico) E i neutroni ? + Uno stesso elemento può essere costituito da atomi aventi un diverso numero di neutroni protoni neutroni - Atomi di uno stesso elemento con numero diverso di neutroni si dicono ISOTOPI elettroni Come esempio vediamo gli isotopi dell’idrogeno (simbolo H, numero atomico 1 (cioè 1 solo protone ed un solo elettrone)) - + - - + + - + - + + - Questi tre atomi chimicamente si comportano allo stesso modo (si tratta sempre di idrogeno) Ma cosa cambia? Cambia solamente il peso! In ogni singolo atomo il peso è sostanzialmente determinato dai protoni e dai neutroni (il peso degli elettroni viene trascurato perché piccolissimo) Per cui: La somma dei protoni e dei neutroni presenti in un atomo viene chiamata numero di massa e si indica con la lettera A A p n Ritorna all’indice generale Metalli e non metalli; Il legame chimico • C1 Metalli e non metalli C2 • Legame ionico C3 • Legame covalente C4 • Legame metallico Metalli e non metalli Abbiamo detto che nel primo strato ci stanno al massimo 2 elettroni, mentre negli altri strati ci stanno al massimo 8 elettroni - Pertanto, mentre le orbite interne - sono piene di elettroni (2 nella - - ++ +++ + ++ + + ++ + - - prima e 8 nelle altre), l’ultima - orbita può essere completamente riempita oppure non completa. Tutti gli elementi “desiderano” avere l’ultima orbita completa Alcuni tendono a reagire perdendo elettroni (in questo modo rimangono con l’orbita sottostante completa) Altri tendono a reagire acquistando elettroni (in questo modo completano l’orbita) Altri ancora si uniscono mettendo in comune elettroni (fino ad avere nell’ultimo strato un assetto completo di elettroni) Gli elementi che tendono a perdere elettroni si chiamano metalli Gli elementi che tendono ad acquistare elettroni si chiamano non metalli Tra gli elementi distinguiamo: Metalli Tendono a perdere elettroni … Elementi con caratteristiche intermedie tra metalli e non metalli Non metalli Tendono ad acquistare elettroni Gas nobili Hanno l’ultima orbita completa; non reagiscono con nessuno Legame ionico Spieghiamolo con un esempio: - - - + +++ ++ + + ++ + - - - - Si chiamerà ione sodio Na (sodio) Ha un solo elettrone nell’ultima orbita, tende a perderlo Il sodio, perdendo un elettrone, non sarà più neutro, ma avrà una carica positiva perché i protoni del nucleo prevalgono sugli elettroni (c’è un elettrone in meno) Na F (fluoro) Ha 7 elettroni nell’ultima orbita (uno in meno rispetto a 8), tende ad acquistare 1 elettrone per avere l’ultima orbita completa - - Il fluoro, acquistando un elettrone, non sarà più neutro, ma avrà una carica negativa (c’è un elettrone in più) + ++++ ++ + + - - - Si chiamerà ione fluoruro F Il sodio cede un elettrone al fluoro e diventa ione positivo Il fluoro diventa ione negativo Ione positivo e ione negativo si attraggono, formando un legame detto legame ionico - - - - - + +++ ++ + + ++ + - - + ++++ ++ + + - - - - - Na Na F - F Quindi il legame ionico si stabilisce tra un atomo che cede elettroni ed un altro atomo che li acquista L’atomo che cede gli elettroni diventa caricato positivamente (ione positivo o catione); L’atomo che acquista gli elettroni diventa caricato negativamente (ione negativo o anione) Ione positivo e ione negativo si attraggono e si uniscono. La forza elettrica che tiene uniti gli ioni positivi con gli ioni negativi costituisce appunto il legame ionico - - - - - - - + +++ ++ + 11 + ++ + - - - - - - - Na (sodio) Na + +++ ++++ + +17 +++ +++ + - - - - - Cl (cloro) Cl - Dall’unione di uno di sodio ed uno di cloro, si forma il composto ionico NaCl, chiamato cloruro di sodio (questo è il sale che usiamo in cucina) - - Mg - F - - + +++ ++ + 12 + ++ ++ - + ++++ + +9 + + - - - - - - - Il magnesio può cedere due elettroni - Il fluoro può ricevere solo un elettrone Allora il magnesio cede l’altro elettrone ad un altro atomo di fluoro Mg 2 F-1 -1 F Si forma il composto - MgF2 F - - + ++++ + +9 + + - - - Confrontiamo NaF con Na F Il sodio cede un solo elettrone e diventa con carica +1 Si dice che il sodio ha valenza 1, cioè ha una singola capacità di combinazione, in quanto mette in gioco 1 solo elettrone per formare il legame MgF2 Mg 2 F-1 F-1 Il magnesio cede due elettroni e diventa con carica +2 Il magnesio ha valenza 2, cioè ha una doppia capacità di combinazione, in quanto mette in gioco 2 elettroni per formare il legame In entrambi i composti il fluoro ha valenza 1, in quanto ogni atomo acquista 1 solo elettrone Legame covalente Abbiamo già detto che: I metalli tendono a cedere elettroni diventando ioni positivi (o cationi) I non metalli tendono ad acquistare elettroni diventando ioni negativi (o anioni) Ioni positivi e ioni negativi si attraggono formando un legame ionico Il legame ionico non è il solo tipo di legame esistente: Spesso due o più atomi si uniscono senza che nessuno ceda e nessuno acquisti elettroni, ma mettendo in comune 1 o più elettoni. In questo modo viene raggiunta la completezza nell’ultima orbita Si parla in questo caso di legame covalente Legame covalente Un atomo di idrogeno ha 1 solo elettrone Per completare l’orbita occorre un altro elettrone (nella prima orbita ci stanno al massimo 2 elettroni) Due atomi di idrogeno possono completarsi mettendo in comune un elettrone ciascuno - - - + + - Quindi i due elettroni impegnati nel legame appartengono ad entrambi gli atomi di idrogeno Si forma la molecola H2 - - - - ++ ++ ++8 ++ - - - - ++ ++ ++8 ++ - - - Due atomi di ossigeno si uniscono formando la molecola O2 - Legame metallico Ricordiamo che i metalli, avendo pochi elettroni nell’ultima orbita, tendono a perderli - - - + +++ ++ + 11 + ++ + Na (sodio) - - In una sbarra di metallo questi elettroni esterni formano una nuvola elettronica che appartiene contemporaneamente a tutti gli atomi del metallo, mantenendoli uniti (legame metallico) Addirittura, applicando una differenza di potenziale elettrico questi elettroni possono spostarsi (corrente elettrica) Ecco perché i metalli sono buoni conduttori di elettricità L’energia del flusso di elettroni nei metalli può essere utilizzata per fare accendere una lampadina
Scarica