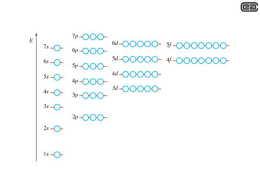
LABORATORIO 3 Questa attività è volta a prendere confidenza e a studiare il fenomeno del Pompaggio Ottico 1. LA STRUMENTAZIONE 1.1. ACCENSIONE E SPEGNIMENTO DEL LASER PANNELLO DI CONTROLLO DEL LASER M M K K ON L L OFF ON B OFF LA TESTA LASER OFF CON D D ON I OFF I DISPLAY A A 1.2. PROCEDURA DI ACCENSIONE E SPEGNIMENTO DEL LASER PRELIMINARI 1. Accertarsi della posizione dell’interruttore generale A: A in OFF 2. Accertarsi che l’interruttore di alimentazione del laser L sia spento: L in OFF 3. Accertarsi che l’interruttore di cortocircuito del Laser C (sulla testa del Laser) sia in off: C in OFF 4. Accertarsi che la manopola di modulazione del Laser sia a zero: K a ZERO 5. Accertarsi che la manopola M della corrente di iniezione del Laser sia a zero: M a ZERO 6. Accertarsi che l’interruttore I di aggancio del controllo di temperatura sia spento: I in OFF 7. Accertarsi che l’interruttore di inserzione della modulazione del Laser sia in off: B in OFF. ACCENSIONE 8. Accendere l’’interruttore generale: A in ON 9. Posizionare il commutatore D della indicazione del display digitale sulla posizione “corrente di iniezione del Laser” Ilaser (prima posizione in senso antiorario). Accertarsi che il display indichi meno di 10 mA: D su Ilaser 10. Posizionare il commutatore D della indicazione del display nella posizione Δt: D su Δt. Attendere che l’indicazione del display sia intorno a 200 (questi sono mK). 11. Quando questo accade, porre in ON l’interruttore I di aggancio del controllo della temperatura: I in ON. 12. Attendere fino a quando l’indicazione del display si riduce a 1-3 mK. Questo è l’errore sulla temperatura. 13. Accendere l’interruttore di alimentazione del Laser: L in ON 14. Mettere in ON l’interruttore sulla testa del Laser: C in ON 15. Posizionare il commutatore D della indicazione del display nella posizione “Corrente di Iniezione del Laser”: D su Ilaser 16. Ruotare lentamente la manopola M della corrente di iniezione e seguire sia l’aumento della corrente sul display che l’apparizione della riga Laser sul monitor inferiore (schermo giallo). Fermarsi a 9095 mA. Se, quando la corrente è intorno a 40 mA non appare la riga gialla sul monitor c’è qualcosa che non va. Diminuire immediatamente la corrente nel Laser e attuare la procedura di spegnimento come segue. 17. Quando la temperatura è stabile, regolare finemente la corrente di iniezione fino a quando appare la fluorescenza nella cella visibile sul monitor verde. Non toccare nessuna delle regolazioni a vite: nessuna di quelle non indicate nelle istruzioni di cui sopra. SPEGNIMENTO 1. Ruotare lentamente all’indietro la manopola M della regolazione della corrente fino a partarla a zero. 2. Mettere in OFF l’interruttore sulla testa del laser C in OFF. 3. Mettere in OFF l’interruttore di alimentazione del Laser: L in OFF 4. Mettere in OFF l’interruttore di aggancio del controllo della temperatura: I in OFF 5. Ora si può spegnere tutto: A in OFF LA TESTA DEL LASER 2. LA STRUMENTAZIONE ELETTRONICA LOCK-IN GENERAT. RF GENERAT. DOPPIO IMP. FREQUENZIM. AMPLIFICAT. MW GENERAT. MW CONTR. LASER 1 DISTRIBUZ. SEGN. SWEEP GENERAT. LF SWEEP CONTR. BOB. HELMOLTZ AMPLIFICATORI RF ALIMENTATORE BOBINE OSCILLOSC. ANALOG. OSCILLOSC. DIGITALE MONITOR CELLA MONITOR LASER AMPL. SWEEP GAUSSMETRO PRESELETTORE ANALIZZATORE DI SPETTRO TELECAMERA CELLA ARIA CALDA CELLA FOTORIVELATORI BOBINE PER IL CAMPO LONGITUDINALE BIAS TEE USCITA RF AMPLIFICAT. POLARIZZAZ. FOTODIODO FOTODIODO 3. MODELLO VETTORIALE DELL’ATOMO 3.1. L’ATOMO DI BOHR Es.: L’atomo di idrogeno - n: numero quantico principale - Orbite in m.q.: distribuzione di probabilità di posizione Orbitali Bohr: 3.2. GLI ORBITALI ATOMICI n=1. Orbitale 1s Gli orbitali atomici n=2. Orbitali 2s e 2p 1s Gli orbitali atomici n=3. Orbitali 3s e 3p e 3d 3.3. I NUMERI QUANTICI I numeri quantici importanti sono: n = 1, 2, 3, …. = numero quantico principale l = 0, 1, 2, 3, ….. ,(n-1) = numero quantico orbitale j = L-S, L-S+1,…,L+S = numero quantico di momento angolare totale, con S spin dell’elettrone. Notazione spettroscopica. Esempio. Il livello fondamentale del 5S1/2 85Rb è: -> 5 è il numero quantico principale. -> S indica il valore del numero quantico orbitale l secondo la denominazione storica seguente: l=0 S (Sottile) l=1 P (Principale) l=2 D (Diffusa) l=3 F (Fondamentale) l=4 G (non ha nome) l=5 H (non ha nome) Ecc. -> 1/2 è il valore del momento angolare totale J Si può quindi conoscere lo spin S = J-l = 1/2 Formazione dei doppietti, dovuta ai due possibili valori dello spin S che introducono differenti valori del momento angolare totale J nella cosiddetta “interazione spin-orbita” (v. nel seguito). Splitting = 2B 3.4. PROPRIETÀ MAGNETICHE DEGLI ATOMI Un elettrone che “ruota su un’orbita” , con momento angolare L, equivale a una corrente I in una spira. Quindi dà origine a un campo magnetico e a un momento di dipolo magnetico L perpendicolari al piano della spira. L = mvr: L --r-- L e v mom. angolare orbitale I = e v = e/2 = ev/2r L = I· = ev/2r x r2 = evr/2: mom. di dipolo magnetico Da queste, dato che poiché e < 0, L ha verso opposto a L, si ha: L = -(g e/2m) · L Qui si è introdotto il fattore g = 1 , detto “Fattore giromagnetico orbitale”, in analogia ad altri casi della fisica atomica. Il momento angolare orbitale L (momento meccanico) è quantizzato. Il valore del modulo di L è dato da: L = l(l+1)· ħ (ShrÖdinger) secondo la seguente tabella: 3.5. IL NUMERO QUANTICO MAGNETICO Abbiamo visto che in meccanica quantistica un elettrone legato a un nucleo ha un momento magnetico, proporzionale a quello angolare L = -(ge/2m) · L L = -(ge/2m) l(l+1) Anche la componente z di L (Lz) è LZ . Infatti, vale Lz = - (ge/2m) Lz = -g (e/2m) ml = - ml B (g = 1) Se l’atomo si trova immerso in un campo B esterno uniforme, sul dipolo magnetico agisce solo un momento torcente e non una forza. All’atomo è associata una energia potenziale magnetica: U = - orb· Best = +(ge/2m) L·Best Se si prende l’asse z lungo Best si ha: Uml = - orb,z Best = +ml(e/2m) Best =+ml B Best Pertanto ml si chiama numero quantico magnetico Il numero quantico magnetico ml è connesso con le posizioni quantizzate del momento angolare orbitale L. Esempio per L=2 L = ħ l(l+1) = 2(2+1) = ħ6 ml = -l, (-l+1),…, 0, 1,…, l ml in unità di ħ Lz = L cos, Esempio per l = 2. (-2 ħ < ml < +2 ħ) cos = ml/l(l+1) Precessione di L attorno all’asse di quantizzaziopne. L non è mai allineato con l’asse z, questo perché ml è sempre minore di l(l+1). Questa è una conseguenza del principio di indeterminazione per il momento angolare che implica che non è possibile conoscere contemporaneamente due componenti di L. Quindi se l’atomo è immerso in un campo magnetico esterno i (2l+1) livelli degeneri corrispondenti allo stesso l ma diverso ml acquistano energie diverse (viene rimossa la degenerazione). Questo fatto spiega l’effetto che è stato scoperto da Pieter Zeeman nel 1896 (molto prima della M.Q.): le righe emesse da un atomo eccitato sottoposto a un campo magnetico si separano in più componenti (con diversa polarizzazione) : splitting Zeeman Splitting dei livelli energetici nell’effetto Zeeman “normale” per i (2l+1) livelli di ”singoletto” (S = 0), l=1 e 2. Di 15 possibili transizioni se ne vedono solo 9 perché ml = 0, ±1 e 6 sono degeneri in energia a 3 a 3. B=0 B>0 3.6. LA PRECESSIONE DI LARMOR Quando un momento magnetico è in un campo magnetico B su di esso si esercita un momento torcente che può essere espresso nella forma di un prodotto vettoriale: = x B Per un momento magnetico statico, o per un anello di corrente classico questo momento torcente tende ad allineare il momento magnetico con il campo magnetico B in modo da porsi nella configurazione di energia minima. Ma se il momento magnetico deriva dal moto di un elettrone attorno al nucleo, esso è proporzionale al momento magnetico dell’elettrone. Il momento torcente produrrà una variazione del momento angolare L perpendicolare ad L, e il momento magnetico avrà un moto di precessione attorno alla direzione z del campo magnetico. Questa è la precessione di Larmor. Se chiamiamo l’angolo di precessione, possiamo descrivere l’effetto del momento torcente come segue (vedi figura alla pagina seguente): Larmor.gif = L/t= L sin /t = B sin = (e/2me) LB sin La velocità angolare di precessione (frequenza di Larmor) si deduce dalle espressioni precedenti: larmor = d/dt = (e/2me) B Questa frequenza angolare è associata con gli “spin flip”, o transizioni degli spin che implicano un cambiamento di energia di 2B per ogni unità ħ. Alla pagina seguente un esempio per un elettrone libero in un campo magnetico di 0,1 mT= 1 Gauss . larmor= 2eB/ħ= [2·2·1/2(5.79 10-5 eV/T) ·10-4 T]/(6,58·10-16 eV·s) = = 1,7608·107 s-1, da cui: fElarmor = larmor/2 = 2,8 MHz In un campo di 1 T si ha: fEelarmor = 28,05 GHz Un identico calcolo per lo spin di un protone (p = 2,79 ·3,15 ·10-8 eV) in un campo di 1 T fornisce il valore: fPlarmor = 42,57 MHz 3.7. IL MOMENTO ANGOLARE DI SPIN In aggiunta al momento angolare orbitale L gli elettroni possiedono un momento angolare intrinseco di spin S, di modulo s = ½ (1 + ½) · ħ, caratterizzato dal numero quantico s = ½, e un corrispondente momento magnetico intrinseco di spin: s = - (g e/2me) · S, (formalmente simile a quella del momento di dipolo magnetico) dove g è il rapporto giromagnetico dell’elettrone e vale g = 2,00232. I due valori possibili dello spin: s= ½ “spin su” s = – ½ “spin giù” I due stati di spin, “su" e “giù“, permettono di avere due elettroni per ogni insieme degli altri numeri quantici n, l, ml. Se si introduce il magnetone di Bohr: B = e ħ /2me = 9,2740·10-24 J/T = 5,7883·10-5 eV/T la componente lungo z del momento magnetico intrinseco dell’elettrone, che è quella che si misura, si può scrivere (ora g = 2): z = ± ½ g B 3.8. STATI, TERMINI, MICROSTATI ATOMICI Il momento angolare orbitale totale L (vettore) è la somma vettoriale dei singoli momenti orbitali degli elettroni: L = l1 + l2 +..... Il modulo è legato al numero quantico di momento angolare orbitale totale L: modulo di L = [L(L + 1)] · ħ Lo spin totale S (vettore) di un atomo è la somma vettoriale dei momenti angolari di spin dei singoli elettroni: S = s1 + s2 +.... Il modulo è legato al numero quantico di spin totale S: modulo di S = S(S + 1)· ħ Questi numeri quantici collettivi definiscono degli stati possibili di energia diversa degli atomi multielettronici, detti termini atomici. Un atomo può avere parecchi stati di momento angolare totale diversi, a ciascuno dei quali corrisponde una distribuzione degli elettroni differente; questi modi diversi per una certa configurazione si dicono microstati. 3.9. ACCOPPIAMENTO SPIN – ORBITA I due momenti magnetici (orbitale e di spin) sono disaccoppiati? Ricordiamo che l’elettrone che ruota attorno al nucleo crea un campo magnetico (Teorema di Ampere). Ma nel sistema di riferimento dell’elettrone è come se il nucleo (carica +Ze) gli ruotasse attorno in senso opposto. Quindi l’elettrone sente l’effetto di un campo magnetico Bn = 0/2r I = 0/2r Zev/2r = 0Zev/4r2. Si dimostra che Bn + L Possiamo, allora, esprimere l’energia di interazione tra il momento magnetico di spin s e il campo magnetico “del nucleo” Bn che sarà Uso = - s· Bn + S• L Ls cos prodotto scalare tra il Momento angolare di Spin e quello Orbitale S può essere circa parallelo a L (</2) o circa antiparallelo (>/2) e questo cambia l’energia dello stato. Uso minore per S antiparall. ad L ! Un calcolo approssimativo dell’intensità del campo magnetico sentito dall’elettrone nell’atomo di Idrogeno dà B = 0.5 T = 5,000 Gauss, un campo molto intenso. Mentre la corrispondente separazione in energia dei due sottolivelli 1s è di circa 10-4 eV. Quindi l’accoppiamento spin-orbita (L.S) prevale fino a campi magnetici esterni dell’ordine di 1 T. Si parla, quindi, di accoppiamento tra L e S (Accoppiamento SpinOrbita) Conviene, allora, introdurre il Momento angolare totale J dello stato, che vale J = L + S somma vettoriale! Quindi, J dipende dall’orientazione reciproca N.B. il momento magnetico totale dell’atomo è tot = orb+ s = -e/2m (L + 2S) quindi tot non sta sulla stessa retta di J Se il campo magnetico esterno B non è troppo intenso l’energia magnetica è data da U = - tot· B cioè l’atomo reagisce come un sistema unico. Se B è molto intenso orb e s reagiscono in maniera indipendente. Tornando al vettore J = L+S, si può vedere che né L né S si conservano separatamente ma J sì. Allora anche Lz e Sz non hanno più valori ben definiti, mentre Jz sì, ma vale ancora Jz = Lz+Sz (Lz e Sz possono variare istante per istante, ma la loro somma no!) Si trova che gli autovalori di J sono: J = j(j+1) ħ con j = l ± s (j= 0, ½ , 1, 3/2, 2,...) (Questo risultato è di carattere generale, anche per S 3/4 ħ, come nei sistemi a più elettroni.) Inoltre Jz = mjħ (mj = -j, -j+1,...j-1, j) quindi gli mj sono 2j +1 Se J = L+S allora J2 = L2 + S2 + 2L·S (L·S = L S cos()) Per un singolo elettrone atomico j = l +½ (L parall. S), l -½ (L antiparall. S) (j>0, se l = 0, solo j = ½ ) Esempio l = 0, j = ½ , mj =- ½ , ½ (mj sono 2j +1, 2 stati, stessa energia) l = 1 , j = ½ , mj = - ½ , ½ (2 stati) l =1,j= 3/2, mj = -3/2, - ½ , ½ , 3/2 (4 stati) Se non si tiene conto dell’interazione spin-orbita, con l = 1, ml = -1, 0, 1 (due stati di spin per ml , tot. 6 stati) Passando a j e mj il numero di stati non cambia ma vengono ridistribuiti in energia, dato che l’energia dipende dall’accoppiamento. Si dimostra, quindi, che l’energia di uno stato, tenendo conto dell’accoppiamento spin-orbita, dipende non solo da n e l ma anche da j. Quindi gli stati con stesso n e l ma diverso j non sono più degeneri ma hanno energie leggermente diverse. L’introduzione dell’interazione spin-orbita separa gli stati di dato l in due componenti, ognuna con un numero diverso di stati, con la stessa energia, ma in numero di 2j+1 (molteplicità). Pertanto essendo diversi i numeri di livelli coinvolti, le transizioni che coinvolgono le due componenti avranno intensità diverse. Molteplicità: I(3/2)/I(1/2) = (2x3/2 +1)/(2x1/2 +1) = 4/2 = 2 I(5/2)/I(3/2) = 6/4= 1.5 I(7/2)/I(5/2) = 8/6= 1.33 Si trova, come regola generale, che nelle transizioni elettroniche che comportano emissione di un’onda e.m., oltre alla regola di selezione trovata (empiricamente) da Sommerfeld n = l = 1 (prima) vale anche: j= 0, 1 (poi) Esempio. La nota riga rossa dell’Idrogeno secondo la teoria di Bohr è una riga singola (3 2). Lo stesso se si risolve l’equazione di Schrödinger. Secondo Bohr la corrispondente è di 656.11 nm, considerando il nucleo fisso. Usando la massa ridotta si trova 656.47 nm per l’idrogeno e 656.29 nm per il deuterio. La differenza tra le due righe è di circa 0.2nm. In realtà ognuna delle due righe è divisa in altre due righe separate di 0.016 nm (0.0025%) corrispondente ad una differenza di energia di 45 eV, per effetto dell’accoppiamento S.O. Ciò corrisponde, a sua volta, ad un campo magnetico sentito dall’elettrone di circa 0.4 T. 3.10. SPIN NUCLEARE E STRUTTURA IPERFINE La struttura iperfine deriva dall’esistenza di uno spin e di un momento magnetico del nucleo. Il momento angolare meccanico nucleare I (vettore) ha modulo: I= I(1 + I)· ħ (I numero quantico) Il numero quantico I può essere intero o semintero. Si conoscono nuclei con I compreso fra 0 e 15/2. Il valore del magnetone nucleare è (1/1836) B, con B = (e/2me)· ħ = 9,27400949(80) × 10-24 J·T-1 Precessione di L attorno a J Precessione di J attorno ad F 3.11. LIVELLI IPERFINI L’interazione fra lo spin del nucleo I e il momento angolare orbitale J provoca uno splitting del livello fondamentale e dei livelli eccitati ciascuno in due livelli detti livelli iperfini. La somma dei vettori J e I genera un nuovo vettore F F = J + I Il suo modulo può assumere uno qualunque fra i valori: F = J+ I, J+ I-1, J+ I-2, …, J-I Lo spin nucleare del 85Rb è I=5/2. Poiché per il 85Rb è J=±1/2, i due livelli iperfini sono caratterizzati dai numeri F=2 e F=3. La regola di selezione per F è: F = 0, ± 1 3.12. SPLITTING MAGNETICO O ZEEMAN Quando un atomo è in un campo magnetico, i livelli iperfini F si splittano. Questo è lo splitting Zeeman o magnetico Scoperto da Pieter Zeeman nel 1896. Le righe emesse da un atomo eccitato sottoposto a un campo magnetico si separano in più componenti (con diversa polarizzazione). Le componenti di F in campo magnetico nella direzione del campo si indicano con mf. Esse sono in numero di 2F +1 e vanno da mf = +F a mf = -F. In un campo magnetico di direzione z anche il vettore F precede attorno a z. SOTTOLIVELLI ZEEMAN NEL CASO F = 2 z 4. IL POMPAGGIO OTTICO 4.1. MOMENTO ANGOLARE DEL FOTONE Se un fascio di luce che si propaga nella direzione positiva dell’asse z è polarizzato circolarmente sinistro (+), ciascun fotone avrà un momento angolare positivo + ħ lungo l’asse z. Se il fascio contiene N fotoni per unità di volume, la densità di energia del fascio, , sarà = N ħ , dove è la frequenza angolare della radiazione, e l’unità di volume avrà un momento angolare Lz = n ħ. Il rapporto / = N ħ è indipendente dalla frequenza ed è uguale in grandezza al momento angolare Lz. In modo simile per un fascio polarizzato circolarmente destro (-) è / = - Lz (un’onda polarizzata linearmente non trasporta alcun momento angolare). 4.2. LO SPETTRO IPERFINE DEL 85Rb La transizione F = 3 è più intensa perché avendo minore energia la sua popolazione è maggiore. 4.3.FLUORESCENZA SULLA TRACCIA DEL FASCIO LASER Riga D1 del 85Rb, livello iperfine F=3, polarizzaz. circolare 4.4. DISPOSIZIONE SPERIMENTALE PER IL POMPAGGIO OTTICO ZEEMAN, O ALLA KASTLER 4.5. MECCANISMO DEL POMPAGGIO OTTICO Regola di selez. per mf con luce polarizzata circolarmente: -Verso un livello eccitato mf=+1 (il fotone trasporta un momento angolare di una unità di ħ) -Da un livello eccitato al livello fondamentale: mf = ±1 Esempio per due elettroni che partono da due sottolivelli diversi del livello fondamentale • Luce + A 795 nm • • • • 4.6. IMPORTANTE: EFFETTO DEL POMPAGGIO OTTICO Conseguenza dell’accumulo di atomi sul livello Zeeman mf = 3 (nel caso del 85Rb irradiato con luce risonante con il livello iperfine F = 3) è il fatto importante che tutti gli spin degli elettroni ottici degli atomi si allineano con la direzione z del campo magnetico, e questo pur continuando F a precedere attorno a z. Il vapore di Rb si magnetizza macroscopicamente. Questo dà luogo ad altri fenomeni interessanti, come per esempio l’effetto Faraday, che in casi particolari può diventare enorme. 4.7. ANCORA L’ESPERIMENTO BOBINE DI HELMOLTZ Il campo al centro delle bobine di Helmoltz è: B = (4/5)3/2 µ0 n i/R , dove i è l’intensità della corrente (che le percorre ambedue nello stesso senso), n il numero di spire, R il raggio e sono disposte a distanza R. Il campo sull’asse x delle bobine è sensibilmente costante nell’intervallo fra –R/2 e +R/2 dal centro del sistema. PICCO DI DEPOMPAGGIO Fluorescenza massima Campo magn. Fluorescenza minima vapore pompato 4.8. POMPAGGIO IPERFINE In condizioni di equilibrio termico i livelli iperfini sono approssimativamente ugualmente popolati. È possibile alterare questo equilibrio per mezzo di una eccitazione ottica di uno dei due livelli iperfini in assenza di campo magnetico e con luce polarizzata linearmente. Le regole di selezione per F determinano il fatto che, con una eccitazione ottica risonante per esempio con il livello F = 2, avverranno decadimenti sia sul livello F = 2 che sul livello F = 3. Ma gli atomi che sono decaduti su F = 3 non interagiscono più con la radiazione. Il livello F = 3 si popola a spese del livello F = 2. Il sistema diviene meno fluorescente. POMPAGGIO IPERFINE La fluorescenza diminuisce Livello Pompato LASER È possibile sopprimere il pompaggio iperfine e ristabilire l’uguaglianza delle popolazioni fra i livelli iperfini eccitando simultaneamente i due livelli. Questo può essere ottenuto per esempio modulando il Laser a 3 GHz (frequenza dello splitting iperfine) in modo da eccitare il livello pompato con una delle due bande laterali che si creano con la modulazione. Se si spazza la frequenza di modulazione del Laser, ogni volta che questa passa sul valore di 3036 MHz si ha l’effetto visibile di un enorme aumento della fluorescenza della cella. Il segnale di depompaggio è un picco di fluorescenza simile al picco di depompaggio Kastler visto in precedenza. 4.9. APPLICAZIONE: OROLOGI ATOMICI CELLA CON 87Rb IN CAMPO MAGNETICO NULLO, POMPAGGIO IPERFINE. SE SI IRRADIA CON FOTONI A R.F. , QUANDO LA FREQUENZA E’ ESATTAMENTE 6076 MHz (PARI ALLO SPLITTING IPERFINE DEL 87Rb ), SI HA UN PICCO NEL SEGNALE DI FLUORESCENZA E UN MINIMO NELLA LUCE TRASMESSA QUESTO SEGNALE SERVE PER AGGANCIARE IL GENERATORE DI R.F. ALLA PROPRIETÀ ATOMICA: LO SPLITTING IPERFINE. PRECISIONE OTTENIBILE: 1 x 10-13 STANDARD DI FREQUENZA ATOMICO AL Rb L C L: Lampada; C: Cavità a microonde che contiene la cella Applicazione fondamentale in fisica atomica. Il pompaggio iperfine è un metodo molto efficace per la determinazione precisa dello splitting iperfine del livello fondamentale degli atomi. 5. ATTIVITÀ POSSIBILI 1. Regolare tutti i parametri dell’esperimento per ottenere un picco di depompaggio Kastler che sia il più ampio e il più stretto possibile 2. Valutare il valore del campo magnetico terrestre 3. Realizzare il pompaggio iperfine 4. Cosa succede se si inserisce la modulazione a 3 GHz del Laser? Questo è importante perché questo fenomeno è alla base del funzionamento degli orologi atomici. Studiare il fenomeno al variare della frequenza. 5. Determinare la carica specifica e/m dell’elettrone FINE
Scaricare