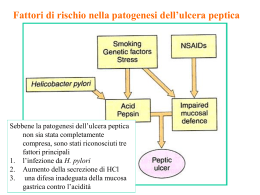
UNIVERSITA’ DEGLI STUDI DI PISA Facoltà di Medicina e Chirurgia MALATTIA PEPTICA Fisiopatologia ed Helicobacter pylori La mucosa gastrica normale Cardias Cellule secernenti muco Piloro Produzione di ormoni (gastrina) che stimolano la produzione di HCl Fondo (corpo) Cellule parietali: acido Cellule principali: pepsinogeno, il quale è attivato dall’HCl e scinde le proteine Funzione dello stomaco • • • • • • Serbatoio del cibo ingerito Demolizione dei materiali residui, (peristalsi) Inizio della digestione (proteine) Difesa contro microorganismi ingeriti Favorire l’assorbimento più a valle di alcune sostanze (vitamina B12, ferro) Assorbimento di acqua, alcuni ioni e composti liposolubili (alcool, l'acido acetilsalicilico, caffeina) . La elevata acidità necessita di un sistema molto efficiente per evitare l’autodigestione: muco, tampone bicarbonato, integrità dell’epitelio Meccanismi di difesa Prima linea: muco e bicarbonato Lo strato di muco adeso impedisce l’azione della pepsina La produzione di bicarbonato crea un gradiente di pH stabilizzato dallo strato di muco Seconda linea: meccanismi epiteliali Lo strato di cellule epiteliali fornisce la seconda linea di difesa attraverso vari fattori quali la produzione di muco, il trasporto ionico delle cellule epiteliali che mantiene il pH intracellulare e la produzione di bicarbonato. Terza linea: flusso ematico mucoso Un elaborato sistema microvascolare all’interno dello strato sottomucoso è la componente fondamentale di questo sistema di difesa/riparazione. Un ricco letto circolatorio sottomucoso fornisce i bicarbonati che neutralizzano l’acidità generata dalla secrezione di HCL delle cellule parietali. Inoltre questo letto microcircolatorio fornisce un adeguato supporto di micronutrienti e di ossigeno e rimuove i prodotti metabolici tossici. Laddove tali elementi difensivi vengano sopraffatti, i meccanismi riparativi intrinseci dell'epitelio consentono di ripristinare la suddetta integrità mucosa. Le malattie dello stomaco PATOLOGIE NON NEOPLASTICHE GASTRITI ACUTE GASTRITI CRONICHE Erosiva emorragica Da disordini alimentari e/o da allergia Corrosiva Da ustione Flemmonosa Da corpi estranei Tubercolare Luetica Actinomicotica o fungina Eosinofila Sarcoidosica Da morbo di Crohn Linite plastica Gastrite cronica aspecifica Gastrite alcalina Gastriti iperplastiche Le malattie dello stomaco PATOLOGIE NEOPLASTICHE TUMORI BENIGNI TUMORI MALIGNI • • • • • • • • Polipi adematosi Leiomiomi Leiomioblastoma gastrico Angiodisplasia gastrica Trattamento: •Enucleazione •Resezione limitata Carcinomi Carcinoidi Linfomi Sarcomi MALATTIA PEPTICA: Definizione Con il termine di ULCERA PEPTICA si indica una perdita di sostanza della parete dello stomaco o del duodeno, che si approfonda oltre la muscularis mucosae e guarisce con cicatrice, a differenza dell'EROSIONE, lesione che interessa gli strati più superficiali. Fondo Cardias Corpo Piloro Antro ULCERA DUODENALE: primi centimetri del duodeno ULCERA GASTRICA: Estremo distale dell’esofago o piccola curvatura della porzione antrale MALATTIA PEPTICA: Epidemiologia Incidenza in diminuzione nelle ultime decadi Il declino é peraltro rapido, come dimostrato dal fatto che in Italia tra il 1997 e il 1999, il numero delle diagnosi di ulcera documentate endoscopicamente é calato del 25% 70 60 50 40 30 20 10 160 140 120 100 80 60 40 20 0 Non bianchi Bianchi UG UD 1970-74 1975-79 1980-84 1985-89 1990-95 ULCERA PEPTICA Epidemiologia ULCERA GASTRICA: M/F = 1.5/1 50-60 anni 2% della popolazione ULCERA DUODENALE: M/F = 3/1 40-50 anni 4-10 volte più frequente dell’ulcera gastrica ULCERA PEPTICA: Fattori di rischio ULCERA DUODENALE ULCERA GASTRICA M/F = 3/1 Influenza genetica M/F = 1.5/1 Non genetica – – – – – familiari I grado gemelli monozigoti gruppo sanguigno 0 ABH secretori HLA-B5 – gruppo sanguigno A FANS Infezione H.P. Acidità, gastrina e n°cell. Parietali = / acidità e gastrina = n° cell. Parietali Incidenza in riduzione Incidenza stabile MALATTIA PEPTICA: Caratteristiche MALATTIA CRONICA CON TENDENZA ALLA CICATRIZZAZIONE SPONTANEA E ALLA RECIDIVA MALATTIA PEPTICA: Fattori coinvolti nella patogenesi Fattori aggressivi Secrezione acida Pepsina (digerisce le proteine) Alterazione Integrità mucosa muco e bicarbonati flusso sanguigno intramucoso turn-over cellulare prostaglandine endogene (PGE2–PGI) Helicobacter pylori Fattori genetici e ambientali FATTORI AGGRESSIVI ULCERA PEPTICA FATTORI EZIOLOGICI POTENZIALI Gastrite cronica da Helicobacter Pylori Fumo Alcool Caffè FANS, corticosteroidi Stress Reflusso duodeno-gastrico Diminuizione di fattori citoprotettivi (Vit. B1-B12, folati, zinco…) Sindrome di Zollinger-Ellison, Cushing MALATTIA PEPTICA: H. pylori e ulcera peptica Nel 95% delle UD e nell’80% delle UG vi è infezione da H. pylori Maggiore frequenza di UD nei pazienti con infezione da H. pylori Recidiva di UP dopo eradicazione dell’infezione da H. pylori Sintomatologia dell' ulcera duodenale Il quadro clinico ha una caratteristica rappresentata dalla periodicità delle sue manifestazioni per cui a periodi di esacerbazione se ne alternano altri in cui la malattia è in fase di quiescenza. Ricorrenza stagionale (primavera ed autunno). Il dolore epigastrico è il sintomo più frequente dell'ulcera duodenale. Spesso viene descritto come sordo o urente, altre volte può essere definito fastidioso, acuto o può essere avvertito come una sensazione di pienezza addominale. Il dolore insorge caratteristicamente a distanza dai pasti (da 90 minuti a 3 ore) e talvolta sveglia di notte il paziente. Classicamente, la diagnosi di ulcera peptica viene considerata probabile in presenza di un dolore epigastrico urente, che compare 2-4 ore dopo il pasto e/o durante le ore notturne, risulta sensibile all'assunzione di antiacidi e/o di cibo e presenta la tendenza a un andamento periodico con ricorrenza a distanza di mesi. MALATTIA PEPTICA: Sintomi - da 1 a 3 ore dopo i pasti DOLORE EPIGASTRICO - spesso notturno - attenuato dal cibo e dagli antiacidi NAUSEA, VOMITO, DISPEPSIA NESSUN SINTOMO MALATTIA PEPTICA: Sintomi Prevalenza % ULCERA DUODENALE ULCERA GASTRICA DISPEPSIA 70 70 30-60 notturne episodiche allev. cibo appetito + appetito – 50-80 50-60 20-65 10-30 25-40 30-45 10-20 5-50 5-10 40-60 25-35 30-40 5-30 10-30 25-40 Meteorismo/ eruttazioni 30-65 30-70 40-80 Epigastralgie - Ulcere in assenza di sintomi 10-40% MALATTIA PEPTICA: Diagnosi SCARSA UTILITA’ DELL’ESAME OBIETTIVO E DEI TEST DI LABORATORIO ENDOSCOPIA + BIOPSIE RX TRATTO DIGESTIVO SUPERIORE ULCERE GASTRICHE ULCERE DUODENALI ULCERA PEPTICA: Complicanze BASSO FLUSSO (anemia microcitica sideropenica, RSO+) EMORRAGIA 15-20% ALTO FLUSSO (melena, talora ematemesi) PERFORAZIONE Peritonite chimica batterica PENETRAZIONE Testa pancreas, vie biliari STENOSI Scompenso gastrico 2% Ogni ulcera gastrica, fino a prova contraria, deve essere considerata un carcinoma gastrico COMPLICANZE 1. 2. 3. 4. 5. 1. PERFORAZIONE PENETRAZIONE ORGANI ADIACENTI STENOSI EMORRAGIA CARCINOMA PERFORAZIONE •PROGREDISCE RAPIDAMENTE •SE SITUATA PARETE ANTERIORE GASTRICA O DUODENALE PERITONITE ACUTA •DIFFUSA O •CIRCOSCRITTA PROGREDIRE DEL PROCESSO: ULCERA PENETRANTE IN ORGANO ADIACENTE (pancreas; fegato; t. adiposo piccolo omento; colon trasverso) SE SEDE POSTERIORE: ASCESSO SUBFRENICO PERFORAZIONE COPERTA: QUANDO LA PERFORAZIONE è PRECEDUTA DA ADERENZE INFIAMMATORIE A ORGANO VICINO NO VERSAMENTO DEL CONTENUTO GASTRICO IN CAVITA’ PERITONEALE ULCERA PEPTICA ENDOSCOPIA: importante la d.d. con ulcera carcinomatosa ULCERA PEPTICA ULCERA CARCINOMATOSA Forma ovoidale <2 cm Margini netti Convergenza delle pliche mucose Vallo rilevato, soffice ed elastico Forma irregolare Maggiori dimensioni Irregolarità delle pliche mucose Vallo rigido e anaelastico ULCERE SANGUINANTI ALTO FLUSSO BASSO FLUSSO L’infezione da Helicobacter pylori NO ACID NO ULCER !! Warren e Marshal – PREMIO NOBEL MEDICINA 2005 HELICOBACTER PYLORI Microbiologia - Batterio Gram negativo, spiraliforme e flagellato. - lunghezza 2,5-4 m e larghezza 0,5-1 m. - 4-6 flagelli unipolari: garantisce motilità - Glicocalice: facilita la colonizzazione della mucosa gastrica. - Richiede un’atmosfera di microaerofilia, con pressione parziale di ossigeno ottimale del 5%: ciò è uno dei fattori limitanti l’allestimento delle colture. - Forma coccoide: viene assunta in condizioni ambientali sfavorevoli alla sopravvivenza. HELICOBACTER PYLORI Microbiologia STRUTTURA FUNZIONE PROTEINA PURIFICATA Ureasi Neutralizzazione acido, Effetto citotossico Subunità piccola (26,5 Kda) Subunità grande (61 Kda) Flagello Motilità Flagelli principali (53 Kda) Flagelli minori (54 Kda) Adesine Legame cellule epitaliali Emoagglutinina fribillare (20,5 Kda) HELICOBACTER PYLORI Epidemiologia: prevalenza dell’infezione Paesi industrializzati Paesi in via di sviluppo 100 % di infetti 80 PANENDEMICA --PANENDEMICA 10%ANNUO ANNUO TRA ANNI --10% TRA 2-8 2-8 ANNI ELEVATA DI ASINTOMATICI --ELEVATA % DI%ASINTOMATICI 60 40 Rara nell’infanzia Rara nell’infanzia 20% 20% << 40 40anni anni 50 % > 60 anni 50 % > 60 anni Basso livello socio-economico predittivo di Basso livello socio-economico predittivo di infezione infezione HP HP Immigrazione responsabile di isolate aree di alta prevalenza Immigrazione responsabile di isolate aree di alta prevalenza 20 0 0 10 20 30 40 Età 50 60 70 80 HELICOBACTER PYLORI Fattori di rischio di acquisizione Elevato numero di fratelli Condivisione del letto nell’infanzia Frequentare una scuola in zone popolari Occupazione manuale del padre Basso reddito del capofamiglia Classe sociale bassa Membro della famiglia infetto Basso livello di istruzione HELICOBACTER PYLORI Trasmissione RESERVOIR ANIMALE sospetto provato OSPITE PRIMARIO UOMO contaminazione oro -fecale Assunzione di vegetali crudi contaminazione oro -fecale Ingestione di acque superficiali (piscine, ...) Relazione tra infezione da H. pylori dei genitori e di altri membri della famiglia Bambini Hp positivi: 40% Genitore Hp positivo Bambini Hp positivi: 3 % Genitore Hp negativo Partner Hp positivo: 60% Partner Hp positivo: 9 % HELICOBACTER PYLORI Trasmissione oro-orale PLACCA DENTARIA (Desai - Scand J Gastroenterol 1991) SALIVA (Ferguson - J Clin Microbiol 1993) ENDOSCOPI E SONDE per pH-METRIA (Katoh - Jpn J Cancer Res 1993) HELICOBACTER PYLORI Patogenesi Infezione Infiammazione della mucosa gastrica (spesso asintomatica) L’infiammazione della mucosa può portare alla ulcera gastrica (o duodenale). HELICOBACTER PYLORI Patogenesi ? GENETICA ? Alterata funzione cellule D/G Infezione H. pylori ↑ massa cellule parietali Gastrite antrale o di tipo B ↑ GASTRINA ↑ secr. ACIDO Migrazione H.pylori in duodeno METAPLASIA GASTRICA in DUODENO DUODENITE ULCERA DUODENALE Helicobacter pylori GASTRITE 100% ULCERA CARCINOMA LINFOMA D.N.U. ASINTOMATICA ULCERA DUODENALE Marshall WCG Los Angeles 1994 92% Hp 5% FANS 1% altro 2% K ULCERA GASTRICA Marshall WCG Los Angeles 1994 70% Hp 2% altro 3% K 25% FANS Diagnosi dell’infezione da H. Pylori ’ INVASIVE NON INVASIVE Esame istologico IgG sieriche - ELISA Esame citologico Western Blot su siero Tests rapidi all’ureasi IgG sangue capillare Coltura IgA salivari Dosaggio ammonio gastrico IgG nelle urine PCR su biopsie ed aspirato 13 C Urea Breath Test 14 C Urea Breath Test Pepsinogeno e gastrina Antigeni Hp nelle feci Coltura e PCR su feci H. pylori - Sierologia Ricerca di Ac. anti-H.pylori di classe Ig G e Ig A - Metodica ELISA - Western Immunoblot Caratteristiche • Non invasivo • Poco costoso • Buona sensibilità (88-99%) • Buona specificità (86-95%) Limiti • Livelli di Anticorpi non dosabili in fase precoce • Importanza della funzionalità del sistema immunitario • Mancanza di informazioni morfologiche UREA BREATH TEST 13CO 2 nel respiro Urea 13C 13CO 2 13CO 2 NH2 Ureasi di Hp 13 C=O NH2 13CO + 2 NH3 UBT - Metodica standard europea T-1’ T0 T5’ T30’ T60’-100’ Campione basale (1°) 100 mg Urea-C13 + ac. citrico + 50 ml acqua Positivo per flora batterica cavo orale Raccolta 2° campione Positività per flora batterica intestinale TEST INVASIVI Il test invasivo si definisce tale in quanto per essere allestito necessita di due metodiche necessariamente invasive E.G.D.S. BIOPSIA TEST RAPIDO ALL’UREASI ESAME ISTOLOGICO ESAME COLTURALE + ANTIBIOGRAMMA (solo per accertata resistenza antibiotici) TEST INVASIVI TEST RAPIDO ALL’UREASI Viene allestito durante l’esame endoscopico ed è in grado di dare una risposta precoce dopo solo 20-40 minuti e quindi consente di impostare immediatamente l’eventuale terapia eradicante. SENSIBILITA’ 92% SPECIFICITA’ 100% NEGATIVO FASE LIQUIDA O SEMISOLIDA + UREA +INDICATORE pH POSITIVO Terapia Modificazioni dello stile di vita Fare 3-4 pasti al giorno Evitare pasti abbondanti Evitare i cibi che accentuano la sintomatologia Non esistono diete “utili” Evitare i farmaci gastrolesivi (es. aspirina, FANS) e, se indispensabili, assumerli a stomaco pieno e associare farmaci gastroprotettori Ridurre l’assunzione di alcoolici, specie a digiuno Smettere di fumare (il fumo rallenta la guarigione e favorisce la recidiva) Terapia Ulcera peptica - Terapia Antiacidi – Idrossido di Al + idrossido di Mg (es. Maalox®) + Na alginato (Gaviscon®) da assumere 1-3 ore dopo i pasti, prima di coricarsi e/o in caso di sintomi. Utilizzati soprattutto come terapia sintomatica, di supporto. – Ricordare che riducono l’assorbimento di anti-H2 e IPP. Altri farmaci – Sucralfato 1 g un’ora prima dei pasti: svolge un ruolo di protezione della mucosa gastrica. – Misoprostolo (derivato sintetico della prostaglandina E) 200 g per os x 4/dì, può aiutare a prevenire gastrolesività da FANS. Terapia Ulcera peptica – Terapia Anti-H2 – Es. ranitidina 150 mg x 2/dì. Miglioramento nel 60% dei casi (oggi poco utilizzati). IPP – Inibitori della pompa protonica – Omeprazolo 20 mg/dì per os, rabeprazolo 20 mg/dì, lansoprazolo 30 mg/dì, esomeprazolo 40 mg, ecc. (sono più efficaci di anti-H2) per 4-6 settimane (nota 48). – Dosaggio può essere raddoppiato, se inefficace (es. omeprazolo 20 mg x 2/dì). – L’uso parenterale deve essere riservato al trattamento delle complicanze o dei pazienti che non possono assumere farmaci per os. Terapia chirurgica – Riservata al trattamento delle complicanze Terapia Ulcera peptica – Terapia Hp L’eradicazione è raccomandata in tutti i pazienti con ulcera peptica HP+ Farmaci utilizzati per l’eradicazione – antisecretori (IPP) in associazione ad uno o più antibiotici (quali amoxicillina, claritromicina, tetraciclina, metronidazolo) ed eventualmente bismuto per 1-2 settimane Terapia Ulcera peptica – Terapia Hp Primo ciclo terapeutico – IPP a dose standard 1 cp x 2/dì per 7 giorni – Claritromicina 500 mg 1 cp x 2/dì per 7 giorni – Amoxicillina 1 g 1 cp x 2/dì per 7 giorni o Nitroimidazolico (metronidazolo o tinidazolo) 500 mg 1 cp x 2/dì per 7 giorni seguito da trattamento con IPP a dose standard 1 cp/dì per altre 4 settimane, se è presente ulcera peptica Ciclo terapeutico in caso di mancata eradicazione (per almeno 7 gg) – IPP a dose standard 1 cp x 2/dì – Bismuto 120 mg 1 cp x 4/dì – Metronidazolo o tinidazolo 500 mg 1 cp x 3/dì – Tetraciclina 500 mg 1 cp x 4/dì Terapia Ulcera peptica – Terapia Nei pazienti con ulcera HP positiva – Vedi schema terapia eradicante Nei pazienti con ulcera HP negativa – Ulcera gastrica: IPP a dose standard per 8-12 settimane – Ulcera duodenale: IPP a dose standard per 4-8 settimane Nei pazienti con ulcere in corso di trattamento con farmaci gastrolesivi – – – – Se possibile sospendere farmaci gastrolesivi Eradicare HP se presente Ulcera gastrica: IPP a dose standard per 8-12 settimane Ulcera duodenale: IPP a dose standard per 4-8 settimane
Scaricare