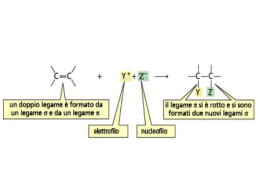
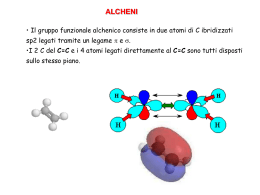
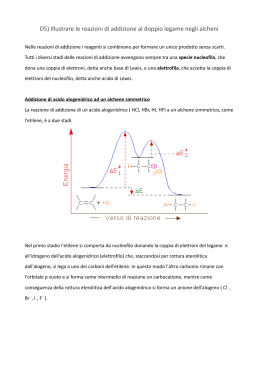
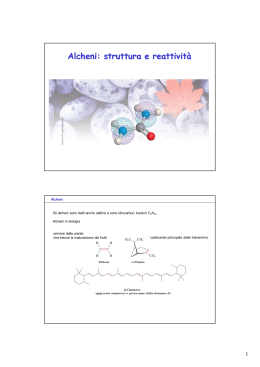
IDROCARBURI II Gli idrocarburi insaturi ALCHENI ED ALCHINI • Nomenclatura • Analisi conformazionale • Reazioni ALCHENI o idrocarburi etilenici o olefine HANNO ALMENO UN DOPPIO LEGAME C=C HANNO FORMULA GENERALE NOMENCLATURA • SCEGLIERE LA CATENA PIU' LUNGA CONTENENTE IL DOPPIO LEGAME, E METTERE IL SUFFISSO –ENE • LA NUMERAZIONE INIZIA DALL’ESTREMITÀ PIÙ VICINA AL LEGAME MULTIPLO • SE IL LEGAME MULTIPLO È EQUIDISTANTE DALLE DUE ESTREMITÀ, LA NUMERAZIONE INIZIA DA QUELLA PIÙ VICINA AL PRIMO PUNTO DI RAMIFICAZIONE • PER INDICARE LA POSIZIONE DEL LEGAME MULTIPLO CI SI RIFERISCE ALL’ATOMO DI CARBONIO DI QUESTO LEGAME CHE HA IL NUMERO PIÙ BASSO • SE I LEGAMI MULTIPLI SONO PIÙ D’UNO, LA NUMERAZIONE INIZIA DALL’ESTREMITÀ PIÙ VICINA A QUELLO CHE VIENE PER PRIMO Esempi e visualizzazioni ALCHENI CICLICI Struttura Elettronica degli Alcheni ibridazione sp2 – Tre orbitali equivalenti a 120º – Quarto orbitale atomico p • Combinazione di elettroni in due orbitali sp2 di due atomi forma legame • Interazione addittiva degli orbitali p crea un orbitale L’orbitale occupato impedisce la rotazione attorno al legame (barriera del legame - circa 268 kJ/mole nell’etilene) Dieni, trieni….polieni •I sistemi con più di un C=C sono definiti “polieni”. •I più semplici sono quelli in cui ci sono 2 doppi legami, i “dieni". •La posizione relativa dei doppi legami determinano le caratteristiche di reattività del sistema. •Sono possibili tre differenti configurazioni. Cumuleni Dieni coniugati Dieni isolati Sistemi coniugati C C C C Tutti e 4 i carboni sono ibridati sp2 Tutti gli atomi nel diene coniugato giacciono sullo stesso piano H H 1,3-butadiene H H H H H H H H H Legame ad elettroni delocalizzati H H H H H H H Legame ad elettroni delocalizzati nei dieni coniugati 1,3-butadiene H H H H H H ISOMERIA CIS-TRANS SE IL LEGAME SI SPEZZA, GLI ISOMERI SI RICONVERTONO Per la biochimica: il b-carotene e la Rodopsina Stabilità degli Alcheni DH della rottura di C=C a C-C più stabile di •Alcheni con più sostituenti sono più stabili • Gli alcheni coniugati sono più stabili degli alcheni isolati. Reattività degli alcheni (C=C) un legame è una regione ad alta densità (rosso) di elettroni, trattenuti più debolmente. • Gli elettrofili sono attratti dagli elettroni rottura del legame • Si forma un Carbocatione come intermedio di reazione. • Un nucleofilo si addiziona al carbocatione. • Gli alcheni danno reazioni di addizione elettrofila che convertono il legame in due nuovi legami . Addizione Elettrofila • Step 1: elettroni attaccano l’elettrofilo. E C C + E + C C + • Step 2: Nucleofilo attacca il carbocatione. E C C+ + _ Nuc: E Nuc C C Reattività degli alcheni (C=C) R1 R3 C R2 C R4 R1 A B R3 R2 C C R 4 A B La molecola A-B è addizionata per intero al composto insaturo Reazioni esotermiche Tipi di Addizione Addizione di acidi È una addizione elettrofila meccanismo REGOLA DI MARKOVNIKOV ADDIZIONE DI REAGENTI ASIMMETRICI AD ALCHENI ASIMMETRICI Reagenti asimmetrici • I PRODOTTI SONO REGIOISOMERI • LA REAZIONE PUÒ ESSERE: REGIO-SPECIFICA O REGIOSELETTIVA Addizione elettrofila ad un alchene asimmetrico SI OTTIENE SOLO 2-PROPANOLO QUANDO UN REAGENTE ASIMMETRICO SI ADDIZIONA AD UN ALCHENE ASIMMETRICO, LA PARTE ELETTROPOSITIVA DEL REAGENTE SI LEGA AL CARBONIO CON IL MAGGIORE NUMERO DI ATOMI DI IDROGENO. REGOLA DI MARKOVNIKOV ADDIZIONE DI REAGENTI ASIMMETRICI AD ALCHENI ASIMMETRICI • Regola di Markovnikov (empirica): “quando un alchene asimmetrico reagisce con un acido alogenidrico per formare un alogenuro alchilico, l’idrogeno si addiziona al carbonio dell’alchene che è legato al maggior numero di atomi di idrogeno e l’alogeno al carbonio che è legato al minor numero di atomi di idrogeno” CINETICA DELLA REAZIONE STABILITA’ I gruppi alchilici sono elettron donatori e quindi per effetto induttivo tendono a stabilizzare la carica positiva del carbocatione. Iperconiugazione Esposizione più generale della regola di Markovnikov: “In un’addizione elettrofila ad un alchene, l’elettrofilo si addiziona in modo da formare l’intermedio (carbocatione) più stabile.” Idratazione di Alcheni + H C C alkene alchene + H2O H OH C C alcohol alcol • Necessita di soluzioni diluite di acidi forti (H2SO4 o H3PO4 , la base coniugata che si forma essendo molto debole sarà anche un nucleofilo scadente (ad es. SO4--)). Questo permette all’H2O di competere con successo nell’attacco nucleofilo. Meccanismo dell’idratazione H H C C + + H O H + H + H O H C C + H2O H + H O H H + C C + C C H2O C C H H O + H2O C C + H3O + ADDIZIONE ELETTROFILA AI DIENI CONIUGATI 1 H 1 H2C C 2 HC 3 C CH2 4 Br H CH2 C 2 H C H addizione 1,2 H H -- Br 1 H Br C CH2 H2C C H H 4 addizione 1,4 Acido bromidrico 1,3 butadiene Distribuzione del potenziale elettrostatico HBr Br - H+ Attacco elettrofilo + carbocatione secondario + carbocatione allilico + Br- + Equilibrio di risonanza: spostamento di un doppietto di elettroni dalla posizione 1-2 a quella 2-3, spostamento della carica positiva dal C3 al C1. Differenti prodotti di reazione a seconda di quale sia il carbocatione “attaccato” dal nucleofilo. Reazioni a controllo cinetico e termodinamico Polimerizzazione • Un alchene (monomero) può addizionarsi ad una molecola simile per formare una catena (polimero). • Tre metodi: – Cationica, con carbocatione intermedio – Radicalica – Anionica, a carbanione intermedio (rara) H C H H C R Polietilene (PE) Polipropilene (PP) Polivinil chloruro (PVC) Polistirene (PS) Polimerizzazione Radicalica In presenza di un radicale libero iniziatore, (p. es. Perossido organico R-O-O-R) si verifica la polimerizzazione radicalica. H H C C Ph H RO H Ph RO C C H H + H H C C Ph H H Ph H Ph RO C C C C H H H H => Idrogenazione • Alchene + H2 Alcano • Necessario un Catalizzatore, di solito Pt, Pd, or Ni. • Addizione Syn Addizione di alogeni • Cl2, Br2, e talvolta I2 si addizionano ad un doppio legame formando dialogenuri vicinali. • Addizione Anti, la reazione è stereospecifica. Br C C + Br2 C C Br Meccanismo dell’alogenazione • Elettroni attaccano la molecola di bromo. • Si separa uno ione bromuro. • Intermedio = ione bromonio ciclico. C C Br C C + Br Br => + Br Ione Br- si aggiunge dal lato opposto a quello dell’anello a tre vertici. Br Br C C IONE BROMONIO C C Br Br Bromo + ciclopentene ALCHINI (ibridazione sp) • ORBITALI IBRIDI DI TIPO sp • HANNO ALMENO UN TRIPLO LEGAME • HANNO FORMULA GENERALE CNHN Formazione del triplo legame H H C C Br CH3 H C Br C Br Br C C Br Br CH3 Br Br H Br Br CH3 Br C C CH3 Br Nomencl. 2-butene Propino Alcheni ciclici e nomi comuni Torna Cicl. e nomi comuni Alcheni ciclici Alcuni composti semplici hanno spesso dei nomi comuni d’uso: etilene, acetilene e propilene (i loro nomi IUPAC sono riportati fra parentesi). Altri gruppi con nomi comuni di largo uso: vinile, allile e propargile (i loro nomi IUPAC sono riportati fra parentesi). Torna Beta carotene IL b-CAROTENE E LA RODOPSINA Il b-carotene La RODOPSINA è costituita da opsina + 11-cis-retinale La rodopsina e il meccanismo della vista Torna orbitali Torna
Scaricare