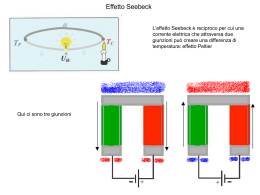
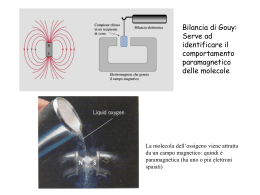
Si conoscono più di 15 milioni di sostanze diverse, ma questo è pur sempre un numero limitato, ben inferiore a quello ottenibile con un calcolo combinatorio tra gli elementi della tavola periodica… Perché le combinazioni tra atomi non sono tutte possibili? Una prima spiegazione può essere cercata pensando alla natura elettrica dell’atomo. L’atomo è fatto da cariche positive (nucleo) e negative (guscio) in movimento, ed è caratterizzato da determinate energie potenziali (Rutherford). La vicinanza con un altro atomo comporta delle interazioni di tipo elettromagnetico, sia attrattive che repulsive, cui saranno associate nuove forze, quindi nuove energie. La maggior parte delle volte, le forze in gioco producono un «repulsione», un allontanamento degli atomi. Solo in alcuni casi la loro combinazione porta ad un equilibrio tale da consentire l’attrazione reciproca tra due o più atomi. Nei casi in cui viene raggiunto un equilibrio più o meno stabile, gli atomi tendono a rimanere «legati» formando una molecola. Regola generale Una molecola si forma solo se il valore della sua energia potenziale è minore della somma di energie potenziali dei singoli atomi isolati che lo costituiscono. Il legame chimico tra atomi dello stesso tipo porta alla formazione di sostanze elementari (o elementi). Quello tra atomi di differente tipo porta a sostanze composte (o composti) Un legame chimico tiene uniti gli atomi con una determinata forza che occorre vincere, se si vuole separare i suoi componenti. Per fare ciò, per rompere cioè tale legame, occorre una determinata energia: Energia di legame quantità di energia che è necessario fornire a una mole di sostanza per rompere il legame che tiene insieme i suoi elementi. L'elettrochimica è quella branca della chimica che studia i fenomeni relativi alla trasformazione dell'energia chimica di legame in energia elettrica e viceversa. Esperienze e ricerca dell’elettrochimica (conducibilità e resistenza elettrica delle sostanze, elettrolisi, pile, galvanostegia ecc ), oltre alle spiegazione delle caratteristiche chimico-fisiche macroscopiche, forniscono significative informazioni relativamente al legame tra gli elementi di una determinata sostanza. Una buona conducibilità elettrica, per esempio, porta ad ammettere la possibilità di formare cariche libere (responsabili della corrente elettrica), Possibilità che, a sua volta, è facilmente imputabile alla debole forza che tiene uniti gli atomi costituenti le sostanze che, per un qualche motivo, possono quindi separarsi facilmente (rottura del legame) per dare origine a ioni. elettricamente molto conducibili, nonché facilmente scomponibili con l’elettrolisi, hanno delle caratteristiche comuni riconoscibili: I composti •Hanno alte temperature di fusione e di ebollizione •Sono fragili (si sgretolano) •Si sciolgono in solventi polari •Formano soluzioni con alta conducibilità el. •Formano cristalli (disposizione poliedrica ordinata delle particelle) Per spiegare le caratteristiche di questi tipi di sostanze, si pervenne all’idea che esse siano costituite da “aggregati” di particelle cariche elettricamente (sia +, sia -), tenute insieme da semplici attrazioni elettromagnetiche. Ora, per caricarsi elettricamente, un atomo deve perdere o acquistare elettroni diventando, così, uno ione. Si introdussero, quindi, concetti come: aggregato ionico, composto ionico, reticolo ionico e, ovviamente, legame ionico. Anche la struttura geometrica dei cristalli, che al microscopio elettronico si presentano come aggregati (o reticoli) atomici ordinati, possono essere perfettamente spiegati ammettendo la natura ionica degli atomi stessi. NaCl CuSO4 Quando il composto ionico è allo stato solido non ha alcuna conducibilità elettrica apprezzabile. Allo stato liquido (fuso) o in soluzione la sua conducibilità è considerevole. Si ha passaggio di corrente solo quando particelle cariche sono libere di muoversi. Allo stato solido ogni ione è vincolato nel reticolo cristallino; negli altri due stati ogni ione è libero di muoversi. (+) Se nel liquido, o nella soluzione, si immergono due elettrodi aventi cariche di segno opposto… (-) …gli ioni positivi migreranno verso l’elettrodo negativo, mentre gli ioni negativi vanno verso l’elettrodo positivo. Il modello ionico, tuttavia, non spiega il comportamento di tutte le sostanze conosciute. Ad esempio, considerando cloro (Cl) in diversi composti… NaCl E’ solido a t° ambiente, ha alte Tfus. e Teb., Cristallizza, si scioglie in solventi polari formando soluzioni con alta conducibilità elettrica, HCl E’ liquido a t° ambiente, ha basse Tfus. e Teb., Non cristallizza, si scioglie in solventi polari formando soluzioni con medio-bassa conducibilità elettrica. Cl2 E’ gassoso a t°ambiente, Non cristallizza, si scioglie in solventi neutri formando soluzioni senza conducibilità elettrica apprezzabile. Possiamo ipotizzare che l’acido cloridrico (HCl) possa formare ioni, ma non tanti quanti quelli di un quantitativo equivalente di sale, mentre il Cl2 non ionizza affatto. Tantissime sostanze dimostrano situazioni di conducibilità parziale. Tantissime altre hanno conducibilità nulla o quasi (come il Cl2). Si può parlare, perciò, di percentuale e di probabilità di ionizzazione specifica per ogni sostanza. Il confronto con le varie sostanze portano all’evidenza che uno stesso atomo cambia la sua tendenza a formare ioni in base al compagno con cui si combina. In altre parole… occorre ammettere che solo in condizioni particolari, e non sempre al 100% delle molecole di una determinata sostanza, gli elettroni “saltano” da un atomo all’altro formando ioni. Ora nasce un problema: Gli atomi che «ionizzano» si caricano elettricamente e, grazie allo loro carica opposta si terranno uniti (forze di Coulomb) formando le molecole… Come spiegare le molecole formate da atomi che non ionizzano? Quali sono le forze in gioco che tengono uniti questi atomi? Nei primi decenni del ‘900 non c’erano indizi che potevano far supporre forze di natura differente da quella elettromagnetica. Occorreva, perciò, pensare a situazioni nuove, a equilibri elettromagnetici alternativi a quelli ionici tali, comunque, da tenere uniti gli atomi senza portare alla formazione di cariche elettriche libere (di ioni). Lewis fu il primo a intuire la possibilità di una situazione, alternativa a quella ionica, in cui l’equilibrio elettromagnetico comportasse non il passaggio di elettroni da un atomo all’altro, bensì la condivisione di doppietti elettronici tra gli atomi. Secondo la sua idea un e- per ogni atomo salterebbe su un nuovo livello energetico comune ai due atomi, tenendo “vincolati” quest’ultimi, l’un all’altro, impedendone la ionizzazione. Accanto a quello ionico, nacque, così, il concetto di legame covalente (legame di condivisione elettronica). Il livello energetico comune fu poi meglio definito come l’orbitale molecolare. Lo stesso Lewis elaborò la prima teoria del legame chimico Si basa su: •Legge di Coulomb (bilanciamento forze elettriche) •Meccanica quantistica configurazione elettronica Tiene conto di: •Energia di ionizzazione (E.I.) •Affinità elettronica (A.E.) •Elettronegatività La teoria di Lewis sul legame chimica fu sintetizzata con la famosa Regola dell’ottetto-duetto (1916). Un atomo è stabile quando si ritrova con otto elettroni nel suo ultimo livello energetico (detto di valenza), fatta eccezione per idrogeno ed elio (ne bastano due). Secondo tale teoria, la stabilità e l’inerzia (non reattività) dei gas nobili risiederebbe proprio nel fatto che, allo stato fondamentale, presentano otto elettroni (due nel caso dell’elio) nel livello più esterno, quello di valenza (così nominato in quanto, sostanzialmente, è questo livello a dettare il comportamento di un atomo). Tutti gli altri elementi tendono a cambiare la configurazione elettronica: cedendo, acquistando o condividendo elettroni, in modo da assomigliare quanto più possibile al gas nobile più vicino nella tavola periodica prevedendo, quindi, 8 e- sul livello esterno Questa tendenza porta a formare legami tra atomi in svariate combinazioni, più o meno stabili, giustificando l’esistenza di … Milioni di sostanze con caratteristiche chimico-fisiche specifiche, dipendenti dai tipi di atomi da cui sono costituite, ma anche dal tipo di legame tra essi. Modello di Lewis del legame in NaCl L’atomo di sodio perde il suo elettrone esterno e diventa uno ione positivo. = Elettrone L’atomo di cloro cattura l’elettrone e diventa uno ione negativo. = Elettrone e- e- = Nucleo di sodio (Na) = Nucleo di Cloro (Cl) Entrambi si ritrovano con 8 esul livello esterno Na Na+ + e- Cl + e- Cl- I due ioni, avendo cariche elettriche di segno opposto, si attirano e restano uniti. NaCl + - Na+ Cl- Considerando le caratteristiche dei singoli atomi e le energie in gioco, espresse come A.E ed E.I., con Lewis si elaborarono formule ed espressioni matematiche che permettono, tuttora, di fare corrette previsioni sul tipo di legame nonché sulle caratteristiche chimico-fisiche delle sostanze risultanti dalle varie combinazioni tra atomi. A.E. Affinità elettronica = energia liberata quando un atomo acquista un elettrone E.I. Energia di ionizzazione = energia necessaria per estrarre un elettrone da un atomo Per semplificare i calcoli fu comodo e più efficace, grazie a Pauling e ad altri, introdurre un nuovo parametro matematico che sintetizza i due precedenti: l’Elettronegatività. “Tendenza (o capacità) di un atomo ad attrarre gli elettroni di legame” Pauling stabilì una prima scala di elettronegatività sulla base della misurazione dell’energia sotto forma di calore liberato durante la formazione di vari composti (entalpia di legame). Sintetizzò la sua idea con le seguenti formule: Altri proposero scale differenti sulla base di altre esperienze o calcoli. Ad esempio, la formula più semplice è quella introdotta da Mulliken: Elettronegatività= (E.I. + A.I.)/2 Qualunque scala si usi, l’aspetto fondamentale è la differenza di elettronegatività tra gli atomi coinvolti in un legame. Il legame ionico ha probabilità considerevoli di formarsi tra atomi la cui differenza dei valori di elettronegatività è superiore a 1,7. Al di sotto di tale valore la probabilità (percentuale) di ionizzazione diminuisce gradualmente e significativamente, mentre aumenta quella di formare orbitali molecolari legame covalente Il legame covalente è il legame chimico più forte conosciuto. Si distinguono due tipi di legame covalente: 1 – Legame covalente puro (o apolare o omopolare o omonucleare o neutro) 2 - Legame covalente polare (o eteropolare o eteronucleare) Legami eteronucleare con diverso grado di polarità Legami omonucleari Il grado di polarizzazione è importante per le caratteristiche chimicofisiche delle sostanze. Formule di Lewis Lewis introdusse anche una simbologia molto semplice, ma efficace, per rappresentare le configurazioni elettroniche esterne dei singoli atomi e i legami nelle molecole, in rispetto delle regola dell’ottetto-duetto. Simboli degli elementi + punti (in coppia o isolati) e/o trattini (un trattino al posto di una coppia di punti) indicanti gli elettroni di valenza, quelli dell’ultimo livello. Ultimo livello La coppia di punti (o il trattino) non utilizzata in un legame si chiama doppietto solitario; Il punto singolo elettrone spaiato o singoletto. Legame omonucleare Singoletti Legame eteronucleare Forze di legame Ordine di legame o di coordinazione E’ un tipo particolare di legame covalente in cui un atomo mette a disposizione una coppia elettronica e l’altro dispone di un orbitale vuoto per riceverli. Lo ione H+ dispone un orbitale vuoto. donatore accettore L’N, possiede un doppietto di e- libero Lo ione H+ dispone un orbitale vuoto. L’O possiede almeno un doppietto di e- libero Il B dispone un orbitale vuoto. L’N possiede un doppietto di e- libero Da un punto di vista chimico-fisico non si distingue da quello covalente polare se non per l’origine degli elettroni e, quindi, per la sua modalità di formazione due elettroni di un solo atomo che “saltano” su un livello comune. Un limite delle formule di Lewis è quello di non considerare la geometria delle molecole, la disposizione cioè nello spazio dei vari atomi. Quest’ultima ha una notevole importanza per comprendere appieno le caratteristiche chimico-fisiche della sostanza. Per fare un esempio, in una molecola bi-atomica i due atomi sono disposti sempre e solo su una linea retta. I vettori forza agiscono in modo linearmente opposto. E’ semplice ottenere la risultante. Si possono, infatti, verificare due casi semplici: Le forze degli atomi sono uguali ed opposte: la risultante è nulla molecola neutra Le forze degli atomi sono differenti ed opposte: la risultante non è nulla molecola polare La disposizione è, comunque, sempre lineare: non ci sono altre possibilità! Si possono facilmente prevedere: solubilità, conducibilità, punto di ebollizione ecc. Più complesse si rivelano le situazioni con tre o più atomi Solo conoscendo bene la geometria molecolare (e le formule di Lewis non lo permoettono) posso fare previsioni esatte sulle proprietà chimico-fisiche Valence Shell Electron Pair Repulsion Repulsione delle coppie elettroniche nel guscio di valenza Questa teoria cerca di spiegare in che modo è possibile conoscere la geometria molecolare, cioè la disposizione geometrica degli atomi e dei legami, e si basa sul numero totale di coppie elettroniche (sia impegnate nei legami, sia libere). Principio della teoria Le coppie elettroniche si dispongono nello spazio in modo da minimizzare la loro mutua repulsione. Una linea indica una coppia condivisa di elettroni (legame) disposta su un piano frontale. Una coppia di punti indica un doppietto elettronico libero. Il triangolo vuoto indica che il doppietto è posto davanti al piano frontale. Il triangolo con le linee indica che il doppietto è posto dietro. Rappresentazioni in 3d 5 Modello VSEPR dell’acqua La molecola dell’ozono (O3) Geometria molecolare VSEPR Formula di Lewis Non c’è motivo di pensare che il doppio legame sia esclusivamente a destra (o a sinistra). E’, invece, più credibile pensare che gli elettroni abbiano la stessa probabilità nei due lati (vedi gatto di Shroedinger). Si può, quindi, ragionevolmente supporre che la molecola reale sia un ibrido delle due forme: si definisce ibrido di risonanza. Un ibrido di risonanza è una molecola la cui struttura reale è intermedia tra due o più possibili strutture di Lewis. Lo ione nitrato (NO3 -) Il benzene C6H6 Anello aromatico Il fluoruro di Boro (BF3) Il fluoro, F, ha 7 e- nel livello esterno Il boro, B, ha 3 e- nel livello esterno Esistono due modi per rappresentare la molecola con la teoria di Lewis (regola dell’ottetto). Il boro avrebbe solo 6 elettroni sul suo livello esterno (non si stabilizzerebbe) Entrambi i modelli risultano INSODDISFACENTI. Uno dei tre fluoro metterebbe a disposizione del boro una coppia di elettroni, stabilizzandolo. Questo comporterebbe, però, una carica parziale positiva sul fluoro, il che lo destabilizzerebbe, dato che la sua elettronegatività è maggiore di quella del boro. Io ione solfato (S04--) Gli atomi di ossigeno, O, sono «soddisfatti» con la regola dell’ottetto, ma non lo zolfo, S, che si ritroverebbe con ben 12 e- sul livello esterno Situazioni analoghe si riscontrano in tantissime altre molecole come: SF6 (S con 12 e- ); con XeO4 (Xe con 16 e-) ecc. Pauling e altri, per superare la teoria ferrea dell’ottetto-duetto, proposero una nuova teoria che considerava il concetto di orbitale (Shroedinger). Tale teoria fu chiamata: teoria del legame di valenza (Valence Bond) Un legame covalente si forma grazie alla “fusione” di due orbitali atomici (OA) costituendo un orbitale molecolare (OM). Gli orbitali atomici che si sovrappongono devono avere energie simili. Gli OA che si fondono devono contenere un solo e- per ciascuno, oppure una coppia di e- l’uno e un orbitale vuoto l’altro, in modo che nell’OM vi si ritrovino due e- aventi spin antiparallelo. Il numero di legami che può formare un atomo è pari al numero di orbitali semivuoti (o di singoletti) disponibili. Frontale Laterale Il legame σ si può formare con la fusione: Laterale • di due OA entrambi di tipo s • di un OA di tipo s e uno di tipo p ma secondo l’asse dei quest’ultimo • di due orbitali di tipo p in modo «frontale», cioè con gli assi coincidenti Il legame π si può ottenere solo dalla fusione di due orbitali di tipo p in modo laterale, cioè con gli assi paralleli, ma non coincidenti. In caso di doppio o triplo legame: uno di essi è di tipo σ, gli altri di tipo π Il legame di tipo σ è più forte di quello π che, quindi, si può rompere più facilmente Sovrapposizione Frontale Sovrapposizione Laterale - Rappresentare molecole poliatomiche con la “fusione” degli orbitali è molto complessa e, praticamente, inefficace. - La teoria non spiega alcune molecole, anche semplici, come il metano CH4 La configurazione elettronica del C allo stato fondamentale, nel suo ultimo livello, è la seguente Secondo la teoria di Pauling (VB), essendoci due elettroni spaiati, il C dovrebbe formare due legami con l’idrogeno CH2 (composto non esistente) L’unica spiegazione plausibile è quella che prevede un salto quantico di un elettrone dall’orbitale 2s a quello 2p vuoto. Dato, inoltre, che i 4 legami nel metano sono equienergetici, occorre supporre la formazione di orbitali molecolari perfettamente uguali. Questa supposizione portò a ipotizzare la fusione del’orbitale di tipo s con i 3 di tipo p. In tal modo risulterebbero 4 orbitali atomici ibridi perfettamente uguali. Tale situazione è nota come ibridazione sp3 Esistono anche ibridazioni sp2 ed sp Forte fu, quindi, la spinta ad elaborare una teoria più complessa e più strutturata al fine di poter spiegare qualsiasi molecola. Tale teoria fu trovata ricorrendo completamente alla meccanica quantistica di Shroedinger: si applicò la sua funzione d’onda ψ2 (utilizzata per trovare gli orbitali atomici) per studiare gli orbitali molecolari. Principio di tale teoria è quello di considerare il legame chimico come il risultato delle interazioni tra tutti gli orbitali atomici degli elementi combinati nella molecola, non solo quelli di valenza. In tal senso vi partecipano tutti gli elettroni. Le interazioni, tra l’altro, erano da immaginare come interferenze di onde. Dallo studio matematico (probabilistico) delle interazioni tra due orbitali atomici, si ottennero due orbitali molecolari (non uno unico, come nella teoria VB): cosa prevedibile, dato sia il fatto che si tratta di funzioni d’onda di II grado (due soluzioni possibili), sia il fatto che l’interferenza di onde simili ha probabilità di avvenire sia in fase (interf. costruttiva) sia in opposizione di fase (interf. distruttiva) Tali orbitali furono definiti: uno di legame (interf. costruttiva), l’altro di antilegame (interf. distruttiva). La presenza di elettroni in orbitali di antilegame destabilizza la molecola, mentre in quelli di legame, la stabilizza. Lo studio quanto-meccanico delle interazioni tra tutti gli orbitali atomici del livello esterno degli elementi che si combinano è in grado di spiegare tutte le molecole conosciute e tutti i comportamenti chimico-fisici delle sostanze. Di seguito i punti fondamentali di questa teoria 1. Gli elettroni disponibili devono essere distribuiti sugli orbitali molecolari 2. Il numero di elettroni disponibili deve essere uguale al numero totale di elettroni contenuti negli orbitali atomici combinati 3. Il numero di orbitali molecolari è uguale al numero di orbitali atomici combinati 4. Il riempimento degli orbitali molecolari avviene secondo l’ordine di energia crescente 5. Ciascun orbitale molecolare sia legante che antilegante può ospitare al massimo due elettroni con spin antiparallelo 6. Il riempimento degli orbitali molecolari aventi la stessa energia avviene secondo la regola di Hund, o della massima molteplicità, 7. Affinché avvenga un legame tra due atomi deve risultare un eccesso di orbitali leganti rispetto a quelli antileganti 8. Il numero totale di legami tra i due atomi, detto ordine di legame, si ottiene dividendo per due l’eccesso di elettroni leganti 9. Orbitali di antilegame Orbitali di legame Orbitale di antilegame Orbitale di legame Legame metallico Gli atomi dei metalli sono caratterizzati da una bassa energia di ionizzazione, facilmente, quindi, tendono a cedere, o a condividere, gli elettroni dell’ultimo livello. Ora, considerando, ad esempio, i metalli con un solo elettrone di valenza (Na, Li, K ecc), nella sostanza elementare (metallo puro) occorre, per la regola dell’ottetto, che ciascun atomo si circondi di altri 7. Nell’insieme, tra tutti gli atomi dell’oggetto metallico si formerà un reticolo compatto tra cui gli elettroni di valenza si muovono da un atomo all’altro non importa, poi, se ritornano a quello di provenienza o passano su un altri allontanandosi dal primo. Da un punto di vista quantistico si afferma che tutti gli elettroni di valenza di tutti gli atomi «saltano» su un nuovo livello energetico comune, su una «banda» (sinomino di orbitale) metallica unica per tutti dove è altissima la probabilità di trovare tutti gli elettroni di valenza. Muovendosi in questa banda, gli elettroni si ritrovano liberi di circolare su tutta l’estensione dell’oggetto metallico: questo spiega la buona conducibilità di calore e di elettricità, la duttilità, la malleabilità ecc.
Scaricare