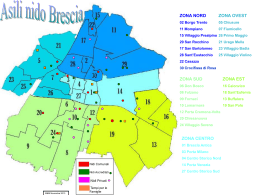
UNA CASA PER IL GRILLAIO – AZIONI PRATICHE PER LA CONSERVAZIONE DEL GRILLAIO FALCO NAUMANNI IN PUGLIA E BASILICATA a cura di Marco Gustin (coordinamento) collaborazione: Michele Bux (capitolo 2), Pino Giglio (capitolo 2 e 3) e Chiara Manghetti (capitolo 3) INDICE 1. AVVIO DEL PROGETTO 1.1. Organizzazione conferenza stampa 3 3 2. ATTIVITÀ DI CONSERVAZIONE 2.1. Premessa 2.2. Biologia, distribuzione e fattori di minaccia della popolazione apulo-lucana di Grillaio Falco naumanni 2.2.1. Biologia 2.2.2. Distribuzione storica 2.2.3 - Distribuzione attuale 2.2.4 - Analisi critica dei fattori di minaccia 2.2.5. - Monitoraggio del Grillaio nelle città di Gravina in Puglia, Altamura, Santeramo in Colle, Cassano delle Murge e Acquaviva delle Fonti 2.2.5.1. - Materiali e metodi 2.2.5.2. – Risultati 2.2.5.3. – Conclusioni 2.3. - Analisi della biologia riproduttiva del Grillaio utilizzando le cassette nido artificiali 2.3.1. Introduzione 2.3.2. Acquisto del materiale per la costruzione delle cassette nido 2.3.3. Realizzazione ed installazione dei nidi artificiali 2.3.3.1. Metodo di installazione 2.3.3.2 - Materiali e metodi sui parametri riproduttivi 2.3.3.3. Risultati sull’occupazione delle cassette nido artificiali 2.3.3.4. Confronto tra siti di nidificazione naturali e cassette nido: risultati e discussione 2.3.3.5. Conclusioni 2.3.4. Studio sulla rete trofica e sul foraggiamento del Grillaio Falco naumanni: risultati preliminari 2.3.4.1. Introduzione 2.3.4.2. Materiali e metodi 2.3.4.3. Risultati 4 4 5 5 9 10 11 13 13 14 14 15 15 16 16 16 18 23 26 30 34 34 34 35 1 3 ATTIVITÀ DI EDUCAZIONE 37 3.1. Il Grillaio questo sconosciuto: una valutazione della percezione e della conoscenza del Grillaio nelle popolazioni di Gravina in Puglia ed Altamura 37 3.1.1. Introduzione 37 3.1.2. Metodi 38 3.1.3. Le domande: questionario sulla percezione del Grillaio 38 3.1.4. Risultati 42 3.1.5. Conclusioni: siamo partiti da un preconcetto sbagliato? 44 3.2. Attività didattiche nelle scuole 46 3.2.1. Contatto con le scuole 46 3.2.2. Gli incontri in classe 50 3.2.3. Concorso tra le scuole: gli elaborati finali 56 3.2.3.1. Chiarimenti su alcuni lavori svolti dai ragazzi 56 3.3. Mostra itinerante sul Grillaio 80 3.4. Primo libretto divulgativo sul Grillaio: il testo 85 3.5. Secondo libretto divulgativo sul Grillaio: il testo 85 Bibliografia 100 2 1. Avvio del progetto Il progetto si propone la realizzazione di una serie di attività di tipo conservazionistico e di educazione ambientale sul Grillaio (Falco naumanni), una specie globalmente minacciata e presente in Italia, soltanto in Basilicata/Lucania, Sicilia e Sardegna. Il Grillaio è una specie minacciata di estinzione. Vive in Portogallo, Italia, Francia, Albania, Grecia, Spagna. In Italia il Grillaio è distribuito soprattutto in Puglia e Basilicata con l’80% della popolazione italiana (Palumbo 1997). 1.1. Organizzazione conferenza stampa Nel mese di febbraio 2007 si è tenuta la conferenza stampa di presentazione del progetto presso il Palazzo di città del comune di Gravina in Puglia (uno dei comuni maggiormente coinvolti nel progetto). Oltre agli ornitologi incaricati dalla LIPU (Dott. Pino Giglio e Dott Michele Bux), sono intervenuti il Sindaco della città e gli Assessori comunali all’Ambiente e alla Cultura. In quest’occasione è stato lanciato un comunicato stampa nazionale in cui è stata menzionata la Fondazione Peretti quale Ente finanziatore del progetto. La conferenza stampa è stata ripresa da una emittente televisiva (Telenorba, la più grande fra le TV private nel sud d’Italia) e la notizia del progetto è stata diffusa dagli organi di stampa locali e nazionali (cfr. Repubblica, sede di Bari, Fig. 1) da numerosi siti web locali e nazionali, permettendo la diffusione del progetto anche su scala nazionale. Fig. 1 – Un esempio di diffusione del comunicato stampa riguardo il progetto “una casa per il Grillaio” (da Repubblica del 23 febbraio 2007). 3 2. ATTIVITÀ DI CONSERVAZIONE Le attività di conservazione, secondo quanto stabilito nel progetto, sono state indirizzate a: • acquisto e costruzione delle cassette nido; • allestimento definitivo ed installazione delle stesse; • monitoraggio dei nidi artificiali occupati dal Grillaio durante la stagione riproduttiva; • verifica in un campione di controllo del successo riproduttivo del Grillaio in nidi “naturali”. 2.1. Premessa Il progetto “una casa per il grillaio – azioni pratiche per la conservazione del Grillaio Falco naumanni in Puglia e Basilicata”, ha rappresentato la più importante iniziativa di conservazione intrapresa sul Grillaio negli ultimi 10 anni nel territorio della Murgia a cavallo tra Puglia e Basilicata. In questo vasto altopiano carsico sopravvive la più importante popolazione italiana di Grillaio che presenta la peculiarità di essere quasi totalmente dipendente dall’uomo per la sua sopravvivenza. Infatti, l’intera popolazione utilizza i centri storici dei comuni della Murgia per nidificare mentre si alimenta in vaste praterie che formano le cosiddette pseudosteppe mediterranee, che circondano i centri urbani. Tale convivenza è attualmente messa in crisi dalle trasformazioni sia del mondo agricolo e zootecnico che dal cambiamento nelle tecniche costruttive e di restauro degli edifici. Soprattutto, la ristrutturazione degli edifici storici ha determinato un forte impatto sulle colonie riproduttive di Grillaio che, spesso, subivano direttamente la perdita di intere nidiate a causa della coincidenza dei lavori di ristrutturazione con la riproduzione (Fig. 2). Inoltre, per impedire l’accesso a specie molto invasive come il Colombo terraiolo, sono stati adottati criteri architettonici tali da eliminare o chiudere qualsiasi anfratto, cavità o sporgenza utile ai grillai per la riproduzione. Fig. 2 – Tipico sottotetto con decine di nidi “naturali” di grillaio. 4 Per impedire la perdita di siti di nidificazione, la Regione Puglia ha emanato un Regolamento Regionale (n. 24 del 28 settembre 2005 “Misure di conservazione relative a specie prioritarie di importanza comunitaria di uccelli selvatici nidificanti nei centri edificati ricadenti in proposti Siti di importanza Comunitaria (pSIC) ed in Zone di Protezione Speciale ZPS”), che impone a tutti i centri urbani ospitanti colonie di Grillaio e rientranti in siti ZPS di attuare delle procedure che impediscano la perdita di siti di nidificazione. Inoltre, i lavori di ristrutturazione non devono svolgersi durante la presenza di nidi attivi. Per attuare efficacemente tale regolamento è però necessario disporre di efficienti metodi alternativi che consentano di mantenere una buona disponibilità di siti di nidificazione idonei per il Grillaio. L’utilizzo di nidi artificiali è apparso fin dall’inizio uno degli strumenti di conservazione più importanti da applicare poiché risultano facili da installare, anche da non addetti ai lavori (come le maestranze edili), e soprattutto con costi accettabili. Il presente progetto di conservazione ha per la prima volta affrontato lo studio su larga scala riguardo l’utilizzo di nidi artificiali in legno da parte del Grillaio valutandone l’efficacia conservazionistica il primo anno dopo l’installazione. 2.2. Biologia, distribuzione e fattori di minaccia della popolazione apulo-lucana di Grillaio Falco naumanni 2.2.1. Biologia Specie monotipica a corologia eurocentroasiatico-mediterranea (Massa, 1992). Nel Paleartico l’areale del Grillaio è costituito da una fascia di territorio a sud del 55° parallelo N, che va dalla penisola iberica alla Cina. In Europa nidifica in Albania, Armenia, Azerbaijan, BosniaHerzegovina, Bulgaria, Croazia, Francia, Georgia, Grecia, Italia, Kazakhistan, Moldavia, Portogallo, Romania, Russia, Slovenia, Spagna, Turchia and Ucraina (Biber, 1996). Le popolazioni più consistenti sono presenti nei paesi circum-mediterranei (BirdLife International 2004). In Italia il Grillaio nidifica in Puglia, Basilicata, Sicilia e Sardegna (Brichetti & Fracasso 2003). L'analisi dell'areale di distribuzione in Italia evidenzia l'esistenza di tre distinte popolazioni: • apulo-lucana, con una superficie media occupata di 9.000 km2; • siciliana, con una superficie media occupata di 12.000 km2; • sarda, con una superficie media occupata di 8.000 km2. La popolazione apulo-lucana occupa l'intera area geografica rappresentata dall'altopiano delle Murge, in cui le Gravine dell'arco ionico e l'area della Gravina di Matera, rappresentano le propaggini sud-orientale. 5 Fig. 3 – Caratteristica ambiente steppico, ideale habitat trofico del Grillaio. In Europa viene stimata una popolazione nidificante di 25000–42000 coppie (BirdLife International 2004), la maggior parte delle quali presenti nei paesi dell’Unione Europea dove in generale la specie è ben monitorata. Essenzialmente insettivoro cattura le prede a seconda della loro disponibilità locale (Cramp e Simmons, 1980). Caccia in gruppo catturando le prede in volo o dopo una breve picchiata da un punto di osservazione. In Europa studi condotti in Spagna, Francia, Italia e Grecia hanno evidenziato l'importanza trofica degli invertebrati con Ortotteri e Coleotteri quali prede principali. In Spagna il 94% delle prede esaminate erano invertebrati e solo il 6% vertebrati (rispettivamente il 64% e il 36% della biomassa predata). Gli Ortotteri (60% delle prede) e i Coleotteri (22%), sono risultati dominanti nella dieta, seguiti da Dermatteri, Chilopodi, Aracnidi, e altri gruppi di insetti (Apidi, Formicidi, Mantidi). Tra i vertebrati vengono catturati essenzialmente piccoli mammiferi (Franco e Andrada, 1977). Numerosi altri studi hanno chiarito le abitudini trofiche in Europa, evidenziando in ogni caso l'importanza degli invertebrati e in primo luogo degli Ortotteri come preda principale del Grillaio (Palumbo 1997). In Italia sono stati compiuti studi sulla popolazione apulo-lucana e siciliana. In Puglia e Basilicata il Grillaio cattura prevalentemente Insetti (89%) e in minor misura scolopendre (4%), ragni (3%), 6 micromammiferi (3%) e Rettili (1%) (Bux et al., 1997 e Pantone e Bux, 1999)(Fig. 4). Fig. 4 – La cavalletta, una tipica specie preda del grillaio. La popolazione siciliana presenta, invece, una dieta più ricca in vertebrati che raggiungono percentuali superiori al 20% (Massa, 1981). Questi dati evidenziano le differenze comportamentali ed ecologiche di queste due popolazioni, che nidificano in habitat molto diversi. La popolazione apulo-lucana solo nei centri urbani, mentre la popolazione siciliana solo su pareti rocciose. Il Grillaio è specie migratrice, parzialmente residente in Spagna e nella Turchia meridionale. Arriva in Italia dai quartieri di svernamento, situati nell’Africa orientale sud-sahariana, a febbraio-marzo. Le colonie vengono abbandonate tra fine luglio e agosto ma la migrazione continua fino a settembre inoltrato. Un contingente di circa 20-40 individui sverna in Sicilia (Ciaccio et al., 1983), mentre 2030 individui svernano tra Basilicata e Calabria (Palumbo, 1997). Il numero degli svernanti varia da un anno all'altro in relazione alle condizioni climatiche. In entrambi i casi non è noto se si tratta di individui residenti. 7 Sono noti pochissimi dati in letteratura circa l’home range della specie. In Spagna 13 adulti seguiti con il metodo del radio-tracking, durante una stagione riproduttiva (Negro et al., 1993), hanno presentato una distanza massima percorsa tra il nido e il luogo di alimentazione di 14,5 km per la femmina e 8 km per il maschio. La superficie coperta dalle femmine ha variato da 51 a 91 km2, mentre per i maschi tale superficie ha variato da 27 a 68 km2. L'home range della colonia di 40 coppie è stato calcolato in 212 km2. Questi dati confermano, almeno in parte, quanto evidenziato per la popolazione apulo-lucana con un’area "utilizzata" intorno alla colonia, durante la fase di nidificazione, compresa tra 0-9 km (Sigismondi et al., 2003). Frequenta aree aperte, calde, secche, semi-steppiche generalmente al disotto dei 1.000 m, evitando le aree umide e forestate e le aree coltivate intensivamente in quanto necessita di elevate densità di insetti di grosse dimensioni (sopratutto Ortotteri). In parte dell'areale occupa anche aree urbanizzate utilizzate per la nidificazione (Cramp e Simmons, 1980). In Italia vive in ambienti aperti, zone stepposo-cerealicole, con ampie distese di pascoli, praterie, ambienti rocciosi, con scarsa copertura arborea e arbustiva (Massa, 1992). Frequenta durante la riproduzione anche ambienti urbani nelle sole colonie presenti in Puglia e Basilicata. Il Grillaio nidifica in cavità dei muri, sottotetti, anfratti e mensole di vecchie costruzioni (chiese, castelli, masserie, palazzi antichi) e su pareti rocciose naturali (Cramp e Simmons, 1980). Molto più rare sono le nidificazioni in cavità degli alberi, in vecchi nidi di corvidi e al suolo tra cumuli di sassi (Cramp e Simmons, 1980; Negro, 1997). In Spagna il 58% delle colonie di grandi dimensioni (> 20 coppie) sono localizzate in costruzioni storiche, come chiese, cattedrali, castelli e monasteri (Gonzàlez e Merino, 1990)(Fig.5). Fig. 5 – Un sito riproduttivo del grillaio, ubicato in una costruzione storica. 8 Nell'area mediterranea le uova vengono deposte dall'ultima settimana di aprile alla fine maggio (Cramp e Simmons, 1980). Nella penisola iberica l'inizio della deposizione è risultato essere, in media, il 26 aprile nel Portogallo meridionale (Azenha da Costa, 1995), il 29 aprile in Estremadura (Spagna) (Bijlsma et al., 1988) e tra il 5 e l'11 maggio, a seconda degli anni, in Andalusia (Spagna) (Negro, 1991). Le uova vengono deposte con intervalli di 24-48 ore e la cova inizia subito dopo la deposizione dell'ultimo uovo. La schiusa é sincrona con la covata che in media é 3-5 uova (min 2 max 8) (Cramp e Simmons, 1980). L'incubazione dura in media 28-29 giorni e se ne occupa quasi esclusivamente la femmina con brevi cambi del maschio. E' possibile una seconda covata di sostituzione in caso di perdita della prima. Il successo riproduttivo, per diverse località della penisola iberica, ha variato da 1,53 a 2,31 giovani involati/coppia che hanno deposto uova (Negro, 1997). Per l'Italia, in Sicilia la deposizione va dagli inizi di maggio alla fine di giugno (Massa, 1985) ed è stato registrato un successo riproduttivo medio di 3,5 giovani/uova deposte (Massa, 1980; Cairone, 1982; Mascara, 1984). I dati di biologia riproduttiva disponibili per Puglia e Basilicata sono più esaustivi e sono stati recentemente sintetizzati da Bux (2005). La sopravvivenza annuale degli adulti è del 71%, la sopravvivenza dei giovani nel primo anno è del 34%. Giovani involati che arrivano a riprodursi sono il 38% del totale, mentre la probabilità di un adulto di riprodursi l'anno seguente è del 92% (popolazione spagnola) (Hiraldo et al., 1996). Il fattore che più influenza la crescita di una popolazione è la sopravvivenza degli adulti seguito, in ordine di importanza, dalla sopravvivenza dei giovani, dalla produttività dei nidiacei, dalla proporzione di adulti che si riproducono e dall'età della prima nidificazione. Il Grillaio più anziano inanellato (1 maschio) aveva 9 anni (Negro, 1997). 2.2.2. Distribuzione storica A partire dalla seconda metà del 1900 il Grillaio ha subito un forte declino in tutto il suo areale di distribuzione, assumendo cosi lo status di specie Globalmente Minacciata (SPEC 1) (Collar et al., 1994). In particolare, nel Paleartico occidentale e nei paesi per i quali sono disponibili dati storici attendibili, si è assistito ad un calo spesso drammatico. La più importante popolazione, di quest'area, presente in Spagna è passata da 100.000 coppie stimate nel 1960 a 20.000-30.000 coppie nel 1980 e 4.200-5.100 coppie censite nel 1990 (Gonzàlez et al., 1990) alle 11.902-12.212 del più recente censimento (Sociedad Espanola de Ornitologia, 2000)(Fig.6). Attualmente, la popolazione spagnola mostra di aver reagito positivamente alla diverse iniziative di conservazione attuate (Pomarol, 1993) con diversi progetti di reintroduzione in corso in varie aree della Spagna. 9 Fig. 6 - Distribuzione del Grillaio Falco naumanni nel Paleartico occidentale. In Italia, pur in assenza di dati numerici storici, l’areale distributivo si è notevolmente ridotto. Nel periodo 1985-87 (Meschini e Frugis, 1993), la specie era presente in aree nelle quali non è più risultata presente nelle indagini condotte successivamente. In particolare il grillaio è scomparso in Puglia da tutte le aree esterne alle Murge e alle Gravine, mentre era stata segnalata nel Salento, sul Gargano e sull’Appennino Dauno e in Basilicata é scomparsa dalle aree più in interne del potentino e del confine calabro. In provincia di Foggia erano probabilmente presenti alcune delle più grandi colonie, soprattutto, durante la fase di massima espansione della pastorizia. Per l'area del Gargano sono note nidificazioni fino alla prima metà degli anni '80 del secolo XX, soprattutto sul versante occidentale e meridionale del promontorio, in coincidenza delle maggiori estensioni di habitat sub-steppico. 2.2.3 - Distribuzione attuale Negli ultimi anni la popolazione apulo-lucana sembra, almeno numericamente, in ripresa con censimenti di oltre 15.000 – 20.000 individui ai dormitori notturni nel periodo post-riproduttivo (Bux, in prep.). L'intera popolazione nidificante è distribuita in 17 colonie principali, di cui 14 in Puglia, nei comuni di Minervino Murge, Gravina in Puglia, Altamura, Cassano, Acquaviva delle Fonti, Santeramo in Colle, Gioia del Colle, Alberobello, Sanmichele di Bari per la Provincia di Bari, Laterza, Ginosa, Massafra, Mottola e Grottaglie per la Provincia di Taranto, e 3 in Basilicata, nei comuni di Matera, Montescaglioso e Grassano. 10 Circa l'80% delle coppie è presente nelle 5 colonie più grandi di Minervino Murge, Gravina in Puglia, Altamura, Santeramo in Colle e Matera. Negli ultimi 5 anni, la specie ha evidenziato un’espansione dell’areale occupando con piccole colonie (2-4 coppie) le pianure circostanti il Gargano e alcuni piccoli comuni al confine della penisola salentina (Fig.7). Fig. 7 – Areale distributivo del grillaio all’interno della regione apulo-lucana. 2.2.4 - Analisi critica dei fattori di minaccia La vistosa diminuzione della popolazione mondiale del Grillaio è stata attribuita, da diversi autori, ad una serie di cause che in diversa misura hanno contribuito alla scomparsa della specie da vaste porzioni del suo areale. Le cause che hanno giocato un ruolo chiave possono essere riassunte in: 1. Scomparsa degli habitat idonei nelle aree di riproduzione - La modificazione delle pratiche agricole tradizionali ha determinato un generale impoverimento della disponibilità trofica (in particolare ortotteri). I pascoli naturali e le coltivazioni non-intensive hanno subito un forte ridimensionamento sotto la spinta della Politica Agraria Comunitaria (PAC), che ha favorito le trasformazioni fondiarie, e del generale abbandono delle attività di 11 allevamento brado degli ovi-caprini. In Puglia e Basilicata, e più in generale in Italia meridionale, la pastorizia ha lasciato il posto ad attività agricole intensive (orticoltura, olivicoltura, cerealicoltura), che hanno determinato la progressiva riduzione dell'habitat trofico elettivo della specie. 2. Scomparsa degli habitat idonei nei quartieri di svernamento e nei siti di sosta migratoria - La progressiva desertificazione nell'area del Sahel, ha determinato la scomparsa di vaste aree di savana utilizzate dai grillai per alimentarsi durante le soste migratorie e durante lo svernamento. Inoltre, il prosciugamento di paludi e la regimentazione dei fiumi, ha determinato una progressiva alterazione del clima locale accelerando i fenomeni di desertificazione. Anche se i dati relativi alle aree africane di svernamento sono scarsi, la maggior parte degli studiosi ritiene che questa sia una delle cause più importanti che hanno determinato la scomparsa del grillaio da vaste porzioni del suo areale. 3. Distruzione dei siti di nidificazione - La più importante causa di perdita di siti di nidificazione, nelle colonie urbane, è rappresentata dalla chiusura e distruzione delle cavità nido durante le operazioni di demolizione e ristrutturazione. Questo può comportare, nei casi più gravi, l'abbandono della colonia riproduttiva o la riduzione della popolazione nidificante. La sub-popolazione apulo-lucana nidifica soltanto in colonie urbane e quindi risulta fortemente dipendente dalla presenza di edifici storici ricchi di cavità e con ampi sottotetti. 4. Pesticidi - Sebbene non siano emersi effetti diretti sulla specie (i livelli di PCB e metalli pesanti nelle uova di Grillaio in Spagna hanno presentato un livello inferiore al limite di pericolosità), l’eventuale presenza di pesticidi può determinare un forte impoverimento della disponibilità trofica, rendendo molte aree non più idonee all’alimentazione. L'uso incontrollato di pesticidi, soprattutto in Africa, sembra aver determinato un generale impoverimento delle risorse trofiche per la specie. 5. Competizione interspecifica - La presenza di abbondanti popolazioni di Taccola (Corvus monedula), può contribuire all'abbandono di una colonia riproduttiva, a causa del disturbo alle coppie in riproduzione e attraverso la predazione di uova e nidiacei. In diverse colonie è stata evidenziata la presenza di competizione, tra Grillaio, Taccola e Colombo torraiolo, per l'occupazione delle cavità di nidificazione. In generale, tale minaccia è da ritenersi importante solo in situazioni di scarsa disponibilità di siti di nidificazione e per piccole colonie riproduttive. 6. Disturbo e persecuzione diretta - Nell'area mediterranea la principale azione di persecuzione diretta è rappresentata dal bracconaggio, soprattutto quando l’attività venatoria 12 é consentita durante la stagione migratoria. In ogni caso, questa minaccia non sembra rappresentare attualmente un fattore importante di rischio per la specie. In Puglia le progressive trasformazioni del paesaggio agricolo, avutesi nel secondo dopo guerra, hanno determinato una forte riduzione delle aree a pascolo e la diffusione crescente di nuove tipologie di coltivazione che hanno favorito le colture intensive (vite e olivo). Questi cambiamenti oltre che eliminare direttamente habitat favorevoli alla specie hanno determinato, attraverso l'uso di biocidi, un notevole impoverimento delle popolazioni di insetti che rappresentano la risorsa trofica principale del Grillaio. L'effetto sulla popolazione locale è stato graduale con l'iniziale scomparsa delle colonie presenti a nord in Provincia di Foggia e a sud nel Salento, seguita progressivamente da una marcata rarefazione anche nell’area di presenza più importante rappresentata dall’altopiano delle Murge baresi e materane, a cavallo tra Puglia e Basilicata. In questo comprensorio, che costituisce la roccaforte italiana del Grillaio, si assiste attualmente ad un progressivo fenomeno di frammentazione e scomparsa degli habitat idonei al Grillaio. Fortunatamente, la nuova politica di gestione territoriale e, soprattutto, una nuova visione delle problematiche ambientali e di sviluppo, hanno portato alla ridefinizione dell'assetto del territorio, favorendo la conservazione e la gestione naturalistica di vaste aree. A riprova di questa nuova politica di gestione territoriale si può citare la creazione del Parco Nazionale dell’Alta Murgia in Puglia e del Parco delle Chiese rupestri del materano in Basilicata. 2.2.5. - Monitoraggio del Grillaio Falco naumanni nelle città di Gravina in Puglia, Altamura, Santeramo in Colle, Cassano delle Murge e Acquaviva delle Fonti. La conoscenza della dimensione di una popolazione rappresenta spesso l’informazione di base per avviare qualsiasi programma di conservazione. E’ necessario conoscere lo stato attuale della popolazione al fine di verificare gli effetti delle misure di conservazione e di conseguenza valutarne l’efficacia. Sulla base di tale considerazione, si è deciso di avviare un programma di censimento delle colonie di Grillaio nidificanti nei centri urbani dove si sono state avviate le misure di conservazione nell’ambito del progetto. 2.2.5.1. - Materiali e metodi Sono stati effettuati conteggi ai dormitori utilizzati dalla specie nei periodi pre- e post-riproduttivi nelle colonie di Gravina in Puglia, Altamura, Santeramo in Colle, Cassano delle Murge e Acquaviva delle Fonti in provincia di Bari. 13 La stima del numero di coppie nidificanti in queste due colonie è stata ricavata considerando una percentuale di individui non riproduttivi variabile tra il 10 e il 20% (Bux, in prep.). I conteggi ai dormitori notturni sono stati effettuati sia nel periodo pre-riproduttivo nei primi 15 giorni di maggio, che nel periodo post-riproduttivo, tra l'ultima settimana di luglio e la prima di agosto. 2.2.5.2. - Risultati La stima del numero di coppie nidificanti nelle diverse colonie studiate nel corso del 2007 è compreso tra 2784–3132. In Tab.1, si riportano i dati relativi a ciascuna colonia riguardo il numero di individui e la stima delle coppie nidificanti. Tab. 1 - Risultati dei conteggi pre-riproduttivi ai dormitori e stima della coppie nidificanti. Colonia N° ind. Stima coppie nidificanti Gravina in Puglia 2680 1072 - 1206 Altamura 1832 733 - 825 Santeramo in Colle 1468 587 - 661 Cassano delle Murge 453 182 - 204 Acquaviva delle Fonti 72 29 - 32 6505 2784 - 3132 Totale La colonia di maggiori dimensioni è risultata quella di Gravina in Puglia per cui si stima la presenza di 1072 – 1206 coppie nidificanti. Questa rappresenta una delle colonie di Grillaio di maggiori dimensioni presenti in Italia ed in Europa e ospita da sola circa il 10-15% dell’intera popolazione apulo-lucana. La colonia di Altamura con 733 – 825 coppie nidificanti è risultata la seconda per dimensione. Il confronto con i dati degli anni precedenti evidenzia, comunque, per Altamura un calo di circa il 15% delle coppie presenti. Tra le restanti colonie censite assume particolare rilievo Santeramo in Colle con 587 – 661 coppie nidificanti, mentre le colonie di Cassano delle Murge e Acquaviva delle Fonti hanno numerosità ben al disotto delle 500 coppie. 2.2.5.3. - Conclusioni La popolazione di Grillaio nidificante nelle 5 colonie studiate, rappresenta una porzione significativa della popolazione italiana ed europea. Infatti, essa rappresenta ben il 45-50% dell’intera popolazione nazionale (Palumbo, in Spagnesi e Serra, 2002; Bux, in prep.) e il 10-15% della popolazione europea (BirdLife International, 2004). 14 2.3. - Analisi della biologia riproduttiva del Grillaio Falco naumanni utilizzando le cassette nido artificiali. 2.3.1. - Introduzione Il Grillaio si riproduce in cavità su pareti rocciose o su manufatti di origine antropica e più raramente al suolo (Cramp & Simmons, 1980; Vlachos et al., 2004). In alcune aree di riproduzione è strettamente antropofilo, nidificando principalmente all’interno dei centri urbani (Negro, 1997; Palumbo, 1997; Bux, 2005), situazione prevalente nelle colonie di Puglia e Basilicata, dove rarissimi sono i casi di nidificazione in aree rurali o in contesti naturali. Le conoscenze attuali sulla biologia riproduttiva del Grillaio derivano essenzialmente dagli studi condotti in Spagna (Negro, 1997) e in minima parte negli altri paesi europei, tra cui l'Italia (Massa, 1980; Cairone, 1982; Mascara, 1984; Palumbo, 1997; Bux, 2005 e 2007). I dati disponibili per la Puglia e la Basilicata sono stati sintetizzati da Bux (2005). I grillai rioccupano la colonia dalla seconda metà di marzo, anche se i primi avvistamenti possono aversi già a febbraio. In maggio vengono registrate oltre il 90% delle deposizioni del I uovo, con un picco (53%) nell'ultima decade. La covata media è di 3,7 ± 0,14 ed è cosi ripartita: 3 (6%) di un uovo, 2 (4%) di due, 11 (22%) di tre, 28 (55%) di quattro, 6 (12%) di cinque e 1 (2%) di sei. L'incubazione inizia dopo la deposizione del III - IV uovo è ha una durata di 29,7 ± 0,46 gg. Il tasso di schiusa risulta pari all’88%, determinando una nidiata media alla schiusa di 3,3 ± 0,23 uova. Il 60% delle schiuse si ha nella seconda decade di giugno. Il successo riproduttivo (n. juv. involati/n. di coppie che hanno deposto) è pari a 2,4. Le principali cause di fallimento totale della nidificazione è dovuta alla predazione della covata da parte di Taccola Corvus monedula, Ratto nero Rattus rattus e Gatto domestico (Felis catus domesticus). Uno degli scopi del progetto è quello di verificare tramite l’installazione di cassette nido artificiali, il tasso di occupazione ed il successo riproduttivo delle stesse in confronto ai nidi “naturali”. 15 2.3.2. Acquisto del materiale per la costruzione delle cassette nido Il materiale in legno è stato acquisito tramite una ferramenta in Gravina in Puglia e consegnato al Dott. Pino Giglio che ha assemblato il materiale grezzo. 2.3.3. Realizzazione ed installazione dei nidi artificiali 2.3.3.1. Metodo di installazione I nidi artificiali sono stati realizzati sulla base dell’esperienza maturata nel corso degli anni dal Dott. Pino Giglio, che dalla fine degli anni ‘90 aveva iniziato tale attività su scala locale utilizzando materiale diverso ad esempio per quanto riguarda il tetto delle cassette nido (Fig. 8). Fig. 8 – Primi nidi artificiali costruiti con i “coppi” e realizzati a Gravina in Puglia. 16 Il materiale di legno grezzo consegnato presso la sezione LIPU di Gravina ed é stato completato con l’aggiunta di una guaina impermeabile sul tetto (in precedenza venivano usati dei coppi, cfr. Fig. 2), un elemento che ha fornito una maggiore protezione e durata alla struttura (Fig. 9). Fig. 9 – Il nuovo modello di cassetta nido Inoltre, sono stati posizionati dei piedini al vertice dei quattro lati della cassetta nido che hanno permesso di sollevare la stessa da terra così da evitare il contatto diretto al suolo e preservandola dall’umidità. Il foro di accesso per il grillaio, dal diametro di 6 cm, ha permesso solo a questi ultimi di occupare la cassetta nido, rendendola selettiva ed escludendone l’uso da parte ad esempio dei piccioni Columba livia var. domestica, una specie che convive in città con il Grillaio. Una finestrella laterale, del diametro di 10 cm, con copertura a scorrimento girevole, realizzata o a destra o a sinistra a seconda del luogo di installazione, ha permesso una migliore ispezione della cassetta nido facilitando le operazioni di pulizia e l’eventuale inanellamento dei pulli. Ogni cassetta nido è stata numerata per facilitare le operazioni di identificazione durante la fase di monitoraggio delle stesse durante la stagione riproduttiva. Già dal mese di ottobre 2006 sono stati presi i necessari contatti per avere la disponibilità dei siti dove poter collocare le cassette nido. Per gli edifici pubblici (scuole, comuni, Ente Parco Nazionale 17 dell’Alta Murgia), è stato necessario formalizzare una richiesta di disponibilità con un’istanza scritta, rallentando in alcuni casi le operazioni di installazione dei nidi a causa dei ritardi nell’ottenimento delle autorizzazioni. L’installazione dei nidi artificiali è iniziata il 22 febbraio 2007, ed è proseguita per tutto il mese di marzo, mentre ad aprile sono state collocate quelle cassette nido per le quali all’ultimo momento sono venuti meno i siti previsti. Infatti, alcuni siti di installazione sono imprevedibilmente venuti meno proprio nel periodo febbraio-marzo 2007, per lavori di ristrutturazione sugli edifici interessati, che hanno comportato la collocazione tardiva di circa 65 cassette nido (32,5% del totale), per molte delle quali non è stato possibile scegliere una collocazione migliore. Tale ritardo ha probabilmente influito sulla percentuale di occupazione, sebbene in due casi, uno ad Altamura ed uno ad Acquaviva, è stata registrata la nidificazione o la frequentazione delle cassette nido installate rispettivamente il 13 e il 14 aprile 2007. Su un’apposita tabella sono stati riportati i dati relativi all’ubicazione di ogni cassetta nido, ovvero: numero progressivo, coordinate geografiche, indirizzo edificio, nome e numero di telefono del referente (necessario per le scuole ed altri edifici pubblici), data di installazione (Tab. 2). Tab. 2 – Ubicazione nidi artificiali per città. Tabella ubicazione nidi artificiali Città: n°nido Data coordinate geografiche indirizzo e proprietà edificio (pubblico/privato) nome referente telefono 2.3.3.2 - Materiali e metodi sui parametri riproduttivi Sono stati installati 200 nidi artificiali. I nidi sono stati installati nelle città di Gravina in Puglia (n=102, 51% del totale), Altamura (n = 50, 25% del totale), Acquaviva (n = 22, 11% del totale), Cassano (n =12, 6% del totale), Laterza (n = 14, 7% del totale). Sono stati raccolti i principali parametri riproduttivi (dimensione covata, data deposizione, successo di schiusa, successo riproduttivo (n. juv. involati/n. di coppie che hanno deposto). Un nido è stato considerato occupato solo quando è stata osservata la deposizione di almeno un uovo. Solo per Gravina in Puglia dove è stato collocato il maggior numero di nidi artificiali, è stata riportata la distribuzione dei nidi nell’ambito del centro urbano (Fig. 10). 18 La legenda della distribuzione dei nidi artificiali a Gravina in Puglia: Punto rosso: nidi artificiali non occupati Punto verde: nidi artificiali occupati o visitati Punto blu: nidi artificiali collocati prima del 2006 (al di fuori di questo progetto) La grandezza del cerchio indica il numero di nidi per sito: cerchio piccolo 1-2 nidi cerchio intermedio 3-6 nidi cerchio grande 7-10 nidi In verde sono indicati i dormitori urbani, tre dei quali sono utilizzati sia nel periodo pre-riproduttivo che nel periodo post-riproduttivo. Fig. 10 - Distribuzione dei nidi artificiali a Gravina in Puglia In Tab. 3 di evidenzia la scheda di monitoraggio dei nidi artificiali con: nido, esposizione, la data del primo, secondo, terzo, quarto e quinto controllo delle uova e dei nidi. 19 Tab. 3 -Scheda monitoraggio nidi artificiali città anno 1° controllo 2° controllo 3° controllo 4° controllo 5° controllo nido esp.ne data uova pulli data uova pulli data uova pulli data uova pulli data uova pulli 20 Per nidi visitati dal Grillaio, si intendono quelli nei quali sono state trovate solo tracce di frequentazione da parte della specie, ovvero segni del suo passaggio all’interno del nido (segni delle zampe sul terriccio interno), presenza di borre, resti di prede. Per nidi occupati si intendono quelli nei quali è avvenuta la deposizione ed è stato effettuato il ciclo riproduttivo. Per nidi tardivi si intendono quelli installati nel mese di aprile. Tutti e 200 i nidi artificiali installati per il progetto sono stati controllati almeno due volte tra il 15 maggio e il 20 giugno. In tale periodo si concentra infatti la fase di deposizione (dal 15 a 30 maggio) e la prima fase di allevamento dei pulli. Se in tale periodo non veniva osservata nessuna deposizione il nido non era più sottoposto a controllo. Inoltre, gli stessi parametri sono stati raccolti su di un campione di 37 nidi “naturali” presenti nelle colonie riproduttive di Gravina in Puglia e Altamura e su 10 nidi artificiali installati nel 2004. Ogni sito di nidificazione occupato è stato classificato come appartenente ad una delle 4 categorie: a) sottotetto, b) sporgenza, c) cavità, d) nido artificiale (Fig. 11a,b,c) Tutti i dati sono espressi come media ± ds (deviazione standard). Fig. 11a: Nido di Grillaio Falco naumanni in un sottotetto (Gravina in Puglia, 2007). Le uova vengono deposte sul pavimento in piccoli conche creata dalla femmina con le zampe. 21 Fig. 11b - Nido di Grillaio Falco naumanni in una cavità su di muro perimetrale (Gravina in Puglia, 2007). Per la gran parte non sono raggiungibili dall’interno degli edifici. Fig. 11c - Nido artificiale di Grillaio Falco naumanni in cassetta di legno posizionata su di un solaio di un edificio moderno (Gravina in Puglia, 2007). 22 2.3.3.3. Risultati sull’occupazione delle cassette nido artificiali Complessivamente 16 cassette nido sono stati occupati dalla specie (8% del totale), mentre 39 sono stati visitate (Tab. 4). 11 nidi sono stati occupati a Gravina in Puglia (10,8% del totale), 2 ad Altamura (4% del totale), 6 ad Acquaviva delle fonti (13,6% del totale), mentre nessuna cassetta nido è stato occupata dalla specie a Cassano delle Murge e Laterza. Tab. 4 – Tabella riepilogativa dei 200 nidi artificiali installati a Gravina in Puglia (Ba), Altamura (Ba), Acquaviva delle fonti (Ba) , Cassano delle Murge (Ba) e Laterza (Ta). Gravina in Nidi artificiali Puglia Altamura Acquaviva Installati 102 50 22 Visitati dal Grillaio 30 (29,4%) 2 (4%) 6 (27,3%) Occupati dal Grillaio 11 (10,8%) 2 (4%) 3 (13,6%) N. siti/edifici utilizzati 27 8 3 N. siti/edifici frequentati 12 1 2 N. siti edifici occupati 8 1 1 Cassano 12 0 0 1 0 0 Laterza 14 0 0 2 0 0 totale 200 39 (19,5%) 16 (8%) 41 15 10 In Tab. 5 si riportano i dati riguardanti le cassette nido effettivamente occupate nelle quali vi è stata la deposizione di uova (n = 16). Sono state deposte complessivamente 53 uova, sono nati 18 pulli, e di questi 11 si sono involati. Nei casi di nidi frequentati, sono stati rinvenuti borre, resti alimentari o piume. Il tasso di occupazione di 10 nidi artificiali installati da almeno 3 anni è stato invece pari al 60%, evidenziando chiaramente l’importanza che tali strutture assumono nel tempo e come vengano pienamente utilizzate dopo alcuni anni dall’installazione. Tab. 5 – Numero cassetta nido, uova deposte, pulli nati, involati e disturbo per singolo nido nel 2007. uova nido n° deposte pulli nati involati Disturbo 1 4 1 0 No 3 3 2 2 No 5 4 1 0 No 9 3 3 2 No 10 3 0 0 No 23 5 3 3 No 28 3 1 1 No 23 31 6 0 0 No 34 4 3 0 No 55 3 0 0 No 66 3 1 0 Si 141 2 2 2 No 142 3 1 1 No 97 1 0 0 Si 98 5 0 0 Si 101 1 0 0 Si 53 18 11 La percentuale di nidi frequentati è stata del 19,5 % (39 nidi). Se si escludono dal calcolo 65 nidi installati tardivamente e quindi considerando solo 135 nidi collocati, la percentuale di occupazione aumenta all’11,9 %. Se si considera il numero di siti/edifici sui quali sono stati installati i nidi, pari a 41, e si calcola la percentuale dei siti occupati si ottiene un valore pari al 24,4 % (10 siti). Delle 16 cassette nido occupate, (Fig. 12), 4 hanno avuto un certo disturbo dovuto a lavori di ristrutturazione dell’edificio sulle quali erano state collocate le cassette nido. Ciò ha probabilmente determinato l’abbandono della covata (successo riproduttivo nullo), ed impedendo ovviamente anche che altre cassette nido collocate in questi siti potessero essere occupate. Fig. 12 – L’interno di una cassetta nido artificiale con una femmina adulta e quattro pulli di circa 10 giorni. 24 Dai risultati ottenuti e dalle osservazioni condotte sono emersi alcuni aspetti che potrebbero contribuire all’aumento della percentuale di occupazione dei nidi artificiali e che di seguito si elencano nel dettaglio: 1- La scelta del sito/edificio dove collocare i nidi, deve essere fatta preferendo quelli nelle cui vicinanze (100-200 metri) è già presente qualche coppia di grillaio nidificante; 2- Occorre assicurarsi che sull’edificio scelto, non siano in programma lavori di ristrutturazione durante la stagione riproduttiva, in tal caso occorre evitare di installare i nidi oppure scegliere una parte dell’edificio non interessata dai lavori di ristrutturazione che arrecano inevitabilmente disturbo; 3- Per la collocazione del nido è auspicabile la preferenza di un lato del tetto o lastrico solare che sia parzialmente ombrato per evitare eccessiva insolazione ed innalzamento della temperatura all’interno della cassetta nido che possa portare a sofferenza i pulli; 4- Collocare i nidi preferibilmente entro il mese di febbraio-marzo, ma possibilmente entro gennaio, poiché le installazioni effettuate dal mese di aprile non producono risultati utili. Per quanto menzionato e verificato durante la stagione riproduttiva 2007, si consiglia quindi di effettuare una ridistribuzione delle cassette nido per le quali sono risultate scarse le probabilità di essere occupate. In alcuni casi, potrebbe essere necessaria una manutenzione dei nidi maggiormente esposti alle intemperie. 25 2.3.3.4. Confronto tra siti di nidificazione naturali e cassette nido: risultati e discussione. Metodi. In totale nel 2007 sono state seguite 58 nidificazioni, di cui 14 nei nidi artificiali installati per il progetto, 6 nei nidi artificiali installati da almeno 3 anni e 38 in siti “naturali”. In totale sono stati controllati 27 (47%) siti di nidificazioni appartenenti alla categoria a (sottotetto), 11 (19%) alla categoria c (cavità) e 20 (34%) alla categoria d (cassette nido artificiali). Non sono stati registrati casi di nidificazione su sporgenze (ad es. cornicioni). Il confronto statistico fra la dimensione media della covata ed il successo di schiusa nelle tre tipologie prese in considerazione è stata effettuata con il test one-way ANOVA. Dimensione della covata La covata media è stata per tutti e 58 le nidificazioni controllate (nidi artificiali 2007, nidi artificiali 2004, e “naturali”), pari a 3,9 ± 1,17 uova (N = 58) ed è stata cosi ripartita: 1 (2%) di un uovo, 4 (9%) di due, 15 (26%) di tre, 20 (34%) di quattro, 13 (22%) di cinque, 3 (5%) di sei e 1 (2%) di sette (Fig. 13a). Per i nidi nei sottotetti (tipologia - a) il suo valore è stato pari a 3,81 ± 1,36 (N = 27); per i nidi in cavità (tipologia - c) la covata media è stata di 4,00 ± 0,77 (N = 11), mentre per i nidi artificiali (tipologia - d) è stata pari a 3,95 ± 1,10 uova (N = 20), non evidenziando variazioni statisticamente significative tra le 3 tipologie di siti considerati (one-way ANOVA F2,55=0,1268, P=0,88 – Fig. 13 b). 22 20 18 No. di osservazioni 16 14 12 10 8 6 4 2 0 0 1 2 3 4 5 6 7 dimensione covata 26 Fig. 13a - Frequenza dell'andamento della dimensione della covata del Grillaio Falco naumanni per 58 nidificazioni seguite nel 2007. La variabile assume un andamento tendente alla normalità (test KolmogorovSmirnov d=0,17331, p<0,10). 5,0 4,8 4,6 4,4 covata 4,2 4,0 3,8 3,6 3,4 3,2 3,0 a d c Tipo_nido Fig. 13b - Dimensione della covata del Grillaio Falco naumanni per ciascuna delle 3 tipologie di siti di nidificazione considerati - a) sottotetto, c) cavità, d) nido artificiale. In maggio sono state registrate oltre il 90% delle deposizioni del I uovo, con un picco nella seconda decade. La deposizione più precoce si è avuta il 9 maggio, mentre la più tardiva il 3 giugno. Successo di schiusa Il successo di schiusa è stato pari al 67% (N = 52), determinando una nidiata media alla schiusa di 2,56 ± 1,33 uova (N = 52). Il 63% delle schiuse si è avuto nella seconda decade di giugno. L’analisi differenziale in base alle tre tipologie di siti di nidificazione riscontrate evidenzia che i nidi in cavità hanno avuto un maggior successo di schiusa, pari a 3,10 ± 0,74 uova (N = 10), rispetto sia ai nidi nei sottotetti con 2,52 ± 1,31 (N = 23) uova schiuse che ai nidi artificiali con 2,32 ± 1,56 (N = 19) uova schiuse. Tale variabilità non è, comunque, statisticamente significativa (one-way ANOVA F2,49=1,1531, P=0,32 – Fig. 13c). 27 4,5 4,0 uova_schiuse 3,5 3,0 2,5 2,0 1,5 1,0 a d c Tipo_nido Fig. 13c - Successo di schiusa delle covate di Grillaio Falco naumanni per ciascuna delle 3 tipologie di siti di nidificazione considerati - a) sottotetto, c) cavità, d) nido artificiale. Accorpando le due categorie di nidi “naturali”, sottotetti e cavità, e confrontandoli con i nidi artificiali, non emerge una variazione statisticamente significativa (t-test, t50=0,99 P=0,326 – Fig. 13d). 28 4,5 4,0 3,5 uova_schiuse 3,0 2,5 2,0 1,5 1,0 0,5 x z Mean Mean±SE Mean±SD nidi naturali vs nidi artificiali Fig. 13d - Confronto tra il successo di schiusa dei nidi naturali (Z = sottotetti + cavità) e dei nidi artificiali (X). Successo riproduttivo Il successo riproduttivo (n. juv. involati/n. di cp. che hanno deposto) totale, calcolato su tutte le tipologie di nido, è stato pari a 1,9 (N = 45) e non ha evidenziato variazioni statisticamente significative (Kruskal-Wallis test: H = 4,681 df = 45 P=0,0963). L’analisi differenziale per ciascuna tipologia di nido, evidenzia la presenza di un’ampia variabilità per i nidi nei sottotetti e per i nidi artificiali, a differenza di quel che accade per i nidi nelle cavità. Questi ultimi evidenziano un successo riproduttivo di 2,70 ± 0,82 (N = 10) ben superiore rispetto alle altre due tipologie di nidi; sottotetti 1,66 ± 1,14 (N = 18) e nidi artificiali 1,82 ± 1, 47 (N = 17). Il confronto a coppie consente di evidenziare come le cavità presentino un successo riproduttivo statisticamente più alto rispetto ai sottotetti (Mann-Whitney U Test, U = 36 P = 0,035) ma non rispetto ai nidi artificiali (Mann-Whitney U Test, U = 54 P = 0,119). In quest’ultimo caso l’ampia variabilità del successo riproduttivo nei nidi artificiali tende a nascondere possibili differenze legate a diversi livelli di sicurezza del sito (Fig. 13e). 29 4,0 3,5 Successo riproduttivo 3,0 2,5 2,0 1,5 1,0 0,5 0,0 d a c Mean Mean±SE Mean±SD tipo_nido Fig. 13e - Box-plot con i valori del successo riproduttivo registrati nelle 3 tipologie di nidi considerate. 2.3.3.5. Conclusioni Il tasso di occupazione dei nidi artificiali installati per il progetto di conservazione non è stato particolarmente alto. In solo 16 nidi artificiali si è avuta la deposizione di almeno un uovo mentre almeno altri 23 nidi, che sono risultati frequentati dai grillai, sono stati abbandonati duranti le prime fasi della riproduzione. Come hanno ampiamente evidenziato numerosi studi sull’utilizzo di cassette nido da parte dei passeriformi (Lack 1955, 1958, Perrins 1979, Ulfstrand et al. 1981), il tasso di occupazione nel primo anno non è mai elevato ed è spesso necessario attendere 1 o 2 anni, affinché queste strutture vengano pienamente accettate dagli uccelli. Ciò si riscontra anche per il Grillaio. Infatti, dei 10 nidi artificiali presenti da almeno 3 anni ben 6 sono stati occupati (60%). Inoltre, durante gli studi sulla biologia riproduttiva della colonia di Santeramo in Colle, condotti tra il 2003 e il 2005, sono stati registrati tassi di occupazione del 12% nel primo anno, del 38% nel secondo e del 58% nel terzo (Bux et al., 2005). Inoltre, gli studi finora condotti evidenziano che la tendenza ad occupare siti nuovi (come i nidi artificiali), sia condizionata fortemente dall’andamento della stagione riproduttiva. 30 In pratica, gli anni in cui si registrano valori bassi nel tasso di schiusa e nel successo riproduttivo, a causa di stagioni metereologicamente instabili o per carenza di cibo, sono anche gli anni in cui minore è l’utilizzo dei nidi artificiali (Bux in prep.). Il confronto dei principali parametri riproduttivi tra le diverse tipologie di sito di nidificazione sembra confermare tale ipotesi. Infatti, sebbene i parametri riproduttivi fatti registrare dai nidi artificiali non appaiono mai i migliori, questi non variano in maniera significativa rispetto ai siti naturali quali cavità e sottotetti. Soprattutto rispetto a questi ultimi i nidi artificiali sembrano del tutto equiparabili. In Fig 14, si riportano i valori a titolo di esempio di due parametri riproduttivi dal 2003 al 2007 quali, dimensione media della schiusa e la percentuale del tasso di schiusa. Il 2007 è stato l’anno con la peggiore performance riproduttiva negli ultimi 5 anni. 100 7 90 5 80 4 70 3 60 tasso di schiusa (%) dimensione nidiata alla schiusa 6 2 50 1 0 40 2003 2004 2005 2006 2007 anni Fig. 14 - Andamento della dimensione della nidiata alla schiusa e del tasso di schiusa nel quinquennio 20032005. In sintesi, è stato osservato che i nidi artificiali in legno, rappresentano un’azione di conservazione utile a limitare la scomparsa dei siti di nidificazione del Grillaio e possono essere utilizzati con successo in quelle situazioni in cui occorra intervenire rapidamente come nel caso di edifici in ristrutturazione. Appare altresì necessario proseguire con il monitoraggio dei nidi al fine di valutare il reale tasso di accettazione di tali strutture ed eventualmente valutare alcuni miglioramenti nella progettazione e nel posizionamento dei nidi. 31 Ringraziamenti Per aver permesso l’installazione dei nidi: Angela Capone ed Emanuele Caroselli, Pasqua Capone, coop. Questa Città, Antonella Deveteris, Francesca Festa, Franco Gesualdo, Graziano e Achille Granieri, Gino Laddaga, Nicola Lagreca, Giuseppe Lorusso, Mariapia Matera, Mimmo Misciagna, Vincenzo Paterno, Franco Taccogna, Enzo Tremamunno, Parco nazionale dell’Alta Murgia, comune di Gravina, comune di Altamura, Ass.ne Torre di Nebbia, scuola elementare Scacchi (Gravina), scuola elementare Padre Pio (Gravina), scuola elementare Soranno (Gravina), scuola elementare Nardone (Gravina), scuola media statale Santomasi (Gravina), scuola media statale Montemurro (Gravina), Polizia Municipale di Gravina, scuola media statale Ruffo (Cassano), scuola media statale De Amicis (Acquaviva), scuola elementare Don Milani (Altamura), scuola elementare Madre Teresa di Calcutta (Altamura), scuola elementare Roncalli (Altamura), ITG Nervi (Altamura), liceo classico Cagnazzi (Altamura), liceo scientifico Federico II di Svevia (Altamura), scuola media statale Giovanni XIII (Acquaviva), comune di Laterza. Per aver collaborato: Vincenzo Artal, Filippo Bellini, Salvatore Cilifrese, Nicola e Marisa Cillo, Saverio D’Erasmo, Gelly de Leonardis, Vittorio Giacoia, Mimmo Lapolla, Mina Lorusso, Giuditta Maletik, Stefania Pellegrino, Giacinto Squeo, Luca Trionfo, Maria Tucci, Amedeo Visci, Roberto Zuccaro. Un ringraziamento particolare al dott. Tommaso Piarulli che da più anni permette di accedere all’ampio sottotetto dell’edificio di sua proprietà, adatto alla nidificazione di diverse decine di coppie di grillai. 32 2.3.4 Studio sulla rete trofica e sul foraggiamento del Grillaio Falco naumanni: risultati preliminari 2.3.4.1. Introduzione Il Grillaio Falco naumanni è un piccolo falco dalle abitudini coloniali associato ad habitat aperti dove è prevalente una vegetazione di tipo erbaceo con scarsa o nulla presenza di copertura arborea (Dell’Hoyo et al., 1994). La dieta si basa principalmente su artropodi di medie e grandi dimensioni come Ortotteri, Coleotteri, Scolopendre che vengono catturate al suolo (Cramp e Simmons, 1980; Negro et al., 1997) dopo un breve “tuffo” successivo all’individuazione della potenziale preda. L’attività di ricerca delle prede avviene soprattutto in volo con gli uccelli in “hovering” ad altezze dal suolo variabili, ma generalmente comprese tra i 5 e i 25 metri. I grillai in attività di foraggiamento sono perciò facilmente osservabili ed è possibile seguirne il comportamento. Questo capitolo illustra i primi risultati in forma sintetica sull’attività di ricerca svolta nell’ambito dell’attività di foraggiamento. 2.3.4.2. Materiali e metodi Nei mesi di maggio-luglio sono stati individuati 3 transetti nei pressi delle colonie di Gravina in Puglia e Altamura. La loro disposizione radiale rispetto alla colonia ha consentito di poter analizzare l’effetto della distanza dalla colonia riproduttiva. Tutti i transetti hanno coinciso con le strade secondarie a bassa intensità di traffico. Attività di foraggiamento I campionamenti sono stati effettuati ogni 500 m. In ogni punto di campionamento sono stati osservati in sequenza fino ad un massimo di 3 individui di grillaio in attività di caccia. Ciascun individuo focale è stato seguito per 3 minuti registrando, su apposite schede, i seguenti parametri: 1. sesso; 2. tipo habitat utilizzato; 3. n° di full strike; 4. n° di half strike; 5. n° di strike (pari alla somma di 3+4); 6. n° di strike con cattura preda; 7. % di successo dei strike (pari a 6/5). Sono stati ritenuti buoni individui focali solo quelli presenti al momento della prima osservazione entro un raggio di 250 m dal punto di campionamento. La registrazione dei parametri è stata 33 ritenuta valida se l’individuo focale si manteneva entro i 500 m di raggio dal punto di campionamento e se non cambiava tipologia di habitat. Sono stati considerati in attività di foraggiamento solo gli individui in volo e in evidente attività di ricerca, mentre gli individui in volo veloce e direzionale o gli individui posati non sono mai stati considerati. Disponibilità trofica Sono state individuate 8 aree di campionamento per la valutazione della disponibilità trofica in ortotteri e coleotteri. Le otto aree di campionamento sono state scelte casualmente nei pressi dei transetti selezionati per lo studio del comportamento trofico. In ciascuna delle 4 tipologie di habitat presenti (Tab. 6) sono state selezionate due superfici che sono state controllate ogni 15 gg. Il campionamento è stato effettuato utilizzando un retino a sfalcio in aree di forma quadrata di 2 m di lato. L’abbondanza di ortotteri e coleotteri è stata espressa in termini relativi: n° di esemplari campionati in ogni raccolta in rapporto al numero totale di esemplari campionati. 2.3.4.3. Risultati Attività di foraggiamento In totale sono state effettuate osservazioni su 827 individui in attività di caccia, di cui 511 (62%) sono risultate valide in quanto l’individuo focale non è scomparso alla vista (rimaneva entro un raggio di 500 m dall’osservatore) e non ha cambiato l’habitat di caccia. I parametri comportamentali osservati relativi all’attività trofica sono riportati in Tab.6. Tab. 6 - Comportamento trofico del Grillaio Habitat Parametro n° di ind. in caccia ind. in caccia che hanno effettuato strike n° di strike n° di half strike n° di full strike n° di strike con cattura preda % di successo strike pascoli naturali seminativi non irrigui incolti 243 203 297 37 260 188 63 219 101 148 12 136 61 41 32 11 27 4 23 9 33 Erborato (oliveti e mandorleti) 17 3 9 0 9 0 0 Totale 511 318 481 53 428 258 54 L’analisi preliminare dei dati evidenzia l’importanza dei pascoli naturali inquadrabili fitosociologicamente nell’associazione Festuco-Brometalia e in minor misura nella TheroBrachypodietea, che costituiscono gli habitat chiave delle pseudosteppe mediterranee. 34 Il successo di cattura è stato pari al 63% superiore a quello fatto registrare nei restanti habitat campionati. Particolare importanza hanno assunto anche i seminativi non irrigui con un successo di cattura del 41%, sebbene il dato necessiti di una più attenta interpretazione. Infatti, importante sembra la disposizione della patch (“macchie”) di seminativo nei confronti dei pascoli naturali. Le patch circondate o inserite in un contesto a maggiore presenza di pascoli naturali sono più importanti, in termini di successo di cattura, delle aree a seminativo molto ampie. Le aree incolte, distribuite nell’area di studio soprattutto lungo i margini delle strade hanno presentato un discreto successo di cattura soprattutto se caratterizzate da vegetazione bassa. In tali fasce di incolto sono state osservate numerose predazione da parte di individui inizialmente posati lungo i pali. Le aree arborate non appaiono idonee all’attività trofica del grillaio, anche quando sono risultate a bassa densità arborea, come spesso è stato osservato nei mandorleti e negli uliveti. Disponibilità trofica In totale sono stati effettuati 80 sfalci nel periodo aprile-agosto 2007 campionando 403 insetti (Tab. 7). L’habitat con la maggiore disponibilità trofica è rappresentato dai pascoli naturali, seguito dagli incolti e dai seminativi non irrigui. La presenza di insetti geofili negli arborati è apparsa particolarmente bassa, sebbene in tali habitat la scarsa presenza di vegetazione erbacea durante la primavera e l’estate condiziona fortemente la presenza di insetti in generale. Tab. 7 – N. insetti “raccolti” nei campionamenti nel periodo aprile-agosto 2007. Habitat Parametro Ortotteri Coleotteri Mantidi Totale pascoli naturali seminativi non irrigui Incolti 171 39 17 227 53 13 2 68 71 13 15 99 arborato (oliveti e mandorleti) 7 2 0 9 Totale 302 67 34 403 Gli ortotteri hanno rappresentato il gruppo più abbondante con circa il 75% della biomassa disponibile, sebbene la loro disponibilità temporale abbia variato ampiamente nei 5 mesi di indagine. La presenza degli ortotteri è stata particolarmente bassa fino a metà maggio con una media di circa 1,5 individui per area di sfalcio, per poi aumentare nettamente in giugno e soprattutto in luglio e agosto, quando hanno rappresentano in media il 90% della biomassa campionata. Interessante è risultata la presenza di insetti lungo gli incolti ai margini delle strade con abbondanze superiori ai seminativi. 35 3 ATTIVITÀ DI EDUCAZIONE 3.1. Il Grillaio questo sconosciuto: una valutazione della percezione e della conoscenza del Grillaio nelle popolazioni di Gravina in Puglia ed Altamura 3.1.1. Introduzione La più grande minaccia in Italia per una specie come il grillaio, dopo la distruzione dell’habitat trofico, risulta essere la distruzione da parte dell’uomo delle cavità nido, di solito localizzate nei centri urbani, in particolare nei sottotetti o cavità. L’intervento proposto dalla LIPU ha previsto, non solo l’installazione di nidi artificiali per sostituire i pertugi presenti nei sottotetti, ampliando la possibilità di trovare siti riproduttivi favorevoli, ma anche una campagna di educazione ambientale per sensibilizzare la popolazione pugliese alla conoscenza e conseguente protezione di questi piccoli rapaci in due città particolarmente importanti per la conservazione di questa specie: Gravina in Puglia e Altamura, entrambe in provincia di Bari. Queste due città si trovano a circa 10 chilometri l’una dall’altra e hanno rispettivamente 45.000 e 65.000 abitanti. Inoltre, la campagna di educazione ambientale in entrambe le città, ha compreso: - una serie di attività didattiche con le scuole: lezioni in classe e sul campo, materiali didattici sul Grillaio; - organizzazione di un concorso fra le classi per la creazione della miglior campagna promozionale di questa specie; - una mostra itinerante sul Grillaio; - un libretto con tutte le informazioni sulla specie rivolto ad un pubblico generico. Affinché la campagna di educazione ambientale fosse realmente efficace, è stato indispensabile raccogliere informazioni sulla percezione della persone riguardo il grillaio, ed in particolare nei luoghi dove si sarebbe svolto il progetto. Che cosa pensano gli abitanti di Gravina in Puglia ed Altamura del Grillaio? Ma, soprattutto, lo conoscono? Sono ancora diffuse credenze popolari su questa specie? L’opinione più diffusa tra i ricercatori, infatti, era che la gente distruggesse i nidi di Grillaio ritenendolo un animale nocivo e che ci fosse bisogno di un intervento educativo che facesse cambiare idea ai cittadini. In realtà, non é mai stato provato che la percezione di questa specie fosse effettivamente negativa nella popolazione. Si è così stabilito un piano di valutazione che indagasse sulla percezione e la conoscenza di questa specie nelle popolazioni di Gravina in Puglia e Altamura utilizzando delle interviste a campione. 36 3.1.2. Metodi Il metodo di indagine è risultata l’intervista aperta e come campione la popolazione di entrambe le città al di sopra dei 15 anni. Due intervistatori, uno per città, sono stati inviati a fermare le persone in modo casuale il sabato pomeriggio sui viali principali delle città. Il protocollo seguito dagli intervistatori è stato molto semplice: i) presentazione alla persona fermata come volontario LIPU; ii) permesso di poter fare alcune domande; iii) in caso affermativo, sono state poste le domande; iv) si riportavano direttamente le risposte sul questionario. La scelta di fare le interviste con domande aperte è stata motivata al fine di percepire meglio il pensiero degli intervistati, evitando che le domande non fossero comprese o che gli intervistati rispondessero in maniera incompleta. Sono state effettuate complessivamente 9 domande (cfr. 3.13), in modo che l’intervista non risultasse troppo lunga e gli intervistati rispondessero con la stessa completezza a tutte le domande. Sono state intervistate complessivamente 101 persone ad Altamura. Gli intervistati sono risultati così suddivisi: 49,5% donne tra i 15 e i 40 anni; 26,7% uomini tra i 15 e i 40 anni; 12% donne sopra i 40 anni; 11,8% uomini sopra i 40 anni. Sono state intervistate complessivamente 100 persone a Gravina in Puglia. Gli intervistati sono risultati così suddivisi: 33% donne tra i 15 e 40 anni; 28% uomini tra i 15 e i 40 anni; 26% donne sopra i 40 anni; 13% uomini sopra i 40 anni. 3.1.3. Le domande: questionario sulla percezione del Grillaio Di seguito si evidenziano le 9 domande tra le quali una in cui vengono mostrate 4 foto:GRILLAIO, TACCOLA, CIVETTA E POIANA (Allegato 1). • L’intervistatore ha segnato per ogni intervista fatta il luogo, l’ora e il suo nome. • L’intervistatore non ha chiesto il nome o i dati personali all’intervistato. • Nelle note l’intervistatore ha segnato una volta terminata l’intervista, il sesso dell’intervistato e la fascia d’età a cui suppone appartenga l’intervistato: 37 • 13- 20 • 20-30 • 30-50 • 50-70 • >70 • Nel caso l’intervistato risponda “No” o “non so” alla domanda n.1 si segna la risposta ma l’intervista non prosegue ( la scheda è stata analizzata ugualmente). Foglio intervista, le domande Luogo Data Ora Nome intervistatore Domanda n. 1 ) Hai mai sentito parlare di Grillaio? Sì No Non so Domanda n. 2) se sì, puoi dirmi che cos’è ? Domanda n. 3) Ne hai mai visto uno? Se non l’hai mai visto, da chi ne hai sentito parlare? Domanda n. 4) Se l’hai visto, dove? Domanda n. 5) Ora ti mostrerò 4 foto, sai dirmi quale di questi è un Grillaio? Domanda n. 6) Con quali aggettivi definiresti il Grillaio? Domanda n. 7) Puoi spiegare perché hai scelto questi aggettivi? Domanda n. 8) Ti piacerebbe vedere un nido di Grillaio? Perché? Domanda n. 9) Ti piacerebbe vedere il Grillaio nella tua città? Perché? Note 38 ALLEGATO 1 Foto questionario POIANA TACCOLA 39 CIVETTA GRILLAIO 40 3.1.4. Risultati La prima domanda che l’intervistatore ha posto riguardava se l’intervistato avesse mai sentito parlare della specie Grillaio. Questa domanda era ovviamente fondamentale per comprendere quanto fosse diffusa la conoscenza di questo rapace nelle due città. I risultati per la prima domanda sono stati simili in entrambe le città: il 60% degli intervistati a Gravina in Puglia ed il 62,3% ad Altamura non ha mai sentito parlare della specie. Il 37,7% degli intervistati che, invece, avevano sentito parlare della specie, l’intervista è proseguita con la seconda domanda, ossia l’intervistatore ha chiesto cosa fosse un Grillaio e in entrambe le città le risposte si sono rivelate corrette nella maggior parte degli intervistati. Ad Altamura, ad esempio, le risposte sono state: 57,8% un uccello; 28,9% un rapace; 13,1% un falco. A Gravina in Puglia le risposte sono state così distribuite: 48% un uccello; 38% un rapace; 14% un falco. Confermando quindi che nel campione intervistato che aveva affermato di aver sentito parlare di Grillaio effettivamente sapeva di che si trattasse. La terza domanda voleva percepire se gli intervistati che dichiaravano di sapere cosa fosse un Grillaio, ne avessero mai visto uno personalmente e di fatto la maggior parte degli intervistati ha dichiarato di averlo visto: ad Altamura, più dell’80% ricorda di averlo visto, a Gravina una percentuale minore, circa il 65% ne ha visto almeno un esemplare. Inoltre, l’intervistatore ha chiesto dove l’intervistato aveva visto il rapace, questo per comprendere se la popolazione fosse cosciente di sapere che la specie è presente in città. In particolare, gli intervistati hanno dichiarato di averlo visto volare in cielo (54%) o stazionare in campagna (20%), solo una piccola percentuale dichiara, invece, di averlo osservato in città (15%). Agli intervistati che rispondevano di non averlo mai visto personalmente, veniva chiesto come facessero, allora, a conoscerlo. In entrambe le città il 30% ne ha sentito parlare da amici o parenti, il 20% da documentari in tv, il 10% a scuola e il resto non ricorda esattamente dove lo avevano visto. Per verificare se gli intervistati avessero riconosciuto effettivamente il Falco Grillaio e non un’altra specie, sono state mostrate loro 4 foto di uccelli diversi: Poiana, Grillaio, Civetta e 41 Taccola (Allegato 1). Queste specie sono state selezionate in modo che ve ne fosse una abbastanza simile nella morfologia del Grillaio (Poiana) e altre due molto diverse ma comunque presenti e diffuse nel territorio. Come si può vedere anche dalle foto mostrate agli intervistati, la Poiana differisce visibilmente per i colori e le dimensioni e non nidifica in città. A Gravina, la maggior parte degli intervistati che avevano dichiarato di conoscere il Grillaio hanno indicato la Poiana (75,%) e solo il 20,6% ha riconosciuto il Grillaio. Una piccola percentuale ha indicato la Taccola (3,4%). In particolare, tra gli intervistati di Gravina in Puglia che avevano dichiarato anche di averlo visto, il 78,9% ha indicato comunque la Poiana. Diversa è la situazione ad Altamura, dove il 50% ha indicato il Grillaio, il 39,4% la Poiana e da alcuni che hanno indicato la Taccola (5,2%) e la Civetta (2,6%). Tra gli intervistati di Altamura che avevano dichiarato di aver visto il Grillaio, il 58% lo ha effettivamente riconosciuto. Per comprendere come il Grillaio fosse percepito dalla popolazione, si è chiesto agli intervistati di abbinare al Grillaio degli aggettivi che ritenevano rappresentarlo. Ad Altamura la maggior parte degli intervistati (80%) ha citato aggettivi positivi come “utile”, “bello”, “intelligente” e solo il 13,3% aggettivi negativi, in particolare “aggressivo”. A Gravina circa il 60% degli intervistati ha citato aggettivi positivi per il Grillaio, ad esempio “bello”, “maestoso”, “simpatico” e circa il 20% negativi, come “spaventoso”, “pericoloso”, e di nuovo “aggressivo”. In entrambe le città, si aggiunge una piccola percentuale di intervistati che ha citato aggettivi che non possono essere definiti come positivi o negativi, ma che abbiamo considerato neutri, ad esempio “silenzioso”, “piumoso”, “piccolo”. E’ stato molto importante, a questo punto, chiedere agli intervistati perché avessero scelto tale o tali aggettivi per descrivere questa specie e la maggior parte degli intervistati (62%), non è riuscito a spiegare la scelta fatta. Ad Altamura, dove era stato definito dal 20% degli intervistati come “utile”, la spiegazione riferita a quell’aggettivo è stata in riferimento all’agricoltura, specialmente perché il rapace si nutre di grilli e cavallette che si cibano nei campi coltivati. A Gravina alcuni intervistati hanno giustificato gli aggettivi negativi come “aggressivo” dicendo che il rapace metteva loro paura. Poiché il progetto educativo “Una casa per il Grillaio” prevedeva anche l’installazione di nidi artificiali sugli edifici delle due città, abbiamo voluto chiedere ai cittadini se avessero gradito di vedere un nido e la domanda è stata posta anche ai cittadini che avevano dichiarato alla prima domanda di non sapere cosa fosse un Grillaio. Tra chi conosceva già il Grillaio, l’81,5% ad Altamura gradirebbe l’installazione delle cassette nido in città; di questi il 32% per curiosità, il 22% per riuscire a vedere i pulli, il 46% dichiara di 42 volerlo vedere perché ama la natura. Tra chi, invece, non sapeva di cosa si trattasse, il 68% dichiara che avrebbe piacere a vedere un nido, il resto dichiara al contrario di non avere alcun interesse. A Gravina, invece, tra chi conosce la specie il 58,6% gradirebbe l’installazione delle cassette nido in città per vedere un nido, il 28,5% dei quali dichiarano di volerlo vedere per curiosità, il 4,7% per raccontarlo ai figli, il 14,2% perché la ritiene una bella esperienza, il resto non specifica. Tra chi aveva dichiarato di non sapere cosa fosse, invece, il 55% non ha interesse nel vedere la specie, il 9,2% avrebbe addirittura paura ad avvicinarsi. Il 34% che contrariamente vorrebbe vederlo, la maggior parte dichiara che lo vorrebbe vedere per curiosità. L’ultima domanda dell’intervista chiedeva se avessero piacere a vedere il Grillaio nella loro città. Questa domanda aveva lo scopo di approfondire l’interesse e la curiosità dei cittadini verso questo rapace, ma anche comprendere quanti di loro fossero a conoscenza di poterlo già osservare in città. Ad Altamura, il 47,3% ha dichiarato che avrebbe piacere a vederlo in città, soprattutto perché si tratta di un bell’animale (27,7%), perché fa parte dell’ambiente naturale (27,7%), qualcuno dichiara per il suo ruolo contro le cavallette (11,1%). Il 15% dichiara invece che l’animale è già presente in città. A Gravina, il 44,8% avrebbe piacere ad osservarlo in città, soprattutto perché: i) é una bella esperienza (38,4%) ii) educativa per i propri figli (7,6%). Il 13,9% dichiara invece che il rapace è già presente. 3.1.5. Conclusioni: siamo partiti da un preconcetto sbagliato? Partendo dall’idea che i nidi di Grillaio fossero distrutti intenzionalmente perché il rapace era ritenuto dannoso per gli uomini, i risultati di questo studio ci fanno trarre, invece, altre conclusioni. Innanzitutto i dati raccolti con le interviste, dimostrano che il grillaio è scarsamente conosciuto nelle due città scelte per lo studio e per il progetto di educazione ambientale. Sia la prima domanda che quelle successive volte ad approfondire e comprendere se le persone sapessero effettivamente di che uccello si trattasse, lo hanno svelato. Inoltre, dalle domande poste sembra che effettivamente la maggior parte dei cittadini non si renda conto che questa specie vive nelle loro città, anzi, dichiara che avrebbe piacere vederlo ed osservare il nido. Quindi, la maggior parte della distruzione dei nidi di Grillaio, molto probabilmente, avviene per ignoranza e non come atto voluto contro questa specie. Queste informazioni hanno sicuramente cambiato il punto di partenza e le azioni da svolgere nel progetto educativo. Non si trattava più, infatti, di far cambiare opinione alle persone sul grillaio, ma di farlo conoscere e dare loro la 43 possibilità di apprezzarlo, osservandolo. Per questo motivo, nel materiale scolastico, come anche in quello dedicato al pubblico adulto (libretto, mostra, ecc.), molto risalto è stato dato alle caratteristiche del rapace e alle sue curiosità, nonché alla tipologia di nido che il Grillaio occupa, in modo che sia riconosciuto. Sarebbe auspicabile effettuare nei prossimi 1-2 anni da questa prima intervista, un’altra valutazione delle conoscenze degli abitanti delle due città per verificare se e come la campagna di educazione ambientale abbia influito sulla percezione della popolazione su questo rapace “cittadino”. 44 3.2. Attività didattiche nelle scuole 3.2.1. Contatto con le scuole Sono state contattate complessivamente 43 scuole di cui 9 ad Acquaviva delle Fonti, 10 ad Altamura, 5 a Cassano delle Murge, 8 a Gravina in Puglia, 4 a Laterza, e 7 a Santeramo (Tab. 6). E’ stato inviato un fax al dirigente scolastico o al Preside del singolo Istituto contattato nel novembre 2006 (Allegato 2). 21 classi di 7 diverse scuole di cui 4 a Gravina in Puglia, 1 Cassano delle Murge, 1 ad Acquaviva delle Fonti ed 1 ad Altamura, hanno aderito complessivamente al progetto (Tab. 7). Fra le 21 classi che hanno aderito, 11 sono risultate della scuola secondaria di 1° grado (4 prime classi, 2 seconde classi, 5 terze classi), 10 sono risultate della scuola primaria, (6 terza classe, 1 quarta classe, 3 quinta classe). Tab. 6 – Scuole contattate durante la ricerca “una casa per il grillaio”. ACQUAVIVA SCUOLA ELEMENTARE I CIRCOLO SCUOLA MEDIA STATALE GIOVANNI XXIII SCUOLA ELEMENTARE ALDO MORO SCUOLA ELEMENTARE II CIRCOLO COLLODI SCUOLA ELEMENTARE II CIRCOLO COLLODI SCUOLA ELEMENTARE E MATERNA I CIRCOLO SCUOLA ELEMENTARE E MATERNA I CIRCOLO SCUOLA ELEMENTARE I CIRCOLO SCUOLA MEDIA STATALE A. LUCARELLI ALTAMURA SCUOLA ELEMENTARE I CIRCOLO SCUOLA ELEMENTARE VI CIRCOLO DON L. MILANI SCUOLA MEDIA STATALE S. MERCADANTE SCUOLA MEDIA EUGENIO PACELLI SCUOLA ELEMENTARE II CIRCOLO GARIBALDI SCUOLA ELEMENTARE IV CIRCOLO DIDATTICO S.G.BOSCO SCUOLA ELEMENTARE V CIRC.S.F. D'ASSISI SCUOLA MEDIA OTTAVIO SERENA SCUOLA MEDIA STATALE PADRE PIO SCUOLA MEDIA STATALE T. FIORE CASSANO DELLE MURGE SCUOLA ELEMENTARE "A. PEROTTI" SCUOLA MEDIA STATALE V. RUFFO SCUOLA ELEMENTARE SCUOLA ELEMENTARE ARMANDO PEROTTI SCUOLA MEDIA STATALE V. RUFFO GRAVINA IN PUGLIA UFFICIO DIREZIONE, V. FOSSE ARDEATINE 45 I CIRCOLO DIDATTICO S.G. BOSCO, C.MORO, 1 V. MATTEOTTI, 33 V TRIPOLI DIREZIONE V. PUNZI V. BARACCA, 62 C. MORO V. F.LLI CERVI LATERZA SCUOLA ELEMENTARE A.DIAZ SCUOLA MEDIA STATALE MICHELANGELO SCUOLA ELEMENTARE STATALE A.MANZONI SCUOLA MEDIA STATALE DANTE ALIGHIERI SANTERAMO SCUOLA ELEMENTARE DI BORGO SANTORO SCUOLA MEDIA STATALE "FRANCESCO NETTI" SCUOLA ELEMENTARE S. FRANCESCO D'ASSISI SCUOLE ELEMENTARI BALILLA SCUOLE ELEMENTARI I CIRCOLO DIDATTICO SCUOLA MEDIA STATALE FRANCESCO NITTI SCUOLA MEDIA STATALE S. GIOVANNI BOSCO Tab. 7 – Scuole e classi che hanno aderito al progetto “una casa per il Grillaio”. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 Scuola secondaria di I° grado "Benedetto XIII" Scuola secondaria di I° grado "Benedetto XIII" Scuola media statale "Don E. Montemurro" Scuola media statale "Don E. Montemurro" Scuola media statale "Don E. Montemurro" Scuola media statale "Don E. Montemurro" Scuola media statale "Don E. Montemurro" Scuola elementare "Don Saverio Valerio" Scuola Secondaria di I° grado "Vincenzo Ruffo" Scuola Secondaria di I° grado "Vincenzo Ruffo" Scuola Secondaria di I° grado "Vincenzo Ruffo" Scuola Secondaria di I° grado "Vincenzo Ruffo" Scuola elementare I° Circolo Plesso "Luciani" Scuola elementare VI° Circolo "Don Milani" Scuola elementare VI° Circolo "Don Milani" Scuola elementare I° Circolo "San Giovanni Bosco" Scuola elementare I° Circolo "San Giovanni Bosco" Scuola elementare I° Circolo "San Giovanni Bosco" Scuola elementare I° Circolo "San Giovanni Bosco" Scuola elementare I° Circolo "San Giovanni Bosco" Scuola elementare I° Circolo "San Giovanni Bosco" Via Libertà, 2 - 70024 Gravina in Puglia Via Libertà, 2 - 70024 Gravina in Puglia Via Caserta, 1 - 70024 Gravina in Puglia Via Caserta, 1 - 70024 Gravina in Puglia Via Caserta, 1 - 70024 Gravina in Puglia Via Caserta, 1 - 70024 Gravina in Puglia Via Caserta, 1 - 70024 Gravina in Puglia Via S. Pertini - 70024 Gravina in Puglia Via Mameli, 9 - 70020 Cassano delle Murge Via Mameli, 9 - 70020 Cassano delle Murge Via Mameli, 9 - 70020 Cassano delle Murge Via Mameli, 9 - 70020 Cassano delle Murge Via Luciani - 70021 Acquaviva delle Fonti Via Golgota - 70022 Altamura Via Golgota - 70022 Altamura Via V. Veneto - 70024 Gravina in Puglia Via V. Veneto - 70024 Gravina in Puglia Via V. Veneto - 70024 Gravina in Puglia Via V. Veneto - 70024 Gravina in Puglia Via V. Veneto - 70024 Gravina in Puglia Via V. Veneto - 70024 Gravina in Puglia 1A 3A 2D 1B 1E 2F 1A 5A 3A 3C 3E 3F IV E VB VC 3° 3B 3C 3D 3E 3F 20 era il numero massimo di classi che si era concordato di far partecipare. Le lezioni di presentazione del progetto e del concorso, sono state svolte tutte nel mese di marzo, eccetto una che, rinviata più volte dalle insegnanti, si è svolta il 4 maggio. 46 L'8 maggio è stata fatta una lezione, fuori programma e fuori concorso, su richiesta della preside, per 6 classi del liceo scientifico "Federico II di Svevia" di Altamura. Nel mese di maggio sono state svolte alcune escursioni sulla Murgia barese per sei classi di Gravina in Puglia e due di Cassano delle Murge. Le lezioni di presentazione sono state seguite con interesse ed entusiasmo da tutti gli studenti, anche se nonostante l’impegno non si è avuto un positivo riscontro per quanto riguarda la realizzazione dei lavori al concorso previsto. Solo una scuola ha mantenuto l'impegno di partecipazione producendo numerosi lavori. inviando un fax di trasmissione. Allegato 2 - Fax di trasmissione al Dirigente scolastico (ugualmente per il Preside) per la partecipazione al progetto “una casa del Grillaio”. Alla cortese attenzione del Dirigente scolastico La LIPU (Lega Italiana Protezione Uccelli), associazione Onlus impegnata nella tutela e conservazione della natura, ha programmato per l’anno scolastico in corso una serie di attività didattiche miranti alla conoscenza di una importantissima specie nidificante in loco, il Falco grillaio Falco naumanni. Il progetto, denominato Una casa per il Grillaio, prevede l’installazione di cassette nido per favorirne la nidificazione, interessando le scuole del territorio e incoraggiare quindi la conoscenza di questa specie minacciata di estinzione. In particolare, il programma consiste nel coinvolgimento di due classi del Vostro Istituto, preferibilmente di IV e V classe, attraverso una lezione sulle peculiarità del Falco grillaio, cui potrà fare seguito un secondo incontro sul campo per l’osservazione dei nidi. Ovviamente, sarà fornito anche del materiale educativo e informativo per facilitare ed approfondire le attività in classe. Verrà anche indetto un concorso, tra le scuole che aderiscono, per la creazione di una campagna pubblicitaria intesa a diffondere la conoscenza del Grillaio e la sua conservazione utilizzando qualsiasi forma artistica (foto, disegni, elaborati scritti, ecc.). Vi ricordiamo che la partecipazione al nostro programma non comporta costi per la scuola e per gli alunni; è una campagna realizzata dalla LIPU con il contributo della Nando Peretti Fundation. 47 Vi preghiamo di compilare e inviare, prima possibile, via fax o via mail il modulo di adesione allegato, per consentire che un nostro collaboratore possa contattarvi e programmare le attività previste che potranno partire già dal mese di novembre. Fax 080-3269748; Mail: [email protected]; cell. 347.7578517 Restiamo a disposizione per eventuali chiarimenti o informazioni, Cordialmente, Chiara Manghetti LIPU-Responsabile Settore Educazione Pino Giglio LIPU-Responsabile per le attività didattiche “Una casa per il Grillaio” Modulo di adesione Nome e indirizzo Istituto Scolastico: Classi che aderiscono all’iniziativa: Docenti di riferimento: Numeri di telefono: Vi preghiamo di compilare e inviare, prima possibile, via fax o via mail il modulo di adesione allegato, per consentire che un nostro collaboratore possa contattarvi e programmare le attività previste che potranno partire già dal mese di novembre. Fax 080-3269748; Mail: [email protected]; cell. 347.7578517 48 3.2.2. Gli incontri in classe L'incontro nelle classi è consistito nella proiezione commentata di una presentazione in power point costituita di 20 slides con testo e immagini nella quale sono evidenziati i loghi della LIPU e dell'ente finanziatore del progetto, la Fondazione Peretti. Sono state spiegate le finalità del progetto, la biologia riproduttiva del grillaio, l'importanza di questa specie a livello mondiale, la fenologia, le modalità operative del progetto “una casa per il grillaio” (Fig 15a). Sia nella prima che nell'ultima diapositiva è stato spiegato il regolamento del concorso, proprio per stimolare la partecipazione attiva dei ragazzi attraverso la realizzazione di elaborati grafici, testuali. Per alcune di queste classi è seguito un secondo incontro che è consistito in una escursione sul territorio delle Murge, ovvero l’ambiente dove è possibile osservare il grillaio nel suo ambiente naturale, al fine di far conoscere meglio ai bambini la vita del rapace. Non è stato possibile fare lo stesso per tutte le classi in quanto non tutte le scuole avevano la disponibilità di un mezzo di trasporto gratuito. Le scolaresche che hanno aderito al concorso hanno seguito con interesse ed entusiasmo la lezione fatta in classe, molti bambini per la prima volta hanno scoperto da vicino il grillaio, rendendosi conto anche della sua importanza essendo una specie minacciata di estinzione, concetto spesso di difficile comprensione se non adeguatamente spiegato. Lezioni aggiuntive, non previste dal programma di attività, sono state fatte per altre scuole che hanno fatto esplicita richiesta. Ad esempio per il liceo scientifico di Altamura, su richiesta della preside, si è organizzata una lezione per sei classi nell’auditorium della scuola. In totale sono stati circa un migliaio gli alunni che hanno assistito alla presentazione del progetto “una casa per il grillaio” (Fig. 15b). Durante l’incontro in classe è stata fornita una scheda per spiegare il progetto “una casa per il Grillaio”, descrivendo cosa prevede il progetto, scoprendo chi è il Grillaio, dove si trova , come riconoscerlo, la sua biologia riproduttiva, la migrazione e cosa magia (Allegato 3). Gli incontri nelle classi sono stati tenuti nelle seguenti date: - 20 marzo 2007: tre classi della scuola media Montemurro di Gravina (1B, 2F, 2D). Per ogni classe l'incontro è durato 2 ore circa e si è svolto nelle rispettive classi; - 21 marzo 2007: una classe (5A con regolare adesione) + altre 4 classi di quinta (fuori concorso) della scuola elementare Don Saverio Valerio di Gravina. L'incontro si è svolto nell'auditorium per tutte le classi ed è durato 2 ore; - 22 marzo 2007: due classi (5B, 5C) della scuola elementare don Milani di Altamura. L'incontro è durato 3 ore per le due classi insieme (Fig. 15c); - 23 marzo 2007: due classi (1A, 1E) della scuola media Montemurro di Gravina. Per ognuna l'incontro è durato 2 ore circa e si è svolto nelle rispettive classi; 49 - 26 marzo 2007: una classe (1F) della scuola media Montemurro di Gravina. L'incontro è durato 2 ore circa e si è tenuto in classe; - 27 marzo 2007: quattro classi (3A, 3C, 3E, 3F) della scuola media Ruffo di Cassano. L'incontro si è tenuto nell'auditorium della scuola ed è durato circa 3 ore; - 28 marzo 2007: una classe (4E) della scuola elementare Luciani di Acquaviva. L'incontro è durato 2 ore circa e si è tenuto in classe (Fig. 15d); - 29 marzo 2007: due classi (1A, 3A) della scuola media Benedetto XIII. L'incontro si è tenuto per entrambe le classi nell'auditorium della scuola ed è durato circa 2 ore; - 4 maggio 2007: sei classi terze della scuola elementare San Giovanni Bosco di Gravina. L'incontro si è tenuto nella sala di informatica dell'istituto scolastico ed è durato circa 2 ore. - 5 maggio 2007: escursione sulla Murgia del territorio di Cassano per le classi della scuola media Ruffo di Cassano. L'escursione è durata cinque ore (tutta la mattinata scolastica) e si è svolta lungo un tratturo (strada sterrata) tipico che attraversa il paesaggio murgiano. Durante l'escursione sono stati osservati i grillai in caccia nel classico volo a “spirito santo” che consentiva ai ragazzi di ammirare le capacità di volo di questa specie. Sono state inoltre, osservate anche le tipiche specie della vegetazione che compone l'habitat prioritario della murgia: la Stipa austroitalica, le orchidee, i pascoli tipici con fioritura di ferule e asfodelo. Sono state infine osservate alcune specie di insetti e vertebrati di cui il grillaio si nutre: cavallette, coleotteri, lucertole, luscengole e topo selvatico. - 8 maggio 2007: sei classi (fuori concorso) del liceo scientifico Federico II di Svevia di Altamura. L'incontro si è svolto nell'auditorium della scuola ed è durato circa tre ore. Altre escursioni non sono state effettuate per l'indisponibilità dei mezzi di trasporto da parte delle scuole. 50 Fig. 15a – Incontri in classe con presentazione in power point 15b – Centinaia di studenti hanno partecipato agli incontri in classe. 51 15c – Incontri in classe con presentazione in Power Poinr con la scuola Don Milani di Altamura 15d – Incontri per la predisposizione delle cassette nido con una classe elementare di Acquaviva 52 Allegato 3 - Scheda di approfondimento utilizzata nelle classi scolastiche Che cos’è il progetto “Una casa per il Grillaio” “Una casa per il Grillaio” è un progetto della LIPU-Lega Italiana Protezione Uccelli che prevede delle azioni pratiche per la conservazione del Falco grillaio Falco naumanni in Puglia e Basilicata grazie al contributo della Fondazione Peretti. Perché un progetto sul Falco Grillaio? La principale popolazione di Grillaio in Italia nidifica proprio nelle aree delle Murge tra Puglia e Balisicata. Le colonie di nidificazione sono tutte localizzate in centri urbani e variano da poche coppie alle oltre 800 di Matera. Questa specie nidifica in genere in cavità e sottotetti e proprio le ristrutturazioni degli edifici che non tengono conto della presenza dei nidi, creano notevoli problemi alla specie. Cosa prevede il progetto? Proprio per questo, il progetto LIPU prevede l’installazione di un totale 200 nidi artificiali in siti non accessibili e sorvegliati ed il successivo monitoraggio dei nidi e della popolazione di Grillaio. Il progetto però, vuole anche coinvolgere la popolazione locale facendo conoscere questo meraviglioso rapace. I bambini in età scolare, in particolare delle scuole elementari e medie inferiori, saranno coinvolti quindi in attività didattiche offerte gratuitamente alle scuole (un incontro in classe più una uscita sul campo). Verrà anche lanciato un concorso tra le scuole per la creazione di una campagna pubblicitaria per diffondere la conoscenza del Grillaio e come può essere protetto utilizzando qualsiasi forma artistica (foto, disegni, elaborati scritti, ecc.). Tutti gli elaborati verranno raccolti in un libretto per le scuole. Inoltre, le popolazioni locali verranno informate del progetto anche attraverso una mostra itinerante sul Grillaio, che fornirà informazioni sulla specie e sugli interventi che ogni cittadino può fare per la sua salvaguardia (mantenimento di cavità per la nidificazione, offerta di nidi artificiali, ecc). La mostra sarà offerta a tutti i Comuni delle Murge. 53 Scopriamo chi è il Grillaio Dove troviamo il Grillaio? Il Grillaio è una specie globalmente minacciata in tutto il suo areale distributivo, che comprende nell’Unione europea: Portogallo, Italia, Francia, Albania, Grecia, Spagna, paese, quest’ultimo, che ospita la popolazione più importante. Nel nostro paese la specie ha attualmente uno status di conservazione stabile o in leggero aumento. In Italia il Grillaio è distribuito soprattutto in Puglia e Basilicata (80% della popolazione italiana), ed è presente secondariamente nelle due isole maggiori: Sicilia e Sardegna. Come lo riconosciamo? Il Grillaio è un rapace di piccole dimensioni, che presenta un piumaggio con un evidente dimorfismo sessuale. Il maschio è più colorato della femmina e del giovane del 1° anno di vita. L’apertura alare è di 70-75 cm ed assomiglia ad un piccolo Gheppio brillantemente colorato, in particolare il maschio adulto ha parti superiori rosso castano brillante senza macchie, coda e testa bluastre. Le unghie sono gialle (quelle del Gheppio sono nere). Qual è la sua biologia riproduttiva? Le coppie sono monogame, restando insieme per tutta la stagione riproduttiva (anche in anni successivi). In Italia le deposizioni avvengono tra la fine di aprile e gli inizi di giugno. Le uova sono biancastre macchiettate di rossastro, con la dimensione media delle covate che varia in media da 3 a 5 uova. L’incubazione dura circa un mese ed è effettuata di giorno da entrambi i genitori e di notte dalla femmina. L’involo dei giovani avviene dopo circa 31-32 giorni dalla nascita, quindi tra la seconda decade di giugno e la prima decade di luglio. I giovani restano nella colonia per altre uno-due settimane nutriti dai propri genitori. Il Grillaio migra? Sì e durante la migrazione che lo porta a svernare in Africa sub-sahariana da ottobre a febbraio, migra spesso in gruppetti formati da diversi a centinaia di individui. Di preferenza utilizza durante la migrazioni dei passaggi obbligati come stretti o isole, che gli permettono di facilitare la traversata del mare aperto. In Italia quindi la specie si incontra da fine marzo a fine settembre. Cosa mangia? L’alimentazione è quasi esclusivamente insettivora e comprende ragni, insetti (soprattutto cavallette e coleotteri). Non tutto il materiale ingerito viene “digerito”. I peli, le penne e gli esoscheletri degli insetti, non vengono digeriti, ma, vengono espulsi dal becco (rigurgitati), formando i cosiddetti boli alimentari o borre. 54 3.2.3. Concorso tra le scuole: gli elaborati finali Per il concorso “una casa per il grillaio” sono stati realizzati 18 lavori esclusivamente da 30 ragazzi della Scuola statale secondaria di primo grado "Don Eustachio Montemurro" di Gravina in Puglia, che sono stati tutti premiati. In Tab. 6, si evidenziano i lavori realizzati per il concorso. Tab. 6 – Titolo, autore/i, tipo di lavoro e classe dell’autore dei partecipanti al concorso “una casa del grillaio”. N 1 2 3 Titolo Amici Diario del falco Il falco grillaio Autore/i Sardone Pina Tucci Olga Matera Marcella, Nuzzi Mariapia 4 Leggenda sul falco grillaio Santomasi Walter, Tarturo Vito 5 L'origine del falco grillaio 6 Falco grillaio Ruggieri Marco, Clemente Giancarlo Riviello Vincenzo 7 L'imperatore e il falco grillaio Duro Mariangela, Branà Angela, 8 Plastico cassetta nido 9 Slogan pubblicitario Squicciarini Ferdinando, Lorusso Vincenzo, Alloggio Pamela Granieri Tobia 10 Il grillaio un ospite da salvare Lombardi Mario, Laddaga Giulia, 11 Un messaggio per il falco grillaio 12 Poesia sul grillaio Tucci Olga Cilifrese Michele, Capriolo Mariapia Capriolo Mariapia 13 Slogan pubblicitario Ariano Picciallo Grazia 14 Slogan pubblicitario Aquilino Michele 15 Slogan pubblicitario D'Agostino Paola, Cicala Rossana 16 Slogan pubblicitario Porzia Daniele, Ventura Alessandro 17 Slogan pubblicitario Varvara Angelo, Larocca Domenico 18 Slogan pubblicitario Picciallo Antonio, Gramigna Teodosio Tipo di lavoro testo su file doc testo su file doc testo scansione su file jpg testo scansione su file jpg testo scansione su file jpg disegno scansione su file jpg testo e disegno scansione su file jpg In cartoncino - foto e testo jpg cartellone 100x70 foto cartellone 100x70 foto Portamessaggi foto testo scansione su file jpg testo scansione su file jpg disegno scansione su file jpg disegno scansione su file jpg disegno scansione su file jpg disegno scansione su file jpg disegno scansione su file jpg Classe 1F 2D 1E 1E 1E 3D 1E 1A 1A 1E 2D 2D 2D 2D 2D 2D 2D 3D 3.2.3.1. Chiarimenti su alcuni lavori svolti dai ragazzi 1. Il lavoro n°8 è una ricostruzione in cartoncino della cassetta nido sulle cui tre facciate, aprendo il cartoncino, sono riportate alcune fasi della vita del grillaio (le uova, i pulli e l'adulto) delle dimensioni di circa 30x20 cm. Sono poi visibili un numero (ovvero la numerazione delle nostre cassette nido che abbiamo installato) e il nome della LIPU; 55 2. Il lavoro n°11 è un box portamessaggi/portalettere realizzato in cartoncino. I ragazzi lo hanno tenuto esposto sulla porta della loro classe promuovendo e stimolando ulteriormente la conoscenza del grillaio nell'ambito di tutta la scuola. Inoltre, questo oggetto è stato esposto per tutto il periodo di una manifestazione scolastica detta: “Settimana della Sensibilizzazione”. Di seguito, si evidenziano i 18 lavori realizzati dalla scuola media Don Eustachio Montemurro di Gravina in Puglia. 56 1. Pina Sardone – 1 F – anno scolastico 2006/07 Scuola Media Statale “Don E. Montemurro” Amici L’altro giorno ero andata sul terrazzo per assistere allo spettacolo del volo di un falco, che si esibisce tutti i giorni come se stesse cercando di attirare la mia attenzione quando, all’improvviso, l’ho visto uscire da una finestrella: un piccolo falco variopinto, con una cravatta color bronzo, una coda minuscola e un piumaggio sottile. Mi sono avvicinata per toccarlo, ma non ce l’ho fatta perché ha emesso uno strano verso; a questo punto mi sono offesa e me ne sono andata nella mia cameretta. Mentre svolgevo i compiti di matematica, ho sentito un forte rumore proveniente dalla finestra aperta; mi sono spaventata e sono corsa a chiuderla: inutilmente perché, senza chiedere il permesso, era entrato in camera, e si era appollaiato sul mio bel copriletto di piume, il falchetto incravattato, dolce e morbido come un peluche e che, essendo immerso nei suoi pensieri, sembrava vivesse in un mondo incantato, ispirandomi tanta tenerezza. Con un filo di voce, rotta dall’emozione, gli ho chiesto “Piccolo, cosa ci fai qui?” “Sto cercando la felicità!” “Lo sai che non puoi stare qui,” gli ho risposto ”non è il tuo habitat naturale.” Senza replicare ed emettendo versi strazianti, sollevandosi in volo, si è diretto verso la finestra che io mi sono precipitata ad aprire, per permettergli di uscire, e lo ho visto scomparire senza alcuna spiegazione. Il pomeriggio, in seguito a quello che era successo, si è trascinato malinconicamente verso la sera, fino a che, triste e sconsolata, sono sprofondata finalmente nel sonno. Era notte fonda, quando ho sentito uno stormo di uccelli che cercava di richiamare la mia attenzione, emettendo strani suoni; senza esitare, sono corsa subito alla finestra per vedere cosa stesse succedendo, ed ho trovato, con mia grande e gradita sorpresa, una lettera il cui mittente era il minuscolo “Signor Falco”. Mi scriveva: Cara Pina, pensavo di aver trovato l’amica del cuore, ma mi sbagliavo e per questo ho deciso di abbandonare questa città. In quel momento mi è balenata un’idea: l’avrei ospitato nella soffitta della mia casa, che è un posto caldo ed accogliente, formato da tante stanze color limone, dove sarebbe stato al sicuro, accudito con amore e libero di poter uscire ogni qual volta lo avesse desiderato, per potersi librare nei cieli della città. E così è avvenuto: ogni giorno, prima di andare a scuola, passavo a salutarlo, cercando di portargli qualche buon bocconcino per la colazione, anche se le cose che preferiva mangiare mi disgustavano un po’. Con il passare del tempo, il piccolo falchetto è diventato grande ed ha finalmente trovato la sua anima gemella. Era pronto per ritornare, in sua compagnia, nel meraviglioso e suggestivo Parco dell’Alta Murgia, dove mi reco molto spesso per poterli incontrare e continuare così la nostra preziosa amicizia. 57 2. Tucci Olga Classe 2 D Scuola Media Montemurro DIARIO DEL FALCO Ciao, sono il Falco Grillaio o Falco Naumanni, più tipicamente “U’ falcunette”…ah ah! Lasciamo stare, il mio vero nome è Lilly, ho cinque “pulli”, tra noi detti, “pulcini”: Pio, Pio Pio, Pioppo, Trilly e Trillo che portano i nomi dei miei suoceri, sai com’è, per non offenderli. Ecco! Arriva mio marito: si chiama Laiolo, conosciuto nel Parco dell’Alta Murgia. Mi colpì il suo fascinoso modo di volare e la sua meravigliosa testa turchese, anche se è una dota comune, lui era speciale. Ha preso il nome da suo nonno, il nostro medico di famiglia. Mio marito alle 7, alle 12 e alle 19 va per i campi per procurarsi il cibo. Io non posso ancora uscire; sai come sono i tempi oggi, non ci si può tanto fidare di lasciare soli i piccoletti. Laiolo esce volentieri perché è tranquillo che i piccoli sono con me eppoi per i campi incontra molti suoi amici. Oggi sono proprio felice perché i miei piccoli pulli hanno compiuto 31 giorni e, finalmente, possono cominciare ad uscire di casa e volare per la prima volta. Che emozione! Speriamo che vada tutto bene e che il volo sia per loro sicuro e piacevole. Sai, io sono una migratrice e non è sempre facile trovare una casa. Qui però mi trovo bene, sono tutti ospitali ed attenti. Io adoro il centro storico, è tranquillo, le case hanno sempre un posticino sotto il tetto per noi, almeno quelle che non sono ancora ristrutturate con sistemi moderni. Pensa che quest’anno alcuni ragazzi della associazione LIPU hanno pensato di preparare per noi delle casette sui terrazzi delle case di nuova costruzione, anche in periferia. Dalla periferia è più facile raggiungere lo spazio aperto e pulito della campagna, ma per noi che siamo abitudinari, è un po’ difficile abituarci a questa nuova condizione. Alcuni nostri amici ci hanno provato e appena potrò chiederò come si sono trovati. Speriamo che non abbiano respirato smog e vissuto tra i rumori che fanno malissimo a tutta la specie, ma anche agli uomini. Adesso ti lascio perché devo accompagnare i pulli nel primo volo. Uno, due tre……ciaooo! 58 3. Matera Marcella, Nuzzi Mariapia Classe 1 E Scuola Media Montemurro IL FALCO GRILLAIO 59 4. Santomasi Walter e Tarturo Vito Classe 1 E Scuola Media Montemurro Leggenda sul Falco grillaio 60 5. Ruggeri Marco e Clemente Mastella Classe 1 E Scuola Media Montemurro L’origine del Falco grillaio 61 62 6. Riviello Vincenzo Classe 3 D Scuola Media Montemurro Falco grillaio 63 7. Duro Mariangela, Branà Angela Classe 1 E Scuola Media Montemurro 64 8. Squicciarini Ferdinando, Lorusso Vincenzo, Alloggio Pamela Classe 1 A Scuola Media Montemurro PLASTICO CASSETTA NIDO 65 66 67 9. Granieri Tobia Classe 1 A Scuola Media Montemurro Slogan Pubblicitario 68 10. Lombardi Mario, Laddaga Giulia Classe 1 E Scuola Media Montemurro Il Grillaio un ospite da salvare 69 11. Tucci Olga, Cilifrese Michele, Capriolo Mariapia Classe 2 D Scuola Media Montemurro Un messaggio per il Falco grillaio 70 12. Capriolo Mariapia Classe 2 D Scuola Media Montemurro Poesia sul Grillaio 71 13. Ariano Picciallo Grazia Classe 2 D Scuola Media Montemurro Slogan pubblicitario 72 14. Aquilino Michele Classe 2 D Scuola Media Montemurro Slogan Pubblicitario 73 15. D’Agostino Paola, Cicala Rossana Classe 2 D Scuola Media Montemurro Slogan Pubblicitario 74 16. Porzia Daniele, Ventura Alessandro Classe 2 D Scuola Media Montemurro Slogan Pubblicitario 75 17. Varvara Angelo, Larocca Domenico Classe 2 D Scuola Media Montemurro Slogan Pubblicitario 76 18. Picciallo Antonio, Gramigna Teodosio Classe 3 D Scuola Media Montemurro Slogan Pubblicitario 77 78 3.3. Mostra itinerante sul grillaio La mostra sarà realizzata su 5 pannelli 70X100, utilizzando in parte il lavoro dei ragazzi della scuola Media Montemurro ed in parte altri testi appositamente elaborati per la realizzazione della mostra. Di seguito i testi che sono stati inviati al grafico pannello per pannello. (1° PANNELLO) CHI È IL GRILLAIO Il Grillaio (Falco naumanni) è un piccolo rapace diurno con apertura alare di circa 70-75 cm. La specie presenta un notevole dimorfismo sessuale tra maschi e femmine. I maschi adulti, leggermente più piccoli delle femmine, hanno un piumaggio fortemente colorato, parti superiori del dorso castano brillante, coda e testa bluastre. Le femmine sono invece molto meno appariscenti con dorso e coda color bruno ruggine, con barrature scure. (Inserire foto Grillaio maschio e femmina) C’E FALCO E FALCO La specie è simile ad un altro piccolo rapace molto comune: il Gheppio (Falco tinnunculus). Pur avendo un piumaggio analogo, i maschi del Grillaio si distinguono per avere piume più brillanti e per l’assenza delle tipiche macchie nere sul dorso, che sono invece caratteristiche del Gheppio. Lo stesso non si può dire però per le femmine delle due specie, che appaiono sostanzialmente simili e difficilmente distinguibili. (foto gheppio maschio e femmina) TIPO DI AMBIENTE (foto di ambiente tipico) Il Grillaio è legato ad ambienti aperti quali steppe, ampie distese a pascolo, aree coltivate a cereali e zone rocciose con rupi o falesie. MIGRAZIONE E SVERNAMENTO Il Grillaio è una specie migratrice e in Italia si incontra da fine marzo a fine settembre. Ogni anno, come molti altri migratori, questi uccelli affrontano lunghi viaggi tra i luoghi adatti a passare l’inverno e i luoghi in cui si riproducono. Durante la migrazione che li portano a svernare nell’Africa sub-sahariana da ottobre a febbraio, si spostano spesso in gruppi formati anche da centinaia di unità. Di preferenza in questi viaggi utilizzano passaggi obbligati come stretti o isole, che gli permettono di facilitare la traversata del mare aperto. L’areale di svernamento è situato prevalentemente nell’Africa a sud dell’Equatore, dal Senegal al Sud Africa. Nelle zone di svernamento i grillai si raggruppano la sera in grandi dormitori, spesso su alberi, di migliaia di esemplari. I grillai sono tra i primi migratori ad arrivare dai luoghi di svernamento a quelli di riproduzione tra il finire dell’inverno e l’inizio della primavera (marzo-aprile), per poi ripartire con la fine dell’estate. I primi a giungere sono gli esemplari di due o più anni, mentre quelli nati l’anno precedente si raggruppano solo in un secondo momento. Non tutti i grillai migrano. In Italia sono noti rari casi di piccoli gruppi stanziali, soprattutto in Sicilia e tra Basilicata e Calabria. 79 DOVE NIDIFICA IN ITALIA (inserire cartina) In Italia, al termine della migrazione di ritorno, l’occupazione dei luoghi di nidificazione si realizza prevalentemente tra fine marzo e gli inizi di maggio, con esemplari che spesso tornano di anno in anno negli stessi siti. Le zone prescelte si trovano quasi esclusivamente in Basilicata, Puglia, Sicilia, Sardegna e Toscana. La principale popolazione di Grillaio nidifica proprio nelle aree delle Murge tra Puglia e Balisicata. CASA DOLCE CASA Luoghi di nidificazione prediletti sono costituiti da cavità ricavate naturalmente in rocce, alberi, o in ambienti urbani negli edifici di vecchia costruzione. Il Grillaio è una delle poche specie di falchi che nidifica spesso in colonie. Nelle zone di nidificazione dell’Italia peninsulare le colonie sono tutte localizzate in centri abitati. In questi luoghi il Grillaio si stanzia utilizzando buchi e sporgenze presenti prevalentemente nei sottotetti o sulle pareti dei vecchi edifici dei centri storici. Le colonie nidificanti possono variare da poche coppie (25 a Mottola, Castellaneta e Palagianello) alle oltre 800 di Matera. PULCINI O PULLI Le coppie sono monogame, restano insieme per tutta la stagione riproduttiva (anche in anni successivi). In Italia le deposizioni avvengono tra la fine di aprile e gli inizi di giugno. Le uova sono biancastre macchiettate di rossastro, con la dimensione media delle covate che varia in media da 3 a 5 uova. L’incubazione dura circa un mese ed è effettuata di giorno da entrambi i genitori, di notte solo dalla femmina. I nidiacei, detti pulli, vengono nutriti da entrambi i genitori, che spesso cacciano, anche in piccoli gruppi, spostandosi nel raggio di qualche chilometro dal nido. L’involo dei giovani avviene dopo circa 31-32 giorni dalla nascita, quindi tra la seconda decade di giugno e la prima decade di luglio. I giovani restano nella colonia per altre 1-2 settimane nutriti dai propri genitori. GRILLI A COLAZIONE L’alimentazione è quasi esclusivamente insettivora, con una dieta a base di invertebrati e soprattutto insetti. Tra gli insetti, come richiama il nome della specie, le prede più abbondanti sono costituite da grilli e cavallette. In misura molto minore vengono incluse nell’alimentazione anche piccoli roditori, lucertole, e ancora più raramente anfibi e piccoli uccelli. Per catturare le prede vengono utilizzate tecniche diverse: dall’attendere fermi su posatoi fissi come alberi o tralicci, a sistemi di individuazione in volo come il cosiddetto “Spirito Santo”. Cacciano spesso in piccoli gruppi, soprattutto nelle ore più calde della giornata, perlustrando aree caratterizzate da prati aridi, macchia mediterranea bassa, pascoli e zone coltivate a cereali. Non tutto il materiale ingerito viene “digerito”. I peli, le penne e gli esoscheletri degli insetti non vengono digeriti, ma vengono espulsi dal becco (rigurgitati), formando i cosiddetti boli alimentari o borre. Poiché vengono in genere prodotte una o due borre al giorno per esemplare, è spesso molto facile trovarne un numero abbondante sotto ai siti prescelti come dormitori. 80 (BOX) LO “SPIRITO SANTO” La cosiddetta tecnica dello “Spirito Santo” è una tecnica di caccia adottata da diversi rapaci. Questa tecnica consente al falco di rimanere per qualche minuto perfettamente immobile in volo in modo da individuare le prede sul terreno, catturandole poi con una rapida picchiata. È chiamata così a causa della forma che assume il profilo dell’uccello, che ad un osservatore a terra può ricordare la forma di una croce. (2° PANNELLO) SALVAGUARDIAMO IL GRILLAIO Il Grillaio è una specie globalmente minacciata in tutto il suo areale distributivo, che nell’Unione europea comprende Portogallo, Italia, Francia, Albania, Grecia e Spagna, paese, quest’ultimo, che ospita la popolazione più importante. A causa della diminuzione della popolazione in quasi tutto il suo areale il Grillaio è considerato “Vulnerabile” nella Lista Rossa delle specie minacciate a livello mondiale della IUCN (Unione Mondiale per la Conservazione). A livello europeo è inserito nella categoria SPEC1 (specie altamente minacciata a livello europeo). Il Grillaio infatti è in declino in tutti i paesi d’Europa interessati dalla sua distribuzione. L’Italia ospita la terza maggiore popolazione europea (3640-3840 coppie) con una situazione assai singolare perché la maggioranza di questa popolazione nidifica in contesto urbano. Infatti si calcola che l’80% della popolazione italiana si trova suddivisa in colonie ubicate in centri abitati di medie e piccole dimensioni, situati tra Puglia e Basilicata. Principali pericoli per la conservazione del Grillaio: - la diminuzione e frammentazione dell’habitat idoneo in seguito alla diminuzione dei pascoli e delle aree incolte, come la pseudosteppa tipica delle Murge, fondamentali zone di caccia per il Grillaio. Questi tipi di ambienti, molto preziosi per piante ed animali, divengono oggi sempre più rari perché sostituiti da zone coltivate o cementificate. - l'uso eccessivo e indiscriminato di insetticidi che riducono in modo drastico la quantità di insetti, prede privilegiate dei Grillai, facendo diminuire la quantità di cibo disponibile. - LA RISTRUTTURAZIONE DI VECCHI EDIFICI, CON LA CONSEGUENTE ELIMINAZIONE DI FESSURE E CAVITÀ UTILIZZATE PER LA NIDIFICAZIONE. IN ALCUNI CASI RISTRUTTURAZIONI EFFETTUATE DURANTE IL PERIODO RIPRODUTTIVO POSSONO PROVOCARE LA DISTRUZIONE DIRETTA DI INTERE COVATE. (BOX) IL PROGETTO “UNA CASA PER IL GRILLAIO” Nelle zone di riproduzione situate tra Puglia e Basilicata dove le colonie di Grillaio nidificano in stretta vicinanza con l’uomo, una delle principali problematiche sembra proprio la diminuzione dei luoghi adatti ai nidi in seguito alle ristrutturazioni di vecchi edifici. 81 La LIPU per salvaguardare questa preziosa specie ha istallato 200 nidi artificiali su diversi edifici di due centri abitati, Gravina di Puglia e Altamura, in una delle zone maggiormente frequentate dai Grillai, grazie al contributo della Fondazione Peretti. (inserire foto di cassetta nido per grillaio) I nidi artificiali sistemati su diversi edifici sostituiscono così le cavità che spesso vengono eliminate dalle ristrutturazioni dei vecchi edifici, aiutando così il Grillaio a trovare una casa adatta ai suoi nidi. (3° Pannello) IL CONCORSO PER LE SCUOLE Per aumentare la conoscenza di questo prezioso uccello la LIPU ha proposto alle scuole di alcuni comuni pugliesi un concorso per la realizzazione di una campagna pubblicitaria sulla protezione di questa specie. Gli operatori LIPU hanno incontrato gli studenti per fargli conoscere più da vicino questo abitante dei loro cieli. Abbiamo chiesto loro di proporci il modo migliore per spiegare ai loro concittadini le caratteristiche e le problematiche che devono affrontare nella loro coabitazione con gli umani. Vogliamo ringraziare tutti i ragazzi che hanno partecipato attivamente al progetto e in particolare la scuola media statale "Don Eustachio Montemurro" di Gravina che ha inviato diversi disegni, poesie e piccoli racconti. (BOX) IL VINCITORE Scegliere tra i tanti lavori arrivati non è stato facile, ma alla fine abbiamo scelto: “UN MESSAGGIO PER IL FALCO GRILLAIO” UN PORTAMESSAGGI/PORTALETTERE IN CARTONCINO REALIZZATO DA OLGA TUCCI E MARIAPIA CAPRIUOLO DELLA CLASSE 2D scuola media statale "Don Eustachio Montemurro" di Gravina. (Inserire foto del lavoro vincitore- file Tucci-Capriolo 2D) Inserire foto degli altri partecipanti: • foto file 8-1 squicciarini 1° • foto file 8-2 • foto file 8-3 • foto file 8-4 • file 8-5 con scritto: “Opera realizzata da Ferdinando Squicciarini , 1° A scuola media statale "Don Eustachio Montemurro" di Gravina “ • Granieri 1° 82 con scritto: “Opera realizzata da Tobia Granirei, 1° A scuola media statale “Don Eustachio Montemurro “ di Gravina. • Porzia ventura Con scritto “Opera realizzata da Daniele Porzia e Alessandro Ventura, scuola media statale "Don Eustachio Montemurro" di Gravina “ • Aquilino Con scritto “Opera realizzata da Michele Aquilino, scuola media statale "Don Eustachio Montemurro" di Gravina “ • Capriuolo 2D • Capriuolo 2D Con scritto : “Opera realizzata da Mariapia Capriolo, 2°D scuola media statale "Don Eustachio Montemurro" di Gravina “ (4° pannello) • Amici di sardone pina 1°F Con scritto “Opera realizzata da Pina Sardone, 1°F scuola media statale "Don Eustachio Montemurro" di Gravina “ • Diario del falco di tucci olga 2D Con scritto “Opera realizzata da Olga Tucci e Mariapia Capriolo, 2°D scuola media statale "Don Eustachio Montemurro" di Gravina “ • Lombardi laddaga cilifrese Con scritto “Opera realizzata da Mario Lombardi, Giulia Laddaga, Michele Cilifrese, 1°E scuola media statale "Don Eustachio Montemurro" di Gravina” • Ariano picciallo 2D • Ariano picciallo Con scritto “Opera realizzata da Grazia Ariano Picciallo, 2°D scuola media statale "Don Eustachio Montemurro" di Gravina” • Dagostino cicala 2D Con scritto “Opera realizzata da Paola D’Agostino e Rossana Cicala, 2°D scuola media statale "Don Eustachio Montemurro" di Gravina “ • Varvara larocca 2D Con scritto “Opera realizzata da Angelo Varvara e Domenico Larocca, 2°D scuola media statale "Don Eustachio Montemurro" di Gravina “ • Picciallo gramigna 3D 83 Con scritto “Opera realizzata da Antonio Picciallo e Teodosio Gramegna, 3°D scuola media statale "Don Eustachio Montemurro" di Gravina “ (5° pannello) Matera Nuzzi 1E Con scritto: opera prodotta da Marcella Matera e Mariapia Nuzzi 1° E Scuola Media Statale "Don Eustachio Montemurro" di Gravina in Puglia Santomasi Tarturo 1E Con scritto: opera prodotta da Walter Santomasi e Vito Tarturo 1 E Scuola Media Statale "Don Eustachio Montemurro" di Gravina in Puglia Ruggieri clemente 1E Con scritto: opera realizzata da Marco Ruggirei e Giancarlo Clemente 1 E Scuola Media Statale "Don Eustachio Montemurro" di Gravina in Puglia Riviello 3D Con scritto: opera realizzata da Vincenzo Riviello 3D Scuola Media Statale "Don Eustachio Montemurro" di Gravina in Puglia Duro branà lorusso alloggio 1E Duro branà lorusso alloggio 1E Con scritto: opera realizzata da Mariangela Duro, Angela Branà, Vincenzo Lo russo e Pamela Alloggio 1E Scuola Media Statale "Don Eustachio Montemurro" di Gravina in Puglia 84 3.4. Primo libretto divulgativo sul Grillaio: il testo Questo libretto in stampa dal grafico, per complessive 12 pagine, si avvale dei disegni dei ragazzi della scuola media di Gravina in Puglia. 3.5. Secondo libretto divulgativo sul Grillaio: il testo Questo libretto in stampa dal grafico è composto complessivamente di 24 pagine. Di seguito il testo proposto. IL GRILLAIO, UNA SPECIE GLOBALMENTE MINACCIATA INDICE Capitolo 1 - Biologia della specie 1.1. Descrizione 1.2. Ecologia 1.3. Biologia riproduttiva 1.4. Migrazione e svernamento Capitolo 2 - Status e conservazione 2.1. Distribuzione nel mondo e status di conservazione 2.2. Status e distribuzione in Europa 2.3. Status e distribuzione in Italia 2.4. Status e conservazione in Puglia/Basilicata Capitolo 3 - Distribuzione delle colonie 3.1. Distribuzione delle colonie in Puglia e Basilicata 3.2. Dormitori e censimenti Capitolo 4 – I progetti di conservazione 4.1. Il progetto “una casa per il Grillaio” 4.2. Altri progetti di conservazione Bibliografia Capitolo 1 - Biologia della specie 1.1. Descrizione Il Grillaio (Falco naumanni, Fleischer, 1818) appartiene al gruppo esteso di uccelli conosciuti col nome di rapaci. Appartiene alla Famiglia dei Falconidae e più specificatamente al Genere Falco; le peculiarità che contraddistinguono tale Genere sono il volo spettacolare con rapidi battiti e planate, le lunghe ali appuntite, la coda allungata e stretta, la raffinata tecnica di caccia che si affida alla forte muscolatura, alla vista acuta e alla velocità dell’attacco nonché alla capacità di librarsi immobile in aria, tecnica di volo definita “spirito santo”. 85 Es. Figura 1 – Spirito santo Il Grillaio deve il suo nome al fatto che si nutre principalmente di insetti, inoltre alcune delle sue caratteristiche specifiche sono quelle di essere una specie migratrice transhariana, gregaria e sinantropica (che abita a stretto contatto con l’uomo). Es. Figura 2 – Maschio di Grillaio che spicca il volo Il Grillaio è un falco di piccole dimensioni, che varia tra i 29 e i 32 cm (BirdLife International, 2007). L’apertura alare è piuttosto modesta e raggiunge, negli individui adulti, mediamente 70-72 cm (Palumbo et al., 1997), mentre il peso corporeo differisce notevolmente tra maschio e femmina (dimorfismo sessuale). Quest’ultima infatti, come nella maggior parte dei rapaci, è generalmente più grande, arrivando a pesare tra i 138 e 208 grammi, mentre i maschi tra i 90 e 172 grammi (Cramp e Simmons,1980). Il Grillaio presenta inoltre un netto dimorfismo sessuale anche nel piumaggio. Il maschio ha le parti superiori di un vivace color rosso mattone senza macchie, la cui assenza lo differenzia dal Gheppio 86 (Falco tinnunculus), mentre testa e coda sono grigio-bluastre. La gola e il sottoala appaiono molto chiare, color crema. Figura/Foto Figura/Foto La femmina, simile all’immaturo, ha le parti superiori di un color castano meno intenso, con striature brune. Le parti inferiori sono color crema macchiettate di scuro. Entrambi presentano becco grigio con base gialla, circoli orbitali gialli, tarsi e zampe giallo-aranciato, margini inferiori delle ali nere e unghie bianche. Quest’ultima caratteristica è un tratto distintivo per l’identificazione soprattutto delle femmine, che altrimenti risultano molto simili a quelle del Gheppio. Figura/Foto Figura/Foto Figura/Foto Altri aspetti che lo differenziano dal Gheppio, sono le dimensioni appena più ridotte, le ali più slanciate e aerodinamiche, il comportamento meno diffidente e più rumoroso, la nidificazione in colonie e la voce più variata, con serie più corte e modulate (nota usuale un chiacchierante cit-cit-cit ed un lamentevole uiii in crescendo) (Palumbo et al., 1997). 1.2. Ecologia L’habitat del Grillaio è rappresentato da ambienti agricoli, praterie aperte o boscate, steppe, savane, e ambienti rocciosi con rupi o falesie (BirdLife International, 2007). Tuttavia è facilmente individuabile anche nei centri storici di alcune città, dove trova un ambiente ideale per la nidificazione. Questo falchetto, infatti, spesso nidifica nelle cavità di vecchie costruzioni e sotto i tetti, oltre che in alberi cavi, su pareti di roccia o in vecchi nidi di corvidi abbandonati (Biber, 1990). Nidifica dal livello del mare fino a 1000-1500 metri, occasionalmente fino a 3000 m sulle montagne asiatiche (Dementiev, 1951). 87 Le colonie di nidificazione sono spesso formate da 120-250 coppie ma, con il declino della specie, stanno diventando sempre più comuni situazioni in cui le colonie sono formate da meno di 10 coppie o anche singole coppie (Gensbol, 1988). Non di rado, condivide il luogo di nidificazione con altre specie quali, Tortora (Streptopelia decaocto), Piccione selvatico (Columba livia), Taccola (Corvus monedula) e più raramente Gheppio, Rondine rupestre (Ptyonoprogne rupestris), Passero solitario (Monticola solitarius), Passera sarda (Passer hispaniolensis), Scricciolo (Troglodytes troglodytes), Corvo imperiale (Corvus corax), Falco Pellegrino (Falco peregrinus), Falco della Regina (Falco eleonorae) (Palumbo et al., 1997). Il Grillaio quindi preferisce aree collinari o pianeggianti aride e pietrose, a clima temperato o caldo con vegetazione rada o comunque bassa dove può facilmente individuare le prede. Per mettere in pratica le proprie perlustrazioni di caccia, tuttavia, si sposta a distanze massime di 20-30 km dalla colonia, utilizzando spesso gli stessi territori frequentati da individui di altre colonie. I motivi per cui l’home-range del Grillaio è relativamente ampio in relazione alla taglia ridotta, possono essere legati alle abitudini coloniali e alle tecniche di caccia che spesso coinvolgono più individui (Negro et al., 1993). Come si è detto precedentemente l’alimentazione del Grillaio, consiste prevalentemente di insetti, fra i quali predominano i grandi ortotteri, come grilli e cavallette, e i coleotteri di varie famiglie. Meno frequentemente arricchisce la sua dieta con piccoli vertebrati, essenzialmente piccoli roditori e lucertole, e più raramente anfibi ed uccelli terricoli. Da uno studio effettuato in Spagna sud-occidentale è stato rilevato che la dieta del Grillaio è così costituita: 94% invertebrati e 6% vertebrati. Gli ortotteri hanno costituito il 60% della totalità delle prede, i coleotteri il 22% (Franco e Andrada, 1976). Uno studio austriaco simile, ha dato i seguenti risultati: ortotteri, pari al 67% delle prede e coleotteri pari al 29%. Gli ortotteri maggiormente rappresentativi sono risultati il Grillo campestre (Gryllus campestris) pari al 32,8% del totale, e il Grillotalpa (Grillotalpa grillotalpa) pari al 21,4% del totale (Glutz et al., 1971). Anche in Italia sono state ottenute conclusioni simili, ossia che il 97,7% delle prede è costituito da artropodi, di cui il 41,7% ortotteri, e il 2,3% da vertebrati (Bux et al., 1997). È stato possibile realizzare queste indagini tramite l’analisi di borre, ossia il materiale non digerito, come pelo, esoscheletri di insetti e penne, che viene compattato nello stomaco in forme più o meno oblunghe e in seguito rigurgitate, qualche ora dopo la digestione. Tale materiale é possibile raccoglierne in buone quantità sotto i dormitori. Il Grillaio, infatti, è un rapace che si nutre di molti insetti e rigurgita ogni giorno una o due borre, dalle quali poi è possibile identificare le prede e quindi ottenerne interessanti informazioni sulla sua dieta. 1.3. Biologia riproduttiva 88 Il Grillaio ritorna dalla migrazione transahariana in marzo-aprile. Gli accoppiamenti iniziano presto e possono protrarsi fino alla seconda decade di maggio (Massa, 1985). Durante il periodo di scelta dei siti dei siti, è facile osservare i grillai accoppiarsi anche molte volte al giorno, con una frequenza massima, registrata a Matera nei giorni precedenti la deposizione, di 15-16 volte durante un arco di 3 ore (Palumbo et al., 1997). Le coppie sono tendenzialmente monogame e restano insieme per tutta la stagione riproduttiva. Pochi giorni prima della deposizione le femmine trascorrono la maggior parte del tempo nelle vicinanze del sito prescelto e nel frattempo vengono alimentate dal maschio. Questo permette alla femmina di raggiungere le migliori condizioni energetiche per la formazione delle uova e la loro deposizione. Questa forma di somministrazione di cibo da parte del maschio fu definita inizialmente “ nutrizione di corteggiamento” (Hovette, 1971; Cramp e Simmons, 1980). In realtà questa romantica espressione non è corretta, in quanto il maschio inizia ad integrare il pasto della compagna solo dopo che la coppia si è formata ed ha già scelto il sito di deposizione (Franco, 1982; Negro e Hiraldo, 1991). Figura/Foto Il luogo dove vengono deposte le uova (in mancanza di un nido vero e proprio, così come avviene per tutti i falchi) è molto variabile: anfratti di rocce, terrazzi naturali, cavità in edifici abbandonati e sottotetti. Nelle colonie i nidi possono essere posti a distanza di pochi metri uno dall'altro. Nel bacino del Mediterraneo, la deposizione avviene tra il 15-30 aprile e la prima metà di giugno; in Italia peninsulare, in particolare, la maggior parte delle deposizioni avviene nella seconda decade di maggio. Le uova deposte sono biancastre macchiettate di giallo-aranciato-rossastro e la dimensione media della covata varia da 2 a 8 uova, più frequentemente da 3 a 5 (Cramp e Simmons, 1980), con differenze significative tra i vari paesi del Mediterraneo. Figura/Foto In Marocco ad esempio, nell’80% dei casi, il numero massimo di uova deposte è 4-5 per coppia, mentre in Italia di 3-4 uova. Queste ultime, vengono deposte a intervalli variabili di circa 24-48 ore. Durante la cova i genitori si alimentano separatamente, a differenza di quanto accade per altre specie di falchi. Talora si verifica il temporaneo abbandono delle uova, poiché il rientro di uno degli adulti della coppia non coincide con la partenza dell’altro; in questi brevi istanti che passano prima dell’arrivo del genitore, può accadere che qualche predatore si impossessi di un uovo. L'incubazione 89 dura 28-29 giorni ed è attuata prevalentemente dalla femmina, con brevi intervalli in cui il maschio la sostituisce. Poiché la cova delle uova inizia dopo la deposizione dell'ultimo uovo, la schiusa è sincrona. In caso di fallimento della prima covata ne viene deposta una di rimpiazzo. Figura/Foto Successivamente entrambi i genitori provvedono alla loro alimentazione, con picchi di attività nelle ore calde della giornata in relazione alla massima attività degli insetti. Non vi sono differenze significative nell'attività del maschio e della femmina (Massa, 1985). Durante le prime tre settimane di vita i piccoli vengono imbeccati dai genitori, successivamente gli adulti lasciano le prede nel nido e si allontanano. L’intervallo medio tra un’imbeccata e l’altra è di circa 15 minuti. Le relazioni tra fratelli sono pacifiche e i nidiacei di nidi adiacenti possono riunirsi, ma accettano il cibo solo dai rispettivi genitori. Ciò nonostante non è raro osservare casi di adozione in cui nidiacei occasionalmente abbandonati da altre coppie e portate ad altri nidi, sono stati allevati (Donazar et al., 1991). I pulli iniziano a perdere il piumino bianco dopo circa due settimane, quando iniziano a comparire le remiganti. Figura/Foto L'involo avviene dopo circa un mese di vita e la completa indipendenza è raggiunta dopo altre due settimane o più. In Italia meridionale l'involo avviene generalmente nei primi quindici giorni di luglio. La maturità sessuale è raggiunta in buona parte degli individui già dopo il primo inverno. Figura/Foto Capitolo 2 - Status e conservazione 2.1. Status e distribuzione nel mondo e status di conservazione Il Grillaio è una specie a distribuzione eurocentrasiatico-mediterranea (Boano e Brichetti, 1989). L’area di nidificazione, da Nord a Sud, comprende gli Stati tra il 52° parallelo in Polonia, dove nidifica irregolarmente (Tucker e Heath, 1994) e il 56° parallelo nella zona del Volga (Cade, 1982), 90 estendendosi verso sud sino al Maghreb, e, da est ad ovest, gli Stati dal Portogallo al territorio sovietico, con appendici fino all’Afghanistan, Mongolia e nord-est della Cina (Biber, 1995). L’areale di svernamento è localizzato nel continente africano, in gran parte a sud dell’equatore fino al Sud Africa (Palumbo et al., 1997). La popolazione mondiale di Grillaio era stimata negli anni ’80 intorno le 650.000–800.000 coppie (Cade, 1982). La popolazione europea attuale è quantificata in 25.000–42.000 coppie, di cui circa 12.000–20.000 in Spagna e 3.640–3.840 in Italia (BirdLife International 2004). Dagli anni ’50 ad oggi la popolazione totale di questa specie ha subito un declino drammatico. Impressionante è stata la diminuzione degli individui che frequentavano l’Europa occidentale negli ultimi venti anni con la pressoché totale scomparsa della specie dalla regione degli Urali in Russia e del Kazakhistan, mentre dagli anni ’70 in Africa meridionale si è registrato un calo del 50% degli svernanti, la cui popolazione attualmente non supera i 50.000–60.000 individui (Davygora, 1998). Per questo motivo il Grillaio, è considerato specie Vulnerabile (VU) nella Lista Rossa IUCN, inserito nell’Appendice II della CITES e nell’Appendice I e II della Convenzione delle Specie Migratrici. Nel 2004 è stato classificato nel rapporto sullo stato di conservazione degli uccelli selvatici in Europa (BirdLife International 2004), come SPEC 1, ossia specie minacciata di estinzione a livello mondiale. Tale decisione riguardo la specie è stata decisa per consolidare i criteri di salvaguardia delle specie prioritarie, incorporando quelli utilizzati dalla Lista Rossa IUCN, la maggiore autorità riconosciuta per la conservazione della natura a livello mondiale, rappresentando un modello universalmente accettato per definire il rischio di estinzione di ciascuna specie. 2.2. Status e distribuzione in Europa In Europa le popolazioni più rappresentative sono quelle presenti in Spagna, Turchia, Italia e Grecia (Tab.1). Proprio a causa del generale trend negativo che si è registrato in tutta Europa, in alcune paesi il Grillaio è una specie costantemente monitorata negli ultimi anni. Nazione Albania Armenia Azerbaijan Bosnia & HG Bulgaria Croazia Francia Popolazione riproduttiva (coppie) 0 – 20 15 – 60 (500 – 3,000) (0 – 250) 0-5 0-0 72 - 72 Anno(i) Trend 98–01 00-02 96–00 90-00 95-00 02 03 ? ? (0) ? (-) + 91 Georgia Grecia Italia Macedonia Moldavia Portogallo Romania Russia Serbia & MN Slovenia Spagna Turchia Ucraina Regno Unito Gibilterra Totale (appross.) Areale riproduttivo 20 - 100 2.000 – 3.480 3.640 – 3.840 1.500 – 3.000 3-6 286 - 293 (0 – 5) 400 - 600 0 -6 0-0 12.000 – 20.000 5.000 – 7.000 (5 – 10) 4 - 10 94-03 95-00 01 02 90-00 01 90-02 98-02 90-02 94-00 94-02 01 90-00 00 (0) + (-) 0 (+) (F) + (-) 0 0 25.000 – 42.000 lieve declino 2 > 1.000.000 km Tab. 1 - Status e distribuzione in Europa e nel Mediterraneo 2.3. Status e distribuzione in Italia In Italia il Grillaio è un migratore regolare, nidificante e parzialmente svernante (Brichetti e Massa, 1997). È nidificante esclusivamente in Basilicata, Puglia, Sicilia e Sardegna. Le coppie nidificanti ammontano, come precedentemente accennato, a circa 3.640 – 3.840. L’analisi dell’areale di distribuzione del Grillaio in Italia mette in risalto l’esistenza di tre distinte popolazioni: - popolazione appulo-lucana (superficie mediamente occupata pari a circa 9.000 Km2): 76-81 % della popolazione nazionale; - popolazione siciliana (superficie mediamente occupata pari a circa 12.000 km2): 17-15 % della popolazione nazionale; - popolazione sarda (superficie mediamente occupata pari a circa 8.000 km2): 7-4 % della popolazione nazionale. (Palumbo et al., 1997) In generale, sul territorio siciliano la quasi totalità delle coppie nidifica su pareti naturali rocciose mentre solo un limitato numero di individui si riproduce su vecchie costruzioni. In Sardegna il Grillaio nidifica quasi esclusivamente su pareti rocciose, falesie a picco sul mare e ruderi in colonie sino ad un massimo di 5-10 coppie. In passato erano comuni colonie sinantropiche come nel caso di una di esse che si era insediata sul duomo di Oristano negli anni ’70. Per quanto riguarda invece la popolazione appulo-lucana essa verrà trattata in maniera più approfondita nel paragrafo seguente. 92 2.4 Status e conservazione in Puglia/Basilicata La scarsa densità della popolazione umana, la presenza di habitat favorevoli (pseudosteppa mediterranea alternata a pascoli, gariga, aree non intensamente coltivate, ambienti aridi, ecc.), la persistenza di aree integre e l'isolamento di alcune zone favoriscono in queste due regioni l’elevata presenza di questa specie. Un’altra caratteristica comune a entrambe le regioni è quella di avere centri abitati, adatti all’ubicazione di consistenti colonie, posti nelle immediate vicinanze delle aree trofiche. Figura 17 Le Murge baresi e materane (Figura 18) che ospitano l'unica popolazione di Grillaio (chiamato nel dialetto lucano “scorzlav'nt”) dell'Italia peninsulare, sono costituite da un piatto altopiano calcareo che raggiunge la massima altitudine a 679 m slm e sono caratterizzate, nella loro porzione nordoccidentale, da estese aree aperte, appartenenti alla regione Puglia ed, in parte, alla regione Basilicata (www.rapacigravine.it). CENTRI ABITATI DELLE MURGE CHE OSPITANO LE COLONIE DI GRILLAIO Figura 18 - http:\\www.terredelmediterraneo.org In Basilicata l'areale di distribuzione del Grillaio si limita ad una parte della provincia di Matera ed in particolare ai centri storici di alcuni comuni e al territorio del Parco Regionale della Murgia Materana, considerato tra i più idonei per il foraggiamento del piccolo falco (Palumbo, 1996). Le colonie appulo-lucane, sono distribuite a ridosso del confine che separa le due regioni. In Basilicata, man mano che ci si sposta da est ad ovest, passando gradualmente in zone boscose, la presenza del Grillaio nidificante diminuisce fino a scomparire del tutto nel passaggio dalla Provincia di Matera a quella di Potenza. In Puglia invece il territorio idoneo diminuisce passando da ovest ad est verso le aree costiere, in coincidenza dell’aumento dell’antropizzazione e delle zone intensamente coltivate. Essendo scarse le notizie sulla biologia riproduttiva della specie, a partire dal 1993 si avviò uno studio sistematico attraverso indagini sui siti di nidificazione e specifiche 93 ricerche sull'alimentazione e sulla biologia riproduttiva. Si effettuarono con varie tecniche quantitative, censimenti atti ad evidenziare la consistenza numerica delle colonie. Capitolo 3 – Distribuzione delle colonie 3.1. Distribuzione delle colonie in Puglia e Basilicata Dal 1993 al 1997 nell’intero territorio delle regioni Puglia e Basilicata è stata realizzata un’accurata indagine volta a verificare dove avvenisse la nidificazione del Grillaio. La nidificazione è stata accertata in 15 Comuni ed è stato appurato che nel 99% dei casi, essa ha avuto luogo nei centri urbani (Palumbo et al., 1997). In Basilicata le colonie più numericamente significative sono risultate quelle di Matera e Montescaglioso, mentre in Puglia quelle di Santeramo in Colle, Altamura, Gravina in Puglia, Ginosa e Minervino (Palumbo et al., 1997). Figura/Foto Da sottolineare il fatto che le colonie di Matera, Santeramo in Colle, Altamura, Gravina in Puglia e Minervino, insieme a quelle ospitate da due città della Spagna sud-occidentale, risultano essere le colonie sinantropiche più numerose conosciute in tutto il Paleartico occidentale (Palumbo et al., 1997). In Spagna, nonostante vi sia una popolazione più abbondante di grillai rispetto all’Italia, nella maggior parte dei casi le colonie sono di piccole-medie dimensioni. In Pugnai e Basilicata invece, ben 8 colonie, vale a dire circa il 53% del totale, superano il numero di 20 coppie e di queste 4 superano abbondantemente le 100 (Palumbo et al., 1997). In pratica, oltre il 90% dell’intera popolazione si concentra in 8 colonie localizzate in centri urbani di modeste dimensioni. La grande abbondanza di individui in un ambiente così ridotto, fa si che i nidi vengano a trovarsi a distanze molto ravvicinate tra loro, in alcuni casi inferiori a un metro (Palumbo et al., 1997). L’attività di monitoraggio effettuata a partire dal 1993 sino al 2001, ha consentito di definire lo status della popolazione di alcune colonie che sono arrivate a contare in periodo post-riproduttivo migliaia di individui, come Altamura, Santeramo, Gravina in Puglia e Matera. Colonie di medie dimensioni sono state osservate a Minervino, Cassano Murge, Ginosa, Montescaglioso, Gioia del Colle, mentre a Laterza e ad Acquaviva delle Fonti furono individuate solo colonie costituite da poche unità. Il monitoraggio degli ultimi anni, ha evidenziato sia un aumento complessivo della popolazione sia l’insediarsi di nuove colonie, particolarmente accentuato tra il 1998 ed il 2000, probabilmente grazie ad un’elevata disponibilità di prede, mentre la popolazione ha mostrato una tendenza alla stabilità negli ultimi anni (Sigismondi et al., 1996, 2001). 94 Il numero d’individui post-riproduttivi presenti nelle cinque colonie più numerose è passato dai 6350 del 1996 agli 11000 del 2001, mentre il numero delle colonie è passato dalle 5 conosciute negli anni ‘80 (Sigismondi, 1990) alle 11 del 2001. Utile a valutare eventuali problemi di conservazione nelle aree di svernamento appare il calcolo della percentuale di ritorno della popolazione, giustificato dallo stretto legame che sembra unire i grillai alla colonia di appartenenza (Massa, 1985) e che li riporta ogni anno sempre nello stesso sito riproduttivo. Complessivamente le coppie di Grillaio presenti in Basilicata e Puglia corrispondono al 78% circa della popolazione italiana e all’11% circa di quella nidificante nel Paleartico-occidentale (Palumbo et al., 1997). 3.2. Dormitori e censimenti I dormitori, come accennato precedentemente, vengono tipicamente utilizzati dai grillai nei quartieri si svernamento dove si concentrano diverse migliaia di individui. Relativamente alla mole piuttosto ridotta degli alberi-dormitorio italiani, la presenza dei grillai è comunque notevole. A Matera, ad esempio, su uno dei dormitori utilizzati, in questo caso un pino domestico (Pinus pinea), si concentrano nel periodo post-riproduttivo dai 1200 ai 2100 individi. Gli individui di una colonia utilizzano ogni anno gli stessi alberi dormitorio, quasi sempre Pinacee, posti all’interno o nelle immediate vicinanze dei centri abitati. Gli individui di una colonia risultano molto fedeli al dormitorio nel periodo pre-riproduttivo. Durante il periodo di dispersione post-riproduttivo, tendono, invece, a distribuirsi anche su altri alberi, lontani dai centri urbani o in altre colonie e questo rende meno affidabili i conteggi post-riproduttivi delle singole colonie, ma non il dato complessivo di popolazione (Sigismondi et al., 2001). I dormitori possono essere anche più di uno, in relazione alla dimensione della colonia, e sono distanti l’uno dall’altro anche diverse centinaia di metri in linea d’aria. Variano da uno a tre, nelle colonie di dimensioni maggiori, nel periodo preriproduttivo, e da uno a cinque in quello post-riproduttivo in seguito all’aumento della popolazione. Ogni singolo dormitorio può essere costituito oltre che da alberi isolati anche da gruppi di 4-7 alberi vicini, i quali formano una sola chioma, come succede nelle colonie di Altamura e Gravina (Palumbo et al., 1997). Per determinare la consistenza delle colonie di Grillaio nidificante nell’areale descritto, vengono effettuati diversi tipi di censimenti. Sono state effettuate osservazioni dirette ai nidi, ricavando precisi dati sulla biologia riproduttiva delle popolazioni. Per ogni nido sono stati annotati i seguenti dati: dimensione media della covata, tasso di schiusa, tasso di involo e tasso di involo rispetto al numero di uova deposte. Questi dati sono stati messi in relazione con un metodo quantitativo di conteggio della popolazione al fine di stimare le coppie nidificanti. Tale metodologia consiste nel conteggio, pre e post-riproduttivo, degli individui che si recano ai 95 dormitori per trascorrevi le ore notturne. Il conteggio viene effettuato quando i falchi appartenenti ad una sola colonia, arrivano a piccoli gruppi nelle vicinanze degli alberi-dormitori, negli istanti precedenti il “tuffo” nella chioma. Il periodo ideale per le conte nella fase pre-riproduttiva varia, di solito tra la metà di aprile e la prima decade di maggio, in relazione all’arrivo dei grillai dal periodo di svernamento; quelle post-riproduttive avvengono, generalmente, tra la terza decade di luglio e la prima di agosto, quando tutta la popolazione è ancora presente prima che inizi la fase di dispersione (Palumbo et al., 1997). La tecnica dei conteggi al dormitorio è senz’altro funzionale ad un monitoraggio pluriennale, in grado di fornire i valori dell’andamento demografico della popolazione complessiva, evidenziandone eventuali alterazioni significative da una stagione riproduttiva all’altra (Palumbo et al., 1997). Capitolo 4 – I progetti di conservazione 4.1. Il progetto “una casa per il Grillaio” La diminuzione di questa specie in tutti i centri storici dei Comuni dell’Italia meridionale dove un tempo vi erano colonie molto numerose, è dovuta in buona parte al fatto che i vecchi edifici, le chiese, e le abitazioni sono stati interessati, in varia misura, da lavori di restauro che hanno precluso gradualmente ai grillai la possibilità di trovare siti idonei alla nidificazione. Inoltre, se la ristrutturazione viene effettuata nel periodo riproduttivo (seconda metà di aprile prima metà di giugno), essa può persino provocare la distruzione di intere covate o nidiate di pulcini. Un tipo di intervento utilizzato come alternativa a siti riproduttivi in diminuzione e comunque ottimali per la presenza della specie è quello di installare cassette nido. Le cassette nido possono essere di due tipologie e fabbricati con diversi materiali: - cilindrici di terracotta, da esterno, da utilizzare direttamente sui tetti o tra le tegole; - in legno, adatti per luoghi più riparati, come ad esempio nei sottotetti o sotto i cornicioni e le grondaie. Fra le azioni del progetto “una casa per il Grillaio” finanziato dalla Fondazione Peretti, vi era l’installazione di circa 200 nidi artificiali che dovevano poi essere monitorati durante la stagione riproduttiva. Il foro di accesso adatto per i grillai, è risultato di 6 cm di diametro, permettendo solo a questi ultimi di occupare la cassetta nido, rendendola selettiva ed escludendone l’uso da parte dei piccioni. Una finestrella laterale, del diametro di 10 cm, con copertura a scorrimento girevole, realizzata o a 96 destra o a sinistra a seconda del luogo di installazione, ha permesso una migliore ispezione della cassetta nido, facilitando le operazioni di pulizia. Ogni cassetta nido è stata numerata per facilitare le operazioni di identificazione durante la fase di monitoraggio delle stesse durante la stagione riproduttiva. Le cassette sono state dislocate su scuole, edifici comunali e privati. L’installazione dei nidi artificiali è iniziata il 22 febbraio 2007, proseguendo per tutto il mese di marzo, mentre ad aprile sono state collocate quelle cassette nido per le quali all’ultimo momento erano venuti meno i siti previsti. Sono queste le cassette nido considerate tardive (65 unità). Su un’apposita tabella sono stati riportati i dati relativi all’ubicazione di ogni cassetta nido, ovvero: numero progressivo, coordinate geografiche, indirizzo edificio, nome e numero di telefono del referente (necessario per le scuole ed altri edifici pubblici), data di installazione. I nidi sono stati installati nelle città di Gravina (102), Altamura (50), Acquaviva (22), Cassano (12), Laterza (14). Foto della distribuzione dei nidi artificiali In Tab. 2 sono riportati i dati relativi al numero e percentuale di cassette nido occupate. Per le cassette nido visitate si intendono quelle nelle quali sono state trovate solo tracce di frequentazione da parte del grillaio, ovvero segni del suo passaggio all’interno del nido (segni delle zampe sul terriccio interno), presenza di borre, resti di prede. Per cassette nido occupate si intendono quelle nelle quali è avvenuta la deposizione ed è stato portato a compimento il ciclo riproduttivo. Per nidi tardivi si intendono quelli installati nel mese di aprile. Tab. 2 – Risultati dell’installazione delle cassette nido durante il progetto “una casa per il grillaio”. Cassette nido installate visitate occupate tardive 200 39 16 65 % 19,5 8 32,5 in tempo visitati occupati 135 39 16 % 28,9 11,9 n° siti/edifici frequentati occupati 41 15 10 % 36,6 24,4 La percentuale di cassette nido frequentate è stata del 19,5% (39 nidi) mentre si è registrata la deposizione di uova in 16 nidi artificiali pari all’8 % delle 200 cassette nido totali. Se si escludono dal calcolo i 65 nidi tardivi, ovvero considerando solo i 135 nidi collocati in tempo, la percentuale 97 di occupazione aumenta all’11,9 %. Se si considera il numero di siti/edifici sui quali sono stati installati i nidi, pari a 41, e si calcola la percentuale dei siti occupati si ottiene un valore pari al 24,4% (10 siti). Sulla base dei risultati ottenuti e dalle osservazioni condotte nel corso del progetto “una casa per il grillaio”, sono emersi alcuni aspetti a cui andrebbe data maggiore attenzione in futuro per aumentare la percentuale di occupazione dei nidi artificiali. Essi sono: 5- La scelta del sito/edificio dove collocare i nidi deve essere fatta preferendo quelli nelle cui vicinanze (100-200 metri) è già presente qualche coppia di grillaio nidificante; 6- Occorre assicurarsi che sull’edificio scelto non siano in programma lavori di ristrutturazione durante la stagione riproduttiva. In tal caso occorre evitare di installare i nidi oppure scegliere una parte dell’edificio non interessata dai lavori a causa dell’inevitabile disturbo; 7- Collocare la cassetta nido preferendo un lato del tetto che sia parzialmente ombrato per evitare eccessiva insolazione ed innalzamento della temperatura all’interno della stessa;. 8- Collocare le cassette nido preferibilmente entro il mese di febbraio-marzo; le installazioni effettuate nel mese di aprile non producono risultati utili. 4.2. Altri progetti di conservazione Negli ultimi anni gli interventi di restauro degli edifici soprattutto dei centri storici, hanno provocato una serie di problematiche alla specie. Grazie al Regolamento Regionale del 28 settembre 2005, n. 24 “Misure di conservazione relative a specie di importanza comunitaria di uccelli selvatici nidificanti nei centri edificati ricadenti in proposti siti di importanza comunitaria (pSIC) ed in zone di protezione speciale (ZPS)”, sono state emanate un insieme di regole che potrebbero risolvere il problema a monte, durante i restauri, salvaguardando l’esistenza di determinate cavità idonee alla deposizione, senza, per questo, pregiudicare il buon esito del restauro (Palumbo et al., 1997). Oltre alla ristrutturazione degli edifici, che elimina le fessure e le cavità utili per la nidificazione, altre problematiche relative alla specie, aumentandone sempre più il rischio di declino, sono: - la diminuzione dei pascoli e delle aree incolte, come la pseudosteppa, fondamentali zone di caccia per il Grillaio. Vaste distese di pseudosteppa, sebbene protette da Direttive europee, sono state negli ultimi anni devastate dallo spietramento allo scopo di impiantare nuove colture, con conseguente scomparsa di importanti habitat trofici (Sigismondi et. al., 1996; Palombo et al., 1997; Biber, 1994). Anche l'abbandono della pastorizia e dell’agricoltura tradizionale hanno determinato la diminuzione delle aree di alimentazione del falco, come è avvenuto in varie regioni francesi, dove la popolazione di ovini è drasticamente diminuita nel corso degli ultimi decenni, permettendo una ricrescita della vegetazione e la conseguente diminuzione della popolazione di cavallette; 98 - la bruciatura anticipata delle stoppie che riduce enormemente la quantità di prede; - la siccità che colpisce alcune regioni africane dove sverna la specie; - l'aumento di taccole e piccioni che potrebbe aver innescato una competizione interspecifiche per i siti riproduttivi; - l'uso di insetticidi che, se usato in modo indiscriminato e su vaste superfici, riducono la qualità degli ambienti coltivati come aree trofiche per i grillai (Sigismondi et al., 1996); - il disturbo recato alle colonie riproduttive ed ai quartieri dormitorio. Il problema si pone soprattutto laddove il dormitorio sia un albero situato all’interno di proprietà private, in quanto i proprietari difficilmente sono disposti a tollerare gli inconvenienti derivanti dalla presenza di centinaia di grillai e della conseguente quantità di guano che, inevitabilmente, si accumula sulla pianta e al di sotto di essa. Tuttavia recenti stime effettuate da BirdLife International del trend di popolazione, hanno dimostrato come il declino si sia arrestato in Portogallo, Spagna e Francia, probabilmente come effetto dei programmi di conservazione messi in atto in questi paesi. I progetti per la conservazione del Grillaio, infatti, possono prevenirne l’ulteriore diminuzione. La visione d’insieme di queste problematiche suggerisce che il processo indispensabile attraverso il quale passa la tutela e la conservazione delle popolazioni di Grillaio, dipende dalla corretta divulgazione relativa alla conoscenza del paesaggio e, più in generale, del territorio alla luce di una attenta politica di gestione dello stesso. 99 Bibliografia Aparicio, J.M. 1990. Activity, hunting method selection and daily energy budget of lesser kestrel (Falco naumanni) during premigratory period. Ardeola 37:163-178. Aparicio, J.M. 1990. Use of pellets of kestrels (Falco tinnunculus and Falco naumanni) as a sign of daily biomass intake. Ardeola 37:85-89. Aparicio, J.M. 1997. Costs and benefits of surplus offspring in the lesser kestrel (Falco naumanni). Behavioral Ecology and Sociobiology 41:129-137. Biber, J.-P. 1993. Workshop on lesser kestrel (Falco naumanni) conservation. p. 245. In M.K. Nicholls and R. Clarke [eds.]. Biology and conservation of small falcons: Proceedings of the 1991 Hawk and Owl Trust Conference. The Hawk and Owl Trust, London, England. Biber, J.-P. 1996. International Action Plan for the Lasser Kestrel (Falco naumanni). BirdLife International. European Commision. BirdLife International. 2004. Birds in Europe: population, estimates, trends and conservations status. Cambridge, UK; BirdLife International. (BirLife Conservation Series N. 12). Blanco, G. and J.L. Tella. 1997. Protective association and breeding advantages of choughs nesting in lesser kestrel colonies. Animal Behaviour 54:335-342. Brun, L. and P. Pilard. 1997. Reproduction of lesser kestrel Falco naumanni in Crau (France) in 1997. Faune de Provence (C.E.E.P.) 18:111-112. Brun, L. and P. Pilard. 1999. Adaptation du comportement de nidification chez le faucon crécerellette Falco naumanni en réponse a la compétition avec le choucas des tours Corvus monedula. Alauda 67:15-22. Brun, L., P. Pilard. and B. Kabouche. 1997. Le reproduction du faucon crècerellette Falco naumanni en Crau pour l'annèe 1996 et les premiers resultats du baguage. Faune de Provence (C.E.E.P.), n. 17, pp. 105-107. Bustamante, J. 1997. Predictive models for lesser kestrel Falco naumanni distribution, abundance and extinction in southern Spain. Biological Conservation 80:153-160. Bustamante, J. and J.J. Negro. 1994. The post-fledging dependence period of the lesser kestrel (Falco naumanni) in southwestern Spain. Journal of Raptor Research 28:158-163. Bux M. e Pavone A. 2005 Status del Grillaio Falco naumanni nelle gravine di Puglia e Basilicata. Avocetta 29: 107. Bux M., Pantone N., Massa B., Malacarne G., Rizzi V. E Palumbo G. (1997). Primi dati sull’alimentazione della popolazione di Grillaio Falco naumanni dell’italia peninsulare (Puglia e Basilicata). Avocetta 21: 112. Bux M., Perniola M. e Scillitani G. 2005 Biologia riproduttiva del Grillaio Falco naumanni in Italia meridionale. Avocetta 29: 176 Cade, T. J. 1982. The falcons of the world. Collins, London. 100 Caldarella M., Marrese M., Ventura T., De Lullo L. e Rizzi V. 2007. Nuovi dati sullo status del grillaio Falco naumanni nella provincia di Foggia. XIV Conv. Ital. Ornitologia. Abstract. Cramp S., Simmons K.E.L., 1980. The Birds of Western Paleartic. Vol. II. Oxford University Press, Oxford. Del Hoyo J, Elliott A, Sargatal J (1994). Handbook of the birds of the world. Vol. 2. New World Vultures to Guineafowl. Lynx Edicions, Barcelona. Donázar, J.A., F. Hiraldo and F. Hiraldo. 1993. Foraging habitat selection, land-use changes and population decline in the lesser kestrel Falco naumanna. Journal of Applied Ecology 30:515-522. Donázar, J.A., Negro J.J. and Hiraldo F. 1991. A note on the adoption of alien young by lesser kestrels Falco naumanni. Ardea 79:443-444. Donázar, J.A., Negro J.J. and Hiraldo F. 1992. Functional analysis of mate-feeding in the lesser kestrel Falco naumanni. Ornis Scandinavica 23:190-194. Forero, M.G., Tella J.L., Donázar J.A. and Hiraldo F. 1996. Can interspecific competition and nest site availability explain the decrease of lesser kestrel Falco naumanni populations?. Biological Conservation 78:289-293. Franco, A. 1982. Etograma cuantificado del cortejo en (Falco naumanni). Acta Vertebratica 9:139147. Hagemeijer, W. 1993. Ecological aspects of the lesser kestrel (Falco naumanni) in Extremadura, Spain. pp. 19-23. In M.K. Nicholls and R. Clarke [eds.] . Biology and conservation of small falcons: Proceedings of the 1991 Hawk and Owl Trust Conference. The Hawk and Owl Trust, London, England. Hiraldo, F., J.A. Donázar and J.J. Negro. 1994. Effects of tail-mounted radio-tags on adult lesser kestrels. Journal of Field Ornithology 65:466-471. Hiraldo, F., J.J. Negro and J.A. Donázar. 1991. Aborted polygyny in the lesser kestrel Falco naumanni (aves falconidae). Ethology 89:253-257. Hiraldo, F., J.J. Negro, J.A. Donázar and P. Gaona. 1996. A demographic model for a population of the endangered lesser kestrel in southern Spain. Journal of Applied Ecology 33:1085-1093. Lack D. 1955. Biritish Tits (Parus sp.) in nesting boxes. Ardea 43: 50-84. Lack D. 1958. A quantitative breeding study of British Tits. Ardea 46: 91-124. Lepley, M. 1994. L'etude des pelotes de rejection d'oiseaux insectivores: Methode, limite, et atlas de restes de proies du faucon crecerellete Falco naumanni en Plaine de Crau. Faune de Provence (C.E.E.P.) 15:5-15. Massa, B. 1992. Grillaio Falco naumanni. In: Brichetti P. et al. (eds.) - Fauna d'Italia. XXIX. Aves I. Edizioni Caldarini, Bologna: 346-351. Meschini E., Frugis S.,(Eds), 1993 - Atlante degli uccelli nidificanti in Italia. Suppl. Ric. Biol. Selvaggina, XX: 1-344. 101 Negro J J 1997. Falco naumanni Lesser Kestrel. In: Perrins C (ed). BWP UPDATE The Journal of Birds of the Western Palearctic. Vol. 1, No. 1. Oxford University Press, pp. 49-56. Negro, J.J. and F. Hiraldo. 1992. Sex ratios in broods of the lesser kestrel Falco naumanni. Ibis 134:190-191. Negro, J.J. and F. Hiraldo. 1993. Nest-site selection and breeding success in the lesser Kestrel Falco naumanni. Bird Study 40:115-119. Negro, J.J., F. Hiraldo and J.A. Donázar. 1997. Causes of natal dispersal in the lesser kestrel: inbreeding avoidance or resource competition?. Journal of Animal Ecology 66:640-648. Negro, J.J., J. Bustamante, C. Melguizo, J.L. Ruiz and J.M. Grande. 2000. Nocturnal activity of lesser kestrels under artificial lighting conditions in Seville, Spain. Journal of Raptor Research 34:327-329. Negro, J.J., J.A. Donázar and F. Hiraldo. 1992. Copulatory behaviour in a colony of lesser kestrels: sperm competition and mixed reproductive strategies. Animal Behaviour 43:921-930. Negro, J.J., J.A. Donázar and F. Hiraldo. 1992. Kleptoparasitism and cannibalism in a colony of lesser kestrels (Falco naumanni). Journal of Raptor Research 26:225-228. Negro, J.J., J.A. Donazar and F. Hiraldo. 1993. Home range of lesser kestrels (Falco naumanni) during the breeding season. pp. 144-150. In M.K. Nicholls and R. Clarke [eds.] . Biology and conservation of small falcons: Proceedings of the 1991 Hawk and Owl Trust Conference. The Hawk and Owl Trust, London, England. Negro, J.J., J.A. Donázar, F. Hiraldo, L.M. Hernández and M.A. Fernández. 1993. Organochlorine and heavy metal contamination in non-viable eggs and its relation to breeding success in a Spanish population of lesser kestrels (Falco naumanni). Environmental Pollution 82:201-205. Negro, J.J., M. de la Riva and J. Bustamante. 1991. Patterns of winter distribution and abundance of lesser kestrels (Falco naumanni) in Spain. Journal of Raptor Research 25:30-35. Negro, J.J., M. Villarroel, J.L. Tella, U. Kuhnlein, F. Hiraldo, J.A. Donazar and D.M. Bird. 1996. DNA fingerprinting reveals a low incidence of extra-pair fertilizations in the lesser kestrel. Animal Behaviour 51:935-943. Nicholls, M.K. and R. Clarke. 1993. Biology and conservation of small falcons; proceedings of the 1991 Hawk and Owl Trust conference. The Hawk and Owl Trust, London, England. Palumbo G., Rizzi V. e G. Malacarne. 1997. Contributo alla conoscenza di biologia riproduttiva, distribuzione e consistenza della popolazione di Grillaio (Falco naumanni) dell’Italia peninsulare. Avocetta 21: 206-212. Palumbo, G. 1997. Il Grillaio. Altrimedia Edizioni, Matera. Pantone N., M. Bux e G. Scillitani. 1999. Dieta del Grillaio Falco naumanni nell'Italia peninsulare. Avocetta 23:171. Parr, S., P. Collin, S. Silk, J. Wilbraham, N.P. Williams and M. Yarar. 1995. A baseline survey of lesser kestrels Falco naumanni in central Turkey. Biological Conservation 72:45-53. 102 Parr, S.J., M.A. Naveso and M. Yarar. 1996. Habitat and potential prey surrounding lesser kestrel Falco naumanni colonies in central Turkey. Biological Conservation 79:309-312. Perrins C.M. 1979. British Tits. Collins, London. Pomarol, M. 1993. Lesser kestrel (Falco naumanni) recovery project in Catalonia. pp. 24-28. In M.K. Nicholls and R. Clarke [eds.] . Biology and conservation of small falcons: Proceedings of the 1991 Hawk and Owl Trust Conference. The Hawk and Owl Trust, London, England. Pomarol, M. 1996. Artificial nest structure design and management implications for the lesser kestrel (Falco naumanni). Journal of Raptor Research 30:169-172. Sigismondi A., Cassizzi G., Cillo N., Laterza M., Losacco A., Muscianese E. 2003. Status e problemi di conservazione della popolazione di Grillaio Falco naumanni nelle Murge. Avocetta 27: 44. Sigismondi, A., G. Casizzi, N. Cillo, M. Laterza, V. Rizzi e T. Ventura. 1995. Distribuzione e consistenza delle popolazioni di Accipritiformi e Falconiformi nidificanti nelle regioni Puglia e Basilicata. Suppl. Ric. Biol. selvaggina, 22: 707-710. Tella, J.L. and M.G. Forero. 2000. Farmland habitat selection of wintering lesser kestrels in a Spanish pseudosteppe; implications for conservation strategies. Biodiversity and Conservation 9:433-441. Tella, J.L., F. Hiraldo, J.A. Donázar-Sancho and J.J. Negro. 1996. Costs and benefits of urban nesting in the lesser kestrel. pp. 53-60. In D.M. Bird, D.E. Varland and J.J. Negro [eds.]. Raptors in human landscapes. Academic Press Inc., San Diego, California. Raptor Research Foundation. Tella, J.L., J.A. Donázar and F. Hiraldo. 1996. Variable expression of sexually mosiac plumage in female lesser kestrels. Condor 98:643-644. Tella, J.L., J.A. Donazar, J.J. Negro and F. Hiraldo. 1995. Seasonal and interannual variations in the sex-ratio of lesser kestrel Falco naumanni broods. Ibis 138:342-345. Tella, J.L., J.A. Donazar, J.J. Negro and F. Hiraldo. 1996. Seasonal and interannual variations in the sex-ratio of lesser kestrel. Ibis 138:342-345. Tella, J.L., J.J. Negro, F. Hiraldo, J.A. Donazar, M.R. Villarroel, U. Kuhnlein and D.M. Bird. 1995. Abstract: DNA fingerprinting reveals successful polygyny in the lesser kestrel (Falco naumanni). Journal of Raptor Research 29:68. Tella, J.L., J.J. Negro, M. Villarroel, U. Kuhnlein, F. Hiraldo, J.A. Donázar and D.M. Bird. 1996. DNA fingerprinting reveals polygyny in the lesser kestrel (Falco naumanni). Auk 113:262-265. Tella, J.L., M.G. Forero, A. Gajón, F. Hiraldo and J.A. Donázar. 1996. Absence of bloodparasitization effects on lesser kestrel fitness. Auk 113:253-256. Tella, J.L., M.G. Forero, F. Hiraldo and J.A. Donázar. 1998. Conflicts between lesser kestrel conservation and European agricultural policies as identified by habitat use analyses. Conservation Biology 12:593-604. Tella, J.L., M.G. Forero, J.A. Donázar and F. Hiraldo. 1997. Is the expression of male traits in female lesser kestrels related to sexual selection?. Ethology 103:72-81. 103 Tella, J.L., M.G. Forero, J.A. Donázar, J.J. Negro and F. Hiraldo. 1997. Non-adaptive adoptions of nestlings in the colonial lesser kestrel: proximate causes and fitness consequences. Behavioral Ecology and Sociobiology 40:253-260. Tucker, G. M. and M. F. Heath. 1994. Birds in Europe: their conservation status. Cambridge, UK: BirdLife International (BirdLife Conservation Series n° 3). Ulfstrand S., Alatalo R.V., Carlsoon A. & Lundberg A. 1981. Habitat distribution and body size of the Great Tit Parus major. Ibis 123: 494-499. Zollinger, R. and W.J.M. Hagemeijer. 1994. The lesser kestrel Falco naumanni: review of the status of a globally threatened species. pp. 219-228. In B.-U. Meyburg and R.D. Chancellor [eds.] . Raptor Conservation Today. Pica Press, London. Proceedings of the IV World Conference on birds of prey and owls, Berlin, Germany, May 10-17, 1992.. (World Working Groups on Birds of Prey and Owls). 104
Scaricare