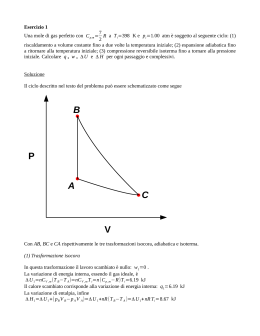
Fotografia al microscopio elettronico del complesso della Piruvato Deidrogenasi di Escherichia coli Estremità ammino terminale Rappresentazione del dominio transacetilasico delle tre subunità di E2. Il dominio di una di esse è rappresentato in colore. In colore è rappresentata la struttra di ciascuno dei tre monomeri che costituiscono gli otto trimeri catalitici componenti il nucleo (E2) del complesso della PDH. BERIBERI malattia neurologica e cardiologica causata da carenza nutrizionale di vitamina B1, osservata anche sporadicamente negli alcolisti in avanzato stato di malnutrizione. Il danno al sistema nervoso periferico si manifesta sotto forma di dolore agli arti, debolezza muscolare ed alterazione della sensibilità cutanea. Il cuore può essere ingrossato e la gittata cardiaca inadeguata. Nel Beriberi le concentrazioni ematiche di Piruvato deidrogenasi e di -chetoglutarato deidrogenasi sono più alte del livello normale. L’aumento della concentrazione ematica di piruvato è particolarmente pronunciato dopo l’ingestione di glucosio. Una sintomatologia simile a quella del Beriberi si manifesta quando un organismo viene esposto al mercurio o all’arsenito (AsO33-) Intossicazione da arsenito Alcuni reagenti sulfidrilici come il 2,3-Dimercaptopropanolo, detto BAL (British antilewisite) perché utilizzato dopo la prima guerra mondiale come antidoto contro la Lewisite, un’arma chimica basata sull’arsenico, attenuano l’inibizione del complesso della PDH, formando un composto che viene escreto con l’urina. CONTROLLO ALLOSTERICO E COVALENTE DELLA PDH PIRUVATO + CoASH + NAD+ PDHK E1, E2, E3 PDHPasi AcetilCoA + CO2 + NADH + H+ I prodotti competono con i substrati per il sito attivo dei rispettivi substrati. Legame del Citrato al complesso ferro-zolfo dell’Aconitasi Centro ferro-zolfo 4Fe-4S, componente del sito attivo dell’aconitasi - 7,6 Kcal/mole - 3,2 Kcal/mole - 5 Kcal/mole + 7,1 Kcal/mole - 0,9 Kcal/mole - 8 Kcal/mole 0 Kcal/mole - 0,7 Kcal/mole G°(totale) = – 32,5 Kcal/mole
Scaricare