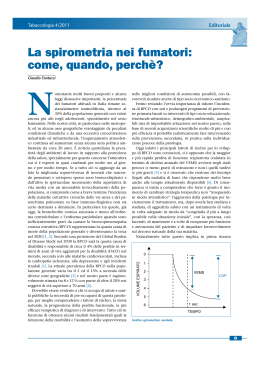
Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 A cura di Mario De Palma e Leonardo Fabbri FEDERAZIONE ITALIANA CONTRO LE MALATTIE POLMONARI SOCIALI E LA TUBERCOLOSI Indice Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Indice Indice Autori pag. 4 Presentazione pag. 6 Definizione, classificazione ed eziopatogenesi pag. 10 Epidemiologia e costi socio-economici pag. 20 BPCO: dimensione sociale pag. 30 Anatomia-patologica pag. 44 Quadri clinici e stadiazione pag. 54 pag. 60 secondaria alla BPCO pag. 70 Ruolo delle infezioni nelle riacutizzazioni della BPCO pag. 80 Disturbi cardio-respiratori nel sonno nella BPCO pag. 90 Terapia e prevenzione pag. 100 Programma educazionale nella BPCO pag. 116 Insufficienza respiratoria cronica e sua terapia pag. 126 La riabilitazione respiratoria nel trattamento della BPCO pag. 136 La BPCO nell’anziano pag. 144 Il medico di Medicina generale nella gestione della BPCO pag. 152 pag. 158 1 2 3 4 5 6 Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale 7 8 9 10 11 12 13 14 15 16 Cuore polmonare cronico ed ipertensione polmonare Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità 3 Indice Autori Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Indice Autori Nicolino Ambrosino Sandra Baldacci Simonetta Baraldo Bianca Beghè Vincenzo Bellia Stefania Bertini Germano Bettoncelli Caterina Brindicci Mauro Carone Laura Carrozzi Cristina Cinti Lorenzo Corbetta Antonio Corrado Mario De Palma Luisa M. Esposito Leonardo M. Fabbri Mariadelaide Franchi Giuseppe Insalaco Fabrizio Luppi Sara Maio Gabriella Matteelli Anna Maria Moretti Oreste Marrone Margherita Neri Marco Piattella Francesco Pistelli Roberta Poggi Alfredo Potena Andrea Rossi Marina Saetta Antonio Scognamiglio Massimiliano Serradori Antonio Spanevello Graziella Turato Giovanni Viegi Renzo Zuin 5 Presentazione Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Presentazione Fra le patologie croniche respiratorie, la broncopneumopatia cronica ostruttiva (BPCO) rappresenta in Italia, come negli altri paesi industrializzati, una delle più frequenti cause di malattia, di invalidità e morte. Condizionata dal fumo di tabacco e dall’inquinamento ambientale e professionale, secondo l’Organizzazione Mondiale della Sanità (OMS), è destinata ad aumentare nei prossimi vent’anni, risultando fra le prime cause di morte e malattia se non saranno prese efficaci misure preventive, diagnostiche e terapeutiche, a carattere individuale e sociale. A causa della BPCO e delle sue riacutizzazioni, ogni anno, è sempre più elevato il numero di soggetti adulti, vecchi ed anche giovani che debbono abbandonare il lavoro e le loro abitudini per periodi prolungati; altrettanto elevato è il numero annuale di ricoveri, giornate di ospedalizzazione e visite ambulatoriali e domiciliari, legato alla malattia ed alle sue complicazioni. Purtroppo, sebbene la diffusione ed il peso socio-sanitario della BPCO siano noti da anni, sebbene siano numerosi, in campo internazionale e nazionale, i tentativi di sensibilizzare le Sanità pubbliche, sebbene siano incisivi gli interventi per migliorare le conoscenze dei medici, per rendere più efficaci le misure preventive, per migliorare il controllo della malattia e la qualità di vita dei soggetti malati, la BPCO è in costante aumento per numero di malati e per gravità, è tuttora poco conosciuta, sottodiagnosticata e soprattutto diagnosticata e curata in ritardo ed in maniera insufficiente. Per questo complesso di ragioni, dal 2001, un gruppo di lavoro, costituito da esperti scelti dall’OMS e dall’Istituto Statunitense per le Malattie Polmonari, Cardiache e del Sangue (NHLBI), ha lanciato il Progetto Mondiale per la Diagnosi, il Trattamento e la Prevenzione della broncopneumopatia cronica ostruttiva (Global Iniziative for Chronic Obstructive Lung Disease-GOLD-COPD) ed ha realizzato e diffuso delle Linee Guida per la Diagnosi ed il Trattamento della BPCO, con aggiornamenti annuali. In Italia, in successione, le Linee Guida GOLD sono state discusse ed adattate alla realtà nazionale, per la redazione di Linee Guida Italiane per la BPCO, disponibili, con tutto il materiale prodotto, nel sito www.goldcopd.it. Il documento, periodicamente aggiornato, è stato pubblicato e diffuso, in ambito specialistico e della Medicina generale, per affrontare, con efficacia sempre maggiore, la BPCO nel nostro paese. Le azioni finalizzate a rimuovere le situazioni problematiche che, fino ad oggi, hanno ostacolato una buona conoscenza ed un controllo ottimale della malattia, si sono moltiplicate sia nel settore scientifico sia 7 nel settore sociale e formativo-educazionale. Le Società Scientifiche nazionali, la Fondazione Pneumologia UIP e l’Associazione pazienti BPCO sollecitano interventi politico-sanitari per la riduzione ed il contenimento dei danni da fumo di tabacco e da inquinamento ambientale e parimenti provvedimenti legislativi a favore dei pazienti allo scopo di migliorare la qualità di vita dei malati e ridurre l’impatto socio-economico della malattia. Anche la Federazione Italiana contro le Malattie Polmonari Sociali e la Tubercolosi, che ritiene fondamentale il continuo approfondimento culturale diretto ad ottimizzare il rapporto medico-paziente e a diffondere, anche all’esterno del mondo specialistico, sulla base di evidenze scientifiche, una cultura specifica rivolta al miglioramento del controllo delle malattie respiratorie più diffuse, intende fornire un ulteriore contributo pratico ed applicativo diretto alle più recenti problematiche della BPCO, pubblicando una monografia, che, secondo una consolidata dizione, si intitola “Rapporto sulla BPCO 2005”. Con la preziosa collaborazione della Delegazione Italiana GOLD, i capitoli della monografia sono stati affidati ad alcuni dei maggiori esperti nazionali in materia, per una trattazione sintetica, ma esauriente e collegata alle Linee Guida, dei 8 principali temi teorici, pratici ed applicativi, con l’obiettivo di dare, soprattutto ai medici di Medicina generale italiani, uno strumento per affrontare quotidianamente ed in prima linea, i problemi della malattia. Altri obiettivi sono: migliorare la prevenzione, diminuire progressivamente la quota di pazienti che sfugge alla diagnosi ed alle terapie, migliorare il grado di aderenza dei pazienti alle prescrizioni, ritardare l’evoluzione della malattia. La monografia, divisa in 16 capitoli, nella prima parte, dopo la definizione, la classificazione e la descrizione dei fattori eziopatogenetici della BPCO, ne esamina gli aspetti epidemiologici, i costi socio-economici e la dimensione sociale. In successione tratta gli aspetti anatomo-patologici, il quadro clinico, la stadiazione, la fisiopatologia della limitazione di flusso, la diagnosi differenziale, il cuore polmonare cronico e l’ipertensione polmonare, secondaria alla BPCO. Nei quattro capitoli successivi prende in esame il ruolo delle infezioni nelle riacutizzazioni della malattia, i disturbi cardio-respiratori nel sonno, gli aspetti della prevenzione con la riduzione dei fattori di rischio, la terapia, ed il programma educazionale. Dopo i capitoli sull’insufficienza respiratoria cronica e sua terapia e sulla riabilitazione respiratoria nel trattamento della malattia, considera il problema della BPCO nell’anziano, il coinvolgimento del medico di Medicina generale nella gestione della BPCO, la qualità di vita, la misurazione dello stato di salute respiratoria ed i problemi di comorbidità. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Gli aspetti comuni, di argomenti confinanti fra loro, hanno portato, probabilmente, ad alcune sovrapposizioni, ad alcune ripetizioni e forse ad apparenti contraddizioni, che sono state conservate, per dare la possibilità di confrontare e valutare visioni ed interpretazioni parallele ed articolate degli stessi problemi. Alla monografia viene allegato un CD, contenente materiale complementare al testo sui principali temi riferiti alla BPCO e sulle Linee Guida GOLD. Siamo certi che la monografia potrà rappresentare uno strumento educazionale di semplice lettura e di facile consultazione, contribuendo da una parte a migliorare le conoscenze sulla malattia, dall’altra a rendere meno problematiche le questioni tuttora aperte nell’ambito della più diffusa patologia cronica respiratoria: ridurne la prevalenza e la mortalità, migliorare il controllo della malattia e delle sue riacutizzazioni, ridurre gli interventi del pronto soccorso, ridurre il numero dei ricoveri ospedalieri e delle degenze, ridurre la perdita di giornate lavorative e conseguentemente migliorare la qualità di vita, la validità lavorativa e le aspettative sociali di tanti pazienti, diminuendo il costo socio-economico che grava sui cittadini e sulla società. Nel dare alle stampe la monografia, ringraziamo gli Autori che hanno assolto l’incarico, in maniera esauriente, condividendo la campagna educazionale e divulgativa della Federazione Italiana contro le Malattie Polmonari Sociali e la Tubercolosi, nello spirito della GOLD-COPD. Parimenti ringraziamo Boehringer-Ingelheim e Pfizer che hanno sostenuto la pubblicazione dell’opera, condividendo anch’essi i nostri obiettivi. Un particolare grato riconoscimento a GPAnet, che ha curato l’organizzazione editoriale ed ha realizzato con puntualità e professionalità la stampa di questo volume. Mario De Palma Leonardo Fabbri Presidente Federazione Italiana contro le Malattie Polmonari Sociali e la Tubercolosi Direttore della Clinica di Malattie dell’Apparato Respiratorio Università degli Studi di Modena e Reggio Emilia 9 1. Definizione, classificazione ed eziopatogenesi A cura di Fabrizio Luppi e Leonardo M. Fabbri Clinica di Malattie dell’Apparato Respiratorio Università degli Studi di Modena e Reggio Emilia 1. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) è una sindrome caratterizzata da limitazione al flusso espiratorio, irreversibile o poco reversibile ed evolutiva, causata da una specifica flogosi cronica delle vie aeree e del parenchima polmonare indotta da irritanti, in particolare dal fumo di sigaretta (1,2). La peculiare alterazione funzionale della BPCO è rappresentata da un’accelerata caduta del VEMS (circa 40-100 ml/anno nel paziente fumatore con BPCO rispetto a circa 10-40 nel normale non fumatore) (3). Nelle sue fasi iniziali, il paziente - pur presentando un deterioramento della funzionalità respiratoria - è spesso asintomatico, in particolare non presenta dispnea, mentre tosse ed escreato cronici possono insorgere anche in soggetti con funzione respiratoria normale. L’insorgenza di dispnea dipende da una certa variabilità interindividuale, ma di solito non insorge fino a quando il paziente non presenta una significativa limitazione al flusso espiratorio. La limitazione al flusso espiratorio può comunque non essere la sola responsabile della dispnea, in quanto ad essa possono contribuire anche l’iperinflazione, le alterazioni dei muscoli scheletrici e l’alterazione degli scambi gassosi con conseguente ipossiemia. L’acronimo BPCO rappresenta un termine non specifico, riferito a due diverse entità nosologiche, la bronchite cronica e l’enfisema, che si sviluppano progressivamente quale risultato di diverse alterazioni anatomo-patologiche e funzionali. Le più recenti Linee Guida limitano le loro indicazioni alla BPCO indotta da irritanti ed in particolare dal fumo di sigaretta, includendo nel termine le entità nosologiche bronchite cronica ed enfisema ed escludendo quindi sia le forme di ostruzione dovute ad altre malattie quali gli esiti di tubercolosi, le bronchiectasie, le neoplasie, la fibrosi cistica in età adulta, che il più frequente sottogruppo di pazienti affetti da asma bronchiale che sviluppano ostruzione poco reversibile. Nel corso degli anni, la BPCO è stata definita in diversi modi e queste diverse definizioni hanno avuto un diverso impatto sulle stime epidemiologiche della malattia (4). Pur tenendo conto delle diverse definizioni, in particolare funzionali (vedi paragrafo sottostante) che possono ovviamente influenzare la prevalenza della malattia (4), a parità di definizione diagnostica, l’incidenza e la mortalità dovute alla BPCO sono in costante, preoccupante incremento negli ultimi anni (1). Definizione di BPCO Il primo documento dell’American Thoracic Society (ATS) ha definito la BPCO “una malattia caratterizzata dalla presenza di limitazione al flusso espiratorio solo parzialmente reversibile, causata da bronchite cronica od enfisema, in genere a carattere evolutivo ed associata ad iperreattività bronchiale” (5). Il primo documento della European Respiratory Society (ERS) ha invece definito la BPCO in termini fisiopatologici più accurati, come “ridotti flussi massimi espiratori con rallentato svuotamento dei polmoni”, sottolinenando ciò che in realtà misuriamo con le prove funzionali respiratorie (non la limitazione al flusso espiratorio), evidenziando che tali alterazioni sono evolutive, in buona parte irreversibili al trattamento farmacologico (5,6). Le Linee Guida GOLD (1) definiscono la BPCO come un quadro nosologico caratterizzato da una limitazione del flusso aereo poco reversibile ed evolutiva, introducendo il concetto che la limitazione del flusso aereo non è solo dovuta all’ostruzione del lume bronchiale conseguente al rimodellamento delle vie aeree, ma anche alla perdita di supporto elastico da parte del parenchima polmonare distrutto dal processo enfisematoso. Tali Linee Guida introducono anche il concetto che la peculiare alterazione funzionale che caratterizza la BPCO (riduzione del flusso) ha di solito carattere evolutivo ed è associata ad un specifica risposta infiammatoria delle vie aeree e del parenchima polmonare all’inalazione di sostanze irritanti, in particolare il fumo di sigaretta (1). L’ultimo documento congiunto ATS/ERS estende la definizione data dalle Linee Guida GOLD, intro- 11 12 ducendo il concetto che la BPCO non è solo una malattia polmonare ma spesso sistemica ed associata a comorbidità (7). Pur se non chiaramente riferito nelle varie Linee Guida, va ribadito che le conoscenze e raccomandazioni da esse riportate fanno tutte riferimento alla limitazione al flusso espiratorio causata da irritanti, e che quindi il termine BPCO dovrebbe forse limitarsi solo a questa malattia. Il che richiede nel singolo paziente almeno la presenza di due criteri orientativi: il primo il fattore di rischio sia esso il fumo e/o la esposizione ad irritanti ed il secondo l’età (ad esempio superiore ai 40 anni) in quanto è improbabile lo sviluppo di BPCO al di sotto di 40 anni tranne nei casi di soggetti predisposti per deficit di α-1 antitripsina (8,9) o di sesso femminile con predisposizione indeterminata, verosimilmente genetica (10). In altre parole la sola diagnosi spirometrica non è mai comunque sufficiente. A parte alcune delle cause di limitazione al flusso espiratorio sopra riferite, va considerata la presenza di un certo numero di soggetti non fumatori che presenta una limitazione al flusso espiratorio di origine non chiara, che può andare, da alterazioni dello sviluppo delle vie aeree ai residui di ricorrenti infezioni broncopolmonari avvenute in età infantile. Nel singolo paziente è quindi indispensabile andare oltre al semplice esame spirometrico e completare gli accertamenti con una accurata anamnesi, esami per immagini (radiografia e a volte TAC toracica), esami ematochimici e microbiologici. Tutte le definizioni di BPCO hanno comunque in comune il concetto di BPCO come malattia funzionale respiratoria, in quanto tutte rimandano a tale valutazione, la spirometria in particolare, il compito di misurare la limitazione al flusso espiratorio e quindi porre la diagnosi. Tuttavia tutte differiscono nella definizione di alterazione funzionale minima considerata significativa e nelle condizioni della sua misura, se in condizioni basali o dopo broncodilatatore (1,5). Limitazione al flusso espiratorio Il concetto comune alle varie Linee Guida è che per limitazione al flusso espiratorio si intende una riduzione del VEMS, del suo rapporto con la capacità vitale forzata (CVF) o lenta (CV) e che tale riduzione non è reversibile al trattamento farmacologico. La definizione di limitazione al flusso espiratorio proposta nel 1995 dall’European Respiratory Society faceva riferimento al rapporto fra VEMS e CV lenta, non forzata, e dava i limiti del 88% per l’uomo e del 89% per la donna, rispetto ai teorici della Comunità Europea (6). Successivamente la definizione di limitazione al flusso espiratorio proposta sia dalle Linee Guida GOLD che dalle Linee Guida ATS/ERS fa riferimento al rapporto limite fisso di 70% del valore assoluto del rapporto VEMS/CVF (1,7). In entrambi i casi, proprio per togliere di mezzo la componente reversibile, si fa riferimento a valori misurati dopo broncodilatatore, anche se purtroppo nessuna delle Linee Guida fornisce protocolli standard di esecuzione della broncodilatazione. Se pure l’uso delle diverse definizioni può portare a stime molto diverse di prevalenza di limitazione al flusso espiratorio (4) ed in particolare ad una sovrastima della prevalenza negli anziani se si fa ricorso al limite del 70% del valore assoluto del rapporto VEMS/CVF, tale sovrastima ha rilevanza puramente epidemiologica in quanto riguarda quasi esclusivamente la BPCO di grado lieve. Lo stesso vale per il limite spirometrico valutato prima o dopo broncodilatatore: è ovvio che se i valori spirometrici sui quali si definisce la diagnosi vengono misurati prima del broncodilatatore vi sarà una sovrastima della percentuale di soggetti con BPCO. REVERSIBILITÀ DELLA LIMITAZIONE AL FLUSSO ESPIRATORIO La reversibilità della limitazione al flusso espiratorio può essere misurata in termini di risposta alla singola somministrazione di un broncodilatatore inalatorio o ad un ciclo di terapia steroidea somministrati per via inalatoria od orale (1). La definizione proposta dall’American Thoracic Society non Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 1. Definizione, classificazione ed eziopatogenesi - F. Luppi, L. M. Fabbri definisce specificamente la reversibilità, nonostante un precedente documento dell’ATS avesse classificato tale parametro come un aumento del VEMS di 200 ml e del 12% dopo somministrazione di un broncodilatatore per via inalatoria (11). La definizione di BPCO della European Respiratory Society definiva invece tale parametro come un aumento del VEMS >10% del teorico dopo somministrazione di un broncodilatatore (6). La GOLD definisce invece la reversibilità come un aumento del VEMS di 200 ml e del 12% rispetto al basale dopo somministrazione di una singola dose di broncodilatatore o dopo un ciclo di corticosteroidi per via inalatoria od orale (1). Il termine “parzialmente reversibile” spesso utilizzato anche se mal definito, fa riferimento a pazienti che presentano un miglioramento della limitazione al flusso espiratorio a seguito di somministrazione di corticosteroidi o broncodilatatori, che tuttavia presentano valori di VEMS e/o di VEMS/CVF che comunque non raggiungono valori normali. In questo ambito, tuttavia, esistono ampi livelli di reversibilità che, se misurata in termini di aumento percentuale di VEMS rispetto al basale, possono andare dallo 0 a >50%. In passato la reversibilità veniva usata per distinguere quadri di BPCO, poco o nulla reversibili, da quadri di asma ampiamente reversibile, oggi tale distinzione si affida di più alla anamnesi e ad esami della infiammazione bronchiale (eosinofili nell’espettorato, concentrazione di ossido nitrico NO nell’aria esalata) (12). Il minor ricorso ai test di reversibilità è anche dovuto alla loro bassa riproducibilità individuale (13) ed al fatto che tali test si basano sul VEMS e non tengono conto dei volumi polmonari, in particolare della iperinflazione presente nei soggetti con BPCO. È possibile infatti che in soggetti definiti come non reversibili in termini di aumento di VEMS, vi sia un significativo aumento di volumi statici quali il volume di riserva inspiratoria (VRI) e la capacità inspiratoria (CI) a spese della riduzione della capacità funzionale residua (CFR). In questi soggetti, la risposta in termini di volume al trattamento farmacologico, può meglio spiegare la risposta clinica sia in termini di riduzione di dispnea a riposo, sia in termini di miglior tolleranza allo sforzo (14). Il test di reversibilità è stato anche molto usato in studi clinici randomizzati per restringere la casistica ai casi più “puri” di BPCO, reclutando solo soggetti con un aumento di VEMS dopo broncodilatatore o ciclo di steroidi di un massimo di 200 ml o 10-15%. Anche questo criterio di inclusione tende ad essere messo in disuso, sia per la bassa riproducibilità dei test di misura, sia perché si è osservato che nella BPCO la risposta ai farmaci in termini clinici (riduzione della dispnea o aumento della tolleranza allo sforzo) si può sviluppare anche in soggetti con bassa reversibilità (14,15). VALUTAZIONE DI GRAVITÀ DELLA BPCO In analogia all’anamnesi, anche la valutazione di gravità della BPCO viene fatta sulla base di parametri funzionali ed in particolare del VEMS. Nelle Linee Guida GOLD (1) si fa riferimento anche all’analisi della concentrazione ematica di O2 e CO2 e del pH misurati su sangue arterioso, nei pazienti gravi, mentre le Linee Guida ATS/ERS citano l’utilità di completare la valutazione con altri test, quali la prova da sforzo, il test del cammino, la percezione della dispnea, ed il body mass index, che sono stati considerati utili nel definire la gravità della BPCO (16). I criteri proposti dall’American Thoracic Society classificano la BPCO in 3 stadi (5): Stadio 1: VEMS ≥50% del teorico Stadio 2: VEMS 35-49% del teorico Stadio 3: VEMS <35% del teorico I criteri proposti dall’European Respiratory Society classificano anch’essi la BPCO in 3 stadi (6): Lieve: VEMS ≥80% del teorico Moderata: VEMS 50-80% del teorico Grave: VEMS <50% del teorico 13 I criteri proposti dal GOLD (1) e dal documento ATS/ERS (7) classificano la BPCO in 4 stadi. In presenza di un rapporto VEMS/CVF postbroncodilatatore inferiore al 70%, la BPCO viene definita: Stadio 1, lieve: in presenza di un VEMS ≥80% del teorico Stadio 2, moderata: in presenza di un VEMS compreso fra il 50% e l’80% del teorico Stadio 3, grave: in presenza di un VEMS compreso fra il 30% e il 50% del teorico Stadio 4, molto grave: in presenza di un VEMS <30% del teorico Gli stadi GOLD risultano quindi i seguenti: Stadio 0 - a rischio: in presenza di sintomi di bronchite cronica e di spirometria normale. Stadio I - BPCO lieve: caratterizzato da presenza di una lieve riduzione del flusso aereo espiratorio (VEMS/CVF <70%, con VEMS >80% del teorico), in presenza o assenza di sintomi respiratori. A questo stadio il soggetto fumato respesso non si rende conto di avere già una alterazione funzionale respiratoria. Stadio II - BPCO moderata: caratterizzato da peggioramento della broncoostruzione 50% <VEMS <80%), associato di solito con sintomi respiratori, in particolare dispnea da sforzo, che compare di solito sotto sforzo. Si tratta dello stadio nel quale più spesso il paziente richiede l’intervento del medico a causa della dispnea da sforzo o per una riacutizzazione della malattia. 14 Stadio III - BPCO grave: caratterizzato da ulteriore peggioramento della broncoostruzione (30% <VEMS <50%) e aumento della dispnea e delle riacutizzazioni che peggiorano la qualità di vita. Stadio IV - BPCO molto grave: caratterizzato da una grave limitazione al flusso espiratorio (VEMS <30% del teorico) o dalla presenza di insufficienza respiratoria cronica. L’insufficienza respiratoria è definita da una pressione parziale dell’ossigeno arterioso (PaO2) inferiore a 8,0 kPa (60 mmHg) con o senza una pressione parziale della CO2 (PaCO2) maggiore di 6.7 kPa (50 mmHg) a livello del mare. L’insufficienza respiratoria può anche avere effetti sul cuore, come nel caso del cuore polmonare (insufficienza cardiaca destra). I segni clinici di cuore polmonare comprendono turgore delle vene giugulari ed edemi declivi. I pazienti possono soffrire di una BPCO grave (Stadio III) anche se il VEMS è maggiore del 30% del teorico nei casi in cui tali complicazioni siano presenti. In questo stadio la qualità di vita è notevolmente compromessa dal peggioramento della broncoostruzione (50%) e le riacutizzazioni possono minacciare la vita del paziente. Queste classificazioni di gravità si sono dimostrate molto utili come riferimenti nosologici per la miglior caratterizzazione della BPCO. Ad esempio un recente elegante studio anatomo-patolgico ha dimostrato una buona correlazione fra infiammazione e rimodellamento broncopolmonare e livello di gravità (17), e buona correlazione si è trovata anche fra gravità e parametri di qualità di vita (18). Va precisato con in ogni caso si tratta di classificazioni di gravità puramente spirometriche, utili ai fini didattici e forse medico-legali, ma certamente non clinici in quanto la correlazione fra alterazione spirometrica e quadro clinico, in particolare gravità dei sintomi e di tolleranza allo sforzo, è significativa ma bassa. La valutazione di gravità individuale quindi e soprattutto la decisione terapeutica devono comunque far riferimento ai sintomi ed alle malattie concomitanti che spesso si accompagnano alle forme più gravi di BPCO. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 1. Definizione, classificazione ed eziopatogenesi - F. Luppi, L. M. Fabbri BRONCHITE CRONICA Nel sottolineare le due componenti della BPCO, la bronchitica e l’enfisema, si introduce il rischio di generare un po’ di confusione in riferimento alla bronchite. In realtà, in termini anatomo-patologici, la componente bronchitica (termine usato per indicare infiammazione a carico dei bronchi) dovrebbe essere definita bronchiolitica, in quanto le alterazioni anatomo-patologiche si sviluppano a carico delle vie aeree più periferiche (fig. 1). Figura 1 – Meccanismi che determinano l’ostruzione bronchiale nel paziente affetto da BPCO INFIAMMAZIONE Patologia delle piccole vie Infiammazione bronchiale Rimodellamento bronchiale Distruzione parenchimale Perdita degli attacchi alveolari Riduzione del ritorno elastico RIDUZIONE DEL FLUSSO AEREO Il termine bronchite cronica dovrebbe invece essere limitato alla entità nosologica clinica caratterizzata dalla presenza di tosse con espettorato cronico per almeno 3 mesi all’anno che perdura da almeno 2 anni (11). Ovviamente anche per la bronchite cronica vanno escluse le altre cause di tosse ed escreato cronici, in particolare l’infezione con il Mycobacterium tuberculosis, il carcinoma del polmone, lo scompenso cardiaco cronico, le bronchiectasie, la fibrosi cistica, ecc. Il termine bronchite cronica è stato criticato in quanto indica la presenza di un’infiammazione e non di un’aumentata secrezione di muco della parete bronchiale. Tuttavia numerosi studi anatomo-patologici hanno dimostrato che i sintomi di bronchite cronica sono più associati ad un’infiammazione cronica della parete bronchiale che ad alterazioni strutturali dell’apparato mucosecernente (19). ENFISEMA POLMONARE Il termine enfisema viene riservato al quadro anatomo-patologico polmonare caratterizzato da un permanente, anomalo ingrandimento degli spazi aerei distali ai bronchioli terminali non respiratori, accompagnato da distruzione delle loro pareti, senza fibrosi evidente. Tale alterazione porta ad una riduzione della forza di ritorno elastico del polmone e ad aumento delle resistenze a livello delle piccole vie aeree, alterazioni strutturali verosimilmente responsabili delle alterazioni funzionali respiratorie (limitazione al flusso espiratorio, aumento della capacità funzionale residua, iperinflazione) e della sintomatologia in particolare la dispnea e la limitata tolleranza allo sforzo. Pur rimanendo l’enfisema una entità nosologica basata essenzialmente sul quadro anatomo-patologico e quindi inutilizzabile nel singolo paziente, oggi è possibile valutarlo mediante la tomografia assiale computerizzata ad alta risoluzione (HRCT scan), il che ha ricadute cliniche rilevanti soprattutto per i pazienti con quadri gravi candidabili al trattamento chirurgico o con riduzione dei volumi polmonari o con trapianto polmonare (20). 15 ASPETTI SISTEMICI DELLA BPCO Nella valutazione del paziente affetto da BPCO, vanno tenuti presenti anche gli aspetti sistemici della malattia. In particolare può essere utile fare una stima della massa magra (21,22) in particolare nei soggetti cachettici, dello stato funzionale (23,24), della tolleranza allo sforzo e della presenza di malattie concomitanti quali lo scompenso cardiaco, l’ipertensione arteriosa, le vasculopatie, la depressione e dei trattamenti per esse instaurati (25). Nonostante questi fattori non siano formalmente compresi nella definizione di BPCO, essi sono importanti in termini clinici nel singolo paziente, e devono essere presi in considerazione. Fattori di rischio In Italia, come nella maggior parte dei paesi sviluppati, la BPCO è essenzialmente una malattia causata dal fumo di sigaretta. Inquinamento domestico, ambientale e lavorativo hanno oggi un peso molto inferiore rispetto al fumo di sigaretta, anche se, in particolare per l’inquinamento ambientale da motoveicoli, è possibile che si vada incontro ad una preoccupante inversione di tendenza. 16 FUMO DI SIGARETTA L’evidenza più solida per un rapporto causale fra uno specifico fattore di rischio e la BPCO riguarda il fumo di sigaretta. Molti studi epidemiologici hanno dimostrato che il fumo di sigaretta rappresenta il principale fattore di rischio per la BPCO. Le persone che fumano presentano più sintomi respiratori, un’accelerata caduta del VEMS ed un più elevato tasso di mortalità per BPCO rispetto ai non fumatori. L’età di inizio, il numero totale di sigarette fumate e lo stato di fumatore sono predittivi di mortalità per BPCO. Non tutti i fumatori sviluppano una BPCO clinicamente rilevante, tuttavia, i più recenti studi epidemiologici hanno mostrato che la maggior parte dei fumatori, se sopravvivono e fumano a sufficienza, svilupperanno limitazione al flusso espiratorio (26). Smettere di fumare rallenta la caduta del VEMS e quindi l’evoluzione della BPCO (27). I fumatori di pipa e sigaro presentano tassi di morbidità e mortalità per BPCO più alti rispetto ai non fumatori, anche se tali tassi sono inferiori rispetto ai fumatori di sigaretta. L’esposizione passiva al fumo di sigaretta aumenta la frequenza di insorgenza dei sintomi respiratori nell’adulto (28), anche se gli effetti del fumo passivo sulla funzione respiratoria sono ovviamente minori del fumo attivo. INQUINAMENTO AMBIENTALE In tutto il mondo, ma in maniera sempre più preoccupante in particolare nei paesi in via di sviluppo, un importante fattore di rischio per lo sviluppo della BPCO è rappresentato dall’esposizione agli inquinanti degli ambienti interni, in particolare quelli prodotti dalla combustione dei materiali utilizzati per il riscaldamento e per cucinare. In alcuni paesi in via di sviluppo, nei quali si cucina e ci si riscalda in abitazioni poco ventilate, si osservano elevati livelli di inquinamento degli ambienti interni per accumulo di particolato ambientale (29, 30). Le donne sono maggiormente esposte a tali fattori di rischio, il che può spiegare una simile prevalenza della BPCO nelle donne rispetto agli uomini in paesi quali l’India, la Cina, l’America Latina, ove esiste una netta differenza nell’abitudine tabagica a favore del sesso maschile (31). Il ruolo dell’inquinamento atmosferico nell’insorgenza della BPCO è meno chiaro, anche se sembra essere di scarso rilievo se paragonato all’abitudine tabagica. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 1. Definizione, classificazione ed eziopatogenesi - F. Luppi, L. M. Fabbri ESPOSIZIONE PROFESSIONALE Una rilevante esposizione a polveri (inorganiche ed organiche), gas o fumi di origine professionale è associata ad un aumentato rischio di insorgenza della BPCO, che è indipendente dall’abitudine tabagica. Tali fattori di rischio professionali sono tuttavia sinergici con il fumo di sigaretta (32). In altre parole, la probabilità di contrarre la BPCO in un paziente esposto a fattori di rischio professionali è significativamente maggiore se tale soggetto fuma abitualmente (33). PREDISPOSIZIONE INDIVIDUALE Nonostante sia noto che il rischio di contrarre la BPCO dipenda essenzialmente dal numero di sigarette fumate e dalla durata dell’abitudine tabagica, è chiaro che esiste un’ampia variabilità interindividuale nei confronti dello sviluppo della malattia. Nonostante gli effetti dell’esposizione a vari fattori di rischio ambientali siano cumulativi, essi non sono tuttavia sufficienti a spiegare le differenze fra vari soggetti fumatori, anche a parità di numero di sigarette fumate, sul deterioramento della funzionalità respiratoria. L’evidenza che i fattori genetici sono importanti nella patogenesi della BPCO deriva dall’osservazione di soggetti con severo deficit di α-1-antitripsina, il principale inibitore delle serino-proteasi, i quali presentano un elevato rischio di sviluppare la BPCO (34). I soggetti che presentano tale deficit e che fumano tendono a sviluppare una malattia più grave e più precoce rispetto ai soggetti con un deficit di α-1-antitripsina di uguale gravità, ma che non fumano (35). Inoltre, parenti di primo grado di pazienti che presentano un grave deficit di α-1-antitripsina presentano una prevalenza più alta rispetto a fumatori che non sono parenti di pazienti che presentano tale deficit genetico (36). Gli studi genetici fino ad ora condotti non hanno tuttavia identificato altri singoli geni chiaramente responsabili dell’insorgenza della BPCO. Sono state descritte associazioni fra la BPCO e diversi polimorfismi genetici, che comprendono l’α-1-antichimotripsina, l’epossido idrolisi microsomiale, la glutatione S-transferasi, l’eme ossigenasi-1 ed il TNF-α (37). I risultati di tali studi sono stati troppo diversi nelle varie popolazioni. Conclusioni In sintesi, la BPCO è una sindrome caratterizzata da una tipica alterazione funzionale respiratoria, la limitazione poco reversibile del flusso massimo espiratorio, associata nella maggior parte dei casi a sintomi respiratori cronici, dispnea tosse ed escreato, e causata nella maggior pare dei casi dal fumo di sigaretta. Nel singolo paziente, la gravità della BPCO va valutata sulla base del quadro funzionale respiratorio e delle manifestazioni cliniche, in particolare i sintomi respiratori, gli aspetti sistemici e le malattie concomitanti. BIBLIOGRAFIA 1. Global Initiative for Chronic Obstructive Lung Disease. Update 1 July 2003. A collaborative project of the National Health L, and Blood Institute, NIH and the World Health Organisation ed. www.goldcopd.com: National Institutes of Health, National Heart Lund and Blood Institute, Bethesda, Md, 2003. 2003. 2. Pauwels RA, Rabe KF. Burden and clinical features of chronic obstructive pulmonary disease (COPD). Lancet 2004; 364:613-20. 3. Fletcher C, Peto R. The natural history of chronic airflow obstruction. Br Med J 1977; 1:1645-8. 4. Viegi G, Pedreschi M, Pistelli F, et al. Prevalence of airways obstruction in a general population: European Respiratory Society vs American Thoracic Society definition. Chest 2000; 117:339S-45S. 5. Standards for the diagnosis and care of patients with chronic obstructive pulmonary disease. American Thoracic Society. Am J Respir Crit Care Med 1995; 152:S77-121. 6. Siafakas NM, Vermeire P, Pride NB, et al. Optimal assessment and management of chronic obstructive pulmonary disease (COPD). The European Respiratory Society Task Force. Eur Respir J 1995; 8:1398-420. 7. Celli BR, MacNee W. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23:932-46. 8. Hersh CP, Dahl M, Ly NP, Berkey CS, Nordestgaard BG, Silverman EK. Chronic obstructive pulmonary disease in alpha1-antitrypsin PI MZ heterozygotes: a meta-analysis. Thorax 2004; 59:843-9. 17 18 9. Calverley PM, Walker P. Chronic obstructive pulmonary disease. Lancet 2003; 362:1053-61. 10. DeMeo DL, Carey VJ, Chapman HA, et al. Familial aggregation of FEF(25-75) and FEF(25-75)/FVC in families with severe, early onset COPD. Thorax 2004; 59:396-400. 11. Lung function testing: selection of reference values and interpretative strategies. American Thoracic Society. Am Rev Respir Dis 1991; 144:1202-18. 12. Fabbri LM, Romagnoli M, Corbetta L, et al. Differences in airway inflammation in patients with fixed airflow obstruction due to asthma or chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2003; 167:418-24. 13. Calverley PM, Burge PS, Spencer S, Anderson JA, Jones PW. Bronchodilator reversibility testing in chronic obstructive pulmonary disease. Thorax 2003; 58:659-64. 14. O'Donnell DE, Fluge T, Gerken F, et al. Effects of tiotropium on lung hyperinflation, dyspnoea and exercise tolerance in COPD. Eur Respir J 2004; 23:832-40. 15. Tashkin D, Kesten S. Long-term treatment benefits with tiotropium in COPD patients with and without short-term bronchodilator responses. Chest 2003; 123:1441-9. 16. Bestall JC, Paul EA, Garrod R, Garnham R, Jones PW, Wedzicha JA. Usefulness of the Medical Research Council (MRC) dyspnoea scale as a measure of disability in patients with chronic obstructive pulmonary disease. Thorax 1999; 54:581-6. 17. Hogg JC, Chu F, Utokaparch S, et al. The nature of small-airway obstruction in chronic obstructive pulmonary disease. N Engl J Med 2004; 350:2645-53. 18. Incalzi RA, Bellia V, Catalano F, et al. Evaluation of health outcomes in elderly patients with asthma and COPD using disease-specific and generic instruments: the Salute Respiratoria nell'Anziano (Sa.R.A.) Study. Chest 2001; 120:734-42. 19. Saetta M, Turato G, Maestrelli P, Mapp CE, Fabbri LM. Cellular and structural bases of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2001; 163:1304-9. 20. Fishman A, Martinez F, Naunheim K, et al. A randomized trial comparing lung-volume-reduction surgery with medical therapy for severe emphysema. N Engl J Med 2003; 348:2059-73. 21. Wouters EF, Creutzberg EC, Schols AM. Systemic effects in COPD. Chest 2002; 121:127S-130S. 22. Sharp DS, Burchfiel CM, Curb JD, Rodriguez BL, Enright PL. The synergy of low lung function and low body mass index predicting allcause mortality among older Japanese-American men. J Am Geriatr Soc 1997; 45:1464-71. 23. Ferrer M, Villasante C, Alonso J, et al. Interpretation of quality of life scores from the St George's Respiratory Questionnaire. Eur Respir J 2002; 19:405-13. 24. Bowen JB, Votto JJ, Thrall RS, et al. Functional status and survival following pulmonary rehabilitation. Chest 2000; 118:697-703. 25. Yohannes AM, Baldwin RC, Connolly MJ. Depression and anxiety in elderly outpatients with chronic obstructive pulmonary disease: prevalence, and validation of the BASDEC screening questionnaire. Int J Geriatr Psychiatry 2000; 15:1090-6. 26. Pena VS, Miravitlles M, Gabriel R, et al. Geographic variations in prevalence and underdiagnosis of COPD: results of the IBERPOC multicentre epidemiological study. Chest 2000; 118:981-9. 27. Anthonisen NR, Connett JE, Murray RP. Smoking and lung function of Lung Health Study participants after 11 years. Am J Respir Crit Care Med 2002; 166:675-9. 28. Coultas DB. Health effects of passive smoking. 8. Passive smoking and risk of adult asthma and COPD: an update. Thorax 1998; 53:3817. 29. Smith KR. Inaugural article: national burden of disease in India from indoor air pollution. Proc Natl Acad Sci U S A 2000; 97:13286-93. 30. Amoli K. Bronchopulmonary disease in Iranian housewives chronically exposed to indoor smoke. Eur Respir J 1998; 11:659-63. 31. Murray CJ, Lopez AD. Global mortality, disability, and the contribution of risk factors: Global Burden of Disease Study. Lancet 1997; 349:1436-42. 32. Balmes J, Becklake M, Blanc P, et al. American Thoracic Society Statement: Occupational contribution to the burden of airway disease. Am J Respir Crit Care Med 2003; 167:787-97. 33. Vogelzang PF, van der Gulden JW, Folgering H, et al. Endotoxin exposure as a major determinant of lung function decline in pig farmers. Am J Respir Crit Care Med 1998; 157:15-8. 34. Eriksson S. Studies in alpha 1-antitrypsin deficiency. Acta Med Scand Suppl 1965; 432:1-85. 35. Stoller JK. Clinical features and natural history of severe alpha 1-antitrypsin deficiency. Roger S. Mitchell Lecture. Chest 1997; 111:123S128S. 36. Silverman EK, Chapman HA, Drazen JM, et al. Genetic epidemiology of severe, early-onset chronic obstructive pulmonary disease. Risk to relatives for airflow obstruction and chronic bronchitis. Am J Respir Crit Care Med 1998; 157:1770-8. 37. Sandford AJ, Silverman EK. Chronic obstructive pulmonary disease. 1: Susceptibility factors for COPD the genotype-environment interaction. Thorax 2002; 57:736-41. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 1. Definizione, classificazione ed eziopatogenesi - F. Luppi, L. M. Fabbri 19 2. Epidemiologia e costi socio-economici A cura di Antonio Scognamiglio (1), Gabriella Matteelli (2), Francesco Pistelli (3), Sandra Baldacci (1), Sara Maio (1), Laura Carrozzi (3) e Giovanni Viegi (1) Unità di Epidemiologia Ambientale Polmonare, Istituto di Fisiologia Clinica CNR, Pisa (2) Centro per la Prevenzione ed il Trattamento dei Danni indotti da Fumo di Tabacco (Centro Antifumo), U.O. Pneumologia, Azienda USL n. 6, Livorno (3) U.O. Pneumologia e Fisiopatologia Respiratoria Universitaria, Dipartimento Cardio-toracico, Azienda Ospedaliera-Universitaria Pisana, Pisa (1) 2. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) rappresenta una delle cause più importanti di mortalità e morbosità nei paesi industrializzati. Secondo l’Organizzazione Mondiale della Sanità (OMS) essa rappresentava, nel 2001, la quinta causa di morte nel mondo (1). In epidemiologia, convergono talora nel termine BPCO entità fenotipiche distinte, in maniera tale che dati di prevalenza e di mortalità concernenti tale malattia sono comprensivi di bronchite cronica, enfisema ed asma in maniera non uniforme. Nonostante la BPCO e l’asma bronchiale siano caratterizzate da un diverso meccanismo fisiopatologico e da un differente pattern cellulare (2), l’asma cronica persistente può evolvere verso una forma irreversibile di ostruzione al flusso delle vie aeree. In tal caso, l’asma deve essere compresa nell’acronimo BPCO e, come tale, è spesso inclusa nel termine di malattia polmonare cronica ostruttiva (3-5). Mortalità Secondo dati forniti dall’OMS, nel 2001, la BPCO era al 5° posto come causa di morte nel mondo con 2.676.000 decessi (1) (tab.1). Sono presenti, a livello mondiale, notevoli differenze nei tassi di mortalità per BPCO tra i vari paesi, in relazione alla diversa distribuzione del tabagismo e degli altri fattori di rischio (4). Differenze rilevanti sono presenti anche a livello europeo, dove 200.000300.000 persone muoiono ogni anno a causa della malattia (6). Sempre secondo l’OMS, nel 1997, la BPCO è stata causa di decesso, in Europa, per il 4,1% dei maschi ed il 2,4% delle femmine (6). In generale, la mortalità per BPCO è stata 2-3 volte più elevata nei maschi rispetto alle femmine, mostrando parallelamente un andamento incrementale nelle fasce di popolazione più anziane. Inoltre, i paesi del nord Europa hanno fatto registrare, nel periodo 1980-1990, un incremento della mortalità per BPCO tra le femmine (6). Tra il 1995 ed il 1999, il fumo ha causato poco meno di 65.000 morti per BPCO ogni anno nella popolazione adulta degli Stati Uniti d’America (7). In Italia, dei 37.782 decessi che si sono realizzati per patologie respiratorie (codici 460-519 ICD IX) nell’anno 2000, circa la metà sono stati causati dalla BPCO (codici 490-496 ICD IX) (8). Tuttavia in molti paesi, al momento della compilazione dei certificati di morte, la patologia respiratoria è notevolmente sottostimata in confronto alle malattie cardiovascolari (4). Per ciò che concerne i fattori correlati con un aumento del rischio di mortalità (o con una minore sopravvivenza) per BPCO, è da sottolineare il ruolo della riduzione del volume espirato forzato nel primo secondo (FEV1) e dell’ipersecrezione cronica di muco (4). Tabella 1 – Le dieci più frequenti cause di morte nel mondo registrate nell’anno 2001 (popolazione totale: 6.122.210.000) [Modificata da voce bibliografica n. 1] CAUSE DI MORTE Malattie ischemiche cardiache NUMERO DI MORTI 7.181.000 Malattie cerebro-vascolari 5.454.000 Infezioni delle basse vie respiratorie 3.871.000 HIV/AIDS 2.866.000 BPCO 2.672.000 Condizioni perinatali 2.504.000 Malattie diarroiche 2.001.000 Tubercolosi 1.644.000 Neoplasie maligne polmonari 1.213.000 Incidenti stradali 1.194.000 21 Morbosità 22 In Europa, il 4-6% della popolazione adulta soffre di BPCO in forma clinicamente rilevante, sebbene i due terzi dei soggetti affetti mostrino alterazioni disventilatorie di lieve entità. La prevalenza cresce in maniera direttamente proporzionale all’età (6). Lo studio multicentrico ECRHS (European Community Respiratory Health Survey), condotto in 16 nazioni in 18.000 soggetti di età compresa tra 20 e 44 anni, ha stimato una prevalenza media di bronchite cronica pari al 2,6% (range: 0,7% - 9,7%) (9). Secondo uno studio condotto dall’Istituto Nazionale di Statistica (ISTAT) nel 2003, su un campione di famiglie italiane, il 6,4% della popolazione ha riferito di essere affetta da bronchite cronica o enfisema o asma (10). Dall’analisi delle schede di dimissione ospedaliera (SDO) del 2002 è emerso che il 18,5% delle dimissioni per patologie respiratorie, cioè 111.453 casi, è stato codificato con il DRG (Diagnosed Related Group) 88 corrispondente alla malattia polmonare cronica ostruttiva. Tali ricoveri hanno comportato un totale di 984.780 giornate di degenza, con una degenza media di 8,8 giorni. Rispetto al triennio 1999-2001, è stata pertanto registrata una riduzione del numero assoluto di ricoveri in acuto (in regime ordinario) per BPCO (11). È probabile che anche i dati provenienti dalle SDO siano sottostimati, in quanto molti ricoveri per BPCO sono comunemente classificati sotto altri DRG. Il carico individuale e sociale della BPCO è destinato ad aumentare nei prossimi decenni, prevalentemente a carico del sesso femminile, principalmente a causa dell’abitudine di fumo dei decenni passati e dell’invecchiamento della popolazione (12). Una problematica rilevante della BPCO è la determinazione della sua reale prevalenza nella popolazione generale, prevalenza che può variare notevolmente in base agli strumenti diagnostici utilizzati: sintomi respiratori riferiti dal paziente, diagnosi medica, presenza di alterazioni della funzione polmonare. Perfino quando la diagnosi di BPCO è basata su un riscontro oggettivo, quale la spirometria, la variabilità all’interno della stessa popolazione può essere ampia in considerazione dei diversi criteri che le principali Società Scientifiche internazionali adottano per definire la presenza di ostruzione bronchiale. Viegi et al. (13) hanno dimostrato, in un campione di popolazione generale adulta, che il tasso di prevalenza dell’ostruzione delle vie aeree varia dall’11%, ottenuto applicando il criterio ERS (European Respiratory Society) (14), al 18% utilizzando il criterio definito “clinico” (criterio successivamente utilizzato per definire il grado 1-4 GOLD (Global Initiative for Chronic Obstructive Pulmonary Disease) (15). È evidentemente necessario individuare un criterio standardizzato, epidemiologicamente valido, che sia accettato da tutte le società che si occupano di medicina respiratoria. Tale obiettivo non è ancora stato raggiunto, anche dopo l’introduzione del criterio GOLD di diagnosi di BPCO, sia per ciò che concerne la capacità di tale criterio di fornire informazioni di valore prognostico nei pazienti, sia per la sua applicabilità all’intera popolazione, a prescindere dall’età (4). Un altro rilevante aspetto epidemiologico è quello della sottodiagnosi della BPCO; nella letteratura scientifica, l’entità di tale sottodiagnosi oscilla tra il 25 ed il 50%, o anche di più, secondo gli studi considerati (4,14). Che la malattia possa essere molto più diffusa di quanto percepito dal senso comune è emerso dalla nostra recente quantizzazione del diagramma di Venn nella popolazione generale italiana (5), la quale ha mostrato che circa il 18% dei soggetti investigati riportava una diagnosi di bronchite cronica o asma o enfisema oppure aveva segni spirometrici di ostruzione bronchiale (fig. 1). La percezione che molti soggetti siano affetti da BPCO senza saperlo, ritardando quindi i tempi dell’intervento terapeutico e permettendo alla patologia di evolvere verso stadi più severi, ha spinto alcuni ricercatori ad ideare studi di diagnosi precoce. Ad esempio, uno screening spirometrico su sogRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 2. Epidemiologia e costi socio-economici - A. Scognamiglio, G. Matteelli, F. Pistelli, S. Baldacci, S. Maio, L. Carrozzi, G. Viegi getti fumatori è stato in grado di identificare soggetti con segni di ostruzione bronchiale. L’aggiunta di un breve intervento di counseling antitabagico è in grado di motivare fortemente i soggetti con ostruzione bronchiale, incrementando parallelamente i tassi di cessazione dell’abitudine di fumo (16). Figura 1 – Distribuzione delle malattie respiratorie ostruttive, con ostruzione bronchiale (a sinistra) e senza ostruzione bronchiale (a destra), nel campione del Delta Padano. [Tradotta da voce bibliografica n.5] Bronchite cronica 0,28% 0,12% Enfisema Bronchite cronica 0,61% 0,24% 0,37% 00,4% % 0,20% 0,28% --- Enfisema --- 0,4% 4% % 1,30% 0,16% 3,25% Ostruzione bronchiale 10,96% Asma Asma Fattori di rischio I fattori di rischio per lo sviluppo di BPCO possono essere suddivisi in due categorie: esogeni ed endogeni. Tali fattori, singolarmente od in sinergia, determinano il grado di suscettibilità del soggetto allo sviluppo della malattia (tab. 2) (4,17,18). Tabella 2 – Tradizionali fattori di rischio per lo sviluppo di BPCO [Modificata da voce bibliografica n. 4] ENDOGENI ESOGENI Sesso Anamnesi familiare positiva per BPCO Predisposizione genetica allo sviluppo di BPCO Deficit di α-1-antitripsina Malattie respiratorie durante l’infanzia Atopia ed iperattività bronchiale Suscettibilità individuale ai fattori di rischio esogeni Fumo di tabacco Esposizione lavorativa Inquinamento ambientale (outdoor e indoor) Esposizione a fumo di tabacco ambientale (ETS) Dieta povera di frutta Abuso di alcool Basso livello socio-economico FATTORI DI RISCHIO ESOGENI Fumo di tabacco Il fumo di tabacco è indubitabilmente il principale fattore di rischio per lo sviluppo della BPCO e per la mortalità ad essa correlata (18,19). Nel 2000, 4,83 milioni di morti nel mondo sono stati attribuiti al fumo di tabacco (12% della mortalità totale registrata nel suddetto anno negli adulti); circa 0,97 milioni di decessi sono stati causati dalla BPCO. Nei paesi industrializzati, la percentuale di mortalità per BPCO attribuibile al fumo è stata pari a 80,5% negli uomini e 61,5% nelle donne (20). In particolare, lo studio prospettico cinquantennale dei medici britannici maschi ha evidenziato come circa due terzi dei fumatori muoiano per cause fumo-correlate e mediamente 10 anni più giovani in confronto ai non fumatori. D’altra parte, la cessazione dell’abitudine di fumo si traduce in una rilevante riduzione del rischio di mortalità (19). È stato, inoltre, dimostrato che i fumatori correnti mostrano un tasso di mortalità per BPCO 12,7 volte maggiore rispetto ai non fumatori. Tale tasso cresce proporzionalmente all’aumentare della media giornaliera di sigarette fumate (4). 23 24 L’età d’inizio dell’abitudine di fumo, la media giornaliera di sigarette fumate, gli anni di fumo trascorsi contribuiscono variamente alla genesi del danno polmonare. È riportato in letteratura che soltanto il 10-20% dei fumatori sviluppa la malattia, tuttavia, recenti indagini epidemiologiche mostrano che segni/sintomi di BPCO sono presenti nel 40-50% dei fumatori (4,18). L’elemento genetico svolge un ruolo rilevante nello sviluppo della malattia; vari studi sembrano indicare l’esistenza di una maggior suscettibilità del sesso femminile ai danni indotti dal fumo di tabacco (21). Nella popolazione americana, Mannino et al. hanno stimato, tra i soggetti maschi, una prevalenza di BPCO del 4,6% nei non fumatori, 7,9% negli ex-fumatori e 11,2% nei fumatori correnti; anche tra le donne è presente lo stesso andamento ed i valori, per le tre categorie, sono 6,8%, 12,1% e 14,7%, rispettivamente (22). In Italia, il 26,2% degli individui adulti (età ≥ di 15 anni) dichiara di essere fumatore (il 30,0% dei maschi ed il 22,5% delle femmine), il 17,9% ex-fumatore (il 24,8% dei maschi e l’11,2% delle femmine), il 55,9% non fumatore (il 45,2% dei maschi ed il 66,3% delle femmine). Rispetto a quanto emerso nel 2003, i fumatori correnti sono diminuiti dal 27,6% al 26,2%, con una riduzione più significativa tra gli uomini a fronte di una sostanziale stabilità fra le donne. Il numero medio di sigarette giornaliere fumate è di 17,1 (19,1 per gli uomini e 13,9 per le donne). Inoltre, gli uomini hanno fatto registrare una riduzione del consumo giornaliero medio di sigarette a fronte di un aumento dello stesso tra le donne (23). In Italia, l’associazione tra fumo e presenza di sintomi respiratori caratteristici della bronchite cronica, quali tosse e catarro cronici, è stata confermata da Viegi et al. (24). Anche la funzione polmonare è influenzata dall’abitudine di fumo. I fumatori presentano, infatti, un accelerato declino del FEV1 rispetto ai non fumatori, secondo una relazione di tipo dose-risposta (18,25). Il trattamento della dipendenza da nicotina è in grado di prevenire o ritardare lo sviluppo di ostruzione bronchiale e, qualora quest’ultima sia già presente, ne ritarda la progressione (26). La cessazione dell’abitudine di fumo è, altresì, in grado di migliorare la sopravvivenza in soggetti affetti da BPCO di grado severo (27). Esposizione professionale L’esposizione professionale cronica ad inquinanti può contribuire allo sviluppo di BPCO, indipendentemente dall’abitudine di fumo. Lavoratori particolarmente esposti a tale rischio appartengono ai settori metallurgico e minerario, edile, agricolo, tessile e chimico, oltre a quello delle cartiere e dell’industria alimentare (4). Soggetti con esposizione lavorativa hanno evidenziato un accelerato declino della funzione polmonare ed un incremento della prevalenza di sintomi e/o malattie respiratori cronici. Il concomitante tabagismo può contribuire, in maniera additiva, all’azione nociva dell’esposizione lavorativa (28) . Recenti articoli di revisione hanno indicato che il rischio attribuibile di popolazione (PAR), dovuto all’esposizione occupazionale, è circa il 15% per la bronchite cronica e il 18% per la presenza di alterazioni della funzione polmonare compatibili con un quadro di BPCO (28). Inquinamento outdoor Nel tempo, le malattie respiratorie e la mortalità ad esse correlata sono state associate, con sempre maggiore evidenza, alla presenza di inquinanti atmosferici (29,30). Inquinanti outdoor convenzionali sono il cosiddetto “fumo nero” (particolato prodotto dalla combustione di sostanze fossili), l’anidride solforosa (SO2), gli ossidi di azoto (NOx) (prodotti dal traffico auto-veicolare e da processi di combustione), e l’ozono (O3) (derivato da reazioni fotochimiche correlate al traffico delle città) (29). L’esposizione cronica ad elevati livelli d’inquinamento atmosferico è apparsa correlata alla pre- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 2. Epidemiologia e costi socio-economici - A. Scognamiglio, G. Matteelli, F. Pistelli, S. Baldacci, S. Maio, L. Carrozzi, G. Viegi senza di bronchite cronica e ad alterazioni della funzione polmonare (29,30). Negli ultimi anni, particolare interesse ha destato nella comunità scientifica lo studio degli effetti di particelle fini con diametro aerodinamico inferiore a 10 µm (PM10) o 2,5 µm (PM2.5), in relazione alla mortalità per cause cardiorespiratorie (29). Un recente studio epidemiologico ha mostrato che ogni incremento di 10 µg/m3 di particelle fini è associato a circa il 6% di aumento del rischio di mortalità per cause cardiorespiratorie (4). Anche l’esposizione a breve termine ad elevati livelli di inquinamento ambientale è stata significativamente correlata ad un incremento delle ammissioni ospedaliere e delle visite urgenti, oltre che della mortalità, per patologie respiratorie (4). Inquinamento indoor Gli ambienti indoor comprendono luoghi di vita e di lavoro quali abitazioni, uffici, strutture comunitarie, locali destinati ad attività ricreative e sociali, mezzi di trasporto pubblici (4). Nei paesi industrializzati, le persone trascorrono la maggior parte del loro tempo in ambienti confinati e sono pertanto esposte, con continuità, agli effetti dannosi degli inquinanti interni. In aggiunta, le concentrazioni della maggior parte degli inquinanti indoor sono generalmente maggiori di quelle outdoor per gli stessi inquinanti (31). Gli inquinanti indoor connessi con il rischio di sviluppare BPCO sono il fumo di tabacco ambientale (ETS), il particolato respirabile sospeso nell’aria ambiente (PM), e la combustione di biomasse, fenomeno tipico dei paesi in via di sviluppo (31). Vari studi hanno dimostrato, nei bambini, una significativa associazione tra esposizione ad ETS ed una riduzione del fisiologico tasso di incremento del FEV1. La conseguente insufficiente maturazione dell’apparato respiratorio durante l’infanzia può condurre allo sviluppo di BPCO nell’età adulta (4). Nella popolazione adulta, studi europei hanno evidenziato una associazione significativa tra sintomi di bronchite cronica e/o diagnosi di BPCO ed esposizione ad ETS (31). Incrementi delle concentrazioni di PM, prodotto essenzialmente dal fumo di tabacco e da processi di combustione, sono stati correlati con un aumento dell’incidenza di sintomi respiratori ed alterazioni della funzione polmonare, sia nei bambini sia negli adulti (18). Stato socio-economico Questo termine comprende una serie di indicatori come il livello d’istruzione, la posizione lavorativa ed il relativo reddito, le condizioni abitative della casa. Vari studi epidemiologici hanno evidenziato una correlazione tra l’appartenenza ad un basso livello socio-economico ed un aumento del rischio di sviluppare BPCO (4). Abitudini dietetiche Il ruolo delle abitudini dietetiche come fattore di rischio per lo sviluppo della malattia è oggi oggetto di numerosi studi (4). In generale, le sostanze ad azione antiossidante sembrano in grado di esercitare un’azione preventiva, modulando, parallelamente, la fisiologica riduzione della funzione polmonare legata all’aumento dell’età (4). Vari studi epidemiologici hanno evidenziato come il consumo regolare di frutta e verdura sia correlato ad una riduzione del rischio di sviluppare BPCO (4,18). Flavonoidi, micronutrienti come il magnesio ed il selenio, gli acidi grassi omega-3, e l’assunzione di moderate quantità di alcool, sono tuttora studiati per una loro possibile azione protettiva sull’apparato respiratorio. L’abuso d’alcool è stato invece associato a prevalenze più elevate di BPCO e, più in generale, ad un accelerato declino della funzione polmonare (4,18). 25 FATTORI DI RISCHIO ENDOGENI Fattori genetici È nota da tempo una trasmissione genetica di tipo mendeliano, determinante il deficit di un inibitore delle proteasi seriche (l’α-1-antitripsina), associato ad un aumentato rischio di sviluppare, in età giovanile, enfisema polmonare di tipo panacinare nei soggetti caratterizzati da un pattern genetico a carattere recessivo (ZZ), e la cui espressione fenotipica è influenzata dall’abitudine al fumo di sigaretta (17). Anche la sola condizione di eterozigosi per l’allele Z è ritenuta fattore di rischio per lo sviluppo di BPCO (4). Altri fattori genetici da menzionare sono: polimorfismi o mutazioni geniche dell’α-1-antichimotripsina, proteina inibitrice delle proteasi; una ridotta azione detossificante sul fumo di tabacco, da parte dell’epossido idrolasi microsomiale e del glutatione S-transferasi; un’insufficiente attività antiossidante del fattore eme ossigenasi-1 (17). I gruppi sanguigni (sistema AB0, secretore ABH, di Lewis), la proteina di legame con la vitamina D, l’antigene d’istocompatibilità HLA e l’α-TNF (Tumour Necrosis Factor) sono attualmente oggetto di studio (4). È importante sottolineare che una complessa interazione gene-ambiente presiede alla piena espressione delle caratteristiche fenotipiche dei soggetti (32). 26 BPCO e genere In molte parti del mondo i tassi di prevalenza della BPCO sono più elevati tra gli uomini rispetto alle donne: ciò è solitamente attribuito a ridotte prevalenze di tabagismo ed a ridotta esposizione lavorativa a sostanze nocive in queste ultime. In realtà, il recente aumento della prevalenza dell’abitudine di fumo tra le donne ha fatto registrare un concomitante aumento della prevalenza di BPCO nello stesso sesso, come riportato, ad esempio, negli USA (21,22). Malattie respiratorie durante l’infanzia Numerosi studi epidemiologici hanno evidenziato il ruolo delle malattie respiratorie avvenute durante l’infanzia, come fattore indipendente di rischio per lo sviluppo di BPCO. La permanente condizione di flogosi dell’epitelio respiratorio, determinata da agenti virali o batterici, può esitare in un’alterata maturazione dell’apparato respiratorio nel corso dell’infanzia, e, nell’età adulta, in una maggiore vulnerabilità all’azione nociva di altri agenti patogeni come il fumo di sigaretta (4). Storia familiare Alterazioni della funzione polmonare sono state associate ad anamnesi familiare positiva per BPCO (18, 33). Questa “aggregazione familiare” per BPCO, talora indipendente dall’abitudine al fumo di sigaretta, può sottendere una predisposizione genetica per lo sviluppo della malattia, che necessità tuttora ulteriori approfondimenti (4,17). Costi della BPCO I costi diretti includono le spese per ricoveri ospedalieri, visite ambulatoriali ed assistenza domiciliare, oltre che per la terapia farmacologica. I costi indiretti sono essenzialmente costituiti dagli effetti disabilitanti della malattia, causa della perdita di giorni lavorativi. Negli USA, è stato stimato nell’anno 2000, un costo complessivo dovuto alla BPCO di circa 30,4 miliardi di dollari americani, dei quali 14,7 addebitabili a costi diretti e 15,7 a costi indiretti (18). Nella Comunità Europea (che include i 15 paesi membri fino all’aprile 2004, più Norvegia e Svizzera), il costo annuale totale addebitabile alla BPCO è di circa 38,8 miliardi di euro, dei quali 10,3 miliardi dovuti a costi diretti e 28,5 miliardi attribuibili a costi indiretti (6). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 2. Epidemiologia e costi socio-economici - A. Scognamiglio, G. Matteelli, F. Pistelli, S. Baldacci, S. Maio, L. Carrozzi, G. Viegi Nell’ambito dello studio “Confronting COPD in North America and Europe”, è stata recentemente stimata in Italia, a causa della BPCO, una spesa media annuale di 7 1.308,54 per paziente. Il trattamento di pazienti affetti da BPCO severa è stato assai più costoso (7 6.366) di quello di pazienti con BPCO di grado lieve (7 441) (4). L’onere della BPCO per le società sviluppate, sia per l’impatto economico sia per l’utilizzazione delle risorse, appare pertanto rilevante e destinato ad incrementarsi nei prossimi decenni (4). Conclusioni La BPCO rappresenta una delle cause più importanti di mortalità e morbosità nei paesi industrializzati. I fattori di rischio per lo sviluppo di tale patologia intersecano variamente le loro azioni. La BPCO è una patologia sotto-diagnosticata e, spesso, trattata solo nelle fasi avanzate, ed appare un rilevante problema perfino tra giovani adulti. L’elevata prevalenza di fumatori al di sotto dei 45 anni di età, registrata a livello mondiale, sottolinea la necessità di migliorare la qualità degli iter preventivi, presupponendo un accresciuto impegno degli specialisti di sanità pubblica e di pneumologia unito a quello dei medici di Medicina generale. In tal senso, l’attuazione della legge concernente la tutela della salute dei non fumatori (Art. 51, comma 2, 16 gennaio 2003, n.3, come modificato dall’art. 7/21 ottobre 2003, n.306), costituisce un ulteriore presupposto per un sistematico approccio diagnostico-terapeutico di fronte al soggetto fumatore. BIBLIOGRAFIA 1. WHO. World Health Report 2002. Sito web: www.who.int/whr/2002 (Ultimo accesso in data 06.12.2004). 2. Fabbri LM, Romagnoli M, Corbetta L, Casoni G, Busljetic K, Turato G, Ligabue G, Ciaccia A, Saetta M, Papi A. Differences in airway inflammation in patients with fixed airflow obstruction due to asthma or chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2003; 167: 418-424. 3. ATS. Standards for the diagnosis and care of patients with chronic obstructive pulmonary disease. American Thoracic Society. Am J Respir Crit Care Med 1995; 152: 77S-121S. 4. Scognamiglio A, Matteelli G, Baldacci S, Pistelli F, Carrozzi L, Viegi G. L’epidemiologia della broncopneumopatia cronica ostruttiva. Ann Ist Super Sanità 2003; 39: 467-484. 5. Viegi G, Matteelli G, Angino A, Scognamiglio A, Baldacci S, Soriano JB, Carrozzi L. The proportional Venn diagram of obstructive lung disease in the Italian general population. Chest 2004; 126: 1093-1101. 6. European Respiratory Society (ERS). Chronic Obstructive Pulmonary Disease. In “European lung white book – The first comprehensive survey on respiratory health in Europe”. Loddenkemper R, Gibson GJ, SibilleY eds. ERSJ 2003: 34-43. 7. CDC. Annual smoking-attributable mortality, years of potential life lost, and economic costs-United States, 1995-1999. MMWR 2002; 51: 300-303. 8. ISTAT. Cause di morte – anno 2000. Sito web: http://www.istat.it/Popolazion/Nati-e-mor/Storico/index.htm (Ultimo accesso in data 06.12.2004). 9. Cerveri I, Accordini S, Verlato G, Corsico A, Zoia MC, Casali L, Burney P, de Marco R. European Community Respiratory Health Survey (ECRHS) Study Group. Variations in the prevalence across countries of chronic bronchitis and smoking habits in young adults. Eur Respir J 2001; 18: 85-92. 10. ISTAT. Annuario Statistico Italiano 2004. Disponibile sul sito web: http://catalogo.istat.it/asi2004/ (Ultimo accesso in data 06.12.2004). 11. Dati del Ministero della Salute. Ricoveri Ospedalieri – Anno 2002. Sito internet: http://www.ministerosalute.it/programmazione/sdo/sezApprofondimenti.jsp?label=osp. 12. Feenstra TL, van Genugten ML, Hoogenveen RT, Wouters EF, Rutten-van Molken MP. The impact of aging and smoking on the future burden of chronic obstructive pulmonary disease: a model analysis in the Netherlands. Am J Respir Crit Care Med 2001;164: 590-596. 13. Viegi G, Pedreschi M, Pistelli F, Di Pede F, Baldacci S, Carrozzi L, Giuntini C. Prevalence of airway obstruction in a general population sample. European Respiratory Society vs American Thoracic Society definition. Chest 2000; 117: 339s-345s. 14. Siafakas NM, Vermeire P, Pride NB, Paoletti P, Gibson J, Howard P, Yernault JC, Decramer M, Higenbottam T, Postma DS on behalf of the European Respiratory Society Task Force. Optimal assessment and management of chronic obstructive pulmonary disease (COPD). Eur Respir J 1995; 8: 1398-1420. 15. Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Pulmonary Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 2001; 163: 1256-1276. 16. Gorecka D, Bednarek M, Nowinski A, Puscinska E, Goljan-Geremek A, Zielinski J. Diagnosis of airflow limitation combined with smoking cessation advice increases stop-smoking rate. Chest 2003; 123: 1916-1923. 17. Luisetti M, Medaglia S, Tamburnotti C, Zorzetto M. Predisposizione genetica alle BPCO. In “Il volto della BPCO che cambia”, vol. n. 1, Giuntini C, Grassi G eds UTET 2001: pp 69-80. 27 18. Viegi G, Scognamiglio A, Baldacci S, Pistelli F, Carrozzi L. Epidemiology of chronic obstructive pulmonary disease (COPD). Respiration 2001; 68: 4-19. 19. Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to smoking: 50 years' observations on male British doctors. BMJ 2004; 328 (7455): 1519 (doi: 10.1136/bmj.38142.554479.AE. Published 22 June 2004). 20. Ezzati M, Lopez AD. Estimates of global mortality attributable to smoking in 2000. Lancet 2003; 362: 847-852. 21. Watson L, Boezen HM, Postma DS. Differences between males and females in the natural history of asthma and COPD. In “Respiratory diseases in women”. Buist S, Mapp CE eds. Eur Respir Mon 2003; 8(monograph 25): 50-73. 22. Mannino DM, Gagnon RC, Petty TL, Lydick E. Obstructive lung disease and low lung function in adults in the United States: Data from the National Health and Nutrition Examination survey, 1988-1994. Arch Intern Med 2000; 160: 1683-1689. 23. Doxa. Indagine sul fumo in Italia – 2004. Sito web: http://www.doxa.it/italiano/home.asp (Ultimo accesso in data 06.12.2004). 24. Viegi G, Pedreschi M, Baldacci S, Chiaffi L, Pistelli F, Modena P, Vellutini M, Di Pede F, Carrozzi L. Prevalence rates of respiratory symptoms and diseases in general population samples of North and Central Italy. Int J Tuberc Lung Dis 1999; 3: 1034-1042. 25. US Surgeon General. The health consequences of smoking: a report of the Surgeon General, 2004. Sito web: http://www.cdc.gov/tobacco/sgr/index.htm (Ultimo accesso in data 06.12.2004). 26. Willemse BW, Postma DS, Timens W, ten Hacken NH. The impact of smoking cessation on respiratory symptoms, lung function, airway hyperresponsiveness and inflammation. Eur Respir J 2004; 23: 464-476. 27. Hersh CP, DeMeo DL, Al-Ansari E, Carey VJ, Reilly JJ, Ginns LC, Silverman EK. Predictors of survival in severe, early onset COPD. Chest 2004; 126: 1443-1451. 28. Balmes J, Becklake M, Blanc P, Henneberger P, Kreiss K, Mapp C, Milton D, Schwartz D, Toren K, Viegi G. American Thoracic Society Statement. Occupational contribution to the burden of the airway disease. Am J Respir Crit Care Med 2003; 167: 787-797. 29. Viegi G, Baldacci S. Epidemiological studies of chronic respiratory conditions in relation to urban air pollution in adults. In:” The impact of air pollution on respiratory health”. D’Amato G, Holgate ST eds. Eur Respir Mon 2002; 7(monograph 21): 1-16. 30. Brunekreef B, Holgate ST. Air pollution and health. Lancet 2002; 360: 1233-1242. 31. Viegi G, Simoni M, Scognamiglio A, Baldacci S, Pistelli F, Carrozzi L, Annesi-Maesano I. Indoor air pollution and airway disease. Int J Tuberc Lung Dis 2004; 8: 1401-1415. 32. Silverman EK. Genetic epidemiology of COPD. Chest 2002; 121: 1s-6s. 33. Nihlen U, Nyberg P, Montnemery P, Lofdahl CG. Influence of family history and smoking habits on the incidence of self-reported physician’s diagnosis of COPD. Respir Med 2004; 98: 263-270. 28 Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 2. Epidemiologia e costi socio-economici - A. Scognamiglio, G. Matteelli, F. Pistelli, S. Baldacci, S. Maio, L. Carrozzi, G. Viegi 29 3. BPCO: dimensione sociale A cura di Mariadelaide Franchi Presidente Associazione Italiana Pazienti BPCO 3. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO), che provoca nel nostro Paese 18.000 morti l’anno e, secondo l’OMS, entro il 2020 potrebbe diventare la terza causa di morte, è una malattia ancora poco “visibile”. Da una recente indagine Eurisko solo il 21% della popolazione italiana ne ha sentito parlare (1). In Europa la percentuale delle persone con BPCO non diagnosticate raggiunge l’allarmante livello del 75% (2). Le previsioni per un prossimo futuro sono per un graduale incremento della prevalenza e della mortalità legato principalmente ai seguenti fattori: - persistenza all'abitudine al fumo, in particolare per la popolazione femminile: la prevalenza della BPCO nelle donne entro 15 anni è destinata ad aumentare del 130%; - innalzamento dell'età media della popolazione; - incremento del rischio d’inquinamento ambientale. Grazie al Progetto Mondiale BPCO (3) negli ultimi cinque anni sono stati compiuti progressi importanti per la sistematizzazione delle informazioni basate sulle evidenze scientifiche necessarie a migliorare la diagnosi, il trattamento, l’educazione, la riabilitazione e la continuità dell’assistenza. Le principali questioni aperte sono: 1. Traduzione nella realtà delle acquisizioni scientifiche; 2. Riconoscimento del rilievo sanitario sociale delle malattie croniche respiratorie - tra le quali la BPCO ha un peso molto rilevante in termini di morbilità, mortalità e costi socio-economici nell’ambito della politica sanitaria e sociale (Piano Sanitario Nazionale e Piani Sanitari delle Regioni); 3. Inserimento delle malattie respiratorie croniche nel piano di prevenzione attiva del CCM-Centro Nazionale per la prevenzione ed il controllo delle malattie del Ministero della Salute, allo scopo di attivare a livello regionale gli interventi e le iniziative di screening e di diagnosi precoce, indispensabili per contrastare l’aumento della prevalenza e della mortalità di queste malattie; 4. L’introduzione della BPCO nel D.M. 329/99 concernente l’elenco delle malattie croniche e invalidanti. Questa richiesta è stata attentamente studiata dalla Direzione Generale della Programmazione che ha sottoposto una proposta favorevole alla Commissione per la definizione e l’aggiornamento dei Livelli Essenziali di Assistenza (LEA) per una decisione finale in merito. Questo capitolo ha lo scopo di fare il punto sugli aspetti sociali della malattia, della tutela assistenziale ai malati e alle famiglie, della strada fatta e di quella ancora da fare per questa patologia respiratoria, tra le più diffuse e al tempo stesso tra le meno conosciute. BPCO: importanza e problematica sociale Nonostante i progressi compiuti nel corso degli ultimi anni, in termini di conoscenze scientifiche relative al trattamento e alla gestione, la BPCO è ancora oggi una malattia molto sottovalutata dal medico, dal paziente stesso, dall’opinione pubblica e dalle Istituzioni. Si tratta di una condizione cronica con un decorso clinico in genere progressivo, irreversibile ed invalidante che costituisce fonte di sofferenze e di disagi per il paziente e la sua famiglia. Secondo i dati forniti dall’ISTAT rappresenta in Italia, insieme all’asma, la quarta causa di malattia cronica (6,3% della popolazione totale nel 2001) (4), dopo l’artrite/artrosi, l’ipertensione e le allergie. La metodologia seguita attraverso questa rilevazione ne sottovaluta tuttavia la prevalenza, che in base a varie fonti, tra cui ricordiamo la recente indagine EURISCO (1), può essere 31 valutata in circa 4 milioni di persone. Nelle forme più avanzate può incidere pesantemente nello svolgimento delle normali attività quotidiane e presentare elevati costi socio-economici, soprattutto in presenza di frequenti riacutizzazioni, con conseguenti e ripetuti ricoveri ospedalieri o ricorsi alla medicina d’urgenza. La BPCO provoca nel nostro paese circa 18.000 decessi l'anno, pari al 47% dei decessi per malattie respiratorie (5). La riduzione degli anni di vita e della sopravvivenza non sono percepite correttamente e riconosciute nella loro dimensione reale né dai pazienti né dalle Istituzioni. Questa è infatti l'unica malattia per cui sia stata registrata una riduzione della aspettativa di vita: se i decessi per coronaropatie sono infatti diminuiti del 59%, per infarto del 64% e per altre malattie cardiovascolari del 35%, le morti per BPCO sono aumentate del 163% (6). 32 Impatto socio-psicologico e qualità di vita I problemi respiratori dovuti alla BPCO causano limiti significativi in molti campi della normale vita quotidiana. La prima indagine condotta allo scopo di misurare l’impatto della BPCO è stata svolta nel periodo 2000-2001 su un campione di 3.265 pazienti negli Stati Uniti, in Canada e in sei paesi europei (Francia, Germania, Italia, Olanda, Spagna e Regno Unito). L’indagine, denominata “Confronting COPD in North America and Europe” (7) ha fornito dati sui disagi vissuti dal paziente e sui limiti allo svolgimento delle normali attività quotidiane con conseguente scarsa qualità di vita, nonché sull’impatto dovuto agli elevati costi socio-economici. I risultati più significativi sono i seguenti: - la BPCO non è solo una malattia “dei vecchi” ma colpisce un gran numero di persone al di sotto di 65 anni (in Italia, 1 intervistato su 4 appartiene alla classe di età 45-54 anni); - le difficoltà respiratorie causano limiti significativi in molti campi della normale vita quotidiana. In funzione del livello di gravità la mancanza di respiro interferisce con i più semplici gesti giornalieri, come vestirsi, lavarsi, parlare, ecc., può causare disturbi del sonno e può indurre un progressivo stato di invalidità; - una caratteristica costante in tutti i paesi è rappresentata da frequenti ricorsi al medico curante e al Pronto Soccorso, da ricoveri ospedalieri per le riacutizzazioni e da giornate perse dal lavoro, con conseguenti elevati costi socio-economici che gravano sul paziente, sulle famiglie e sulla società nel suo insieme; - medici e pazienti sono d’accordo sul fatto che negli ultimi anni sono disponibili migliori possibilità di trattamento della BPCO. I pazienti tuttavia sottostimano i propri sintomi e il livello di gravità, mentre sovrastimano il grado di controllo della malattia, e ciò indica quanto sia in generale inadeguata la gestione di questa patologia, con gravi conseguenze soprattutto sulla qualità di vita; - molti malati percepiscono negativamente l’atteggiamento del medico che, a causa della ormai ben dimostrata correlazione con il fumo, tende a considerare il paziente stesso primo responsabile dell’induzione della malattia. Anche questo fatto può incidere sulle possibilità di controllo ottimale; - in generale gli intervistati sono molto soddisfatti dell’aiuto ricevuto dal loro medico per la gestione ed il trattamento (50%). Questa percentuale è tuttavia più bassa in Italia rispetto agli altri paesi (27%). In tutti i paesi, sia i pazienti sia i medici sono d’accordo sul fatto che occorre una maggiore educazione sulla BPCO e sul modo di gestirla e tenerla sotto controllo. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO: dimensione sociale - M. Franchi L’indagine identifica numerose barriere per una adeguata gestione della malattia e per il suo controllo ottimale, barriere che si situano a livello della diagnosi, del trattamento, del rapporto medico-paziente, dell’informazione e dell’educazione. La BPCO porta ad una sostanziale invalidità e perdita di produttività che influisce in modo rilevante sulla qualità di vita del paziente con un consistente impatto economico legato al costo dei trattamenti prolungati nel tempo ed alle ripetute ospedalizzazioni. Secondo il progetto IQOLA (International Quality of Life Assessment) (8) le persone affette da BPCO dichiarano una qualità di vita peggiore sia rispetto alla norma sia rispetto ai soggetti coetanei di riferimento. Il limite più importante posto dalla malattia riguarda l’esercizio fisico, che influisce sulle normali attività quotidiane lavorative o di svago, sui rapporti sociali e familiari, ecc. Aspettative dei pazienti Le richieste più frequenti espresse dai pazienti e dai familiari nei contatti con l’Associazione Italiana Pazienti BPCO sono: - dove curarsi: quali sono i Centri di eccellenza e gli specialisti ai quali rivolgersi; - come verificare la validità del trattamento seguito e sapere se ci sono nuove cure; - come e dove effettuare la riabilitazione respiratoria; - cosa fare per ottenere l’invalidità, l’assegno di accompagnamento, ecc.; - come ricevere assistenza domiciliare; - come ricevere un supporto psicologico; - come ricevere assistenza giuridica. Queste esigenze sono confermate dall’analisi di più di 3.000 domande presentate tra il novembre 2003 e il novembre 2004 al Telefono Verde 800 585558 che la Fondazione Italiana PneumologiaUIP mette a disposizione dei cittadini. Quasi il 40% delle telefonate è effettuato da familiari e tra i malati solo il 50% sa di essere affetto da BPCO. Politica Sanitaria Nazionale e Piani Regionali Le malattie respiratorie croniche ricevono scarsa attenzione dalle Istituzioni nell’ambito della politica sanitaria del nostro paese. Piano Sanitario Nazionale Il Piano Sanitario nazionale 2003-2005 (9) riconosce il rilievo sociale e l’impatto delle malattie respiratorie e sottolinea la necessità di contrastarne l’aumento di prevalenza e di mortalità attraverso una migliore conoscenza delle cause e dei fattori di rischio e la promozione di campagne di educazione e formazione per il personale sanitario, i pazienti e le loro famiglie. Il PSN fornisce le direttive da seguire per il monitoraggio epidemiologico, la definizione dei percorsi diagnostici, il trattamento, l’assistenza, la prevenzione, l’informazione e la formazione. Si tratta tuttavia di indicazioni di massima che non sono accompagnate da misure programmatiche concrete né dai finanziamenti necessari per la loro realizzazione. Piano Nazionale di Prevenzione Attiva (2004-2006) Il Centro Nazionale per la prevenzione e il Controllo delle Malattie, CCM, è stato istituito presso il Ministero della Salute con la Legge 138 del 2004, “Interventi urgenti per fronteggiare situazioni di pericolo per la salute pubblica”. Il Centro provvede inoltre al coordinamento con le Regioni del Piano di Prevenzione Attiva istitui- 33 to per contrastare il rischio cardiovascolare, le complicanze del diabete, i tumori prevenibili da screening e malattie infettive prevenibili da vaccinazione (10). Le malattie respiratorie croniche dovrebbero far parte delle aree di intervento del Piano di Prevenzione Attiva del CCM, allo scopo di attivare a livello regionale gli interventi e le iniziative di screening e di diagnosi precoce, indispensabili per ridurre l’aumento della prevalenza e della mortalità di queste malattie. 34 Piani Sanitari Regionali La lista dei Piani Sanitari Regionali, è riportata alla fine di questo capitolo. L’analisi di questi documenti mostra in modo molto evidente la scarsa armonizzazione dei contenuti, della metodologia seguita, degli obiettivi e delle azioni concrete previste per la riduzione della prevalenza e della mortalità delle malattie croniche respiratorie, nonché degli interventi per la prevenzione dei fattori di rischio e per la diagnosi precoce. I Piani Regionali mettono inoltre in evidenza la carenza di corrette informazioni statistiche ed epidemiologiche, nonché di indicatori sociali e sanitari standardizzati necessari per l’attuazione di una strategia di interventi e di monitoraggio. Alcuni piani sono elaborati in modo molto tecnico e forniscono un quadro di riferimento completo, ma la loro attuazione pratica avviene solo dove sono presenti Aziende capaci di tradurre nella realtà le soluzioni suggerite dagli specialisti. Il fumo e l’inquinamento ambientale sono spesso i principali “appigli” per interventi in favore dei malati respiratori e dispiace costatare che queste politiche siano dettate allo scopo di prevenire le malattie cardiovascolari e i tumori, senza chiari riferimenti alla prevenzione delle malattie respiratorie croniche. Priorità delle Associazioni dei Pazienti L’EFA, la Federazione Europea delle Associazioni dei Pazienti con Malattie Allergiche e Respiratorie (European Federation of Allergy and Airways Diseases Patients Associations), alla quale hanno aderito Federasma, l’Associazione Italiana Pazienti BPCO e l’ALIR-Associazione per la Lotta contro l’Insufficienza Respiratoria, ha definito le priorità attraverso il Manifesto Europeo BPCO (11). Con questa dichiarazione politica per la prima volta le Associazioni europee dei pazienti hanno rivolto un appello al mondo scientifico e alle Istituzioni affinché portino una maggiore attenzione alle condizioni di salute e alla tutela dei pazienti con BPCO, garantendo in primo luogo per tutti la parità d’accesso alla diagnosi, al trattamento, all’informazione, all’educazione e alla prevenzione. Obiettivo prioritario è consentire al paziente una migliore sopravvivenza e qualità di vita riducendo il numero delle riacutizzazioni e la loro gravità. Le riacutizzazioni della BPCO rappresentano infatti la principale causa di morbilità e mortalità. Il Manifesto Europeo BPCO è una sfida a riconoscere la dimensione sociale e l’impatto economico di questa malattia e ad assicurare una più adeguata tutela dei pazienti e delle famiglie. Il documento definisce una vera e propria strategia di interventi articolati per ognuno dei momenti cruciali necessari al miglioramento delle condizioni di salute e della qualità di vita del paziente: - riduzione dei fattori di rischio; - migliore approccio diagnostico nella fase precoce della malattia; - definizione dei programmi di educazione e di formazione; - maggiori investimenti economici e sociali per l’integrazione e la continuità del percorso terapeutico, educativo e assistenziale; - miglioramento della tutela e della continuità dell’assistenza sanitaria, sociale e psicologica. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO dimensione sociale - M. Franchi Il punto di riferimento per le Associazioni dei Pazienti sono le Linee Guida internazionali GOLD (3), adattate alla situazione italiana ed aggiornate dalle Società Scientifiche operanti nell’area della pneumologia. La loro applicazione è indispensabile per garantire un percorso ottimale per la diagnosi, il trattamento, l’educazione, la riabilitazione e la continuità dell’assistenza dei pazienti. Diagnosi Il dato più allarmante di cui si dispone in Europa è che solo il 25% delle persone affette da BPCO è in realtà diagnosticato. L’intervento assolutamente prioritario è quindi quello di individuare sia le persone ad alto rischio sia i malati che non sanno di esserlo e che sfuggono ad ogni controllo medico. Nonostante le Linee Guida internazionali raccomandino la spirometria come esame essenziale per la conferma dell’ostruzione bronchiale, e quindi della diagnosi, numerose indagini svolte a livello internazionale e nazionale hanno evidenziato che una larga percentuale di pazienti non ha mai effettuato questo esame nella sua vita. In particolare, secondo l’indagine Confronting COPD in North America and Europe (7) il 45% delle persone con BPCO ha dichiarato di non aver mai effettuato una spirometria. Campagne di informazione, di sensibilizzazione e di screening dovrebbero figurare negli interventi sanitari regionali al fine di migliorare l’accesso alla diagnosi promuovendo la spirometria in tutte le persone a rischio, in particolare incrementandone l'uso da parte del medico di Medicina generale. La diagnosi tempestiva e corretta consente al medico di intervenire in una fase precoce della malattia e, nella maggior parte dei casi, di rallentarne la progressione. Trattamento Medici e pazienti sono d’accordo sul fatto che negli ultimi anni sono disponibili migliori possibilità di trattamento delle malattie respiratorie croniche ostruttive. Attualmente dalla BPCO non si può guarire, tuttavia i trattamenti a disposizione permettono al paziente di avere una migliore sopravvivenza e qualità di vita, specialmente se la diagnosi è tempestiva. Ciononostante, frequenti ricorsi alla medicina d’urgenza e ripetuti ricoveri ospedalieri indicano un trattamento inadeguato. La causa principale è che i pazienti hanno difficoltà ad aderire con costanza alle prescrizioni e raccomandazioni del medico, per tutta una serie di motivi, ma anche perché non sono sufficientemente “educati” e non hanno un rapporto regolare e periodico soddisfacente con il loro medico. Educazione del paziente e della famiglia Interventi educazionali mirati ad aumentare l’aderenza (compliance) del malato alle prescrizioni e raccomandazioni del medico curante possono migliorare la qualità di vita e ridurre il rischio di ripetuti ricoveri ospedalieri. L’indagine “Confronting COPD in North America and Europe” indica che: - solo il 61% dei pazienti aderisce con regolarità; - solo il 67% dichiara di aver ricevuto istruzioni dal medico su come usare l’inalatore; - il paziente sottovaluta i sintomi e la gravità della malattia, ma ne sopravvaluta il controllo. Risulta così confermato che i pazienti tendono a non seguire con continuità e regolarità le terapie a lungo termine. I medici hanno un ruolo determinante in questo processo e devono cercare di dialogare di più con i pazienti, per aiutarli a prendere coscienza della propria condizione, a gestire la malattia e a va- 35 lutare le reali possibilità di controllarla, con la consapevolezza dell’importanza e del significato del trattamento, dei suoi rischi e dei suoi vantaggi. La condizione indispensabile affinché le attese dei pazienti siano realizzate è che l’educazione faccia parte integrante del trattamento e della gestione della BPCO e che l’impegno dei medici e del personale sanitario operante in questa area sia riconosciuto adeguatamente. I pazienti non solo devono comprendere la loro malattia e ricevere piani di auto-gestione personalizzati, ma devono conoscere le caratteristiche dei farmaci ed essere addestrati ad usare correttamente i dispositivi inalatori. In tal modo può essere potenziata l’aderenza alla terapia e possono essere prevenute le crisi e le riacutizzazioni. L’ostacolo principale sembra essere quello del tempo, dato che l’educazione non rientra nella durata delle normali visite mediche, e del costo della formazione. Problemi questi che devono trovare adeguate risposte nell’ambito della politica sanitaria, ed in particolare nella definizione dei Livelli Essenziali di Assistenza (LEA). Formazione del personale sanitario I programmi di formazione devono comprendere la divulgazione ed implementazione delle Linee Guida GOLD per la diagnosi ed il trattamento della BPCO (Progetto Mondiale BPCO, www.goldcopd.it) attraverso corsi specifici per il personale sanitario, per i medici di Medicina generale, i medici del Pronto Soccorso ed altri operatori, tra cui gli infermieri, i tecnici di funzionalità respiratoria e i terapisti della riabilitazione. 36 Riabilitazione respiratoria e continuità dell’assistenza È ormai acquisito il fatto che la riabilitazione ha un ruolo estremamente importante nel trattamento della BPCO. Le Linee Guida GOLD (3) evidenziano che, pur sulla scorta di un numero limitato di studi, la durata dei programmi di riabilitazione dovrebbe svolgersi su un periodo di due mesi. Tuttavia, maggiore è la durata, migliori e più efficaci risultano i benefici per il paziente. Infine, è stato dimostrato che l’assistenza infermieristica domiciliare può costituire una valida ed efficace alternativa al ricovero ospedaliero in pazienti con riacutizzazioni di BPCO senza insufficienza respiratoria con acidosi. La necessità di ridurre i costi sanitari e di limitare i ricoveri ospedalieri dovrebbe indurre a portare maggiore attenzione a questo tipo di cura. Insufficienza respiratoria cronica La BPCO porta nella fase più grave ed avanzata all'insufficienza respiratoria cronica che determina uno stato d’invalidità progressiva, limitando le capacità lavorative e, a lungo termine, lo svolgimento di una normale vita di relazione. Si stima che le persone in ventiloterapia o ossigenoterapia a lungo termine, a causa di insufficienza respiratoria cronica conseguente alla BPCO, sono circa 30.000. Le implicazioni di queste sofferenze sono pesanti in termini sia di costi economici sia di costi sociali ed umani, dato che frequentemente si accompagnano ad un progressivo deterioramento psicologico, dovuto all’inabilità, alla percezione dell’ineluttabilità della malattia e al profondo mutamento delle abitudini di vita. Allo stato attuale le risorse terapeutiche disponibili sono l’ossigenoterapia a lungo termine e la ventiloterapia domiciliare che, se attuate in modo precoce, possono controllare e/o ritardare l'evoluzione della malattia. Non esistono tuttavia programmi d’intervento sul territorio, finalizzati ad assicurare una corretta gestione dei vari livelli di gravità della patologia. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO: dimensione sociale - M. Franchi Un fatto di particolare rilevanza da un punto di vista prognostico è lo sviluppo di una insufficienza respiratoria acuta in corso d’insufficienza respiratoria cronica. Il trattamento di questo evento prevede anche l'impiego di ventilazione meccanica invasiva, a cui possono seguire complicazioni ed effetti secondari con ripercussioni negative sulla prognosi a breve e a lungo termine. L'impiego di tecniche ventilatorie non invasive in ambienti pneumologici specializzati ha notevolmente modificato il decorso di tale condizione patologica. È indiscutibile la necessità di definire uno specifico percorso assistenziale a tutela dei portatori d’insufficienza respiratoria cronica che comprenda un migliore assetto territoriale delle strutture di cura, ivi comprese le Unità di Terapia Intensiva Respiratoria (UTIR). La prevenzione e il controllo ambientale Il fumo di tabacco, in particolare quello di sigaretta, è una delle principali cause per l’insorgenza di BPCO. Il fumo, infatti, rende più precoce e accentua il normale declino della funzione respiratoria. L’entità del danno broncopolmonare è direttamente proporzionale agli anni durante i quali si sono fumate sigarette, ma anche il numero di sigarette fumate quotidianamente riveste una notevole importanza. La priorità è dunque intervenire per l’abolizione del fumo, che è indiscutibilmente il primo fattore di rischio della malattia. I risultati di un vasto studio presentato al Congresso dell’ATS-American Thoracic Society tenutosi nel maggio 2004 ad Orlando dimostrano che il fumatore che sviluppa BPCO corre un rischio almeno 3 volte maggiore di essere colpito da tumore al polmone rispetto ai fumatori che non sviluppano BPCO. È quindi evidente l’importanza di controllare i pazienti che hanno fumato per anni per scoprire non solo la BPCO ma anche, in fase sempre più precoce, il tumore del polmone e avere quindi maggiori possibilità di cura. Il fumo passivo favorisce la comparsa di sintomi da BPCO anche in presenza di una ostruzione modesta. Non soltanto i fumatori attivi quindi, ma anche chi vive e lavora in ambienti dove si fuma abitualmente corre il rischio di manifestare tosse, espettorato, senso di ostruzione delle vie respiratorie (12). Carte del rischio respiratorio Le Carte del rischio respiratorio sono il frutto di una ricerca multicentrica coordinata dall’Istituto Superiore di Sanità insieme all’Istituto di Fisiologia Clinica del CNR di Pisa e al Dipartimento di Epidemiologia dell’ASL RME di Roma. Grazie alle Carte del rischio respiratorio (13) i fumatori potranno sapere, d’ora in poi, quante probabilità hanno di contrarre la BPCO nei prossimi 10 anni della loro vita. Questo nuovo strumento rappresenta in Italia un’iniziativa unica per le malattie respiratorie e la sua importanza risulta evidente se si pensa che proprio il fumo è la principale causa evitabile di morbosità e mortalità in Italia, come in tutti i Paesi industrializzati. Dalle Carte del rischio si possono ricavare due diversi tipi di informazioni: - la prima, consente ad ognuno di valutare la probabilità di ammalarsi di BPCO nel corso dei prossimi 10 anni di vita. Per esempio, si può ricavare che un maschio fumatore di 45 anni con esposizione ambientale e lavorativa avrà nei prossimi 10 anni una probabilità di ammalarsi di BPCO del 20-39%. A livello di popolazione ciò significa che in quella fascia di popolazione considerata, fra 10 anni, vi saranno probabilmente 20-39 casi di BPCO su 100 individui; - la seconda, consente di valutare quante volte in più si rischia di contrarre la malattia. Ad esem- 37 pio, un maschio di 45 anni, fumatore e con esposizione lavorativa, nei prossimi 10 anni avrà un rischio superiore di 5 volte di ammalarsi di BPCO rispetto ad un coetaneo non fumatore e senza alcuna esposizione. A livello di popolazione ciò significa che in quella fascia d’età, fra 10 anni, probabilmente vi sarà un aumento di oltre 5 volte nel numero di casi di BPCO tra i fumatori con esposizione lavorativa, rispetto al numero di casi di BPCO tra i non fumatori senza alcuna esposizione. Per ulteriori approfondimenti e informazioni sulle Carte del rischio respiratorio consultare il portale dell’Istituto Superiore di Sanità: www.iss.it. 38 Controllo della BPCO in atto Per quanto concerne il controllo della BPCO in atto, possono essere raccomandate le misure seguenti: - diagnosi precoce e corretta; - diffusione capillare della spirometria, esame non invasivo capace di evidenziare eventuali deficit di respiro di tipo ostruttivo, come esame di screening in tutte le persone a rischio, in particolare incrementandone l'uso da parte del medico di Medicina generale; - diffusione capillare di un corretto trattamento farmacologico, secondo le Linee Guida GOLD; - impegno di tutti gli operatori sanitari e politici, delle amministrazioni e dei mass media nella disassuefazione dal fumo di tabacco; - diffusione capillare della vaccinazione antiinfluenzale (ogni anno) e della vaccinazione antipneumococcica quando raccomandata dal medico; - diffusione capillare dell’uso di pulsossimetri, di spirometri e di distanziatori in tutte le strutture di Pronto Soccorso e negli ospedali; - diffusione territoriale di Reparti attrezzati per la ventilazione meccanica non invasiva in tutti gli ospedali. In questo contesto, deve inoltre essere sottolineata l’importanza dell’ambiente lavorativo e la necessità di prevenire, ridurre o eliminare i rischi “occupazionali”. Controllo ambientale Sulla base delle evidenze epidemiologiche esiste una correlazione tra incidenza della BPCO, non solo con l’abitudine tabagica, ma anche con l’inquinamento ambientale. Il controllo ambientale è un elemento prioritario di salvaguardia della salute e della qualità di vita di tutti, ma soprattutto di chi ha problemi respiratori ed è quindi importante prevedere iniziative mirate alla riduzione dei livelli d’inquinamento dell’aria. Ciò richiede modifiche comportamentali e strutturali importanti. Il Ministero della Salute ha costituito nel 1998 la Commissione tecnico-scientifica per l'elaborazione di proposte di intervento preventivo e legislativo in materia di inquinamento "indoor", che ha elaborato le “Linee Guida per la tutela e la promozione della salute negli ambienti confinati”, pubblicate nella G. U. del 27 novembre 2001, N. 252. Per le Associazioni dei Pazienti è indispensabile che queste direttive siano finalmente tradotte in azioni concrete. Fin dall’inizio degli anni ’90, l’EFA ha denunciato alle Istituzioni europee la scarsa attenzione portata agli effetti dell’inquinamento dell’aria negli ambienti confinati sulla condizione degli allergici ed asmatici. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO: dimensione sociale - M. Franchi Nell’ambito del programma di azioni comunitarie sulle malattie legate agli inquinamenti, l’EFA ha pubblicato nel 2000 uno studio sulla qualità dell’aria nelle scuole che ha messo in evidenza quanto le conseguenze di questo fattore siano sottostimate in molti paesi. A seguito del successo di questo progetto, l’EFA ha successivamente realizzato, sempre con un contributo finanziario della Commissione Europea, uno studio approfondito per migliorare la conoscenza degli effetti degli inquinanti all’interno delle abitazioni e per identificare le misure per contrastarli. I risultati di questo progetto, denominato THADE-Towards Healthy Air in Dwellings in Europe, sono in corso di pubblicazione e possono essere consultati nel sito dell’EFA, www.efanet.org. Normativa in materia di tutela del malato L’Associazione Italiana Pazienti BPCO aderisce al Coordinamento Nazionale delle Associazioni dei Malati Cronici (14) e nell’ambito di questa rete e del Tribunale per i Diritti del Malato ha l’opportunità di interagire con i soggetti istituzionali ai diversi livelli e di formulare proposte per una maggiore tutela del paziente respiratorio cronico condivise da tutte le altre organizzazioni che vi aderiscono. Le priorità attuali dell’associazione sono: 1. La revisione del Decreto Ministeriale 28 maggio 1999, n. 329 “Regolamento recante norme di individuazione delle malattie croniche e invalidanti, ai sensi dell’art. 5, comma 1, lettera a) del Decreto Legislativo 29 aprile 1998, n. 124” (G.U. 226, del 25/9/1999); 2. La revisione della normativa che concerne l’invalidità civile per quanto riguarda sia i criteri clinici sia le percentuali di invalidità ai sensi del D.M. 5/2/1992, G.U. n. 47 del 26/2/1992. Questi valori non tengono conto delle più recenti acquisizioni scientifiche e delle classificazioni per gravità definite dalle Linee Guida internazionali ed è quindi auspicabile un aggiornamento e un adeguamento alle attuali definizioni. Campagne di sensibilizzazione Dal punto di vista delle Associazioni dei Pazienti è indispensabile che sia accresciuta la consapevolezza dell’opinione pubblica attraverso campagne di informazione ed educazione, volte a responsabilizzare il cittadino quanto al ruolo che egli stesso può svolgere per contrastare i rischi respiratori, modificando i propri comportamenti e stili di vita e prendendo i provvedimenti utili alla prevenzione. Un’indagine sulla percezione della prevenzione delle malattie respiratorie, effettuata da Datanalysis nel maggio 2003 su un campione rappresentativo composto da 1.000 cittadini italiani contattati telefonicamente (www.pazientibpco.it), ha messo in evidenza un preoccupante e generale scetticismo quanto alla possibilità di prevenzione e di tutela della salute dei polmoni da parte degli intervistati. Solo una persona su cinque ha mostrato consapevolezza dei rischi per l’apparato respiratorio dovuti al fumo. Da qui l’importanza di un’azione capillare di sensibilizzazione volta ad accrescere la conoscenza della malattia, con iniziative specifiche rivolte alle persone colpite e alle loro famiglie, ma anche all’opinione pubblica ed alle Autorità sanitarie. Ricordiamo i principali appuntamenti annuali, che hanno certamente prodotto risultati positivi in termini di diffusione delle conoscenze scientifiche e assistenziali: - Giornata Nazionale del Respiro (ultimo sabato del mese di maggio); - Giornata Mondiale senza Fumo (31 maggio); - Giornata Mondiale BPCO (terzo mercoledì del mese di novembre). 39 Dialogo con le istituzioni 40 Le Istituzioni hanno un ruolo importante nella lotta alla BPCO perché possono fare delle cose concrete per aiutare a conoscere e combattere la malattia. Per instaurare un dialogo con le Istituzioni su una base di lavoro comune, l’Associazione Italiana Pazienti BPCO ha stilato nel 2004 un vero e proprio “Decalogo delle richieste dei malati di BPCO”, che è stato trasmesso a tutte le Amministrazioni Regionali: 1. Inserire la BPCO nell’agenda politica; 2. Promuovere campagne di sensibilizzazione sul significato della malattia, i sintomi, i fattori di rischio e la sua natura cronica e progressiva; 3. Favorire un largo uso della spirometria; 4. Incoraggiare l’uso della vaccinazione antinfluenzale; 5. Organizzare programmi di formazione per gli operatori sanitari e i medici; 6. Sostenere l’organizzazione di programmi educazionali per i pazienti e i familiari al fine di migliorare la gestione della malattia e arginare il numero e la gravità delle riacutizzazioni, grave fattore di peggioramento del quadro generale e di riduzione dell’aspettativa di vita del malato; 7. Promuovere standard di cura ottimali; 8. Prevedere maggiori investimenti per assicurare la continuità dell’assistenza sociale e sanitaria a livello territoriale; 9. Stanziare più investimenti per la ricerca; 10.Tutelare il diritto del paziente alla parità di accesso alla diagnosi, al trattamento, all’informazione, all’educazione, alla prevenzione e ai programmi di riabilitazione respiratoria. Conclusioni Il punto di partenza e di arrivo quando si parla di BPCO è che essa costituisce realmente una ve- ra e propria emergenza di sanità pubblica. È una malattia che vive un paradosso secondo il quale la sua diffusione è inversamente proporzionale alla sua conoscenza: ossia, nonostante si preveda che diventerà in pochi anni la terza causa di morte a livello mondiale, e nonostante i progressi compiuti nel corso degli ultimi anni in termini di conoscenze scientifiche relative al trattamento e alla gestione, la BPCO continua ad essere ancora oggi una malattia molto sottovalutata dal medico, dal paziente stesso, dall’opinione pubblica e dalle Istituzioni. Numerose sono le barriere per un’adeguata gestione ed un controllo ottimale della malattia. Barriere che si situano a livello della diagnosi, del trattamento, del rapporto medico-paziente, dell’informazione e dell’educazione. I pazienti tuttavia sottostimano i propri sintomi e il livello di gravità, mentre sovrastimano il grado di controllo della malattia, e ciò indica quanto sia in generale inadeguata la gestione di questa patologia, con gravi conseguenze soprattutto sulla qualità di vita. I medici hanno un ruolo determinante in questo processo e devono cercare di dialogare di più con i pazienti, per aiutarli a prendere coscienza della propria condizione, a gestire la malattia e a valutare le reali possibilità di controllarla, con la consapevolezza dell’importanza e del significato del trattamento, dei suoi rischi e dei suoi vantaggi. L’accesso al trattamento farmacologico, raccomandato dalle Linee Guida internazionali basate sulle evidenze e sulle più recenti acquisizioni scientifiche internazionali, costituisce la garanzia per il miglioramento delle condizioni di salute e della qualità di vita dei pazienti e, di conseguenza, per la riduzione dei costi totali di questa patologia. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO: dimensione sociale - M. Franchi Sulla base delle conoscenze attuali, è necessaria la definizione di un programma sanitario volto a ridurre la prevalenza, la mortalità e i costi socio-economici della BPCO. I principali interventi si situano a livello della prevenzione e della ricerca. Contrastare le malattie respiratorie croniche ostruttive è possibile. Tutte le parti interessate hanno un ruolo da svolgere per conseguire nuovi traguardi dal punto di vista umano, sanitario, sociale ed economico. Le Associazioni dei pazienti International COPD Coalition - ICC - www.internationalcopd.org L’International COPD Coalition è un’organizzazione di volontariato composta da organizzazioni mediche e di pazienti di tutto il mondo che ha lo scopo di migliorare la condizione di salute e l’accesso al trattamento dei malati con BPCO. Gli obiettivi principali sono: - definire, finanziare e gestire progetti pilota per migliorare la condizione di salute e l’accesso al trattamento dei pazienti con BPCO, con particolare attenzione ai paesi in via di sviluppo e alle aree meno favorite; - accrescere la conoscenza della BPCO; - sostenere interventi di prevenzione, diagnosi e terapia della BPCO nell’ambito del sistema sanitario di base; - migliorare il trattamento dei pazienti con BPCO. Collaborano con l’ICC importanti organizzazioni quali: EFA (European Federation of Allergy and Airways Diseases Patients Associations), Australian Lung Foundation, Japanese Respiratory Society, Canadian Lung Foundation e altre organizzazioni degli Stati Uniti e dell’America del Sud. EFA – European Federation of Allergy and Airways Diseases Patients Associations - www.efanet.org L’EFA è stata fondata in Svezia nel 1991 per iniziativa di otto paesi europei (Finlandia, Irlanda Islanda, Norvegia, Polonia, Paesi Bassi, Regno Unito e Svezia) allo scopo di migliorare le condizioni di salute e la qualità di vita dei pazienti asmatici e allergici in Europa. Nel 2000 l’EFA ha modificato il suo statuto per comprendere nei suoi obiettivi le malattie croniche respiratorie croniche e in particolare la BPCO. Oggi l’EFA è un importante network di pazienti con 41 associazioni in 22 paesi europei. Le associazioni di pazienti BPCO aderenti all’EFA sono 13. Associazioni di pazienti in Italia AIPAS Onlus -Associazione Italiana Pazienti con Apnee del Sonno http://www.sleepapnea-online.it/ AMOR-Associazione Milanese di Ossigenoterapia Riabilitativa http://divulgativo.pneumonet.it/assovolont.html#associazione Associazione Italiana Pazienti BPCO http://www.pazientibpco.it http://www.pazientibpco.it Associazione Nazionale Alfa1- at http://divulgativo.pneumonet.it/alpha1at/ ALIR- Associazione Italiana per la Lotta all’Insufficienza Respiratoria http://scientifico.pneumonet.it/alir/ Federasma http://www.federasma.it RIMAR- Associazione Riabilitazione Malattie Respiratorie [email protected] 41 Piani Sanitari Regionali in vigore REGIONE ABRUZZO Piano Sanitario Regionale 1999-2001 http://leggi.regione.abruzzo.it/leggireg/1999/l037.html REGIONE BASILICATA Piano Sanitario Regionale 1997-1999 http://www.basilicatanet.it/ REGIONE CALABRIA Piano Sanitario Regionale 2004-2006 http://www.consiglioregionale.calabria.it/hp2/dett_testocoordinato.asp?Codice=2004 REGIONE CAMPANIA Piano Sanitario Regionale 2002-2004 http://www.edscuola.it/archivio/handicap/italia/psrcampania.pdf REGIONE EMILIA ROMAGNA Piano Sanitario Regionale 1999-2001 http://www.saluter.it/wcm/saluter/sanitaer/assessorato/politiche_salute/allegati_pianosanitario_re gionale_2001/psr/linkpsr/indice.htm 42 REGIONE FRIULI VENEZIA GIULIA Piano Sanitario Regionale 2000-2002 http://www.farmindustria.it/farmindustria/documenti/friuli.pdf REGIONE LAZIO Piano Sanitario Regionale 2002-2004 http://www.regione.lazio.it/sanita/PSR/psr.shtml REGIONE LIGURIA Piano Sanitario Regionale 2003-2005 http://www.bur.liguriainrete.it/archiviofile/B_BUR000034604092ss0.pdf REGIONE LOMBARDIA Piano Socio Sanitario Regionale 2002-2004 http://www.famiglia.regione.lombardia.it/pss/pss.asp REGIONE MARCHE Piano Sanitario Regionale 2003-2005 http://salute.regione.marche.it/media/Files/926_psrmarche.pdf REGIONE MOLISE Piano Sanitario Regionale 1997-1999 http://www.regione.molise.it/ REGIONE PIEMONTE Piano Sanitario Regionale 1997-1999 http://arianna.consiglioregionale.piemonte.it/base/leggi/l1997061.html REGIONE PUGLIA Piano Sanitario Regionale 2002-2004 http://www.edscuola.it/archivio/handicap/italia/psrpuglia.pdf Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 3. BPCO: dimensione sociale - M. Franchi REGIONE SARDEGNA Piano Sanitario Regionale in corso di preparazione http://www.regione.sardegna.it REGIONE SICILIA Piano Sanitario Regionale 2000-2002 http://www.edscuola.it/archivio/handicap/italia/psrsicilia.pdf REGIONE TOSCANA Piano Sanitario Regionale 2002-2004 http://www.rete.toscana.it/sett/sanit/piano.htm REGIONE UMBRIA Piano Sanitario Regionale 2003-2005 http://www.regione.umbria.it/resources/Servizio_Sanita/030827A36SO1.pdf REGIONE VALLE D'AOSTA Piano Sanitario Regionale 2002-2004 http://www.regione.vda.it/sanita/programmazione/piano_socio_sanitario_2002_2004/piano_socio_sanitario_2002_2004_i.pdf REGIONE VENETO Piano Sanitario Regionale 2003-2005 http://www.regione.veneto.it/NR/rdonlyres/5AA6DD6D-482A-491E-80FA-E982C5656D57/181/piano_2003.pdf PROVINCIA AUTONOMA DI BOLZANO Piano Sanitario Provinciale 2000-2002 http://www.edscuola.it/archivio/handicap/italia/psrbolzano.pdf PROVINCIA AUTONOMA TRENTO Piano Sanitario Provinciale 1993-1995 http://www.consiglio.provincia.tn.it/ BIBLIOGRAFIA 1. Eurisko, BPCO e disturbi BPCO-compatibili presso gli italiani, giugno 2004. 2. Rudolf M, The reality of drugs use in COPD, Chest 2000;117:29S-32S. 3. Global Initiative for Chronic Obstructive Lung Disease, NHLBI/WHO Workshop Report 2001 e successivi aggiornamenti. 4. ISTAT, Stili di vita e condizioni di salute, Indagine multiscopo annuale su "Aspetti della vita quotidiana", 2001. 5. ISTAT, Morti per causa, 2000. 6. Mannino DM, Homa DM, Akimbani LJ, Ford ES, Redd SC. Chronic Obstructive Pulmonary Disease Surveillance - United States, 1971–2000. MMWR 2002; 51: 1–16. 7. Dal Negro R, Rossi A, Cerveri I. The burden of COPD in Italy: results from Confronting COPD survey Respir Med 2003; 97 Suppl C: S43-50. 8. International Quality of Life Assessment, http://www.iqola.org. 9. www.ministerosalute.it/resources/static/psn/documenti/psn_2003-2005. 10. www.ministerosalute.it/resources/static/primopiano/216/piano_nazionale_di_prevenzione_attiva.pdf. 11. European COPD Patient Manifesto, EFA 2002. 12. de Marco R, Accordini S, Cerveri I, Corsico A, Sunyer J, Neukirch F, Ku¨nzli N, Leynaert B, Janson C, Gislason T, Vermeire P, Svanes C, Anto JM, Burney P, for the European Community Respiratory Health Survey (ECRHS) Study Group: An international survey of chronic obstructive pulmonary disease in young adults according to GOLD stages Thorax 2004;59:120–125. 13. Fumo e patologie respiratorie. Le carte del rischio per broncopneumopatia cronica ostruttiva e Tumore Polmonare. Zuccaro P, Pichini S, Mortali C, Pacifici R, Viegi G, Baldacci S, Angino A, Martini F, Borbotti M, Scognamiglio A, Simoni M, Silvi P, Di Pete F, Carrozzi L, Porta D, Limonato L, Crispo A, Merletti F, Forastiere F, Caraffa G. Istituto Superiore di Sanità, maggio 2004. 14. Coordinamento nazionale delle Associazioni dei Malati Cronici. www.cittadinanzattiva.it. 43 4. Anatomia-patologica A cura di Graziella Turato, Simonetta Baraldo, Bianca Beghè, Renzo Zuin e Marina Saetta Dipartimento di Scienze Cardiologiche Toraciche e Vascolari Università degli Studi di Padova, Padova 4. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) è una malattia caratterizzata da una riduzione di flusso aereo non completamente reversibile. Questa riduzione di flusso è progressiva e associata ad un’anomala risposta infiammatoria del polmone a particelle o gas nocivi, come il fumo di sigaretta (1,2). Il fumo di sigaretta è infatti il principale fattore di rischio per lo sviluppo della BPCO ed è responsabile di circa il 90% dei casi. Tuttavia il fatto che non tutti i fumatori sviluppino la malattia fa supporre che fattori diversi dal fumo di sigaretta, di natura ambientale o genetica, possano contribuire a conferire una particolare suscettibilità ad alcuni individui. La riduzione di flusso aereo non completamente reversibile che definisce la malattia, riflette l’impatto sulla funzionalità respiratoria delle numerose alterazioni anatomo-patologiche presenti nel polmone dei soggetti con BPCO. Poiché i principali fattori che determinano il flusso aereo sono la pressione di spinta che lo genera (dovuta alla forza di retrazione elastica del polmone), e le resistenze che vi si oppongono, una riduzione del flusso aereo può essere causata da una diminuzione della forza di retrazione elastica del polmone o da un aumento delle resistenze. La diminuzione della forza di retrazione elastica del polmone è causata principalmente dalla distruzione parenchimale caratteristica dell’enfisema, mentre l’aumento delle resistenze è dovuto principalmente all’infiammazione delle vie aeree periferiche. Distruzione parenchimale e infiammazione delle vie aeree sono quindi le principali alterazioni responsabili della riduzione di flusso aereo nella BPCO (3). Il ruolo di altri fattori, come ad esempio i sintomi di bronchite cronica, nello sviluppo della riduzione di flusso è ancora controverso. Infatti è stato dimostrato che nei fumatori l’iperproduzione di muco non è prognostica di un successivo sviluppo di broncoostruzione (4,5). D’altra parte è stato riportato che, in pazienti che hanno già sviluppato la broncoostruzione, i sintomi di bronchite cronica sono associati ad un eccessivo declino della funzionalità respiratoria (5,6). È quindi possibile ipotizzare che l’iperproduzione di muco non sia determinante per l’insorgenza della BPCO, ma possa svolgere un ruolo nella progressione della malattia. Il sito principale dell’iperproduzione di muco è costituito dalle vie aeree centrali, e sono ormai numerosi gli studi che hanno dimostrato che i sintomi di bronchite cronica sono associati ad un processo infiammatorio localizzato in queste vie aeree (3). I fumatori con BPCO vanno incontro a frequenti riacutizzazioni della malattia caratterizzate da un peggioramento dei sintomi. Fino a poco tempo fa si riteneva che l’unico fattore capace di accelerare il declino della funzionalità respiratoria nei soggetti con BPCO fosse l’abitudine al fumo di sigaretta. Recentemente è stato dimostrato che un altro fattore in grado di accelerare il declino del VEMS (volume espiratorio massimo nel primo secondo) è la frequenza delle riacutizzazioni. Infatti, nei pazienti con BPCO che hanno avuto numerose riacutizzazioni, il declino annuo del VEMS è maggiore rispetto a quello osservato in pazienti che hanno avuto poche riacutizzazioni (7). Alla luce di questa osservazione le riacutizzazioni, che già avevano una notevole importanza clinica, assumono un ruolo determinante anche nella storia naturale della malattia. Da queste considerazioni emerge che, nella BPCO, alterazioni anatomo-patologiche possono interessare le vie aeree centrali, le vie aeree periferiche ed il parenchima polmonare e possono assumere caratteristiche peculiari nelle diverse fasi cliniche della malattia, ad esempio durante le riacutizzazioni. 45 Anatomia-patologica nelle vie aeree centrali 46 Le vie aeree centrali rappresentano il sito responsabile dell’iperproduzione di muco e quindi della presenza dei sintomi che caratterizzano la bronchite cronica. Sebbene per molti anni si sia ritenuto che la base morfologica della malattia fosse costituita dall’aumento della massa (ipertrofia) della ghiandole bronchiali che secernono muco (8), studi più recenti hanno invece dimostrato che la presenza dei sintomi di bronchite cronica è associata più all’infiammazione delle vie aeree che all’ipertrofia ghiandolare (9,10). La caratterizzazione del processo infiammatorio presente nelle vie aeree centrali di soggetti con bronchite cronica è stata oggetto di numerosi studi. Nelle biopsie bronchiali è stata osservata la presenza di metaplasia squamosa dell’epitelio e di iperplasia delle cellule caliciformi mucipare (11). La zona sottoepiteliale è caratterizzata da un infiltrato infiammatorio costituito prevalentemente da macrofagi e linfociti T (12,13) ed in particolare da linfociti T CD8. Nei pazienti con BPCO i linfociti T CD8, non sono solo aumentati di numero, ma sono anche correlati con il grado di broncoostruzione, avvalorando l’ipotesi che queste cellule possano avere un ruolo nella progressione della malattia (14). È interessante notare che mentre nel lume bronchiale dei fumatori con bronchite cronica si osserva un elevato numero di neutrofili, nella sottomucosa non è in genere presente neutrofilia. Questa discrepanza tra lume e parete potrebbe essere dovuta alla rapida migrazione dei neutrofili dai vasi del circolo bronchiale verso il lume, attraverso la parete e l’epitelio, per cui il loro numero nella zona sottoepiteliale rimane sempre basso. La migrazione dei neutrofili potrebbe essere causata da uno squilibrio tra citochine pro ed anti-infiammatorie. Infatti nei fumatori con BPCO è stata osservata una riduzione dell’interleuchina (IL)-10 (citochina che riduce la risposta infiammatoria) e un aumento di IL-8 (citochina con azione chemiotattica sui neutrofili) e del fattore di necrosi tumorale (TNF)-α (citochina che stimola l’espressione delle molecole di adesione) (3). L’osservazione di una aumentata espressione delle molecole di adesione E-selettina e intracellular adhesion molecole-1 (ICAM-1) sia sui vasi della zona sottoepiteliale che sull’epitelio bronchiale dei fumatori con BPCO rafforza l’ipotesi che i neutrofili migrino dai vasi del circolo bronchiale al lume attraversando la zona sottoepiteliale e l’epitelio (15). I neutrofili che, come abbiamo visto, non sono aumentati nella zona sottoepiteliale, sono invece aumentati nelle ghiandole bronchiali dei fumatori con bronchite cronica (10). Poiché l’elastasi dei neutrofili è in grado di esercitare una potente azione secretagoga sulle cellule ghiandolari, la particolare localizzazione dei neutrofili proprio nelle ghiandole potrebbe avere un ruolo cruciale nell’attivazione della loro funzione secretoria e quindi nell’induzione dell’iperproduzione di muco nei fumatori (3). Anatomia-patologica delle vie aeree periferiche Le vie aeree periferiche sono il sito responsabile dell’aumento delle resistenze e quindi della riduzione di flusso nei soggetti con BPCO (16). Le principali alterazioni anatomo-patologiche presenti nelle vie aeree periferiche di soggetti con BPCO comprendono l’infiammazione, la fibrosi, l’ipertrofia del muscolo liscio, la distruzione degli attacchi alveolari e l’iperplasia delle cellule caliciformi mucipare (17-22). L’infiammazione cronica determina un danno, a cui conseguono processi riparativi della parete bronchiale; questi possono essere responsabili delle alterazioni strutturali che nel loro complesso vengono definite con il termine “rimodellamento” delle vie aeree. Questi processi di rimodellamento, aumentando lo spessore della parete, causano il restringimento del lume e quindi un aumento delle resistenze. L’infiammazione delle vie aeree può favorire la broncoostruzione non solo attraverso l’aumento dello spessore della parete, ma anche attraverso la distruzione degli attacchi alveolari, ovvero di Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 4. Anatomia-patologica - G. Turato, S. Baraldo, B. Beghè, R. Zuin, M. Saetta quelle pareti alveolari che, ancorandosi alle vie aeree, contribuiscono a mantenerle aperte (20). Questa ipotesi è sostenuta dal fatto che il grado di distruzione degli attacchi alveolari è correlato positivamente con il grado di infiammazione delle vie aeree (20). È possibile che l’azione litica di mediatori prodotti dalle cellule infiammatorie che infiltrano la parete bronchiolare indebolisca il tessuto alveolare, facilitandone la rottura, soprattutto nel punto di congiunzione tra parete delle vie aeree e parete alveolare, dove probabilmente lo stress meccanico è massimo. Un altro meccanismo che, in corso di flogosi delle vie aeree periferiche, può contribuire alla riduzione di flusso aereo, è la sostituzione delle cellule di Clara con cellule caliciformi mucipare metaplastiche (21). Questa sostituzione determina infatti una iperproduzione di muco e una diminuzione della produzione di surfattante bronchiolare, che attraverso l’occlusione del lume e l’aumento della tensione superficiale, possono favorire la chiusura delle vie aeree, in particolare durante l’espirazione. È interessante sottolineare che, nell’epitelio delle vie aeree dei fumatori, la metaplasia delle cellule caliciformi mucipare è associata ad un aumento del numero di neutrofili (21). Poiché, come abbiamo già visto, l’elastasi neutrofila può svolgere un’importante azione secretagoga, è possibile che la presenza dei neutrofili nell’epitelio sia rilevante ai fini dell’attivazione della funzione secretoria delle cellule caliciformi mucipare. Di notevole interesse è l’osservazione che i neutrofili sono aumentati di numero oltre che nell'epitelio anche nei fasci della muscolatura liscia delle vie aeree periferiche (23). Poiché i neutrofili non sono normalmente presenti nella parete delle vie aeree nei soggetti con BPCO, la loro presenza proprio nei fasci muscolari fa ipotizzare che queste cellule possano svolgere una funzione specifica in questo particolare compartimento. Infatti i mediatori prodotti dai neutrofili, come ad esempio l’IL-8, sono in grado di stimolare la contrazione del muscolo liscio e quindi di contribuire alla broncoostruzione restringendo il lume delle vie aeree. Gli stessi mediatori sono anche in grado di stimolare la proliferazione delle cellule muscolari e quindi potrebbero spiegare l’aumento della massa di muscolo liscio osservata nei soggetti con BPCO (17,18). Questo aumento dell’area occupata dal muscolo liscio contribuisce ad aumentare lo spessore della parete favorendo la broncoostruzione. Gli studi che hanno esaminato la risposta infiammatoria nelle vie aeree periferiche hanno dimostrato che è caratterizzata da un aumento dei linfociti B nell’avventizia (24) e da un aumento dei linfociti T CD8+ nella zona sottoepiteliale (17). È interessante sottolineare che un aumento di linfociti T CD8+ è presente non solo nelle vie aeree periferiche ma anche nelle vie aeree centrali, nel parenchima polmonare, nelle arterie polmonari (25) e nei linfonodi di soggetti con BPCO (26), avvalorando l’ipotesi che un processo infiammatorio omogeneo (caratterizzato dallo stesso tipo cellulare) coinvolga l’intero albero tracheobronchiale. Inoltre, in ognuno di questi compartimenti, i linfociti T CD8+ non sono solo aumentati di numero ma sono anche correlati al grado di broncoostruzione, facendo supporre che queste cellule possano avere un ruolo importante nella progressione della malattia. La principale attività dei linfociti T CD8+ è la rapida risoluzione delle infezioni virali, che sono un evento frequente nei soggetti con BPCO. È possibile che, in risposta a ripetute infezioni virali, possa verificarsi un eccessivo reclutamento di linfociti T CD8+, e che l’attività citotossica di questo eccesso di linfociti possa danneggiare il polmone attraverso il rilascio di perforine ed enzimi proteolitici (granzimi) (3,27). I linfociti T, in base al tipo di citochine prodotte, possono essere divisi in linfociti di tipo 1 e linfociti di tipo 2. I linfociti di tipo 1 producono l’interferone γ (IFN-γ), che ha un ruolo cruciale nell’attivazione dei macrofagi e nella risposta alle infezioni virali e batteriche. I linfociti di tipo 2 producono l’interleuchina 4 (IL-4) e l’interleuchina 5 (IL-5), che sono coinvolte nella risposta IgE-mediata e nell’eosinofilia, caratteristiche delle malattie allergiche; le due classi di linfociti inoltre esprimono re- 47 48 cettori per le chemochine diversi. In particolare, il recettore CXCR3 viene espresso esclusivamente dai linfociti di tipo 1 e può essere pertanto considerato un marcatore di questo tipo di risposta infiammatoria. Il primo studio che ha quantificato l’espressione del CXCR3 nelle vie aeree periferiche dei fumatori con BPCO ha dimostrato un aumento di questo recettore nell’epitelio e nella parete bronchiale (28). Inoltre l’espressione del CXCR3 era associata ad aumento dell’espressione del suo ligando IP-10 (o CXCL10) ed era localizzata principalmente su linfociti T IFN-γ positivi. In uno studio successivo, Grumelli e collaboratori hanno confermato ed esteso questi risultati. Esaminando linfociti T isolati da tessuto polmonare, hanno dimostrato che i pazienti con BPCO hanno un’elevata percentuale di linfociti T CD4+ e CD8+ che esprimono il recettore per le chemochine CXCR3 e che secernono IFN-γ e IP-10 (29). L’interazione tra CXCR3 e IP-10 sembra essere quindi di fondamentale importanza nel reclutamento dei linfociti T nelle vie aeree periferiche dei fumatori con BPCO. Inoltre, i risultati di questi due studi sembrano confermare che la risposta infiammatoria caratteristica della BPCO sia di tipo 1. Lo studio di Grumelli e collaboratori ha anche dimostrato che, in risposta a IP-10, i macrofagi rilasciano la metalloproteasi di matrice MMP–12, che è in grado di degradare l’elastina causando danni al tessuto polmonare e quindi enfisema. Questo suggerisce che, nel polmone di fumatori con BPCO, i linfociti Th1 partecipino, assieme ai macrofagi, al processo di distruzione parenchimale attraverso l’aumentata espressione di CXCR3 ed il rilascio di IP-10 e di MMP-12 (29). Questa ipotesi è rafforzata dall’osservazione che, in entrambi gli studi appena descritti, l’espressione di CXCR3 sui linfociti Th1 è correlata con la riduzione del flusso espiratorio, che può riflettere la gravità dell’enfisema. Nei pazienti con BPCO si assiste ad un progressivo peggioramento della funzionalità respiratoria, che in alcuni casi può diventare estremamente grave e invalidante. Lo studio del quadro anatomo-patologico presente in questi pazienti è particolarmente interessante per comprendere perché tra i fumatori solo alcuni sviluppino la BPCO grave. Recentemente, esaminando prelievi chirurgici ottenuti da pazienti sottoposti a intervento chirurgico di riduzione dei volumi polmonari per enfisema, è stato dimostrato che nelle vie aeree periferiche di soggetti con BPCO grave vi è un'amplificazione del processo infiammatorio indotto dal fumo di sigaretta (30). Il numero di leucociti totali (CD45+) che infiltrano la parete è infatti più che raddoppiato rispetto a quello presente in soggetti fumatori senza BPCO (fig. 1). La quantificazione delle diverse cellule infiammatorie ha dimostrato che questa risposta infiammatoria è dovuta ad un aumento di linfociti T CD8+ e CD4+ nella parete e ad un aumento di macrofagi nell'epitelio. È interessante osservare che la risposta infiammatoria è correlata con numerosi parametri clinico-funzionali come la riduzione di flusso aereo, il grado di iperinflazione polmonare, la riduzione della capacità di diffusione del CO e il grado radiologico di enfisema (30). Figura 1 – Immagine al microscopio ottico che mostra l’infiltrazione di leucociti totali (CD45+) in una via aerea periferica di un soggetto con BPCO grave (a) e di un soggetto con BPCO lieve di controllo (b). Colorazione immunoistochimica con anticorpo anti CD45 (blu scuro). Ingrandimento originale: 400X. a b Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 4. Anatomia-patologica - G. Turato, S. Baraldo, B. Beghè, R. Zuin, M. Saetta Questi risultati avvalorano l’ipotesi che l’amplificazione della risposta infiammatoria nelle vie aeree possa svolgere un ruolo nella progressione della BPCO. Ciascuno degli studi finora discussi ha preso in considerazione piccoli gruppi di pazienti con BPCO, che avevano un grado di broncoostruzione omogeneo (BPCO lieve/moderata o BPCO grave), per cui le conclusioni che si sono potute trarre erano limitate ad una particolare condizione clinica. Mancavano quindi in letteratura studi che avessero esaminato l’evoluzione delle lesioni anatomo-patologiche in un’ampia casistica di pazienti con BPCO a diversi stadi di gravità. Recentemente il gruppo di James Hogg ha colmato questa lacuna esaminando campioni di tessuto polmonare ottenuti da 159 pazienti con BPCO suddivisi nei 4 stadi di gravità descritti dalle Linee Guida GOLD (22) . Questo studio ha dimostrato che le alterazioni anatomo-patologiche nelle vie aeree periferiche aumentano progressivamente con la gravità della BPCO. Infatti, passando dallo stadio 0 allo stadio 4, è stato osservato un aumento dell’essudato infiammatorio nel lume che gli Autori hanno interpretato come risposta dell’immunità naturale, non specifica, a stimoli dannosi. La progressione della BPCO era inoltre associata ad un aumento della percentuale di vie aeree infiltrate da cellule infiammatorie (in particolare linfociti T e B). Nei pazienti più gravi, queste cellule infiammatorie erano organizzate in veri e propri follicoli con un centro germinale ricco di linfociti B, circondato da una regione periferica ricca di linfociti T. Questa precisa organizzazione della risposta infiammatoria ha suggerito l’ipotesi che, con il progredire della BPCO, si sviluppi una risposta immunologica acquisita nei confronti di un antigene specifico. Sebbene questo antigene non sia stato ancora identificato, gli autori hanno ipotizzato che la colonizzazione batterica delle vie aeree periferiche, evento frequente nei pazienti con BPCO grave, possa indurre questa risposta antigenespecifica (22). Infine questo studio ha dimostrato che la progressione della BPCO è associata ad un ispessimento della parete delle vie aeree periferiche, dovuto all’aumento dello spessore di tutte le sue componenti (epitelio, sottomucosa, muscolo liscio e avventizia). Questo rimodellamento della parete bronchiolare è probabilmente dovuto a dei processi riparativi inadeguati, che vengono attivati in risposta al danno polmonare indotto dal processo infiammatorio. Anatomia-patologica del parenchima polmonare La principale alterazione strutturale del parenchima polmonare nei soggetti fumatori con BPCO è la distruzione parenchimale che caratterizza l’enfisema e che contribuisce alla riduzione di flusso attraverso una diminuzione della forza di retrazione elastica del polmone. L’enfisema viene definito come distruzione e allargamento degli spazi aerei distali al bronchiolo terminale in assenza di evidenti segni di fibrosi (31). Tuttavia, quest’ultima affermazione ”assenza di evidenti segni di fibrosi” è oggi controversa, poiché alcuni studi hanno dimostrato che l’enfisema è associato ad un aumento della deposizione di collagene e quindi alla presenza di fibrosi (32,33). L’enfisema può essere definito centroacinare o panacinare in base della regione dell’acino interessata dal processo di distruzione (34). A questo proposito può essere utile ricordare che l’acino polmonare è l’unità di parenchima ventilata da un bronchiolo terminale. L’enfisema centroacinare è caratterizzato da aree di distruzione localizzate intorno ai bronchioli terminali, nella zona centrale dell’acino, circondate da aree di parenchima normale. L’enfisema centroacinare è caratteristico dei fumatori che sviluppano enfisema dopo una lunga storia di esposizione al fumo ed è localizzato prevalentemente nei lobi superiori del polmone. L’enfisema panacinare è caratterizzato da una distruzione omogenea di tutto l’acino polmonare (34), è caratteristico dei pazienti che sviluppano enfisema in età relativamente giovane (solitamente nei soggetti con deficit di α-1-antitripsina) ed è localizzato prevalentemente nei lobi inferiori. Sebbene nei pazienti con BPCO i due tipi di enfisema possano coesistere, nelle forme più gravi spesso si osserva la prevalenza di uno dei due tipi. È stato osservato 49 50 che, nei fumatori con enfisema prevalentemente centroacinare, la riduzione di flusso aereo è correlata al grado di infiammazione delle vie aeree e non alla perdita della retrazione elastica del polmone, mentre, al contrario, nei fumatori con enfisema prevalentemente panacinare, la riduzione di flusso aereo è correlata alla perdita di forza di retrazione elastica del polmone, ma non al grado di infiammazione delle vie aeree. Sulla base di queste considerazioni è stato ipotizzato che l’enfisema centroacinare possa essere una malattia “air-borne”, cioè che origina dalle vie aeree infiammate, mentre l’enfisema panacinare sarebbe invece una malattia “blood-borne”, che origina da uno squilibrio delle sostanze circolanti nei vasi sanguigni, come nel caso del deficit di α-1-antitripsina (34). Il processo di distruzione non è l’unica alterazione anatomo-patologica presente nel parenchima dei soggetti con BPCO. Recentemente è stato dimostrato che, nel parenchima polmonare di questi soggetti, è presente un processo infiammatorio caratterizzato da un aumento di linfociti T CD8 quando la BPCO è lieve (25) e da un aumento di tutte le cellule infiammatorie quando la malattia diventa grave (35). Sia i meccanismi responsabili dell’infiammazione parenchimale che il ruolo svolto da questo processo infiammatorio nello sviluppo della distruzione parenchimale rimangono ancora ampiamente sconosciuti. Il recente sviluppo delle tecniche di tomografia computerizzata (TC scan) ha evidenziato che un quadro radiologico compatibile con la presenza di enfisema è riscontrabile in circa il 40% dei fumatori e, sorprendentemente, può essere presente anche in fumatori con funzionalità respiratoria normale. Tuttavia l’ipotesi che la presenza precoce di enfisema sia prognostica di un futuro sviluppo di broncoostruzione non è ancora stata adeguatamente studiata. L’osservazione che il 40% dei fumatori sviluppano enfisema, ma solo il 15% sviluppano broncoostruzione conclamata probabilmente riflette il lungo decorso subclinico della BPCO (27) durante il quale i danni indotti dal fumo rimangono silenti nel polmone anche per molti anni. Anatomia-patologica delle riacutizzazioni di BPCO I fumatori con BPCO vanno incontro a frequenti riacutizzazioni della malattia. Sebbene una definizione standardizzata di riacutizzazione di BPCO non sia stata ancora formulata, una riacutizzazione lieve può essere definita clinicamente come un peggioramento dei sintomi di dispnea, tosse ed espettorato tale da far ricorrere il paziente alle cure mediche, mentre una riacutizzazione può essere considerata grave quando è associata ad insufficienza respiratoria acuta (36). È importante sottolineare che non tutte le riacutizzazioni sono caratterizzate da una riduzione marcata della funzionalità respiratoria. I fattori eziologici delle riacutizzazioni di BPCO non sono ancora del tutto noti, tuttavia appare sempre più evidente il coinvolgimento di infezioni, sia batteriche sia virali. I meccanismi attraverso i quali queste infezioni possono causare le riacutizzazioni della BPCO sono poco conosciuti e ciò è in parte dovuto al fatto che soltanto pochi studi istopatologici hanno esaminato pazienti con BPCO durante una riacutizzazione. I risultati di questi studi, eseguiti su biopsie bronchiali, lavaggio broncoalveolare e, più recentemente, su espettorato spontaneo o indotto, hanno dimostrato un'amplificazione del processo infiammatorio associato ad un aumento della produzione di citochine proinfiammatorie (37-41). In particolare, le riacutizzazioni della BPCO sono caratterizzate da un marcato reclutamento di granulociti neutrofili nel polmone. Questa neutrofilia si associa ad una aumentata espressione della chemochina IL-8 (o CXCL8) che ha azione chemotattica sui neutrofili, e dell’enzima mieloperossidasi che è un indice di attivazione dei neutrofili (37,38). Inoltre, durante le riacutizzazioni di BPCO si osserva un aumento di TNF-α (38), una citochina capace di aumentare l'espressione delle molecole di adesione sulle cellule endoteliali, facilitando così la migrazione dei leucociti dai Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 4. Anatomia-patologica - G. Turato, S. Baraldo, B. Beghè, R. Zuin, M. Saetta vasi del circolo bronchiale al tessuto polmonare. Nelle biopsie bronchiali di soggetti con una riacutizzazione lieve di BPCO, si è visto che la neutrofilia è associata ad una marcata eosinofilia e ad un aumento delle chemochine eotassina e RANTES (Regulated upon Activation Normal T cell Expressed and Secreted) (39,40). Questi risultati fanno ipotizzare che le infezioni virali, capaci e di indurre la produzione sia di eotassina sia di RANTES, abbiano un ruolo importante nelle riacutizzazioni della BPCO. Poiché RANTES è in grado di promuovere l'apoptosi di cellule infettate da virus agendo in sinergia con i linfociti T CD8, è possibile che un aumento di RANTES dovuto a ripetute riacutizzazioni virali possa favorire la distruzione del tessuto alveolare nella BPCO che, come abbiamo visto, è caratterizzata proprio da un infiltrazione di linfociti T CD8. Pertanto, come suggerito da Zhu e collaboratori, attraverso questo meccanismo le riacutizzazioni virali potrebbero favorire lo sviluppo di enfisema e quindi la perdita di funzionalità respiratoria (40), un’ipotesi rafforzata dalla recente osservazione che nei soggetti con BPCO, una maggior frequenza di riacutizzazioni è associata ad un maggior declino della funzionalità respiratoria (7). D’altra parte è stato proposto che anche le infezioni batteriche possano avere un ruolo nelle riacutizzazioni di BPCO. Questa ipotesi è avvalorata dalle osservazioni che, in corso di riacutizzazione, i livelli di IL-8 correlano con il numero di unità formanti colonie batteriche (41). Oltre alla chemochina IL-8 (o CXCL-8), anche CXCL-5 sembra avere un ruolo cruciale nel reclutamento dei neutrofili durante le riacutizzazioni di BPCO, soprattutto quelle più gravi. Infatti Qiu e collaboratori hanno recentemente dimostrato che, in pazienti con riacutizzazioni di BPCO così gravi da sviluppare insufficienza respiratoria e richiedere ventilazione meccanica invasiva, la neutrofilia era associata ad un aumento dell’espressione di CXCL-8 e ancor più di CXCL-5 (42). Poiché CXCL-5 e CXCL-8 non sono espresse nel polmone di pazienti con BPCO in fase di stabilità, è ipotizzabile che l’espressione di queste chemochine indichi l’attivazione “de novo” di una serie di eventi che porta al reclutamento dei neutrofili (43). Chiarire questi eventi che sono alla base delle riacutizzazioni di BPCO è fondamentale sia per prevenirle sia per sviluppare nuove e più efficaci terapie. Quest’obiettivo è di importanza primaria poiché è stato dimostrato che, tra i pazienti con riacutizzazioni di BPCO gravi che richiedono ricovero ospedaliero, la mortalità a due anni è del 49%, un tasso drammatico, simile a quello del tumore del polmone (44). BIBLIOGRAFIA 1. Celli BR, MacNee W. ATS/ERS Task Force: Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23: 932-946. 2. Pawels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. GOLD Scientific Committee: Global strategy for the diagnosis, management and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 2001; 163: 1256-1276. 3. Saetta M, Turato G, Maestrelli P, Mapp CE, Fabbri LM. Cellular and structural bases of chronic ostructive pulmonary disease. Am J Respir Crit Care Med 2001; 163: 1304-1309. 4. Peto R, Speizer FE, Cochrane AL, Moore F, Fletcher CM, Tinker CM, Higgins IT, Gray RG, Richards SM, Gilliland J, Norman-Smith B: The relevance in adults of air-flow obstruction, but not of mucus hypersecretion, to mortality from chronic lung disease. Results from 20 years of prospective observation. Am Rev Respir Dis 1983; 128: 491-500. 5. Vestbo J, Lange P. Can GOLD stage 0 provide information of prognostic value in chronic obstructive pulmonary disease? Am J Respir Crit Care Med 2002; 166: 329-332. 6. Vestbo J, Prescott E, Lange P. Association of chronic mucus hypersecretion with FEV1 decline and chronic obstructive pulmonary disease morbility. Copenhagen City Heart Study Group. Am J Respir Crit Care Med 1996; 153: 1530-5. 7. Donaldson GC, Seemungal TA, Bhowmik A Wedzicha JA. Relationship between exacerbation frequency and lung function decline in chronic obstructive pulmonary disease. Thorax 2002; 57:847-852. 8. Reid L. Measurement of the bronchial mucous gland layer: a diagnostic yardstick in chronic bronchitis. Thorax 1960; 15: 132-41. 9. Mullen JB, Wright JL, Wiggs BR, Pare PD, Hogg JC. Reassessment of inflammation of airways in chronic bronchitis. Br Med J (Clin Res Ed) 1985; 291: 1235-9. 10. Saetta M, Turato G, Facchini FM, Corbino L, Lucchini RE, Casoni G, Maestrelli P, Mapp CE, Ciaccia A, Fabbri LM. Inflammatory cells in the bronchial glands of smokers with chronic bronchitis. Am J Respir Crit Care Med 1997; 156: 1633-1639. 11. Jeffery PK. Comparison of the structural and inflammatory features of COPD and asthma. Chest 2000; 117: 251S-260S. 12. Saetta M, Di Stefano A, Maestrelli P, Ferraresco A, Drigo R, Potena A, Ciaccia A, Fabbri LM. Activated T-lymphocytes and macrophages in bronchial 51 52 mucosa of subjects with chronic bronchitis. Am Rev Respir Dis. 1993; 147: 301-306. 13. Di Stefano A, Turato G, Maestrelli P, Mapp CE, Ruggieri MP, Roggeri A, Boschetto P, Fabbri LM, Saetta M. Airflow limitation in chronic bronchitis is associated with T-lymphocyte and macrophage infiltration of the bronchial mucosa. Am J Respir Crit Care Med 1996; 153: 629-632. 14. O’Shaughnessy TC, Ansari TW, Barnes NC, Jeffery PK. Inflammation in bronchial biopsies of subjects with chronic bronchitis: inverse relationship of CD8+ T lymphocytes with FEV1. Am J Respir Crit Care Med 1997; 155: 852-57. 15. Di Stefano A, Maestrelli P, Roggeri A et al. Upregulation Of adhesion molecules in the bronchial mucosa of subjects with chronic obstructive bronchitis. Am j Respir Crit Care med 1994; 149: 803-810. 16. Hogg JC, Macklem PT, Thurlbeck WM. Site and nature of airway obstruction in chronic obstructive lung disease. N Engl J Med 1968; 278: 1355-60. 17. Saetta M, Di Stefano A, Turato G, Facchini FM, Corbino L, Mapp CE, Maestrelli P, Ciaccia A, Fabbri LM. CD8+ T-lymphocytes in peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998; 157: 822-6. 18. Bosken CH, Wiggs BR, Pare PD, Hogg JC: Small airway dimensions in smokers with obstruction to airflow. Am Rev Respir Dis 1990; 142: 563-570. 19. Cosio M, Ghezzo H, Hogg JC, Corbin R, Loveland M, Dosman J, Macklem PT. The relationships between structural changes in small airways and pulmonary-function tests. N Engl J Med 1978; 298: 1277-81. 20. Saetta M, Ghezzo H, Kim WD, King M, Angus CE, Wang NS, Cosio MG. Loss of alveolar attachments in smokers. A morphometric correlate of lung function impairment. Am Rev Respir Dis 1985; 132: 894-900. 21. Saetta M, Turato G, Baraldo S, Zanin A, Braccioni F, Mapp CE, Maestrelli P, Cavallesco G, Papi A, Fabbri LM. Globet cell hyperplasia and epitelial inflammation in peripheral airways of smokers with both symptoms of chronic bronchitis and airflow limitation. Am J Respir Crit Care Med 2000; 161: 1016-21. 22. Hogg JC, Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, Chermack RM, Rogers RM, Sciurba FC, Coxson HO, Pare PD: The nature of smallairway obstruction in chronic obstructive pulmonary disease. N Engl J Med 2004; 350: 2645-53. 23. Baraldo S, Turato G, Badin C, Bazzan E, Beghè B, Zuin R, Calabrese F, Casoni G, Maestrelli P, Papi A, Fabbri LM, Saetta M. Neutrophilic infiltration within the airway smooth muscle in patients with COPD. Thorax 2004; 59: 308-312. 24. Bosken CH, Hards J, Gatter K, Hogg JC. Characterization of the inflammatory reaction in the peripheral airways of cigarette smokers using immunohistochemistry. Am Rev Respir Dis 1992; 911-917. 25. Saetta M, Baraldo S, Corbino L, Turato G, Braccioni F, Rea F, Cavallesco G, Tropeano G, Mapp CE, Maestrelli P, Ciaccia A, Fabbri LM: CD8+ve cells in the lungs of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 160: 711-717. 26. Saetta M, Turato G, Baraldo S, Casoni GL, Bellettato CM, Zuin R, Rea F, Fabbri LM, Papi A. Increased proportion of CD8+ T lymphocytes in the paratracheal lymphnodes of smokers with mild COPD. Sarcoidosis Vasc Lung Dis 2003; 20: 28-32. 27. Hogg J. Pathophysiology of airflow limitation in chronic obstructive pulmonary disease. Lancet 2004: 364:709-721. 28. Saetta M, Mariani M, Panina-Bordignon P, Turato G, Buonsanti C, Baraldo S, Bellettato CM, Papi A, Corbetta L, Zuin R, Sinigaglia F, Fabbri LM: Increased expression of the chemokine receptor CXCR3 and its ligand CXCL10 in peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2002; 165: 1404-9. 29. Grumelli S, Corry D, Song L, Song L, Green L, Huh J, Hacken J, Esapda R, Bag R, Lewis D, Kheradmand F. An immune basis for lung parenchymal destruction in cronic obstructive pulmonary disease and emphysema. Plos Medicine 2004; 1:75-83. 30. Turato G, Zuin R, Miniati M, Baraldo S, Rea F, Beghe B, Monti S, Formichi B, Boschetto P, Harari S, Papi A, Maestrelli P, Fabbri LM, Saetta M. Airway inflammation in ever chronic pulmonary disease: relationship with lung function and radiologic emphysema. Am J Respir Crit Care Med 2002; 166: 105-110. 31. Standard for the diagnosis and care of patients with chronic obstructive pulmonary disease. American Thoracic Society. Am J Respir Crit Care Med 1995; 152(5 Pt 2): S77-121. 32. Vlahovic G, Russel ML, Mercer RR, Crapo JD. Cellular and connective tissue changes in alveolar septal walls in emphysema. Am J Respir Crit Care Med 1999; 160: 2086-92. 33. Lang MR, Fiaux GW, Gillooly M, Stewart JA, Hulmes DJ, Lamb D. Collagen content of alveolar wall tissue in emphysematous and non-emphysematous lungs. Thorax 1994; 49: 319-26. 34. Cosio MG, Cosio Piqueras MG. Pathology of emphysema in chronic obstructive pulmonary disease. Monaldi Arch Chest Dis 2000; 55: 124-129. 35. Retamales I, Elliott W, Meshi B, Coxson O, Parè P, Sciurba F, Rogers R, Hayashi S, Hogg J. Amplification of inflammation in emphysema and its association with latent adenoviral infection. Am J Respir Crit Care Med 2001; 164: 469-473. 36. Fabbri L, Beghe B, Caramori G, Papi A, Saetta M. Similarities and discrepancies between exacerbation of asthma and chronic obstructive pulmonary disease. Thorax 1998; 53: 803-808. 37. Crooks SW, Bayley DL, Hill SL, Stockley RA. Bronchial inflammation in acute bacterial exacerbations of chronic bronchitis: the role of leukotriene B4. Eur Respir J 2000; 15: 274-280. 38. Aaron SD, Angel JB, Lunau M, Wright K, Fex C, Le Saux N, Dales RE. Granulocyte inflammatory markers and airway infection during acute exacerbation of chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2001; 163: 349-55. 39. Saetta M, Di Stefano A, Maestrelli P, Turato G, Ruggeri MP, Roggeri A, Calcagni P, Mapp CE, Ciaccia A, Fabbri LM. Airway eosinophilia in chronic bronchitis durino exacerbations. Am J Respir Crit Care Med 1994; 150: 1646-52. 40. Zhu J, Qui YS, Majumdar S, Gamble E, Matin D, Turato G, Fabbri LM, Barnes N, Saetta M, Jeffery PK. Exacerbations of bronchitis. Bronchial eosinophilia and gene expression for interleukin-4, interleukin-5, and eosinophil chemoattractants. Am J Respir Crit Care Med. 2001; 164: 109-16 41. Patel IS, Seemungal TA, Wilks M, Lloyd-Owen SJ, Donaldson GC, Wedzicha JA. Relationsheep between bacterial colonisation and the frequency, character and severity of COPD exacerbations. Thorax 2002; 57: 759-764. 42. Qiu Y, Zhu J, Bandi V, Atmar RL, Hattotuwa K, Guntupalli KK, Jeffery PK. Biopsy neutrophilia, neutrophil chemokine and receptor gene expression in severe exacerbations of chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2003; 168: 968-975. 43. Saetta M, Baraldo S, Zuin R. Neutrophil chemokines in severe exacerbations of COPD. Fatal chemo-attraction? Am J Respir Crit Care Med 2003; 168: 1-2. 44. Connors FA, Dawson NV, Thomas C, Harrell FE, Desbiens N, Fulkerson WJ, Bellamy P, Goldman L, Knaus WA. Outcomes following acute exacerbation of severe chronic obstructive lung disease. Am J respir Crit care Med 1996; 154: 959-967. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 4. Anatomia-patologica - G. Turato, S. Baraldo, B. Beghè, R. Zuin, M. Saetta 53 5. Quadri clinici e stadiazione A cura di Anna Maria Moretti (1) e Caterina Brindicci (2) (1) (2) Struttura Complessa II° Pneumologia, Ospedale S. Paolo, Bari Royal Brompton Hospital, NHLI, Imperial College, Londra 5. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) è una patologia cronica ad alta prevalenza, caratterizzata da mortalità elevata, capacità di condizionare in modo significativo la qualità di vita dei pazienti che ne sono affetti e di determinare un ingente utilizzo di risorse sanitarie ed economiche. La BPCO, secondo le Linee Guida GOLD, è un “quadro nosologico caratterizzato da progressiva limitazione del flusso aereo non completamente reversibile, associata ad una risposta infiammatoria polmonare conseguente all’inalazione di particelle o gas nocivi” (1). Pertanto la sintomatologia, le alterazioni funzionali e le complicanze della BPCO possono trovare una spiegazione nel quadro flogistico polmonare e nelle conseguenti alterazioni anatomo-patologiche. Diagnosi e trattamento di questa patologia si sono attualmente arricchiti di nuovi ed efficaci strumenti e sono codificati da Linee Guida autorevoli supportate da solide evidenze scientifiche. Sappiamo che la diagnosi di BPCO nella popolazione generale è sottostimata, che la spirometria, metodica indispensabile per diagnosticare correttamente la BPCO e valutarne la progressione, è sottoutilizzata, che molti pazienti non ricevono un trattamento adeguato. D’altra parte, una esatta diagnosi e una corretta valutazione dei sintomi e della funzione consentono di attuare precocemente provvedimenti capaci di migliorare la qualità di vita e rallentare la progressione della patologia. Il fumo di sigaretta rappresenta il più importante fattore di rischio nell’insorgenza della BPCO. La relazione fra il fumo di sigaretta e l’infiammazione è stata studiata molto dettagliatamente (2-9), ma studi recenti dimostrano che l’infiammazione è presente anche nei polmoni dei fumatori asintomatici con caratteristiche simili per tipologia, ma di minore intensità di quella osservata nei soggetti con BPCO (10-15). Numerosi studi hanno dimostrato che altri tipi di particelle (ad esempio, gli scarichi dei motori diesel o le polveri di cereali) possono indurre infiammazione nelle vie respiratorie (16-18). È probabile che l’inquinamento degli ambienti interni, determinato dai prodotti di combustione di combustibili da biomasse, abbia effetti simili. Nel corso della BPCO le alterazioni caratteristiche sono l’ipersecrezione mucosa, la disfunzione delle ciglia, la riduzione del flusso aereo espiratorio, l’iperdistensione polmonare, le alterazioni dello scambio gassoso, l’ipertensione polmonare ed il cuore polmonare. Tali alterazioni contribuiscono all’insorgenza dei sintomi caratteristici della malattia quali tosse cronica, espettorazione e dispnea. La tosse cronica e l’espettorazione rappresentano le manifestazioni cliniche più caratteristiche dell’infiammazione bronchiale, che provoca ipersecrezione mucosa ed alterazione della clearance muco-ciliare. In corso di BPCO l’espettorato prodotto non viene totalmente eliminato a causa di una clearance inefficace. La dispnea è la percezione di un respiro alterato e la sua intensità viene influenzata da svariati fattori. Nella BPCO la dispnea è soprattutto la conseguenza di un’alterata meccanica respiratoria. Nelle fasi iniziali della malattia la dispnea compare dopo sforzo fisico, ma può essere presente anche a riposo se le alterazioni della meccanica respiratoria divengono gravi. Stadiazione La gravità della BPCO attualmente si classifica in 4 livelli e la classificazione si basa sulla riduzione del flusso aereo espiratorio, oltre che sulla presenza di sintomi caratteristici che inducono il paziente a recarsi dal medico. I livelli di gravità di patologia sono così definiti: Livello 0 (a rischio): presenza di tosse cronica ed espettorazione. La funzionalità ventilatoria, misurata con metodica spirometrica, è ancora nella norma. 55 Livello I (BPCO lieve): presenza di lieve riduzione del flusso aereo espiratorio (VEMS/CVF <70%, ma VEMS >80% del teorico) e presenza non obbligatoria di tosse ed espettorazione. In molti casi il paziente in tale stadio è asintomatico. Livello II (BPCO di media gravità): peggioramento della broncoostruzione (50% <VEMS <80% del teorico) e aggravamento dei sintomi caratteristici, con particolare riguardo alla dispnea da sforzo. Livello III (BPCO grave): ulteriore peggioramento della broncostruzione (30% <VEMS <50% del teorico), incremento della dispnea e presenza di frequenti episodi di riacutizzazione che influiscono negativamente sulla qualità di vita dei pazienti. Livello IV (BPCO molto grave): grave ostruzione bronchiale (VEMS <30% del predetto) e presenza di insufficienza respiratoria cronica definita da una pressione parziale di ossigeno arterioso (PaO2) inferiore a 60 mmHg con o senza una pressione parziale della CO2 (PaCO2) superiore a 50 mmHg e caratterizzata da manifestazioni di insufficienza cardiaca destra (cuore polmonare) quali turgore delle vene giugulari ed edemi declivi. 56 In pazienti con malattia grave, la pressione arteriosa polmonare è di solito solo modestamente aumentata a riposo, ma aumenta significativamente durante lo sforzo e, se non trattata, lentamente peggiora. Nella BPCO avanzata, la principale causa di ipertensione polmonare è l’ipossia che causa vasocostrizione delle arterie polmonari e determina rimodellamento della parete vasale (19). L’ipertensione polmonare determina lo sviluppo di cuore polmonare, caratterizzato da ipertrofia del ventricolo destro, anche se in alcuni pazienti la funzionalità ventricolare destra sembra essere conservata nonostante l’ipertensione polmonare (20). La BPCO è attualmente considerata una patologia sistemica perché si associa a manifestazioni infiammatorie a carico di altri organi o apparati, causate da stress ossidativo sistemico (21), anormale concentrazione di citochine circolanti (29) e attivazione delle cellule infiammatorie (22,24). Le alterazioni a carico dell’apparato osteo-muscolare, comprendono la perdita progressiva di massa muscolo-scheletrica e la presenza di diverse alterazioni bioenergetiche (25) che contribuiscono a limitare la tolleranza allo sforzo fisico, determinando un peggioramento delle condizioni cliniche del paziente ed un impatto negativo sulla prognosi (26). Sintomi della BPCO I sintomi della BPCO sono caratteristici e si relazionano allo stadio di malattia. Allo Stadio 0 ed allo Stadio I i sintomi caratteristici sono la tosse cronica e la produzione di escreato. Questi sintomi possono essere presenti per molti anni prima che compaiano le caratteristiche anomalie funzionali e spesso sono tenuti in scarsa considerazione dai pazienti. Nello Stadio II i pazienti iniziano a soffrire di una difficoltà respiratoria capace di interferire con le attività quotidiane e molti pazienti si rivolgono al medico in questo stadio. Il ricorso al medico curante però in molti casi si verifica solo a seguito di un peggioramento acuto in corso di un’infezione dell’apparato respiratorio. Nello Stadio III sono presenti tosse e produzione di espettorazione abbondante, accompagnati da peggioramento della dispnea. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 5. Quadri clinici e stadiazione - A. M. Moretti, C. Brindicci Tosse: la tosse cronica è di solito il primo sintomo che insorge in corso di BPCO. Il paziente, ritenendola un’inevitabile conseguenza dell’esposizione al fumo e/o a fattori ambientali, spesso la sottovaluta. All’inizio la tosse può essere occasionale, stizzosa, ma con il progredire della malattia diventa catarrale e si presenta quotidianamente, talora anche nelle ore notturne. Escreato: la regolare produzione di escreato per 3 o più mesi/anno per almeno 2 anni consecutivi rappresenta una caratteristica della definizione di bronchite cronica. L’espettorato può essere denso e presentarsi dopo accessi di tosse. È spesso difficile quantificare la produzione di escreato, perché i pazienti ne trascurano spesso un corretto esame. Dispnea: la dispnea costituisce la principale motivazione per la quale i pazienti si rivolgono al medico ed è la causa principale di invalidità ed ansia legate alla malattia. È descritta, dai pazienti affetti da BPCO, come una sensazione di aumentata fatica respiratoria e di fame d’aria. Attualmente la dispnea viene misurata in maniera semplice mediante il questionario del British Medical Research Council (MRC). Nella BPCO tale sintomo è persistente e progressivo; nelle prime fasi di malattia compare solo dopo sforzo (per esempio, salire rapidamente una rampa di scale) che il paziente tende accuratamente ad evitare. Con il progredire della malattia, la dispnea peggiora determinando un deterioramento della qualità di vita, quando il paziente realizza di avere difficoltà a svolgere attività, regolarmente svolte da soggetti della stessa età. Negli stadi avanzati della BPCO la dispnea è presente anche durante lo svolgimento delle normali attività quotidiane, quali vestirsi o lavarsi, ed in corso di insufficienza respiratoria compare anche a riposo. Sintomi sistemici: nella BPCO avanzata sono frequentemente presenti calo ponderale ed anoressia. L’emoftoe può essere presente in corso di riacutizzazioni respiratorie, ma la sua presenza deve costituire sempre motivo di approfondimento diagnostico nel sospetto di altre patologie respiratorie (TBC, neoplasia polmonare). Una tosse particolarmente intensa può talvolta essere causa di dolore toracico associato occasionalmente a fratture costali che possono decorrere asintomatiche. La depressione e l’ansia sono i sintomi psichiatrici più frequenti nei pazienti affetti da BPCO in fase avanzato. Gli edemi declivi possono rappresentare l’unico segno che indica l’insorgenza di cuore polmonare. Sintomi in corso di riacutizzazioni: le riacutizzazioni hanno un notevole impatto sulla qualità di vita del paziente, sulla evoluzione della malattia e determinano un frequente ricorso alle strutture sanitarie. Gestione della malattia Lo spettro di gravità è estremamente ampio e può variare dal lieve e transitorio incremento dei sintomi, gestibili autonomamente da parte del paziente ben istruito, fino a condizioni di estrema gravità per le quali è necessario il ricovero in unità di terapia intensiva. La decisione relativa alla opportunità di ricoverare un paziente con BPCO riacutizzata può influenzare in modo significativo sia la prognosi sia la qualità di vita del paziente. Non vi è dubbio che la gestione complessiva di una patologia cronica ad elevato impatto sociale, quale è la BPCO, necessiti dell’azione coordinata di differenti figure professionali e che non possa esaurirsi completamente né nell’ambito delle cure primarie né in quello della medicina specialistica. È fondamentale pertanto disegnare, attuare e valutare un sistema di cura che si faccia carico della malattia in tutte le sue fasi e che preveda una forte integrazione di tutte le figure professionali coinvolte. 57 58 È pertanto estremamente difficile tracciare un confine tra i livelli di competenza della Medicina generale e della Medicina specialistica. Senza dubbio allo pneumologo è affidata la supervisione dei pazienti, giunti presso le strutture ospedaliere o specialistiche territoriali, che può concludersi, dopo una valutazione clinica e strumentale (spirometria, Rx torace, emogasanalisi), con il riaffidamento al medico di Medicina generale ovvero con ricovero in DH, in reparto di degenza o in terapia intensiva. Al medico di Medicina generale è affidato il compito di identificare correttamente e tempestivamente i sintomi e segni della riacutizzazione, di valutare l’opportunità dell’attivazione dell’assistenza domiciliare integrata o del ricovero ospedaliero, di gestire, in collaborazione con lo specialista, il trattamento domiciliare dopo l’eventuale ricovero. Le Linee Guida GOLD evidenziano che “I soggetti che presentano tosse cronica ed escreato ed una storia di esposizione a fattori di rischio dovrebbero essere studiati, anche se non riferiscono dispnea, per valutare la presenza di una riduzione del flusso aereo espiratorio”. I soggetti con fattori di rischio (soprattutto fumo di tabacco), potrebbero avere già un danno funzionale anche se non riferiscono una sintomatologia evidente. In questa categoria di soggetti la presenza di tosse cronica, espettorazione o dispnea va ricercata attivamente in quanto spesso tali sintomi vengono sottovalutati e sottaciuti dal paziente perché considerati naturale conseguenza del proprio stato di fumatore. Nello screening dei soggetti con possibile BPCO e nella valutazione di gravità di malattia, un ruolo strategico è affidato pertanto alla corretta ricerca dei sintomi ed alla gestione degli stessi da parte dello specialista pneumologo e del medico di Medicina generale perché questo tipo di intervento rappresenta una delle attività più caratteristiche e rilevanti dal punto di vista della qualità dell’assistenza. BIBLIOGRAFIA 1. Celli BR, MacNee W. ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J. 2004 Jun;23(6):932-46. 2. Wright JL, Lawson LM, Pare PD, Wiggs BJ, Kennedy S, Hogg JC. Morphology of peripheral airways in current smokers and exsmokers. Am Rev Respir Dis 1983; 127: 474-7. 3. McLean KA. Pathogenesis of pulmonary emphysema. Am J Med 1958; 25: 62-74. 4. Niewoehner DE, Kleinerman J, Rice DB. Pathologic changes in the peripheral airways of young cigarette smokers. N Engl J Med 1974; 291: 755-8. 5. Auerbach O, Garfinkel L, Hammond EC. Relation of smoking and age to findings in lung parenchyma: a microscopic study. Chest 1974; 65: 29-35. 6. Auerbach O, Hammond EC, Garfinkel L, Benante C. Relation of smoking and age to emphysema. Whole-lung section study. N Engl J Med 1972; 286: 853-7. 7. Gadek JE, Fells GA, Crystal RG. Cigarette smoking induces functional antiprotease deficiency in the lower respiratory tract of humans. Science 1979; 206: 1315-6. 8. Stone PJ, Calore JD, McGowan SE, Bernardo J, Snider GL, Franzblau C. Functional α 1-protease inhibitor in the lower respiratory tract of cigarette smokers is not decreased. Science 1983; 221: 1187-9. 9. Hunninghake GW, Crystal RG. Cigarette smoking and lung destruction. Accumulation of neutrophils in the lungs of cigarette smokers. Am Rev Respir Dis 1983; 128: 833-8. 10. Keatings VM, Collins PD, Scott DM, Barnes PJ. Differences in interleukin-8 and tumor necrosis factor-α in induced sputum from patients with chronic obstructive pulmonary disease or asthma. Am J Respir Crit Care Med 1996; 153: 530-4. 11. Thompson AB, Daughton D, Robbins RA, Ghafouri MA, Oehlerking M, Rennard SI. Intraluminal airway inflammation in chronic bronchitis. Characterization and correlation with clinical parameters. Am Rev Respir Dis 1989; 140: 1527-37. 12. Stockley RA. Neutrophils and the pathogenesis of COPD. Chest 2002; 121: 151S-155S. 13. Peleman RA, Rytila PH, Kips JC, Joos GF, Pauwels RA. The cellular composition of induced sputum in chronic obstructive pulmonary disease. Eur Respir J 1999; 13: 839-43. 14. Speizer FE, Tager IB. Epidemiology of chronic mucus hypersecretion and obstructive airways disease. Epidemiol Rev 1979; 1: 124-42. 15. Turato G, Di Stefano A, Maestrelli P, Mapp CE, Ruggieri MP, Roggeri A, et al. Effect of smoking cessation on airway inflammation in chronic bronchitis. Am J Respir Crit Care Med 1995; 152: 1262-7. 16. Monn C, Becker S. Cytotoxicity and induction of proinflammatory cytokines from human monocytes exposed to fine (PM2.5) and coarse particles (PM10-2.5) in outdoor and indoor air. Toxicol Appl Pharmacol1999; 155: 245-52. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 5. Quadri clinici e stadiazione - A. M. Moretti, C. Brindicci 17. Salvi S, Blomberg A, Rudell B, Kelly F, Sandstrom T, Holgate ST, et al. Acute inflammatory responses in the airways and peripheral blood after short-term exposure to diesel exhaust in healthy human volunteers. Am J Respir Crit Care Med 1999; 159: 702-9. 18. Von Essen SG, Robbins RA, Thompson AB, Ertl RF, Linder J, Rennard SI. Mechanisms of neutrophil recruitment to the lung by grain dust exposure [published erratum appears in Am Rev Respir Dis 1989; 139:1065]. Am Rev Respir Dis 1988; 138: 921-7. 19. Knighton DR, Hunt TK, Scheuenstuhl H, Halliday BJ, Werb Z, Banda MJ. Oxygen tension regulates the expression of angiogenesis factor by macrophages. Science 1983; 221: 1283-5. 20. Biernacki W, Flenley DC, Muir AL, MacNee W. Pulmonary hypertension and right ventricular function in patients with COPD. Chest 1988; 94: 1169-75. 21. Rahman I, Morrison D, Donaldson K, MacNee W. Systemic oxidative stress in asthma, COPD, and smokers. Am J Respir Crit Care Med 1996; 154: 1055-60. 22. Schols AM, Buurman WA, Staal van den Brekel AJ, Dentener MA, Wouters EF. Evidence for a relation between metabolic derangements and increased levels of inflammatory mediators in a subgroup of patients with chronic obstructive pulmonary disease. Thorax 1996; 51: 819-24. 23. Sauleda J, Garcia-Palmer FJ, Gonzalez G, Palou A, Agusti AG. The activity of cytochrome oxidase is increased in circulating lymphocytes of patients with chronic obstructive pulmonary disease, asthma, and chronic arthritis. Am J Respir Crit Care Med 2000; 161: 325. 24. Sauleda J, Garcia-Palmer F, Wiesner RJ, Tarraga S, Harting I, Tomas P, et al. Cytochrome oxidase activity and mitochondrial gene expression in skeletal muscle of patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998; 157: 1413-7. 25. American Thoracic Society and European Respiratory Society. Skeletal muscle dysfunction in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 159: S1-40. 26. Schols AM, Slangen J, Volovics L, Wouters EF.Weight loss is a reversible factor in the prognosis of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998; 157: 1791-7. 59 6. Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale A cura di Roberta Poggi (1) e Andrea Rossi (2) Unità di Struttura Complessa di Pneumologia, Azienda Ospedaliera Ospedale Maggiore di Borgo Trento, Verona (2) Unità di Struttura Complessa di Pneumologia, Azienda Ospedaliera Ospedali Riuniti, Bergamo (1) 6. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) è una delle poche malattie respiratorie che contiene nella definizione un commento sulle sue caratteristiche di funzionalità respiratoria e precisamente sulla riduzione dei flussi espiratori forzati. La fisiopatologia della BPCO è un argomento davvero complesso ma molto interessante (1), perché la malattia è assai eterogenea in termini di presentazione clinica e fisiopatologica. Sono presenti infatti contemporaneamente anomalie della meccanica del polmone e della gabbia toracica, alterazioni dello scambio gassoso, ma anche della struttura e della funzione dei muscoli respiratori e scheletrici, nonché aspetti sistemici (2). Probabilmente l’origine della malattia è l’infiammazione delle vie aeree, per una esagerata riposta all’inalazione di agenti nocivi come il fumo di sigaretta o l’aria inquinata (3). Gli eventi finali sono la grave inabilità fisica e la morte prematura del paziente. In questa complessità la “limitazione di flusso” è un elemento centrale che unisce i danni biologici e fisiopatologici alle manifestazioni cliniche. In definitiva la limitazione di flusso è il meccanismo chiave che determina la dispnea, la progressiva inabilità ed infine l’insufficienza ventilatoria nei pazienti con BPCO. La comprensione della fisiopatologia della limitazione di flusso è quindi un passo essenziale per mettere in atto efficaci interventi farmacologici, riabilitativi e di modificazioni nello stile di vita (4). Lo scopo di questo capitolo è di puntualizzare la differenza tra broncoostruzione e limitazione di flusso e la loro relazione con l’iperinflazione polmonare e le manifestazioni cliniche. È nostra convinzione, e fortunatamente non solo nostra, che ostruzione delle vie aeree/flusso aereo e limitazione di flusso non dovrebbero essere usati come sinonimi. L’acronimo BPCO caratterizza la patologia con il termine di “ostruttiva”. Tuttavia, in alcune recenti Linee Guida (5) viene utilizzato il termine di “ostruzione del flusso aereo”, mentre in altre (4,6) si preferisce il termine di “limitazione del flusso aereo”. Nella prima definizione (ostruzione) si sottolinea come il risultato finale, indipendentemente dal meccanismo fisiopatologico, sia una riduzione del calibro delle vie aeree con conseguente ritardo nel flusso espiratorio. Con il termine “limitazione” si pone invece in rilievo come l’ostruzione delle vie aeree, dovuta alla flogosi della parete bronchiale e all’ipersecrezione di muco, rallenti il flusso aereo ma a ciò si associ la perdita di retrazione elastica del polmone (quindi della pressione di spinta) e la distruzione dei setti alveolari responsabili del sostegno delle piccole vie aeree. L’ostruzione delle vie aeree e la perdita di retrazione elastica del polmone contribuiscono entrambi alla presenza e al grado di limitazione di flusso (7). Un possibile problema legato all’uso del termine “limitazione di flusso espiratorio” è l’implicazione di una condizione di “flusso espiratorio illimitato” che non esiste neppure nelle migliori condizioni fisiologiche. I soggetti normali, ad esempio, non sono limitati nel flusso a riposo ma possono divenirlo durante l’esercizio quando vi sia un incremento della ventilazione. Molti fisiologi preferiscono restringere la definizione di limitazione di flusso espiratorio alla condizione in cui il flusso espiratorio non può aumentare ad un dato volume polmonare anche in presenza di una forte attivazione dei muscoli espiratori, poiché il volume corrente si trova già a coincidere con i flussi espiratori massimi, ottenuti, ad esempio su una curva flusso volume da una espiratoria forzata. Rapporti struttura-funzione La BPCO è conseguenza di una risposta infiammatoria abnorme all’inalazione di agenti nocivi come il fumo di sigaretta, agenti occupazionali ed inquinamento atmosferico. Anche fattori individuali, attualmente poco noti, hanno un ruolo rilevante. Si stima che una percentuale variabile dal 15% al 40% dei grandi fumatori sviluppi una malattia clinicamente evidenziabile. La patogenesi e la fisiopatologia della BPCO sono state ampiamente indagate con un progressivo miglioramento delle nostre conoscenze scientifiche sui meccanismi della malattia. Hogg et al. nei 61 62 loro primi lavori (8) ponevano già in correlazione funzione e variazioni strutturali nella BPCO e concludevano che la sede principale dell’ostruzione al flusso era nelle piccole vie e cioè nei bronchioli con un diametro interno inferiore a 2 mm, e che la causa di quell’ostruzione era l’abbondante produzione di muco, la fibrosi, il restringimento e l’obliterazione delle piccole vie. La misura delle resistenze polmonari e la loro ripartizione in periferiche e centrali venne fatta con la tecnica del catetere periferico. Hogg et al. (8) dimostrarono che estese modificazioni patologiche nelle piccole vie aeree avvenivano nei pazienti con BPCO senza importanti anomalie funzionali sia nella spirometria sia nelle resistenze polmonari totali (9). Ciò era dovuto alla scarsa influenza delle resistenze delle vie periferiche sulle resistenze totali. Nel suo classico editoriale Mead (10) definì le piccole vie come “la zona silente” proprio perché una estesa patologia nelle vie aeree periferiche poteva svilupparsi in soggetti peraltro asintomatici. Tuttavia, il parenchima a valle delle piccole vie ostruite doveva comunque essere ventilato tramite canali collaterali così che la distribuzione della ventilazione veniva ad essere marcatamente anormale e conseguentemente anche gli scambi gassosi. Trent’anni più tardi questo dato è stato confermato da Barbera et al. (11) con la tecnica MIGET (multiple inert gas expiratory technique) dimostrando che la disomogeneità della distribuzione di ventilazione e perfusione erano entrambe determinate dalle anomalie delle piccole vie e dalla distruzione di parenchima con scarsa correlazione tra le misure della distribuzione del rapporto ventilazione-perfusione ed il valore di FEV1. Dieci anni dopo il lavoro di Hogg et al. (13), Cosio et al.(12) pubblicarono uno studio sulla correlazione tra modificazioni strutturali delle piccole vie ed i test di funzionalità respiratoria. Esaminando biopsie polmonari di fumatori con lesioni polmonari localizzate, trovarono che la lesione primaria era una progressiva infiammazione che portava a fibrosi con deposito di tessuto connettivo nelle piccole vie aeree. Quelle lesioni potevano essere rivelate da misure funzionali più sensibili come la capacità di chiusura (closing capacity), il volume di isoflusso e la curva della fase III del washout del singolo respiro. Questi test dimostravano valori anomali quando la variazioni patologiche erano ancora potenzialmente reversibili e quando altri test più comunemente utilizzati, come la spirometria, non rilevavano cambiamenti significativi. Qualche anno dopo un gruppo di ricercatori giapponesi evidenziava come alcuni pazienti con asma e tutti i pazienti con BPCO avessero un incremento delle resistenze totali dovuto ad un aumento sia delle resistenze centrali sia periferiche, ma mentre le prime aumentavano del 50% in media, le resistenza delle piccole vie aumentavano di 5 volte. Ulteriori informazioni sulla natura dell’ostruzione delle piccole vie aeree nella BPCO sono state ricavate da uno studio su 159 pazienti con BPCO grave (secondo la classificazione GOLD) sottoposti a resezione chirurgica di tessuto polmonare (13). Hogg et al. (13) hanno dimostrato che la progressione della BPCO era associata ad accumulo di essudato infiammatorio nel lume e ad infiltrato di cellule infiammatorie immunitarie nella parete bronchiale e che vi era una significativa correlazione tra le alterazioni patologiche delle piccole vie e la classificazione di gravità delle Linee Guida GOLD. In conclusione quindi vi sono ampie conferme che le anomalie patologiche a carico delle piccole vie hanno un ruolo rilevante nella patogenesi della BPCO (14), ed in particolare che l’infiammazione delle piccole vie aeree è un determinante essenziale dell’ostruzione al flusso e della progressione e gravità della malattia (3). È noto da molti anni che il maggior determinante della riduzione del flusso espiratorio nell’enfisema è la perdita di forza di retrazione elastica del polmone (15). Sebbene la meccanica della ritardata espirazione si spieghi con la presenza di una ridotta pressione di spinta, il meccanismo biologico che sta alla base della relazione fra perdita di tessuto e riduzione del flusso espiratorio non è altrettanto chiaro. Un gruppo di ricercatori (16) ha dimostrato che la perdita dei setti inter-alveolari è correlata alla riduzione del flusso espiratorio forzato e che tale perdita è in relazione con l’infiammazione nella periferia del polmoni. Kim et al. (16) hanno riportato che l’infiammazione ed il ri- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 6. Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale - R. Poggi, A. Rossi modellamento delle vie aeree e del parenchima sono diversi nei polmoni con enfisema centrolobulare e panlobulare. Nell’enfisema centrolobulare le vie aeree sono più strette e ispessite di quello panlobulare, essendo il primo caratteristico dei fumatori e l’altro maggiormente correlato al deficit di α-1-antitripsina (17). Diagnosi di BPCO Il sospetto diagnostico di BPCO è fondato sul riscontro di: - fattori di rischio come il fumo di sigaretta, esposizioni professionali, inquinamento urbano e domestico; - presenza di sintomi come la tosse cronica con espettorato, la dispnea durante esercizio; - riscontro di segni come alterazioni della configurazione toracica, rumori polmonari patologici. La diagnosi di BPCO necessita invece di conferma per mezzo dell’esame spirometrico. Indipendentemente dal fatto che venga utilizzato il termine ostruzione o limitazione, tutte le Linee Guida nazionali ed internazionali indicano il FEV1 (o VEMS, volume espiratorio forzato in un secondo) come il parametro funzionale di riferimento per la diagnosi, la valutazione di gravità ed il monitoraggio della BPCO (GOLD). Il FEV1 viene misurato sul tracciato volume/tempo o flusso/volume di una manovra espiratoria forzata dal punto di massima inspirazione all’espirazione completa alla massima velocità possibile. Si misura anche la capacità vitale forzata (FVC). Un valore del rapporto FEV1 /FVC <70% dopo broncodilatatore, indipendentemente da età, sesso, razza, altezza e peso, è indicativo di BPCO (4,6). Nonostante il limite di identificare un valore assoluto, vi è un generale consenso sul fatto che sia necessario un mezzo semplice per ovviare all’ampia sottodiagnosi di BPCO, malattia che ha un grave impatto sulla salute pubblica (18). Alcuni anni addietro le Linee Guida dell’European Respiratory Society (6) sulla BPCO indicavano come parametro diagnostico di BPCO un rapporto FEV1 /VC <88% e 89% del predetto rispettivamente per maschio e femmina, ma la misura di questo parametro (noto come indice di Tiffenau) richiedeva due manovre di espirazione completa, una lenta e una forzata, con una evidente restrizione sulla possibilità di uso massificato della spirometria. Il valore di FEV1 viene attualmente suggerito per stadiare la gravità della BPCO come segue: FEV1 % predetto > 80% lieve 1 FEV % predetto <80% >50% moderata FEV1 % predetto <50% >30% severa molto severa FEV1 % predetto <30% In questo contesto è da ricordare l’interessante relazione recentemente sottolineata da Hogg et al. (13) tra alcune modificazioni infiammatorie delle piccole vie aeree e la stadiazione di BPCO sopra riportata. Dopo la pubblicazione di Fletcher et al. (19) il FEV1 viene utilizzato anche per valutare la progressione di malattia, in quanto risulta accelerato nei soggetti fumatori e con BPCO. L’accelerato declino del FEV1 porta a invalidità e morte prematura. La cessazione del fumo rallenta il declino del FEV1 ad ogni età. È comunque necessario ricordare che i valori di FEV1 e FVC sono entrambi influenzati dalla velocità dell’inspirazione che precede l’espirazione forzata e dalla presenza e durata della pausa di fine inspirazione. Se la manovra di espirazione forzata è preceduta da una lenta inspirazione con una lunga (4-5 sec) pausa inspiratoria, i flussi espiratori sono inferiori a quelli ottenuti con un’espirazione forzata preceduta da un’inspirazione massimale veloce e senza pausa di fine inspiratoria (20). Quindi la manovra di espirazione forzata della spirometria deve essere standardizzata. 63 Per ottenere i flussi massimali l’inspirazione deve essere effettuata a massima velocità e seguita immediatamente dall’espirazione forzata senza pause (20). Corrispondenza tra ostruzione e limitazione 64 Un approccio semplice potrebbe essere quello di considerare la limitazione di flusso come una forma di broncoostruzione grave delle vie aeree. La limitazione di flusso non è tuttavia correlata con il grado di ostruzione delle vie aeree valutato e classificato con la misura del FEV1. Questa interessante osservazione è stata fatta da Eltayara et al. (21) che hanno paragonando il valore di FEV1 con i risultati della tecnica della NEP (negativ expiratory pressure), in una popolazione di BPCO a diversi stadi di gravità. Il valore di “flow limitation” valutato con la NEP non era assolutamente correlato con il valore di FEV1 a riposo. Un primo fattore per questa mancata associazione può essere legata a problemi metodologici della NEP. Tuttavia, è necessario considerare che fattore predominante della limitazione di flusso è la distruzione parenchimale con riduzione del ritorno elastico del polmone, mentre il FEV1 è influenzato in modo importante anche dalla contrazione della muscolatura liscia e dell’ispessimento della parete bronchiale. Ad esempio una grave broncocostrizione può determinare una evidente broncoostruzione, ma senza limitazione del flusso perché la broncocostrizione rende le vie aeree più rigide e quindi non compressibili durante l’espirazione forzata. Una più completa valutazione funzionale della BPCO si avvale della misura dei volumi polmonari che permettere l’identificazione e la distinzione di un alterazioni di tipo ostruttivo o restrittivo. La capacità polmonare totale (CPT) risente soprattutto delle caratteristiche delle proprietà elastiche del polmone. Modificazioni della CPT richiedono tempo, oppure una grave ostruzione acuta come può avvenire nell’attacco asmatico grave. Una misura recentemente rivalutata e assai semplice da eseguire è la capacità inspiratoria (IC), somma del volume corrente più il volume di riserva inspiratorio (22). La IC è lo specchio della capacità funzionale residua (CFR) e delle sue variazioni. Il valore di IC è significativamente correlata sia con la dispnea che con la tolleranza all’esercizio fisico (22,23), sì da essere un buon predittore della capacità individuale di attività fisica più del valore di FEV1. Inoltre risulta un buon predittore del volume corrente massimo durante esercizio e quindi della ventilazione massimale. La IC riflette infatti la reale riserva inspiratoria, particolarmente nei pazienti che non possono utilizzare la riserva espiratoria a causa della limitazione di flusso. Alcuni studi hanno dimostrato che, nella maggior parte dei pazienti con BPCO e con limitazione di flusso a riposo, la IC è più bassa dei soggetti normali e che, nei pazienti BPCO stabili con “flow limitation” a riposo, vi è una correlazione significativa tra la ridotta IC e la presenza di ipercapnia. Considerate le importanti conseguenze dell’iperinflazione polmonare statica nella BPCO, è stato recentemente proposto l’indice IC/TLC nella valutazione di questi pazienti. Uno studio condotto su una coorte di 689 pazienti BPCO in un periodo di 34 mesi ha individuato la riduzione del rapporto IC/TLC come importante predittore di mortalità per cause respiratorie indipendente da altri fattori (24). Limitazione di flusso ed iperinflazione polmonare La conseguenza maggiore dell’ostruzione delle vie aeree è l’aumento del lavoro respiratorio (lavoro resistivo), mentre la maggior conseguenza della limitazione di flusso è l’iperinflazione polmonare. Quest’ultima incrementa il lavoro respiratorio perché sposta la ventilazione polmonare nella porzione alta e più piatta della curva pressione-volume, dove la compliance è minore (lavoro elastico). L’iperinflazione polmonare è definita come un aumento della quantità di aria che rimane nei polmoni alla fine di un’espirazione corrente (capacità funzionale residua, CFR). La CFR nei soggetti normali corrisponde al punto di equilibro elastico, circa il 40% della CPT. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 6. Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale - R. Poggi, A. Rossi Iperinflazione polmonare statica: nei pazienti con BPCO, il punto di equilibrio elastico del sistema respiratorio si stabilisce a volumi più alti rispetto ai normali ed è la conseguenza alla perdita di retrazione elastica del polmone. Iperinflazione polmonare dinamica: è la conseguenza principale del ritardato flusso espiratorio per la limitazione di flusso e l’ostruzione delle vie aeree nei pazienti BPCO, inizialmente durante esercizio e in seguito anche a riposo. In presenza di un ritardato flusso espiratorio, il tempo tra due successive inspirazioni non è sufficiente perché l’apparato respiratorio si svuoti al punto di equilibrio elastico. In queste condizioni, lo sforzo inspiratorio inizia prima della fine dell’espirazione, quando la pressione alveolare è ancora positiva. Chiaramente quella pressione positiva deve essere controbilanciata dalla contrazione dei muscoli inspiratori perché si crei una pressione subatmosferica nelle vie aeree centrali ed inizi il flusso inspiratorio. La pressione alveolare positiva di fine espirazione è stata definita “intrinsic positive end-expiratory pressure” (PEEPi). Questa costituisce una pressione di soglia inspiratoria che aumenta ulteriormente il carico meccanico della ventilazione, aggiungendosi al maggiore lavoro resistivo ed elastico. La PEEPi è sempre associata con una FRC superiore al punto di equilibrio elastico. Entrambi i meccanismi, statico e dinamico, contribuiscono all’iperinflazione polmonare nella BPCO. L’iperinflazione polmonare compromette le proprietà forza-lunghezza delle fibre dei muscoli inspiratori e l’arrangiamento geometrico del diaframma con una riduzione importante sia della capacità di generare pressione sia dell’azione sull’area di apposizione che viene significativamente ridotta nella ventilazione ad alti volumi polmonari (25). L’iperinflazione polmonare ed insufficienza ventilatoria L’iperinflazione polmonare svolge quindi un ruolo rilevante nella patogenesi dell’insufficienza respiratoria della BPCO. In breve la riacutizzazione grave di BPCO provoca un incremento delle resistenze delle vie aeree e un aumento del lavoro respiratorio e dell’intrappolamento d’aria. Quest’ultimo peggiora l’iperinflazione polmonare e rende incapaci i muscoli respiratori di supportare il più grande carico ventilatorio. L’aumento compensatorio di attività del centro respiratorio può essere in questo caso deleterio in quanto l’aumento della frequenza respiratoria con un respiro rapido e superficiale peggiora l’iperinflazione polmonare ed è inefficace nell’eliminare la CO2. Tuttavia, l’aumento della frequenza a scapito della profondità della respirazione appare come l’unico modo per difendere i muscoli respiratori dalla fatica e per prevenire l’esaurimento della pompa ventilatoria. Tuttavia, l’aumento di PaCO2 aggraverà progressivamente l’acidosi che diverrà gravissima se non vi sarà un intervento tempestivo con il supporto ventilatorio meccanico. Dispnea Uno dei sintomi più debilitanti per i pazienti con BPCO è la dispnea, definita come una spiacevole sensazione di difficoltà respiratoria, sebbene anche la tosse e l’espettorato possano complicare la vita sociale di questi pazienti ed essere associate con un accelerato declino del FEV1 (26). La dispnea inizialmente è associata all’esercizio e in seguito si presenta anche durante le attività meno pesanti. La gravità della dispnea è in relazione individualmente modesta con il grado di broncoostruzione ed è influenzata anche dalla presenza di comorbidità quali patologie cardiovascolari, stati nutrizionali carenziali (2) e diversi stili di vita dei pazienti. Tantucci et al. (27) e Diaz et al. (23) confrontando in senso strettamente fisiologico pazienti con e senza limitazione di flusso hanno dimostrato che i primi tollerano un esercizio minore rispetto ai secondi anche in presenza di grave broncoostruzione. Durante l’esercizio fisico infatti, l’aumento di 65 ventilazione richiesto dal maggiore metabolismo è fronteggiato dal reclutamento dei muscoli espiratori e dall’utilizzazione del volume di riserva espiratorio oltre che della riserva inspiratoria. In presenza di limitazione del flusso espiratorio, l’attivazione dei muscoli espiratori è inefficace perché i flussi espiratori sono già massimali. È utilizzabile solo la riserva inspiratoria. Inoltre per ottenere maggiori flussi, la ventilazione deve essere spostata in una zona della curva flusso-volume dove questo sia possibile, cioè a più elevati volumi polmonari dove il flusso espiratorio non è limitato. La maggiore ventilazione richiesta dall’esercizio fisico è quindi associata, nei pazienti con limitazione del flusso espiratorio, ad iperinflazione polmonare dinamica e conseguentemente ad una più precoce comparsa della dispnea, rispetto ai pazienti senza limitazione del flusso a volume corrente. Naturalmente, l’iperinflazione dinamica nell’esercizio fisico ha le stesse caratteristiche di aumento del carico meccanico (maggiore lavoro elastico e resistivo e carico soglia della PEEPi) e di riduzione della capacità dei muscoli inspiratori di generare pressione, del meccanismo che guida all’insufficienza ventilatoria. Diagnosi differenziale tra asma bronchiale e BPCO Confrontando i due estremi di una ideale curva di distribuzione dell’asma e della BPCO sulla popolazione generale, non è difficile estrapolare una semplice tabella che dimostri con grande facilità la diagnosi differenziale tra le due malattie. (tab. 1) Tabella 1 – Diagnosi differenzile tra asma e BPCO 66 CARATTERISTICA ASMA BPCO Età Atopia Fumo Dispnea Spirometria IBA °°° giovane ++++ — (+) accessionale normale ° ++++ medio-anziana —— ++++ da sforzo FEV1 /FVC<0,7 °° —++ ° nei periodi intercritici; °° dopo broncodilatatore; °°° iperreattività bronchiale aspecifica. In realtà esiste una vasta area grigia in cui le differenze tra le due malattie ed i due gruppi di pazienti non sono così nette, soprattutto se l’asma si manifesta per la prima volta in età post-giovanile. Allora, la dispnea può essere da sforzo, le crisi accessionali possono essere non intensissime, l’atopia è sfumata o poco correlata ai sintomi, vi può essere anamnesi di fumo. Sia l’asma sia la BPCO sono malattie respiratorie con un’importante prevalenza nella popolazione generale, per cui è possibilissimo che un soggetto sia affetto da entrambe, come può accadere per l’ipertensione arteriosa e le cardiopatie o il diabete etc. Tuttavia, l’asma conserva una caratteristica che non è costante nella BPCO, cioè la larga reversibilità dell’ostruzione. Se questa reversibilità è completa, cioè se i valori spirometrici, misurati prima del broncodilatatore, dimostrano una condizione di ostruzione delle vie aeree mentre dopo broncodilatatore ritornano nei limiti di norma, la diagnosi più probabile è di asma bronchiale. Se la reversibilità è importante, ad esempio un aumento >25% di FEV1 dopo broncodilatatore rispetto al basale, ma il valore del FEV1 postbroncodilatore rimane al di sotto dei limiti di norma, la diagnosi più probabile è: “Asma bronchiale. BPCO”, ricordando la “dutch hypothesis” menzionata precedentemente. In sintesi, la diagnosi di asma richiede la dimostrazione spirometrica di un’ostruzione in larga misura potenzialmente reversibile. Altri test, come la misura dell’iperreattività bronchiale specifica mediante il test alla metacolina e/o la misura dell’ossido nitrico (NO) esalato (28), possono essere utili, ma hanno dei limiti che devono essere ben conosciuti per evitare errori di interpretazione sia nel senso della sensibilità che della Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 6. Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale - R. Poggi, A. Rossi specificità. Sia l’iperreattività bronchiale aspecifica sia l’aumentata concentrazione di NO nell’aria esalata esistono in soggetti non asmatici, anche se negli asmatici il fenomeno può essere (non costantemente) quantitativamente più rilevante (29). Una recente pubblicazione valorizza l’uso della misura di NO esalato più della iperreattività bronchiale nella diagnosi di asma (30). Tuttavia, si tratta di conclusioni su piccoli gruppi in laboratorio che vanno certamente confrontate con indagini su ben più vaste popolazioni. Si può quindi sintetizzare che: - in presenza di un chiaro fenotipo clinico, la diagnosi differenziale tra asma bronchiale e BPCO non presenta insormontabili difficoltà; - nell’area grigia, oltre al quadro clinico è importante l’evidenza spirometrica con documentazione del grado di reversibilità dell’ostruzione. Conclusioni La BPCO è una patologia complessa per la cui completa comprensione sono necessari ulteriori studi, particolarmente sul rapporto struttura-funzione. Per quanto finora conosciuto, i termini “ostruzione delle vie aeree” e “limitazione di flusso” sono spesso utilizzati come sinonimi ma hanno significati diversi nella fisiopatologia della BPCO. Tali differenze hanno notevole rilevanza per le implicazioni cliniche in termini di tolleranza all’esercizio e rischio di insufficienza ventilatoria. La sede principale del danno che porta alla limitazione di flusso sono le piccole vie e l’infiammazione è il meccanismo eziopatogenetico associato alla distruzione del parenchima che determina perdita di retrazione elastica del polmone e dei legami alveolari che supportano le vie aeree intratoraciche. La conseguenza principale della limitazione di flusso è l’iperinflazione polmonare che oltre ad incrementare il lavoro respiratorio induce importanti modificazioni nell’attività dei muscoli respiratori e favorisce l’insufficienza ventilatoria. Per la diagnosi di BPCO è necessaria la spirometria ma la misura dei volumi polmonari è importante per una maggior comprensione della fisiopatologia dei pazienti con BPCO. Risulta inoltre molto utile la misura della IC (semplice e ricca di informazioni) per spiegare manifestazioni cliniche quali la dispnea e predire la tolleranza all’esercizio. BIBLIOGRAFIA 1. Pride NB, Milic-Emili J. Lung mechanics. In Calverley P, Pride NB (Eds): Chronic Obstructive Lung Disease. Chapman Hall, London, UK 1995, 135-160. 2. Celli BR, Cote CG, Marin JM, Casanova C, Montes de Oca M, Mendez RA, Pinto Plata V, Cabral HJ. The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med 350:1005-1012, 2004. 3. Barnes PJ. Small airways in COPD. N Engl J Med 350: 2635-2637, 2004. 4. Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. The GOLD Scientific Committee. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 163: 1256-1276, 2001. 5. BTS guidelines for the management of chronic obstructive pulmonary disease. The COPD Guidelines Group of the Standards of Care Committee of the BTS (British Thoracic Society). Thorax 52: S1-S28, 1997. 6. Celli BR, MacNee W. ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 23: 932-946, 2004. 7. Hyatt RE. Forced expiration. In: Macklem, PT, J. Mead (Eds.), Handbook of physiology, Section 3: The Respiratory System. Mechanics of breathing, Part 1, vol. III. American Physiological Society, Bethesda, Maryland, (chapt. 19): pp. 295-314, 1986. 8. Hogg JC, Macklem PT, Thurlbeck WM. Site and nature of airway obstruction in chronic obstructive lung disease. New Engl. J. Med. 278: 1355-1360, 1968. 9. Mead J, Whittenberger JL. Evaluation of airway interruption technique as a method for measuring pulmonary air-flow resistance. J Appl Physiol 6: 408-416, 1954. 10. Mead J. The lung’s “quiet zone”. N Engl J Med 282: 1318-1319, 1970. 11. Barbera JA, Roca J, Ferrer A, Felez MA, Diaz O, Roger N, Rodriguez-Roisin R. Mechanisms of worsening gas exchange during acute exacerbations of chronic obstructive pulmonary disease. Eur Respir J 10: 1285-1291, 1997. 67 68 12. Cosio M, Ghezzo H, Hogg JC, Corbin R, Loveland M, Dosman J, Macklem PT. The relations between structural change in small airways and pulmonary function tests. N Engl J Med 298: 1277-1281, 1978. 13. Hogg JC,Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, Cherniack RM, Rogers RM, Sciurba FC, Coxson HO,Paré PD. The nature of small airway obstruction in chronic obstructive pulmonary disease. N Engl J Med 350: 2645-2653, 2004b. 14. Calverlay PMA, Walker P. Chronic Obstructive Pulmonary disease. The Lancet 362: 1053-1061, 2003. 15. Mead J, Turner JM, Macklem PT, Little JB. Significance of the relationship between lung recoil and maximum expiratory flow. J. Appl. Physiol. 22 : 95-108, 1967. 16. Kim WD, Eidelman DH, Izquierdo JL, Ghezzo H, Saetta MP, Cosio MG. Centrilobular and panlobular emphysema in smokers. Am Rev Respir Dis 144:1385-1390, 1991. 17. Finkelstein R, Ma H-D, Ghezzo H,Whittaker K, Fraser RS, Cosio MG. Morphometric of small airway in smokers and its relationship to emphysema type and hyperresponsiveness. Am J Respir Crit Care Med 152: 267-276, 1995. 18. European Lung White Book. The first comprehensive survey on respiratory health in Europe. European Respiratory Society Journals, The Charlesworth Group, Huddersfield, UK, 2003. 19. Fletcher C, Peto R. The natural history of chronic airflow obstruction. Br Med J. 1: 1645-1648, 1977. 20. Milic-Emili J. Recent advances in spirometry and flow-volume loop. Seminars in Respiratory and Critical Care Medicine 19(4): 309-316, 1998. 21. Eltayara L, Becklake MR, Volta CA, Milic-Emili J. Relationship between chronic dyspnea and expiratory flow limitation in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 154: 1726-1734, 1996. 22. Diaz O, Villafranca C, Ghezzo H, Borzone G, Leiva A, Milic-Emili J, Lisboa C. Role of inspiratory capacity on exercise tolerance in COPD patients with and without tidal expiratory flow limitation at rest. Eur Respir J 16: 269-275, 2000. 23. Diaz O, Villafranca C, Ghezzo H, Borzone G, Leiva A, Milic-Emili J, Lisboa C. Breathing pattern and gas exchange at peak exercise in COPD patients with and without tidal flow limitation at rest. Eur Respir J. 17: 1120-1127, 2001. 24. Casanova C, Cote C, De Torres JP, Aguirre-Jaime A, Marin JM, Pinto-Plata V, Celli BR. The inspiratory to total lung capacity ratio predicts mortality in patients with COPD. Am J Respir Crit Care Med 2004 Dec 10. 25. Rossi A, Polese G, Brandi G, Conti G. Intrinsic positive end-expiratory pressure (PEEPi). Intensive Care Med. 21: 522-536, 1995. 26. Vestbo J, Prescott E, Lange P. Association of chronic mucus hypersecretion with FEV1 decline and chronic obstructive pulmonary disease morbidity. Copenhagen City Heart Study Group. Am J Respir Crit Care Med. 153: 1530-1535, 1996. 27. Tantucci C, Grassi V. Flow limitation: an overview. Monaldi Arch. Chest Dis. 54: 353-7, 1999. 28. Ricciardolo F l, Sterk PJ, Gaston B, Folkers G, Nitric oxide in health and disease of respiratory system. Physiol Rev. Jul; 84: 731-65, 2004. 29. Sterk P J, Heterogeneity of airway hyperresponsiveness: time for unconventional, but traditional, studies. J Appl Physiol. Jun; 96: 20178, 2004. 30. Smith AD, Cowan JO, Filsell S, McLachlan C, Monti-Sheehan G, Jackson P, Taylor DR. Diagnostic Asthma. Comparison between exhaled nitric oxide measurements and conventional tests. Am J Respir Crit Care Med 169. 473-478, 2004. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 6. Fisiopatologia della limitazione di flusso nella BPCO. Diagnosi differenziale - R. Poggi, A. Rossi 69 7. Cuore polmonare cronico ed ipertensione polmonare secondaria alla BPCO A cura di Alfredo Potena e Marco Piattella UO Fisiopatologia Respiratoria Azienda Ospedaliero-Universitaria Arcispedale S. Anna, Ferrara 7. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Definizioni Cor Pulmonale: ipertrofia e/o dilatazione del ventricolo destro associata ad ipertensione arteriosa polmonare derivata da malattie respiratorie che limitano la funzione e/o la struttura dei polmoni. Clinicamente il cor pulmonale è caratterizzato dalla presenza di edema associato ad insufficienza respiratoria. Ipertensione arteriosa polmonare: pressione arteriosa polmonare (PAP) media a riposo superiore ai 20 mmHg. Nei pazienti BPCO la comparsa di ipertensione arteriosa polmonare di solito è preceduta da un aumento dei valori pressori superiori a 30 mmHg durante test da sforzo rettangolari con carico di lavoro leggero (30 watts) (1). L’ipertensione polmonare associata a malattie polmonari e/o ipossiemia, nella nuova e più recente classificazione, non viene più considerata una forma di ipertensione arteriosa secondaria, ma è ritenuta una forma a parte nel contesto di un gruppo di malattie respiratorie (2). Epidemiologia Anche se dati indiretti fanno ritenere che siano piuttosto rilevanti, le attuali prevalenze di cor pulmonale e di ipertensione arteriosa polmonare nella BPCO non sono note, non essendo state sistematicamente ricercate con strumenti diagnostici affidabili, quali ad esempio la cateterizzazione del cuore destro. Un tentativo di individuare la prevalenza di ipertensione arteriosa polmonare in pazienti a rischio, con ostruzione bronchiale ed insufficienza respiratoria (VEMS <50% del teorico e PaO2 <55 mmHg) ha prodotto una stima, in uno studio condotto nel Regno Unito, pari allo 0,3% della popolazione generale (3). Studi autoptici hanno evidenziato alterazioni di tipo ipertrofico a carico del ventricolo destro in più del 40% dei pazienti con BPCO, anche se sono state riportate discrepanze tra serie differenti per la mancanza di omogeneità dei criteri morfologici utilizzati (4,5). Studi recenti eseguiti in pazienti con enfisema grave (VEMS 27% del teorico) hanno riportato una elevata incidenza di ipertensione polmonare; il 91% dei pazienti, infatti, aveva una pressione in arteria polmonare media, rilevata mediante cateterizzazione, superiore a 20 mmHg (6). Rilevanza clinica L’ipertensione polmonare, nella BPCO, oltre ad essere un fattore prognostico sfavorevole in termini di sopravvivenza, è anche associata ad una peggior evoluzione clinica e ad un più frequente utilizzo di risorse sanitarie. Il cor pulmonale è una condizione che accompagna molto spesso la BPCO, di cui viene ritenuta la causa principale di disabilità e di morte (7,8). In uno studio longitudinale, della durata di 7 anni, eseguito su 50 pazienti con BPCO si è osservato che la loro sopravvivenza era inversamente correlata alle resistenze vascolari periferiche (RVP), e che la correlazione della sopravvivenza con le RVP era simile a quella ottenuta con il VEMS (9). In un altro studio, della durata di 15 anni, si è dimostrato che la presenza o l’assenza di cuore polmonare, dopo la correzione per l’età, era uno dei migliori fattori predittivi per il rischio di mortalità (10). La PAP, inoltre, si è confermata come miglior singolo fattore predittivo di mortalità anche su pazienti BPCO in ossigenoterapia domiciliare a lungo termine (11). Storia naturale nella BPCO L’evoluzione dell’ipertensione polmonare nella BPCO è progressiva, e la sua gravità è correlata al grado di ostruzione delle vie aeree ed alle alterazioni degli scambi gassosi (6). 71 Tuttavia, il tasso di progressione dell’ipertensione nella BPCO è lento, e di solito la PAP è soltanto moderatamente aumentata, anche in pazienti con patologia di base avanzata. Non è chiaro in che fase della storia naturale della BPCO si manifesti l’ipertensione polmonare, tanto che spesso i segni clinici compaiono tardi, nello stadio avanzato di malattia quando le modificazioni a carico del circolo polmonare e l’ipertensione arteriosa polmonare dovrebbero essere presenti già da tempo. Patogenesi 72 Diversi fattori possono contribuire allo sviluppo ed al mantenimento dell’ipertensione polmonare nella BPCO, e dunque alla comparsa di cor pulmonale. Nelle malattie respiratorie croniche l’ipertensione deriva da un aumento delle resistenze vascolari polmonari mentre la portata cardiaca e la pressione capillare da incuneamento, la cosiddetta “pulmonary capillary wedge pressure” (Ppcw), sono normali. In questi casi si parla di ipertensione arteriosa polmonare pre-capillare. I più importanti fattori che sostengono l’aumento delle RVP sembrano essere la vasocostrizione ipossica, che induce un’ipertrofia permanente della tonaca media ed il conseguente rimodellamento dei vasi polmonari. La comprensione dei meccanismi eziopatogenetici responsabili di queste alterazioni vascolari nella BPCO rimane non completamente chiarita ma, come nelle altre malattie respiratorie croniche, l’ipossia alveolare conseguente alla riduzione della ventilazione gioca un ruolo prevalente. L’abitudine di continuare a fumare che molti pazienti BPCO manifestano anche negli stadi avanzati di malattia può avere un ulteriore effetto aggravante su questi fenomeni (12). L’ipossia alveolare cronica che porta al rimodellamento vascolare polmonare con ipertrofia della tonaca muscolare media dei piccoli vasi e delle arteriole polmonari e fibrosi dell’intima, è comparabile a quella osservata nelle popolazioni che nascono e vivono a grandi altezze. Caratteristiche del rimodellamento vascolare polmonare I pazienti BPCO in fase di cuore polmonare cronico e negli stadi terminali di malattia, presentano modificazioni a carico delle arterie polmonari e dei vasi pre-capillari tali da giustificare l’irreversibile aumento delle resistenze vascolari polmonari. Tutti gli strati laminari che compongono i vasi sono coinvolti e le alterazioni dell’intima sono le più importanti. Questo aspetto può derivare dall’associazione tra ipossia, danno meccanico e reazione infiammatoria cioè da tutti i fenomeni che derivano dallo stiramento ripetuto di parenchima polmonare iperinsufflato (13,14). L’ispessimento dell’intima è secondario alla proliferazione di cellule muscolari lisce, alcune delle quali hanno perduto il loro fenotipo contrattile, e al deposito di fibre collagene ed elastiche. Su soggetti fumatori con normale funzionalità respiratoria, è stato documentato un ispessimento dell’intima nelle arterie polmonari, non dissimile da quello che si osserva in pazienti con BPCO lieve (15). Fisiopatologia L’ipertensione polmonare secondaria a BPCO è definita dalla presenza di una pressione media in arteria polmonare (PAP) superiore al normale limite di 20 mmHg (16,17). Nella maggior parte dei casi, il grado di ipertensione polmonare in corso di BPCO è di entità lieve-moderata e si attesta intorno ai 25-30 mmHg, superando raramente i 35-40 mmHg, con una portata cardiaca normale. Sia la pressione in atrio destro sia la Ppcw tendono ad essere normali. Questo profilo emodinamico è diverso da quello che si riscontra nell’ipertensione polmonare da altre cause (primitiva, post embolica), dove la PAP raggiunge valori considerevoli e la portata cardiaca è generalmente ridotta (9,17). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 7. Cuore polmonare cronico ed ipertensione polmonare secondaria alla BPCO - A. Potena, M. Piattella Vasocostrizione polmonare ipossica L’ipossia determina vasocostrizione sulla circolazione polmonare e vasodilatazione su quella sistemica. La vasocostrizione arteriolare su base ipossica, riduce la perfusione delle unità alveolari scarsamente o per nulla ventilate, e la ridistribuisce verso unità alveolari meglio ventilate, mantenendo in equilibrio il rapporto ventilo-perfusorio, migliorando quindi la pressione parziale di O2 nel sangue arterioso. La somministrazione di ossigeno supplementare nei pazienti con BPCO inibisce lo stimolo ipossico, determinando un peggioramento del rapporto ventilo-perfusorio. In generale, il contributo della vasocostrizione ipossica sul rapporto ventilo-perfusorio tende ad essere maggiore nei pazienti con BPCO meno grave, mentre risulta essere meno efficace nei soggetti con forme più severe di malattia (18). Studi condotti su anelli arteriosi isolati, hanno evidenziato che l’intensità della contrazione indotta dalla ipossia è inversamente correlata alla funzione endoteliale, e direttamente correlata alla PO2 arteriosa (19). Questo dati fanno ritenere che l’alterazione della funzione endoteliale sia associata ad una alterata risposta allo stimolo ipossico, con ulteriore peggioramento degli scambi gassosi. Funzione del ventricolo destro L’ipertensione arteriosa polmonare accresce il post-carico e quindi il lavoro ventricolare destro cui fanno seguito l’ipertrofia e la dilatazione e successivamente una disfunzione sistolica e diastolica. Il ventricolo destro, rispetto al sinistro, presenta una parete meno spessa ed un maggior rapporto volume/superficie d’area. Il ventricolo destro è considerato una pompa di volume, piuttosto che di pressione, ed in termini fisiologici si adatta meglio a modificazioni del pre-carico, rispetto a cambiamenti repentini del post-carico. Ciò spiega perché nei soggetti con BPCO in cui la PAP è modestamente elevata e la progressione è sostanzialmente lenta, il ventricolo destro ha il tempo necessario per adattarsi. Quando la PAP è cronicamente elevata il ventricolo destro si dilata, con incremento del volume sia tele-diastolico che tele-sistolico. Nella BPCO il volume sistolico del ventricolo destro è generalmente mantenuto, mentre la frazione di eiezione è ridotta. Durante le riacutizzazioni di BPCO, in corrispondenza di un marcato incremento della PAP, la contrattilità del ventricolo destro si riduce nei pazienti con segni clinici di insufficienza del ventricolo destro (20, 21). Ciò è causa, sul piano clinico, della sindrome denominata scompenso ventricolare destro, con congestione sistemica del circolo venoso ed impossibilità di adattare la portata ventricolare destra alle esigenze muscolari periferiche ed allo sforzo muscolare anche lieve. Segni clinici Alcuni segni clinici del cor pulmonale sono mascherati dalla iperinflazione polmonare e possono essere riscontrati in fase tardiva di malattia, molto tempo dopo l’insorgenza di ipertensione arteriosa polmonare. L’edema malleolare o pretibiale è il più classico di questi, anche se poco specifico perchè lo si può osservare in altre malattie respiratorie croniche o perché in alcuni pazienti con ipertensione polmonare può mancare del tutto. L’edema periferico è la testimonianza clinica dello scompenso cardiaco destro e consegue la congestione venosa secondaria alla trasmissione a monte della pressione di riempimento del ventricolo destro. Nella BPCO, l’ipossiemia e l’ipercapnia possono aggravare la congestione venosa, inducendo una attivazione del sistema nervoso simpatico, già stimolato dalla distensione dell’atrio destro. 73 L’attivazione simpatica riduce il flusso plasmatico renale, stimola il sistema renina-angiotensina-aldosterone, e promuove l’assorbimento di bicarbonato, sodio ed acqua. Anche la vasopressina, rilasciata quando il paziente diviene iponatriemico, in pazienti con ipossiemia ed ipercapnia, contribuisce alla formazione dell’edema (22). La distensione della parete atriale determina la messa in circolo dell’ormone natriuretico atriale, che agisce come un fattore protettivo verso l’edema, a causa della sua azione vasodilatatrice, natriuretica e diuretica; i suoi effetti, tuttavia, possono essere insufficienti per controbilanciare i meccanismi che favoriscono la formazione dell’edema. Durante episodi di riacutizzazione di BPCO si può assistere allo sviluppo o alla progressione di un edema già presente. La riacutizzazione spesso può comportare un’insufficienza respiratoria acuta o acuta su cronico (come viene chiamata in gergo quando l’episodio di insufficienza respiratoria è una recidiva in un soggetto BPCO nel quale erano già presenti segni di insufficienza respiratoria cronica) che determina aumenti di PAP di oltre 20 mmHg. Questi valori accresciuti, dopo un corretto trattamento, possono ritornare ai livelli di base al termine dell’episodio di riacutizzazione (23,24). La presenza di edema periferico, però, non dev’essere necessariamente ritenuta come un segno di scompenso cardiaco destro perchè può indicare, più semplicemente, la presenza di iperaldosteronismo conseguente ad insufficienza respiratoria. Un segno tardivo di cor pulmonale è l’insufficienza tricuspidalica accompagnata da un soffio sistolico generato dal rigurgito valvolare. 74 Esercizio L’esercizio determina un anomalo aumento della PAP, specialmente in pazienti con ipertensione polmonare a riposo. Pazienti che sembrano più suscettibili di sviluppare ipertensione polmonare, possono evidenziare un aumento della PAP sotto sforzo anni prima che l’ipertensione si manifesti a riposo (25). Diversi studi hanno identificato un certo numero di meccanismi per spiegare l’ipertensione polmonare indotta dall’esercizio nella BPCO, tra cui la vasocostrizione ipossica, la riduzione del letto capillare conseguente all’enfisema, la compressione extramurale per l’aumentata pressione alveolare o lo squilibrio nella produzione di fattori di rilassamento vascolare di derivazione endoteliale (26). In corso di BPCO, la PAP sotto sforzo è maggiore di quella predetta dall’equazione delle RVP, suggerendo una vasocostrizione attiva sotto sforzo (27). Durante l’esercizio, i pazienti con BPCO possono sviluppare una iperinflazione dinamica secondaria alla limitazione del flusso espiratorio, che ha come risultato un aumento della pressione alveolare, a sua volta trasmesso alla Ppcw (28). Oltre a ciò, l’aumento della ventilazione sotto sforzo, in presenza di ostruzione al flusso, determina significative oscillazioni della parete toracica. Questi cambiamenti pressori possono portare ad una riduzione dell’output cardiaco per alterazione del ritorno venoso sistemico o per aumento del post-carico ventricolare sinistro (29,30). Diagnosi della ipertensione polmonare nella BPCO Il riconoscimento della ipertensione polmonare nella BPCO può non essere agevole, specialmente nelle forme più lievi. I sintomi dovuti alla ipertensione polmonare, come dispnea o affaticamento, sono difficili da differenziare rispetto a quelli tipici del quadro clinico della BPCO. Nella maggior parte dei casi, il rilievo di edema periferico in un paziente con BPCO deve far pensare ad una manifestazione dell’ipertensione polmonare, anche se non sempre è un segno di insufficienza del ventricolo destro. I toni cardiaci possono non essere apprezzati bene per la soRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 7. Cuore polmonare cronico ed ipertensione polmonare secondaria alla BPCO - A. Potena, M. Piattella vrapposizione di rantoli bronchiali da ipersecrezione, o per l’iperinflazione polmonare. Inoltre, i tipici reperti auscultatori dell’ipertensione polmonare, click di eiezione, rinforzo del secondo tono e soffio olosistolico da rigurgito mitralico, non sono frequenti nei pazienti con BPCO. Radiografia del torace La principale caratteristica radiologica dell’ipertensione polmonare è l’aumento degli ili vascolari con oligoemia nei campi polmonari periferici. Altri segni sono la cardiomegalia, dovuta ad una dilatazione del ventricolo destro e del tronco polmonare. L’allargamento ilare può essere stimato dall’indice toraco-ilare, che è definito dal rapporto tra la larghezza transilare (distanza tra l’inizio delle divisioni delle arterie polmonari destra e sinistra) con il diametro traverso del torace (31). Un rapporto >0,36 è suggestivo di ipertensione polmonare (32). Un altro potenziale indicatore nella radiografia del torace è l’allargamento del diametro dell’arteria polmonare discendente di destra (normalmente <16 mm) fino a 18 mm. L’allargamento del ventricolo destro giustifica un aumento dell’indice cardio-toracico >0,5, assieme all’ampliamento degli spazi aerei retrosternali visibile nella proiezione laterale. Elettrocardiogramma La sensibilità dell’elettrocardiogramma nell’identificare l’ipertensione polmonare è relativamente bassa, e modificazioni del tracciato non sono strettamente correlate alla gravità dell’ipertensione. Alterazioni elettrocardiografiche associate a cuore polmonare comprendono: una P polmonare suggestiva di sovraccarico atriale destro nelle derivazioni D2, D3 ed aVF; un aspetto S1-S2-S3 oppure S1-Q3; un blocco di branca destro incompleto; l’ipertrofia del ventricolo destro definita da un QRS della durata superiore a 0,10 sec; predominanza dell’onda R in V1 ampiezza del rapporto R/S <1 in V5 e V6; basso voltaggio QRS. Tra queste alterazioni elettrocardiografiche, il pattern S1-S2-S3 ed i segni di sovraccarico destro sono stati associati ad una riduzione della sopravvivenza in pazienti con BPCO, monitorati dopo una riacutizzazione (33). Le modificazioni elettrocardiografiche presentano una specificità dell’86% ed una sensibilità del 51% nell’evidenziare ipertensione polmonare. Prove di funzionalità respiratoria Le prove di funzionalità respiratoria sono necessarie per la diagnosi di BPCO, ma non ci sono pattern specifici associati all’ipertensione polmonare che di per sé ha scarso effetto sulla meccanica polmonare o sugli scambi gassosi. In condizioni di integrità del parenchima polmonare, l’ipertensione polmonare può ridurre la diffusione del monossido di carbonio anche se, nella BPCO, questa alterazione può essere spiegata dalla presenza di enfisema polmonare. Ecocardiografia L’ecocardiografia fornisce utili informazioni sulla funzione del ventricolo destro e sulla sua rilevanza prognostica, ed anche se la metodica possiede alcuni limiti se ne raccomanda l’utilizzo per la valutazione della ipertensione polmonare nella BPCO. L’ecocardiografia doppler misura la velocità di flusso del rigurgito tricuspidalico, e può essere utilizzata per determinare il gradiente pressorio ventricolo-atrio destro. Questo, sommato alla pressione atriale destra, permette una valutazione della pressione sistolica ventricolare destra. In caso di insufficienza della valvola polmonare la velocità di flusso può essere utile per misurare il gradiente pressorio diastolico fra l’arteria polmonare ed il ventricolo destro, e quindi la 75 76 pressione polmonare diastolica. Recentemente è stato dimostrato che la misurazione transcutanea del flusso a livello delle vene giugulari, mediante tecnica ecodoppler, può avere un potenziale ruolo nel predire la pressione in arteria polmonare in pazienti con BPCO (34). Il metodo si basa sulla analisi della velocità di flusso diastolico e sistolico del polso venoso giugulare, il cui rapporto sembra correlato con la PAP stimata mediante cateterizzazione destra, e sembra essere più specifico rispetto a quello tradizionale con ecocardiografia doppler. I limiti di questa metodica comprendono una bassa sensibilità in pazienti con ipertensione polmonare lieve, ed i potenziali errori tecnici in presenza di tachicardia od aritmia. L’ecocardiografia bidimensionale fornisce informazioni sulla morfologia e sulla dinamica delle strutture cardiache, ed è anche essenziale per la diagnosi delle patologie associate al cuore sinistro. Segni tipici di cuore polmonare sono l’allargamento di atrio e ventricolo destri l’aumento di spessore ventricolare destro con cavità ventricolare sinistra normale o ridotta ed eventualmente inversione della normale curvatura del setto. L’ecocardiografia da sforzo ha permesso di identificare un anomalo movimento del setto ventricolare con distorsione del ventricolo sinistro nei pazienti con BPCO. Questo aspetto può aiutare ad identificare disfunzioni occulte del ventricolo destro. Un problema dell’ecocardiografia doppler è che spesso questo esame diagnostico può fornire stime errate dei valori pressori, con differenze superiori a 10 mmHg rispetto ai valori misurati con il cateterismo. La specificità è stata stimata nel 52% ed il valore positivo predittivo nel 52%, offrendo dunque un rischio per eccesso diagnostico di ipertensione polmonare nei pazienti BPCO (35,36). Alcuni autori hanno valutato il valore prognostico dell’ecocardiografia sulla funzione ventricolare destra in pazienti con BPCO. Da questo studio risulta che il diametro ventricolare destro di fine diastole e la velocità di riempimento diastolico tardivo erano fattori predittivi indipendenti di sopravvivenza (37,38). L’ecocardiografia M-mode consente di ipotizzare una ipertensione polmonare sulla base dei movimenti della valvola polmonare (onda A, pendenza E-F, incisura mesosistolica, tempi sistolici del ventricolo destro). Risonanza magnetica La risonanza magnetica polmonare con angiografia è forse la migliore modalità diagnostica perché produce le migliori immagini del ventricolo destro ed è un ottimo sistema per valutare alterazioni funzionali del ventricolo destro. Un diametro dell’arteria polmonare destra superiore a 28 mm, risulta essere un fattore predittivo di ipertensione polmonare sensibile ed altamente specifico, anche se la sua applicazione nella BPCO non è ancora stata studiata (39). È bene sottolineare, in ogni caso, che questa tecnica è particolarmente costosa e non disponibile dappertutto. Pertanto il suo impiego deve essere considerato solo ai fini di ricerca. Test da sforzo Il principale fattore limitante la tolleranza all’esercizio nella BPCO è lo squilibrio della ventilazione (40). Durante lo sforzo eseguito con un test rettangolare (30-40 watts per 10’) la PAP aumenta notevolmente nei pazienti BPCO in stadio avanzato con PAP aumentata già a riposo, perché le resistenze vascolari polmonari in questi soggetti non diminuiscono con lo sforzo e ad un raddoppio della portata cardiaca corrisponde un incremento del 100% della PAP (41). Il polso di ossigeno al culmine dell’esercizio è di solito ridotto nei pazienti con BPCO, ed il suo valore correla con la capacità di esercizio (42). In pazienti con ipertensione polmonare primitiva la distanza percorsa durante test del cammino Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 7. Cuore polmonare cronico ed ipertensione polmonare secondaria alla BPCO - A. Potena, M. Piattella dei 6 minuti, è stata utilizzata come esito principale per valutare l’efficacia di nuove terapie (43). Questo test si è dimostrato particolarmente efficace nella valutazione prognostica delle malattie respiratorie; nella BPCO, pertanto, sarebbe interessante valutarne la sensibilità anche nella determinazione dell’ipertensione polmonare (44). Analisi dell’aria espirata L’ossido nitrico è un importante regolatore del tono vascolare e nei pazienti BPCO il suo rilascio a livello delle arterie polmonari è alterato. L’ossido nitrico di derivazione polmonare può essere analizzato nell’aria espirata, tanto che variazioni di concentrazione sono state osservate in varie patologie respiratorie, e lo si ritiene un utile strumento diagnostico di malattia in fase attiva (45). La presenza di ipertensione polmonare è stata associata ad una ridotta produzione di ossido nitrico sia a riposo sia sotto sforzo (46, 47), mentre in pazienti con insufficienza cardiaca ed ipertensione polmonare l’ossido nitrico è risultato inversamente correlato con le RVP (47). Un recente studio, ha valutato la relazione tra ossido nitrico nell’aria espirata e la funzione ventricolare destra in un gruppo di pazienti con BPCO, evidenziando che la stima ecocardiografica della PAP e della funzione ventricolare destra erano significativamente correlate con la concentrazione di ossido nitrico espirato. I pazienti con disfunzione ventricolare destra presentavano una ridotta concentrazione di ossido nitrico nell’aria espirata, suggerendo che questi pazienti potrebbero avere sia un ridotto rilascio che una ridotta diffusione dell’ossido nitrico dall’endotelio verso le vie aeree (48). Tuttavia l’esatta origine dell’ossido nitrico espirato non è chiara. Cateterismo cardiaco destro Il cateterismo cardiaco destro è il GOLD standard, cioè la tecnica di riferimento per la diagnosi di ipertensione polmonare e determina una misura diretta della PAP, dell’output cardiaco e delle resistenze vascolari polmonari. Può anche essere utilizzato per valutare gli effetti acuti dell’intervento terapeutico. Si tratta di una procedura sicura in mani esperte anche se, in considerazione della sua invasività, non è raccomandata come esame di routine nei pazienti con BPCO. Terapia L’ipertensione polmonare nella BPCO è di solito lieve o moderata e pertanto potrebbe essere non necessario un suo trattamento specifico. Al contrario si possono ottenere buoni vantaggi da un corretto schema terapeutico della malattia di base. Diversa è la condizione di scompenso cardio-congestizio del ventricolo destro associata ad insufficienza respiratoria che necessita di un trattamento con diuretici e la correzione dell’insufficienza respiratoria con ossigenoterapia ed eventualmente, in caso di ipercapnia, con ventilazione meccanica non-invasiva. In corso di terapia diuretica è necessario controllare periodicamente la funzione renale e gli elettroliti plasmatici. L’impiego di farmaci inotropo-positivi, quali ad esempio la digitale, deve essere riservata alla coesistenza di segni di insufficienza ventricolare sinistra o di fibrillazione atriale. L’ossigenoterapia a lungo termine si è dimostrata utile nel ridurre i valori di PAP nei pazienti con BPCO ipossiemica permettendo di ridurre gli episodi di scompenso congestizio e di accrescere la sopravvivenza nei pazienti che ne facevano uso per oltre 15 ore/die (49,50). Nonostante i vasodilatatori sistemici possano produrre una lieve riduzione della PAP ed un aumento dell’output cardiaco nella BPCO, la loro somministrazione è usualmente associata ad un 77 peggioramento degli scambi gassosi. Inoltre, non esiste evidenza che un trattamento a lungo termine con vasodilatatori sia associato ad un beneficio clinico. Per tali motivi i vasodilatatori non sono raccomandati nel trattamento dell’ipertensione polmonare nella BPCO (8). Studi in acuto ed a lungo termine hanno dato risultati contrastanti sull’impiego della nifedipina e dei calcio antagonisti più in generale; questi farmaci dopo un trattamento a lungo termine non hanno prodotto un reale beneficio clinico (51). L’ossido nitrico può essere somministrato con sicurezza nei pazienti con BPCO per 24 ore di seguito, tuttavia non vi è evidenza che la somministrazione combinata a lungo termine di ossigeno ed ossido nitrico determini un miglioramento della ipertensione polmonare nella BPCO (52). Uno studio recente indica nella tecnica di somministrazione “pulsata” una modalità più efficace per ottenere risultati favorevoli sulla PAP media, sulle resistenze vascolari polmonari e sulla portata cardiaca, senza riduzione dell’ossigenazione sul sangue arterioso (53). La somministrazione di prostaciclina, dei suoi analoghi sintetici o dell’antagonista recettoriale bosentan, ha fornito ottimi risultati nell’ipertensione arteriosa polmonare, che sono stati attribuiti alla regressione del rimodellamento vascolare (43). In considerazione di questi dati, e del fatto che l’ipertensione polmonare secondaria a BPCO presenta tratti patogenetici comuni all’ipertensione polmonare primitiva, è ragionevole supporre che questi farmaci, correggendo lo squilibrio vasocostrizione-vasodilatazione, possano avere anche in questa patologia qualche beneficio clinico (14). Prostacicline, sildenafil e bosentan, in ogni caso, allo stato attuale non hanno indicazione per l’impiego nei pazienti BPCO con ipertensione polmonare. 78 BIBLIOGRAFIA 1. Weitzenblum E. Chronic cor pulmonale. Heart 2003; 89(2): 225-30. 2. Rich S ed. Primary Pulmonary Hypertension. Executive summary from the World Symposium on Pulmonary Hypertension 1998, Evian, France, Sept 6-10, cosponsored by the world Health Organization. 1998. 3. Williams BT, Nicholl JP. Prevalence of hypoxaemic chronic obstructive lung disease with reference to long-term oxygen therapy. Lancet 1985; 2(8451): 369-72. 4. Weitzenblum E, Kessler R, Oswald M, Fraisse P. Medical treatment of pulmonary hypertension in chronic lung disease. Eur Respir J 1994; 7(1): 148-52. 5. Pietra G. Pathology of the pulmonary vasculature and hearth. In: Cherniack NS, ed. Chronic obstructive pulmonary disease. Philadelphia, WB Saunders; 1991: 21-26. 6. Scharf SM, Iqbal M, Keller C, Criner G, Lee S, Fessler HE. Hemodynamic characterization of patients with severe emphysema. Am J Respir Crit Care Med 2002; 166(3): 314-22. 7. Kessler R, Faller M, Fourgaut G, Mennecier B, Weitzenblum E. Predictive factors of hospitalization for acute exacerbation in a series of 64 patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 159(1): 158-64. 8. Pauwels RA, Buist AS, Ma P, Jenkins CR, Hurd SS. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: National Heart, Lung, and Blood Institute and World Health Organization Global Initiative for Chronic Obstructive Lung Disease (GOLD): executive summary. Respir Care 2001; 46(8): 798-825. 9. Burrows B, Kettel LJ, Niden AH, Rabinowitz M, Diener CF. Patterns of cardiovascular dysfunction in chronic obstructive lung disease. N Engl J Med 1972; 286(17): 912-8. 10. Traver GA, Cline MG, Burrows B. Predictors of mortality in chronic obstructive pulmonary disease. A 15-year follow-up study. Am Rev Respir Dis 1979; 119(6): 895-902. 11. Oswald-Mammosser M, Weitzenblum E, Quoix E, Moser G, Chaouat A, Charpentier C, Kessler R. Prognostic factors in COPD patients receiving long-term oxygen therapy. Importance of pulmonary artery pressure. Chest 1995; 107(5): 1193-8. 12. Presberg KW, Dincer HE. Pathophysiology of pulmonary hypertension due to lung disease. Curr Opin Pulm Med 2003; 9(2): 131-8. 13. Wright JL, Petty T, Thurlbeck WM. Analysis of the structure of the muscular pulmonary arteries in patients with pulmonary hypertension and COPD: National Institutes of Health nocturnal oxygen therapy trial. Lung 1992; 170(2): 109-24. 14. Naeije R, Barbera JA Pulmonary hypertension associated with COPD. Crit Care 2001; 5(6): 286-9. 15. Santos S, Peinado VI, Ramirez J, Melgosa T, Roca J, Rodriguez-Roisin R, Barbera JA. Characterization of pulmonary vascular remodelling in smokers and patients with mild COPD. Eur Respir J 2002; 19(4): 632-8. 16. Weitzenblum E, Hirth C, Ducolone A, Mirhom R, Rasaholinjanahary J, Ehrhart M. Prognostic value of pulmonary artery pressure in chronic obstructive pulmonary disease. Thorax 1981; 36(10): 752-8. 17. Naeije R. Should pulmonary hypertension be treated in chronic obstructive pulmonary disease? in Weir EK, Archer SL, Reeves JT eds. The diagnosis and treatment of pulmonary hypertension. Mount Kisco Futura Publishing, 1992: 209 - 239. 18. Barbera JA, Roger N, Roca J, Rovira I, Higenbottam TW, Rodriguez-Roisin R. Worsening of pulmonary gas exchange with nitric oxide inhalation in chronic obstructive pulmonary disease. Lancet 1996; 347(8999): 436-40. 19. Peinado VI, Santos S, Ramirez J, Roca J, Rodriguez-Roisin R, Barbera JA. Response to hypoxia of pulmonary arteries in chronic ob- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 7. Cuore polmonare cronico ed ipertensione polmonare secondaria alla BPCO - A. Potena, M. Piattella structive pulmonary disease: an in vitro study. Eur Respir J 2002; 20(2): 332-8. 20. MacNee W. Pathophysiology of cor pulmonale in chronic obstructive pulmonary disease. Part two. Am J Respir Crit Care Med 1994; 150(4): 1158-68. 21. MacNee W. Pathophysiology of cor pulmonale in chronic obstructive pulmonary disease. Part One. Am J Respir Crit Care Med 1994; 150(3): 833-52. 22. Lee Chiong TMR. The hearth in the stable COPD patients. In: Similowski T, Whitelaw WA, Derenne JP eds. Clinical management of chronic obstructive pulmonary disease. New York, Marcel Dekker, Inc. 2002; 475 - 532. 23. Abraham AS, Cole RB, Green ID, Hedworth-Whitty RB, Clarke SW, Bishop JM. Factors contributing to the reversible pulmonary hypertension of patients with acute respiratory failure studies by serial observations during recovery. Circ Res 1969; 24(1): 51-60. 24. Barbera JA, Roca J, Ferrer A, Felez MA, Diaz O, Roger N, Rodriguez-Roisin R Mechanisms of worsening gas exchange during acute exacerbations of chronic obstructive pulmonary disease. Eur Respir J, 1997; 10(6): 1285-91. 25. Kessler R, Faller M, Weitzenblum E, Chaouat A, Aykut A, Ducolone A, Ehrhart M, Oswald-Mammosser M. “Natural history” of pulmonary hypertension in a series of 131 patients with chronic obstructive lung disease. Am J Respir Crit Care Med 2001; 164(2): 219-24. 26. Barbera JA, Riverola A, Roca J, Ramirez J, Wagner PD, Ros D, Wiggs BR, Rodriguez-Roisin R. Pulmonary vascular abnormalities and ventilation-perfusion relationships in mild chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1994; 149(2 Pt 1): 423-9. 27. Agusti AG, Barbera JA, Roca J, Wagner PD, Guitart R, Rodriguez-Roisin R. Hypoxic pulmonary vasoconstriction and gas exchange during exercise in chronic obstructive pulmonary disease. Chest 1990; 97(2): 268-75. 28. Butler J, Schrijen F, Henriquez A, Polu JM, Albert RK. Cause of increased right and left atrial pressures in patients with obstructed airflow disease. Chest 1988; 93(3 Suppl): 171S-172S. 29. Montes de Oca M, Rassulo J, Celli BR. Respiratory muscle and cardiopulmonary function during exercise in very severe COPD. Am J Respir Crit Care Med 1996; 154(5): 1284-9. 30. Rubanyi GM, Romero JC, Vanhoutte PM. Flow-induced release of endothelium-derived relaxing factor. Am J Physiol 1986; 250(6 Pt 2): H1145-9. 31. Chetty KG, Brown SE, Light RW. Identification of pulmonary hypertension in chronic obstructive pulmonary disease from routine chest radiographs. Am Rev Respir Dis 1982; 126(2): 338-41. 32. Wiedemann HM, RA. Heart Disease. A textboox of cardiovascular medicine. 5th Edn. Philadelphia,WB Saunders Company 1997. 33. Incalzi RA, Fuso L, De Rosa M, Di Napoli A, Basso S, Pagliari G, Pistelli R. Electrocardiographic signs of chronic cor pulmonale: A negative prognostic finding in chronic obstructive pulmonary disease. Circulation 1999; 99(12): 1600-5. 34. Matsuyama W, Ohkubo R, Michizono K, Abe M, Nakamura Y, Kawabata M, Osame M. Usefulness of transcutaneous Doppler jugular venous echo to predict pulmonary hypertension in COPD patients. Eur Respir J 2001; 17(6): 1128-31. 35. Arcasoy SM, Christie JD, Ferrari VA, Sutton MS, Zisman DA, Blumenthal NP, Pochettino A, Kotloff RM. Echocardiographic assessment of pulmonary hypertension in patients with advanced lung disease. Am J Respir Crit Care Med 2003; 167(5): 735-40. 36. Takakura M, Harada T, Fukuno H, Okushi H, Taniguchi T, Sawada S, Fujinaga H, Wakatsuki T, Oki T. Echocardiographic Detection of Occult Cor Pulmonale During Exercise in Patients with Chronic Obstructive Pulmonary Disease. Echocardiography, 1999. 16(2): 127-134. 37. Burgess MI, Bright-Thomas RJ, Ray SG. Echocardiographic evaluation of right ventricular function. Eur J Echocardiogr 2002; 3(4): 252-62. 38. Burgess MI, Mogulkoc N, Bright-Thomas RJ, Bishop P, Egan JJ, Ray SG. Comparison of echocardiographic markers of right ventricular function in determining prognosis in chronic pulmonary disease. J Am Soc Echocardiogr 2002; 15(6): 633-9. 39. Kruger S, Haage P, Hoffmann R, Breuer C, Bucker A, Hanrath P, Gunther RW. Diagnosis of pulmonary arterial hypertension and pulmonary embolism with magnetic resonance angiography. Chest 2001; 120(5): 1556-61. 40. Agustì AC, Wagner J. Responses to exercise in lung disease. Eur Respir Mon 1997(6): 32-50. 41. Horsfield R, Segel N, Bishop JM. Pulmonary circulation in chronic bronchitis at rest and during exercise breathing air or 80% oxygen. Clin Sci 1968; 43: 473-83. 42. Minh VD, Lee HM, Dolan GF, Light RW, Bell J, Vasquez P. Hypoxemia during exercise in patients with chronic obstructive pulmonary disease. Am Rev Respir Dis 1979 Oct; 120(4): 787-794. 43. Galie N, Manes A, Branzi A. Emerging medical therapies for pulmonary arterial hypertension. Prog Cardiovasc Dis 2002; 45(3): 213-24. 44. Troosters T, Vilaro J, Rabinovich R, Casas A, Barbera JA, Rodriguez-Roisin R, Roca J. Physiological responses to the 6-min walk test in patients with chronic obstructive pulmonary disease. Eur Respir J 2002; 20(3): 564-9. 45. Kharitonov SA, Barnes PJ. Exhaled markers of pulmonary disease. Am J Respir Crit Care Med 2001; 163(7): 1693-722. 46. Kharitonov SA, Cailes JB, Black CM, du Bois RM, Barnes PJ. Decreased nitric oxide in the exhaled air of patients with systemic sclerosis with pulmonary hypertension. Thorax 1997; 52(12): 1051-5. 47. Riley MS, Porszasz J, Miranda J, Engelen MP, Brundage B, Wasserman K. Exhaled nitric oxide during exercise in primary pulmonary hypertension and pulmonary fibrosis. Chest 1997; 111(1): 44-50. 48. Clini E, Cremona G, Campana M, Scotti C, Pagani M, Bianchi L, Giordano A, Ambrosino N. Production of endogenous nitric oxide in chronic obstructive pulmonary disease and patients with cor pulmonale. Correlates with echo-Doppler assessment. Am J Respir Crit Care Med 2000; 162(2 Pt 1): 446-50. 49. Medical Research Council Working Party. Long-term domiciliaryoxygen therapy in chronic hypoxic cor pulmonale complicating chronicbronchitis and emphysema. Lancet, 1981(i): 681-686. 50. Nocturnal Oxygen Therapy Trial Group. Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease. Ann Intern Med 1980; 93: 391-398. 51. Kanazawa H, Tateishi Y, Yoshikawa J. Acute effects of nifedipine administration in pulmonary haemodynamics and oxygen delivery during exercise in patients with chronic obstructive pulmonary disease: implication of the angiotensin-converting enzyme gene polymorphisms. Clin Physiol Funct Imaging 2004; 24(4): 224-8. 52. Ashutosh K, Phadke K, Jackson JF, Steele D. Use of nitric oxide inhalation in chronic obstructive pulmonary disease. Thorax 2000; 55(2): 109-13. 53. Vonbank K, Ziesche R, Higenbottam TW, Stiebellehner L, Petkov V, Schenk P, Germann P, Block LH. Controlled prospective randomised trial on the effects on pulmonary haemodynamics of the ambulatory long term use of nitric oxide and oxygen in patients with severe COPD. Thorax 2003; 58(4): 289-93. 79 8. Ruolo delle infezioni nelle riacutizzazioni della BPCO A cura di Antonio Spanevello e Luisa M. Esposito Dipartimento di Pneumologia Riabilitativa Fondazione Salvatore Maugeri Istituto Scientifico di Cassano Murge, (Bari) 8. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Definizioni e Diagnosi La broncopneumopatia cronica ostruttiva (BPCO) è una malattia cronica disabilitante, caratterizzata da frequenti e sistematiche riacutizzazioni associate ad un progressivo, quanto repentino, deterioramento fisiologico e della funzione polmonare, ad aumento delle alterazioni infiammatorie delle vie aeree ed ad un considerevole aumento della sintomatologia di base. Le riacutizzazioni della BPCO sono oggi riconosciute come rilevante causa di morbilità e mortalità connessa con tale patologia e la loro frequenza rappresenta uno dei più rilevanti fattori determinanti la qualità di vita oltre che essere un’importante causa di ricovero ospedaliero. È ancora controversa l’origine delle riacutizzazioni bronchitiche, infatti numerosi fattori eziologici, soli o concomitanti, ne sono responsabili. Negli ultimi anni la scienza medica, attraverso innovative tecniche di ricerca, ha fatto notevoli progressi nella patogenesi della BPCO e sui fattori scatenanti una riacutizzazione, riscontrando numerose evidenze sia per l’eziologia infiammatoria sia per quella infettiva. Riacutizzazione della BPCO: nonostante gli sia stato riconosciuto un ruolo clinico e biologico importante per frequenza ed impatto, nella storia naturale della malattia, ancor oggi non se ne dispone una definizione definitiva universalmente accettata. Nel 1968 Fisher ha scritto “Il valore dei lavori futuri in questo campo sarebbe maggiore se si potesse raggiungere l’accordo sulla definizione di riacutizzazione”(1) ma, purtroppo, le contraddizioni continuano e i numerosi tentativi per raggiungere un consenso unanime sono stati decisamente vani (2,3). Un tentativo di standardizzazione della definizione di riacutizzazione della BPCO fu dato da Anthonisen et al. nel 1987 (4). In quello studio le riacutizzazioni sono state suddivise in tre gruppi, (in associazione ai principali sintomi della malattia): - riacutizzazioni del 1° Tipo: caratterizzate da aumento della dispnea, del volume e della purulenza dell’espettorato; - riacutizzazioni di 2° Tipo: caratterizzate da due dei precedenti sintomi; - riacutizzazioni di 3° Tipo: caratterizzata da uno qualunque dei precedenti sintomi associato ad almeno uno dei sintomi supplementari quali faringodinia, ipersecrezione nasale per almeno 5 giorni, febbre, incremento della dispnea e della tosse, incremento della frequenza cardiaca o respiratoria di oltre il 20% se rapportata a quella basale. Una recente dichiarazione, emersa da un gruppo di esperti (Aspen Conference) ha definito la riacutizzazione come un “significativo peggioramento delle condizioni di un paziente affetto da BPCO, dallo stato di stabilità clinica, che va al di là delle normali variazioni quotidiane, ha inizio acuto e necessita di un cambiamento nella terapia di base”(5). È molto probabile che tale definizione sia in futuro universalmente accettata. Attualmente, la definizione più comunemente usata per definire tale evento clinico è la seguente: “incremento soggettivo dal livello di soglia di uno o più sintomi cronici”. Sintomi che includono (5): - aumento della tosse (per frequenza e gravità); - aumento del volume dell’espettorato; - presenza di espettorato purulento e persistenza dello stesso; - aumento della dispnea e della sensazione di ostruzione bronchiale. 81 Numerose altre patologie possono determinare un aumento degli stessi sintomi ed è necessario che queste possano essere ragionevolmente escluse con certezza attraverso la valutazione clinica. Nella maggior parte dei casi, infatti, la storia clinica del paziente e un esame completo permettono di formulare una corretta diagnosi (6). Le diagnosi differenziali includono la polmonite, lo scompenso cardiaco congestizio, l’ischemia del miocardio, l’infezione delle vie respiratorie superiori, l’embolia polmonare, l’inspirazione ricorrente e la scarsa compliance al trattamento farmacologico (7). Fisiopatologia delle riacutizzazioni 82 Lo stato di stabilità clinica è caratterizzato da vari stadi di infiammazione che interessano le grandi e le piccole vie aeree così come gli alveoli, con conseguente ipersecrezione di muco, riduzione del calibro delle vie aeree e distruzione alveolare, rispettivamente. I mediatori principali, direttamente responsabili di questi danni, sono le proteinasi rilasciate dalle cellule infiammatorie, specialmente i neutrofili, che si riscontrano numerosi nelle secrezioni bronchiali dei pazienti con BPCO (8-11). I neutrofili sono richiamati in circolo in risposta ai “chemoattractants”, specialmente l’interleuchina-8 (IL-8) e il leucotriene B4 (LTB4) attraverso le molecole di adesione intercellulare 1 (quali la selectina E e l’ICAM-1) espresse sull’endotelio vascolare. Questi recettori si pensa siano iperespressi sulle cellule epiteliali di pazienti con BPCO (9), implicati, oltre che nel reclutamento, nell’adesione dei neutrofili (quale la MAC-1, molecola di adesione della famiglia delle integrine) (10). La degranulazione neutrofila comporta rilascio di elastasi e di altre proteinasi (quali la catepsina G, la proteinasi 3 e la metalloproteinasi) che si pensa siano responsabili di varie funzioni ai danni del tessuto (parenchimale), così come la mieloperossidasi (MPO) (12). Una percentuale di pazienti, inoltre, presenta un aumento della quota di eosinofili bronchiali che possono contribuire al processo infiammatorio (13-15). Con questo background vi è la comune convinzione che le riacutizzazioni siano eventi in cui si osserva un’incremento del processo infiammatorio, anche se tali processi e relative conseguenze restano ancora non del tutto compresi. Infatti, non è stato possibile il confronto tra i diversi studi a causa della mancanza di una standardizzazione nelle definizioni utilizzate, nella metodologia di ricerca e nella selezione della popolazione con relativa caratterizzazione del paziente. Eziologia infettiva nella riacutizzazione della BPCO Le riacutizzazioni della BPCO sono state associate con un certo numero di fattori eziologici, un posto di rilievo è occupato dagli episodi infettivi. Queste, infatti, sono frequentemente innescate da infezioni del tratto respiratorio superiore prevalentemente nei mesi invernali, quando sono più diffuse nella collettività le infezioni respiratorie (16), anche se ciò potrebbe essere dovuto anche al fatto che la funzione polmonare dei pazienti affetti da BPCO mostra piccole ma significative diminuzioni associate alla riduzione della temperatura esterna (17). Tre classi di agenti patogeni sono stati individuati come causa scatenante di una riacutizzazione acuta di BPCO attraverso le infezioni delle basse vie respiratorie: i virus respiratori, i batteri aerobici gram-positivi e gram-negativi e i batteri atipici (18). I contributi relativi a queste tre classi differenti di agenti patogeni possono cambiare a secondo della severità della malattia ostruttiva sottostante. Così come potrebbero variare i contributi relativi agli agenti patogeni appartenenti ad una stessa classe, in particolar modo se si tratta di agenti patogeni batterici (6). In particolare il grado di compromissione funzionale del soggetto BPCO sembra in qualche modo poter condizionare il tipo di microrganismo coinvolto nella riacutizzazione, è, infatti, stata dimostrata l’esistenza di una correlazione tra il deterioramento della funzione respiratoria ed i batteri isolati nel corso della riacutizzazione stessa (19). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 8. Ruolo delle infezioni nelle riacutizzazioni della BPCO - A. Spanevello, L. M. Esposito Ruolo dei virus nella riacutizzazione della BPCO Le infezioni virali delle basse vie respiratorie in pazienti con BPCO possono anche essere una causa diretta del danno all’epitelio delle vie aeree, con conseguente perdita delle cellule ciliate, ipersecrezione di muco ed espulsione delle cellule necrotiche nel lume delle vie aeree, associata ad aumento della trasudazione plasmatica (20). Inoltre, causando una riduzione del calibro delle vie aeree (21), le alterazioni atmosferiche possono facilitare le infezioni batteriche secondarie determinando un peggioramento dell’infiammazione. Si è dimostrato che le infezioni virali sono responsabili dell’aumento dell’iperreattività delle vie aeree e ciò può essere dovuto ad un’alterazione dell’equilibrio delle sostanze broncocostrittrici e broncodilatatrici nelle vie respiratorie (20,22). Effettivamente, è stato dimostrato che le infezioni virali correlano con l’aumento del livello di endotelina -1 (ET-1), inducendo stati asmatici acuti, e incrementando le già elevate concentrazioni plasmatiche di ET-1 durante le riacutizzazioni di BPCO (23). Inoltre, i virus possono anche incrementare il rilascio di acetilcolina per mezzo degli effetti direttti ed indiretti dei recettori muscarinici M2 facilitando la tendenza al broncospasmo (24). Quindi, sono molti i meccanismi attraverso i quali i virus possono provocare una riacutizzazione acuta di BPCO (AECOPD). Le infezioni virali Le infezioni virali rappresentano un importante fattore scatenante per le riacutizzazioni bronchitiche innescate frequentemente, appunto, dalle infezioni delle vie aeree superiori. Tuttavia la loro reale incidenza è tuttora sconosciuta perché test virali, a causa della loro complessità, non sono routinariamente applicabili alla pratica clinica. A partire dagli anni ’70, numerosi studi longitudinali hanno esaminato il ruolo dei virus come causa di riacutizzazione della BPCO (25-27). In questi studi l’infezione virale, considerata responsabile di circa il 30% degli episodi di riacutizzazione, è stata solitamente documentata da analisi sierologiche ed occasionalmente da analisi colturali. Il Rhinovirus è attualmente considerato il fattore scatenante più importante alla base di una riacutizzazione bronchitica. Insieme agli Enterovirus, i Rhinovirus appartengono al gruppo dei Picornavirus, virus dell’RNA, e si trasmettono direttamente da un ospite all’altro attraverso le secrezioni respiratorie infette. È soltanto in tempi recenti che è stata riconosciuta la sua importanza come causa di riacutizzazione nella BPCO, grazie ad adeguate tecniche di laboratorio, come la “reazione a catena polimerasica” (PCR), che hanno permesso il suo isolamento nelle colture cellulari e sierologiche. Infatti, questo virus presenta particolari meccanismi di crescita e si manifesta in oltre 100 sierotipi, pertanto la sua individuazione mediante colture o metodi sierologici è particolarmente difficile, da qui la sottostima negli studi, condotti finora, sulle cause delle riacutizzazioni che facevano largo uso di tali metodiche (28). Altri virus, oltre al Rhinovirus, possono innescare riacutizzazioni bronchitiche. In ordine di importanza, per la frequenza con cui è isolato, va citato l’Influenza-virus (25-27), considerato la seconda causa di riacutizzazioni dovute ad infezioni virali, seguono il Parainfluenza-virus, il Coronavirus, associato con una piccola percentuale di riacutizzazioni asmatiche, pertanto si suppone non svolga un ruolo maggiore nella BPCO (25), l’Adenovirus ed il Virus Sinciziale Respiratorio (VRS) (tab. 1). Vi sono un certo numero di meccanismi che possono essere coinvolti nelle interazioni fra i virus e le riacutizzazioni. È stato dimostrato che, nel corso di una riacutizzazione, usando metodi sierologici ed i campioni biologici da tampone nasale per la coltura virale, il Rhinovirus può essere trovato più frequentemente nell’espettorato che nell’esalato nasale (29-31), ciò suggerisce che la specie più aggressiva di Rhinovirus può infettare le basse vie respiratorie e contribuire ai processi in- 83 fiammatori associati alla riacutizzazione (29). Inoltre, è stato osservato che le riacutizzazioni associate alla presenza del Rhinovirus nell’espettorato indotto sono anche associate ad un incremento maggiore dei livelli di interleuchina-6 (IL-6) nelle vie aeree (29). Ciò suggerisce che i virus aumentano la severità dell’infiammazione delle vie aeree in fase di riacutizzazione. Quanto trovato è in accordo con il dato che i virus respiratori determinano le riacutizzazioni più lunghe e più severe con una conseguente maggiore incidenza sull’utilizzo delle risorse sanitarie (29,30,32). È stato riscontrato, inoltre, un sistematico aumento dei markers infiammatori laddove vi era una evidente infezione virale delle vie aeree. Il recettore principale dei Rhinovirus è la molecola di adesione intercellulare (ICAM-1), che è situata sulle cellule epiteliali del tratto respiratorio. Gli attacchi, dovuti al Rhinovirus, all’epitelio delle vie aeree attraverso la molecola di adesione ICAM-1, stimolano l’espressione dell’ICAM-1, quindi promuovono il reclutamento e l’attivazione delle cellule infiammatorie, come è visto accadere nelle riacutizzazioni (33). Vi è una certa evidenza che nella BPCO, sulla superfice dell’epitelio bronchiale, l’espressione della molecola di adesione ICAM-1 potrebbe essere iperespressa e ciò suggerirebbe una maggiore predisposizione all’infezione da Rhinovirus (34). Quindi l’iperespressione dell’ICAM-1 può rappresentare un importante obiettivo terapeutico nelle riacutizzazioni associate a Rhinovirus (35). Tuttavia ad oggi non vi è evidenza che pazienti bronchitici cronici siano soggetti a più infezioni di natura virale, anche se l’effetto infiammatorio delle infezioni rinovirali può essere maggiore in tali pazienti. 84 Ruolo dei batteri nella riacutizzazione della BPCO Il ruolo dei batteri nella progressione della malattia è stato largamente studiato anche se resta relativamente poco chiaro. Ci sono un certo numero di potenziali meccanismi che potrebbero coinvolgere i batteri nella sintomatologia della BPCO. Specie di “Hemophilus influenzae”, “Pseudomonas aeruginosa”, e “Streptococcus pneumoniae” sono stati mostrati essere in grado di stimolare l’ipersecrezione del muco in vitro (36) ed i primi due organismi sono stati individuati come inibitori della frequenza del battito ciliare (37). Ancora, l’Hemophilus influenzae può causare danni all’epitelio bronchiale (38), infatti, la relativa endotossina si è riscontrata essere responsabile di determinare l’iperespressione epiteliale di citochine proinfiammatorie, quali l’IL-6, l’IL-8 e TNF-α (Tumor necrosis factor-α) in vitro (39), causando i potenziali meccanismi dell’iperespresssione infiammatoria. A sostegno di questa tesi, pazienti con bronchite cronica e BPCO, che presentano una coltura batterica positiva di Hemophilus influenzae, presentano concentrazioni più alte di TNF-α nel loro espettorato (40). In uno studio di pazienti con bronchite cronica stabile, il carico batterico delle vie aeree si è trovato in diretta correlazione con i markers dell’infiammazione neutrofila, indipendentemente dall’agente patogeno isolato (26). Similmente, la presenza di potenziali agenti patogeni microbici isolati dal liquido del lavaggio broncoalveolare è significativamente associata con l’incremento dei neutrofili e le concentrazioni di TNF-α (41). L’estirpazione o la riduzione dei batteri è associata con risoluzione dell’infiammazione. Alcuni autori affermano che non esistano prove definitive del fatto che i batteri svolgano un ruolo nelle riacutizzazioni acute (42). La maggior parte degli studi microbiologici determinati a stabilire il ruolo dei batteri ha fatto uso di colture di espettorato spontaneamente prodotto confrontando lo stato stabile con quello riacutizzato. Poiché gli stessi organismi sono stati trovati frequentemente negli stessi paziente sia nella fase stabile sia durante una riacutizzazione, l’interpretazione del loro ruolo risulta tuttora difficile. Tuttavia, è stato riscontrato che la percentuale di pazienti con colture batteriche positive e con un alto carico batterico aumenta durante le riacutizzazione nella maggior Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 8. Ruolo delle infezioni nelle riacutizzazioni della BPCO - A. Spanevello, L. M. Esposito parte degli studi (1,43,44). Recentemente le più innovative tecniche molecolari hanno evidenziato che la colonizzazione batterica non è stabile e ci sono frequenti turnover di alcuni ceppi di Hemophilus influenzae che determinano specifiche host-responses alla membrana esterna alla proteina (45). È quindi probabile che una mutazione dell’agente patogeno può essere responsabile dei sintomi di una riacutizzazione; ciò potrebbe spiegare perché gli studi che non sono riusciti a discriminare i differenti ceppi batterici (46) non abbiano riscontrate evidenze di una nuova infezione. Le infezioni batteriche Nel corso degli ultimi quattro decenni l’opinione, relativa al contributo dell’infezione batterica nella patogenesi delle riacutizzazioni bronchitiche, si è progressivamente modificata, passando da un ruolo preponderante, voluto dalla “British Hypothesis” degli anni ’50-’60, all’idea che l’infezione batterica fosse soltanto una mera conseguenza (epifenomeno) (33,47) degli anni ’70-’80. Nell’ultimo decennio nuovi metodi d’indagine sono stati utilizzati nello studio di questo problema che hanno portato ad una migliore determinazione del contributo dell’infezione batterica nelle riacutizzazioni della BPCO. Le potenziali vie attraverso cui i batteri potrebbero contribuire alla patogenesi di una riacutizzazione acuta possono essere sintetizzate nelle seguenti tre (48): - infezione primaria delle basse vie aeree; - infezione secondaria delle vie aeree dopo un’infezione virale antecedente; - antigeni batterici che inducono l’iperreattività bronchiale e l’infiammazione eosinofila. Le nuove metodiche di laboratorio, messe a punto negli ultimi anni, hanno permesso, appunto, di ricercare evidenze di una responsabilità dei batteri come causa primaria di una riacutizzazioni; responsabilità la cui entità, ad oggi, risulta ancora non ben determinata a causa dei risultati, non definitivi e spesso contraddittori, riflettenti la scarsa sensibilità e specificità di metodiche quali ad esempio l’analisi colturale dell’espettorato. Infatti, i progressi fatti nella comprensione della patogenesi batterica nei decenni passati hanno mostrato che la tecnica della coltura dell’espettorato, una volta usata come unico mezzo d’indagine per determinare la causa della riacutizzazione bronchiale, presenta notevoli limiti per quanto ne possa essere ancora considerata la pietra per la diagnostica eziologia. Limiti dovuti soprattutto al metodo di raccolta dell’espettorato e alla relativa, quanto inevitabile, contaminazione delle secrezioni con la flora orofaringea, spesso contenente potenziali patogeni, con conseguente minore specificità del risultato della coltura. Limiti che oggi possono essere superati se si esaminano secrezioni delle vie aeree più basse ottenute con metodi broncoscopici in test colturali quantitativi (49). Infatt,i i campioni ottenuti dalle secrezioni delle vie aeree distali mediante la tecnica del PBS (Protected Specimen Brush) o quella del BAL (Lavaggio Bronco Alveolare) sono incontaminate dalle secrezioni delle vie respiratorie superiori e le concentrazioni batteriche oltre determinati livelli di soglia nelle colture quantitative correlano con l’infezione del tessuto (50). Studi recenti (51-54), utilizzando tali metodiche hanno dimostrato un’infezione batterica costantemente significativa delle vie aeree distali in circa il 50% di pazienti riacutizzati. Le specie batteriche isolate coprono la stessa gamma di patogeni comunemente isolati nelle analisi colturali dei campioni di espettorato raccolti in pazienti bronchitici cronici durante una riacutizzazione acuta (49). Vi è comune accordo sul fatto che gli agenti batterici più comunemente isolati nelle vie aeree dei pazienti, sia con BPCO stabile sia durante una riacutizzazione, appartengono a ceppi non classificabili di Hemophilus influenzae, Streptococcus pneumoniae e Moraxella catarrhalis (55). Come anticipato, la specie batterica isolata durante una riacutizzazione bronchitica sembra dipendere dalla 85 severità dell’affezione polmonare sottostante. Gli Streptococcus pneumoniae ed altri Cocci grampositivi sono isolati più comunemente in pazienti con moderata ostruzione del flusso aereo mentre i pazienti con ostruzione più severa del flusso presentano più comunemente batteri gram-negativi quali quelli appartenenti al genere delle Enterobacteriaceae e delle Pseudomonas (56) (tab. 1). Tabella 1 – Batteri e virus respiratori associati a riacutizzazioni della BPCO CAUSE INFETTIVE DI RIACUTIZZAZIONE DELLA BPCO VIRUS Rhinovirus Influenza-virus Parainfluenza-virus Coronavirus Adenovirus Virus respiratorio sinciziale BATTERI Hemophilus influenzae Streptococcus pneumoniae Streptococcus gram-positivi Bacilli enterici gram-negativi (GNEB) Moraxella catarrhalis Staphylococcus aureus Pseudomonas aeruginosa BATTERI ATIPICI Chlamydia pneumoniae Legionella Mycoplasma pneumoniae 86 La presenza di batteri nelle vie aeree più basse di bronchitici cronici determina una breccia nei meccanismi di difesa dell’ospite, che da l’avvio ad un “circolo vizioso” ai danni delle cellule epiteliali, un’ipotesi ben definita la quale sostiene che i batteri che colonizazano il tratto respiratorio producono endotossine ed altri prodotti che associati ad un aumento della “perdita della sottomucosa vascolare” inducono l’infiammazione, aumentano l’iperreattività delle vie aeree e determinano il deterioramento dei meccanismi di clearance mucociliare associato ad ipersecrezione di muco. Questi prodotti batterici sono attivatori potenti dei macrofagi alveolari, che reclutano i neutrofili ed altre cellule infiammatorie nel polmone, comportando una aumento nella produzione delle proteasi o peggio ancora determinando lo squilibrio fra proteinasi ed antiproteinasi che si ipotizza possa determinare la distruzione del parenchima polmonare (16). Numerosi studi recenti hanno dimostrato l’esistenza di una associazione tra il carico batterico delle vie aeree e la presenza di markers infiammatori, oltre che la diretta proporzionalità tra l’estensione della colonizzazione batterica e l’incremento dell’infiammazione delle stesse vie aeree (57). In particolar modo è stato dimostrato che le riacutizzazioni associate ad Hemophilus influenzae e Moraxella catarrhalis sono associate a livelli significativamente più elevati dei markers infiammatori delle vie aeree e dell’elastasi neutrofila, rispetto a riacutizzazioni non patologiche (58). Un altro studio ha messo in evidenza che il tipo di specie batterica è legato al grado di infiammazione, con la colonizzazione dello pseudomonas aeruginosa, che mostra un incremento della mieloperossidasi (MPO), una misura indiretta dell’attivazione neutrofila (57). Infine, in un altro studio è stato dimostrato che la colonizzazione batterica delle vie aeree dei pazienti è variabile quando i campioni sono prelevati a circa 1 anno di distanza e che i cambiamenti nel carico batterico presente nelle vie aeree è correlato al declino del FEV1 (59). I pazienti bronchitici che hanno mostrato maggiori cambiamenti nella natura della colonizzazione batterica hanno sofferto di declini più repentini della funzione polmonare. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 8. Ruolo delle infezioni nelle riacutizzazioni della BPCO - A. Spanevello, L. M. Esposito. I livelli elevati nell’espettorato di interleuchina-8 (IL-8) sono associati a carico batterico maggiore ed ad un declino più repentino del FEV1 (16). In conclusione se la colonizzazione batterica è correlata ad un aumento dell’infiammazione allora può essere associata all’aumento della frequenza delle riacutizzazioni. La colonizzazione batterica, inoltre, modula il carattere delle riacutizzazioni ed un suo incremento si è dimostrato di recente essere direttamente proporzionale all’incremento della frequenza delle riacutizzazioni. Batteri atipici. Negli ultimi anni il progredire delle metodiche di laboratorio ha migliorato notevolmente le nuove conoscenze a riguardo, anche se queste sono ancora molto limitate per quanto concerne la diagnosi e l’identificazione, di agenti patogeni batterici atipici ed il loro ruolo nelle riacutizzazioni bronchitiche. Un ruolo tutto sommato piuttosto marginale considerato il loro coinvolgimento in circa il 5-10% delle riacutizzazioni di tipo infettivo. In particolare i patogeni atipici più frequentemente isolati sono: la Chlamydia pneumoniae, la Legionella ed il Mycoplasma pneumonie (25-27,53) (tab. 1). Molto probabilmente i meccanismi che implicano le riacutizzazioni di BPCO sono simili a quelli coinvolti nelle infezioni virali e, inoltre, le ricerche sul ruolo di questi organismi dipende in gran parte dall’analisi sierologica (27,57,60,61). La Chlamydia pneumoniae è un batterio intracellulare che causa bronchite acuta e polmonite. Un recente interesse ha messo a fuoco il ruolo dell’infezione clamidiale cronica nella BPCO, associata ad una percentuale di riacutizzazione che va dal 24% al 34% (62,63). Per la sua diagnosi vengono utilizzate combinazioni in concentrazioni elevate degli anticorpi Immunoglobulina G (IgG) e Immunoglobulina A (IgA) nel siero, concentrazioni Immunoglobulina A secrete nell’espettorato, o la tecnica della “reazione a catena polimerasica” su campioni di espettorato (64). Tuttavia nonostante gli ultimi studi ancora non è chiaro il suo ruolo nella patogenesi delle riacutizzazioni bronchitiche, cioè se ne sia in qualche modo coinvolto oppure se è soltanto un “innocente spettatore” (16). Inoltre gli studi fino ad ora condotti non hanno dimostrato alcuna associazione tra questo batterio e la presenza di markers infiammatori (65). Le infezioni da Mycoplasma pneumoniae, invece, interessano principalmente gli adulti in giovane età i quali per la maggior parte raggiungono l’immunità all’età in cui la riacutizzazione acuta della BPCO si è trasformata in un problema clinico. Quindi non c’è da sorprendersi se numerosi studi hanno riscontrato che soltanto una piccola percentuale di riacutizzazioni è associata con la presenza diretta di questo organismo (66). Le infezioni eterogenee Sono ancora limitate le nostre conoscenze su questo argomento, infatti, nonostante, alcuni studi abbiano riscontrato la presenza di infezioni eterogenee virali e batteriche in percentuali variabili dal 30 al 60% dei casi di riacutizazione, nessuna chiara evidenza è stata riscontrata circa il fatto che le infezioni virali siano promotrici dirette di quelle batteriche (25-27). Piuttosto, la percentuale di batteri isolati associata a riacutizzazioni infettive di natura virale non differisce rispetto a quella associata a riacutizzazioni non virali. Ulteriori approfondimenti sono però necessari in questo campo. Lo stesso si può dire circa le interazioni tra agenti batterici “tipici” ed “atipici” (25). Conclusioni Vi è una significativa morbilità e mortalità associata alle riacutizzazioni bronchitiche. Il ruolo delle infezioni del tratto respiratorio come causa principale di riacutizzazione è stato fonte di controversie per numerosi decenni e rappresenta tuttora un campo di ricerca aperto. Tuttavia sono state riscontrate numerose evidenze scientifiche a supporto del fatto che un’alta percentuale di riacutizzazioni possa essere attribuita ad agenti infettivi come virus e batteri. L’in- 87 fezione della via aerea tracheobronchiale è un processo dinamico complesso. Capire questo processo e la risposta immunitaria dell’ospite è di fondamentale importanza per la messa a punto di nuovi modelli preventivi e terapeutici. 88 BIBLIOGRAFIA 1. Fisher M, Akhtar AJ, Calder MA, et al. Pilot study of factors associated with exacerbations in chronic bronchitis. BMJ 1969;4:187–92. 2. COPD Guidelines Group of the Standards of Care Committee of the British Thoracic Society. BTS guidelines for the management of chronic obstructive pulmonary disease. Thorax 1997;52(Suppl 5):S1–28. 3. Pauwels R, Buist AS, Calverley PM, et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease disease: NHLBI/WHO global initiative for chronic obstructive lung disease (GOLD) workshop summary. Am J Respir Crit Care Med 2001;163:1256–76. 4. Anthonisen NR, Manfreda J, Warren CPW et al. Antibiotic therapy in exacerbations of chronic obstructive pulmonary disease. Ann Intern Med 1987; 106(2): 196-204. 5. Rodriguez-Roisin R. Toward a consensus definition for COPD exacerbations. Chest 2000; 117:325S-401S. 6. Sethi S. Infectious Etiology of Acute Exacerbations of Chronic Bronchitis. Chest 2000; 117: 380S-385S. 7. American Thoracic Society. Standards for the diagnosis and care of patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1995; 152:S77-S120. 8. Di Stefano A, Capelli A, Lusuardi M, et al. Severity of airflow limitation is associated with severity of airway inflammation in smokers. Am J Respir Crit Care Med 1998;158:1277–85. 9. VM, Collins PD, Scott DM, et al. Differences in interleukin-8 and tumor necrosis factor-alpha in induced sputum from patients with chronic obstructive pulmonary disease or asthma. Am J Respir Crit Care Med 1996;153:530–4. 10. Stanescu D, Sanna A, Veriter C, et al. Airways obstruction, chronic expectoration, and rapid decline of FEV1 in smokers are associated with increased levels of sputum neutrophils. Thorax 1996;51:267–71. 11. Thompson AB, Daughton D, Robbins RA, et al. Intraluminal airway inflammation in chronic bronchitis: characterisation and correlation with clinical parameters. Am Rev Respir Dis 1989;140:1527–37. 12. Noguera A, Batle S, Miralles C, et al. Enhanced neutrophil response in chronic obstructive pulmonary disease. Thorax 2001;56:432–7. 13. Lacoste J-Y, Bousquet J, Chanez P, et al. Eosinophilic and neutrophilic inflammation in asthma, chronic bronchitis, and chronic obstructive pulmonary disease. J Allergy Clin Immunol 1993;92:537–48. 14. O’Connel JM, Baird LI, Campbell AH. Sputum eosinophilia in chronic bronchitis and asthma. Respiration 1978;35:65–72. 15. Pesci A, Balbi B, Majori M, et al. Inflammatory cells and mediators in bronchial lavage of patients with chronic obstructive pulmonary disease. Eur Respir J 1998;12:380–6. 16. Wedzicha JA, Donaldson GC. Exacerbations of Chronic Obstructive Pulmonary Disease. Respir Care 2003; 48(12), 1204-1208. 17. Donaldson GC, Seemungal T, Jeffries et al. Effect of temperature on lung function and symptoms in chronic obstructive pulmonary disease. Eur respir J 1999; 13(4): 844-849. 18. Sethi S. Management of acute exacerbations of chronic bronchitis. Infect Dis Clin Pract 1998; 7: S300-S308 19. Eller J, Ede A, Schaberg T et al. Infective exacerbations of chronic bronchitis: Relation between bacteriologic etiology and lung function. Chest 1998; 113: 1542-1548. 20. Hegele RG, Hayashi S, Hogg JC, et al. Mechanisms of airway narrowing and hyperresponsiveness in viral respiratory tract infections. Am J Respir Crit Care Med 1995;151:1659–64. 21. Smith CB, Kanner RE, Golden CA, et al. Effect of viral infections on pulmonary function in patients with chronic obstructive pulmonary diseases. J Infect Dis 1980;141:271–80. 22. Melbye H, Kongerud J, Vorland L. Reversible airflow limitation in adults with respiratory infection. Eur Respir J 1994;7:1239–45. 23. Roland M, Bhowmik A, Sapsford RJ, et al. Sputum and plasma endothelin-1 levels in exacerbations of chronic obstructive pulmonary disease. Thorax 2001;56:30–5. 24. Jacoby DB, Fryer AD. Interaction of viral infections with muscarinic receptors. Clin Exp Immunol 1999;29:59–64. 25. Gump DW, Phillips CA, Forsyth BR et al. Role of infection in chronic bronchitis. Am Rev Respir Dis 1976; 113: 465-473. 26. Buscho RO, Saxtan D,Shultz PS, et al. Infections with viruses and Mycoplasma pneumoniae during exacerbations of chronic bronchitis. J Infect Dis 1978; 137:377-383. 27. Smith CB, Golden C, Kanner R et al. Association of viral and Mycoplasma pneumoniae infections with acute respiratory illness in patients with chronic obstructive pulmonary disease. Am Rev Respir Dis 1980; 121: 225-232. 28. Wedzicha JA. Role of Viruses in Exacerbations of Chronic Obstructive Pulmonary Disease. Proc Am Thorac Soc 2004; 1: 115-120. 29. Seemungal TAR, Harper-Owen R, Bhowmik A et al. Detection of rhinovirus in induced sputum at exacerbations of chronic obstructive pulmonary disease. Eur Respir J 2000; 16(4): 677-683. 30. Seemungal TAR, Harper-Owen R, Bhowmik A et al. Respiratory viruses, symptoms, and inflammatory markers in acute exacerbations and stable chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2001; 164(9): 1618-1623. 31. Rohde G, Wiethege A, Borg I, et al. respiratory viruses hospitalisation: a case-control study. Thorax 2003; 58(1): 37-42. 32. Seemungal TAR, Donaldson GC, Bhowmik A et al. Time course and recovery of exacerbations in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2000; 161: 608-613. 33. Tager I, Speizer FE. Role of infection in chronic bronchitis. N Engl J Med 1975; 292: 563-571. 34. Di Stefano A, Maestrelli P, Ruggeri A, et al. Upregulation of adhesion molecules in the bronchial mucosa of subjects with chronic obstructive bronchitis. Am J Respir Crit Care Med 1994; 149: 803-810. 35. Wedzicha JA. Exacerbations. Etiology and Pathophysiologic Mechanisms. Chest 2002; 121: 136S-141S. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 8. Ruolo delle infezioni nelle riacutizzazioni della BPCO - A. Spanevello, L. M. Esposito 36. Adler KB, Hendley DD, Davis GS. Bacteria associated with obstructive pulmonary disease elaborate extracellular products that stimulate mucin secretion by explants of guinea pig airways. Am J Pathol 1986;125:501–14. 37. Wilson R, Roberts D, Cole P. Effects of bacterial products on human ciliary function in vitro. Thorax 1984;40:125–31. 38. Read RC, Wilson R, Rutman A, et al. Interaction of nontypeable Haemophilus influenzae with human respiratory mucosa in vitro. J Infect Dis 1991;163:549–58. 39. Khair OA, Devalia JL, Abdelaziz MM, et al. Effect of Haemophilus influenzae endotoxin on the synthesis of IL-6, IL- 8, TNF-alpha and expression of ICAM-1 in cultured human bronchial epithelial cells. Eur Respir J 1994;7:2109–16. 40. Bresser P, Out TA, van Alphen L, et al. Airway inflammation in nonobstructive and obstructive chronic bronchitis with chronic haemophilus influenzae airway infection. Comparison with noninfected patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2000;162:947–52. 41. Soler N, Ewig S, Torres A, et al. Airway inflammation and bronchial microbial patterns in patients with stable chronic obstructive pulmonary disease. Eur Respir J 1999;14:1015–22. 42. Hirschman JV. Do bacteria cause exacerbations of COPD. Chest 2000;118:193–203. 43. Stockley RA, O’Brien C, Pye A, et al. Relationship of sputum colour to nature and outpatient management of acute exacerbations of COPD. Chest 2001;117:1638–45. 44. Scott KW. Bacteriology of the sputum in exacerbation and remission of chronic bronchitis. Br J Dis Chest 1973;67:43–8. 45. Murphy TF, Sethi S, Klingman KL, et al. Simultaneous respiratory tract colonisation by multiple strains of nontypeable Haemophylus influenzae in chronic obstructive pulmonary disease: implications for antibiotic therapy. J Infect Dis 1999;180:404–9. 46. Aaron S, Angel JB, Lunau M, et al. Granulocyte inflammatory markers and airway infection during acute exacerbation of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2001;163:349–55. 47. Medical Research Council. Definitions and classification of chronic bronchitis for clinical epidemiological purposes: a report to the Medical Research Council by their committee on the aetiology of chronic bronchitis. Lancet 1965; 1: 775-779. 48. Sethi S, Murphy TF. Bacterial infection in chronic obstructive pulmonary disease in 2000: a state-of-the-art review. Clin Microbiol Rev 2001; 14: 336-363. 49. Sethi S. Bacteria in Exacerbations of Chronic Obstructive Pulmonary Disease. Proc Am Thorac Soc 2004; Vol 1: 109-114. 50. Chastre J, Fagon J-Y, Bornet-Lesco M et al. Evaluation of bronchoscopic techniques for the diagnosis of nosocomial pneumonia. Am J Respir Crit Care Med 1995; 152: 231-240. 51. Monso E, Ruiz J, Rosell A, et al. Bacterial infection in chronic obstructive pulmonary disease: a study of stable and exacerbated outpatients using the protected specimen brush. Am J Respir Crit Care Med 1995; 152: 1316-1320. 52. Fagon J-Y, Chastre J, trouillet J-L, et al. Characterization of distal bronchial microflora during acute exacerbation of chronic bronchitis. Am Rev Respir Dis 1990; 142: 1004-1008. 53. Soler N, Torres A, Ewig S, et al. Bronchial microbial patterns in severe exacerbations of chronic obstructive pulmonary disease (COPD) requiring mechanical ventilation. Am J Respir Crit Care Med 1998; 157: 1498-1505. 54. Pela R, Marchesani F, Agostinelli C, et al. Airways microbial flora in COPD patients in stable clinical conditions and during exacerbations: a bronchoscopic investigation. Monaldi Arch Chest Dis 1998; 53: 262-267. 55. Wilson R. Evidence of bacterial infection in acute exacerbations of chronic bronchitis. Semin Respir Infect 2000; 15: 208-215. 56. Miravitlles M, Espinosa C, Fernadez-Laso E, et al. Relationship between bacterial flora in sputum and functional impairment in patients with acute exacerbations of COPD. Study Group of Bacterial Infection in COPD. Chest 1999; 116: 40-46. 57. Hill AT, Campbell EJ, Hill SL, et al. Association between airway bacterial load and markers of airway inflammation in patients with chronic bronchitis. Am J Med 2000; 109(4): 288-295. 58. Sethi S, Muscarella K, Evans N, et al. Airway inflammation and etiology of acute exacerbations of chronic bronchitis. Chest 2000; 118: 1557-1565. 59. Wilkinson TMA, Patel IS, Wilks M, et al. Airway bacterial load FEV1 decline in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2003; 167(8): 1090-1095. 60. Beaty CD, Grayston JT, Wang SP, et al. Chlamydia pneumoniae, strain TWAR, infection in patients with chronic obstructive pulmonary disease. Am Rev.Respir Dis 1991;144:1408–10. 61. Verkooyen RP, Van Lent NA, Mousavi Joulandan SA, et al. Diagnosis of Chlamydia pneumoniae infection in patients with chronic obstructive pulmonary disease by micro-immunofluorescence and ELISA. J Med Microbiol 1997;46:959–64. 62. Mogulkoc N, Karakurt S, Isalska B, et al. Acute purulent exacerbation of chronic obstructive pulmonary disease and Chlamydia pneumoniae infection. Am J Respir Crit Care Med 1999;160:349–53. 63. Karnak D, Beng Sun S, Beder S, et al. Chlamydia pneumoniae infection and acute exacerbation of chronic obstructive pulmonary disease (COPD). Respir Med 2001;95: 811–6. 64. Von Hertzen L, Alakarppa H, Koskinen R, et al. Chlamydia pneumoniae infection in patients with chronic obstructive pulmonary disease. Epidemiol Infect 1997; 118:155-164. 65. Seemungal TAR, Wedzicha JA, MacCallum P, et al. Chlamydia pneumoniae and COPD exacerbations (letter). Thorax 2002; 57(12): 10871088. 66. White AJ, Gompertz S, Stockley RA. Chronic obstructive pulmonary disease – 6: The aetiology of exacerbations of chronic obstructive pulmonary disease. Thorax 2003; 58:73-80. 89 9. Disturbi cardio-respiratori nel sonno nella BPCO A cura di Giuseppe Insalaco e Oreste Marrone Consiglio Nazionale delle Ricerche Istituto di Biomedicina e Immunologia Molecolare “A. Monroy”, Sezione di Fisiopatologia Respiratoria, Palermo 9. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La diagnosi di broncopneumopatia cronica ostruttiva (BPCO) è basata su una anamnesi che evidenzi l’esposizione a fattori di rischio e sulla limitata reversibilità della ostruzione al flusso aereo, con o senza sintomi (1). La BPCO è sottodiagnosticata in quanto spesso non è riconosciuta fino a quando non raggiunge uno stadio di evidenza clinica moderatamente avanzata. I pazienti con BPCO presentano alterazioni della funzione respiratoria che, durante la veglia, vengono dimostrate dai classici test di funzionalità respiratoria, i quali permettono di definire il grado di severità della malattia. L’esame di riferimento più importante è la spirometria. Una completa valutazione funzionale del paziente con BPCO richiede anche di mettere in evidenza il grado di compromissione della funzione respiratoria durante il sonno. Nel sonno, infatti, si verifica costantemente un peggioramento delle tensioni dei gas arteriosi, che raggiungono solitamente livelli tanto peggiori quanto più alterati sono i valori emogasanalitici nella veglia. In alcuni pazienti un quadro clinico di compromissione cardio-respiratoria difficilmente spiegabile sulla base dei test funzionali eseguibili durante la veglia potrebbe trovare spiegazione in disturbi respiratori nel sonno. Inoltre un trattamento mirato alla correzione dei disturbi respiratori nel sonno può in alcuni casi contribuire a migliorare il quadro funzionale presente nella veglia e quindi l’evoluzione della malattia. È importante quindi conoscere a quali fenomeni possa andare incontro il paziente con BPCO durante il sonno, da cosa siano determinati, e quali possano essere le loro conseguenze. Caratteristiche dei disturbi respiratori nel sonno Una riduzione della PaO2 ed un aumento della PaCO2 rispetto alla veglia sono un fenomeno fisiologico sia durante il sonno non-REM, sia durante il REM, e coincidono con una riduzione della ventilazione minuto (2). Nei soggetti sani e nella maggior parte dei pazienti con malattie respiratorie ma normossiemici in veglia, la riduzione della PaO2 durante il sonno non determina apprezzabili cadute della saturazione ossiemoglobinica (SaO2); queste, invece, compaiono facilmente in caso di ipossiemia in veglia, specialmente quando la PaO2 si trova sulla parte ripida della curva di dissociazione dell’ossigeno dall’emoglobina. In questi casi, piccole ulteriori riduzioni di PaO2 nel sonno facilitano la comparsa di desaturazioni significative. Anche nei pazienti con BPCO la PaO2 diurna è l’elemento predittivo piú rilevante delle desaturazioni notturne. Nel sonno non-REM è raro osservare profonde cadute della SaO2, a meno che non sia presente una severa insufficienza respiratoria. L’evenienza più frequente è rappresentata da una riduzione della SaO2 di poche unità percentuali, con un pattern respiratorio regolare. Durante il sonno REM compaiono invece facilmente desaturazioni arteriose prolungate (3), spesso per tutta la sua durata (fig. 1). La durata prolungata della desaturazione distingue gli episodi ipossiemici della BPCO da quelli della sindrome dell’apnea ostruttiva, che sono invece caratterizzati da durate solitamente inferiori al minuto e da una rapida risoluzione (4). Gli episodi ipossiemici prolungati nel sonno REM non sono un fenomeno specifico della BPCO, ma si verificano anche in altre malattie respiratorie e, in una certa misura, in soggetti normali anziani. La registrazione del flusso aereo e dei movimenti della parete toracica e addominale in coincidenza con questi episodi ipossiemici non mette solitamente in evidenza alterazioni del pattern respiratorio ben definibili; per lo più si osservano modificazioni che suggeriscono prolungate riduzioni della ventilazione inframezzate, specie in coincidenza con i movimenti oculari rapidi, da ipopnee con caratteristiche a volte di tipo centrale, altre di tipo ostruttivo (5). 91 Figura 1 - Successione delle fasi di sonno e andamento della saturazione ossiemoglobinica durante la notte in un paziente con BPCO SaO2(%) 100 90 80 70 60 Stadio sonno W REM 1 2 3 1h 4 23:00 92 2:30 6:00 Per quanto riguarda la PaCO2, vi sono solo scarse informazioni sulle sue variazioni durante il sonno, per la difficoltà di ottenere sue misure sufficientemente accurate in modo non invasivo. I pochi dati disponibili indicano che essa aumenta (6), ma le sue variazioni sembrerebbero minori rispetto a quelle della SaO2. Alcuni pazienti presentano una casuale associazione tra la BPCO e la sindrome dell’apnea ostruttiva nel sonno (OSAS), associazione che rientra nel gruppo delle “overlap syndromes”, caratterizzate dalla sovrapposizione tra apnee ostruttive nel sonno e patologie polmonari (7). In questo caso, le alterazioni del pattern respiratorio e l’andamento della SaO2 nel sonno mantengono caratteristiche più simili a quelle dell’OSAS o della BPCO, secondo quale di queste condizioni sia maggiormente conclamata, e nel complesso determinano quadri clinici e funzionali più severi. Correlati dei disturbi respiratori nel sonno Vi è una correlazione significativa tra i valori di PaO2 diurni e quelli di SaO2 nel sonno. A parità di PaO2 mostrano peggiori desaturazioni nel sonno i soggetti più ipercapnici (8). Ciò è in accordo con la vecchia osservazione che i “pink puffers” presentano durante il sonno desaturazioni meno gravi rispetto ai “blue bloaters”. Vari studi hanno mostrato correlazioni significative tra risposte ventilatorie ad ipossia e ad ipercapnia misurate in veglia e desaturazioni notturne (9), ma non è chiaro quanto queste correlazioni siano indipendenti dai valori emogasanalitici. Una relazione tra l’ipossiemia notturna e il grado di ostruzione bronchiale non è stata sempre riscontrata, e se esiste, è certamente più debole rispetto a quella con i valori emogasanalitici. Il problema della comparsa di ipossiemia notturna si pone soprattutto per i pazienti con modesta ipossiemia in veglia, non tale da giustificare da sola un’ossigenoterapia a lungo termine. Infatti, è improbabile che pazienti con PaO2 elevata presentino ipossiemia nel sonno; per contro pazienti con livelli molto bassi di PaO2 non possono che essere ipossiemici anche nel sonno (in grado variabilmente maggiore che nella veglia) e ricevono un trattamento per la loro insufficienza respiratoria anche quando il comportamento dei loro scambi gassosi nel sonno non è rilevato strumentalmente. Nella popolazione dei pazienti con PaO2 comprese tra 60 e 70 mmHg la correlazione fra PaO2 diurna ed ipossiemia notturna non è tale da consentire di prevedere quali soggetti vadano incontro ad ipossiemia nel sonno. In questi pazienti solo un monitoraggio notturno consente di distinguere con certezza i “desaturatori” dai “non-desaturatori”. Due criteri sono stati proposti per definire i pazienti “desaturatori”: il primo è rappresentato dalla presenza di valori di SaO2 <90% per Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 9. Disturbi cardio-respiratori nel sonno nella BPCO - G. Insalaco, O. Marrone almeno il 30% della registrazione notturna (10); il secondo dalla presenza di cadute della SaO2 rispetto alla linea di base della durata di almeno 5 minuti, nella quale sia raggiunto un valore di SaO2 ≤85% (11). Patogenesi dei disordini respiratori notturni Durante la veglia e nel sonno non-REM la ventilazione è mantenuta in rapporto alle esigenze metaboliche. Nella veglia essa può essere modificata in funzione dello svolgimento di attività fisica e di esigenze comportamentali, come la fonazione; inoltre lo stesso stato di veglia fornisce uno stimolo continuo ai centri nervosi (drive di veglia) che riesce a mantenere la ventilazione anche in assenza di stimoli chimici efficaci (iperossia, ipocapnia). Nel sonno non-REM, variazioni delle tensioni dei gas arteriosi sono da imputare a due fenomeni: la rimozione del drive di veglia e l’aumento del carico resistivo dovuto all’incremento delle resistenze al flusso nelle alte vie aeree. L’aumento delle resistenze faringee è legato ad una riduzione del tono muscolare, che coinvolge anche i muscoli dilatatori faringei; questo causa una riduzione della ventilazione per una minor capacità di risposta al carico resistivo rispetto alla veglia. Il sonno REM è caratterizzato da una completa perdita dell’attività dei muscoli intercostali ed accessori della respirazione insieme con quella di tutti i muscoli ad attività tonica, da un’estrema riduzione della risposta ventilatoria agli stimoli chimici e da alterazioni del pattern respiratorio che diviene caratteristicamente irregolare in coincidenza con l’attività fasica (coincidente con i movimenti oculari rapidi) di questo stato di sonno (12). Le principali modificazioni a carico della respirazione nel sonno sono riportate nella seguente tabella per fase di sonno: NREM 1,2 NREM 3,4 REM tonico REM fasico Regolazione Metabolica Metabolica Metabolica Comportamentale Pattern respiratorio Periodico/Regolare Regolare Regolare/Irregolare Irregolare Risposta ventilatoria a O2 e CO2 Ridotta + Ridotta + Ridotta ++ Ridotta +++ Resistenze vie aeree superiori Normale Aumentata + Aumentata + Aumentata ++ Ventilazione minuto Ridotta + Ridotta ++ Ridotta +++ Variabile Attività dei muscoli intercostali e accessori Normale Assente Assente Assente Nei soggetti con BPCO, la più importante variazione della funzione respiratoria che interviene nel sonno REM è quella che riguarda l’attività muscolare (13). I pazienti con BPCO, specie se iperinsufflati, hanno una ridotta efficienza della contrazione diaframmatica. Quando il diaframma, come avviene nel sonno REM, diviene l’unico muscolo responsabile del mantenimento dell’attività respiratoria, la ventilazione minuto si riduce in misura maggiore che nei soggetti normali (14). Un’altra conseguenza della perdita di attività dei muscoli accessori può essere una riduzione della capacità funzionale residua. In realtà quest’ultima non è stata chiaramente dimostrata, salvo che in soggetti asmatici iperinsufflati (15). È comunque ritenuta una possibile causa di aumento del volume di chiusura, e quindi di una diminuzione del rapporto ventilazione/perfusione e di ipossiemia. La riduzione della responsività agli stimoli chimici nel sonno REM rispetto alla veglia, in soggetti con bassa responsività già in veglia, potrebbe teoricamente favorire lo sviluppo di un’importante ipossiemia, ma non è chiaro se essa svolga effettivamente un ruolo; la possibilità che essa entri in gioco è suggerita dall’osservazione di una correlazione tra risposta agli stimoli chimici in veglia e ipossiemia nel sonno rilevata sia in soggetti con BPCO (9), sia in soggetti sani in condizioni sperimentali (16). 93 Un certo contributo all’ipossiemia può essere fornito dal tipico pattern respiratorio rapido e poco profondo che spesso si verifica in coincidenza con i movimenti oculari rapidi, con conseguente aumento della ventilazione dello spazio morto e diminuzione della ventilazione alveolare. In conclusione, gli episodi di ipossiemia notturna riconoscono come meccanismi patogenetici: 1. Le alterazioni del rapporto ventilazione/perfusione, in parte spiegate dal decubito e dalla riduzione della capacità funzionale residua, in parte dall’abolizione del riflesso della tosse durante il sonno con possibile ristagno di secrezioni; 2. L’ipoventilazione secondaria allo stato di sonno (17). Quest’ultima costituisce la causa più importante dell’ipossiemia, che tende ad essere tanto più profonda quanto peggiore è la compromissione funzionale in veglia, sia dal punto di vista della meccanica respiratoria, sia, soprattutto, degli scambi gassosi. La forma della curva di dissociazione dell’ossigeno dall’emoglobina è il motivo principale per cui le cadute della SaO2 nel sonno sono più accentuate nei soggetti con livelli di PaO2 ridotti già in veglia. Conseguenze dei disturbi respiratori nel sonno 94 I pazienti con BPCO lamentano più disturbi del sonno, tra i quali, soprattutto risveglio precoce (18,19) rispetto a soggetti di controllo. Anche l’elettroencefalogramma dimostra spesso un sonno di cattiva qualità, con numerosi risvegli e relativa prevalenza di fasi di sonno leggero (20). Sembra che in assenza di apnee l’ipossiemia possa fornire al più un contributo trascurabile ad un peggioramento della qualità del sonno, come anche dimostrato dagli effetti incostanti dell’ossigenoterapia sulla struttura del sonno (21). È verosimile che un ruolo maggiore sia invece svolto dalla tosse, dalla dispnea o dall’uso di farmaci come la teofillina. Uno studio più recente, mirato ai pazienti con BPCO lieve, non ha trovato disturbi del sonno se non nei casi in cui coesistevano apnee (22). Persistono incertezze sul significato delle desaturazioni notturne in pazienti con BPCO senza ipossiemia nelle ore diurne. Sembra accertato che l’ipossiemia nel sonno favorisca un aumento delle aritmie cardiache, almeno nel caso di episodi ipossiemici piuttosto severi. La somministrazione di ossigeno previene l’aumento delle aritmie notturne (23). Non è noto se queste possano influenzare la prognosi dei pazienti con BPCO. È possibile che episodi di desaturazione ossiemoglobinica notturna possano provocare aumenti della pressione arteriosa sistemica. I dati della letteratura riguardanti questo aspetto sono comunque ad oggi molto limitati (24). Studi emodinamici eseguiti nel sonno hanno chiaramente dimostrato come la pressione arteriosa polmonare aumenti durante gli episodi ipossiemici (25). Alcuni dati della letteratura avevano suggerito un piú rapido deterioramento clinico, con progressivo aumento della pressione arteriosa polmonare (26,27), nei pazienti che desaturano nelle ore notturne rispetto ai non-desaturatori, e avevano indicato come con l’utilizzo di O2 durante il sonno la pressione arteriosa polmonare rimanesse invece stabile nel tempo (28). Tuttavia dati pubblicati successivamente suggeriscono che l’ipossiemia notturna di modesta entità, anche se prolungata per almeno il 30% della notte, non sia importante nell’evoluzione della malattia, e nessun vantaggio emodinamico sarebbe ottenuto dalla somministrazione notturna di O2 ai pazienti con desaturazioni esclusivamente notturne (29). La conseguenza potenzialmente più importante dell’ipossiemia notturna potrebbe essere un peggioramento della prognosi dei pazienti. Iniziali osservazioni su pazienti ricoverati per riacutizzazione di una BPCO indicavano come il decesso durante il ricovero fosse più frequente nelle ore della notte, suggerendo che l’ipossiemia nel sonno potesse compromettere in modo diretto ed immediato la sopravvivenza (30). Un successivo lavoro multicentrico su soggetti in ossigenoterapia Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 9. Disturbi cardio-respiratori nel sonno nella BPCO - G. Insalaco, O. Marrone studiati retrospettivamente ha però puntualizzato come in molti pazienti che muoiono nelle ore notturne il decesso non avvenga durante il sonno (31). Altri studi, infine, hanno valutato il valore prognostico dell’ipossiemia notturna, indipendentemente da quella diurna, nei pazienti con BPCO (32,33), ma non sono riusciti a dimostrare un suo effetto sfavorevole. Pertanto, il significato clinico delle desaturazioni notturne nella BPCO lieve-moderata e l’effetto della loro correzione rimangono ancora poco chiari. Quasi tutti gli studi su questo argomento hanno riguardato solo poche decine di individui. Sono necessari ulteriori studi su casistiche molto più numerose. Va sottolineato come i dati sopra riportati riguardino l’ipossiemia notturna da ipoventilazione, quella cioè che più tipicamente si osserva nella BPCO. Diverse possono essere le conseguenze dell’ipossiemia in caso di “overlap syndrome”. In pazienti con l’associazione tra BPCO ed apnee ostruttive è molto più frequente rispetto ai pazienti con sola BPCO, o con sola OSAS, il riscontro di ipertensione polmonare, insufficienza ventricolare destra, poliglobulia o sensazione di affaticamento sproporzionate alle alterazioni emogasanalitiche rilevate in veglia, come pure più frequente è il riscontro di alterazioni emogasanalitiche apparentemente sproporzionate rispetto al grado dell’ostruzione bronchiale (34). Monitoraggio notturno Il monitoraggio notturno della respirazione nella BPCO è volto a ricercare e quantificare la comparsa o il peggioramento degli scambi gassosi durante il sonno. A questo scopo si possono utilizzare la polisonnografia o monitoraggi più semplici come l’ossimetria. La polisonnografia consiste nel monitoraggio continuo e contemporaneo durante il sonno di più tipi di segnali che comunemente riguardano la funzione cardio-respiratoria e lo stato di vigilanza. Il pattern ventilatorio è studiato mediante il rilevamento del flusso aereo e dei movimenti toracoaddominali; l’ossigenazione arteriosa mediante rilevamento non invasivo della SaO2; lo stato di vigilanza mediante registrazione dell’elettroencefalogramma (EEG), elettrooculogramma (EOG) ed elettromiogramma (EMG) sottomentoiero. Il flusso aereo può essere rilevato con cannule nasali collegate ad un trasduttore di pressione; l’uso di termistori e termocoppie consente di identificare agevolmente le apnee, ma non altri tipi di disturbi respiratori caratterizzati da riduzioni parziali del flusso aereo. Il metodo non invasivo più accurato dal punto di vista quantitativo per il rilevamento dei movimenti respiratori è rappresentato dalla pletismografia induttiva. Più frequente è l’uso di altri tipi di sensori (piezoelettrici, impedenziometrici, strain gauge) che forniscono un segnale di tipo qualitativo. L’incoordinazione dei movimenti toraco-addominali può essere indice di vari eventi respiratori (ostruzione delle vie aeree, apnee ostruttive, condizioni di ostruzione parziale delle vie aeree superiori). Informazioni quantitative sullo sforzo respiratorio si ottengono con il monitoraggio della pressione esofagea ma, a causa della invasività del posizionamento del catetere esofageo, è più impiegato a fini di ricerca che di routine clinica. La SaO2, rilevata mediante ossimetria non invasiva, può essere analizzata con riferimento al tempo totale della registrazione o allo stadio di sonno. L’analisi del complesso dei segnali respiratori consente di rilevare, oltre al grado di ipossiemia, la presenza di disordini respiratori (“eventi”: apnee, ipopnee, limitazione di flusso). Nei pazienti con BPCO i parametri più utili nella analisi della SaO2 sono il livello di SaO2 medio e il tempo trascorso al di sotto di alcuni valori di riferimento di SaO2 (solitamente 90, 85 o 80%). Comunemente è segnalato anche il valore minimo di SaO2 nella notte. Il valore minimo di SaO2 raggiunto in media al termine di ogni desaturazione (“media dei minimi”) è un parametro poco utile nella BPCO pura, 95 96 mentre può essere utile nei casi di “overlap syndrome”. Come già accennato, frequenti eventi respiratori e desaturazioni caratterizzano l’”overlap syndrome”. La frequenza cardiaca è monitorata durante il sonno con una derivazione elettrocardiografica. In questo modo risulta agevole misurare la frequenza ed identificare eventuali turbe del ritmo. La frequenza cardiaca può essere ottenuta anche con i pulsossimetri, che la forniscono automaticamente mentre rilevano i valori di SaO2. La valutazione dello stato di vigilanza permette di correlare eventuali disturbi respiratori con la condizione di sonno e i suoi stadi. Più comunemente si utilizzano derivazioni EEG unipolari centrali (C3A2 e/o C4A1) e occipitali (O1A2 e/o O2A1). L’EOG consente il riconoscimento dei movimenti oculari. Movimenti oculari rapidi compaiono in veglia e nel sonno REM. L’EMG sottomentoniero fornisce una stima del tono muscolare, che normalmente diminuisce col passaggio dalla veglia al sonno e si annulla nel sonno REM. L’ossimetria può essere eseguita indipendentemente dalla polisonnografia. L’accuratezza dei saturimetri dipende dal tempo di risposta alle variazioni di SaO2 e dalla frequenza di campionamento del segnale da parte dello strumento, e può essere alterata da emoglobine patologiche, da elevati valori di metaemoglobina e carbossiemoglobina. In particolare, i saturimetri misurano la SaO2 come percentuale dell’emoglobina coniugata all’O2, escludendo dal calcolo l’emoglobina legata al CO. Pertanto, in soggetti con elevate percentuali di HbCO, come i fumatori, il rilevamento di elevati valori di SaO2 da parte di un ossimetro può condurre a conclusioni ingannevoli. Gli studi polisonnografici sono stati utili in passato a mettere in evidenza con precisione le modalità con cui i disturbi respiratori nel sonno si verificano. Oggi, in considerazione dell’elevato costo degli esami polisonnografici, della difficoltà di molti pazienti a tollerare questi complessi esami e della possibilità, nella maggior parte dei casi, di ottenere sufficienti informazioni con il solo, economico, monitoraggio saturimetrico, si tende ad utilizzare in modo diffuso quest’ultimo esame per la valutazione dell’ipossiemia notturna. Esso è eseguito soprattutto allo scopo di ottimizzare il trattamento con O2 (35). Nei pazienti con sintomi come dispnea, cefalea mattutina o con ipertensione polmonare o poliglobulia sproporzionati rispetto al quadro funzionale diurno sono indicati monitoraggi più complessi. Infatti, la maggior parte di questi pazienti presenta una “overlap syndrome”, per la dimostrazione della quale non è sufficiente la sola ossimetria. Trattamento dei disturbi respiratori nel sonno Nei soggetti in stato di riacutizzazione lo stato di sonno non può che accompagnarsi ad un peggioramento degli scambi gassosi. In questi pazienti, il trattamento dell’insufficienza respiratoria si avvale della ventiloterapia, che si è indiscutibilmente rivelata efficace (36), ma non vi sono indicazioni terapeutiche specifiche basate sul comportamento degli scambi gassosi nel sonno. Gli studi più approfonditi sulla respirazione nel sonno nella BPCO hanno finora riguardato soltanto pazienti in fase di stabilità clinica. In questi ultimi, nè la necessità, nè le modalità del trattamento dei disturbi respiratori nel sonno sono ancora ben chiarite. L’aspetto che richiama più discussioni è la necessità del trattamento dell’ipossia in eccesso rispetto a quella presente in veglia. La controversia è in rapporto all’incertezza, sopra riportata, sull’effettiva pericolosità dell’ipossiemia limitata alle ore notturne. Peraltro, esiste un solo studio che ha paragonato gli effetti sulla sopravvivenza di soggetti normossiemici in veglia ma desaturatori nella notte, trattati o non con ossigeno notturno: per quanto i dati suggerissero un effetto benefico del trattamento, non si osservavano differenze significative nella sopravvivenza tra i due gruppi, probabilmente per la scarsa numerosità del campione (28). Vi sono solo pochi studi sulla possibile efficacia di vari trattamenti farmacologici sull’ipossia notRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 9. Disturbi cardio-respiratori nel sonno nella BPCO - G. Insalaco, O. Marrone turna nella BPCO. Tra questi, un recente lavoro ha messo in evidenza come l’assunzione di tiotropio determina un lieve aumento della SaO2 senza interferire sulla qualità del sonno (37). Per i soggetti che rientrano nelle classiche indicazioni all’ossigenoterapia a lungo termine (38), si tende ad aumentare l’erogazione di ossigeno nelle ore notturne per cercare di prevenire le inevitabili desaturazioni nel sonno. È stato osservato però che non sempre è facile prevenire le desaturazioni notturne con l’aumento del flusso di ossigeno, specie nei soggetti più ipercapnici (39). Le desaturazioni notturne possono essere oggetto di trattamento ventilatorio anche in pazienti con BPCO in fase stabile. Si tende ad utilizzare soltanto ventilazione a pressione positiva, per lo più “bi-level”. Molti pazienti mostrano una scarsa compliance a questo trattamento. Le indicazioni sono limitate a soggetti ipercapnici. Tra questi, è stato proposto di istituire il trattamento ventilatorio, in associazione all’O2, in coloro che durante la notte mantengono valori di SaO2 ≤88% per almeno 5 minuti consecutivi nonostante la somministrazione di O2 al flusso di 2l/min (40). La prevenzione dell’aumento di PCO2 nel sonno, dimostrato in uno studio (41), andrebbe possibilmente ricercata durante monitoraggio notturno e può accompagnarsi ad un certo miglioramento dei valori emogasanalitici in veglia. Anche la qualità del sonno ed il numero di ricoveri potrebbero risentire beneficamente della ventiloterapia. Non è invece ancora stato dimostrato un suo effetto benefico sulla sopravvivenza (42). Un discorso a parte va fatto per i pazienti con “overlap syndrome”. Questi pazienti vanno sempre trattati mediante ventiloterapia notturna. Per l’eliminazione delle apnee ostruttive è sufficiente la ventilazione a pressione positiva continua (CPAP), ma spesso questa non è sufficiente a correggere l’ipossiemia nel sonno. Va allora valutato, sulla scorta dei risultati di monitoraggi notturni e di ripetute valutazioni emogasanalitiche diurne, se occorra sostituire la CPAP con una ventilazione “bi-level” e se sia necessario associare alla ventilazione meccanica la somministrazione di ossigeno. BIBLIOGRAFIA 1. Linee Guida GOLD. Progetto mondiale per la diagnosi e la prevenzione della broncopneumopatia cronica ostruttiva. In: L. Fabbri eds. “Time Science” International Medical Publisher. 2003. 2. Douglas NJ, White DP, Pickett CK, Weil JV, Zwillich CW. Respiration during sleep in normal man. Thorax 1982; 37: 840-844. 3. Catterall JR, Douglas NJ, Calverley PM, Shapiro CM, Brezinova V, Brash HM, Flenley DC. Transient hypoxemia during sleep in chronic obstructive pulmonary disease is not a sleep apnea syndrome. Am Rev Respir Dis 1983; 128: 24-29. 4. Bonsignore G, Marrone O, Macaluso C, Salvaggio A, Stallone A, Bellia V. Validation of oximetry as a screening test for obstructive sleep apnoea syndrome. Eur Respir J Suppl 1990; 11: 542s-544s. 5. White JE, Drinnan MJ, Smithson AJ, Griffiths CJ, Gibson GJ. Respiratory muscle activity during rapid eye movement (REM) sleep in patients with chronic obstructive pulmonary disease. Thorax 1995; 50: 376-382. 6. O’Donoghue FJ, Catcheside PG, Ellis EE, Grunstein RR, Pierce RJ, Rowland LS, Collins ER, Rochford SE, McEvoy RD. Australian trial of Noninvasive Ventilation in Chronic Airflow Limitation investigators. Sleep hypoventilation in hypercapnic chronic obstructive pulmonary disease: prevalence and associated factors. Eur Respir J 2003; 21: 977-984. 7. Flenley DC. Sleep in chronic obstructive lung disease. Clin Chest Med 1985; 6: 651-661. 8. Bradley TD, Mateika J, Li D, Avendano M, Goldstein RS. Daytime hypercapnia in the development of nocturnal hypoxemia in COPD. Chest 1990; 97: 308-312. 9. Tatsumi K, Kimura H, Kunitomo F, Kuriyama T, Watanabe S, Honda Y. Sleep arterial oxygen desaturation and chemical control of breathing during wakefulness in COPD. Chest 1986; 90: 68-73. 10. Levi-Valensi P, Aubry P, Rida Z. Nocturnal hypoxemia and long-term oxygen therapy in COPD patients with daytime PaO2 60-70 mmHg. Lung 1990; 168 Suppl: 770-775. 11. Fletcher EC, Miller J, Divine GW, Fletcher JG, Miller T. Nocturnal oxyhemoglobin desaturation in COPD patients with arterial oxygen tensions above 60 mmHg. Chest 1987; 92: 604-608. 12. Phillipson EA. Control of breathing during sleep. In: NS Cherniack, JS Widdicombe (eds). Handbook of Physiology – The respiratory system. Control of breathing (vol II, part 2). Waverly Press Inc, Bethesda MD/Am. Physiol.Soc., 1986, sect III; 649-689. 13. Johnson MW, Remmers JE. Accessory muscle activity during sleep in chronic obstructive pulmonary disease. J Appl Physiol 1984; 57: 1011-1017. 14. Ballard RD, Clover CW, Suh BY. Influence of sleep on respiratory function in emphysema. Am J Respir Crit Care Med. 1995; 151: 945951. 15. Ballard RD, Irvin CG, Martin RJ, Pak J, Pandey R, White DP. Influence of sleep on lung volume in asthmatic patients and normal subjects. 97 98 J Appl Physiol 1990; 68: 2034-2041. 16. Dunroy HM, Adams L, Corfield DR, Morrell MJ. CO2 retention in lung disease; could there be a pre-existing difference in respiratory physiology. Respir Physiol Neurobiol 2003; 136: 179-186. 17. Hudgel DW, Martin RJ, Capehart M, Johnson B, Hill P. Contribution of hypoventilation to sleep oxygen desaturation in chronic obstructive pulmonary disease. J Appl Physiol 1983; 55: 669-677. 18. Klink ME, Dodge R, Quan SF. The relation of sleep complaints to respiratory symptoms in a general population. Chest 1994; 105: 151154. 19. Bellia V, Catalano F, Scichilone N, Incalzi RA, Spatafora M, Vergani C, Rengo F. Sleep disorders in the elderly with and without chronic airflow obstruction: the SARA study. Sleep 2003; 26: 318-323. 20. Brezinova V, Catterall JR, Douglas NJ, Calverley PM, Flenley DC. Night sleep of patients with chronic ventilatory failure and age matched controls: number and duration of the EEG episodes of intervening wakefulness and drowsiness. Sleep 1982; 5: 123-130. 21. McKeon JL, Murree-Allen K, Saunders NA. Supplemental oxygen and quality of sleep in patients with chronic obstructive lung disease. Thorax 1989; 44: 184-188. 22. Sanders MH, Newman AB, Haggerty CL, Redline S, Lebowitz M, Samet J, O’Connor GT, Punjabi NM, Shahar E. Sleep Heart Health Study. Sleep and sleep-disordered breathing in adults with predominantly mild obstructive airway disease. Am J Respir Crit Care Med 2003; 167: 7-14. 23. Tirlapur VG, Mir MA. Nocturnal hypoxemia and associated electrocardiographic changes in patients with chronic obstructive airways disease. N Engl J Med 1982; 306: 125-130. 24. Shepard JW, Schweitzer PK, Keller CA, Chun DS, Dolan GF. Myocardial stress. Exercise versus sleep in patients with COPD. Chest 1984; 86: 366-374. 25. Coccagna G, Lugaresi E. Arterial blood gases and pulmonary and systemic arterial pressure during sleep in chronic obstructive pulmonary disease. Sleep 1978; 1: 117-124. 26. Fletcher EC, Luckett RA, Miller T, Costarangos C, Kutka N, Fletcher JG. Pulmonary vascular hemodynamics in chronic lung disease patients with and without oxyhemoglobin desaturation during sleep. Chest 1989; 95: 757-764. 27. Levi-Valensi P, Weitzenblum E, Rida Z, Aubry P, Braghiroli A, Donner C, Aprill M, Zielinski J, Würtemberger G. Sleep-related oxygen desaturation and daytime pulmonary haemodynamics in COPD patients. Eur Respir J 1992; 5: 301-307. 28. Fletcher EC, Luckett RA, Goodnight-White S, Miller CC, Qian W, Costarangos-Galarza C. A double-blind trial of nocturnal supplemental oxygen for sleep desaturation in patients with chronic obstructive pulmonary disease and a daytime PaO2 above 60 mmHg. Am Rev Respir Dis 1992; 145: 1070-1076. 29. Chaouat A, Weitzenblum E, Kessler R, Charpentier C, Enrhart M, Schott R, Levi-Valensi P, Zielinski J, Delaunois L, Cornudella R, Moutinho dos Santos J. A randomized trial of nocturnal oxygen therapy in chronic obstructive pulmonary disease patients. Eur Respir J 1999; 14: 1002-1008. 30. McNicholas WT, Fitzgerald MX. Nocturnal deaths among patients with chronic bronchitis and emphysema. Br Med J 1984; 289: 878. 31. Zielinski J, MacNee W, Wedzicha J, Ambrosino N, Braghiroli A, Dolensky J, Howard P, Gorzelak K, Lahdensuo A, Strom K, Tobiasz M, Weitzenblum E. Causes of death in patients with COPD and chronic respiratory failure. Monaldi Arch Chest Dis 1997; 52: 43-47. 32. Connaughton JJ, Catterall JR, Elton RA, Stradling JR, Douglas NJ. Do sleep studies contribute to the management of patients with severe chronic obstructive pulmonary disease? Am Rev Respir Dis 1988; 138: 341-344. 33. Chaouat A, Weitzenblum E, Kessler R, Schott R, Charpentier C, Levi-Valensi P, Zielinski J, Delaunois L, Cornudella R, Moutinho dos Santos J. Outcome of COPD patients with mild daytime hypoxaemia with or without sleep-related oxygen desaturation. Eur Respir J 2001; 17: 848-855. 34. Chaouat A, Weitzenblum E, Krieger J, Ifoundza T, Oswald M, Kessler R. Association of chronic obstructive pulmonary disease and sleep apnea syndrome. Am J Respir Crit Care Med 1995; 151: 82-86. 35. Indications and standards for cardiopulmonary sleep studies. American Thoracic Society. Medical Section of the American Lung Association. Am Rev Respir Dis 1989; 139: 559-568. 36. Brochard L, Mancebo J, Wysocki M, Lofaso F, Conti G, Rauss A, Simonneau G, Benito S, Gasparetto A, Lemaire F, et al. Noninvasive ventilation for acute exacerbations of chronic obstructive pulmonary disease. N Engl J Med 1995; 333: 817-822. 37. McNicholas WT, Calverley PM, Lee A, Edwards JC. Tiotropium Sleep Study in COPD Investigators. Long-acting inhaled anticholinergic therapy improves sleeping oxygen saturation. Eur Respir J 2004; 23: 825-831. 38. Nocturnal oxygen therapy trial group. Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease: a clinical trial. Ann Intern Med 1980; 93: 391-398. 39. Plywaczewski R, Sliwinski P, Nowinski A, Kaminski D, Zielinski J. Incidence of nocturnal desaturation while breathing oxygen in COPD patients undergoing long-term oxygen therapy. Chest 2000; 117: 679-683. 40. Consensus Conference: Clinical Indications for Noninvasive Positive Pressure Ventilation in Chronic Respiratory Failure Due to Restrictive Lung Disease, COPD, and Nocturnal Hypoventilation—A Consensus Conference Report. Chest 1999;116:521-534. 41. Meecham Jones DJ, Paul EA, Jones PW, Wedzicha JA. Nasal pressure support ventilation plus oxygen compared with oxygen therapy alone in hypercapnic COPD. Am J Respir Crit Care Med 1995; 152: 538-544. 42. Clini E, Sturani C, Rossi A, Viaggi S, Corrado A, Donner CF, Ambrosino N on behalf of the Rehabilitation and Chronic Care Study Group, Italian Association of Hospital Pulmonologists (AIPO). The Italian multicentre study on noninvasive ventilation in chronic obstructive pulmonary disease patients. Eur Respir J 2002; 20: 529-538. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 9. Disturbi cardio-respiratori nel sonno nella BPCO - G. Insalaco, O. Marrone 99 10. Terapia e prevenzione A cura di Lorenzo Corbetta Clinica di Malattie dell’Apparato Respiratorio Università degli Studi di Modena e Reggio Emilia, Modena 10. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione La broncopneumopatia cronica ostruttiva (BPCO) è una malattia scarsamente reversibile per quanto riguarda le alterazioni funzionali e anatomo-patologiche ma trattabile con possibilità di successo dal punto di vista clinico. Le caratteristiche patologiche della malattia e la tipologia del paziente affetto da BPCO che è spesso un fumatore che “si autoinfligge” la malattia inducono erroneamente medici e pazienti a un atteggiamento fatalistico che porta ad una sottostima della malattia e a una sottovalutazione delle possibilità terapeutiche. Premesso che la cessazione del fumo di sigaretta resta l’unico trattamento in grado di rallentare la progressione della BPCO, è necessario ricordare che esistono trattamenti farmacologici e riabilitativi in grado di migliorare i sintomi, aumentare la tolleranza all’esercizio fisico e ridurre le riacutizzazioni, migliorando alla fine la qualità di vita del paziente. Inoltre un corretto trattamento domiciliare delle riacutizzazioni permette al paziente di evitare il disagio del ricovero e del trattamento intensivo. È opportuno quindi considerare l’intervento terapeutico dalla prospettiva del paziente, che non è solo interessato al miglioramento della funzionalità polmonare come tale, ma soprattutto alla riduzione di sintomi estremamente invalidanti come dispnea, tosse e catarro, ad avere meno riacutizzazioni e meno ricoveri, a poter svolgere senza limitazioni le comuni attività quotidiane come lavorare, camminare, vestirsi, lavarsi e avere rapporti sessuali. In assenza di farmaci in grado di modificare la storia naturale della malattia, i pazienti possono pertanto trarre beneficio da programmi individualizzati integrati che impiegano terapie farmacologiche e non farmacologiche in grado di raggiungere “outcomes” diversi. Dal 2001 la Global Initiative for Chronic Obstructive Lung Disease (GOLD) in collaborazione con l’Organizzazione Mondiale della Sanità, ha realizzato Linee Guida che vengono aggiornate annualmente sulla diagnosi e i trattamenti di provata efficacia per la BPCO (1,2); in seguito sono inoltre state pubblicate Linee Guida da parte delle più importanti Società Scientifiche Internazionali come la British Toracic Society (BTS)(3) l’American Thoracic Society (ATS) in collaborazione con l’European Respiratory Society (ERS)(4) e la Canadian Thoracic Society (CTS) (5). Tali Linee Guida sono caratterizzate da un approccio “evidence based” con assegnazione di livelli di evidenza alle raccomandazioni contenute nei documenti (tab. 1). Tabella 1 – Descrizione dei livelli di evidenza (1) LIVELLO FONTE A Studi randomizzati, controllati (RCT) Elevato numero di studi B Studi randomizzati, controllati (RCT) Scarso numero di studi C Studi non randomizzati Studi osservazionali D Giudizio di un Gruppo di Esperti Strategia terapeutica basata sulla gravità della BPCO Lo strategia terapeutica della BPCO in fase stabile raccomandata pressoché uniformemente dalle Linee Guida più accreditate (1-5) prevede uno schema a gradini, cumulativo, con un crescendo del trattamento in rapporto alla gravità della malattia, iniziando dall’intervento preventivo sull’eliminazione dei fattori di rischio e proseguendo con l’aggiunta e integrazione di trattamenti farmacologici e non farmacologici. Nella BPCO, rispetto all’asma bronchiale, non è normalmente possibile ridurre la terapia una volta raggiunto il controllo della sintomatologia; al con- 101 trario la progressione della malattia e del danno funzione respiratorio caratteristico della BPCO richiede la somministrazione del trattamento per periodi molto lunghi con necessità spesso di incrementare il trattamento. La disponibilità di trattamenti farmacologici con meccanismo d’azione diverso offre inoltre la possibilità di sostituire o integrare diverse classi di farmaci individualizzando il piano terapeutico al singolo paziente attraverso un attento monitoraggio degli effetti del trattamento (6). Il trattamento mira a raggiungere i seguenti obiettivi nella BPCO (1): - prevenire l’evoluzione della malattia; - migliorare i sintomi; - migliorare la tolleranza allo sforzo; - migliorare la qualità di vita; - prevenire e trattare le complicanze; - prevenire e trattare le riacutizzazioni; - ridurre la mortalità. 102 Questi obiettivi dovrebbero essere raggiunti con una trascurabile incidenza degli effetti collaterali. La figura 1 fornisce un riassunto di questa strategia terapeutica “a step” basata sulla gravità della BPCO. In pratica tutti i pazienti dovrebbero essere sottoposti ad intervento per la cessazione del fumo di sigaretta. In pazienti con sintomi modesti o saltuari e con minima ostruzione bronchiale (Stadio I: BPCO lieve) è sufficiente una terapia al bisogno con farmaci a breve durata d’azione per controllare i sintomi, in particolare dispnea o tosse. In pazienti compresi fra lo Stadio II (BPCO moderata) e lo Stadio IV (BPCO molto grave), i cui sintomi non sono controllati con broncodilatatori a breve durata d’azione al bisogno e con chiari segni di limitazione al flusso aereo (VEMS <80% del teorico con VEMS/CVF <70), è raccomandata la somministrazione regolare di broncodilatatori a lunga durata d’azione (Evidenza A) ed un programma di riabilitazione. In pazienti con un VEMS misurato dopo broncodilatazione inferiore al 50% del teorico (Stadio III: BPCO grave e Stadio IV: BPCO molto grave) ed una storia di ripetute riacutizzazioni (per esempio 3 negli ultimi 3 anni) un trattamento regolare con corticosteroidi per via inalatoria riduce la frequenza delle riacutizzazioni e migliora la qualità di vita (Evidenza A) (1,2). Figura 1 – Terapia della BPCO ad ogni stadio t Trat a to men a st ep + O2 terapia a lungo termine in caso di insufficienza respiratoria considerare NIV e trattamenti chirurgici + Steroidi per via inalatoria in caso di ripetute riacutizzazioni + Trattamento regolare con uno o più broncodilatatori a lunga durata d’azione + riabilitazione + Broncodilatatori a breve durata d’azione al bisogno EVITARE I FATTORI DI RISCHIO; VACCINAZIONI ANTINFLUENZALE Caratteristiche • Sintomi cronici • Esposizione a fattori di rischio • Spirometria normale • FEV1/CVF <70% • FEV1 ≥80% • Con o senza sintomi • FEV1/CVF <70% • FEV1/CVF <70% • FEV1/CVF <70% • 50% >FEV1 <80% • 30% >FEV1 <50% FEV1 <30% o • Con o senza • Con o senza presenza di sintomi sintomi insufficienza respiratoria cronica o scompenso cardiaco destro STADIO 0: A RISCHIO I: LIEVE II : MODERATA III: GRAVE PROGRESSIONE DELLA MALATTIA IV: MOLTO GRAVE Sintomi Tosse produttiva Dispnea-Riacutizzazioni FEV1 Disabilità-Insufficienza Respiratoria Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta Riduzione dei fattori di rischio Cessazione del fumo di sigaretta: il controllo della BPCO inizia con la prevenzione, diretta principalmente sul fumo di sigaretta. Un programma completo per la cessazione del fumo richiede un approccio multidisciplinare che comprende l’educazione sanitaria, le politiche pubbliche e i programmi di informazione rivolti a scoraggiare tale abitudine a cui devono essere affiancati programmi diretti alla sospensione dell’abitudine tabagica in soggetti che soffrono già di BPCO e in soggetti considerati a rischio di BPCO in quanto fumatori. La sospensione dell’abitudine tabagica è l’intervento più efficace ed economicamente più vantaggioso per ridurre il rischio di sviluppare la BPCO e per fermarne la progressione (fig. 2) (1,6) poiché rallenta il declino della funzione respiratoria ed in particolare del VEMS che nella BPCO è accelerato, riduce i sintomi e la reattività bronchiale. Figura 2 – Effetti del fumo e della sua cessazione sulla funzione polmonare Non fumatori o fumarori suscettibili ai danni da fumo 100 FEV1 75 Fumatori suscettibili ai danni da fumo Sospensione del fumo a 45 anni 50 Disabilità Sospensione del fumo a 65 anni 25 Mortalità Età (anni) 25 50 75 Fletcher and Peto, BMJ 1977, 1, 1645-1648 La dipendenza da fumo è attualmente riconosciuto come una dipendenza a cui contribuiscono fattori genetici ed ambientali in cui la nicotina gioca un ruolo importante. Per la cessazione del fumo sul singolo paziente è raccomandato un approccio multidisciplinare che prevede un programma integrato comportamentale e farmacologico. Il supporto comportamentale: i risultati del supporto comportamentale sono strettamente correlati al numero e alla durata degli incontri con i fumatori con risultati che raggiungono il 20% dei partecipanti rispetto al 2% dei tentativi senza alcun supporto. L’approccio cognitivo-comportamentale proprio del trattamento di gruppo può essere sostituito in certi casi con un approccio individuale che meglio si adatta alla situazione ambulatoriale dove operano prevalentemente il medico di Medicina generale e lo specialista pneumologo e che presenta il vantaggio del rapporto personale tra paziente e medico e la possibilità di associare un trattamento farmacologico (7-9). Anche brevi incontri di counseling individuale diretti a chi non può o non vuole partecipare a interventi comportamentali intensivi e di gruppo possono raggiungere risultati fino al 6% (6). Il Rapporto del Public Health Service per aiutare gli operatori sanitari interessati a migliorare le loro abilità dissuasorie contro il fumo suggerisce un programma di intervento che si articola in 5 (10,11) punti (le 5 A) per identificare e supportare chi vuole smettere di fumare : 1. Chiedere (Ask): identificare sistematicamente tutti i fumatori ad ogni visita; 2. Consigliare (Advise): invitare decisamente tutti i fumatori a smettere; 3. Valutare (Asses): la volontà del fumatore di smettere; 103 4. Assistere (Assist): aiutare il paziente a smettere; 5. Organizzare (Arrange): un programma di follow-up. Sempre in 5 punti (le 5 R) si articola il programma per motivare i fumatori che non intendono smettere di fumare: 1. Rilevanza (Rilevance): per ogni singolo paziente; 2. Rischi (Risk): presentare i rischi di continuare a fumare; 3. Benefici (Rewards): presentare i benefici dello smettere; 4. Barriere (Roadblocks): identificare le barriere; 5. Ripetizione (Repetition): rinforzare ad ogni visita il messaggio motivazionale. Terapia farmacologica: sono oggigiorno disponibili diverse terapie farmacologiche efficaci per la sospensione dell’abitudine tabagica. 104 1. Terapia sostitutiva con nicotina I prodotti sostitutivi della nicotina aumentano il successo dell’intervento per la sospensione dell’abitudine tabagica indipendentemente dagli interventi comportamentali o psicosociali. Dunque, l’uso di terapia sostitutiva con nicotina dovrebbe essere utilizzata in tutti i fumatori che non sono stati in grado di smettere spontaneamente e che non presentino serie controindicazioni (angina instabile, ulcera peptica non trattata, recente infarto del miocardio o ictus) (1,6). Nel Lung Health Study, un trial clinico controllato multicentrico, è stata utilizzata la seguente combinazione: il consiglio del medico, il gruppo di supporto, esercizi di abilità e la terapia sostitutiva con nicotina, con un tasso di sospensione ad un anno del 35%, mantenuto del 22% a distanza di 5 anni. Nello stesso studio è stato dimostrato che il declino del VEMS era significativamente inferiore nel gruppo che aveva smesso di fumare rispetto ai fumatori (13-16). Tutte le forme di terapia sostitutiva con nicotina sono considerevolmente più efficaci del placebo, nonostante il cerotto sia di solito preferito rispetto alla preparazione in gomma da masticare per la migliore facilità d’uso. I prodotti contenenti nicotina sono stati meno studiati nei modesti fumatori che sono spesso in grado di smettere più facilmente. In tale categoria è necessario considerare la somministrazione di una dose iniziale più bassa nei cerotti o nella gomma da masticare. a) Cerotti di nicotina: i cerotti sono la modalità più utlizzata e rappresentano la prima scelta: sono disponibili in dosaggi differenti (5-10-15 mg durata d’azione 16 ore; 7-14-21 mg durata d’azione 24 ore; 15-30 mg/24 ore). Nel prescrivere il dosaggio, il medico deve principalmente tener conto del numero di sigarette fumate e del punteggio raggiunto nel Test di Fagerstrom unitamente alla misurazione del CO nell’espirato. Ad un fumatore medio (20 sig./die; Test di Fagerstrom tra 5 e 7) si potrà prescrivere un dosaggio iniziale di 15 mg da scalare regolarmente nei mesi successivi. b) Gomme da masticare di nicotina: esistono due dosaggi: 2 e 4 mg. Dal primo dosaggio il paziente può avere a disposizione circa 0,8 mg di nicotina; dal secondo circa 1,2 mg. In generale si può consigliare al fumatore di masticare una gomma in sostituzione di ogni sigaretta, in altri termini almeno una gomma/ora per avere una corretta copertura. Il dosaggio di 2 mg dovrebbe essere utilizzato dai pazienti con un Test di Fagerstrom inferiore a 6 ed un basso numero di sigarette fumate e il dosaggio superiore (4 mg) per gli altri. La corretta tecnica di assunzione consiste nel masticarle lentamente. Il fumatore deve fermarsi dopo i primi 5-10 atti masticatori e riprendere dopo una pausa. Ogni gomma va masticata per circa 20-30 minuti. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta c) Inalatori di nicotina: la nicotina è contenuta in cartucce (10 mg) e viene vaporizzata ad ogni inspirazione. La nicotina viene assorbita attraverso il cavo orale e le prime vie respiratorie. L’inalatore garantisce la gratificazione della gestualità e della stimolazione orale della sigaretta senza avere il potenziale di innescare tossicodipendenza. Quando il fumatore sente il bisogno della sigaretta deve semplicemente portare alla bocca l’inalatore e aspirare. Il dosaggio deve essere personalizzato: da 4 a 10 cartucce al giorno. Utile l’associazione con il cerotto. d) Compresse sub-linguali di nicotina: hanno la stessa indicazione delle gomme. La compressa deve essere posta sotto la lingua dove si dissolve lentamente (circa 30 minuti). La dose deve essere personalizzata come per le altre formulazioni in base al numero di sigarette fumate e del punteggio raggiunto nel Test di Fagerstrom unitamente alla misurazione del CO nell’espirato. Inizialmente si consiglia l’assunzione di una compressa ogni 1 o 2 ore; la dose mediamente utilizzata è di 8-12 compresse al giorno. La dose può essere raddoppiata fino a raggiungere una dose giornaliera di 16-24 compresse. 2. Bupropione Il farmaco sembra agire inibendo il re-uptake neuronale della dopamina e della noradrenalina con un conseguente effetto sul meccanismo biochimico della dipendenza da nicotina attenuando il desiderio di fumare e la sindrome di astinenza nei pazienti che smettono. Il trattamento deve iniziare mentre il paziente è ancora fumatore. Deve smettere di fumare entro la seconda settimana. La dose iniziale è di 150 mg da assumere una volta al giorno per sei giorni, aumentando a 150 mg due volte al giorno a partire dal settimo giorno. Il bupropione combinato con la terapia sostitutiva con nicotina aumenta la percentuale di successo. L’uso di questo farmaco è controindicato nei soggetti con anamnesi di epilessia. 105 Trattamento di fondo della BPCO Il trattamento di fondo della BPCO prevede un progressivo incremento dei farmaci che vanno integrati con il trattamento non farmacologico (riabilitazione, ossigenoterapia domiciliare, ventilazione non invasiva, terapia chirurgica) basandosi sulla gravità della malattia. (fig. 1 - tab. 2). La gravità è determinata principalmente dalla riduzione del flusso aereo espiratorio e quindi dalla spirometria, ma anche da altri fattori quali la gravità dei sintomi, la frequenza e la gravità delle riacutizzazioni, l’insorgenza di complicanze, la presenza di insufficienza respiratoria, di comorbidità (malattie cardiovascolari, patologie legate al sonno, etc.) e dallo stato di salute complessivo del paziente. La classificazione basata sulla funzione respiratoria e soprattutto sulla riduzione del VEMS rispetto al teorico raccomandato dalle principali Linee Guida, sebbene arbitraria, rappresenta comunque il criterio più semplice ed efficace (1,3). Tabella 2 – Principali trattamenti farmacologici e non farmacologici di fondo della BPCO TRATTAMENTI FARMACOLOGICI Categorie di farmaci utilizzati β2-agonisti e anticolinergici (A) Corticosteroidi inalatori (A) Vaccino anti-influenzale (A) Teofillina (B) Immunomodulatori (B) Antiossidanti (B) Mucolitici (D) TRATTAMENTI NON FARMACOLOGICI Riabilitazione Ossigenoterapia a lungo termine Ventilazione meccanica a lungo termine Terapia chirurgica Progetto Mondiale BPCO Terapia farmacologica: la terapia farmacologica di fondo ha lo scopo di prevenire e controllare i sintomi, ridurre la frequenza e la gravità delle riacutizzazioni, migliorare lo stato di salute e la tolleranza allo sforzo. I farmaci raccomandati sono i broncodilatatori (β2-agonisti, anticolinergici) e gli steroidi, con preferenza per la via inalatoria. La teofillina è un broncodilatatore il cui uso deve essere valutato nel singolo paziente in termini di rapporto rischio/beneficio, in considerazione dei possibili effetti collaterali e della necessità di monitoraggio dei livelli plasmatici. Nessuno dei farmaci disponibili nel trattamento della BPCO (tab. 3) è efficace nel modificare la progressiva riduzione del flusso aereo espiratorio che è l’elemento caratteristico della malattia ma ne è raccomandato l’uso per ridurre la morbilità e migliorare la qualità di vita. Tabella 3 – Farmaci comunemente utilizzati nel trattamento della BPCO [Modificata da voce bibliografica 1] FARMACIa INALATORI PREDOSATI (µg)b AEROSOL (mg/ml)b VIA ORALE (mg) DURATA D’AZIONE (ore) 0,1 5 -4 4-6 β2-agonisti: a breve durata d’azione Fenoterolo Salbutamolo (albuterolo) Terbutalina 100-200 100-200 500 4-6 β2-agonisti: a lunga durata d’azione Formoterolo Salmeterolo 4,5-1,2 25-50 --- 12+ 12+ --- 6-8 7-9 Anticolinergici: a breve durata d’azione 106 Ipratropio bromuro Oxitropio bromuro 20-40 100 0,25-0,5 1,5 Anticolinergici: a lunga durata d’azione Tiotropio 18 24+ Combinazione dei β2-agonisti a breve durata d’azione con gli anticolinergici somministrati in un unico inalatore Fenoterolo/ipratropio Salbutamolo/ipratropio 100/40 75/15 1,25/0,5 --- --- 6-8 6-8 Metilxanthine Aminofillina (LR) Teofillina (LR) 200-600 100-600 Variabile fino a 24 Variabile fino a 24 Glucocorticosteroidi somministrati per via inalatoria Beclometasone Budesonide Flunisolide Fluticasone 100-400 100-400 250 100-500 0,2-0,4 0,2-0,25-0,5 0,5-1 0,25-1 Combinazione dei β2-agonisti a lunga durata d’azione con i glucocortisteroidi somministrati in un unico inalatore Formoterolo/budesonide Salmeterolo/fluticasone 4,5-9/160-320 25/50-125/250 50/100-250/500 Steroidi sistemici Prednisone Metil-prednisolone 5-60 4-16 a: dosi: la dose dei β2-agonisti si riferisce ad un dosaggio medio ripetibile fino a quattro volte al giorno nel caso delle molecole a breve durata d’azione e fino a 2 volte al giorno nel caso delle molecole a lunga durata d’azione (salmeterolo, formoterolo); gli anticolinergici a breve durata d’azione vengono in genere somministrati 3-4 al giorno mentre quelli a lunga durata d’azione (tiotropio) 1 sola volta al giorno. b: le metilxantine richiedono il monitoraggio della concentrazione plasmatica da cui dipende il dosaggio da somministrare, che condiziona sia l’insorgenza di effetti collaterali sia i livelli plasmatici. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta 1. Broncodilatatori I farmaci broncodilatatori hanno un ruolo centrale nel trattamento sintomatico e nel trattamento regolare della BPCO (Evidenza A). Sono denominati broncodilatatori i farmaci che migliorano il VEMS o modificano altri parametri spirometrici, di solito agendo sul tono della muscolatura liscia bronchiale. Questi farmaci riducono inoltre il volume residuo, tendono a ridurre l’insufflazione polmonare a riposo e durante lo sforzo e migliorano la performance ventilatoria durante l’esercizio. Per questo motivo nelle forme moderate e severe le variazioni del VEMS non rappresentano l’unico indice predittivo dell’efficacia del trattamento e la presenza di reversibilità del VEMS non è un criterio indispensabile per la prescrizione dei broncodilatatori. Infatti nel BPCO moderato-grave i broncodilalatori possono migliorare solo parzialmente il VEMS ma indurre un miglioramento dei sintomi agendo sull’iperdistensione dinamica che impedisce al polmone di raggiungere il suo volume di rilasciamento durante l’espirazione. Ad esempio un paziente con un VEMS di 1500 ml che ha un valore di base intorno al 35% del suo valore teorico, anche se migliora di 300 ml dopo l’assunzione di broncodilatatore resterà sempre marcatamente sotto la norma. Il paziente percepisce comunque un beneficio dall’uso di questi farmaci perchè viene ridotta l’iperinflazione dinamica sotto sforzo. Come risultato clinico si ottiene un miglioramento dei sintomi, una maggior tolleranza allo sforzo, una miglior qualità di vita e inoltre una riduzione del numero di riacutizzazioni (6). Vi sono 3 classi principali di broncodilatatori: β2-agonisti, anticolinergici e metilxantine. a) β2-agonisti: agiscono sui ß recettori delle vie aeree; il capostipite è il salbutamolo che è un β2agonista a breve durata d’azione per cui viene somministrato al bisogno per alleviare i sintomi nella BPCO lieve o il riacutizzarsi della dispnea nelle forme moderato-gravi. L’effetto inizia dopo 5 minuti, raggiunge il picco entro 30 minuti e persiste per 2-4 ore. Tale effetto è utile nel paziente asmatico in cui la crisi asmatica è spesso improvvisa in risposta a determinati stimoli; lo è meno nel BPCO in cui la dispnea è costante e peggiorata eventualmente dall’esercizio fisico. Il paziente con BPCO necessita pertanto di una broncodilatazione continua per cui sono preferibili broncodilatori con azioni più prolungata, i cosiddetti β2-agonisti a lunga durata d’azione (salmeterolo, formoterolo) che hanno effetto per 12 ore senza una riduzione della loro efficacia durante la notte con l’uso regolare; possono perciò essere somministrati 2 volte al giorno per prevenire o migliorare i sintomi e per aumentare la tolleranza allo sforzo. Per tale motivo le Linee Guida ritengono più conveniente l’uso dei broncodilatatori a lunga durata d’azione nelle forme di BPCO da moderata a molto grave (1-4,19,20). Salmeterolo è un agonista parziale con un effetto più ritardato rispetto al salbutamolo, che inizia dopo 30’ dalla somministrazione, ha un picco dopo 2 ore e persiste 12 ore. Formoterolo è un agonista completo con azione rapida come salbutamolo e durata di 12 ore. Gli effetti collaterali dei β2-agonisti sono prevedibili e dose-dipendenti per cui non è conveniente andare oltre le dosi consigliate. Sono meno frequenti e si risolvono più rapidamente quando somministrati per via inalatoria piuttosto che per via orale anche se è necessario prestare maggiore attenzione alla corretta assunzione del farmaco. Per questo motivo è sempre preferibile la via inalatoria rispetto a quella orale che è stata quasi completamente abbandonata. La stimolazione dei β2-recettori può determinare tachicardia sinusale ed è in grado di aggravare un’aritmia cardiaca preesistente in pazienti suscettibili; tali eventi sono tuttavia rari con la somministrazione del farmaco per via inalatoria. In soggetti anziani trattati con alte dosi di β2-agonisti può comparire tremore, indipendentemente dalla modalità di somministrazione, limitando così la dose che può essere tollerata. Sebbene possa insorgere ipokaliemia, specialmente quando si associa un trattamento con diuretici tiazidici, ed il consumo di ossigeno possa risultare aumentato in condizioni di 107 riposo, questi effetti metabolici presentano tachifilassi a differenza degli effetti broncodilatatori. Modeste riduzioni nella PO2 arteriosa insorgono dopo somministrazione di β2-agonisti sia a breve sia a lunga durata d’azione, ma il significato clinico di queste variazioni è dubbio. 108 b) Anticolinergici: agiscono principalmente bloccando l’azione dell’acetilcolina sui recettori muscarinici M3 responsabili della contrazione muscolare liscia delle vie aeree. A livello delle vie aeree sono presenti anche altri 2 recettori: M1, che potenziano gli effetti del riflesso colinergico e M2, che hanno invece un effetto di feed-back inibitorio. I farmaci anticolinergici attualmente disponibili non sono farmacologicamente selettivi per i recettori M1 e M3 ma bloccano anche i recettori M2. Come per i β2-agonisti si differenziano anticolinergici a breve durata d’azione (ipratropio e oxitropio) e a lunga durata d’azione (tiotropio). Ipratropio inizia la sua azione dopo 10-15 minuti, raggiunge il suo picco dopo 30 min. -1 ora con una durata d’azione variabile tra 3 e 6 ore. Tiotropio, unico anticolinergico a lunga durata d’azione, si dissocia molto lentamente dai recettori M3 (dopo circa 35 ore) e più rapidamente dai recettori M2 (36 ore) con il risultato che alla dose consigliata di 18 mcg/die la sua durata d’azione risulta superiore alle 24 ore. Lo steady-state farmacologico viene raggiunto entro 3 settimane. L’efficacia e la sicurezza di tiotropio è stata valutata con numerosi studi verso placebo, ipratropio e salmeterolo: questi hanno dimostrato un miglioramento significativo e persistente sull’ostruzione bronchiale in particolare sul VEMS, sul PEF e sulla Capacità Vitale Forzata (CVF) anche quando vengono misurati al mattino prima dell’inalazione della dose giornaliera, un miglioramento della dispnea e della tolleranza allo sforzo, una riduzione delle riacutizzazioni bronchiali ed un miglioramento della qualità di vita (21-27). È stato avviato inoltre nel 2004 uno studio (UPLIFT: Understanding the Potential Long-Term Impacts on Function with Tiotropium) della durata di 4 anni, per valutare l’efficacia a lungo termine del tiotropio sul declino del VEMS (28). L’utilizzo di questa classe di farmaci per via inalatoria ha dimostrato di essere notevolmente sicura. Il più importante effetto collaterale si è dimostrato essere la secchezza delle fauci. Nonostante siano stati riportati occasionalmente disturbi prostatici, non vi sono dati che provino una relazione causale tra tali sintomi e l’assunzione degli anticolinergici. È riportato in letteratura che la prescrizione di soluzioni erogate da nebulizzatori con maschera facciale ha indotto l’aggravamento acuto di un glaucoma, probabilmente per un effetto diretto sull’occhio (6,29). c) Xantinici (teofillina): la teofillina è l’unica metilxantina utilizzata per la terapia della BPCO. È un modesto broncodilatatore ma a causa della sua potenziale tossicità, viene considerata di seconda scelta rispetto ai broncodilatatori inalatori nonostante i suoi possibili effetti terapeutici addizionali di tipo antinfiammatorio, diuretico, inotropo positivo e di aumento della forza muscolare dimostrati in alcuni studi. La tossicità dei derivati delle xantine è dose-dipendente, e questo costituisce un problema poiché il suo effetto terapeutico è significativo a dosi prossime a quelle tossiche. Richiede pertanto uno stretto monitoraggio della concentrazione plasmatica che deve essere mantenuta tra 5 e 10 mcg/ml valutando anche attentamente le possibili interferenze farmacologiche. Le metilxantine sono inibitori non specifici di tutte le fosfodiesterasi e ciò spiega l’ampia varietà degli effetti tossici, i più importanti dei quali sono rappresentati dall’insorgenza di aritmie atriali e ventricolari, che possono risultare fatali. Possono anche favorire l’insorgenza di attacchi epilettici, tipo “grande male”, anche in pazienti che non hanno una storia di epilessia. Effetti collaterali meno drammatici sono comuni e comprendono cefalee, insonnia, nausea ed epigastralgie (1,6). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta 2. Glucocorticosteroidi a) Steroidi inalatori: il trattamento regolare con steroidi inalatori non è raccomandato routinariamente in tutti i pazienti con BPCO ma le Linee Guida più accreditate ne raccomandano l’uso nei pazienti sintomatici con BPCO grave e molto grave, che presentano quindi un VEMS <50% del teorico e con ripetute riacutizzazioni, ad es. 3 negli ultimi 3 anni per le Linee Guida GOLD (1) e 2 negli ultimi 12 mesi per le BTS (4) (Evidenza A). I 4 trials principali sul loro uso nella BPCO hanno infatti dimostrato che gli steroidi inalatori non rallentano il declino funzionale caratteristico della BPCO e non modificano la storia naturale della malattia ma determinano un miglioramento dell’ostruzione bronchiale e riducono del 25% le riacutizzazioni migliorando quindi la qualità di vita dei pazienti (30-34); la sospensione del trattamento con steroidi può inoltre portare alla comparsa di riacutizzazioni (35). Studi retrospettivi, criticati per la possibilità di artefatti, suggeriscono che la somministrazione di steroidi inalatori dopo un ricovero per riacutizzazione possa associarsi ad una riduzione della mortalità del 30% legata ad una riduzione delle riacutizzazioni (36,37). Sono pertanto in corso studi prospettici per valutare questo importante aspetto (38). Gli steroidi inalatori possono dare effetti collaterali locali come candidosi e manifestazioni cutanee. Uno studio a lungo termine ha dimostrato che il trattamento con triamcinolone acetomide per via inalatoria, peraltro non in commercio in Italia, si associava ad una rarefazione della densità ossea. Un altro studio a lungo termine ha dimostrato invece che la budesonide non riduce la densità della trama ossea e non aumenta la frequenza di fratture (31,33). b) Steroidi orali: non si consiglia di utilizzare cronicamente gli steroidi orali nella BPCO (Evidenza A). Non vi è infatti evidenza di un beneficio derivante dalla somministrazione continuativa di tali farmaci. Un importante effetto collaterale del trattamento a lungo termine con corticosteroidi per via sistemica è miopatia da steroidi, che contribuisce alla comparsa della debolezza muscolare, delle alterazioni funzionali e dell’insufficienza respiratoria nei pazienti con BPCO avanzata (1). Terapia di combinazione Nei pazienti con BPCO da moderata a molto grave la somministrazione di un singolo farmaco (di solito un broncodilatatore) spesso non è sufficiente a controllare i sintomi per cui è razionale utilizzare combinazioni di broncodilatatori con meccanismo d’azione e durata diversi per aumentare l’entità della broncodilatazione, riducendo al minimo l’insorgenza di effetti collaterali e l’associazione di questi con gli steroidi inalatori (1,3,4). Combinazione tra broncodilatatori: la combinazione di β2-agonisti a breve durata d’azione e di un anticolinergico determina un miglioramento maggiore e più prolungato del VEMS rispetto a ciascuno dei due farmaci considerati singolarmente e non determina tachifilassi nei successivi 90 giorni di trattamento (Evidenza A) (38). L’associazione di un β2-agonista e di un anticolinergico con teofillina può determinare un ulteriore miglioramento del quadro funzionale respiratorio e della qualità di vita (39-40). L’associazione di un anticolinergico a breve durata d’azione (ipratropio) e un β2-agonista a lunga durata d’azione (salmeterolo o formoterolo) ha dimostrato una broncodilatazione superiore rispetto al singolo farmaco (41,42). Sebbene sia razionale che anche l’associazione β2-agonisti a lunga durata d’azione e tiotropio determini effetti sinergici, i vantaggi clinici di tale associazione sono ancora oggetto di studio (6,43-45). Aumentare il numero dei farmaci infatti comporta un aumento dei costi per cui deve essere attentamente valutata la reale necessità e i benefici monitorando il paziente nelle successive 4 settimane dalla prescrizione (4). 109 Combinazioni steroidi/broncodilatatori: almeno 4 studi hanno dimostrato che l’associazione fra corticosteroidi e β2-agonisti a lunga durata d’azione (salmeterolo più fluticasone, formoterolo più budesonide), somministrati con un unico inalatore, è più efficace della somministrazione dei singoli componenti sulla funzione polmonare, sui sintomi, sulla qualità di vita e sulla comparsa di riacutizzazioni (Evidenza A) (46-48) e può migliorare l’aderenza al trattamento (Evidenza C). Altre terapie farmacologiche Terapia sostitutiva con α-1-antitripsina: giovani pazienti con deficit ereditario di α-1-antitripsina e con un enfisema consolidato possono essere candidati alla terapia sostitutiva. Tale terapia tuttavia è molto costosa e non è disponibile in molti Paesi; non è inoltre consigliata per le forme di BPCO che non sono determinate da un deficit di α-1-antitripsina (Evidenza C) (1). Antibiotici: la terapia antibiotica è consigliata soltanto nel trattamento delle riacutizzazioni infettive e di eventuali altre infezioni batteriche e non nel trattamento a lungo termine della BPCO (Evidenza A) (1). 110 Mucolitici (mucocinetici, mucoregolatori - ambroxol, erdosteina, carbocisteina, glicerolo iodinato): nonostante alcuni pazienti, che manifestano tosse produttiva possano trarre beneficio dai mucolitici, i risultati complessivi sembrano limitati. (Evidenza D) (1). In ogni caso la terapia mucolitica dovrebbe essere continuata solo se viene ottenuto un miglioramento dei sintomi (es. una riduzione della frequenza della tosse e della produzione di muco) (4). Antiossidanti: gli antiossidanti, in particolare l’N-acetilcisteina, hanno dimostrato di ridurre la frequenza delle riacutizzazioni e potrebbero pertanto avere un possibile ruolo nel trattamento di tali pazienti con frequenti riacutizzazioni (Evidenza B) (50). Trattamento palliativo della dispnea: la somministrazione per via orale o parenterale di oppioidi è indicata nel trattamento palliativo della dispnea nei pazienti con BPCO con malattia in fase terminale quando non c’è risposta al trattamento, al punto che tali pazienti dovrebbero avere accesso ai servizi multidisciplinari per le cure palliative, compreso il ricovero in “hospice” (4,51). Trattamento dell’ansia e della depressione: ansia e depressione sono spesso presenti nei pazienti con BPCO ipossici, con grave dispnea e con frequenti ricoveri ospedalieri. In tali pazienti, oltre al trattamento causale, dovrebbe essere preso in considerazione anche una valutazione approfondita ed un trattamento antidepressivo(4). Immunoregolatori (immunostimolanti, immunomodulatori): sebbene uno studio recente con un farmaco immunostimolante abbia mostrato una riduzione della gravità delle riacutizzazioni in corso di BPCO, ma non della loro frequenza, nessun altro autore ha ottenuto analoghi risultati. L’utilizzo regolare di questa classe di farmaci non può pertanto essere raccomandata sulla base delle attuali evidenze (Evidenza B) (1). Antitussivi: nonostante la tosse sia talvolta un sintomo fastidioso ha anche un significato protettivo, per tale ragione l’uso regolare di antitussivi è sconsigliato nella BPCO stabilizzata (Evidenza D) (1). Stimolanti respiratori: l’utilizzo prolungato di doxapram, uno stimolante respiratorio non speciRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta fico, disponibile soltanto nella formulazione per via endovenosa, non è raccomandato nei pazienti con BPCO stabilizzata (Evidenza D). Anche la somministrazione prolungata di almitrina bimesilato non è raccomandata nei soggetti con BPCO stabilizzata (Evidenza B) (1). Altri: nedocromile, leucotrieni o metodi di cura alternativi (per esempio medicine a base di erbe, agopuntura e omeopatia) non sono state adeguatamente sperimentate in soggetti con BPCO ed il loro utilizzo non può pertanto essere al momento raccomandato (1). Terapia non farmacologica La terapia non farmacologia viene trattata per esteso nei capitoli successivi. È molto importante nel trattamento di fondo della BPCO e riguarda principalmente la riabilitazione, l’ossigenoterapia, la ventilazione domiciliare e l’approccio chirurgico. I principali obiettivi della riabilitazione sono rappresentati dal miglioramento dei sintomi, della qualità di vita e dall’aumento della partecipazione fisica e psicologica alle attività quotidiane (Evidenza A). Rientra nella riabilitazione anche il supporto nutrizionale da considerare nei pazienti con Body Mass Index (BMI) <20 e deve utilizzare anche preparati per il supplemento nutrizionale (4,52). L’ossigenoterapia a lungo termine (>15 ore al giorno) a pazienti con insufficienza respiratoria cronica ha dimostrato di incrementarne la sopravvivenza (Evidenza A). Può anche essere importante per l’emodinamica, per il profilo ematologico, per la capacità di esercizio, per la meccanica polmonare e per lo stato mentale. I trattamenti chirurgici sono rappresentati da: 1. Bullectomia In pazienti adeguatamente selezionati, questa tecnica risulta efficace nel ridurre la dispnea e migliorare la funzionalità respiratoria (Evidenza C). 2. Chirurgia di riduzione del parenchima polmonare (LVRS) Nonostante siano già disponibili dati incoraggianti (Evidenza C), la LVRS è considerata ancora una procedura chirurgica palliativa sperimentale. Sono in corso diversi grandi studi per dimostrare l’efficacia ed i costi della LVRS a confronto con la terapia medica convenzionale. Si è osservato che i pazienti che presentano un VEMS <20% del predetto, a cui si associa alla TC ad alta risoluzione un quadro di enfisema omogeneamente distribuito, od una diffusione del CO <20% del predetto presentano un elevato rischio di morte dopo LVRS ed è inoltre improbabile che, in caso di sopravvivenza, tali pazienti possano trarre beneficio da questo tipo di intervento chirurgico. Fino a quando non saranno disponibili ulteriori risultati la LVRS non potrà essere utilizzata se non in casi selezionati e l’utilizzo della LVRS non potrà essere raccomandato su larga scala (1). 3. Trapianto polmonare In pazienti adeguatamente selezionati con BPCO molto avanzata, il trapianto polmonare ha dimostrato di essere in grado di migliorare la qualità di vita e la funzionalità respiratoria (Evidenza C). I criteri per il trapianto polmonare comprendono un VEMS <35% del predetto, una PaO2 <7,3-8.0 kPa (55-60 mmHg), una PaCO2 >6,7 kPa (50 mmHg) ed una ipertensione polmonare secondaria. Prevenzione delle infezioni I vaccini antinfluenzali possono ridurre l’incidenza di riacutizzazioni e la morte in circa il 50% dei pazienti con BPCO. Essi dovrebbero essere somministrati una volta (in autunno) o due volte (in autunno ed in inverno) ogni anno. Nella pratica clinica è stato impiegato il vaccino pneumococci- 111 co, che contiene 23 sierotipi; sulla base di studi in combinazione con il vaccino antinfluenzale le Linee Guida BTS ne raccomandano la somministrazione anche nella prevenzione delle riacutizzazioni della BPCO oltrechè di quella della polmonite pneumococcica (4,17,18). Trattamento delle riacutizzazioni La BPCO è spesso associata a riacutizzazione della sintomatologia. Una riacutizzazione di BPCO è un evento importante nella storia naturale della malattia ed è caratterizzata dalla modifica, rispetto alla variabilità giornaliera, della dispnea, della tosse e/o della produzione di escreato, tale da richiedere una variazione del trattamento. Il peso economico e sociale delle riacutizzazioni della BPCO è estremamente alto. Le cause più comuni di riacutizzazione sono rappresentate dalle infezioni dell’albero tracheo-bronchiale e dall’inquinamento ambientale, ma la causa di circa un terzo delle riacutizzazioni severe rimane ad eziologia sconosciuta. Figura 3 – Algoritmo per il trattamento della riacutizzazione della BPCO a domicilio Inizio o aumento dei broncodilatatori ed eventuale antibiotico-terapia Rivalutare entro poche ore Risoluzione o miglioramento dei segni e dei sintomi SE Nessun miglioramento Corticosteroidi per via orale Continua il trattamento riducendolo quando è possibile 112 Rivalutare il trattamento a lungo termine Rivalutare entro poche ore Peggioramento dei sintomi Ospedalizzazione Il trattamento farmacologico del paziente con riacutizzazione di BPCO si basa sull’incremento della terapia broncodilatatrice a breve durata d’azione in aggiunta a la terapia di fondo, sull’aggiunta di steroidi sistemici, preferibilmente per via orale e, in alcuni casi, degli antibiotici (fig. 3). Gli steroidi sistemici contribuiscono a ridurre i giorni di degenza ospedaliera ed accelerano la ripresa della funzionalità respiratoria (Evidenza A). Dovrebbero pertanto essere impiegati in associazione alla terapia broncodilatatrice se il valore del VEMS basale è inferiore al 50% del predetto. Si consiglia la somministrazione di 30-40 mg/die di prednisolone per 7-10 giorni a seconda della gravità (Evidenza D). Gli antibiotici sono efficaci solo quando il paziente con dispnea ingravescente e tosse presenta un espettorato aumentato di volume e purulento (Evidenza B) (1). La scelta degli antibiotici più appropriati è determinata dalle sensibilità locali a S. pneumoniae, H. influenzae e M. catarrhalis, sulla base dello schema riportato in tabella 4. La mortalità in corso di riacutizzazione di BPCO è strettamente correlata all’insorgenza di acidosi respiratoria che si manifesta con segni neurologici fino al coma, alla presenza di patologie concomitanti ed alla necessità di ventilazione. I pazienti che presentano una BPCO grave o molto grave necessitano spesso dell’ospedalizzazione. Nella tabella 5 sono elencati i criteri che suggeriscono di avviare il paziente ad una valutazione specialistica e/o al ricovero ospedaliero. È comunque opportuno che i pazienti a rischio siano informati su come riconoscere i sintomi di riacutizzazione e quando rivolgersi al medico e che tengano a domicilio i farmaci per il trattamento della riacutizzazione per un rapido intervento guidato dal proprio medico curante (4). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta Tabella 4 – Trattamento della BPCO riacutizzata per livello di gravità (ERS-ATS); Livello I: trattamento domiciliare 1. Educazione del paziente Controllare la tecnica di inalazione Considerare l’uso di spaziatori 2. Broncodilatatori β2-agonisti short acting# e/o ipatroprio MDI con spaziatore o nebulizzatori al bisogno Considerare l’aggiunta di broncodilatatori long-acting se il paziente non li sta usando 3. Corticosteroidi (la dose può variare) Prednisone 30-40 mg per os per 7-10 giorni considerare l’uso di un corticosteroide inalatorio 4. Antibiotici Può essere prescritto in presenza di alterazioni delle caratteristiche dell’espettorato† La scelta dovrebbe essere guidata dagli spettri di resistenza locali: - amoxicillina/ampicillina¶, cefalosporine - doxiciline - macrolidi∫ Se il paziente non ha risposto ad un precedente antibiotico-terapia, considerare: - amoxicillina/clavunato - fluorochinoloniƒ MDI: inalatori a dose fissa; #: salbutamolo, terbutalina; †: purulenza e/o volume; ¶: a seconda delle prevalenze locali delle beta-lattamasi batteriche; ∫: aziromicina, claritromicina, eritromicina, roxitromicina; ƒ: levofloxacina e moxifloxacina Tabella 5 – Indicazioni alla valutazione e/o ricovero ospedaliero in corso di riacutizzazione di BPCO • Sintomi severi, quali il significativo peggioramento della gravità dei sintomi, quale l’improvvisa insorgenza di dispnea a riposo • Storia di BPCO severa • Insorgenza di nuovi segni fisici, quali la cianosi, gli edemi periferici • Assenza di miglioramento con il trattamento medico iniziale • Importanti patologie associate • Aritmie cardiache di recente insorgenza • Incertezza diagnostica • Età avanzata • Insufficiente supporto familiare 113 BIBLIOGRAFIA 1. Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. GOLD Scientific Committee. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 2001 Apr;163(5):1256-76. 2. Fabbri LM, Hurd SS. Global strategy for the diagnosis, management and prevention of COPD: 2003 update for the GOLD Scientific Committee Eur Respir J 2003;22:1-2. 3. Celli BR, MacNee W. ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004 Jun;23(6):932-46. 4. National Collaborating Centre for Chronic Conditions. Chronic obstructive pulmonary disease: national clinical guideline for management of chronic obstructive pulmonary disease in adults in primary and secondary care. Thorax 2004;59 Suppl 1:1-232. 5. O'Donnell DE, Aaron S, Bourbeau J, Hernandez P, Marciniuk D, Balter M, Ford G, Gervais A, Goldstein R, Hodder R, Maltais F, Road J. Canadian Thoracic Society. Canadian Thoracic Society recommendations for management of chronic obstructive pulmonary disease 2003. Can Respir J 2003 May-Jun;10 Suppl A:11A-65A. 6. Rennard SI. Treatment of stable chronic obstructive pulmonary disease. Lancet 2004;364(9436):791-802. 7. Nardini S, Bertoletti R, Carrozzi L, Sabato E. Raccomandazioni per la attivazione e la gestione di un ambulatorio per il trattamento della dipendenza da fumo di tabacco in ambito pneumologico. Rassegna di Patologia dell'Apparato Respiratorio 2000;15:201-231. 8. Invernizzi G, Nardini S, Bettoncelli G, Codifava A, Corti F, Fossati R, Guerra C, Lavecchia C, Lazzaro C, Sabato E, Zuccaro P. L’intervento del medico di Medicina generale nel controllo del fumo: raccomandazioni per un approccio ottimale al paziente fumatore. Rassegna di patologia dell’apparato respiratorio 2002;17:55-70. 9. Latini R, Marino L, Cardini S. Trattamento individuale e di gruppo per la disassuefazione dal fumo. Rassegna di patologia dell’apparato respiratorio 2002;17:298-301. 10. A clinical practice guideline for treating tobacco use and dependence: A US Public Health Service report. The tobacco use and dependence clinical practice guideline panel, staff, and consortium representatives. JAMA 2000 Jun 28;283(24):3244-54. 11. Fiore MC. US public health service clinical practice guideline: treating tobacco use and dependence. Respir Care 2000 Oct; 45(10):1200-62. 12. Jorenby DE, et al. A controlled trial of sustained-release bupropion, a nicotine patch, or both for smoking cessation. NEJM 1999; 340 9:685-691. 13. Anthonisen NR, Connett JE, Kiley JP, Altose MD, Bailey WC, Buist AS, et al. Effects of smoking intervention and the use of an inhaled anticholinergic bronchodilator on the rate of decline of FEV1. The Lung Health Study. JAMA 1994;272:1497-505. 14. Scanlon PD, Connett JE, Waller LA, Altose MD, Bailey WC, Buist AS, et al. Smoking cessation and lung function in mild-to-moderate chro- 114 nic obstructive pulmonary disease - The Lung Health Study. American Journal of Respiratory and Critical Care Medicine 2000;161:381-90. 15. Transdermal Nicotine Study Group. Transdermal nicotine for smoking cessation: six-month results from two multicenter controlled clinical trials. JAMA 1991;266:3133–38. 16. Tonnesen P, Paoletti P, Gustavsson G, et al. Higher dosage nicotine patches increase one-year smoking cessation rates: results from the European CEASE trial—collaborative European anti-smoking evaluation. Eur Respir J 1999;13:238–46. 17. Nichol KL, Baken L, Wuorenma J, Nelson A. The health and economic benefits associated with pneumococcal vaccination of elderly persons with chronic lung disease. Archives of Internal Medicine 1999;159:2437-42. 18. Nichol KL. The additive benefits of influenza and pneumococcal vaccinations during influenza seasons among elderly persons with chronic lung disease. Vaccine 1999;17 Suppl 1:S91-S93. 19. Dahl R, Greefhorst LAPM, Nowak D, Nonikov V, Byrne AM, Thomson MH, Till D, Della Cioppa G. Inhaled formoterol dry powder versus ipratropium bromide in chronic obstructive pulmonary disease. American Journal of Respiratory and Critical Care Medicine 2001;164(5):778-784. 20. Rennard SI, Anderson W, ZuWallack R, Broughton J, Bailey W, Friedman M, Wisniewski M, Rickard K. Use of a long-acting inhaled beta2adrenergic agonist, salmeterol xinafoate, in patients with chronic obstructive pulmonary disease. American Journal of Respiratory and Critical Care Medicine 2001;163(5):1087-1092. 21. Casaburi R, Briggs DD, Donohue JF, Serby CW, Menjoge SS, Witek TJ. The spirometric efficacy of once-daily dosing with tiotropium in stable COPD. Chest 2000;118:1294-1302. 22. Casaburi R, Mahler DA, Jones PW, Wanner A, San Pedro G, ZuWallack RL, Menjoge SS, Serby CW, Witek T. A long-term evaluation of once-daily inhaled tiotropium in chronic obstructive pulmonary disease: European Respiratory Journal 2002;19(2):217-224. 23. Vincken W, van Noord JA, Greefhorst APM, Bantje ThA, Kesten S, Korducki L, Cornelissen PJC. Improved outcomes in patients with COPD during 1 yr’s treatment with tiotropium Eur Respir J 2002;19:209-216. 24. Brusasco V, Hodder R, Miravitlles M, et al. Health outcomes following six months’ treatment with once-daily tiotropium compared to twice daily salmeterol in patients with COPD. Thorax 2003;58:399-404. 25. Donohue JF, van Noord JA, Bateman ED, Langley SJ, Lee A, Witek TJ, Kesten S, Towse L. A 6-month, placebo-controlled study comparing lung function and health status changes in COPD patients treated with tiotropium or salmeterol. Chest 2002;122:47-55. 26. Donohue JF, van Noord JA, Langley SJ, Lee A, Kesten S, Towse LJ. Superior bronchodilation of once daily tiotropium compared to twice daily salmeterol in patients with COPD. Eur Respir J 2001;18(suppl 33):26s. Abstract P289. 27. O’Donnell DE, Fluge T, Gerken F, Hamilton A, Webb K, Aguilaniu B, Make B, Magnussen H. Effects of tiotropium on lung hyperinflation, dyspnoea and exercise tolerance in COPD. Eur Respir J 2004; 23:832-840. 28. Decramer MMD, Celli B, Tashkin DP, Pauwels RA, Burkhart D, Cassino C, Kesten S. Clinical trial design considerations in assessing longterm functional impacts of tiotropium in COPD: the Uplift Trial. COPD. Journal of Chronic obstructive pulmonary disease 2004;1:303-312. 29. Morganroth J, Golisch W, Kesten S. Eletrocardiographic monitoring in COPD patients receiving tiotropium COPD. Journal of chronic obstructive pulmonary disease 2004;1(2):181–190. 30. Vestbo J, Sorensen T, Lange P, Brix A, Torre P, Viskum K. Long-term effect of inhaled budesonide in mild and moderate chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 1999;353(9167):1819-1823. 31. Pauwels RA, Lofdahl CG, Laitinen LA, Schouten JP, Postma DS, Pride NB, Ohlsson SV. Long-term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. New England Journal of Medicine 1999;340(25):19481953. 32. Burge PS, Calverley PMA, Jones PW, Spencer S, Anderson JA, Maslen TK. Randomised, double blind, placebo controlled study of fluticasone propionate in patients with moderate to severe chronic obstructive pulmonary disease: the ISOLDE trial. British Medical Journal 2000;320(7245):1297-1303. 33. The Lung Health Study Research Group, Altose MD, Redline S, Deitz, et al. Effect of inhaled triamcinolone on the decline in pulmonary function in chronic obstructive pulmonary disease. New England Journal of Medicine 2000;343(26):1902-1909. 34. Jones PW, Willitis LR, Burge PS, Calverley PMA, on behalf of the inhaled steroids in obstructive lung disease in Europe Study Investigators. Disease severity and the effect of fluticasone propionate on chronic obstructive pulmonary disease exacerbations. Eur Respir J 2003;21:68-73. 35. Calverley PM, Spencer S, Willits L, Burge PS, Jones PW. IOSLDE Study Group. Withdrawal from treatment as an outcome in the ISOLDE study of COPD. Chest 2003 Oct;124(4):1350-6. 36. Sin DD, Man SFP. Inhaled corticosteroids and survival in chronic obstructive pulmonary disease: does the dose matter? European Respiratory Journal 2003;21:260-266. 37. Vestbo J, TORCH Study Group. The TORCH (towards a revolution in COPD health) survival study protocol. Eur Respir J 2004 Aug;24(2):206-10. 38. COMBIVENT Inhalation Aerosol Study Group. In chronic obstructive pulmonary disease, a combination of ipratropiumand albuterol is more effective than either agent alone. An 85- day multicenter trial. Chest 1994;105:1411-9. 39. Bellia V, Foresi A, Bianco S, Grassi V, Olivieri D, Bensi G, et al. Efficacy and safety of oxitropium bromide, theophylline and their combination in COPD patients: a double-blind, randomized, multicentre study (BREATH Trial). Respir Med 2002;96:881-9. 40. ZuWallack RL, Mahler DA, Reilly D, Church N, Emmett A, Rickard K, et al. Salmeterol plus theophylline combination therapy in the treatment of COPD. Chest 2001;119:1661-70. 41. van Noord JA, de Munck DR, Bantje TA, Hop WC, Akveld ML,Bommer AM. Long-term treatment of chronic obstructive pulmonary disease with salmeterol and the additive effect of ipratropium. Eur Respir J 2000;15:878-85. 42. D’Urzo AD, De Salvo MC, Ramirez-Rivera A, et al. In patients with COPD, treatment with a combination of formoterol and ipratropium is more effective than a combination of salbutamol and ipratropium: a 3-week, randomized, double-blind, within-patient, multicenter study. Chest 2001;119:1347-1356. 43. Tennant RC, Erin EM, Barnes PJ, Hansel T T. Long-acting β2-adrenoceptor agonists or tiotropium bromide for patients with COPD: is combination therapy justified? Current Opinion in Pharmacology 2003;3:270-276. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 10. Terapia e prevenzione - L. Corbetta 44. Cazzola M, Centanni S, Santus P, Verga M, Mondoni M, di Marco F, Matera MG. The functional impact of adding salmeterol and tiotropium in patients with stable COPD. Respir Med 2004 Dec;98(12):1214-21. 45. Aaron SD, Vandemheen K, Fergusson D, Fitzgerald M, Maltais F, Bourbeau J, Goldstein R, McIvor A, Balter M, O'donnell D. The Canadian Optimal Therapy of COPD Trial: design, organization and patient recruitment. Can Respir J 2004 Nov-Dec;11(8):581-5. 46. Calverley P, Pauwels R, Vestbo J, Jones P, Pride N, Gulsvik A, Anderson J, Maden C. Combined Salmeterol and fluticasone in the treatment of chronic obstructive pulmonary disease: A randomised controlled trial. Lancet 2003;361(9356):449-456. 47. Szafranski W, Cukier A, Ramirez A, Menga G, Sansores R, Nahabedian S, Peterson S, Olsson H. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. European Respiratory Journal 2003;21(1):74-81. 48. Mahler DA, Wire P, Horstman D, Chang CN, Yates J, Fischer T, Shah T. Effectiveness of fluticasone propionate and salmeterol combination delivered via the Diskus device in the treatment of chronic obstructive pulmonary disease. American Journal of Respiratory & Critical Care Medicine 2002;166(8):1084-1091. 49. Calverley PM, Boonsawat W, Cseke Z, Zhong N, Peterson S, Olsson H. Maintenance therapy with budesonide and formoterol in chronicobstructive pulmonary disease. Eur Respir J 2003;22:912-919. 50. Rasmussen JB, Glennow C. Reduction in days of illness after long-term treatment with N- acetylcysteine controlled-release tablets in patients with chronic bronchitis. Eur Respir 1988;1:351-5. 51. Jennings AL, Davies AN, Higgins JP, Gibbs JS, Broadley KE. A systematic review of the use of opioids in the management of dyspnoea. Thorax 2002;57:939-44. 52. Wouters EF. Management of severe COPD. Lancet 2004;364(9437):883-95. 115 11. Programma educazionale nella BPCO A cura di Margherita Neri (1) e Cristina Cinti (2) Con la collaborazione del Gruppo di Studio AIPO “Attività Educazionale” (1) (2) UO Pneumologia, Fondazione S. Maugeri IRCCS, Tradate UO Pneumotisiatria, AUSL di Bologna, Bologna 11. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione L’efficacia e l’efficienza dell’attività educazionale nelle malattie respiratorie croniche è sostenuta da molteplici evidenze scientifiche (EBM), tanto che viene raccomandata nelle Linee Guida recentissimamente approntate dalla comunità scientifica (1,2). Tuttavia ancora troppi Sanitari la ritengono “opzionale” e la omettono, con evidente discrepanza tra il comportamento ideale, secondo EBM, e quello reale di specialisti pneumologi e medici di Medicina generale (MMG) nella gestione del paziente portatore di BPCO. L’utilizzo appropriato degli interventi più efficaci non è una pratica attuata dall’intera classe medica, probabilmente per retaggi del passato, dubbi sull’effetto del trattamento per le scarse modificazioni dei parametri facilmente misurabili, dimenticanze, mancato rimborso della prestazione se non è ancora “ufficialmente” codificata; tutto ciò porta a non avvalersi interamente delle potenzialità diagnostiche e terapeutiche attualmente disponibili (3,4,5). I documenti con le maggiori evidenze dell’utilità dell’attività educativa ed informativa ai pazienti con malattie respiratorie croniche si riferiscono all’asma. Nelle recenti Linee Guida Internazionali per la gestione della BPCO è ribadita l’importanza dell’educazione ma sono ancora poche le evidenze documentate in letteratura (1,2,3). Gli obiettivi del trattamento nella BPCO sono noti: ridurre o rallentare la progressione del danno funzionale, prevenire, se possibile, e trattare le maggiori complicanze quali ipossiemia e infezioni, ridurre i sintomi (soprattutto la dispnea) e migliorare la qualità di vita utilizzando razionalmente le risorse disponibili. Una revisione critica delle indicazioni fornite al paziente BPCO durante la visita ambulatoriale ha evidenziato che l’abolizione del fumo è trattata sufficientemente solo in una piccola percentuale dei casi e la prescrizione farmacologica è spesso inadeguata (eccessiva o insufficiente), rispetto alle raccomandazioni EBM (4,5). In oltre nel 50% dei casi vi è una sottovalutazione dei sintomi da parte dei pazienti e dei Sanitari, con un conseguente fallimento diagnostico e terapeutico (4,5,6). Tosse, produzione di escreato e dispnea sono i sintomi prevalenti della BPCO ma, spesso, divengono manifesti quando il rimodellamento strutturale (inizialmente broncopolmonare e poi vascolare) è già presente, irreversibile e quantificabile con un esame funzionale. I segni clinici, poi, non sono sempre facilmente rilevabili nelle fasi precoci del deficit funzionale; devono, quindi, essere ricercati e correttamente interpretati in qualunque fase della malattia perché consentono di confermare la diagnosi di BPCO e iniziare prontamente gli interventi terapeutici e educazionali indispensabili (7). Nel Nord America è evidente una sottodiagnosi della BPCO in ambo i sessi, in particolare nelle donne, da parte dei MMG, correlabile ad una carente valutazione funzionale. L’indagine spirometrica, mezzo diagnostico semplice, economico, non invasivo e ripetibile, dovrebbe essere perciò implementata attraverso l’attività educativa ed informativa anche nella Popolazione Generale (8). Sono ipotizzabili alcune spiegazioni delle discrepanze tra le strategie raccomandate dalle Linee Guida e la corrente pratica clinica: scarsa praticità e ricaduta concreta. Il Sanitario può, talvolta, essere coscientemente in disaccordo con le raccomandazioni dello “stato dell’arte” e ritenere più affidabile la propria esperienza o il parere di Colleghi stimati. Non si deve, perciò, discutere solo della necessità di educare i pazienti per ottimizzarne l’aderenza al trattamento, ma anche come implementare l’adesione dei Sanitari alle Linee Guida. Il rapporto Sanitario/Paziente deve essere rivalutato per portare ad un’efficace comunicazione “empatica”. L’empatia rappresenta, infatti, il fondamento di una buona relazione medico-paziente e, quindi, una garanzia di maggior successo per ogni terapia. È interessante sottolineare, infine, che il rapporto medico-paziente può presentare delle peculiarità di genere: i medici donna pongono una maggiore accuratezza nella relazione e fanno attenzione non soltanto agli 117 aspetti verbali della comunicazione, ma anche a quelli non verbali, e dedicano una maggiore cura alle informazioni fornite e al modo di proporle. Prevenire i dubbi, le perplessità e i timori del proprio assistito, rendendolo partecipe delle decisioni, ascoltandolo empaticamente, senza stancarsi di dare spiegazioni, sono tutti elementi che contribuiscono ad attuare quella “alleanza terapeutica” che migliora l’adesione al trattamento e determina la soddisfazione dell’utente (9). Peculiarità di genere nella BPCO 118 La BPCO costituisce un modello delle complesse differenze di genere e sesso, fra uomini e donne, in tema di salute. La BPCO sembra avere una maggiore prevalenza negli uomini rispetto alle donne attribuibile alla maggiore abitudine tabagica ed al superiore rischio d’esposizione occupazionale (10). Un’indagine pubblicata su Epidemiology nel 2001 ha però confermato una scarsa rappresentatività femminile, già segnalata dai primi anni novanta, negli studi clinici ed epidemiologici attuati tra il 1966 ed il 1990 per la BPCO, l’AIDS e le malattie cardiache (11). D’altro canto, purtroppo, nelle donne la prevalenza dell’abitudine tabagica è in aumento e sembra documentata una maggiore suscettibilità del polmone femminile ai danni da fumo. Gli effetti del fumo sulla crescita della funzione polmonare sono maggiori in assoluto nelle ragazze. In due campioni indipendenti della popolazione danese risultava che il rischio di ospedalizzazione era più alto nelle donne che negli uomini per un dato numero di pacchetti/anno; la differenza fra i generi negli effetti del fumo sulla funzione polmonare risulta parallela al conseguente rischio di ricovero ospedaliero per BPCO (12,13). C’è, quindi, una crescente evidenza che le donne sono più suscettibili a diversi fattori di rischio ambientale, un aspetto finora mascherato dalla predominanza del fumo nell’uomo e l’aggiustamento per genere è il primo analitico passo da effettuare in molti studi. Le differenze fra i sessi nella percezione della dispnea è, poi, uno degli esempi più persuasivi della complessa interazione fra i fattori ambientali, socio-culturali e biologici. La sensazione d’alterata funzione respiratoria nelle donne può essere più sensibile, ma meno specifica che negli uomini, poiché le loro vie aeree sono soggette a variazioni cicliche ormonali, in particolare per azione del progesterone, con effetti stimolanti sulla ventilazione al minuto durante l’età riproduttiva (13,14). Ne consegue che la dispnea, un elemento chiave nella scala della qualità di vita, può essere percepita dalla donne, più che dagli uomini, come un indicatore globale della salute. Oltre alle differenze nella percezione dei sintomi, c’è evidenza della diversità di genere nel loro riconoscimento e descrizione; questo può ulteriormente influenzare l’interpretazione dei sintomi riportati dalle donne anche riluttanti nel descrivere il secreto bronchiale, mentre gli uomini più difficilmente ammettono la dispnea. La mortalità per BPCO negli Stati Uniti è in continua crescita nelle femmine mentre sembra stabilizzata nei maschi (8). In uno studio effettuato in Canada su 7210 soggetti d’età 35-64, dei quali 3654 uomini, la prevalenza femminile di BPCO era 2,1% nelle non fumatrici, 2,7% nelle ex fumatrici e 8,2% nelle fumatrici; negli uomini le prevalenze erano rispettivamente 0,8%, 2,9%, 3,5%. L’OR per un fumatore che aveva iniziato prima dei diciotto anni, era pari a 3 nei maschi e 5,9 nelle femmine comparato con i non fumatori. Il sovrappeso incrementava nelle donne la prevalenza di BPCO di 2,4 e la correlazione tra il precoce inizio del tabagismo ed il sovrappeso era molto forte. Un altro studio pubblicato su Chest nel 2001 evidenziava differenze di genere nella riabilitazione respiratoria che risultava meno efficace nelle donne (15). La terapia steroidea orale nei pazienti in OLT determina un incremento della sopravvivenza degli uomini ed un’aumentata mortalità nelle donne che associano una maggiore necessità di ricovero ospedaliero prolungato specie nelle fasi più avanzate della malattia (16). Deriva da tutto quanto esposto la necessità di ipotizzare un diverso approccio terapeutico e, di conseguenza, educazionale, prestando attenzione anche alle peculiarità legate alle differenze di genere. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 11. Programma educazionale nella BPCO - M. Neri, C. Cinti, Gruppo di Studio AIPO “Attività Educazionale” L’educazione dei pazienti Anticipare la diagnosi e, quindi, iniziare precocemente il trattamento della BPCO è assolutamente auspicabile, prima di tutto nell’ambito della Medicina generale, poi in ogni occasione di contatto fra il paziente ed i Servizi Sanitari. Tale sforzo non dovrebbe essere esercitato solo sui soggetti sintomatici, ma anche nei confronti di chi è considerato a maggiore rischio di ammalarsi di BPCO: i fumatori. Diversi studi hanno confermato per la BPCO ciò che già era evidente per l’asma bronchiale: l’aderenza al trattamento da parte dei pazienti è generalmente scarsa. Persino nel corso dei trial clinici più rigorosi, con stretto controllo e supervisione dei pazienti, il fenomeno ha spesso caratteristiche disarmanti. Nel corso del Lung Health Study (12), ad esempio, l’utilizzo del broncodilatatore dopo un anno dalla prescrizione era riferito solo nel 60% dei casi e nel 50% dopo cinque anni. I riscontri potrebbero essere peggiori se si utilizzasse una metodica obiettiva con conteggio delle dosi residue, sistemi di registrazione delle inalazioni e monitoraggio delle prescrizioni farmaceutiche per verificare realmente l’assunzione dei farmaci (17). Scarsa aderenza al trattamento significa anche uso eccessivo o improprio dei farmaci, perciò si ritorna all’importanza di aumentare nel portatore di BPCO, e nei Sanitari che lo seguono, il livello di conoscenza dei principi d’utilizzo degli aerosol predosati, inalatori di polvere secca, nebulizzatori ed erogatori di ossigeno. L’educazione del paziente portatore di BPCO è un intervento mirato ad ottimizzarne il programma terapeutico-riabilitativo anche attraverso importanti modificazioni dello stile di vita: sospensione del tabagismo, applicazione di regole igieniche e dietetiche, regolare attuazione di programmi riabilitativi ed anche convivenza con protesi respiratorie spesso non accettate dal paziente perché troppo visibili agli “estranei”. L’educazione non è, quindi, solo un apprendimento nozionistico da parte del paziente, ma anche attività di supporto e condivisione del carico terapeutico con i Sanitari che lo curano. Per raggiungere il primo obiettivo è indispensabile la comunicazione di messaggi basati su rigorose informazioni scientifiche, per il secondo bisogna personalizzare le informazioni strutturando un reale rapporto di alleanza terapeutica e co-gestione della malattia. La BPCO è curata in un’ottica multidisciplinare dove l’azione educazionale deve essere svolta da tutte le figure, sanitarie, e non, che entrano in contatto con il paziente: il MMG, lo specialista pneumologo, i terapisti della Riabilitazione, gli infermieri professionali, i familiari e le associazioni di volontariato e d’assistenza (3,17). Con l’intervento educazionale è possibile, quindi, promuovere l’applicazione d’abitudini comportamentali corrette ed incidere positivamente sul mantenimento delle condizioni di stabilità della malattia. Nelle fasi di riacutizzazione, anche in ambiente specialistico ospedaliero, è doveroso sensibilizzare il paziente a seguire scrupolosamente la terapia prescritta, insegnando, o correggendo, l’uso degli inalatori, consigliando di evitare ipnotici e sedativi, mantenere una sufficiente idratazione, praticare l’autodrenaggio delle secrezioni ed osservare un’alimentazione con pasti non abbondanti e frequenti (18). Al paziente ed i suoi familiari, sarebbe utile fornire delle istruzioni scritte che rammentassero i segni e i sintomi indicativi di una situazione di pericolo, con le relative azioni da intraprendere, così come viene suggerito per la gestione dell’asma bronchiale. 119 La terapia inalatoria 120 Nei pazienti BPCO è particolarmente importante attuare in modo corretto la terapia inalatoria perché, come principale via d’assunzione dei farmaci, influenza notevolmente il successo terapeutico. La somministrazione della dose terapeutica è possibile utilizzando appositi erogatori che consentono di inalare una quantità prefissata di farmaco disperso in un aerosol o preparati in polvere. Questi apparecchi richiedono la collaborazione del pazienti, per ottimizzarne la somministrazione, ed ognuno è dotato di caratteristiche diverse e di specifica manualità d’uso. Per valutare il grado d’adesione dei pazienti alle manovre previste da ciascuno dei più comuni inalatori ed erogatori il gruppo Attività Educazionale AIPO ha organizzato e svolto i Progetti di ricerca GEINA e GENEBU (19,20). Questi studi hanno indagato in Italia le modalità abituali di utilizzo della tecnica inalatoria evidenziando i numerosi errori frequentemente attuati dai pazienti che usano aerosolterapia e le scarsissime istruzioni ricevute sull’uso e sulla manutenzione degli aerosolizzatori. Questi studi hanno confermato una bassa aderenza, in Italia, anche dei pazienti BPCO alle terapie prescritte. Nonostante la estrema diffusione nel nostro Paese della aerosolterapia con nebulizzatori e le evidenze che le caratteristiche del nebulizzatore sono essenziali per assicurare i migliori risultati, è lo pneumologo stesso che non riceve in Italia informazioni sulle proprietà dei nebulizzatori disponibili per eseguire una aerosolterapia e di conseguenza l’utente è poco istruito ad utilizzare al meglio questo mezzo terapeutico (20). Numerosi studi hanno comunque confermato che la non aderenza del paziente, anche intenzionale, all’utilizzo corretto della terapia inalatoria è un problema estremamente importante (21-24). Il paziente con BPCO, quando assume la terapia inalatoria, ha bisogno dello stesso tipo d’informazioni pratiche che dovrebbero, ormai d’abitudine, essere fornite all’asmatico; l’età mediamente più avanzata può però spesso causare difficoltà all’utilizzo corretto della terapia inalatoria, ad esempio per patologia articolare delle mani, maggiori difficoltà nel leggere le prescrizioni e minor coordinamento erogazione-inalazione (25). Taluni autori non sembrano evidenziare un miglioramento dei risultati clinici in pazienti BPCO sottoposti ad attività educative-informative durante trattamento riabilitativo rispetto al gruppo controllo (26). Altri autori hanno dimostrato che un intervento educazionale rivolto a pazienti BPCO può rivelarsi efficace in termini di migliore conoscenza della malattia, dell’utilizzo corretto dei farmaci e del PEF, nonché sul ricorso ai servizi sanitari (27). Non sempre si è visto un favorevole rapporto costo/beneficio, in termini economici, per una maggior consapevolezza dei segni e sintomi d’aggravamento della malattia che può portare ad un’aumentata richiesta di visite mediche e, in taluni casi, un aumento del ricorso al ricovero ospedaliero. Una metanalisi dei risultati dell’educazione nella BPCO conclude che l’evidenza dell’efficacia dell’educazione esiste ma è piuttosto debole (28). Un corretto intervento d’educazione potrebbe ottenere la riduzione del rischio di ripetuti ricoveri ospedalieri che sono anche la conseguenza comportamenti modificabili (29). Un lavoro italiano ha evidenziato che i pazienti BPCO assegnati all’intervento d’educazione e rinforzo motivazionale hanno avuto miglioramenti statisticamente significativi della qualità di vita e della capacità di performance (30). Mancano studi di lunga durata per valutare l’efficacia di un intervento educazionale sulla qualità di vita e la sopravvivenza a lungo termine del malato con BPCO. L’ossigenoterapia a lungo termine (OLT) La storia naturale della BPCO è caratterizzata dall’inarrestabile progressione del danno funzionale polmonare fino all’alterazione degli scambi gassosi con insufficienza respiratoria. Uno stato ipossiemico può anche presentarsi transitoriamente nel corso degli episodi di riacutizzazione. La somministrazione d’ossigenoterapia a lungo termine (OLT) aumenta la sopravvivenza dei pa- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 11. Programma educazionale nella BPCO - M. Neri, C. Cinti, Gruppo di Studio AIPO “Attività Educazionale” zienti affetti da BPCO di grado severo con ipossiemia a riposo e tale effetto è più marcato quanto più la terapia viene condotta in modo regolare e continuativo (31). L’intervento educazionale nell’OLT dovrebbe essere soprattutto finalizzato a convincere il paziente a rispettare le ore di somministrazione quotidiana prescritte, curando quei momenti in cui è maggiore il rischio d’ipossiemia, come il sonno e soprattutto l’attività fisica. Tale presidio terapeutico non è utilizzato correttamente da molti medici ed è accettato con difficoltà da parte dei pazienti: questo si traduce spesso in una scarsa compliance. Molte inadempienze dei medici, e dei pazienti, sono state confermate da uno studio multicentrico italiano in corso di pubblicazione, dal quale deriveranno programmi educazionali ad hoc per le varie realtà documentate. Esistono, infatti, alcune evidenze che un intervento d’informazione e educazione, reiterato ed approfondito, potrebbe, ancora una volta, aumentare la compliance nell’OLT (32). Le esperienze Italiane della Scuola dell’ossigenoterapia domiciliare nella BPCO sono ancora sporadiche (33). Negli studi nazionali ed internazionali viene messa in luce, infatti, la frequente carenza di informazioni, addirittura, da parte dei medici prescrittori, sull’utilizzo corretto dell’ossigenoterapia; in più della metà di casi il paziente non è informato della necessità di utilizzare l’ossigeno durante l’attività fisica e comunque solo un terzo dei pazienti utilizza lo “stroller” portatile quando esce di casa. È fondamentale l’opera di educazione anche del MMG che segue a domicilio e conosce bene il paziente; convincere i pazienti a continuare l’OLT con il portatile, quando escono e vanno in comunità, spesso è particolarmente difficile per il disagio che manifestano nella vita di relazione e può essere necessario coinvolgere nell’intervento educazionale i familiari e conviventi del BPCO in OLT, fornendo le informazioni basilari sulla ossigenoterapia a tutti. La ventiloterapia domiciliare Negli ultimi anni il paziente affetto da BPCO con insufficienza respiratoria globale, in passato, purtroppo, considerato non suscettibile di intervento terapeutico di tipo ventilatorio, soprattutto per via non invasiva, viene sempre più frequentemente avviato a ventiloterapia domiciliare, sia pur in casi selezionati: pazienti con severa ipossiemia notturna o segni di fatica dei muscoli respiratori (34). Inoltre, spesso, esiste un doppio problema d’associazione della BPCO con la sindrome delle apnee ostruttive del sonno (OSAS) che comporta la necessità d’utilizzo di dispositivi come la ventilazione a pressione positiva continua (CPAP). La prescrizione di una protesi ventilatoria domiciliare comporta la necessità di affrontare, e risolvere, numerosi problemi pratici organizzativi, gestionali, relazionali e psicologici che coinvolgono il paziente e la sua famiglia, modificandone radicalmente l’impostazione della vita quotidiana. È evidente, pertanto, la grandissima attenzione che va posta nel fornire, sia al paziente sia al suo gruppo familiare, tutte le informazioni sulla necessità, e finalità, della ventiloterapia e della manutenzione quotidiana dell’apparecchiatura. Il paziente non potrà essere dimesso dall’ospedale se non dopo un adeguato “training” che deve coinvolgere anche i familiari-conviventi, verificando l’accettazione, e la comprensione, dei concetti fondamentali di questa particolare terapia. È anche molto importante fornire un supporto psicologico al paziente ed alla sua famiglia e prevedere la possibilità di prolungare quest’intervento, anche dopo le dimissioni, in occasione di controlli ambulatoriali o domiciliari. Esiste, però, il problema della compliance al suo utilizzo. Bisogna educare il paziente riguardo all’uso della protesi ventilatoria spiegandone i relativi benefici, il meccanismo d’azione della ventilazione meccanica e come risolvere gli effetti collaterali della maschera nasale o facciale che possono influenzare negativamente l’aderenza al trattamento. I dati obiettivi relativi all’uso dei ventilatori sono solo quelli provenienti dagli ultimi modelli dotati di conta-ore d’utilizzo legati all’attivazione diretta del paziente mediante l’inspirazione. La compliance può essere in ogni modo au- 121 mentata con semplici provvedimenti immediati sul singolo paziente o con la realizzazione di lezioni di gruppo; il programma gestionale può essere sviluppato nel centro pneumologico al momento della diagnosi e della prescrizione terapeutica, e completato da un intensivo supporto domiciliare nel medio termine con visite periodiche. Nel caso delle lezioni di gruppo (scuola della BPCO e dell’insufficienza respiratoria in ossigeno e ventiloterapia domiciliare sulla falsariga della già collaudate scuole dell’asma), impartite dai sanitari dei Centri specialistici pneumologici, il fine è sempre l’educazione, il supporto, il trattamento degli effetti collaterali ed il monitoraggio delle attrezzature in possesso del paziente con una metodologia che permette un’interazione tra i singoli partecipanti con confronto e condivisione delle esperienze personali di ciascuno (35). L’abolizione del fumo 122 Il fumo di sigaretta costituisce il maggiore fattore di rischio per BPCO e la sua sospensione è il solo intervento terapeutico, con l’OLT nelle fasi avanzate della malattia, che influenza la sopravvivenza. I Sanitari hanno il dovere di fare azione antitabagica in occasione d’ogni incontro con la Popolazione Generale ed, in particolare, con il portatore di BPCO (36). Il Lung Health Study ha evidenziato che negli Stati Uniti i pazienti sottoposti ad un intenso programma antifumo riducevano significativamente il declino annuale del FEV1, già dopo un anno (11). I pazienti erano sottoposti a colloqui individuali con il medico ed a successive frequenti sedute di gruppo (12 incontri in 10 settimane) guidate da figure sanitarie, con un eventuale supporto farmacologico (terapia nicotinica sostitutiva) e un tentativo precoce “di salvataggio” in caso di ricaduta. I messaggi che si possono trasmettere hanno il vantaggio della semplicità, dell’economicità e dell’ampio numero di soggetti raggiungibili con risultati simili a quelli d’interventi più strutturati su piccoli gruppi. I soggetti maggiormente motivati hanno superiori possibilità di smettere definitivamente di fumare, tuttavia anche in chi manifesta le più serie intenzioni sono possibili insuccessi e ricadute. È sempre opportuno sfruttare, senza ricorrere a politiche di “terrorismo psicologico”, qualsiasi ricorso al medico da parte del paziente che lamenta vaghi sintomi respiratori o cardiaci, a maggior ragione se non conducenti ad una diagnosi definitiva. Il supporto dei familiari è importante: se è stata concordata con il medico una data precisa di sospensione del fumo, c’è la possibilità di non lasciare il paziente a gestire la tentazione della ricaduta da solo. Nel paziente con BPCO i test di funzionalità respiratoria possono essere sfruttati come strumento di motivazione, all’inizio del trattamento, citando le “crude” percentuali del danno funzionale e, poi, l’effetto confortante che il miglioramento dei parametri spirometrici nel tempo può esercitare. Il National Cancer Institute consiglia al medico di svolgere quattro azioni: informarsi sull’abitudine tabagica del paziente, comunicare i rischi per la salute, considerare i possibili interventi per l’abolizione del fumo e pianificare un follow-up (ask, advise, assess, assist, arrange) (37). Nel sistema di classificazione americano dei disturbi mentali sono codificati i sintomi da astinenza da nicotina che raggiungono l’acme di norma entro la prima settimana dall’abolizione del fumo: irritabilità, ansia, difficoltà di concentrazione, riduzione della frequenza cardiaca, sudorazione, insonnia, incremento dell’appetito e perdita di peso. Le possibilità d’interventi di sostegno farmacologico sono ormai ampie. La terapia nicotinica sostitutiva (nicotine replacement therapy - NRT) è usualmente prescritta per attenuare le ripercussioni comportamentali, e psicologiche, che l’astensione dal fumo può determinare, soprattutto nei primi mesi, quando avvengono la maggior parte delle ricadute. I livelli plasmatici di nicotina che il fumo assicura non sono, però, raggiunti mediante NRT e ciò, in aggiunRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 11. Programma educazionale nella BPCO - M. Neri, C. Cinti, Gruppo di Studio AIPO “Attività Educazionale” ta alla perdita di quello che viene comunemente identificato come “il piacere di fumare”, giustifica i bassi tassi di successo, dell’ordine del 15-25% a 12 mesi. La terapia sostitutiva può essere attuata con: chewing gum, pasticche, cerotti transdermici, spray nasali e inalatori. Ogni sistema ha delle peculiarità. Uno dei vantaggi della somministrazione orale è la possibilità di modificare autonomamente le dosi di nicotina assunte rispetto, ad esempio, ai cerotti transdermici che rilasciano una dose fissa, ma può potenzialmente portare anche a fenomeni di sottodosaggio. I cerotti hanno dimostrato di essere efficaci soprattutto se utilizzati come supporto di minimi interventi educazionali e rappresentano probabilmente l’attuale prima scelta di trattamento nei casi più importanti. Nel soggetto che fuma meno di dieci sigarette al giorno le gomme da masticare e gli inalatori possono essere più adatti. Bupropione è un agente dopaminergico con meccanismo d’azione centrale, associato alla terapia nicotinica sostitutiva per via transdermica ha presentato tassi di successo più alti rispetto al solo cerotto; ha però anche mostrato di favorire la comparsa di uno stato convulsivo, soprattutto nei soggetti affetti da epilessia e bulimia, per cui deve essere usato con molta cautela. La terapia comportamentale di supporto varia da interventi strutturati in modo semplice a programmi complessi gestiti da veri e propri “smoking specialist”. I programmi più aggressivi raggiungono tassi di successo approssimativi del 20%, più elevati se uniti al trattamento farmacologico. Investire risorse nei programmi antitabagici si è dimostrato essere costo-efficace (raccomandazione A delle Linee Guida GOLD) se si prendono in considerazione il rallentamento del declino della funzionalità respiratoria e l’incremento della sopravvivenza (1,12). Aspetti nutrizionali Il paziente con BPCO presenta caratteristiche costituzionali riconducibili a due tipologie: l’eccedenza ponderale del bronchitico cronico e la magrezza dell’enfisematoso. Nel caso del sovrappeso, che determina ripercussioni più gravi nelle donne, sono comuni uno stato edematoso periferico con ritenzione idrica agli arti inferiori e ipotrofismo di cute e annessi, mentre nell’enfisematoso prevale l’inappetenza e la tendenza a perdere peso (8). Il mantenimento o la ripresa del peso corporeo ideale è un obiettivo importante nella terapia della BPCO. In condizioni d’incremento ponderale è aumentato il lavoro cardiorespiratorio per assicurare l’ossigenazione a tutti i distretti corporei e l’eccesso d’adipe in regione addominale, ostacola i movimenti del diaframma e non consente l’ottimale espansione dei polmoni. Nel paziente denutrito, all’opposto, c’è ipotonia e ipotrofia della muscolatura corporea, anche dei muscoli respiratori e conseguente circolo vizioso ove la deplezione muscolare incrementa ulteriormente il fabbisogno calorico. Lo stato nutrizionale si ripercuote anche sulle difese immunitarie: una dieta ipocalorica, con poche vitamine, minerali e, in particolare, proteine, riduce la produzione d’immunoglobuline. Nella BPCO è necessaria un’adeguata idratazione per ridurre la viscosità delle secrezioni e, se è in corso l’OLT, per contrastare la secchezza delle mucose secondaria all’ossigenoterapia. L’apporto proteico dovrebbe essere individualizzato per favorire i processi di difesa e di riparazione cellulare. Un supplemento di calcio è utile soprattutto nelle donne e nei pazienti in terapia steroidea, mentre quello di potassio serve per regolare il controllo della pressione arteriosa, della contrazione muscolare e trasmissione nelle fibre nervose. La correzione d’eventuali squilibri dei fosfati e del magnesio può favorire la funzionalità diaframmatica. Il ruolo del contenuto lipidico nella dieta è ancora da chiarire: da una parte la dieta iperlipidica contribuirebbe a ridurre la formazione d’anidride carbonica, dall’altra la minore assunzione di grassi favorirebbe lo svuotamento gastrico migliorando la meccanica respiratoria. 123 Contenuti di un programma di educazione rivolto al paziente BPCO Le nozioni d’anatomia e fisiologia cardio-respiratoria sono importanti informazioni da dare, così come la definizione di BPCO, sia pur in modo semplificato e comprensibile a tutti. Dovranno essere descritti i test di laboratorio e gli strumentali utili per la diagnosi di BPCO, spiegando per sommi capi le procedure e l’interpretazione dei risultati. Altro importante argomento è la terapia farmacologia della BPCO: meccanismo d’azione, benefici attesi, effetti collaterali, modalità di assunzione, metodi per ricordarsi di assumere il farmaco. Importantissima, oltre alla campagna contro il fumo di sigaretta, è quella contro le abitudini di vita scorrette (vita sedentaria, rinuncia all’attività fisica, ecc). L’esercizio fisico e gli interventi di riabilitazione devono essere dettagliati: quali, quando, quanto tempo e perché attuarli regolarmente. Sarà molto utile ribadire le tecniche di conservazione dell’energia nelle normali attività quotidiane, il rilassamento e la riduzione dello stress, la gestione degli aspetti emotivi relativi alla malattia, la nutrizione ideale e il trattamento dei sintomi principali. Il razionale e le modalità di utilizzo dei presidi non farmacologici (l’ossigenoterapia, il ventilatore) devono essere ampiamente descritti, così come le modalità per riconoscere le riacutizzazioni e le emergenze, cosa fare e chi contattare in caso di necessità. Un opuscolo educazionale o schede illustrative possono aiutare il discorso dell’educatore ed essere poi consegnati al paziente (vedi materiale disponibile sul sito: www.pneumologiospedalieri.it) (tab.1 e 2). Tabella 1 – Contenuti teorici di un programma educazionale per pazienti con BPCO 124 TEORICI Argomento Dettagli Mezzi Persone coinvolte Sede Nozioni sulla malattia Cause, evoluzione, sintomi, riacutizzazioni Illustrazioni e disegni semplici Medici, infermieri, terapisti della Riabilitazione Ambulatorio, degenza ordinaria, DH, incontri informali Nozioni sui farmaci Utilità, effetti, possibili effetti collaterali, modalità di assunzione Schemi scritti, foglietti illustrativi Medici, infermieri, terapisti della Riabilitazione Ambulatorio, degenza ordinaria, DH Informazioni sui danni da fumo A livello respiratorio e di tutto l’organismo Opuscoli, videoproiezioni Psicologi, medici, infermieri, terapisti della Riabilitazione Occasioni pubbliche: - conferenze - Giornata del respiro Ambulatorio, degenza ordinaria, DH Informazioni sulla fisio-kinesiterapia Finalità, durata, modalità, Opuscoli, video indicazioni, risultati previsti Terapisti della Riabilitazione, medici Ambulatorio, degenza ordinaria, DH Tabella 2 – Contenuti pratici di un programma educazionale per pazienti con BPCO PRATICI Argomento Dettagli Mezzi Persone coinvolte Sede Modalità di corretto utilizzo di farmaci Dimostrazioni pratiche sull’utilizzo della terapia inalatoria Dispositivi “placebo”, illustrazioni, foglietti illustrativi Medici, infermieri, terapisti della Riabilitazione Ambulatorio, degenza ordinaria, DH Modalità per “Economia” dei minimizzare la dispnea movimenti, ed eliminare le secrezioni utilizzo “Peep” e simili Dimostrazioni pratiche, Terapisti della illustrazioni ed Riabilitazione, informazioni scritte medici Degenza ordinaria, DH Strategie di disassuefazione dal fumo Sostegno medico e psicologico attraverso un programma basato sulle “5 A” Questionari (Fagerstrom, Ask, Advise, Assess, ecc) Psicologi, medici, infermieri, terapisti della Riabilitazione Ambulatorio, degenza ordinaria, DH Programmi di mantenimento dell’attività fisica Consigli preferibilmente scritti Opuscoli e programmi di FKT sintetici ma precisi Terapisti della Riabilitazione, medici Ambulatorio, degenza ordinaria, DH Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 11. Programma educazionale nella BPCO - M. Neri, C. Cinti, Gruppo di Studio AIPO “Attività Educazionale” BIBLIOGRAFIA 1. GOLD Global Initiative for Chronic Obstructive Lung Disease (GOLD) NIH/NHLBI/WHO Publication N 2701 A April 2001. 2. Celli BR, MacNee W. Standards for thr diagnosisi and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23: 932-946. 3. Neri M in Giuntini C, Grassi V. I quaderni della BPCO: il volto della BPCO che cambia. UTET, Torino 2002. 4. Ramsey SD. Suboptimal medical therapy in COPD: exploring the causes and consequences. Chest 2000; 117(2 Suppl):33S-37S. 5. Voelkel NF. Raising awareness of COPD in primary care. Chest 2000; 117 (5 Suppl 2):372S-375S. 6. Janson C, Anto J, Burney P, Chinn S et al. The European Community Respiratory Health Survey: what are the main results so far? European Community Respiratory Health Survey II. Eur Respir J 2001; 18(3):598-611. 7. Van de Boom G, Van Schayck CP, Rutten Van Molken, Tirimanna PRS, Den Otter JJ, Van Grunsven PM, Buitendijk, Herwaarden CLA, Van Weel C. Active detection of chronic obstructive pulmonary disease and asthma in the general population. Am J Crit Care Med 1998;158:1730-1738. 8. Chen Y, Breithaupt K, Muhajarine N. Occurrence of chronic obstructive pulmonary disease among Canadians and sex-related risk factors. J Clin Epidemiol 2000; 53: 755-761. 9. Gozzoli E, Cinti C, Neri M. Prevenzione Respiratoria 2004, in stampa. 10. Chapman KR, Tashkin DP, Pye DJ. Gender bias in the diagnosis of COPD. CHEST 2001; 119:1691-1695. 11. Bartlett EE. Did medical research routinely exclude women? An examination of the evidence. Epidemiology 2001; 12(5):584-586. 12. Anthonisen NR, Connett JE, Kiley JP et al. Effects of smoking intervention and the use of a inhaled anticholinergic bronchodilator on the rate of decline of FEV1. The Lung Health Study. JAMA 1994; 272: 1497-1585. 13. Kauffman F, Becklake MR. Sex and gender. 15, 288-304 in Eur Respir Monograph, respiratory Epidemiology in Europe, 2000 by AnnesiMaesano I, Guisvik A, Vieri G. 14. Cinti C, Mariano V, Coloretti I, Martucci P, Neri M. La pneumologia al femminile. Prevenzione Respiratoria 2002; 1:18-22. 15. Capri G, Rejeski J, Berry MJ, Zaccaro D, Woodart M. Gender moderates the effects of exercise therapy on health related quality of life among COPD patients. Chest 2001; 119:70-76. 16. Strom K. Oral corticosteroid treatment during long-term oxygen therapy in chronic obstructive pulmonary disease: a risk factor for hospitalization and mortality in women. Respiratory Medicine 1998; 92: 50-56. 17. Neri M, Cinti C. Educazione e compliance nell’asma. In Rapporto sull’asma 2001 a cura di Mario De Palma, Leonardo M Fabbri, Carlo Grassi. Centrostampa73, Castelseprio (VA) 2001: 379-400. 18. Numata Y, Bourbeau J, Ernst P, Duquette G, Schwartzman K. Teaching time for Metered-dose Inhalers in the Emergency setting Chest 2002 122, 2: 498-504. 19. Cinti C, Mariano V, Cappiello V, Cilenti V, Aiolfi S, Bancalari L, Canessa PA, Melani AS, Frigo A, Neri M. Modalità di uso di Aerolizer: risultati preliminari di una valutazione multicentrica in Italia. Progetto GEINA. Rassegna di Patologia dell’Apparato Respiratorio 2003; 18: 352-357. 20. Melani AS, Sestini P, Aiolfi S, Barbato N, Canessa PA, De Angelis G, Zanchetta D, DeTullio F, Cinti C, Neri M. GENebu Project: home nebulizer use and maintenance in Italy. Eur Respir J 2001; 18:1-6. 21. Simmons MS, Nides MA, Rand CS, Wise RA, Tashkin DP. Unpredictability of deception in compliance with physician-prescribed bronchodilator inhaler use in a clinical trial. Chest 2000; 118(2):290-25. 22. Viejo JL, Martin Escribano P, Romero S, Rodriguez Suarez JR. Compliance with inhalation treatment of patients with chronic obstructive pulmonary disease. Arch Bronchopneumol 2000; 36(6):319-325. 23. Melani AS, Neri M. Uso degli inalatori pressurizzati e di polveri: revisione critica della letteratura. Rassegna di Patologia dell’Apparato Respiratorio 2001; 16: 43-64. 24. Gruppo di lavoro educazionale AIPO per i nebulizzatori, - Progetto GENebu (Gruppo Educazionale per i Nebulizzatori: alcuni risultati preliminari. Rassegna di Patologia dell’Apparato Respiratorio 2001; 16: 251-260. 25. Carrion Valero F, Maya Martinez M, Fontana Sanchis I, Diaz Lopez J, Marin Pardo J. Inhalation Technique In Patients With Chronic Respiratory Diseases Arch Bronchopneumol 2000; 36(5):236-240. 26. Gallefoss F, Bakke PS. Cost-benefit and cost-effectiveness analysis of self-management in patients with COPD— a 1-year follow-up randomised, controlled trial. Respir Med 2002; 96(6):424-431. 27. Dehyn Y Muns-Lederer C, Worth H. Long term effects of a structured education programme for patients with COPD under out-patients condition. A pilot study Eur Respir J 1997; 10 (Suppl 25): 420-426. 28. Devine E C Pearcy J M. Meta-analysis of the effects of psychoeducational care in adults with COPD. Patients Educ Couns 1996; 29(2): 167-178. 29. Garcia-Aymerich J, Barreiro E, Farrero E, Marrades RM. Patients hospitalised for COPD have a high prevalence of modifiable risk factors for exacerbation (EFRAM study). Eur Respir J 2000; 16(6):1037-1042. 30. Carone M, Bertolotti G, Cerveri I, De Benedetto F, EDU-CARE, a randomised, multicentre, parallel group study on education and quality of life in COPD. Monaldi Arch Chest Dis 2002; 57(1):25-29. 31. Nocturnal Oxygen Therapy Trial. Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease. A clinical trial. Ann Intern Med 1980; 93 : 391-398. 32. Pépin J L, Barjhoux, Deschaux C, Brambilla C Long-term Oxigen Therapy at Home Compliance with medical prescription and effective use of therapy Chest 1996; 109(5): 1144-1150. 33. Fiorentini F, Cinti C, Giovannini M, Grandi P, Greco N, Neri M, Falcone F. Modello educativo AIPO Emilia-Romagna per l’ossigenoterapia domiciliare a lungo termine (OLT) Rassegna di Patologia dell’apparato Respiratorio 2001; 16S:90-91. 34. Plant PK, Owen JL, Elliot MW. Early use of non-invasive ventilation for acute exacerbations of chronic obstructive pulmonary disease on general respiratory wards: a multicentre randomised controlled trial. Lancet 2000; 355:1931-1935. 35. Aiolfi S, Aliani M, Cinti C, Canessa PA, Neri M, Insalco G. Sindrome dell’apnea ostruttiva nel sonno(OSAS). Aspetti diagnostici, terapeutici ed educazionali. Rassegna di Patologia dell’Apparato Respiratorio 2001; 16: 191-211. 36. Roussos C. Banning tobacco advertisements: is there a question ? Eur Respir J 1998; 11: 517-519. 37. A clinical practice guideline for treating tobacco use and dependence: A US Public Health Service report. The Tobacco Use and Dependence Clinical Practice Guideline Panel, Staff, and Consortium Representatives. JAMA 2000 28;283(24):3244-3254. 125 12. Insufficienza respiratoria cronica e sua terapia A cura di Antonio Corrado e Stefania Bertini UO Terapia Intensiva Pneumologica e Fisiopatologia Toracica, Azienda Ospedaliera Universitaria Careggi, Firenze 12. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Definizione e classificazione Con il termine di insufficienza respiratoria (IR) si intende la condizione caratterizzata da un’alterata pressione parziale dei gas (O2 e CO2) nel sangue arterioso. I criteri necessari per porre diagnosi di IR sono una pressione parziale arteriosa di ossigeno (PaO2) <55-60 mmHg durante respirazione in aria ambiente o un rapporto fra PaO2 e frazione inspiratoria di ossigeno (FIO2) (PaO2/FIO2) <300, accompagnata o meno da ipercapnia (pressione parziale arteriosa di anidride carbonica (PaCO2) >45 mmHg). La diagnosi di IR non è, quindi, una diagnosi clinica ma richiede sempre la misurazione della pressione parziale dei gas nel sangue arterioso (1). Il sistema respiratorio è costituito da due entità funzionali anatomicamente distinte ma integrate tra loro: il polmone, comprendente il parenchima, le vie aeree ed i vasi polmonari, che svolge la funzione di scambiatore di gas; la pompa ventilatoria, costituita dai centri respiratori, i muscoli respiratori, ed il torace (nei suoi comparti diaframmatico ed addominale), che ha invece la funzione di sostenere la ventilazione alveolare (V’A) (2). Dal punto di vista fisiopatologico, si possono considerare due principali quadri di insufficienza respiratoria: - insufficienza polmonare (insufficienza di scambio), caratterizzata prevalentemente da ipossiemia con un aumento della differenza alveolo-arteriosa di O2 [(A-a)DO2 >15-20 mmHg]. L’ipoventilazione alveolare, lo shunt intrapolmonare, le alterazione della diffusione, e l’ineguaglianza del rapporto ventilazione/perfusione (V’A/Q’) sono i possibili meccanismi che conducono all’ipossiemia e riconoscono cause intrapolmonari ed extrapolmonari; - insufficienza ventilatoria (insufficienza di pompa), rappresentata dall’ipercapnia con ipossiemia. L’ipercapnia dipende generalmente da una insufficiente ventilazione alveolare. Un aumento della PaCO2 segnala che l’eliminazione da parte del polmone della CO2 è inadeguata cioè che la quantità prodotta dal metabolismo cellulare è superiore a quella che l’apparato respiratorio può eliminare con la ventilazione. Il rapporto tra la quantità di CO2 prodotta e quella eliminata è definito dall’equazione 1: PaCO2 = K* V’CO2/V’E (1-VD/VT) dove PaCO2 è la pressione parziale di anidride carbonica nel sangue arterioso, V’CO2 è la produzione metabolica di anidride carbonica, V’E è la ventilazione minuto, VD è lo spazio morto anatomico, VT il volume corrente. L’incapacità di mantenere una adeguata ventilazione alveolare (V’A) dipende essenzialmente da tre fattori: - depressione dei centri respiratori (ad es. sedazione, uso di oppiacei); - eccessivo carico meccanico respiratorio (ad es broncospasmo, ipersecrezione); - ridotta capacità della pompa (ad es. riduzione della forza dei muscoli respiratori). Da un punto di vista clinico, l’IR è comunemente classificata in: 1. Acuta (IRA): insorge rapidamente in un apparato respiratorio sostanzialmente intatto fino al momento dell’episodio acuto; 2. Cronica (IRC): evento insidioso, progressivo e tardivo nella storia naturale della patologia cronica; 3. Cronica riacutizzata (IRCR) o insufficienza respiratoria acuta su cronica. La presenza di iperbicarbonatemia suggerisce che l’ipercapnia è di tipo cronica piuttosto che acuta mentre il valore del pH è indicativo del livello di compenso dell’insufficienza respiratoria; un valore di pH inferiore a 7,35 con valori di PaCO2 >45 mmHg indica una acidosi respiratoria scompensata. 127 Per l’insufficienza respiratoria cronica riacutizzata è l’entità delle oscillazioni dei valori dei gas ematici rispetto ai valori abituali rilevati in condizione di stabilità clinica a segnalare la presenza di IRA: si considerano indicative variazioni ≥5 mmHg in più o in meno rispettivamente per la PaCO2 e la PaO2. Trattamento della insufficienza respiratoria cronica Il trattamento della IRC prevede l’impiego di risorse terapeutiche quali l’ossigeno-terapia a lungo termine e la ventilazione meccanica domiciliare al fine di stabilizzare e rallentare la progressione della malattia cronica. 128 Ossigeno terapia a lungo termine (OTLT) L’ossigenoterapia consiste nella somministrazione di O2 in concentrazione maggiore di quella presente nell’aria ambiente, allo scopo di trattare o prevenire i sintomi e le manifestazioni dell’ipossiemia arteriosa. Il trattamento con O2 può essere applicato sia in situazioni di acuzie, per il periodo necessario a superare l’evento acuto, sia a lungo termine (OTLT), quando esiste una grave ipossiemia cronica stabilizzata. Tutti i pazienti con insufficienza respiratoria cronica e con grave ipossiemia arteriosa suscettibile di correzione possono essere trattati con OTLT, anche se la indicazione provata al momento è solo per i soggetti affetti da IRC secondaria a broncopneumopatia cronica ostruttiva (BPCO). Pertanto nelle patologie diverse dalla BPCO complicate da insufficienza respiratoria, pur in assenza di evidenza che dimostri l’efficacia della OTLT sulla sopravvivenza si consiglia la somministrazione di O2 laddove si dimostri la reale efficacia in termini di correzione della ipossiemia e di miglioramenti clinici o sintomatologici documentabili. Numerosi studi clinici hanno dimostrato che l’ossigeno terapia a lungo termine nei pazienti affetti da BPCO complicata da IRC è in grado di: - aumentare la sopravvivenza (3-6); - migliorare la qualità di vita (7-11); - ridurre i costi di gestione della malattia di base tramite riduzione del numero di ricoveri e di giorni di degenza annua (10-13). Tali risultati si ottengono solo se l’ossigeno-terapia viene: 1. Prescritta in modo mirato a pazienti che realmente necessitano del trattamento continuativo dopo opportuni controlli e verifiche presso strutture specialistiche; 2. Strettamente integrata al trattamento medico e riabilitativo; 3. Condotta in modo corretto e continuativo per un periodo di ore giornaliere di almeno 18 possibilmente 24, con un flusso di Ossigeno (l/min) il minimo sufficiente a mantenere valori di PaO2 compresi tra 60-70 mmHg senza pericolose variazioni della PaCO2; 4. Controllata con un corretto follow-up del paziente. Per chi? Tutti i pazienti con IRC e con grave ipossiemia arteriosa suscettibile di correzione possono essere trattati con OTLT, anche se l’indicazione provata al momento è solo per i soggetti affetti da BPCO (3,4). I pazienti candidati all’OTLT devono essere sottoposti ad una attenta osservazione clinica per un certo periodo di tempo (almeno tre mesi dopo un episodio di scompenso respiratorio) e ad un complesso iter diagnostico al fine di stabilire la reale necessità del trattamento con relative modalità di esecuzione dello stesso (14). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 12. Insufficienza respiratoria cronica e sua terapia - A. Corrado, S. Bertini Durante il periodo di osservazione si dovrà procedere alla monitorizzazione dei valori della PaO2 e PaCO2 a riposo da eseguirsi con cadenza bimensile per un periodo di 2-3 mesi. Si dovrà inoltre valutare il paziente nel tempo mediante controllo clinico, esami ematochimici quali l’ematocrito, prove di funzionalità respiratoria, radiografia del torace, elettrocardiogramma, ecocardiogramma (con eventuale determinazione delle pressioni del piccolo circolo). Per determinare con esattezza il flusso di ossigeno ottimale durante lo sforzo e durante il sonno sarà necessario eseguire un test da sforzo in aria ed in O2 e una monitorizzazione notturna dei gas ematici e della saturazione (per via indiretta) in aria e in O2. Criteri di ammissione all’OTLT I pazienti che presentano ipossiemia continua con valori diurni a riposo di PaO2 stabilmente inferiori a 55 mmHg, hanno una indicazione assoluta al trattamento. Tale limite può essere aumentato a 59 mmHg qualora siano associati policitemia e/o cuore polmonare cronico e/o cardiopatia ischemica. Nella tabella 1 vengono riportati le indicazioni assolute e relative per la prescrizione di OTLT. Per i pazienti che presentano valori di base di PaO2 uguali o lievemente superiore a 60 mmHg ma che presentano episodi di desaturazione sotto sforzo e/o durante il sonno, la somministrazione andrebbe limitata alla situazione che induce le pousses di desaturazione. Stabilita l’effettiva indicazione all’OTLT deve essere poi saggiata la tolleranza al trattamento e si deve ricercare la dose ottimale che eviti da un lato il pericolo di una iperossigenazione, che può causare acidosi ipercapnica o danni da tossicità (produzione di radicali liberi), dall’altro un’insufficiente ossigenazione con conseguente inutilità del trattamento. Tabella 1 – Ossigeno terapia a lungo termine (OTLT) INDICAZIONE ASSOLUTA INDICAZIONE RELATIVA PaO2 ≤55 mmHg PaO2 tra 55 e 60 mmHg in presenza di almeno uno dei seguenti criteri aggiuntivi: • Policitemia (Hct > 55%) • Segni di ipertensione polmonare • Segni di ipossia tissutale (edemi da scompenso cardiaco destro, deterioramento dello stato mentale) • Cardiopatia ischemia Costi e fattori correlati La OTLT ha un costo di gestione non indifferente per la collettività. Pellettier-Fleury et al. (15) hanno riportato che in Francia il costo annuale diretto (medico e non medico) per l’assistenza respiratoria fornita a un paziente con BPCO in OTLT è di 9.868±9.208 $; nell’ambito della ripartizione del costo le cure ambulatoriali e la ospedalizzazione rappresentano il 50,3% e 49,3% rispettivamente del costo totale. L’OTLT da sola rappresenta l’86,6% del costo delle cure ambulatoriali e il 36,9% dei costi totali. Dall’analisi dei costi ne consegue che l’indicazione alla OTLT va rigorosamente subordinata a un reale stato di necessità, a una razionale pianificazione assistenziale (medica, infermieristica, tecnica), a disponibilità di risorse economiche ed a periodiche verifiche di controllo della efficacia e qualità dei servizi prestati nonchè del grado di compliance alla terapia assegnata. Da quando i Trials MRC (3) e NOTT (4) (fig. 1) hanno dimostrato che la OTLT migliorava la sopravvivenza nei pazienti BPCO con valori di PaO2 stabilmente inferiori a 60 mmHg sembrò logico valutare se gli effetti benefici della somministrazione di ossigeno fossero rilevanti in termine di miglioramento della sopravvivenza anche in pazienti con moderata ipossiemia. 129 Figura 1 – Curve di sopravvivenza in pazienti BPCO in OTLT. Lo studio MRC compara 15 ore/die di trattamento con ossigeno con un gruppo di controllo che non assumeva ossigeno; lo studio NOT-COT compara 12 ore di trattamento contro 24 ore di trattamento. [da Rees PJ, Dudley. ABC of oxygen: oxygen therapy in chronic lung disease. BMJ 1998; 317:871 - 874.] 100 O2 24 h/die 90 O2 15 h/die Sopravvivenza (%) 80 O2 12 h/die 70 Controllo (No O2) 60 50 40 30 20 10 Mesi 0 0 130 10 20 30 40 50 60 Un dilemma di frequente riscontro nell’ambito della prescrizione dell’OTLT è stato sempre quello di cosa fare nei pazienti con valori di PaO2 compresi tra 56–65 mmHg. Prescrivere ossigeno in questi casi si traduce in un miglioramento della sopravvivenza? Nel 1997 Goreka et al. (16) hanno pubblicato uno studio longitudinale randomizzato e controllato con periodo osservazionale di 7 anni sugli effetti dell’OTLT in pazienti con BPCO e moderata ipossiemia. Dei 135 pazienti arruolati: 68 (gruppo di studio) con valori di PaO2 di 59,5±2,7 mmHg ricevevano OTLT (tramite concentratore per 17/24 ore/die) + terapia farmacologica, 67 (gruppo di controllo) con valori di PaO2 di 61,3±2,7 mmHg ricevevano solo la medesima terapia farmacologica del gruppo di studio. L’analisi delle curve di sopravvivenza non evidenziava alcuna differenza tra il gruppo di studio e quello di controllo e pertanto gli autori concludevano che la precrizione dell’OTLT in questo specifico gruppo di pazienti dovrebbe essere fatta con molta cautela riservando questo oneroso trattamento a pazienti con grave ipossiemia. Queste conclusioni condivisibili nella sostanza vanno tuttavia interpretate alla luce di due aspetti importanti per la valutazione dei risultati ottenuti. Il primo aspetto è legato al numero medio effettivo di ore giornaliere di trattamento eseguito dai pazienti in OTLT che risultava di 13,5 h/die contro le 17 ore prescritte all’inizio dello studio, il secondo aspetto riguarda la sorgente di ossigeno impiegata ovverosia il concentratore. L’impiego della sorgente fissa può aver influenzato la ridotta compliance al trattamento (numero di ore di terapia effettivamente eseguite inferiori a quelle prescritte) e questa ultima a sua volta può aver influenzato la sopravvivenza. Un recente studio (17) sui fattori prognostici in pazienti con BPCO ha dimostrato infatti che i pazienti in OTLT che necessitavano e assumevano in modo regolare l’ossigeno (in conformità alla prescrizione) erano sottoposti a un più basso rischio di morte rispetto ai pazienti che necessitavano di ossigeno ma lo assumevano in modo irregolare (non conforme all’atto prescrittivo). Il problema della compliance al trattamento rappresenta un altro elemento che può inficiare l’efficacia della terapia e quindi gravare sui costi di gestione senza un apprezzabile risultato clinico o un miglioramento della qualità di vita. La mancata aderenza al trattamento specifico è sempre ed esclusivamente colpa del paziente o anche di chi prescrive? Un recente lavoro di Pepin et al. (18) condotto su 930 pazienti con BPCO in OTLT ha evidenziato che l’ossigeno veniva utilizzato dai pazienti per un numero di ore /die: ≥15 solo nel 45% dei casi mentre veniva prescritto per 15 o Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 12. Insufficienza respiratoria cronica e sua terapia - A. Corrado, S. Bertini più ore al giorno dall’87% dei medici, la prescrizione della OTLT nel 20% dei casi avveniva senza il riscontro iniziale di una emogasanalisi. Le istruzioni impartite dal medico prescrittore sulle modalità di impiego del trattamento erano particolarmente carenti, infatti solo al 33% dei pazienti veniva raccomandato l’impiego dell’ossigeno durante l’igiene personale, solo al 24% veniva raccomandato l’uso dell’ossigeno durante i pasti e infine solo al 37% dei pazienti veniva spiegato e raccomandato l’uso dell’ossigeno durante attività ricreative. Questi dati dovrebbero farci riflettere sul significato del processo educativo che dovrebbe essere indirizzato non solo al paziente ma anche al medico prescrittore. L’ossigeno terapia rappresenta al momento l’unica terapia in grado di modificare il decorso della BPCO, tuttavia gli elevati costi che comporta dovrebbero spingerci sempre di più a essere più selettivi nella prescrizione e a dedicare più tempo ai nostri pazienti per fare in modo che la compliance al trattamento aumenti e l’efficacia della cura prescritta si traduca in un reale beneficio per il singolo e la collettività. Problemi aperti 1. L’associazione all’ossigenoterapia cronica di un potente e selettivo vasodilatatore sul circolo polmonare quale l’ossido nitrico (No) può migliorare ulteriormente la prognosi dei pazienti BPCO con grave ipossiemia cronica? Uno studio recente (19) condotto per tre mesi ha dimostrato che l’associazione della somministrazione di ossigeno con No rispetto alla somministrazione del solo ossigeno era in grado di ridurre in modo statisticamente significativo la pressione arteriosa polmonare media da 27,6 (4,4) mmHg a 20,6 (4,9) mmHg, p<0,001, e l’indice delle resistenze vascolari polmonari da 569,7 (208,1) a 351,3 (159,9) dynezs–1zcm–5zm–2, p<0,001 senza ridurre l’ossigenazione arteriosa. Inoltre la gittata cardiaca aumentava di 0,5 litri (da 5,6 (1,3) l/min a 6,1 (1,0) l/min, p=0,025) e tutto questo in assenza di incremento della produzione di sostanze tossiche derivanti dalla somministrazione di No. Il piccolo gruppo di pazienti studiati (40 pazienti) e il periodo limitato di somministrazione non ci permettono di trarre conclusioni definitive anche se i dati sono di estremo interesse e con implicazioni pratiche rilevanti qualora venissero confermati su una casistica maggiore e un più lungo periodo di osservazione. 2. Poichè l’iperossia aumenta lo stress ossidativo tramite la formazione di radicali liberi potrebbe indurre un processo infiammatorio nei polmoni? Un recente studio (20) condotto su 23 soggetti sani e 23 pazienti con BPCO ha dimostrato che la somministrazione di ossigeno per 1 ora ad una concentrazione del 28% aumentava le concentrazioni di 8-isoprostano e di interleukina 6 (IL-6) nell’aria espirata sia dei soggetti sani sia dei pazienti con BPCO e che questo non si verificava respirando aria. Le conclusioni di questo studio va sottolineato che si riferiscono ad un breve periodo di osservazione (1 ora) e pertanto al momento non possono essere estrapolate a pazienti in somministrazione cronica di ossigeno. 3. Durante l’iter prescrittivo dell’ossigeno, che avviene in strutture specialistiche pneumologiche, nello stabilire la dose ottimale di correzione della ipossiemia cronica ci avvaliamo di flussimetri di ossigeno collegati alle prese dell’ossigeno in rete o direttamente collegati a contenitori di ossigeno liquido o a riduttori di pressione delle fonti di ossigeno gassoso. In queste condizioni il flusso determinato per la correzione della ipossiemia non è automaticamente trasferibile ai concentrari di ossigeno soprattutto nei pazienti ipossiemici cronici con grave deficit ventilatorio ostruttivo (FEV1 % predetto <30%). Un recente lavoro (21) infatti evidenzia come la prescrizione di un flusso di ossigeno in questa categoria di pazienti sottostima significativamente il flusso ottimale da concentratore per ottenere una adeguata ossigenazione, e questo può avere delle importanti implicazioni per la ossigenoterapia domiciliare a lungo termine. 131 Ventilazione Meccanica Domiciliare (VMD) Gli scopi della ventilazione meccanica a domicilio sono: - continuare un trattamento ventilatorio iniziato in ospedale per patologia acuta che ha compromesso in modo irreversibile l’autonomia ventilatoria del soggetto (pazienti ventilatore-dipendenti); - controllare l’evolutività di alcune malattie respiratorie e/o neuromuscolari croniche (22); - correggere particolari alterazioni respiratorie che insorgono durante il sonno (23). 132 Pur non disponendo di studi randomizzati e controllati che dimostrino l’utilità della VMD nelle malattie toraciche o nelle malattie neuromuscolari, la vasta mole di dati pubblicati in letteratura inerente l’efficacia della NPPV in questa categoria di pazienti può essere considerata sufficientemente dimostrativa (24). Due studi retrospettivi (22,25) a lungo termine inerenti la NPPV domiciliare (prevalentemente notturna) su oltre 450 pazienti sono stati riportati negli ultimi anni. A seconda delle patologie di base la percentuale di sopravvivenza, che coincide in questo caso con la probabilità di continuare la NPPV, varia fra l’80 e il 100% a distanza di 5 anni. Questo outcome favorevole si aveva prevalentemente nei pazienti con cifoscoliosi, con sequele post polio, e sequele post-tubercolari. L’effetto fisiologico più importante pare rappresentato dal miglioramento degli scambi gassosi in stato di veglia per il migliore controllo ottenuto durante il sonno con la VM (26). Nei pazienti con malattie restrittive della parete toracica in assenza di condizioni reversibili che contribuiscano a peggiorare la ventilazione alveolare e che possano essere corrette, l’indicazione alla VMD viene posta in presenza delle seguenti condizioni (27): - sintomi (fatica, dispnea, cefalea mattutina, sonno disturbato, ipersonnia diurna) associati a uno dei seguenti criteri: - PaCO2 ≥45 mmHg; - episodi di desaturazione di HbO2 durante monitorizzazione notturna con SaO2 ≤88% per 5’ consecutivi; - pressione massima inspiratoria (MIP) <60% o FVC <50% del predetto nei pazienti con malattie neuromuscolari progressive. Quale modalità di ventilazione? La VMD può essere effettuata in modo: - non invasivo: tramite maschere facciali o nasali (ventilazione a pressione positiva) o tramite poncho, corazze o polmone d’acciaio (ventilazione a pressione negativa); - invasivo: tramite cannula tracheostomica. 1.Ventilazione non invasiva a pressione positiva (NPPV) Viene oggi considerata di prima scelta, qualora non vi siano controindicazioni alla ventilazione non invasiva (28). Prima di iniziare il trattamento ventilatorio va verificato che: - la deglutizione e la tosse siano efficienti; - il paziente abbia una autonomia ventilatoria >12 ore al giorno. I pazienti che sviluppano insufficienza ventilatoria possono cominciare con la NPPV e poi proseguire con la VM per via tracheostomica, man mano che peggiora l’autonomia ventilatoria oppure continuare con la NPV se si verificano complicazioni legati all’uso della maschera. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 12. Insufficienza respiratoria cronica e sua terapia - A. Corrado, S. Bertini Nella tabella 2 vengono riportati i vantaggi ed i limiti della ventilazione non invasiva a pressione positiva. Tabella 2 – Ventilazione non invasiva a pressione positiva (NPPV) VANTAGGI DELLA NPPV LIMITI DELLA NPPV Stabilizza la sindrome da insufficienza respiratoria cronica Richiede la collaborazione del paziente Preserva i meccanismi di difesa delle vie aeree Non consente facile accesso alle vie aeree e l’aspirazione delle secrezioni Permette di parlare e non influenza la deglutizione Possibili complicanze legate alla maschera (ulcere cutanee, rinite, secchezza nasale, congiuntivite, aerofagia, rischio di inalazione in caso di vomito) Consente un’applicazione intermittente Perdite d’aria con possibili limitazioni d’efficacia legate alla conformazione del volto 2.Ventilazione a pressione negativa (NPV) (29) È riservata attualmente a pazienti in cui la NPPV non ha avuto successo e rappresenta un’alternativa di seconda scelta per pazienti che usano altri metodi di ventilazione assistita. Nella tabella 3 sono riportate le indacazioni e gli svantaggi della ventilazione non invasiva a pressione negativa. Tabella 3 – Ventilazione non invasiva a pressione negativa INDICAZIONI DELLA NPV Non tolleranza delle maschere SVANTAGGI DELLA NPPV Può provocare o accentuare il collasso delle vie aeree superiori (nei pazienti con OSAS e nei pazienti con SLA con interessamento bulbare) Presenza di lesioni da decubito provocate dalle maschere È di difficile applicazione in caso di severa deformità della cassa toracica e grave obesità Presenza di una conformazione facciale che preclude l’utilizzazione delle maschere 133 Presenza di paresi del diaframma 3.Ventilazione per via tracheostomica La tracheotomia viene generalmente eseguita in seguito ad episodio di insufficienza respiratoria acuta o cronica riacutizzata, per via elettiva o dopo prolungata intubazione orotracheale. - Perchè il paziente non è svezzabile dalla ventilazione meccanica invasiva; - per assicurare una gestione migliore delle vie aeree (tosse inefficace, disturbi della deglutizione). La tracheotomia determina una riduzione dello spazio morto anatomico, un più facile approccio alle vie aeree sia per le necessità di aspirazione delle secrezioni sia per eventuali emergenze respiratorie. Nella tabella 4 vengono riportate le complicanze della tracheostomia. Tabella 4 – Complicanze della tracheostomia • Stenosi tracheale • Tracheomalacia • Ipersecrezione • Possibilità di frequenti reinfezioni • Impedimento alla fonazione • Alterazioni del meccanismo della deglutizione Indicazioni alla VM invasiva 1. Incontrollabili secrezioni delle vie aeree nonostante l’uso di strumenti espiratori non invasivi; 2. Compromissione della deglutizione conducente ad aspirazione cronica e polmoniti ripetute; 3. Il paziente ha insufficienza respiratoria sintomatica persistente e non tollera o non migliora con la VM non invasiva; 4. Il paziente ha bisogno di supporto ventilatorio prolungato (>12 ore/die) a causa di muscolatura respiratoria indebolita o paralizzata (es. tetraplegia o malattie neuromuscolari in fase terminale). Nella tabella 5 sono riportati i vantaggi ed i limiti della ventilazione meccanica domiciliare invasiva. Tabella 5 – Ventilazione meccanica domiciliare invasiva VANTAGGI LIMITI Stabilizza la sindrome da IRC Richiede maggiore coinvolgimento dei familiari Assicura un controllo delle vie aeree Necessita di accurata cura infermieristica del foro tracheostomico Fornisce un rapido accesso alle vie aeree Maggiore rischio di infezioni alle vie aeree (aspirazione ecc.) Perfetta interazione tra paziente e ventilatore senza perdite d’aria 134 VMD nella BPCO L’ossigeno-terapia a lungo termine (OTLT) rimane il trattamento di scelta nella IRC dovuta a BPCO. Però è stato suggerito che la NPPV offra vantaggi nel controllare l’insufficienza respiratoria ipercapnica e nel ridurre il lavoro respiratorio mettendo a riposo i muscoli respiratori i questi pazienti. Allo stato dei fatti il valore della NPPV nella insufficienza respiratoria ipercapnica del paziente BPCO è controverso. Nonostante infatti alcune esperienze dimostrino un peggioramento della qualità di vita (valutata attraverso apposito questionario) e della qualità del sonno (30-32), altri studi dimostrano un miglioramento di entrambe (33,34) anche attraverso il miglioramento di tutte le componenti attinenti con la sintomatologia, la sensazione di dispnea, e lo stato di umore (35). Tuttavia i risultati più incoraggianti e forse destinati a promuovere un’oculata prescrizione di NPPV anche per pazienti BPCO appaiono quelli che si riferiscono all’outcome clinico dei pazienti in termini di ospedalizzazioni. In ampie casistiche di individui ventilati a lungo termine in maniera non invasiva (28) e invasiva (36) anche la sottopopolazione dei pazienti BPCO dimostra una flessione dei ricoveri ospedalieri costante entro i primi 2 anni di follow-up. Tuttavia l’unico studio multicentrico, randomizzato e controllato (37) condotto su 122 pazienti BPCO stabili, ipercapnici ha evidenziato che l’aggiunta della NPPV alla OTLT induceva: - lieve riduzione della ipercapnia nei pazienti in OTLT; - miglioramento della dispnea e qualità di vita (HRQL). Per quanto concerne la ventilazione a pressione negativa esterna l’unico studio pubblicato in letteratura sugli effetti a lungo termine della NPV non ha evidenziato vantaggi dall’impiego di questa tecnica ventilatoria. Tuttavia va sottolineato che la metodologia di questo studio è criticabile in quanto includeva pazienti BPCO stabili ma normocapnici (38). Non esistono al momento attuale studi basati sull’evidenza scientifica che indichino la necessità di un uso generalizzato della VMD nel paziente BPCO con o senza ipercapnia, con autonomia ventilatoria e senza episodi di ipoventilazione. L’uso della VMD in pazienti BPCO selezionati con ipercapnia complicata da ipoventilazione notturna appare più giustificato (39). In pazienti con fibrosi cistica viene riportato che la NPPV è in grado di migliorare lo stato respiratorio e le condizioni generali in pazienti con malattia in fase terminale ed in attesa di trapianto (40,41). BIBLIOGRAFIA 1. Hall JB, Schmidt GA, Wood LDH. Acute Hypoxemic Respiratory Failure. In: Murray JF, Nadel JA (eds):Textbook of Respiratory Medicine, vol 2. Philadelphia, WB Saunders, 1994, 2589-2613. 2. Osmond DG. Functional anatomy of the chest wall. In Mcklem PT, Roussos C (eds). The Thorax, part A. Marcel Dekker, New York, 1985,199-234. 3. Nocturnal Oxygen Therapy Trial Group. Continuous or nocturnal oxygen therapy in chronic obstructive lung disease. Ann Intern Med 1980;93:391-8. 4. Medical Research Council-Working Group. Long-term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complicating chronic bronchitis and emphysema. Lancet 1981,1(8222):681-686. 5. Cooper CB, Waterhous JC, Howard P. A 12 year clinical study of patients with hypoxic cor pulmonale given long-term domiciliary oxygen therapy. Thorax 1987;42:105-110. 6. Corrado A, De Paola E, Messori A, Bruscoli G, Nutini S. The effect of intermittent negative pressure ventilation and long- term oxygen the- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 12. Insufficienza respiratoria cronica e sua terapia - A. Corrado, S. Bertini 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. rapy for patients with COPD. A four years study. Chest 1994;105:95-99. Heaton RK, Grant I, Petty TL. Psycological effects of continuous and nocturnal oxygen therapy in hypoxemic chronic obstructive pulmonary disease. Arch Intern Med 1983;143:1941. McSweeny AJ, Grant I, Heaton RK, Adams KM, Timms RM. Life quality of patients with chronic obstructive pulmonary disease. Arch Intern Med 1982;142:473-8. Guyatt GH, Berman LB, Townsend M, Pughsley SO, Chambers LW. A measure of quality of life for clinical trials in chronic lung disease. Thorax 1987;42:773-8. Brambilla I, Micaleff E, Chiusa I, Sacerdoti C, Arlati S, Rolo J. Influenza dell'ossigenoterapia a lungo termine sulla qualità di vita e sulla durata della degenza ospedaliera. Risultati di una indagine su 104 pazienti ipossiemici. Medicina Toracica 1989;11:279-85. De Paola E, Corrado A, Bruscoli G, Ciardi-Duprè GF. Esperienza di O2TLT nell'area fiorentina. In L'ossigenoterapia a lungo termine nella riabilitazione delle malattie respiratorie. Rocco Curti editore 1989;pag.125-131. Petty TL. Prescribing home oxygen for chronic obstructive pulmonary disease. Thieme Stratton Inc. N.Y. 1982. Ringbaek TJ, Viskum K, Lange P. Does long-term oxygen therapy reduce hospitalisation in hypoxaemic chronic obstructive pulmonary disease? Eur Respir J 2002; 20: 38–42. Levi-Valensi P, Aubry P, Rida Z, Rose D, Ndarurinze S, Jounieaux V. Selection of patients for long-term oxygen therapy (LTO). Eur Respir J 1989;2:624s-629s. Pelletier-Fleury N. et al. The cost of treating COPD patients with Long-Term Oxygen Therapy in a French population. Chest 1996; 110: 411. Goreka D, Gorzelak K, Sliwinski P, Tobiasz M, Zielinski J. Effect of long term oxygen therapy on survival in patients with chronic obstructive pulmonary disease with moderate hypoxemia. Thorax 1997; 52: 674. Piccioni P, Caria E, Bignamini E, Forconi G, Nebiolo F, Arossa W, and Buggiani M. Predictors of survival in a group of patients with chronic airflow obstruction. J Clin Epidemiol 1998;51 (7): 547-55. Pepin JL et al. Long-Term Oxygen therapy at home Compliance with medical prescription and effective use of therapy. Chest 1996;109:1144-50. Vonbank K, Ziesche R, Higenbottam TW, Stiebellehner L, Petkov V, Schenk P, Germann P, Block LH. Controlled prospective randomised trial on the effects on pulmonary haemodynamics of the ambulatory long term use of nitric oxide and oxygen in patients with severe COPD. Thorax 2003;58:289–293. Carpagnano GE, Kharitonov SA, Foschino-Barbaro MP, Resta O, Gramiccioni E, Barnes PJ. Supplementary oxygen in healthy subjects and those with COPD increases oxidative stress and airway inflammation. Thorax 2004;59:1016–1019. Dheda K, Lim K, Ollivere B, Leftley J, Lampe FC, Salisbury A, Dilworth JP, Rajakulasingum RK. Assessments for oxygen therapy in COPD: are we under correcting arterial oxygen tensions? Eur Respir J 2004; 24: 954–957. Simonds AK, Elliott MW. Outcome of domiciliary nasal intermittent positive pressure ventilation in restrictive and obstructive disorders. Thorax 1995; 50: 604-609. Indications for positive airway pressure treatment of adult obstructive sleep apnea patients. A consensus statement. Chest 1999;115:863-866. Hill NS. Noninvasive positive pressure ventilation in neuromuscular disease. Enough is enough. Chest 1994;105:337– 8. Leger P, Bedicam JM, Cornette A et al. Nasal intermittent positive pressure ventilation. Long term follow-up in patients with severe chronic respiratory insufficiency. Chest 1994; 105: 100-105. Piper AJ, Sullivan CE. Effects of long term nocturnal nasal ventilation on spontaneous breathing during sleep in neuromuscular and chest wall disorders. Thorax 1996; 9: 1515-1522. Clinical indications for non invasive positive pressure ventilation in chronic respiratory failure due to restrictive lung disease, COPD, and nocturnal hypoventilation-a consensus conference Report. Chest 1999;116:521-534. Make BJ, Hill NS, Goldberg AI et al. Mechanical ventilation beyond the intensive care unit. Report of a consensus conference of the American College of Chest Physicians. Chest 1998; 113: 289S-344S. Corrado A, Gorini M. Negative pressure ventilation: is there still a role? Eur Respir J 2002;20:1-11. Strumpf DA, Millman RP, Carlisle CC, et al. Nocturnal positive-pressure ventilation via nasal mask in patients with severe chronic obstructive pulmonary disease. Am Rev Respir Dis 1991; 144:1234-1239. Gay PC, Hubmayr RD, Stroetz RW. Efficacy of nocturnal nasal ventilation in stable severe chronic obstructive pulmonary disease during a 3 month controlled trial. Mayo Clin Proc 1996; 71: 533-542. Lin CC. Comparison between nocturnal nasal positive pressure ventilation combined with oxygen therapy and oxygen monotherapy in patients with severe COPD. Am J Respir Crit Care Med 1996; 54: 353-358. Simonds AK, Muntoni F, Heather S, Fielding S. Impact of nasal ventilation on survival in hypercapnic Duchenne muscular dystrophy. Thorax 1998; 53: 949-952. Meecham-Jones DJ, Paul EA, Jones PW, Wedzicha JA. Nasal pressure support ventilation plus oxygen compared with oxygen therapy alone in hypercapnic COPD. Am J Respir Crit Care Med 1995; 152: 538-544. Krachman SL, Quaranta AJ, Berger TJ, Criner GJ. Effects of noninvasive positive pressure ventilation on gas exchange and sleep in COPD patients. Chest 1997; 112: 623-628. Elliott MW, Simonds AK, Carroll MP, Wedzicha JA, Branthwaite MA. Domiciliary nocturnal nasal intermittent positive pressure ventilation in hypercapnic respiratory failure due to chronic obstructive lung disease: effects on sleep and quality of life. Thorax 1992; 47: 342-348. Muir JF, Girault C, Cardinaud JP, Polu JM and the French Cooperative Study Group. Survival and long-term follow-up of tracheostomized patients with COPD treated by home mechanical ventilation. Chest 1994; 106: 201-209. The Italian multicentric study of non invasive positive pressure ventilation in COPD patients. ERJ, in press. Shapiro SH, Ernst P, Gray-Donald K et al. Effect of negative pressure ventilation in severe chronic obstructive pulmonary disease. Lancet 1992; 340: 1425-1429.Donner CF, Howard P, Robert D. Patient selection and techniques for home mechanical ventilation. Monaldi Arch Chest Dis 1993; 1: 40-47. Shneerson JM. The changing role of mechanical ventilation in COPD. Eur Respir J 1996; 9: 393-398. Piper AJ, Parker S, Torzillo PJ et al. Nocturnal nasal IPPV stabilizes patients with cystic fibrosis and hypercapnic respiratory failure. Chest 1992; 102: 846-850. Hodson ME, Madden BP, Steven MH et al. Non-invasive mechanical ventilation for cystic fibrosis patients-a potential bridge to transplantation. Eur Respir J 1991; 4: 524-527. 135 13. La riabilitazione respiratoria nel trattamento della BPCO A cura di Nicolino Ambrosino e Massimiliano Serradori U.O. Pneumologia Dipartimento Cardio-Toracico, Azienda Ospedaliera-Universitaria Pisana, Pisa 13. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione Nella broncopneumopatia cronica ostruttiva (BPCO) solo la sospensione del fumo può ridurre il progressivo peggioramento del flusso delle vie aeree (1) e solo l’ossigeno terapia a lungo termine (OTLT) è in grado di migliorare la sopravvivenza dei pazienti ipossiemici (2). In uno studio di pazienti con severa BPCO in OTLT, il 50% (con dispnea del grado 5 della scala del Medical Research Council: MRC) non lasciava la casa e il 78% era dispnoico nel camminare per casa e nell’eseguire le attività della vita quotidiana (ADL: activities of daily living) (3). L’utilizzazione di risorse sanitarie da parte dei pazienti BPCO è correlato più alla forza dei muscoli respiratori e periferici che all’ostruzione delle vie aeree (4). In aggiunta, pazienti ospedalizzati per una riacutizzazione di BPCO severa hanno una sopravvivenza ad un anno che è correlata in modo indipendente all’indice di massa corporea (BMI) e alla capacità di far fronte alle ADL in fase stabile (5). I programmi di riabilitazione respiratoria (PRR) possono essere utili sotto questo aspetto: essi infatti possono influenzare positivamente la funzione dei muscoli periferici e respiratori, lo stato nutrizionale e le ADL. Una volta considerata più arte che scienza, la riabilitazione respiratoria è stata definita come “un insieme multidimensionale di servizi diretti a persone con malattie polmonari e alle loro famiglie, di solito sotto la guida di un team interdisciplinare di specialisti con lo scopo di raggiungere e mantenere il massimo livello di indipendenza e di attività nella comunità” (6-10). Vi è evidenza scientifica che i PRR migliorano la dispnea e il controllo della BPCO (10). Tale evidenza deriva da studi prospettici, randomizzati e controllati (11-15) e da meta-analisi (16). Nelle recenti Linee Guida “GOLD” (17) l’evidenza scientifica di efficacia della riabilitazione nella BPCO è stata definita come “A”, cioè massima, superiore per esempio a quella di farmaci comunemente usati nel trattamento farmacologico a lungo termine. La riabilitazione è dunque parte integrante del trattamento globale della BPCO (18,19). Una attenta selezione del paziente può servire per l’individualizzazione del PRR ed è fondamentale per il suo successo (20,21). L’unica controindicazione assoluta ai PRR è la mancata volontà di parteciparvi e/o una cattiva compliance ad essi. L’età non è considerata un fattore limitante dei PRR (21). Il miglioramento della tolleranza all’esercizio dopo PRR non si correla con la severità della emogasanalisi o della ostruzione delle vie aeree (22,23). In particolare, i PRR sono parte integrante di nuove modalità terapeutiche come la resezione di volume ed il trapianto polmonare (24-26). Misure di Outcome Il Test da sforzo incrementale è generalmente usato per valutare l’outcome dei PRR e allo stesso tempo per definire l’intensità dell’allenamento. La valutazione dell’esercizio dovrebbe essere fatta usando il tipo di esercizio, cicloergometro, pedana mobile o ergometro a braccia, che sarà impiegato nell’allenamento, però i risultati di un tipo di test da sforzo possono essere applicati a differenti forme di esercizio (28). La misura della distanza coperta durante il cammino (6 o 12 minuti) e lo “Shuttle Test” sono considerati metodi semplici e riproducibili per valutare la tolleranza all’esercizio (29). Dispnea: la severità della dispnea si correla solo debolmente con i dati funzionali (30). Esistono metodi di misura nella pratica clinica per quantificare la dispnea (31,32). Qualità di vita correlata alla salute (Health Related Qualità of Life, HRQL): in generale i questionari della HRQL misurano l’impatto della salute di un paziente sulla sua capacità di eseguire le ADL. 137 Gli strumenti per la determinazione della HRQL variano da misure malattia-specifiche per un singolo sintomo (per es dispnea) a valutazione globale generica di molti aspetti che includono quelli emozionali, il ruolo sociale, le ADL. Questi questionari hanno buona riproducibilità anche se la funzione polmonare e la tolleranza allo sforzo non vi si correlano fortemente (33). Risultati I risultati pubblicati forniscono una solida base scientifica a sostegno dell’utilizzo di PRR. Dopo PRR i pazienti riferiscono miglioramento della loro HRQL con una riduzione dei sintomi respiratori, aumento della tolleranza all’esercizio e della capacità di affrontare le ADL ed una maggiore indipendenza (11-16) (tab. 1). Tabella 1 – Ragionevoli obiettivi della riabilitazione respiratoria OUTCOME 138 EVIDENZA SCIENTIFICA DI BENEFICIO Dispnea A Tolleranza all’esercizio fisico A Qualità divita B Consumo di risorse sanitarie C Forza dei muscoli respiratori B Sopravvivenza ? Funzione respiratoria - Dispnea: studi controllati e una meta-analisi hanno confermato che i PRR migliorano la dispnea e il controllo sulla BPCO (10,16). Questi effetti persistono per almeno 12 mesi (13-15,34-37). Capacità di esercizio: i PRR nella BPCO hanno chiaramente dimostrato effetti positivi sulla tolleranza all’esercizio e la performance funzionale (10,16). I benefici si possono ottenere con PRR in regime di degenza ordinaria, in regime di Day-Hospital e domiciliare (38,39). Stato di salute: studi ben disegnati hanno dimostrato miglioramenti dello stato di salute dopo PRR. Questi miglioramenti sono di lunga durata e comprendono differenti aspetti dello stato di salute come dispnea, fatica, funzione emozionale e controllo di malattia (12-16,34-36,40). Riacutizzazioni, ospedalizzazioni e uso di risorse sanitarie: alcuni studi hanno mostrato che I PRR sono associati a riduzioni del numero delle riacutizzazioni e delle ospedalizzazioni nell’anno successivo alla loro esecuzione (15,35,36). Uno studio randomizzato di Griffiths et al. (13) ha osservato una minore richiesta di visite domiciliari da parte del medico di Medicina generale nei pazienti sottoposti anche a PRR, tale da rendere i programmi di trattamento della BPCO includenti anche PRR, più convenienti dal punto di vista economico (41,42). Sopravvivenza: per quanto ci siano delle evidenze indirette di migliore sopravvivenza nei pazienti capaci di maggiori prestazioni fisiche (5,43,44) al momento non si può definire che i PRR siano in grado di migliorare la sopravvivenza. I PRR sono efficaci quando eseguiti in regime di degenza ordinaria (11), in regime di Day-Hospital (35,36) ed in regime domiciliare (38) (tab. 2). Probabilmente sono la strutturazione e le componenti del programma, piuttosto che la sede in se a determinarne l’efficacia. Il successo dei PRR sono attribuiti all’equipe multidisciplinare, mentre i miglioramenti attribuibili alle singole componenti sono difficili da valutare (45) a causa dell’approccio multidisciplinare (tab. 3). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 13. La riabilitazione respiratoria nel trattamento della BPCO - N. Ambrosino, M. Serradori Tabella 2 – Componenti dei programmi di riabilitazione polmonare e loro relativa evidenza scientifica attuale di efficacia COMPONENTE EVIDENZA Ottimizzazione della terapia medica A Cessazione dal fumo A Educazione C Fisioterapia toracica B Allenamento all’esercizio fisico generale A Allenamento dei muscoli respiratori B Allenamento di gruppi muscolari degli arti superiori B Coordinazione respiratoria C Terapia occupazionale C Ossigeno terapia a lungo termine A Riposo dei muscoli respiratori (ventilazione meccanica) B Supporto psico-sociale C Nutrizione B Tabella 3 – Sede dell’intervento riabilitativo SEDE INDICAZIONE Domiciliare Mantenimento, stabile con problemi di trasporto, non trasportabili, che non vogliono ricoverarsi Ambulatoriale Singoli interventi di fisioterapia Day-Hospital Paziente in fase stabile senza problemi di trasporto Degenza ordinaria Paziente severo, instabile, con necessità di UTIR ventilazione domiciliare, stabili con problemi di trasporto Indicazioni alla UTIR Componenti dei PRR Allenamento all’esercizio: l’allenamento aerobico, in particolare quello degli arti inferiori è obbligatorio (11) e benefici possono essere ottenuti con carichi di lavoro di varia intensità (46-49). I maggiori benefici nella risposta massimale e sottomassimale possono essere ottenuti dopo esercizio ad alto carico (per es. maggiore del 60% del carico di lavoro massimale, cioè sopra la soglia anaerobica) (46). L’allenamento di pazienti BPCO al 60-75% del carico massimale si associa a sostanziali incrementi della massima capacità di esercizio con riduzione della ventilazione e dei livelli di lattati a isocarico. La maggior parte dei PRR include allenamento all’endurance con periodi di esercizio sostenuto per circa 20-30 minuti, da 2 a 5 volte la settimana. In pazienti che non possono tollerare alti livelli di intensità, l’“interval training” consistente in 2-3 minuti di esercizio ad alta intensità con uguali periodi di riposo, può essere una alternativa (50). Per quanto l’esatto meccanismo fisiopatologico sottostante sia ancora non chiaro, vi è evidenza che la CPAP e differenti modalità di ventilazione non invasive a pressione positiva (NPPV) possono ridurre la dispnea e aumentare la tolleranza all’esercizio fisico. Lo scarico dei muscoli respiratori e la riduzione della pressione positiva di fine espirazione “intrinseca” (PEEPi) sono stati considerati fra i meccanismi alla base di questi effetti. Tuttavia il ruolo della NPPV nella riabilitazione respiratoria, se pure c’è, è ancora controverso. L’aggiunta di NPPV domiciliare notturna a un programma di esercizio diurno in pazienti con BPCO severa ha determinato un vantaggio sulla capacità di esercizio e sulla qualità di vita (51-58). Nei pazienti con BPCO severa l’applicazione di stimolazione elettrica dei muscoli periferici combinata con mobilitazione attiva degli arti, ha miglio- 139 rato significativamente la forza muscolare e l’“interval training” si è dimostrato capace di indurre effetti fisiologici di allenamento (50,59-62). La somministrazione di ossigeno in pazienti che non desaturano durante l’esercizio sembra essere promettente poiché permette più alte intensità di allenamento e quindi maggiore efficacia di allenamento (63-69). 140 Altri interventi: il supporto nutrizionale, gli steroidi anabolizzanti (70), l’ormone della crescita (71) sono stati usati con risultati contrastanti come complementi ai PRR. Il contributo dei programmi educazionali “per se”, non inseriti in PRR comprendenti allenamento all’esercizio è incerto (12). Con il termine di “rieducazione respiratoria” si intende un insieme di tecniche come la “respirazione a labbra socchiuse” e la “respirazione diaframmatica”. Gli studi sulla “respirazione diaframmatica” hanno mostrato una mancanza di beneficio, se non addirittura effetti negativi, in pazienti BPCO di varia gravità (72,73). L’allenamento dei muscoli respiratori è in grado di aumentarne la forza e l’endurance. Tuttavia nei pazienti BPCO, una meta-analisi ha riportato solo scarsa evidenza di benefici clinicamente importanti in pazienti con BPCO (74). Questa modalità non dovrebbe essere usata in pazienti con fibre muscolari danneggiate e in adattamento funzionale (75). Nonostante i progressi fatti, maggiori informazioni sono necessarie per garantire un trattamento appropriato al crescente numero di pazienti con BPCO che partecipano ai PRR. Quali sono i correlati biologici dei miglioramenti indotti dall’allenamento all’esercizio? Studi preliminari mostrano che programmi di allenamento all’endurance sono in grado di aumentare la concentrazione di ossido nitrico esalato nei pazienti BPCO (76). Quale ne è il significato? Abbiamo bisogno di maggiori informazioni sull’impatto sui costi della sanità (41,42) e sulla sopravvivenza (43,44). Sebbene i vantaggi dell’allenamento all’esercizio siano ben definiti, poco si conosce sull’efficacia delle singole componenti dei PRR (31,77). Qual è il ruolo (se esiste) della messa a riposo dei muscoli respiratori con la ventilazione meccanica non invasiva (78) ? Quale potrebbe essere l’utilità di altre modalità come la respirazione di miscele di elio durante i programmi di allenamento (79) ? Qual è il ruolo della riabilitazione respiratoria nei pazienti con riacutizzazioni (80) ? Conclusioni C’è evidenza scientifica che la riabilitazione respiratoria nei pazienti con malattie respiratorie croniche abbia effetti clinici positivi. La dispnea e la tolleranza all’esercizio fisico sono i sintomi che più migliorano dopo un PRP. Questi programmi sono impegnativi per il paziente, dal punto di vista economico ed organizzativo, di conseguenza dovrebbero essere inseriti in programmi standard di trattamento dei pazienti con BPCO e dovrebbero quindi essere applicati in centri e da personale specializzati. BIBLIOGRAFIA 1. Anthonisen NR, Connett JE, Kiley JP et al. Effects of smoking intervention and the use of an inhaled anticholinergic bronchodilator on the rate of decline of FEV1. JAMA 1994; 272: 1497-1505. 2. Report of British Research Medical Council Working Party. Long-term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complication in chronic bronchitis and emphysema. Lancet 1981; i: 681-686. 3. Restrick LJ, Paul EA, Braid GM et al. Assessment and follow up of patients prescribed long term oxygen therapy. Thorax 1993; 48: 708713. 4. Decramer M, Gosselink R, Trooster T et al. Muscle weakness is related to utilization of health care resources in COPD patients. Eur Respir J 1997; 10: 417-423. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 13. La riabilitazione respiratoria nel trattamento della BPCO - N. Ambrosino, M. Serradori 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. Connors AFJr, Dawson NV, Thomas C et al. Outcomes following acute exacerbation of severe chronic obstructive lung disease. Am J Respir Crit Care Med 1996; 154: 959-967. NIH Workshop Summary. Pulmonary Rehabilitation Research. Am J Respir Crit Care Med 1994; 149: 825-833. Donner CF, Howard P. Pulmonary rehabilitation in chronic obstructive pulmonary disease (COPD) with recommendations for its use. Eur Respir J 1992; 5: 266-275. American Thoracic Society. Pulmonary Rehabilitation 1999. Am J Respir Crit Care Med 1999; 159: 1666-168. BTS Standards of Care Subcommittee on Pulmonary Rehabilitation. Pulmonary Rehabilitation. Thorax 2001; 56; 827-834. ACCP/AACVPR. Pulmonary rehabilitation. Joint ACCP/AACVPR evidence-based guidelines. Chest 1997; 112: 1363-1396. Goldstein RS, Gort EH, Stubbing D et al. Randomised controlled trial of respiratory rehabilitation. Lancet 1994; 344: 1394-1397. Ries Al, Kaplan RM, Limberg TM, Prewitt LM. Effects of pulmonary rehabilitation on physiologic and psychosocial outcomes in patients with chronic obstructive pulmonary disease. Ann Intern Med 1995; 122: 823-832. Griffiths TL, Burr ML, Campbell IA et al. Results at 1 year of outpatient multidisciplinary pulmonary rehabilitation: a randomized controlled trial. Lancet 2000; 355: 362-368. Troosters T, Gosselink R, Decramer M. Short- and long-term effects of outpatient rehabilitation in patients with chronic obstructive pulmonary disease: a randomized trial. Am J Med 2000; 109:207-212. Guell R, Casan P, Belda J et al. Long-term effects of outpatient rehabilitation of COPD. A randomized trial. Chest 2000; 117: 976-983. Lacasse Y, Wong E, Guyatt GH et al. Meta-analysis of respiratory rehabilitation in chronic obstructive pulmonary disease. Lancet 1996; 348: 1115-1119. Pauwels RA, Buist AS, Calverley PMA et al. on behalf of the GOLD Scientific Committee. Global strategy for the diagnosis, management and prevention of chronic obstructive lung disease. NHLBI/WHO global initiative for chronic obstructive lung disease (GOLD) workshop summary. Am J Respir Crit Care Med, 2001; 163: 1256-1276. Calverley PM, Walker P. Chronic obstructive pulmonary disease. Lancet 2003 27; 362: 1053-61. Rennard SI. Treatment of stable chronic obstructive pulmonary disease. Lancet 2004; 364: 791-802. Ambrosino N, Foglio K. Selection criteria for pulmonary rehabilitation. Respir Med 1996; 90: 317-322. Couser JI, Guthmann R, Hamadeh MA, Kane CS. Pulmonary rehabilitation improves exercise capacity in older elderly patients with COPD. Chest 1995; 107: 730-734. Foster S, Lopez D, Thomas H M III. Pulmonary rehabilitation in COPD patients with elevated PCO2. Am Rev Respir Dis 1988; 138: 15191523. Berry MJ, Rejeski WJ, Adair NE, Zaccaro D. Exercise rehabilitation and chronic obstructive pulmonary disease stage. Am J Respir Crit Care Med 1999; 160: 1248-1253. Criner GJ, Cordova FC, Furukawa S et al. Prospective randomized trial comparing bilateral lung volume reduction surgery to pulmonary rehabilitation in severe chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 160: 2018-2027. Pompeo E, Marino M, Nofroni I et al. Reduction pneumoplasty versus respiratory rehabilitation in severe emphysema: a randomised study. Ann Thorac Surg 2000; 70: 948-954. Stiebellehner L, Quittan M, End A et al. Aerobic endurance training program improves exercise performance in lung transplant recipients. Chest 1998; 113: 906-912. Ries AL, Farrow JT, Clausen JL. Pulmonary function tests cannot predict exercise-induced hypoxemia in chronic obstructive pulmonary disease. Chest 1988; 93: 454-459. Mathur RS, Revill SM, Vara DD et al. Comparison of peak oxygen consumption during cycle and treadmill exercise in severe chronic obstructive pulmonary disease. Thorax 1995; 50: 829-833. Ambrosino N. Field tests in pulmonary disease. Thorax 1999; 54; 191-193. Foglio K, Carone M, Pagani M et al. Physiological and symptom determinants of exercise performance in patients with chronic airway obstruction (CAO). Respir Med 2000; 94: 256-263. Mahler D, Guyatt GH, Jones PW. Clinical measurement of dyspnea. In Mahler D. Dyspnea. Marcel Dekker Pub. New York, 1998, 149198. Mahler DA, Weinberg DH, Wells CK, Feinstein AR. The measurements of dyspnea, contents, interobserver agreement and physiologic correlates of two new clinical indexes. Chest 1984; 85: 751-758. Lacasse Y, Wong E, Guyatt G, Goldstein RS. Health-Status measurement and Cardiopulmonary Rehabilitation. In Jobin J, Maltais F, LeBlanc P, Simard C. Advances in Cardiopulmonary Rehabilitation (eds). Human Kinetics (Pub), Champaign, IL, USA, 2000, 228-246. Ketelaars CAJ, Abu-Saad HH, Schlösser MAG et al. Long-term outcome of pulmonary rehabilitation in patients with COPD. Chest 1997; 112:363-369. Foglio K, Bianchi L, Bruletti G et al. Long-term effectiveness of pulmonary rehabilitation in patients with chronic airway obstruction.(CAO). Eur Resp J 1999; 11: 125-132. Foglio K, Bianchi L, Ambrosino N. Is it really useful to repeat outpatient pulmonary rehabilitation programs in patients with chronic airway obstruction? A 2-year controlled study. Chest 2001; 119:1696-1704. Ries AL, Kaplan RM, Myers R, Prewitt LM. Maintenance after pulmonary rehabilitation in chronic lung disease: a randomized trial. Am J Respir Crit Care Med 2003;167: 880-8. Wijkstra PJ, van der Mark TW, Kraan J et al. Effects of home rehabilitation on physical performance in patients with chronic obstructive pulmonary disease (COPD). Eur Respir J 1996; 9:104-110. Clini E, Foglio K, Bianchi L et al. In-hospital short-term training program in patients with chronic airway obstruction (CAO). Chest 2001; 120: 1500-1505. Wedzicha JA, Bestall JC, Garrod R et al. Randomized controlled trial of pulmonary rehabilitation in severe chronic obstructive pulmonary disease patients, stratified with the MRC dyspnoea scale. Eur Respir J 1998; 12:363-369. Griffiths TL, Phillips CJ, Davies S et al. Cost effectiveness of an outpatient multidisciplinary pulmonary rehabilitation programme. Thorax 2001; 56:779-784. 141 142 42. Golmohammadi K, Jacobs P, Sin D. Economic evaluation of a community-based pulmonary rehabilitation program for chronic obstructive pulmonary disease. Lung 2004;182:187-96. 43. Gerardi DA, Lovett ML, Benoit-Connors JZ, Zu Wallack RL. Variables related to increased mortality following out-patient pulmonary rehabilitation. Eur Respir J 1996; 9: 431-435. 44. Bowen JB, Votto JJ, Thrall RS et al. Functional status and survival following pulmonary rehabilitation. Chest 2000; 118: 697-703. 45. Lacasse Y, Guyatt GH, Goldstein RS. The Component of a Respiratory Rehabilitation Program. A Systematic Overview. Chest 1997; 111: 1077-1088. 46. Casaburi R, Patessio A Ioli F, et al. Reductions in exercise lactic acidosis and ventilation as a result of exercise training in patients with obstructive lung disease. Am Rev Respir Dis 1991; 143: 9-18. 47. Maltais F, LeBlanc P, Jobin J et al. Intensity of training and physiologic adaptation in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1997; 155: 555-561. 48. Maltais F, LeBlanc P, Simard C et al. Skeletal muscle adaptation to endurance training in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1996; 154: 442-447. 49. O’Shea SD, Taylor NF, Paratz J. Peripheral muscle strength training in COPD. A systematic review. Chest 2004; 126: 903-914. 50. Coppoolose R, Schols AMWJ, Baarends EM et al. Interval versus continuous training in patients with severe COPD: a randomized clinical trial. Eur Respir J 1999; 14: 258-263. 51. Bianchi L, Foglio K, Pagani M, Vitacca M, Rossi A, Ambrosino N. Effects of proportional assist ventilation on exercise tolerance in COPD patients with chronic hypercapnia. Eur Resp J 1998; 11: 422-427. 52. Hernandez P, Maltais F, Gursahaney A, Leblanc P, Gottfried SB. Proportional Assist Ventilation may improve exercise perfor-mance in severe chronic obstructive pulmonary disease. J Cardiopulm Rehabil 2001; 21: 135–142. 53. van't Hul A, Kwakkel G, Gosselink R. The acute effects of noninvasive ventilatory support during exercise on exercise endurance and dyspnea in patients with chronic obstructive pulmonary disease: a systematic review. J Cardiopulm Rehabil 2002; 22: 290-297. 54. Bianchi L, Foglio K, Porta R, Baiardi R, Vitacca M, Ambrosino N. Lack of additional effect of adjunct of assisted ventilation to pulmonary rehabilitation in mild COPD patients. Respir Med 2002; 96: 359-367. 55. Hawkins P, Johnson LC, Nikoletou D, et al. Proportional assist ventilation as an aid to exercise training in severe chronic obstructive pulmonary disease Thorax 2002; 57: 853-859. 56. Johnson JE, Gavin DJ, Usar M, Adams-Dramiga S. Effects of Training With Heliox and Noninvasive Positive Pressure Ventilation on Exercise Ability in Patients With Severe COPD. Chest 2002; 122: 464-472. 57. Costes F, Agresti A, Court-Fortune I, Roche F, Vergnon JM, Barthelemy JC. Noninvasive ventilation during exercise training improves exercise tolerance in patients with chronic obstructive pulmonary disease. J Cardiopulm Rehabil 2003; 23: 307-313. 58. Garrod R, Mikelsons C, Paul EA, Wedzicha JA. Randomized controlled trial of domiciliary noninvasive positive pressure ventilation and physical training in severe chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2000; 162: 1335-1341. 59. Neder JA, Sword D, Ward SA, Mackay E, Cochrane LM, Clark CJ. Home based neuromuscular electrical stimulation as a new rehabilitative strategy for severely disabled patients with chronic obstructive pulmonary disease (COPD). Thorax 2002; 57: 333-337. 60. Bourjeily-Habr G, Rochester CL, Palermo F, Snyder P, Mohsenin V. Randomised controlled trial of transcutaneous electrical muscle stimulation of the lower extremities in patients with chronic obstructive pulmonary disease. Thorax 2002; 57: 1045-1049. 61. Zanotti E, Felicetti G, Maini M, Fracchia C. Peripheral muscle strength training in bed-bound patients with COPD receiving mechanical ventilation. Effect of electrical stimulation. Chest 2003; 124: 292-296. 62. Vogiatzis I, Nanas S, Roussos C. Interval training as an alternative modality to continuous exercise in patients with COPD. Eur Respir J 2002;20:12-19. 63. Terrados N, Jansson E, Sylven C, Kaijser L. Is hypoxia a stimulus for synthesis of oxidative enzymes and myoglobin? J Appl Physiol 1990; 68: 2369-2372. 64. Garrod R, Paul EA, Wedzicha JA. Supplemental oxygen during pulmonary rehabilitation in patients with COPD with exercise hypoxaemia. Thorax 2000; 55: 539-543. 65. Fichter J, Fleckenstein J, Stahl C, Sybrecht GW. Effect of oxygen (FI02: 0.35) on the aerobic capacity in patients with COPD. Pneumologie 1999; 53: 121-126. 66. McDonald CF, Blyth CM, Lazarus MD, Marschner I, Barter CE. Exertional oxygen of limited benefit in patients with chronic obstructive pulmonary disease and mild hypoxemia. Am J Respir Crit Care Med 1995; 152: 1616-1619. 67. Rooyackers JM, Dekhuijzen PN, Van Herwaarden CL, Folgering HT. Training with supplemental oxygen in patients with COPD and hypoxaemia at peak exercise. Eur Respir J 1997; 10: 1278-1284. 68. Wadell K, Henriksson-Larsen K, Lundgren R. Physical training with and without oxygen in patients with chronic obstructive pulmonary disease and exercise-induced hypoxaemia. J Rehabil Med 2001; 33: 200-205. 69. Emtner M, Porszasz J, Burns M, Somfay A, Casaburi R. Benefits of supplemental oxygen in exercise training in non-hypoxemic COPD patients. Am J Respir Crit Care Med 2003; 68: 1034-1042. 70. Schols AMWJ, Soeters PB, Mostert R et al. Physiologic effects of nutritional support and anabolic steroids in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1995; 152: 1268-1274. 71. Burdet L, de Muralt B, Schutz Y et al. Administration of growth hormone to underweight patients with chronic obstructive pulmonary disease. A prospective randomized, controlled study. Am J Respir Crit Care Med 1997; 156: 1800-1806. 72. Gosselink R, Foglio K, Ambrosino N. Breathing exercises. In Ambrosino N, Donner CF, Rampulla C. Topics in pulmonary rehabilitation. Maugeri Foundations Book. 199; 209-228. 73. Vitacca M, Clini E, Bianchi L, Ambrosino N. Acute effects of deep diaphragmatic breathing in COPD patients with chronic respiratory insufficiency. Eur Respir J 1998; 11, 408-415. 74. Smith K, Cook D, Guyatt GH et al. Respiratory muscle training in chronic airflow limitation: a meta-analysis. Am Rev Respir Dis 1992; 145: 533-539. 75. Orozco-Levi M, Lloreta J, Minguella J et al. Injury of the human diaphragm associated with exertion and chronic obstructive pulmonary di- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 13. La riabilitazione respiratoria nel trattamento della BPCO - N. Ambrosino, M. Serradori sease. Am J Respir Crit Care Med 2001; 164: 1734-1739. 76. Clini E, Bianchi L, Foglio K et al. Effect of pulmonary rehabilitation on exhaled nitric oxide in patients with chronic obstructive pulmonary disease. Thorax 2001, 56: 519-523. 77. Mador MJ, Bozkanat E, Aggarwal A, Shaffer M, Kufel TJ. Endurance and strength training in patients with COPD. Chest. 2004;125:203645. 78. Ambrosino N, Strambi S. New strategies to improve exercise tolerance in chronic obstructive pulmonary disease. Eur Resp J 2004; 23: 313-322. 79. Palange P, Valli G, Onorati P, et al. Effect of heliox on lung dynamic hyperinflation, dyspnea and exercise endurance cpacity in COPD patients. J Appl Physiol 2004; 97: 1637-1642. 80. Man WD, Polkey MI, Donaldson N, Gray BJ, Moxham J. Community pulmonary rehabilitation after hospitalisation for acute exacerbations of chronic obstructive pulmonary disease: randomised controlled study. BMJ 2004; 329: 1209-13. 143 14. La BPCO nell’anziano A cura di Vincenzo Bellia Istituto di Medicina generale e Pneumologia Università di Palermo, Palermo 14. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione Secondo le recenti Linee Guida NICE “la broncopneumopatia cronica ostruttiva (BPCO) è caratterizzata da ostruzione al flusso aereo. L’ostruzione è solitamente progressiva, non completamente reversibile e non si modifica marcatamente nell’arco di parecchi mesi”. Su questa base l’espressione “la BPCO nell’anziano” che dà il titolo a questo capitolo costituisce di fatto un pleonasmo: la BPCO infatti, è comunque una malattia dell’anziano, almeno se considerata nei suoi quadri conclamati, in cui trovano espressione più piena i caratteri distintivi dell’ostruzione irreversibile, per non parlare dei disordini dei gas ematici e della disabilità: di fatto la maggior parte dei casi riceve la prima volta una diagnosi di BPCO dopo aver compiuto i 50 anni, mentre l’età media dei pazienti in ossigenoterapia a lungo termine si pone intorno ai 70 anni. È pur vero però che secondo le Linee Guida GOLD può essere inquadrata nella BPCO anche la condizione di chi, in assenza di riduzione della pervietà bronchiale e della limitazione del flusso espiratorio, presenta sintomi quali tosse ed espettorazione croniche, il cosiddetto Stadio 0. Su questa base la prevalenza della malattia nei soggetti di età compresa tra 20 e 44 anni in Europa sarebbe superiore al 10%. Questa impostazione estensiva dei termini applicativi della diagnosi di BPCO è però messa in discussione poiché lo Stadio 0 corrisponderebbe ad una condizione di instabilità che non ha necessariamente valore predittivo nei confronti del rischio di sviluppare la BPCO conclamata nelle fasi ulteriori della vita. Peraltro, come dimostrato dallo studio multicentrico italiano “Salute Respiratoria nell’Anziano” (Sa.R.A.), anche in età avanzata è frequente il riscontro di quadri caratterizzati dai sintomi della bronchite cronica “semplice”, nei quali, cioè, nonostante l’esposizione per molti decenni a fattori di rischio come il fumo di tabacco, non si è registrata (né più si registrerà) l’evoluzione verso l’ostruzione bronchiale dimostrata spirometricamente. Comunque si consideri la questione, sul piano pragmatico non vi è dubbio sul fatto che il maggior impegno assistenziale ed il maggior carico di costi gravino sulle fasce d’età geriatrica: la BPCO rappresenta la seconda causa di disabilità nella popolazione anziana. Nonostante la consapevolezza dei rapporti tra invecchiamento e BPCO vada diffondendosi, sono ancora in numero limitato gli studi diretti a definire i caratteri peculiari che la malattia assume per il fatto di sovrapporre i suoi effetti a quelli prodotti dal fisiologico avanzare dell’età. Inoltre appare indubbio il fatto che la patologia respiratoria dell’anziano continui a ricevere un’attenzione molto scarsa, particolarmente fuori dell’ambiente specialistico pneumologico: era e continua ad essere frequente il caso di mancata o errata diagnosi particolarmente nell’evenienza assai comune di pazienti con multiple comorbilità. Per conseguenza non è raro il riscontro di casi di mancanza o inadeguatezza dei trattamenti. Valutazione dell’anziano con BPCO L’inquadramento diagnostico della BPCO si realizza nell’anziano con modalità non dissimili da quelle valide in generale e tradizionalmente basate sull’anamnesi (fattori di rischio, sintomi compatibili), nonché sulla valutazione funzionale (spirometria con test di broncodilatazione). Tuttavia non si può ignorare il fatto che l’invecchiamento dell’apparato respiratorio determina alcuni effetti di confondimento. Se si considera come il polmone senile mimi molte caratteristiche dell’enfisema (per es. la forma del torace a botte, la perdita di elasticità parenchimale, la disfunzione dei muscoli respiratori) non è sorprendente che soggetti con sintomi respiratori occasionali e transitori (per es. tosse da flogosi acuta delle vie aeree) o con sintomi derivanti da patologie extrapolmonari (per es. dispnea o riduzione della tolleranza allo sforzo da cause cardiovascolari) ricevano una diagnosi impropria di BPCO che spesso li accompagnerà acriticamente come un marchio per il resto della vita; questo tipo di errori ricorre più frequentemente nel sesso maschile. Un’altra possibile occasione di errori diagnostici in tema di BPCO interessa i soggetti anziani affetti da asma bronchiale: è diffuso infatti un pregiudizio culturale che ancora og- 145 146 gi induce a ritenere assai raro il riscontro dell’asma in età geriatrica. Pertanto, l’anziano che presenti tosse e dispnea croniche è esposto ad un rischio significativo di essere comunque etichettato come affetto da BPCO, talora anche se in assenza di riconosciuti fattori di rischio per questa malattia (per es. non fumatore) e spesso senza una adeguata valutazione spirometrica del tipo della broncoostruzione e della sua reversibilità. Oltre all’età anche la presenza di una disabilità costituisce un fattore di rischio per erronea diagnosi di BPCO in asmatici anziani. La valutazione spirometrica costituisce una componente essenziale del corretto approccio diagnostico alla BPCO nel senso più ampio: tuttavia nel paziente geriatrico occorre mettere in atto alcuni adattamenti esecutivi del test ed è necessario pure adottare alcune cautele interpretative nella lettura dei risultati. Per quanto riguarda l’esecuzione delle misure, i risultati dello studio Sa.R.A. indicano che oltre l’80% degli anziani non ospedalizzati e deambulanti sono in grado di eseguire una spirometria complessivamente rispondente ai criteri di accettabilità dell’ATS: tuttavia la compliance con i diversi criteri è variabile. In particolare i risultati meno soddisfacenti sono stati registrati per quanto riguarda il criterio relativo al tempo del plateau teleespiratorio (cioè almeno un secondo per un minimo di tre curve). Su questo criterio deve dunque essere esercitata una certa tolleranza, tenendo conto del fatto che tra i fattori di rischio per una performance spirometrica imperfetta sono compresi un deficit cognitivo ed un basso livello di scolarità, che determinano la difficoltà ad interagire con l’operatore, a comprenderne le istruzioni e a metterle in atto. Il terzo fattore di rischio per scarsa accettabilità secondo lo studio Sa.R.A. è rappresentato da un risultato scadente al test del cammino per sei minuti: in altri termini la complessiva performance fisica e l’assenza di disabilità rappresentano una delle principali condizioni per l’esecuzione di una corretta spirometria. Per quanto riguarda l’interpretazione dei risultati, secondo le indicazioni dell’ATS occorre innanzitutto fare riferimento a valori teorici derivati da una adeguata popolazione della stessa fascia d’età e della medesima origine etnica rispetto ai pazienti in corso di valutazione. Recentemente equazioni di calcolo dei teorici sulla popolazione geriatrica italiana sono stati prodotti e resi disponibili sulla base dei risultati dello studio Sa.R.A. già citato. Dato poi per scontato il riferimento a valori “normali” appropriati, la definizione del significato diagnostico delle misure ed in particolare la scelta dei livelli di cut-off necessari per definire l’esistenza di una patologia necessitano l’esercizio di senso critico. L’analisi del decadimento senile di molti parametri funzionali dimostra che la variabilità delle misure attorno alla media aumenta con l’avanzare dell’età: ne deriva che livelli di taglio che risultano appropriati in età giovanile possono condurre ad errori di sovradiagnosi in età geriatrica. In uno studio norvegese condotto su soggetti asintomatici ultrasettantenni non fumatori è stato rilevato che sulla base dell’applicazione dei criteri GOLD alla spirometria circa il 35% dei soggetti sarebbe stato impropriamente considerato affetto da BPCO in Stadio I, mentre la percentuale poteva salire a circa il 50% negli ultraottantenni. Occorre pertanto ridefinire i criteri di determinazione dei livelli di cut-off delle Linee Guida; questi, peraltro mostrano anche altri limiti qualora si correlino gli stadi classificativi con la condizione di salute valutata con specifiche metodologie nell’intento di rilevare le differenze corrispondenti a ciascun passaggio di stadio. Nell’ambito dello studio Sa.R.A., condotto su pazienti ultrasessantacinquenni, il confronto degli stadi GOLD con il punteggio conseguito al Saint Georgès Respiratory Questionnaire (SGRQ), uno strumento di misura della percezione soggettiva dello stato di salute (ovvero della cosiddetta qualità di vita correlata alla salute) specifico per le pneumopatie ostruttive croniche, ha dimostrato che gli Stadi 0, I e II posseggono una scarsa capacità discriminativa in quanto corrispondono ad un declino molto graduale dello stato di salute, mentre i punteggi mostrano una marcata sovrapposizione fra i tre Stadi. È invece il passaggio dallo Stadio IIa al IIb (corrispondenti agli Stadi II e III della classificazione aggiornata) ad essere segnato dal più rilevante peggioramento dello stato di salute, mentre i punteggi fanno registrare una scarsa so- Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 14. La BPCO nell’anziano - V. Bellia vrapposizione tra questi due Stadi. Anche il passaggio dallo Stadio II al III (ovvero III e IV della nuova classificazione) è segnato da un ulteriore scadimento del punteggio del SGRQ. Questi risultati inducono a formulare due ordini di considerazioni. In primo luogo se si considera come il passaggio allo Stadio IIb, che è risultato così determinante ai fini del deterioramento dello stato di salute, corrisponda ad un FEV1 contenuto tra il 30 ed il 49% del teorico, si conferma l’assoluta inappropriatezza dell’uso di soglie arbitrarie come l’80% già messo in discussione dallo studio norvegese ed emerge assai viva l’esigenza di riscrivere il sistema classificativo, almeno all’interno della popolazione geriatrica. In secondo luogo scaturisce evidente l’importanza di supportare l’approccio diagnostico alla BPCO (in generale, ma massime nell’anziano) con una valutazione multidimensionale che tenga conto dei molteplici aspetti della disfunzione e della disabilità cui si accompagna la BPCO. Per completare la valutazione respiratoria una stima del grado di dispnea (mediante questionario o scale analogico-visive) deve obbligatoriamente fare parte dell’approccio basilare a ciascun paziente in stato stabile. Questa valutazione è stata recentemente inclusa insieme con il body mass index (BMI), la misura del FEV1 e la distanza percorsa in sei minuti in un indice definito BODE, del quale è stato dimostrato l’elevato valore prognostico della mortalità. Per quanto riguarda gli aspetti extrarespiratori della valutazione multidimensionale, questi devono innanzi tutto comprendere il rilievo della condizione socio-economica e familiare che spesso condiziona drammaticamente qualunque possibilità di trattamento efficace dell’anziano; indispensabile è inoltre una determinazione della complessiva capacità di performance fisica attraverso questionari come il test di Barthel, o prove sul campo come il test del cammino per sei minuti. Mentre questo ultimo test va sempre più affermandosi, ancora scarso utilizzo fuori degli ambienti specialistici geriatrici hanno i test di screening della performance cognitiva come il Mini Mental Status test e quelli relativi allo stato affettivo, come la Geriatric Depression Scale che esplora la depressione o la scala di Hamilton che valuta sia l’ansia che la depressione. Infine la valutazione complessiva dell’anziano con BPCO non può trascurare una sistematica identificazione e “pesatura” delle patologie indipendenti dalla BPCO e che coesistono nel caso in esame: la polipatologia costituisce un connotato dell’età avanzata che sovrappone i suoi effetti a quelli della BPCO influenzando il quadro clinico, la prognosi e la risposta ai trattamenti. La frequenza di tale condizione è variamente stimata nelle diverse popolazioni (minore nei pazienti ambulatoriali, come quelli dello studio Sa.R.A., maggiore in quelli ospedalizzati o comunque istituzionalizzati), anche in relazione alla metodologia utilizzata per il rilievo e la codifica (uso di questionari specifici, registrazione “passiva” etc.): essa appare comunque elevata e crescente con l’avanzare dell’età (fig. 1). È stato dimostrato che la coesistenza di altre patologie può influenzare negativamente vari aspetti della prognosi della BPCO, quali la severità delle riacutizzazioni (per es. nel caso del diabete mellito) e la mortalità (per es. nel caso dell’insufficienza renale). Figura 1 – Frequenza di patologie associate nell’anziano 25 Frequenza (%) 20 15 10 5 0 Ipertensione Osteoartrosi Cardiopatia ischemica Diabete Scompenso II classe Deficit visivo Deficit uditivo Ipertrofia prostatica 147 La valutazione della multimorbilità deve infine far parte del processo decisionale che conduce alle scelte terapeutiche: si pensi alle limitazioni all’uso di teofillinici e simpaticomimetici nei cardiopatici o alle cautele nell’uso dei corticosteroidi negli ipertesi o nei pazienti affetti da osteoporosi. Principi di trattamento Nell’impostazione del trattamento diretto all’anziano occorre innanzitutto porre attenzione alle condizioni generali che spesso influenzano in modo rilevante la sintomatologia, la qualità di vita ed infine la prognosi: è questo il caso della condizione nutrizionale: tanto la malnutrizione (espressa da un BMI<22) quanto l’obesità (BMI>28) hanno effetti negativi: tuttavia la prima deve essere particolarmente oggetto di attenzione a causa della sua prevalenza (pari almeno al 20%) e poiché implica una perdita di massa magra che penalizza soprattutto l’apparato muscolare. Figura 2 – Patogenesi della sarcopenia 148 Invecchiamento Fattori genetici Ipossia Acidosi Perdita della massa muscolare Ridotta attività fisica Sedentarietà-allettamento Flogosi Comorbilità Stress ossidativo Malattie endocrine Scompenso cardiaco Infezioni Terapia steroidea Alimentazione Deficit calorico-proteico Deficit vitaminici La ridotta efficienza muscolare, oltre a contribuire a determinare la limitazione della tolleranza allo sforzo, può facilitare l’insorgenza di insufficienza respiratoria globale dal momento che il deficit muscolare non risparmia i muscoli respiratori che nella BPCO sono chiamati a sostenere l’aumentato carico ventilatorio determinato dall’ostruzione bronchiale; inoltre un deficit trofico e/o funzionale dei muscoli dà luogo ad una limitazione dell’efficacia espulsiva della tosse cui è riconosciuta un’importanza fondamentale nel complesso dei meccanismi di protezione dell’albero respiratorio. Occorre pertanto controllare correggere o, ancor meglio, prevenire la malnutrizione assicurando un adeguato introito calorico ed eventualmente integrando la dieta con supplementi ricchi di lipidi allo scopo di ridurre la produzione endogena di CO2. È però doveroso segnalare che gli studi diretti a valutare l’efficacia degli interventi nutrizionali ai fini della modificazione della prognosi non hanno sinora dato risultati significativi. Nell’ambito dell’attenzione alle condizioni muscolari occorre pure prevenire la possibilità di insorgenza di miopatia da steroidi, i cui effetti negativi si sommerebbero a quelli della sarcopenia: è pertanto necessario limitare l’uso degli steroidi sistemici e incoraggiare una costante attività fisica. Sotto questo profilo è raccomandabile un programma riabilitativo strutturato sia in ambito propriamente respiratorio, sia in ambito motorio più generale: esso può prevenire, ritardare o limitare la disabilità e migliorare lo stato di salute. Sul piano farmacologico i principi di trattamento della BPCO nell’anziano non sono diversi da quelli codificati per la popolazione generale dei soggetti affetti: in particolare non cambiano i presidi disponibili, né le loro strategie di impiego. Tuttavia numerosi aspetti dell’invecchiamento possono condizionare l’efficacia o la sicurezza di impiego dei diversi trattamenti oppure limitarne l’applicabilità, (per es. attraverso una limitazione della compliance al trattamento dovuta al difetto della memoria o dell’attenzione). Modificazioni involutive dei tessuti, nella distribuzione e funzionalità dei recettori, o nei meccanismi di controllo possono condizionare l’efficacia dei farmaci nel paziente anziano; inoltre modificazioni di organi e funzioni non respiratori, dovuti ad involuzione senile (per es. a carico del rene o del fegato) o a patologie associate (per es. a carico dell’apparato cardiovascolare), possono interferire sulla farmacocinetica o sulla farmacodinamica dei trattamenti. L’efficacia di questi ultimi può anche essere liRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 14. La BPCO nell’anziano - V. Bellia mitata da altri fenomeni connessi con l’involuzione senile dell’organismo: si pensi a vari aspetti della disabilità (riduzione della destrezza, perdita della forza muscolare, progressiva diminuzione del visus etc.) che possono interferire con la capacità di eseguire trattamenti complessi o di utilizzare tecnologie inusuali quali le sorgenti per l’ossigenoterapia o i presidi per la ventilazione meccanica non invasiva domiciliare. In realtà il problema è di riscontro molto più frequente e banale in quanto in primo luogo interessa diffusamente l’uso quotidiano dei dispositivi per l’erogazione di aerosol dosati o di polveri. La via inalatoria costituisce la scelta prioritaria poiché assicura la prontezza degli effetti terapeutici sulle vie aeree e la riduzione di quelli indesiderati extrarespiratori a causa della ridotta distribuzione sistemica dei farmaci. L’efficacia è funzione della percentuale di deposizione lungo l’albero bronchiale e questa, a sua volta, dipende in una misura importante dalle modalità di esecuzione dell’inalazione. Almeno il 50% dei pazienti mostra qualche difficoltà nell’uso dei dispositivi commerciali erogatori di aerosol dosati o di polveri. Il problema è ancor più frequente negli anziani: in uno studio su ultrasessantacinquenni soltanto il 10% mostrava una tecnica soddisfacente. Poiché tale tecnica costituisce oggetto di apprendimento non sorprende che il correlato più importante della qualità della performance inalatoria sia rappresentato dalla condizione delle funzioni cognitive. L’uso di spaziatori può migliorare l’efficienza dell’inalazione: tuttavia il confronto tra l’uso di erogatori di aerosol dosato dotati di spaziatori e quello di erogatori di polvere inalatoria in soggetti di età 75-101 anni dimostra che la probabilità di uso corretto è maggiore con i secondi che con i primi. Né può essere dimenticato il problema delle interferenze da parte di farmaci utilizzati per le patologie associate e capaci di influenzare il quadro clinico-funzionale (si pensi al peggioramento della broncocostrizione indotto dai β-bloccanti) o di aumentare il rischio di effetti collaterali (come può accadere nell’interazione tra diuretici e simpaticomimetici). Trattamento dello stato stabile Per quanto riguarda le modalità di trattamento a lungo termine dei soggetti anziani con BPCO in fase di stabilità clinica, in considerazione di quanto sin qui discusso, occorre privilegiare trattamenti di facile applicabilità ed utilizzabili nel lungo periodo (teoricamente sine die), senza o con limitati rischi di tachililassi e di effetti indesiderati. In questa prospettiva gli anticolinergici inalatori risultano spesso più efficaci dei β-stimolanti, verosimilmente in relazione ad una riduzione dell’attività dei β-recettori che accompagna l’invecchiamento. Nonostante osservazioni ormai remote suggerissero l’esistenza nell’anziano di una riduzione nel numero dei β-recettori, ricerche più recenti escludono modificazioni della densità dei recettori stessi. Questi sembrano piuttosto andare incontro ad una riduzione dell’affinità con l’invecchiamento; inoltre alterazioni dei meccanismi postrecettoriali potrebbero contribuire a giustificare il declino della risposta ai simpaticomimetici che si riscontra negli anziani. Anche per gli anticolinergici si osserva un certo declino dell’attività con l’invecchiamento; tuttavia questo si realizza meno rapidamente che con i simpaticomimetici. Il complessivo favore riscosso dagli antimuscarinici nella popolazione geriatrica è dovuto non soltanto a tale vantaggio farmacodinamico, ma anche alla migliore tolleranza ed all’assenza di rischio di tachifilassi. Infine gli anticolinergici inalatori non deprimono significativamente la clearance mucociliare e risultano di impiego sicuro anche nei pazienti di età avanzata che presentano una ipertrofia prostatica od altra patologia delle vie urinarie. L’indicazione prevalente è quella all’uso del tiotropio bromuro che offre il vantaggio addizionale della monosomministrazione quotidiana che favorisce l’aderenza alla prescrizione da parte dell’anziano. Occorre segnalare che un certo numero di pazienti anziani appaiono comunque più responsivi ai simpaticomimetici: in particolare i β-stimolanti trovano indicazione preferenziale nei pazienti che presentino una manifesta quota di reversibilità spirometrica al broncodilatatore in relazione o me- 149 150 no ad una anamnesi che risulti compatibile oltre che con la BPCO anche con asma e/o allergie (bronchite asmatiforme). Anche nei soggetti in cui la spirometria non mostri una apparente reversibilità, può essere indicato un trial con broncodilatatori sfruttando gli effetti non broncospasmolitici degli stessi (sulla clearance, sulla contrazione muscolare, sul circolo). In altri casi l’uso dei broncodilatatori in presenza di un’apparente negatività al test spirometrico di reversibilità può essere giustificato dal fatto che la mancata risposta ai simpaticomimetici o agli antimuscarinici è dovuta ad un prevalente effetto della flogosi bronchiale e della secrezione endoluminale: in queste circostanze, un ciclo adeguato di terapia steroidea ed un efficace drenaggio delle secrezioni possono ripristinare l’evidenza spirometrica della reversibilità. Nella scelta sulla modalità di somministrazione dei farmaci occorre valutare caso per caso in relazione alla performance funzionale, allo scopo di evitare sia il rischio di abuso e conseguente sovradosaggio (che potrebbe essere particolarmente pericoloso nell’anziano), sia il rischio di assunzione insufficiente per deficit della compliance o di assunzione inadeguata per uso erroneo del dispositivo inalatorio indicato dal medico. La miglior prevenzione di questi problemi si realizza attraverso un’attenta attività educazionale diretta ad insegnare a ciascun paziente le tecniche corrette: questa attività passa attraverso la verifica da parte del medico delle abilità conseguite e attraverso la reiterazione dei messaggi ed il rinforzo della motivazione. I derivati teofillinici hanno un ruolo secondario nel trattamento della BPCO in generale: ancor più limitata ne è la prospettiva di impiego nel paziente anziano. Infatti il rischio di eventi avversi, presente comunque a causa del limitato indice terapeutico, aumenta in età geriatrica, manifestandosi anche per livelli di teofillinemia entro range ritenuti accettabili nella popolazione generale. Occorre anche tenere in conto il rischio di alterazioni della cinetica dovute ai frequenti trattamenti concomitanti cui è costretto l’anziano a causa della comorbilità. L’uso dei teofillinici nella forma di preparati orali a lento rilascio può essere indicato in aggiunta agli altri broncodilatatori in caso di controllo insoddisfacente della broncocostrizione, particolarmente nelle ore notturne. Per quanto si riferisce all’uso dei corticosteroidi, occorre porre grande attenzione al rischio di accentuare l’osteoporosi assai frequente nel paziente anziano, con il pericolo di facilitare il verificarsi di fratture, con particolare riferimento a quelle vertebrali. Questi rischi sono ovviamente più elevati nel caso dell’impiego della via sistemica, ma la completa sicurezza dell’uso dei preparati inalatori in età geriatrica attende una conferma sperimentale. Trattamento delle riacutizzazioni Le riacutizzazioni nell’anziano possono essere particolarmente frequenti innanzitutto per effetto del deficit immunitario che caratterizza la senescenza e che facilita le infezioni; inoltre ricorrono più frequentemente eventi diversi, per lo più connessi con le comorbilità, capaci di scatenare i fenomeni della dispnea e della tosse e di motivare aggiustamenti terapeutici (tab. 1). I convenzionali principi terapeutici validi in senso generale si applicano anche nell’anziano. Occorre nei diversi casi intraprendere una terapia antibiotica ovvero iniziare o incrementare una terapia steroidea. Questa può inizialmente essere attuata per via sistemica con le cautele rese necessarie dalle frequenti patologie associate (ipertensione, diabete, cataratta etc.) che nell’anziano riducono la sicurezza di impiego dei corticosteroidi. In considerazione della rilevanza clnico-prognostica sfavorevole che le sempre più frequenti riacutizzazioni posseggono nell’anziano, è altamente raccomandabile la prassi delle vaccinazioni regolari, sia quella antiinfluenzale, da ripetere annualmente, sia quella antipneumococcica, da ripetere ogni 5 anni. Tabella 1 – Diagnostica differenziale delle riacutizzazioni della BPCO nell’anziano • • • • Insufficienza ventricolare sinistra, edema polmonare Embolia polmonare Polmoniti acquisite in comunità Polmoniti da aspirazioni • Versamenti pleurici • Ostruzione delle prime vie aeree • Carcinoma polmonare Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 14. La BPCO nell’anziano - V. Bellia Trattamenti concomitanti Per quanto riguarda la terapia mucolitica, pur se le valutazioni sono controverse, occorre segnalare che esistono evidenze sperimentali e metanalisi a favore di un azione positiva dei mucolitici nella direzione della riduzione delle riacutizzazioni. Recentemente è divenuta oggetto di rinnovato interesse l’acetilcisteina, un farmaco a lungo utilizzato come mucolitico, che possiede proprietà antiossidanti che potrebbero trovare utile impiego nella BPCO, possibilmente contribuendo a prevenire il declino strutturale e funzionale nel tempo: si attendono ulteriori e più ampie conferme sperimentali. Per quanto riguarda l’ossigenoterapia a lungo termine nel trattamento dell’insufficienza respiratoria parziale, indicazioni, precauzioni e controindicazioni sono sovrapponibili a quelle valide nella popolazione generale. Nel paziente geriatrico il regime di vita preferibilmente sedentario facilita la somministrazione: tuttavia in relazione al possibile deficit dell’attenzione e della memoria occorre che si eserciti un frequente controllo esterno sui parametri di erogazione, sull’effettiva assunzione, sul rispetto delle norme di sicurezza. Appare superfluo in una trattazione sulla gestione dell’anziano con BPCO sottolineare il ruolo fondamentale che può essere svolto dal complesso delle pratiche riabilitative: queste devono essere realizzate da personale dotato di specifica esperienza dei problemi geriatrici e deve comprendere non soltanto attività dirette all’apparato respiratorio, ma anche pratiche indirizzate ad un ripristino di adeguate capacità motorie. Il complesso di queste attività deve essere inquadrato all’interno di un articolato programma assistenziale che tenga conto delle specificità del quadro clinico, della situazione socio-familiare ed economica, nonché della condizione cognitiva ed affettiva, con particolare riferimento alla depressione. Infine, un cenno merita la pratica della ventilazione meccanica non invasiva in ospedale durante le riacutizzazioni e a domicilio nel paziente avanzato che presenti una condizione di insufficienza respiratoria globale cronicizzata. Caduti ormai i pregiudizi culturali che in altri tempi avrebbero sconsigliato una tale pratica nell’anziano, non vi sono praticamente limiti d’età all’istituzione di questo trattamento: tuttavia è opportuno ribadire che da una parte esso è condizionato all’adesione e all’adattamento continuo del paziente e pertanto non è attuabile nel caso di condizioni mentali o affettive compromesse; d’altra parte la ventilazione assistita richiede una stretta sorveglianza clinica, un controllo regolare delle caratteristiche di funzionamento della protesi ed un monitoraggio gasanalitico frequente che configurano un onere organizzativo non sempre alla portata del paziente anziano, particolarmente in una realtà disomogenea sul piano socio-assistenziale come è quella del nostro paese. BIBLIOGRAFIA - Agustì AGN, Noguera A, Sauleda J, Sala E, Pons J, Busquets X Systemic effects of chronic obstructive pulmonary disease. Eur Respir J 2003; 21: 347-360. - Antonelli Incalzi R. Comorbilità e qualità della vita nella BPCO. In: Il volto della BPCO che cambia. Vol.4. Giuntini C, Fabbri LM, Grassi V, Eds, UTET 2002; 67-78. - Antonelli Incalzi R, Bellia V. Il trattamento della BPCO in età geriatrica. In: Il volto della BPCO che cambia. Vol.5. Giuntini C, Fabbri LM, Grassi V, Eds, UTET 2002; 79-86. - Bellia V. Broncopneumopatia cronica ostruttiva ed asma nel paziente anziano. Mc Graw Hill Libri Italia, 1998; 1-178. - Bellia V, Grassi V, Rengo F, Catalano F, Cossi S, Scichilone N. Anziano e BPCO. In: Il volto della BPCO che cambia. Vol.4. Giuntini C, Fabbri LM, Grassi V, Eds, UTET 2002; 51-66. - BelliaV, Rengo F, Battaglia S. La BPCO nel contesto della geriatria. In: Il volto della BPCO che cambia. Vol.6. Giuntini C, Fabbri LM, Grassi V, Eds, UTET 2003; 96-100. - Celli BR, Cote CG, Marin JM, Casanova C, Montes De Oca M, Mendez RA, Pinto Plata V, Cabral HJ. The body-mass index, airflow obstruction, dyspnea and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med 2004; 350: 1005-1012. - Fabbri LM, Hurd SS. Global strategy for the diagnosis, management and prevention of COPD. 2003 update. Eur Respir J 2003; 22: 1-2. - Hardy C, Connolly M. Chronic air flow obstruction in elderly patients. In: Respiratory disease in the elderly patient. Chapman and Hall Medical, 1996; 81-94. - National Collaborating Center for Chronic Conditions. Chronic obstructive pulmonary disease. NICE guidelines. Thorax 2004; 59: 1-232. - Pistelli R, Bellia V, Catalano F, Antonelli Incalzi R, Scichilone N, Rengo F. The SARA Study Group. Spirometry reference values for women and men aged 65-85 living in southern Europe: the effect of health outcomes. Respiration 2003; 70(5):484-9. - Trabucchi M, Rozzini R. La valutazione multidimensionale del paziente anziano. In: Aging lung: dalla fisiologia alla clinica. grassi, Rengo F, Olivieri D Eds, Scientific Press, 1996; 17-30. - www.goldcopd.it. 151 15. Il medico di Medicina generale nella gestione della BPCO A cura di Germano Bettoncelli Medico di Medicina generale, Brescia 15. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione È opinione diffusa ed esistono diversi motivi a sostegno della necessità di un forte coinvolgimento del medico di Medicina generale (MMG) nella gestione del paziente affetto da broncopneumopatia cronica ostruttiva (BPCO). Alcuni di questi motivi hanno carattere generale, altri sono legati allo specifico della malattia (tab.1). Tabella 1 – Coinvolgimento dell’MMG nella gestione della BPCO CARATTERISTICHE DELLA BPCO CARATTERISTICHE E RUOLO DEL MMG Prevalenza elevata Cronicità della patologia Mortalità e morbilità in aumento Consumo di risorse elevato Importanza interventi preventivi Declino funzionale progressivo Esacerbazioni Prospettive di terapia farmacologica Diffusione capillare sul territorio Continuità assistenziale Rilevazione dati epidemiologici Responsabilizzazione controllo spesa Interventi di primo livello su popolazione Diagnosi tempestiva Valutazione gravità Verifica appropriato uso delle risorse nella vita reale Le previsioni di forte incremento della mortalità e della morbilità(1) che si riferiscono a questa malattia ne fanno un fenomeno preoccupante, caratterizzato da un andamento negativo del tutto peculiare, specialmente se rapportato ad altre condizioni quali le patologie cardiovascolari e quelle neoplastiche, oggi decisamente in netta controtendenza. Il pessimismo degli osservatori si fonda sui dati di incremento di prevalenza della BPCO nella popolazione e sul suo peculiare andamento clinico, caratterizzato dallo sviluppo di una progressiva riduzione della funzionalità respiratoria, che può giungere fino alla grave insufficienza respiratoria, riscontrabile nelle fasi avanzate della malattia. Per questi motivi la maggior parte dei costi indotti dalla BPCO, si concentra negli stadi più evoluti della patologia, quando le esacerbazioni si fanno più numerose e gravi ed i ricoveri ospedalieri più frequenti (2,3). Se da una lato ci troviamo di fronte ad un tale scenario piuttosto cupo, numerose evidenze ci indicano per contro che molto si potrebbe fare per impedire l’insorgenza della malattia e che, quand’anche la malattia appaia già insorta, molto ancora resterebbe da fare per frenarne la deriva verso gli stadi più gravi. Sebbene molti ritengano che la Medicina generale (MG), sotto questo punto di vista, potrebbe/dovrebbe avere un ruolo importante, fino ad oggi essa sembra aver tenuto di fatto un basso profilo nell’impegno su questo fronte. In particolare si registra una certa difficoltà e ritardo nell’adozione delle indicazioni provenienti da documenti scientifici e Linee Guida redatte da autorevoli comitati di esperti ed ampiamente diffuse (4,5,6). Per altro va osservato che la produzione di questi documenti è abbastanza vasta e la loro revisione piuttosto frequente, a testimonianza forse di una non ancora elevata stabilità delle conoscenze in materia. Si stima che circa il 50% dei soggetti portatori di BPCO non ne sia informato, ovvero non abbia mai ricevuto una corretta diagnosi medica. È ragionevole pensare che si tratti di pazienti per la maggior parte in uno stadio di malattia lieve, destinati ad essere riconosciuti solo in momenti successivi, alla comparsa di sintomi più gravi e invalidanti. Merita a tale proposito ricordare la grande capacità di assuefazione ai disturbi respiratori che spesso questi pazienti presentano e che è raro riscontrare in altre patologie. La più o meno consapevole riduzione delle proprie preformances con l’adeguamento al livello di funzionalità respiratoria possibile, rappresenta un fattore determinante per mantenere la sottostima della malattia e procrastinarne a tempo inde- 153 finito la diagnosi. Alla scarsa consapevolezza del paziente circa il significato dei sintomi di allarme, si accompagna l’atteggiamento del medico che, nella maggior parte dei casi, non va incontro al problema, ma lo aspetta secondo modi e tempi di presentazione di fatto lasciati alla decisione del paziente. Di solito, nella pratica quotidiana, accade che il paziente ricorra al medico per la presenza di un sintomo particolarmente disturbante o di una limitazione funzionale di una certa importanza: a quel punto ci si trova facilmente già in presenza di una condizione piuttosto evoluta e sensibilmente deteriorata sul piano clinico. Frequentemente l’incontro col medico avviene in concomitanza di un episodio di esacerbazione della BPCO; evento non di rado omologato ad altre condizioni più o meno banali di flogosi dell’apparato respiratorio - magari stagionali - e quindi trattato con farmaci sintomatici o antibiotici, o comunque percepito come “episodio” e non quale epifenomeno della condizione patologica cronica sottostante. Non di rado tale approccio tende ad essere reiterato, nel corso di più visite mediche, con variazioni prescrittive prevalentemente inefficaci. In realtà questo incontro tra medico e paziente, seppur con i limiti ed i ritardi descritti, potrebbe comunque ancora rappresentare un’occasione favorevole per impostare un iter in grado di mettere a fuoco la diagnosi e stadiare la gravità della patologia. Nella realtà, non sempre purtroppo questa opportunità viene colta. 154 Quali motivi si possono ipotizzare alla base di questo comportamento? Per certi versi i MMG sembrano molto affezionati alla prima definizione di Anthoniseen di bronchite cronica, quella nella quale non veniva citato il fenomeno dell’ostruzione bronchiale completamente o prevalentemente non reversibile ed in relazione alla quale poco si conosceva riguardo agli indirizzi terapeutici. A sostegno di questa affermazione vi sono le osservazioni relative al basso utilizzo della spirometria in MG (ma non solo), test ritenuto essenziale per la formulazione corretta della diagnosi. Studi non ancora pubblicati tratti da un database della MG italiana, Health Search, mostrano infatti che la spirometria è prescritta solo in circa il 30% dei casi etichettati come BPCO. Nello stesso osservatorio, per altro, la prevalenza di malattia riportata nella popolazione sembra abbastanza sottodimensionata rispetto alle stime riportate in letteratura (2,2% nei soggetti di età >40 anni). Si ha l’impressione che i MMG preferiscano in molti casi porre una diagnosi esclusivamente sulla scorta dei dati desunti dall’osservazione del paziente, cioè della sua obiettività ed ancor più della sua storia clinica, che non sulla base di una valutazione strumentale. Purtroppo non esistono ad oggi evidenze scientifiche che dimostrino se questo comportamento sia corretto. Per contro, medici esposti ad interventi educativi ben strutturati e ben condotti, migliorano sotto il profilo della qualità della diagnosi, sia nel senso del numero di casi riconosciuti sia per l’applicazione delle procedure standard raccomandate dalle principali Linee Guida. Quali strategie possono essere pertanto delineate ai fini di migliorare gli standard di cura della BPCO in Medicina generale? L’individuazione di un soggetto con caratteristiche tali da far porre al medico il sospetto di BPCO non sembrerebbe, in linea di principio, comportare grandi difficoltà. Si tratta di una persona di età >40 anni, forte fumatore o con anamnesi positiva per l’esposizione a fattori di rischio, con sintomi significativi quali tosse cronica, produzione cronica di espettorato, dispnea (tab. 2). Tabella 2 – Soggetto potenziale candidato a sviluppare BPCO >40 anni, fumatore o ex forte fumatore con spesso (ma non sempre necessariamente) Presenza di tosse cronica Espettorato cronico in genere mucoso Dispnea, all’inizio da sforzo poi anche a riposo Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 15. Il medico di Medicina generale nella gestione della BPCO - G. Bettoncelli Il primo passo è quindi che il MG disponga di un archivio pazienti in cui venga sistematicamente raccolto il dato anamnestico relativo all’abitudine tabagica ed all’esposizione ai fattori di rischio la BPCO. Sebbene il fumo di tabacco rappresenti il principale fattore di rischio per la salute nelle popolazioni dei paesi industrializzati, ancora troppo limitato è l’intervento svolto dai medici per contrastare questo fenomeno. Rilevare la presenza dell’abitudine tabagica e dimensionarla per intensità e durata, è un intervento di minimo impegno dal punto di vista del tempo e della difficoltà, quando indirizzato al singolo soggetto (7). Più complesso diventa invece il problema nell’ipotesi di un intervento esteso a tutti i fumatori (circa il 26% della popolazione totale), che preveda anche la somministrazione di test per la valutazione del grado di dipendenza dalla nicotina (test di Fagestrom) o della disponibilità alla sospensione del fumo. Si consideri, a tale proposito, che l’intervento educazionale minimo standardizzato di tre minuti (minimal advice) raccomandato dalle Linee Guida, se attuato in maniera estesa, comporta per un generalista con 1500 pazienti un impegno di 2 settimane di attività ambulatoriale (4 ore al giorno per 5 giorni/sett.), totalmente dedicate allo svolgimento di questo compito. Con questo non si intende evidentemente esprimere un giudizio sull’opportunità ne sulla praticabilità reale di tale intervento (probabilmente, per altro, esso è opportuno e, in ultima analisi, praticabile), ma solo porre in evidenza l’impegno reale richiesto, in un’ottica di popolazione, per l’attuazione di interventi di per sé molto semplici se considerati singolarmente. La sola raccolta del dato anamnestico e l’avviso minimo sono in grado di produrre la sospensione del fumo nel 2% dei fumatori; questa percentuale, all’apparenza modesta, assume un deciso rilievo se proiettata sui larghi numeri di popolazione coinvolti. La presenza di collaboratori di studio che affiancano il medico può rappresentare un’ulteriore opportunità per effettuare questi interventi in modo più capillare e sistematico e per sollevare in parte il lavoro del medico. Nell’intento di conoscere il maggior numero di pazienti a rischio di BPCO, possono essere utili cartelli esposti nella sala d’attesa che richiamano i sintomi patognomonici della malattia o brevi questionari autocompilati da riconsegnare al medico al momento della visita (tab. 3). Tabella 3 – Questionario ambulatoriale per lo screening dei soggetti con BPCO Sai cos’è la BPCO? È la broncopneumopatia cronica ostruttiva, una malattia dei polmoni molto frequente, anche se molti pazienti ne sono affetti senza saperlo. Rispondi alle domande e scopri se sei affetto da BPCO 1. 2. 3. 4. 5. Hai tosse frequente? Hai frequentemente catarro nei bronchi? Fai fatica a respirare rispetto ai tuoi coetanei? Hai più di 40 anni? Sei un fumatore o lo sei stato? SI SI SI SI SI NO NO NO NO NO Se hai risposto sì a tre o più domande potresti essere affetto da BPCO, chiedi al tuo medico se ritiene necessario che tu faccia una spirometria. Una diagnosi precoce di BPCO è fondamentale nel prevenire un aggravamento di questa malattia. La diagnosi di BPCO deve essere confermata dalla dimostrazione oggettiva della presenza di un’ostruzione bronchiale, ottenuta con l’esecuzione di una spirometria. Va ricordato che la tosse cronica e la produzione di escreato spesso precedono di molti anni la comparsa della riduzione del flusso aereo espiratorio. Ciò nonostante non tutti i soggetti con tosse e produzione di escreato svilupperanno in seguito un’ostruzione bronchiale vera e propria. Come già ricordato esiste una certa riluttanza (e non solo in MG) ad utilizzare l’esame spirometrico per diagnosticare le malattie broncostruttive. Dai dati di Health Search emerge che questo te- 155 156 st è stato richiesto in circa il 30% dei soggetti per i quali il medico ha registrato in cartella una diagnosi di BPCO. Vi sono spiegazioni di tale comportamento? Il fenomeno può probabilmente essere legato a diverse cause, tra le quali problemi logistici e di difficoltà di accesso ai servizi diagnostici, indisponibilità del paziente ad effettuare l’accertamento prescritto, carenze culturali del medico. È possibile anche, tuttavia, che molti medici pur conoscendo perfettamente il significato dell’esame spirometrico, siano convinti di poter gestire il problema BPCO basandosi esclusivamente sui dati clinico-anamnestici del paziente. Questo comportamento, tendente a prescindere dai dati di funzionalità respiraoria sembra trovare riscontro anche nella posizione recentemente assunta dalle recenti Linee Guida NICE (8). La lenta evoluzione della malattia e la scarsa pressione (in termini di domanda assistenziale) che fino ad un determinato stadio di gravità viene esercitata dal paziente sul medico, possono favorire questo particolare tipo di valutazione. La conseguenza dello scarso ricorso allo studio funzionale del paziente, si traduce nella pressochè inesistente consuetudine ad effettuare la stadiazione di gravità della malattia. Non stadiare la BPCO o farlo secondo modelli personali del medico, impedisce di attuare una gestione della malattia standardizzata e coerente. Tale comportamento ha potenziali, pesanti, conseguenze sotto molti punti di vista: da quello delle scelte terapeutiche, a quello della corretta comunicazione con gli altri medici ed operatori sanitari. Per il medico generale, che di solito non dispone di strumenti di misura della funzione respiratoria, è utile conoscere la correlazione esistente fra il grado di riduzione del flusso aereo espiratorio e la presenza ed entità dei sintomi. La classificazione in stadi è pertanto utile non solo per inquadrare il livello di gravità del paziente, ma anche per fornire un’indicazione obiettiva alla programmazione del trattamento. Naturalmente la necessaria valutazione globale del paziente, deve prendere in considerazione anche altri parametri, tra i quali: gravità dei sintomi, frequenza e gravità delle riacutizzazioni, presenza di complicanze della malattia, presenza di insufficienza respiratoria, co-morbidità, stato di salute generale, numero di farmaci richiesti per controllare la malattia. In assenza di un dato spirometrico, è utile ricordare che una valutazione approssimativa del grado di dispnea riferito dal paziente, può essere effettuato con l’uso della scala MRC (Medical Research Council). Anche questo semplice strumento valutativo è pressochè sconosciuto in Medicina generale. Classificazione MRC della dispnea - Dispnea solo durante sforzi intensi; - dispnea se cammina in fretta in piano, o in lieve pendenza, o su una rampa di scale, a passo normale; - dispnea se cammina con coetanei a passo normale in piano; - deve fermarsi a riprendere fiato se cammina a passo normale in piano; - dispnea forte per uscire di casa o per vestirsi e svestirsi. L’adozione dello schema di classificazione in 4 stadi di gravità progressiva, proposto dalle Linee Guida GOLD, farebbe compiere alla Medicina generale un salto qualitativo importante nella gestione della malattia. Per altro, vi sono state recenti pubblicazioni secondo le quali, in realtà, il riferimento per la valutazione del paziente sembra essere nella pratica più che lo scadimento dei valori di funzionalità respiratoria, la percezione soggettiva dello stato di salute del paziente stesso, valutata con gli appositi questionari per la misura della qualità di vita, valutazione in buona misura correlata con il numero di esacerbazioni registrate (9). Recenti importanti studi per la valutazione di efficacia di farmaci quali β2 long-acting/steroidi e tiotropio, hanno utilizzato infatti proprio outcomes di questo tiRapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 15. Il medico di Medicina generale nella gestione della BPCO - G. Bettoncelli po (10,11,12). Si discute molto, non solo nel nostro Paese, attorno alla possibilità/opportunità che il medico generale di esegua l’esame spirometrico nell’ambito della sua normale routine ambulatoriale. L’ostacolo maggiore all’introduzione di questa attività è rappresentato dall’impatto dei tempi richiesti per effettuare tali accertamenti su una popolazione numerosa come quella potenzialmente interessata, a fronte di tutte le altre attività che normalmente il medico generale deve gestire. Anche qui, modelli organizzativi innovativi potrebbero fornire soluzioni adatte. Un’ipotesi potrebbe vedere gruppi di medici organizzati che condividono metodi, sede e strumenti di lavoro (medicina di gruppo), ad esempio 7-8 medici con 10.000 assistiti, la cui organizzazione potrebbe consentire la collaborazione con tecnici esperti (fisioterapisti) operanti all’interno delle strutture della medicina di gruppo, secondo un calendario di interventi periodici, in grado di soddisfare la domanda di quella data popolazione. Ad una prima selezione potrebbe far seguito l’invio di quei pazienti che presentano problemi particolari a centri di secondo livello, per determinazioni più selettive ed accurate. Sono inoltre in corso anche esperienze di telemedicina che suscitano interesse e che potrebbero dare un contributo allo sviluppo di queste problematiche. L’approccio terapeutico farmacologico al paziente con BPCO ha avuto negli ultimi anni il supporto di evidenze scientifiche che hanno mostrato come sia possibile intervenire per tentare di frenare il decorso della malattia e migliorare la qualità di vita del paziente. Le numerose Linee Guida esistenti ed in particolare le GOLD, assegnano ad ogni stadio di gravità un approccio terapeutico preciso. La stadiazione della malattia diviene dunque un requisito necessario per impostare una terapia farmacologica appropriata. In un’epoca nella quale tutti, compresi i MMG, sono richiamati al maggior controllo della spesa, il perseguire una prescrizione appropriata rappresenta, oltre che l’interesse del paziente, anche un’arma di tutela per il medico a difesa della propria responsabilità in campo economico. Ovviamente la prescrizione farmacologica va inserita all’interno di un piano gestionale complessivo del paziente che preveda anche un preciso follow up, interventi educazionali, integrazione con le diverse figure sanitarie di volta in volta necessarie. Questo modo di procedere può favorire il miglioramento qualitativo delle cure offerte nel setting della medicina di famiglia al paziente con BPCO, compatibilmente con le risorse esistenti. Palesemente questi concetti sottendono le linee di indirizzo volte ad orientare il modello di gestione verso i principi della clinical governance. Un obiettivo ambizioso, certo, ma oggi probabilmente senza alternative. BIBLIOGRAFIA 1. Murray CJ et al. Lancet 1997; 349: 1498-1504. 2. Dal Negro R et al. Respir Med 2003;97(Suppl.C):S43-S50. 3. Dati Min.Sal. SDO 2001. 4. Global Strategy for the Diagnosis, Management and Prevention of COPD: 2003 update L.M. Fabbri, S.S. Hurd, for the GOLD Scientific Committee Eur Respir J 2003; 22: 1–2. 5. Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS; GOLD Scientific Committee. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med. 2001 Apr;163(5):1256-76. 6. British Thoracic Society Guidelines for the management of chronic obstructive pulmonary disease. Thorax 1997; 53(suppl 5):s1-26. 7. Invernizzi G, Nardini S, Bettoncelli G, et al. L’intervento del medico di Medicina generale nel controllo del fumo: raccomandazioni per un approccio ottimale al paziente fumatore. Rassegna di patologia dell’apparato respiratorio 2002; 17: 55-70. 8. National Collaborating Centre for Chronic Conditions. Chronic obstructive pulmonary disease. National clinical guideline on management of chronic obstructive pulmonary disease in adults in primary and secondary care. Thorax 2004;59(suppl 1): 1-232. 9. Haughney J, Gruffydd-Jones K. Patient-centred outcomes in primary care management of COPD – wath do recent clinical trial data tell us? Primary Care Resp J 2004; 13(4): 185-97. 10. Calverley PM, Pauwels R, et al. Eur Respir J 2003; 22: 912-9. 11. Szafransky W, Cukier A, et al. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. E 21(1): 74-81. 12. Brusasco V, Hodder R, et al. Health outcomes following treatment for 6 months with once daily tiotropium compared with twice daily salmeterol in patients with COPD. Thorax 2003; 58(5): 399-404. 157 16. Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità A cura di Mauro Carone Divisione di Pneumologia. Fondazione Salvatore Maugeri, IRCCS. Istituto Scientifico di Veruno (NO) 16. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 Introduzione Negli ultimi anni si è verificato un crescente interesse per la “qualità di vita” (QdV). Lo scopo che si prefigge questo metodo di valutazione è quello di fornire una accurata valutazione dei benefici che i pazienti possono trarre dalle cure mediche. Purtroppo il termine QdV non è ben definito, tanto che spesso sono utilizzati indifferentemente altri termini quali “qualità di vita correlata alla salute” e “stato di salute”. L’approccio più semplice per definire la “qualità di vita” è quello di vederla come la distanza tra ciò che è desiderato e ciò che è invece raggiungibile. Tuttavia, ciascuno di noi ha desideri non appagati, specialmente quando è presente una malattia cronica come la BPCO. Allora in contesto medico è subentrato il termine di “qualità di vita correlata alla salute”, utilizzato per esprimere la distanza tra ciò che è desiderato e ciò che è possibile ottenere a causa del nostro limitato stato di salute. Ciò nonostante, anche quest’ultima definizione è troppo generica perché abbia un’applicazione pratica, giacché i desideri di un paziente possono essere diversi da quelli di un altro. Per esempio un paziente tracheostomizzato potrebbe essere aver avuto come principale passione della propria vita l’immersione subacquea. Ovviamente la tracheostomia influenzerà pesantemente questo aspetto della vita di quel paziente, ma tale limitazione sarà pressoché unica di quel singolo paziente, o al massimo sarà una delle componenti di pochi pazienti. Si è dunque cercato di superare queste limitazioni mediante una definizione più pratica, quella che vede la qualità di vita come la “quantificazione dell’impatto della malattia sulla vita di tutti i giorni e sul benessere in un modo formale e standardizzato” (1). Questa definizione sottolinea l’importanza di avere questionari “standardizzati”. In tal senso, i questionari di stato di salute comprendono un gruppo di domande, dette items, appropriate e applicabili a tutti i pazienti con quella determinata patologia, che esplorano le aree di compromissione della salute comuni a tutti quei pazienti. Di conseguenza si può dire che un questionario di stato di salute rappresenta il minimo comun denominatore di una determinata malattia. Ciò permette di includere le misure della salute nel gruppo di tutte le altre misurazioni, come la spirometria, per le quali i parametri di normalità sono comunemente utilizzati. QdV e broncopneumopatia cronica ostruttiva La broncopneumopatia cronica ostruttiva (BPCO) è una patologia essenzialmente “inguaribile”. Infatti l’unico approccio in grado di influenzare la storia naturale della malattia è la sospensione dell’abitudine tabagica. Al contrario, le terapie sono quasi dei “palliativi” sintomatologici, e sono principalmente rivolte alla prevenzione delle riacutizzazioni e alla riduzione della gravità dei sintomi. In tal modo si cerca di migliorare lo stato di salute globale del paziente, o quanto meno di evitarne il peggioramento. La BPCO ha anche la caratteristica negativa di essere inesorabilmente progressiva. Quando il FEV1 scende sotto il litro, vi è un rapido aumento dell’impatto della malattia sulla vita quotidiana del paziente e sul suo benessere (2), con una riduzione delle normali attività della vita quotidiana (3) tanto che a questo livello i pazienti sono e si sentono handicappati. In queste circostanze, l’effetto della terapia sul benessere del paziente e sulla vita quotidiana rappresenta il più importante risultato soggettivo del trattamento. Tuttavia, tutte le misurazioni comunemente utilizzate come indice di danno funzionale correlano scarsamente con la QdV e perciò forniscono un quadro incompleto dello stato di salute (4). 159 La figura 1 mostra una tipica relazione tra il volume espiratorio forzato in 1 secondo (FEV1) e lo stato di salute come misurato dal St. George’s Respiratory Questionnaire (SGRQ) (5): l’ampia dispersione attorno alla linea di regressione non permette al FEV1 di predire adeguatamente lo stato di salute dell’individuo. Infatti, se consideriamo due pazienti chiamati A e B, possiamo notare che il FEV1 è al limite inferiore della normalità in entrambi. Tuttavia, il paziente A non presenta compromissione del proprio stato di salute, mentre il paziente B mostra un marcato effetto della malattia sulla sua salute. Figura 1 – Correlazione tra FEV1% e punteggi del SGRQ in un gruppo di pazienti respiratori [Modificato da 1] 90 80 paziente B 70 SGRQ 60 50 40 30 20 10 160 paziente A FEV1 % 0 0 20 40 60 80 100 120 140 Tutto ciò è legato alla complessità dei fattori in grado di determinare alterazioni dello stato di salute nei pazienti con BPCO (fig. 2). Due aspetti di questa figura devono essere sottolineati. Innanzitutto la possibilità che si creino dei circoli viziosi, ad esempio l’atrofia da disuso dei muscoli delle gambe causato dalla limitazione all’esercizio conseguente alla dispnea. Il secondo aspetto importante è che anche le alterazioni dello stato dell’umore del paziente, essenzialmente ansia e depressione, possono influenzare direttamente la capacità ad eseguire esercizio, il livello di dispnea e lo stato di salute globale. Questo fenomeno è importante perché molti pazienti con BPCO presentano come conseguenza della cronicità dei sintomi una risposta reattiva di ansia o depressione. Figura 2 – Fattori in grado di determinare alterazioni dello stato di salute nei pazienti affetti da BPCO Perdita di massa muscolare Malattia respiratoria Dispnea Limitazione al flusso Iperinflazione Alterazioni Va/Q Limitazione all’esercizio Alterazioni dell’umore Fatica Alterazione dello stato di salute Tosse Riacutizzazioni Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 16. Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità - M. Carone È chiaro, dalla precedente, che una stima globale della salute del paziente non può essere dedotta da altre misure. Una adeguata valutazione della qualità di vita può essere ottenuta solo dal paziente stesso, attraverso l’utilizzo di questionari validi e affidabili (1). Gli strumenti sviluppati negli ultimi 30 anni per quantificare l’impatto della malattia sulla vita quotidiana e sullo stato di benessere consistono essenzialmente in una serie di domande o affermazioni (items) che vengono autosomministrate da parte del paziente stesso oppure raccolte da un intervistatore direttamente o per via telefonica. Le risposte possono essere dicotomiche (es. il paziente sceglie fra vero e falso), oppure prevedono più risposte (generalmente 3-5 intervalli, per es. moltissimo, molto, indifferente, poco, pochissimo) in scale dette tipo Likert. Un’ultima possibilità è che la risposta venga espressa su scala analogico-visiva (VAS) (per es. una linea di 10 cm che alle estremità presenta due valori pari all’intensità minima ed a quella massima). Il modo più semplice per valutare lo stato di salute dei pazienti è quello di porre al paziente una singola ed unica domanda globale, del tipo Come valuta la propria qualità di vita? Tuttavia questo tipo di questionario, detto “olistico”, non valuta in modo appropriato lo stato di salute, poiché sottostima l’impatto della malattia polmonare sulla percezione di salute del paziente. Ciò che accade è un fenomeno di adattamento chiamato “response shift”: i pazienti modificano la loro stima di ciò che è la salute normale perché si abituano ai sintomi causati dalla loro malattia. Questo fenomeno non si verifica con questionari più complessi che, al contrario, forniscono una stima globale, affidabile e sensibile della salute. I questionari più complessi prevedono numerosi items. Le risposte ai singoli items o i pesi dati ai singoli items vengono sommate permettendo di fornire dei punteggi di QdV che possono essere totali (su tutti gli items) o parziali di alcune sottoscale (es. attività fisica, stato emozionale, sintomi, ecc.). Sostanzialmente i gruppi di questionari che sono utilizzabili nella valutazione della QdV sono due, quelli generici e quelli specifici per patologia. Un questionario, sia esso generico o specifico per una data patologia, deve possedere alcune proprietà (7,8) per essere definito standardizzato: - stesse domande; - stesso formato; - stesse istruzioni; - stessa scelta di risposta; - stesso sistema di calcolo dei punteggi. Questionari generici sulla salute I questionari generici sono state le prime misure della salute utilizzate nelle patologie respiratorie. Esprimono una misura dei disturbi della salute senza tenere conto delle cause. Questi questionari presentano il vantaggio che la loro riproducibilità e validità è stata verificata in differenti patologie, che lo stesso questionario può essere presentato a ciascun paziente e che la procedura per il calcolo dei punteggi è sempre la stessa. Tuttavia, essi non sono stati appositamente studiati per pazienti BPCO o asmatici risultando perciò non adeguatamente sensibili a variazioni clinicamente significative della salute conseguenti al trattamento (tab.1). Tra questi ricordiamo il Il Sickness Impact Profile (SIP) (9), di cui esiste una versione Italiana (10); la short form del Medical Outcome Study - MOS o SF-36 (11-14); il Nottingham Health Profile (NHP) (15,16); la Quality of Well-being scale (QWB) (17); l’Euroqol (18-19). 161 Tabella 1 – Questionari generici di qualità di vita utilizzabili in pazienti affetti da patologie delle vie aeree Questionario Items (n) Componenti (n) Tempo di completamento/ somministrazione Sickness Impact Profile (SIP) 136 12 componenti (interazione sociale; deambulazione; mobilità; cura del corpo; sonno e riposo; alimentazione; lavoro; vita familiare; comunicazione; tempo libero; emozioni; affetti) 20-30 min/auto-somministrabile o intervista Medical Outcome Study, short form 36 items (SF36) 36 8 componenti (attività fisica; limitazione di ruolo dovuta a problemi fisici; dolore; percezione di salute generale; vitalità; attività sociale; limitazione di ruolo dovuta a stato emotivo; salute mentale) 5-10 min auto-somministrabile Quality of Well-being (QWB) 50 3 componenti (mobilità; attività fisica; attività sociale) 10-15 min/intervista Nottingham Health Profile (NHP) 38 6 componenti (energia; dolore; mobilità fisica; sonno; isolamento sociale; reazione emotiva) 5-10 min/auto-somministrabile Euroqol (5D) 5 mobilità, self-care, attività usuali, dolore/disagio, ansia/depressione 5-10 min Questionari specifici per patologia 162 I questionari generici sono utilizzabili in più patologie. Questo però riduce il numero di item che sono adeguati per una singola patologia, aumentando di conseguenza il numero di quelli non adeguati o non completamente pertinenti con quella patologia stessa. Per tale motivo i questionari generici possono risultare poco sensibili a variazioni di QdV nelle malattie respiratorie. Per poter misurare adeguatamente differenze in QdV tra gruppi di pazienti o per valutare correttamente le variazioni determinate da trattamenti farmacologici o da cicli di riabilitazione respiratoria sono state sviluppate misure di stato di salute specifiche per i pazienti BPCO. Il primo questionario sviluppato specificatamente per la BPCO è stato il Chronic Respiratory Questionnaire (CRQ) (20). Il CRQ misura la funzione fisica e quella emotiva suddivise in quattro dimensioni: Dispnea, Fatica, Funzione emotiva, Mastery o senso di controllo sulla malattia. Il questionario necessita di circa 20 minuti per essere completato. I pazienti rispondono a ciascun item tramite una scala tipo Likert a sette punti dove il punteggio più alto indica un miglior stato di salute. Il CRQ ha mostrato di essere affidabile, cioè di saper differenziare tra differenti livelli di salute in differenti pazienti, e di essere sensibile alle variazioni della salute correlate alla terapia (21). Il St. George’s Respiratory Questionnaire (SGRQ) (5) è attualmente il più diffuso questionario di stato di salute utilizzato nella BPCO. È stato creato con lo scopo di avere una misura sensibile da utilizzare nelle patologie respiratorie, sia asma sia BPCO. Il SGRQ è composto da 50 items (con 72 possibili risposte pesate) suddivisi in 3 sezioni: Sintomi, ovvero i sintomi clinici; Attività, che riguarda le attività che causano o che sono limitate dalla dispnea; Impatto, una misura delle conseguenze soggettive determinate dalla malattia respiratoria sulla vita quotidiana e sullo stato di benessere. Ciascuna componente ha un punteggio. È inoltre possibile calcolare un punteggio totale: i punteggi variano da 0% (il miglior livello di salute) a 100% (il peggior livello di salute). Una variazione del punteggio nel tempo di almeno 4 punti è considerata clinicamente significativa (22). Il SGRQ è auto-somministrabile o somministrabile tramite intervista telefonica e necessita di circa 15 minuti per essere completato. È disponibile in tutta Europa, Italia compresa (23), nel Nord e Sud America, in alcuni Paesi dell’Est Europeo e del lontano Oriente. Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 16. Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità - M. Carone Il Maugeri Foundation Respiratory Failure Questionnaire (MRF-28) (24-26) è composto da 28 items, ed è specifico per pazienti con insufficienza respiratoria cronica (CRF), Le 28 domande possono essere raggruppate in tre fattori: Attività quotidiana, associata alle attività che sono limitate dai sintomi; Funzione cognitiva, che si correla agli effetti della compromessa funzione cognitiva sulla vita quotidiana; e Invalidità, che è correlata all’inabilità del paziente a fare sforzi, all’esperienza dell’isolamento sociale o della dipendenza da altri (tab. 2). Tabella 2 – Questionari di qualità di vita specifici per patologia utilizzabili in pazienti affetti da patologie delle vie aeree. Questionario Chronic Respiratory Questionnaire (CRQ) St George’s Respiratory Questionnaire (SGRQ) Maugeri Foundation Respiratory Failure Questionnaire (MRF28) Items (n) Componenti (n) Tempo di completamento/ somministrazione 20 4 (dispnea; funzione emotiva; mastery o senso di controllo sulla malattia; fatica) 15-25 min (la prima volta); 10-15 min (le successive) intervista/solo per BPCO 50 (76 risposte pesate) 3 (sintomi; attività; impatto) 10-15 min auto-somministrabile/ sia per asma che BPCO 28 3 (attività quotidiana; funzione cognitiva; invalidità) 5-10 min/ auto-somministrabile/ per BPCO e cifoscoliosi con insufficienza respiratoria cronica In quale ambito utilizzare i questionari di QdV? I fattori della malattia che contribuiscono ad uno stato di salute alterato dei pazienti con la BPCO sono stati estensivamente studiati. Ridotta tolleranza allo sforzo, intensità dei sintomi giornalieri, ed elevato numero di riacutizzazioni contribuiscono significativamente al peggioramento dello stato di salute (27). I fattori emozionali (l’ansia e la depressione) sono altrettanto importanti. Nella valutazione dello stato di salute e dell’impatto dei vari interventi terapeutici è molto importante conoscere la soglia clinicamente significativa o la differenza minima clinicamente significativa. Questi due concetti riflettono il giudizio dei medici e dei pazienti e hanno più importanza nel campo pratico che quello della variazione statisticamente significativa (28,29). Gli studi attuali hanno dimostrato che una differenza di 4 unità per il SGRQ (28) e di 0.5 unità per il CRQ (30) può essere considerata differenza minima significativa dal punto di vista clinico. Riabilitazione La misurazione dello stato di salute globale del paziente, o QdV, sta progressivamente crescendo di interesse tra i medici, in particolare nel campo della riabilitazione. La riabilitazione polmonare rappresenta, infatti, l’ambito appropriato per la misurazione dello stato di salute, giacché queste misure permettono una stima dell’impatto generale del trattamento (31,32). In particolare, in uno studio su 182 pazienti BPCO in trattamento riabilitativo per 6 settimane (32), al termine il miglioramento dei punteggi del SGRQ era sia statisticamente sia clinicamente significativo (fig. 3). Il dato interessante è che tale miglioramento si manteneva anche a distanza di un anno dal termine del programma di riabilitazione. 163 Figura 3 – Efficacia di un ciclo di riabilitazione respiratoria in termini di miglioramento dello Stato di Salute [Modificato da 32] Dopo 6 settimane Dopo 1 anno Variazione del punteggio del SGRQ 0 -1 -2 -3 -5 -6 -7 p<0,01 -8 -9 -10 -11 -12 164 Soglia di significatività clinica -4 p<0,0001 Trattamento farmacologico Altro ambito di applicazione dei questionari di QdV è la terapia farmacologica. Uno dei primi studi condotti sul trattamento della BPCO ha riguardato il salmererolo (33). Lo studio era effettuato in doppio-cieco, randomizzato, per gruppi paralleli e contro placebo. I pazienti randomizzati ricevevano salmeterolo 50 mcg due volte al giorno, salmeterolo 100 mcg due volte al giorno o placebo. Nonostante il fatto che non c’erano differenze tra i due trattamenti attivi in termini di utilizzo di broncodilatatori addizionali o di stime medico/paziente sull’efficacia del trattamento, il SGRQ ha dimostrato miglioramenti dello stato di salute solo nei pazienti che avevano ricevuto salmeterolo 50 mcg due volte al giorno. Al contrario, il risultato ottenuto con una dose maggiore di salmeterolo era simile a quello del placebo, e vi sono prove dai dati dell’SF-36 che questo era probabilmente imputabile a qualche effetto collaterale del salmeterolo 100 mcg due volte al giorno, come la stimolazione del sistema nervoso centrale. Più recentemente è stato valutato l’impatto della terapia con un nuovo anticolinergico a lunga durata di azione, il tiotropio: i risultati hanno dimostrato che dopo un anno di terapia si evidenziava un miglioramento dei parametri fisiologici (FEV1%), nonché una diminuzione della dispnea, una riduzione del numero delle riacutizzazioni e del tempo fino alla successiva riacutizzazione, nonché un miglioramento dello stato di salute misurato con il SGRQ (34,35). Il tiotropio si è dimostrato più efficace dell’ipratropio e del salmeterolo nel ridurre la dispnea e migliorare lo stato di salute (36). Programmi educazionali Nell’asma bronchiale l’efficacia dei programmi educazionali è ormai definita da parecchi anni. Al contrario, la reale efficacia di tali programmi nella BPCO non è ancora stata indagata completamente, sebbene, dal punto di vista clinico, anche le più recenti Linee Guida le indicano come un elemento fondamentale di qualunque strategia terapeutica (37). Quello che manca è la dimostrazione scientifica che i programmi educazionali nella BPCO siano in grado di migliorare lo stato di salute dei pazienti. Allo stato attuale l’unico dato presente in letteratura riguarda un lavoro multicentrico italiano (38) effettuato su circa 1200 pazienti. Questi soggetti sono stati randomizzati ad entrare o meno un programma educazionale ben strutturato. Il dato più interessante risultato al termine dei 6 mesi di osservazione è stato il miglioramento dello stato di salute e la riduzione delle riacutizzazioni bronchiali nel gruppo con programma educazionale (39). Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 16. Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità - M. Carone Come scegliere un questionario di QdV? Non esiste il questionario ideale. Esiste il questionario più appropriato per lo scopo che ci prefiggiamo. Di conseguenza, bisogna prima conoscere o informarsi sulle caratteristiche degli strumenti disponibili. Vi sono diverse caratteristiche da prendere in considerazione. Una volta verificato che lo strumento che ci proponiamo di utilizzare sia stato validato, bisogna solo accertarsi che la validazione sia stata anche trans-culturale, cioè che il questionario sia stato adattato in modo corretto alla realtà Italiana. La scelta fra questionari generici e questionari specifici è legata allo scopo della misurazione della QdV. In generale, se si vogliono paragonare patologie differenti fra loro o se lo scopo è di valutare lo stato di salute generale di una popolazione, magari confrontandolo con quello dei soggetti “sani”, allora può essere sufficiente un questionario generico. Al contrario, se lo scopo principale è quello di valutare come lo stato di salute sia alterato da una patologia specifica o se una particolare terapia o trattamento è in grado di modificare la QdV, allora sarà necessario utilizzare strumenti specifici. BPCO e comorbidità Quello delle comorbidità è un capitolo strettamente legato alla qualità di vita. La BPCO rappresenta infatti un “problema” a lungo termine. Di conseguenza i pazienti possono acquisire altre condizioni patologiche durante la propria vita. Queste, a loro volta, possono essere esacerbate dalla BPCO o dai suoi trattamenti, oppure possono a loro volta causare sintomi che peggiorano la disabilità della BPCO. Allorquando ad una patologia cronica quale la BPCO si associa un’altra patologia cronica (ad es. cardiopatia ischemica, diabete, sleep apnea, depressione, artropatie, osteoporosi) l’effetto “invalidante” delle singole malattie si potenzia vicendevolmente. Ad esempio, la disfunzione ventricolare sinistra è abbastanza comune e può determinare peggioramento della dispnea. Altre patologie cardiache (coronaropatie, ipertensione essenziale) possono coesistere con la BPCO e un ventricolo destro dilatato può interessare la funzione diastolica ventricolare sinistra. Anche le patologie respiratorie durante il sonno possono rappresentare un aggravamento del problema, specialmente durante il sonno non-rem. Di conseguenza studi polisonnografici notturni sono indicati in tutti quei pazienti con sospetto di apnee notturne o quando i livelli diurni di ipossiemia non sono in relazione al danno funzionale respiratorio. Questo è tanto vero se si pensa che anche le Linee Guida GOLD sulla BPCO (35) includono le comorbidità tra i fattori determinanti la gravità della BPCO, insieme a gravità dei sintomi, gravità della riduzione del flusso aereo respiratorio, frequenza e gravità delle riacutizzazioni, presenza di complicanze della malattia, presenza di insufficienza respiratoria, stato di salute generale e quantità di farmaci richiesti per controllare la malattia. È interessante notare come i due argomenti trattati in questo capitolo (stato di salute - QdV - e comorbidità) vengano entrambi inclusi tra questi fattori. Una delle conseguenze della comorbidità è l’aumento della degenza ospedaliera nei pazienti che presentano più di 3 patologie concomitanti alla BPCO (40). Tra le varie patologie concomitanti, quelle che aumentano di più la mortalità dei pazienti BPCO sono l’insufficienza renale cronica e l’ipertrofia o il sovraccarico ventricolare destro (41). 165 Conclusioni I pazienti affetti da BPCO rappresentano una popolazione di soggetti progressivamente più anziani e compromessi. Negli stadi più avanzati di malattia, infatti, la BPCO si accompagna molto spesso ad altre patologie che rendono lo stato di salute dei pazienti sempre più compromesso. È allora importante misurare la QdV dei pazienti BPCO. È però noto che non è possibile predire lo stato di salute da misurazioni fisiopatologiche quali la spirometria o la capacità di esecuzione dell’esercizio. Parimenti, al termine di trattamenti farmacologici o di programmi di riabilitazione non è possibile prevedere il livello di miglioramento della QdV a partire dalle variazioni delle misure fisiologiche. L’effetto delle terapie e della riabilitazione sul benessere e sulla vita quotidiana del paziente rappresenta il risultato soggettivo più importante del trattamento. Perciò, un’adeguata valutazione dello stato di salute può solo essere effettuata direttamente tramite questionari appropriati. In contesto pratico, lo stato di salute deve rappresentare un test complementare alla spirometria ed agli altri test fisiologici, in quanto riflette la percezione della malattia di ogni paziente. Ne consegue che la misura dello stato di salute può diventare una misura di outcome utilizzata di routine per valutare l’effetto dei vari interventi terapeutici. 166 BIBLIOGRAFIA 1. Jones PW, Quirk FH, Baveystock CM. Why quality of life should be used in the treatment of patients with respiratory illness. Monaldi Arch Chest Dis 1994;49(1):79-82. 2. Jones PW, Baveystock CM, Littlejohns P. Relationships between general health measured with the Sickness Impact Profile and respiratory symptoms, physiological measures and mood in patients with chronic airflow limitation. Am Rev Respir Dis 1989;140:1538-1543. 3. Jones PW. Quality of life measurement for patients with diseases of the airways. Thorax 1991;46:676-682. 4. Williams SJ. Chronic respiratory illness and disability; a critical review of the psychosocial literature. Soc Sci Med 1989;28:791-803. 5. Jones PW, Quirk FH, Baveystock CM, Littlejohns P. A self-complete measure for chronic airflow limitation - the St George’s Respiratory Questionnaire. Am Rev Respir Dis 1992;145:1321-1327. 6. Carone M, Jones PW. Health Status. In: C.F. Donner & M. Decramer (Eds). Pulmonary Rehabilitation. Eur Respir Mon 2000; 13:22-35. 7. Jones P. Measurement of health in asthma and chronic obstructive airways disease. Pharm Med 1992;6:13-22. 8. Guyatt G. Measuring health status in chronic airflow limitation. Eur Respir J 1988;1:560-564. 9. Bergner M, Bobbit RA, Carter WB, Gilson BS. The Sickness Impact Profile:development and final revision of a health status measure. Med Care 1981;19:787-805. 10. Bertolotti G, Vidotto G, Carone M, Sommaruga M, Zotti AM, & Baiardi P. (1999) Il Sickness Impact Profile: traduzione e adattamento Italiano. Psicoterapia Cognitiva e Comportamentale 1999; 2: 109-121. 11. Stewart AL, Hays RD, Ware JE. The MOS Short Form General Health Survey:reliability and validity in a patient population. Med Care 1988;26:724.-732. 12. Mahler DA, Mackowiak JI. Evaluation of the short-form 36-item questionnaire to measure health-related quality of life in patients with COPD. Chest 1995;107:1585-1589. 13. Jones PW, Bosh TK. Quality of life changes in COPD patients treated with salmeterol. Am J Respir Crit Care Med 1997;155:1283-1289. 14. Aaronson NK, Acquadro C, Alonso J. International Quality of Life Assessment (IQDVA) Project. Quality of Life Research 1992; 1:349-351. 15. Crockett AJ, Cranston JM, Moss JR, Alpers JH. The MOS SF-36 health survey questionnaire in severe chronic airflow limitation:comparison with the Nottingham Health Profile. Qual Life Res 1996;5:330-338. 16. Tsukino M, Nishimura K, Ikeda A, Koyama H, Mishima M, Izumi T. Physiologic factors that determine the health-related quality of life in patients with COPD. Chest 1996;110:896-903. 17. Kaplan RM, Atkins CJ, Timms R. Validity of a quality of well-being scale as an outcome measure in chronic obstructive pulmonary disease. J Chron Dis 1984;37(2):85-95. 18. The Euroqol group. Euroqol - a facility for the measurement of health-related quality of life. Health Policy 1990; 16.199-208. 19. Stavem K. Reliability, validity and responsiveness of two multiatribute utility measures in patients with chronic obstructive pulmonary disease. Quality of Life Research 1999; 8: 45-54. 20. Guyatt GH, Berman LB, Townsend M, Pugsley SO, Chambers LW. A measure of quality of life for clinical trials in chronic lung disease. Thorax 1987;42:773-778. 21. Wijkstra PJ, TenVergert EM, van Altena R, Otten V, Postma DS, Kraan J, Koeter GH. Reliability and validity of the chronic respiratory questionnaire (CRQ). Thorax 1994;49:465-467. 22. Jones PW, Quirk FH, Baveystock CM. The St George’s Respiratory Questionnaire. Resp Med 1991;85(Suppl. B):25-31. 23. Carone M, Bertolotti G, Anchisi F, Spagnolatti L, Zotti AM, Jones PW, Donner CF. Il St. George’s Respiratory Questionnaire (SGRQ): la versione italiana. Rass Pat App Respir 1999; 14: 31-37. 24. Carone M, Bertolotti G, Zotti AM, Donner CF, Jones PW. Development process of a new quality of life questionnaire suitable for patients Rapporto sulla Broncopneumopatia Cronica Ostruttiva (BPCO) 2005 16. Qualità di vita. Misurazione dello stato di salute respiratoria e comorbidità - M. Carone with chronic respiratory failure. Eur Respir J 1996;9(Suppl. 23):143s. 25. Carone M, Bertolotti G, Anchisi F, Zotti AM, Donner CF, Jones PW. Analysis of factors that characterise health impairment in patients with chronic respiratory failure. Eur Respir J 1999; 13:1293-300. 26. Carone M, et al on behalf of the QuESS Group. Quality of Life Evaluation and Survival Study: a 3-yr prospective multinational study on patients with chronic respiratory failure. Monaldi Arch Chest Dis 2001; 56:17-22. 27. Keetalars CA, Schlosser MA, Moster R et al. Determinants of health related quality of life in patients with chronic obstructive pulmonary disease. Thorax 1996;51:39-43. 28. Jones PW. Interpreting thresholds for clinically significant change in health status in asthma and COPD. Eur Respir J 2002; 19: 398-404. 29. Hajiro T, Nishimura K. Minimal clinically significant difference in health status: the thorny path of health status measures. Eur Respir J 2002; 19: 390-391. 30. Jaeschke R, Singer J, Guyatt GH. Measurement of health status. Ascertaining the minimal clinically importnat difference. Controlled Clin Trials 1989; 10: 407-415. 31. Lacasse Y, Wong E, Guyatt GH, et al. Meta-analysis ofrespiratory rehabilitation in chronic obstructive pulmonary disease. Lancet 1996;348:1115-9. 32. Griffiths TL, Burr ML, Campbell IA, Lewis-Jenkins V, Mullins J, Shiels K, Turner-Lawlor PJ, Payne N, Newcombe RG, Ionescu AA, Thomas J, Tunbridge J, Lonescu AA. Results at 1 year of outpatient multidisciplinary pulmonary rehabilitation: a randomised controlled trial. Lancet 2000 Jan 29;355(9201):362-8. 33. Jones PW, Bosh TK. Quality of life changes in COPD patients treated with salmeterol. Am J Respir Crit Care Med 1997;155:1283-1289. 34. Casaburi R, Mahler DA, Jones PW, Wanner PW, San Pedro G, ZuWallack RL, et al. A long-term evaluation of once-daily tiotropium in chronic obstructive pulmonary disease. Eur Respir J 2002; 19: 217-224. 35. GOLD. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO workshop report: National Heart, Lung, and Blood Institute, 2001. 36. Vincken W, van Noord JA, Greefhorst APM, Bantje TA, Kesten S, Korducki L, on behalf of Dutch/Belgian Tiotropium Study Group. Improved health outcomes in patients with COPD during 1 year treatment with tiotropium. Eur Respir J 2002; 19: 209-216. 37. Hvizdos KM, Goa KL. Tiotropium bromide. Drugs 2002; 62: 1195-1203. 38. Carone M, Bertolotti G, Cerveri I, et al. EDU-CARE, a randomised, multicentre, parallel group study on education and quality of life in COPD. Monaldi Arch Chest Dis 2002; 57(1):25-29. 39. Carone M, Bertolotti G, Cerveri I, et al. Edu-Care, a randomised, multicenter study on educational and quality of life in patients with chronic obstructive pulmonary disease (COPD). Eur Respir J 2002; 20(38): 221s. 40. Antonelli Incalzi R, Pedone C, Onder G, et al. Predicting lenght of stay of older patients with exacerbated chronic obstructive pulmonary disease. Aging 2001; 13:49-57. 41. Antonelli Incalzi R, Fuso L, De Rosa M, et al. Comorbidity contributes to predict mortality of patients with chronic obstructive pulmonary disease. Eur Respir J 1997; 10:2794-2800. 167 Realizzato grazie al supporto di Boehringer Ingelheim. Edizione fuori commercio. Omaggio riservato ai Sigg. Medici Pubblicato da GPAnet srl Corso Sempione, 44 – 20154 Milano Finito di stampare nel mese di Aprile 2005 – presso Grafiche Mazzucchelli Tutti i diritti sono riservati. Nessuna parte di questa pubblicazione, può essere riprodotta, inserita in banche dati o trasmessa in qualsivoglia forma o tramite strumentazione elettronica, meccanica, in fotocopia, registrazione o altro, senza il permesso scritto dell’editore.
Scaricare