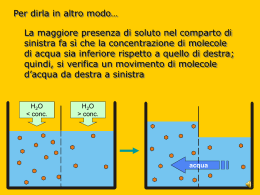
Diffusione e osmosi Roberto Cirio Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico 2007 – 2008 Corso di Fisica La lezione di oggi Sostanze sciolte in liquidi, se utilizzate con membrane, hanno comportamenti particolari Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 2 Soluzioni Diffusione Membrane L’osmosi Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 3 Un facile esperimento •Bicchiere d’acqua •Colorante •Velocita’ iniziale del colorante = 0 Aspetto un po’ di tempo Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 Arrivo a un equilibrio 4 Soluzioni Una sostanza viene disciolta in un liquido Liquido Î solvente Sostanza Î soluto Solvente + soluto Î soluzione Concentrazione molare (o molarita’): c = n/V z z n: numero di moli di soluto V: volume di solvente Esempio: Qual’e’ la concentrazione molare di una soluzione formata di 2g di saccarosio C12H22O11, disciolti in 100 cm3 di acqua ? M(C12H22O11) = 12.(12) + 22.(1) + 11. (16) = 342 u.m.a. n = 2/342 = 5.85.10-3 moli c = n/V = (5. 85.10-3 moli)/(100.10-6 m3) = 58.5 moli/m3 = 5.85.10-2 moli/l Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 5 Soluzioni Diffusione Membrane L’osmosi Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 6 Il moto delle molecole in una soluzione Soluzione (solvente+soluto) Ad esempio: acqua e zucchero Parete divisoria Solvente puro Ad esempio: acqua Fase 1: Le molecole di soluto urtano contro tutte le pareti del recipiente (energia cinetica) Energia cinetica delle molecole 3 K m = kT 2 Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 7 Il moto delle molecole in una soluzione Fase 2: Tolgo la parete divisoria La linea tratteggiata indica la posizione dov’era la parete divisoria, che ora e’ stata tolta Alcune molecole di soluto diffondono nel lato destro del recipiente Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 8 Il moto delle molecole in una soluzione La linea tratteggiata indica la posizione dov’era la parete divisoria, che ora e’ stata tolta Fase 3 Alcune molecole di soluto diffondono nel lato destro del recipiente Alcune molecole di soluto diffondono nel lato sinistro del recipiente Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 9 Il moto delle molecole in una soluzione La linea tratteggiata indica la posizione dov’era la parete divisoria, che ora e’ stata tolta Fase 4 Si e’ raggiunto l’equilibrio La concentrazione e’ identica in entrambe le parti Diffusione (sinistraÎdestra) = Diffusione (destra Îsinistra) All’equilibrio, non c’e’ flusso (molecole/(cm2 s)) di molecole nella soluzione Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 Φd-s = Φs-d 10 La legge di Fick Vediamo la stessa cosa, in un modo diverso cdestra < csinistra Nel volume A.Δx arrivano piu’ molecole da sinistra che da destra Flusso netto (o risultante) da sinistra a destra Quando cdestra = csinistra, il flusso si ferma Δx Definisco J: velocita’ di diffusione: z z Numero di molecole/s Numero di moli/s Legge di Fick Diffusione e osmosi Considero D, il coefficiente diffusione e ottengo la c1 - c 2 J =Corso DAdi laurea in CTF Δ2007/8 x Fisica – a.a. di 11 Coefficienti di diffusione Diffusione e osmosi Molecola diffondente Mezzo D (m2/s) H2 aria 6.3.10-5 O2 aria 1.8.10-5 O2 acqua 100.10-11 Emoglobina del sangue acqua 6.9.10-11 Glicina (amminoacido) acqua 95.10-11 DNA (M=6.106 uma) acqua 0.13.10-11 Corso di laurea in CTF Fisica – a.a. 2007/8 12 Soluzioni Diffusione Membrane L’osmosi Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 13 Membrane semipermeabili Considero una membrana semipermeabile z z z z z z Membrana Forata Diametro dei fori permette il passaggio di molecole piccole Diametro dei fori evita il passaggio di molecole grandi Esempio: lascia passare le molecole di acqua e blocca le molecole di zucchero Le pareti delle cellule e le superfici epiteliali sono semipermeabili Molecole di H2O possono diffondere verso destra e verso sinistra Molecole di zucchero non possono attraversare la membrana semipermeabile Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 14 Membrane semipermeabili Per la legge di Fick, si cerca di avere due concentrazioni uguali Non potendo aumentare la concentrazione a destra, le molecole si muovono per diminuire la concentrazione a sinistra Ho un flusso da destra a sinistra (netto o risultante) Il volume di solvente a sinistra aumenta Il livello a sinistra si alza rispetto al livello a destra Perche’ ? B •In un certo istante, ho 10 molecole vicino ai fori della membrana con la velocita’ diretta verso i fori •Da A a B passano tutte le 10 molecole •Da B ad A ne passano solo 6 A Diffusione e osmosi •Ho un flusso netto di 4 molecole da A a B Corso di laurea in CTF Fisica – a.a. 2007/8 •Statisticamente, 15 questo si rinnova continuamente Soluzioni Diffusione Membrane L’osmosi Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 16 L’osmosi Osmosi: diffusione dell’acqua da una zona a bassa concentrazione verso una zona ad alta concentrazione, attraverso una membrana semipermeabile Il meccanismo e’ uguale a quello della diffusione libera Voglio raggiungere un equilibrio nella concentrazione Ma se utilizzo acqua pura, non riesco a raggiungere l’equilibrio Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 17 La pressione osmotica Sono arrivato all’equilibrio Posmotica = Pidrostatica h Posmotica mi e’ data dalla legge dei gas perfetti, considerando il soluto come un gas nRT Psoluto = Equazione di van ‘t Hoff V • la costante δ: coefficiente di dissociazione elettrolitica, e’ il rapporto tra particelle di soluto in soluzione e molecole di soluto indissociato •Se non si dissocia: δ=1 Posmotica = δ c R T •Se si dissocia completamente (1 molecola, 2 ioni): δ=2 •c: concentrazione del soluto Diffusione e osmosi •T: Corso di laurea in CTF Fisica temperatura in–Ka.a. 2007/8 18 Esercizio Problema. In un osmometro e’ contenuta una soluzione diluita di saccarosio (C12H 22O 11) ottenuta disciogliendo 1.0 g di zucchero in 1 l di acqua. Una volta immerso l’osmometro in acqua pura, qual’e’ il dislivello che si determina a 20 C in condizioni di equilibrio ? M(C12H 22O 11)=12.(12)+22.(1)+11.(16)=342 n=(1.0)/(342)=2.9.10-3 moli Posmotica = δ c R T = (2.9⋅10-3 ) moli/l = (1) (8.31) ⋅ (273 + 20) = −3 3 10 m /l = 7.1 ⋅ 10 3 Pa Membrana semipermeabile Diffusione e osmosi Posmotica 7.1 ⋅ 10 3 h= = =0.72 m 3 ρg (10 ) ⋅ (9.81) Corso di laurea in CTF Fisica – a.a. 2007/8 19 L’osmole Una unita’ di misura pratica e’ l’osmole 1 osmole: 1 mole di soluto non elettrolita (δ=1) La Posmotica di 1 osmole disciolta in 1 l di H2O a T=0 C e’: 1 6 ) ⋅ ( 8 . 31 ) ⋅ ( 273 ) = 2 . 27 ⋅ 10 Pa = 22.4 atm −3 10 P = δ c R T = (1) ⋅ ( L’osmolalita’ Prendo un solvente Sciolgo nel solvente vari tipi di soluto Quale sara’ la concentrazione ? c sara’ la concentrazione di tutte le molecole che non diffondono attraverso la membrana Corso di laurea in CTF Diffusione e osmosi in osmole/litro Fisica – a.a. 2007/8 Si misura 20 Le soluzioni isotoniche Ho un fenomeno osmotico quando e’ presente una membrana semipermeabile che separa due soluzioni a c diversa Il flusso di solvente va dalla c piu’ piccola alla c piu’ grande Lo scopo e’ di uniformare le due c Se tra i due comportamenti c’e anche una Δpidraulica, si deve tener conto anche di questa Due soluzioni con uguale c si dicono isotoniche Con soluzioni isotoniche, Δposmotica = 0 Ogni sostanza iniettata nel sangue deve essere isotonica al plasma, per evitare: z z Flusso di solvente da cellule a plasma (atrofizzazione delle cellule) con soluzione ipertonica (csoluzione > cplasma) Flusso di solvente da plasma a cellule (le cellule si gonfiano ed eventualmente si rompono; fenomeno dell’emolisi) con soluzione ipotonica (csoluzione < cplasma) Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 21 Esempio Problema. Qual’e’ la pressione osmotica del fluido intracellulare che ha un’osmolalita’ di 0.30 osmoli/l alla temperatura corporea di 37 C ? ⎞ 5 -1 Posmotica=cRT= ⎛⎜ 0.30-osmoli 7.73 ⋅ 10 Pa = 7.6 atm ⋅ ⋅ + = (8.31 J K ) (273 37 K) ⎟ 3 3 ⎝ 10 m ⎠ Nella realta’ la Posmotica cellulare dipende dalla rigidita’ della parete cellulare e dalla osmolalita’ del fluido che circonda la cellula Problema. Calcolare la quantita’ di glucosio (C6H12O6) da sciogliere in 1 l di acqua per ottenere una soluzione isotonica. Voglio ottenere una osmolalita’ di 0.30 osmoli/l M C 6 H12 O 6 = 6 ⋅ (12) + 12 ⋅ (1) + 6 ⋅ (16) = 180 m C 6 H12 O 6 = (0.3) ⋅ (180 g) = 54 g Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 22 Riassumendo La diffusione e’ un fenomeno semplice Membrane e soluzioni permettono il funzionamento di molti aspetti della fisiologia Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 23 Esercizio da svolgere a casa n. 17.14 pag. 106 Celasco-Panzieri. 2000 problemi di fisica-ECIG In un osmometro come illustrato in figura, viene immessa una soluzione di densita’ incognita. La membrana semipermeabile situata sul fondo dell’osmometro, si trova ad una profondita’ h2 = 60 cm sotto il pelo libero del solvente puro.All’istante iniziale la differenza di pressione attraverso la membrana e’ 0 e l’altezza della soluzione nell’osmometro e’ h1=10 cm. Alla fine la soluzione raggiunge il valore h3= 80 cm. Determinare: 1. 2. 3. Diffusione e osmosi La densita’ della soluzione all’istante iniziale se la densita’ del solvente puro e’ ρ=103 kg/m3 La pressione osmotica della soluzione La concentrazione della soluzione, nell’ipotesi che la densita’ della soluzione alla fine dell’esperimento sia praticamente invariata rispetto alla densita’ iniziale e che la temperatura sia 27 C. Corso di laurea in CTF Fisica – a.a. 2007/8 24 Soluzione 1 domanda Se ΔP=0, allora le pressioni idrostatiche sono uguali. Psolvente = ρ solvente g h 2 Psoluzione = ρ soluzione g (h 2 - h 1 ) Psoluzione = Psolvente ρ soluzione ρ solvente g h 2 (10 3 )( 9 . 8 )( 0 . 6 ) = = = 1 . 2 ⋅ 10 3 kg m 3 g (h 2 - h 1 ) (9.8)(0.6 - 0.1) Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 25 Soluzione 2 domanda All’equilibrio, la pressione osmotica deve essere uguale alla pressione idrostatica Posmotica = ρ soluzione g h 3 = (1.2 ⋅ 10 )(9.8)(0.8) = 9.4 ⋅ 10 Pa 3 Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 3 26 Soluzione 3 domanda Posmotica = c R T Posmotica 9.4 ⋅ 10 3 c = = 3.78 moli/m3 = RT (8.31)(273 + 27) Diffusione e osmosi Corso di laurea in CTF Fisica – a.a. 2007/8 27
Scaricare