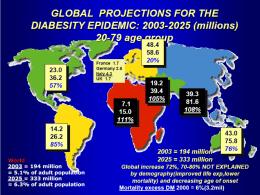
Diabete mellito in pillole Claudio Taboga Ambulatori diabetologici di Gemona del Friuli e Tolmezzo ASS n° 3 «Alto Friuli-Collinare-Friuli Centrale» Classificazione Standard Italiani per la Cura del Diabete Mellito 2014 Fenotipi del diabete tipo 2 LADA Pancreatite Steroidi Diabete tipo 2 vero (≈86%) Classico Iperinsulinemico, alto rischio CV Insulinopenico, basso rischio CV Sottotipi rari (MODY) Groop L. EASD Meeting 2013 Diagnosi di diabete In assenza dei sintomi tipici la diagnosi di diabete deve essere posta con il riscontro, confermato in almeno due diverse occasioni di: glicemia a digiuno 126 mg/dl (con dosaggio su prelievo eseguito al mattino, alle ore 8 circa, dopo almeno 8 ore di digiuno) oppure glicemia 200 mg/dl 2 ore dopo carico orale di glucosio eseguito con 75 g (Oral Glucose Tolerance Test, OGTT) in entrambi i casi da confermare con un secondo test. (LdP III, FdR A) oppure HbA1c 6,5% (solo con dosaggio standardizzato). (LdP III, FdR A) In presenza di sintomi tipici della malattia, la diagnosi di diabete deve essere posta con il riscontro, anche in una sola occasione di: glicemia casuale 200 mg/dl (indipendentemente dall’assunzione di cibo). (LdP III, FdR A) diabete gestazionale 3. 4. 5. Glicemia plasmatica Mg/dl Mmmol/l digiuno 92 5,1 Dopo 1 h 180 10,0 Dopo 2 h 153 8,5 Per lo screening del diabete gestazionale non devono essere utilizzati la glicemia plasmatica a digiuno, glicemie random, glucose challenge test (GCT) o minicurva, glicosuria, OGTT 100 g. I professionisti devono informare le donne in gravidanza che: - nella maggioranza delle donne il diabete gestazionale viene controllato da modifiche della dieta e dall'attività fisica - se dieta e attività fisica non sono sufficienti per controllare il diabete gestazionale, e necessario assumere insulina; questa condizione si verifica in una percentuale compresa fra il 10% e il 20% delle donne - se il diabete gestazionale non viene controllato, c‘è il rischio di una aumentata frequenza di complicazioni della gravidanza e del parto, come pre-eclampsia e distocia di spalla - la diagnosi di diabete gestazionale e associata a un potenziale incremento negli interventi di monitoraggio e assistenziali in gravidanza e durante il parto - le donne con diabete gestazionale hanno un rischio aumentato, difficile da quantificare, di sviluppare un diabete tipo 2, particolarmente nei primi 5 anni dopo il parto. Alle donne cui e stato diagnosticato un diabete gestazionale deve essere offerto un OGTT 75 g non prima che siano trascorse sei settimane dal parto. ISS: AMD, SID, CeVEAS. 2011 Hb glicata & glicemia Vecchio metodo Nuovo metodo HbA1c (%) HbA1c mmol/mol 4.0 20 5.0 31 6.0 42 6.5 48 7.0 53 7.5 59 8.0 64 9.0 75 10.0 86 11.0 97 12 108 [DCCT HbA1C (%) - 2.15] x 10.929 Mmol/l=mg/dl:18 Buon controllo metabolico Il criterio della “normoglicemia” è necessario ma non sufficiente per definire il “buon controllo metabolico” Il buon controllo metabolico del Diabete tipo 2 si raggiunge quando tutti i fattori della Sindrome Metabolica sono sotto “buon controllo” Il diabete non è solo una malattia cronica ma anche evolutiva. Diabetologi udinesi, anni ‘80 Diabete tipo 2. Terapia Stile di vita Sulfoniluree, glinidi (repaglinide, nateglinide) Metformina Alfa-glucosidase inibitori (acarbose, miglitolo) Tiazolidinedioni (pioglitazone, rosiglitazone) Insuline e analoghi Incretine (exenatide, exenatide LAR, liraglutide, lixisenatide) Inibitori della DPP-IV (saxagliptin, sitagliptin, vildagliptin, linagliptin, alogliptin) Inibitori del riassorbimento tubulare del glucosio (SGLUT2: canaglifozin, dapaglifozoin, empaglifozin) Potenza dei farmaci per il diabete * Nathan DM et al. Diabetes Care, 2009 The Number of Medications Taken Usually Increases With Duration of Disease Diabetes diagnosed Beta-cell function (%) 100 Monotherapy failure Requiring insulin 80 Monotherapy Dual-drug regimens 60 40 Multidrug combination +/– insulin Insulinbased regimens 20 IGT 0 0 10 15–25 Approximate time (years) IGT=impaired glucose tolerance. UKPDS 16. Diabetes. 1995;44:1249–1258. Turner RC et al. JAMA. 1999;281:2005–2012; Warren RE. Diabetes Res Clin Pract. 2004;65:S3–S8; Lebovitz HE. Med Clin N Am. 2004;88:847–863. Conservative versus proactive management of type 2 diabetes Adapted from Campbell IW. Br J Cardiol 7, 625-631, 2000 Traditional stepwise management + 10 Diet & exercise Oral monotherapy + ± Oral Oral ± insulin combination Intensive insulin HbA1c (%) 9 8 7 Target HbA1c 6.5% 6 Stepwise treatment Adapted from Campbell IW. Br J Cardiol 2000; 7: 625-631 Strategia terapeutica di tipo intensivo Dieta OAD in monoterapia 10 OADs massima titolazione HbA1c (%) OAD in combinazione OAD + insulina basale 9 8 7 6 Durata del diabete Del Prato S et al. Int J Clin Pract 2005; 59: 1345–1355. OAD + insulina basal/bolus Strategia terapeutica di tipo intensivo INSULINA Dieta OAD in monoterapia 10 OADs massima titolazione HbA1c (%) OAD in combinazione OAD + insulina basale 9 8 7 6 Durata del diabete Del Prato S et al. Int J Clin Pract 2005; 59: 1345–1355. OAD + insulina basal/bolus Summary of Incretin Actions on Different Target Tissues Neuroprotection Appetite Brain Stomach Heart Gastric emptying Cardioprotection Cardiac output GLP-1 Liver GI tract Insulin sensitivity Muscle Glucose production Insulin biosynthesis Beta–cell proliferation Beta–cell apoptosis Insulin secretion Glucagon secretion Adapted from Drucker DJ. Cell Metab. 2006;3:153–165. Incretinomimetici vs DPP-IV inibitori Holst JJ et al. Trends in Molec Med, 14, 161, 2008 Indicazioni Inzucchi et al. Diabetes Care Volume 38, January 2015 Statement of ADA/EASD: a patientcentered approach. Key points Obiettivi glicemici e terapie ipoglicemizzanti devono essere personalizzati Dieta, esercizio fisico ed educazione sono basilari Salvo controindicazioni la metformina rappresenta la prima scelta; per gli step successivi ci sono pochi riferimenti: ha senso aggiungere 1-2 farmaci orali o iniettivi con l’obiettivo di limitare gli effetti collaterali. L’insulina, da sola o in combinazione, è in fondo necessaria per il controllo glicemico Considerare anche preferenze, bisogni e contesto del paziente Obiettivo prioritario è la riduzione del rischio cardiovascolare globale Inzucchi SE et al. Diabetes Care 35:1364–1379, 2012 Figura 2. Flow-chart per la terapia del diabete mellito di tipo 2. Iniziare con solo intervento su stile di vita (se non grave scompenso metabolico [ref. 1]) Aggiungere gradualmente metformina, fino alla dose di almeno 2 g/die Ipoglic. Peso Effetti indesid. CVD Fattori rischio CV Scomp. cardiaco Effetti GI Costo Gliptina 1A 1B Rari 1A 1B 2B (2) 1A Elevato A.R. GLP-1 1A 1A Non indicato in IRC 3B 1A 2B 1C Elevato Sulfonilurea o repaglinide 1D 1D Non indicato in IRC (3) 3C (2) 1B 1B 1A Basso Pioglitazione 1A 1D Fratture 1A 1A 1E 1A Medio Acarbosio 1A 1D Rari 2B 2B 3C 1C Basso Gliflozina 1A 1A Infezioni GU 3C 2B 2B 1A ??? Insulina basale 1D 1A Rari 1B 1A 1B 1A Medio Add on a metformina In presenza di un fallimento della terapia iniziale volta a modificare lo stile di vita, prescrivere metformina, che dovrà accompagnare sempre, se tollerata e non controindicata, ogni altro farmaco, alla dose di almeno 2 g/die. Se fallisce la metformina, aggiungere un secondo o anche un terzo farmaco secondo lo schema indicato, valutando comunque la possibilità di inserire una terapia insulinica, anche temporaneamente. Sebbene un approccio fisiopatologico nella scelta del farmaco da associare alla metformina appaia il più razionale, non esiste alcuna evidenza che lo stesso sia maggiormente efficace o indicato. Al contrario, i possibili effetti collaterali o pleiotropici dei farmaci sono noti e dimostrati e devono essere considerati nella scelta terapeutica. Nota: in presenza di HbA1c >2% all’obiettivo, iniziare direttamente terapia combinata, eventualmente anche con insulina solo saxagliptin: minimo rischio per scompenso cardiaco; non dati per altre molecole alcuni farmaci di questa classe non hanno metabolismo renale, ma non hanno comunque indicazione in scheda tecnica solo per glibenclamide, possibili rischi cardiaci. Colori: effetto o parametro negativo o sconsigliato effetto o parametro parzialmente negativo o sconsigliato effetto o parametro positivo o probabilmente positivo il farmaco non ha effetti significativi sul parametro o viene dato un giudizio neutro Sigle: rappresentano il grado di evidenza (1-6) e di forza (A-E). Antihyperglycemic Agents and Renal Function CKD Stage: GFR (mL/min): 5 < 15 4 15-29 3 30-59 30 Metformin Linagliptin 15 Saxagliptin 15 Sitagliptin 25 mg 2.5 mg ≥ 90 60 50 30 50 mg 50 30 Exenatide 50 50 Liraglutide Glyburide 1 25 Acarbose Gliclazide/Glimepiride 2 60-89 15 30 30 50 Repaglinide Thiazolidinediones 30 Not recommended / contraindicated Caution and/or dose reduction Safe Adapted from: Product Monographs as of March 1, 2013; CDA Guidelines 2008; and Yale JF. J Am Soc Nephrol 2005; 16:S7-S10. guidelines.diabetes.ca | 1-800-BANTING (226-8464) | diabetes.ca Copyright © 2013 Canadian Diabetes Association Designing insulin degludec: structure Jonassen et al. Pharm Res 2012; 29:2104–14 Insulin degludec: immediately after injection Jonassen et al. Pharm Res 2012; 29:2104–14 Insulin degludec: slow release following injection Jonassen et al. Pharm Res 2012; 29:2104–14 Insulin degludec: slow release following injection Jonassen et al. Pharm Res 2012; 29:2104–14 Insulin degludec: slow release following injection Jonassen et al. Pharm Res 2012; 29:2104–14 Revisiting the ideal basal insulin: key characteristics Insulin degludec: PD profiles in T2D at steady state (mg/kg/min) GIR (mg/kg/min) GIR 5 0.8 U/kg 0.6 U/kg 0.4 U/kg 4 3 2 1 0 Day 6 T2D, type 2 diabetes; PD, pharmacodynamic Heise et al. Diabetes Obes Metab 2012; DOI: 10.1111/j.1463-1326.2012.01638.x Day 7 Study conclusions Steady-state studies The glucose-lowering effect of insulin degludec: is flat and stable is evenly distributed over a 24-hour period lasts beyond 42 hours Half-life study Insulin degludec has a half-life of more than 25 hours (twice as long as that for insulin glargine) Insulin degludec has a flat and stable glucose-lowering effect. The glucose-lowering effect of insulin degludec is consistent and evenly distributed over the 24 hour period Heise et al. Diabetes Obes Metab 2012; DOI: 10.1111/j.1463-1326.2012.01638.x; Kurtzhals et al. Diabetologia 2011;54(Suppl. 1):S426; Diabetes 2011;60(Suppl. 1A):LB12; Heise et al. IDF 2011:P-1444; Diabetologia 2011;54(Suppl. 1):S425; Diabetes 2011;60(Suppl. 1A):LB11 Conclusions Insulin degludec has a flat and stable glucoselowering effect, equally distributed over 24 hours Half-life twice as long as that of insulin glargine Variability considerably lower than that of insulin glargine This may facilitate titration to lower FPG targets with potentially a lower risk of hypoglycaemia Heise et al. Diabetes Obes Metab 2012; DOI: 10.1111/j.1463-1326.2012.01638.x; Kurtzhals et al. Diabetologia 2011;54(Suppl. 1):S426; Diabetes 2011;60(Suppl. 1A):LB12; Heise et al. IDF 2011:P-1444; Diabetologia 2011;54(Suppl. 1):S425; Diabetes 2011;60(Suppl. 1A):LB11; Heise et al. Diabetes Obes Metab 2012;14:859–64 Dosing of insulin degludec Initiation Patients with T2D: the recommended daily starting dose is 10 U followed by individual dosage adjustments Patients with T1D: to be used in combination with meal-time insulin and requires subsequent individual dosage adjustments Transfer from other insulins Patients with T2D: unit-to-unit switch from any basal insulin OD or BID or basal component of prior basal-bolus or premix insulin Patients with T1D: OD basal insulin therapy: unit-to-unit switch BID basal insulin therapy or a HbA1c <8.0% at the time of transfer, the dose needs to be determined on an individual basis (consider dose reduction) Flexibility: On occasions when administration at the same time of the day is not possible, insulin degludec allows for flexibility in the timing of insulin administration. A minimum of 8 hours between injections should always be ensured. BID, twice daily Tresiba® SmPC, Novo Nordisk, May 2013 Renal glucose re-absorption under healthy conditions1,2 Filtered glucose load 180 g/day SGLT2 ~ 90% SGLT1 ~ 10% Virtually all of the filtered glucose is re-absorbed in the proximal tubules through SGLT2 and SGLT1 with SGLT2 accounting In healthyfor ~ 90% in the S1 individuals, and S2 the segments renal and SGLT1 glomeruli filter accounting ~180 g for ~ glucose 10% in the of per S3 segment day SGLT, sodium glucose cotransporter. 1. Adapted from: Gerich JE. Diabet Med. 2010;27:136–142; 2. Bakris GL, et al. Kidney Int. 2009;75;1272–1277. 31 Renal glucose re-absorption in patients with diabetes1,2 Filtered glucose load > 180 g/day SGLT2 ~ 90% SGLT1 ~ 10% SGLT, sodium glucose cotransporter. 1. Adapted from: Gerich JE. Diabet Med. 2010;27:136–142; 2. Bakris GL, et al. Kidney Int. 2009;75;1272–1277. When blood glucose increases above the renal threshold (~ 11 mmol/l or 190 mg/dL), the capacity of the transporters is exceeded, resulting in urinary glucose excretion 32 Urinary glucose excretion via SGLT2 inhibition1 Filtered glucose load > 180 g/day SGLT2 SGLT2 inhibitor SGLT1 SGLT, sodium glucose cotransporter. *Loss of ~ 80 g of glucose per day = 240 cal/day. 1. Bakris GL, et al. Kidney Int. 2009;75;1272–1277. SGLT2 inhibitors reduce glucose re-absorption in the proximal tubule, leading to urinary glucose excretion* and osmotic diuresis 33 Strutture chimiche degli inibitori di SGLT 2 Empagliflozin Comparison with placebo 0.00 (95% CI: -0.15, -0.14; p = 0.9697) -0.12 (95% CI:-0.26, 0.03; p = 0.1060) -0.73 (95% CI: -0.88, -0.59) p < 0.001 -0.74 (95% CI: -0.88, -0.59) p < 0.001 -0.85 (95% CI: -0.99, -0.71) p < 0.001 Placebo Empa 10 mg QD Empa 25 mg QD SITA 100 mg QD Mean baseline HbA1c (%) 7.91 7.87 7.86 7.85 End HbA1c (%) 7.98 7.21 7.09 7.20 CI, confidence interval; Empa, empagliflozin; HbA1c, glycosylated haemoglobin; QD, once daily; SE, standard error; SITA, sitagliptin. FAS (LOCF). 35 Roden M, et al. Lancet Diabetes Endocrinol. 2013; 1: 208–19. EMPA-REG MONO 24-week empagliflozin monotherapy versus placebo and sitagliptin Change in HbA1c Placebo (n = 226) Empagliflozin 10 mg QD 25 mg QD (n = 223) (n = 223) Comparison with placebo Sitagliptin 100 mg QD (n = 223) Adjusted mean change from baseline in FPG (mg/dL)* -12.43 (95% CI: -18.45, -7.02; p < 0.0001) -17.48 (95% CI: -23.06, -12.07; p < 0.0001) -31.17 (95% CI: -36.57, -25.76) p < 0.0001 EMPA-REG MONO 24-week empagliflozin monotherapy versus placebo and sitagliptin. Change in FPG (mg/dL) -18.73 (95% CI: -24.14, -13.15) p < 0.0001 -36.21 (95% CI: -41.62, -30.81) p < 0.0001 Placebo Baseline mean 154.78 Empa 10 mg Empa 25 mg QD QD 152.79 152.61 SITA 100 mg QD 147.02 CI, confidence interval ; Empa, empagliflozin; FPG, fasting plasma glucose; QD, once daily; SITA, sitagliptin. *Not measured in 2 patients in the placebo group, 1 patient in the empagliflozin 10-mg QD group and 1 patient in the empagliflozin 25-mg QD group. ANCOVA, FAS (LOCF). 36 Roden M, et al. Lancet Diabetes Endocrinol. 2013; 1: 208–19. Placebo (n = 228) Empagliflozin Sitagliptin 10 mg QD 25 mg QD 100 mg QD (n = 224) (n = 223) (n = 224) EMPA-REG MONO 24-week empagliflozin monotherapy versus placebo and sitagliptin. Change in body weight Comparison with placebo -2.45 (95% CI: -2.93, -1.96; p < 0.0001) -2.67 (95% CI: -3.15, -2.18; p < 0.0001) -1.93 (95% CI: -2.41, -1.45) p < 0.0001 -2.15 (95% CI: -2.63, -1.67) p < 0.0001 0.52 (95% CI: 0.04, 1.00) p = 0.0355 Mean baseline 78.2 78.4 77.8 CI, confidence interval; QD, once daily; SE, standard error. FAS (LOCF). Roden M, et al. Lancet Diabetes Endocrinol. 2013; 1: 208–19. 79.3 37 Placebo (n = 228) Empagliflozin Sitagliptin 10 mg QD 25 mg QD 100 mg QD (n = 224) (n = 223) (n = 224) EMPA-REG MONO 24-week empagliflozin monotherapy versus placebo and sitagliptin. Change in SBP Comparison with placebo -3.4 (95% CI: -5.7, -1.2; p < 0.0031) -4.2 (95% CI: -6.5, -2.0; p < 0.0003) -2.6 (95% CI: -4.9, 0.4) p = 0.0231 -3.4 (95% CI: -5.7, -1.2) p = 0.0028 0.8 (95% CI: -1.4, 3.1) p = 0.4803 Mean baseline 130.4 133.0 129.9 132.5 CI, confidence interval ; QD, once daily; SBP, systolic blood pressure; SE, standard error. FAS (LOCF). Roden M, et al. Lancet Diabetes Endocrinol. 2013; 1: 208–19. 38 EMPA-REG MONO 24-week empagliflozin monotherapy versus placebo and sitagliptin. Adverse events of special interest (n = 229) 10 mg QD (n = 224) 25 mg QD (n = 223) (n = 223) OL empagliflozin 25 mg QD (n = 87) Confirmed hypoglycaemia* 1 (0.4%) 1 (0.4%) 1 (0.4%) 1 (0.4%) 0 Urinary tract infections 12 ( 5) 15 ( 7) 12 ( 5) 11 ( 5) 3 ( 3) Male† 3 (2) 3 (2) 2 (1) 4 (3) 2 (3) Female‡ 9 (9) 12 (15) 10 (13) 7 (9) 1 (4) 0 ( 0.0) 7 ( 3) 9 ( 4) 2 ( 1) 1 ( 1) Male† 0 4 (3) 2 (1) 1 (1) 1 (2) Female‡ 0 3 (4) 7 (9) 1 (1) 0 Placebo n (%) Genital infections Sitagliptin Empagliflozin QD, once daily. *Plasma glucose ≤ 70 mg/dL and/or requiring assistance. †Percentage of males in group. ‡Percentage of females in group. Roden M, et al. Lancet Diabetes Endocrinol. 2013; 1: 208–19. 39 PT glifozine - 22-4-2015 GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale Kit formativo in pillole. Anno 2012 Addestramento all’uso di (Eurotouch) MyStar: anagrafica, esami di laboratorio, dati clinici, scarico fotometri. Rapportarsi con il paziente cronico, per la patologia e per la dipendenza dalla Struttura. Griglia per la front-line Il Diabete: che cos’è, come si tratta (classi di farmaci, tipi di insuline), come e da chi viene monitorato, complicanze e comorbidità, ipoglicemia e iperglicemia Ambulatorio infermieristico dedicato con attività refertata e contabilizzata per Istruzione, Addestramento e Verifica (=EDUCAZIONE) su (Il materiale va mostrato, non raccontato!) Autocontrollo glicemico: chi, come, quando Tecniche di iniezione dell’insulina o GLP-1 Igiene della persona (pieghe, piedi…) Rudimenti di stile di vita (per i casi non da dietista) Kit educativo “di sopravvivenza” per tutte le prime visite, diversificato per tipo di diabete. The Third Injection Technique Workshop In Athens (TITAN) La Lipoipertrofia si correla con: Durata della terapia insulinica (P<0.001), Uso ripetuto degli aghi (P=0.002), Stravaso dell’insulina dai siti di iniezione (P=0.002) Utilizzo di aree addominali relativamente piccole (P<0.029). Pazienti con lipoipertrofia hanno escursioni glicemiche inspiegabili più frequenti (P<0.001). Fried A et al. Diabetes & Metabolism 36, S19-S29, 2010 Lipoipertrofia da insulina Lipoatrofia da insulina Skin and subcutaneous adipose layer thickness in adults with diabetes at sites used for insulin injections: implications for needle length recommendations Spessore mm Pelle Sottocutaneo braccio 2,23±0,44 10,77±5,62 coscia 1,87±0,39 10,35±5,65 Addome 2,15±0,42 13,92±7,26 gluteo 2,41±0,48 15,45±7,27 Gibney MA et al. Current Medical Research & Opinion 26, 1519-30, 2010 Skin and subcutaneous adipose layer thickness in adults with diabetes at sites used for insulin injections: implications for needle length recommendations Parte superolaterale della coscia, angolo a 90°, senza pizzicotto Gibney MA et al. Current Medical Research & Opinion 26, 1519-30, 2010 Autocontrollo nel tipo 2 non insulinotrattato PRO CON Observational Observational ROSSO1 Kaiser Permanente3 Fremantle Diabetes Study2 QuED4 Randomized Controlled Trial Randomized Controlled Trial German-Austrian5 DINAMIC 16 ASIA7 STeP 11 ROSES 12 PRISMA 13 St Carlos 14 King-Drew Medical Center8 ESMON9 DiGEM10 1. Martin S et al. Diabetologia, 2006. 2. Davis WA et al. Diabetologia, 2007. 3. Kater A et al. Diabetes Care, 2006. 4. Franciosi M et al. Diabet Med, 2005. 5. Schwedes U et al. Diabetes Care, 2002.. Barnett AH et al. BMJ, 2008. 7. Guerci B et al. Diabetes Metab, 2003. 8. Davidson M et al. Am J Med, 2005. 9. O’Kane MJ et al. BMJ, 2008. 10. Farmer A et al. BMJ, 2007 11. Polonsky WH et al. Diabetes Care 2011. 12. Franciosi M et al. Diabetic Medicine, 2011. 13 Bosi E et al. Diabetes Care 2013. 14. Garcia de la Torre et al. Acta Diabetol, 2013. Scelta ed uso del glucometro Le caratteristiche che devono essere tenute presenti e che possono condizionare la scelta di uno strumento rispetto ad un altro in relazione al tipo di paziente (stile di vita, limitazioni manuali o visive,….) nella cura a domicilio devono garantire praticità d’uso e adeguatezza alla fenotipizzazione del paziente accuratezza e precisione controllo di qualità Il team diabetologico che ha in carico il paziente ha gli elementi per operare la scelta più appropriata rispettando le esigenze, le caratteristiche e le capacità manuali ed intellettive del singolo paziente. Consensus Autocontrollo 2012 Tipologie di glucometro tipo Indicazione Basic facile, funzioni di base I° livello gestionale ed intellettuale, ADO Medium Elaborazione, commento e scarico dati, visualizzazione medie e diari, ADO, tipo 2 o tipo 1 non intensivo Specifico Chetonemia, calcolo bolo, comunicazione con microinfusore Abilità e propensione alla tecnologia Multi-iniettiva o microinfusore Girelli A et al. G It Diabetol Metab 34, 93-100, 2014 Autocontrollo. Consensus intersociatario. (AMD-SID-SIEDP-OSDI-SIBioC–SIMeL) Raccomandazioni L’autocontrollo quotidiano (almeno 3-4 controlli/die) è INDISPENSABILE per la persona con diabete tipo 1 in terapia insulinica intensiva (Livello della prova II, Forza della raccomandazione A) L’autocontrollo glicemico continuativo, con frequenza e modalità diverse, è UTILE per la persona con diabete tipo 2 insulinotrattato (Livello della prova II, Forza della raccomandazione B) L’autocontrollo glicemico non continuativo è UTILE per i pazienti con diabete tipo 2 in terapia orale o dietetica solo in presenza di una adeguata azione educativa e di un intervento strutturato ed attivo nelle modifiche della terapia (Livello di evidenza II, Forza della raccomandazione B) http://www.aemmedi.it/files/Linee-guida_Raccomandazioni/2013/... Utilizzo dei dati SMBG Dati dal Kaiser Permanente Northern California (KPNC) diabetes registry 7320 tipo 2 non insulina e in SMBG Utilizzo dati per aggiustamenti tx Paziente+provider 37% Solo paziente 34% Solo provider 14% Non utilizzati 15% Grant RW et al. ADA 2014. Am J Managed Care, 2015 (accepted) Self-monitoring of blood glucose in patients with diabetes who do not use insulin—are guidelines evidence-based? 18 clinical practice guidelines or position statements referred to: 15 systematic reviews, 14 randomized controlled trials, 33 nonrandomized controlled trials papers and 18 clinical practice guidelines or position statements. 21 randomized controlled trials were included in the systematic reviews. Approximately half of these evaluated an educational intervention where the effect of self-monitoring of blood glucose could not be clearly isolated. IL risultato principale dello studio è stato che…le linee guida erano più a favore dell’autocontrollo rispetto alle systematic reviews che ne valutavano gli effetti e quindi non è chiaro il criterio utilizzato per formulare le raccomandazioni. E’ possibile che la sponsorizzazione dell’Industria abbia indotto una “more positive attitude” towards use of self-monitoring. Aakre KM et al. Diabet Med 29, 1226–1236, 2012 Self monitoring of glucose in Type 2 diabetes: guidelines fail to reflect evidence Self-monitoring è diffuso: si stima che il suo costo annuale per il NHS relativo ai tipo 2 non insulinotrattati è £34m. Con questa spesa si ottiene una riduzione minima [HbA1c 2–3 mmol⁄mol (0.2–0.35%)] e con benefici inmprobabili sugli outcomes clinici. Inoltre, “spingendo” sull’autocontrollo glicemico, si rinforza l’approccio glucocentrico la cui rilevanza si riduce in molti pazienti con diabete tipo 2 di lunga durata . L’autocontrollo del peso, della PA e dell’attività fisica sarebbe molto più logico. E’ ora che le linee guida sull’ autocontrollo riportino correttamente la chiara evidenza della sua inutilità: dobbiamo frenare le spese inutili scoraggiando l’uso dell’autocontrollo nella grande maggioranza dei DM tipo 2. Lehman R. Diabet. Med. 29, 1225, 2012 Autocontrollo Misurazione ≠ miglioramento; statisticamente vs clinicamente significativo (riduzione HbA1c≥0,5%) Non è una terapia e quindi non andrebbe valutata mediante RCT. È un supporto per la terapia, stile di vita e farmaci. Non trascurabile la riduzione delle ipoglicemie Costa come la terapia e merita perlomeno altrettanta attenzione Lo stabilisce il medico (prescrizione): tipo di strumento, tempi e modi. Il MMG non può limitarsi alla trascrizione Infermiere e farmacista hanno compiti di addestramento, verifica, motivazione, rinforzo contribuendo in tal modo al kit educativo Cartella diabetologica In regione Totale AFIR gen-giu 2012/2013 n. ricette spesa lorda 2012 2013 ∆% 2012 2013 ∆% ASS 1 51.885 52.117 0,4% 2.575.666,37 2.394.108,59 -7,0% ASS 2 21.827 21.772 -0,3% 1.324.150,28 1.246.872,10 -5,8% ASS 3 9.231 9.152 -0,9% 440.252,03 394.643,42 -10,4% ASS 4 47.809 48.431 1,3% 2.407.531,92 2.206.675,38 -8,3% ASS 5 18.593 18.956 2,0% 891.496,39 841.179,60 -5,6% ASS 6 47.644 46.070 -3,3% 2.470.906,38 2.230.067,34 -9,7% 196.989 196.498 REGIONE -0,2% 10.110.003,37 9.313.546,43 -7,9% F. Tosolini, A Morsanutto, M. Cristiani. Direzione regionale Sanità In regione Diabete IVA 4% Dettaglio AFIR gen-giu 2013 n. ricette Diabete IVA 21% spesa lorda n. ricette spesa lorda AFIR n. ricette spesa lorda ASS 1 33.480 1.434.718,89 1.058 42.866,34 17.579 916.523,36 ASS 2 17.043 860.365,08 272 15.644,63 4.457 370.862,39 ASS 3 7.020 337.227,20 130 5.203,38 2.002 52.212,84 ASS 4 39.172 1.850.767,00 817 32.852,92 8.442 323.055,46 ASS 5 11.653 427.262,36 113 5.271,40 7.190 408.645,84 ASS 6 34.524 1.552.657,59 699 36.395,16 10.847 641.014,59 142.892 6.462.998,12 3.089 138.233,83 REGIONE 50.517 2.712.314,48 F. Tosolini, A Morsanutto, M. Cristiani. Direzione regionale Sanità ASS 3. gennaio-giugno 2013 Farmaci n. pezzi Spesa lorda AFIR ATC 10A (orali+incretine) 38.644 124.750,00 DM IVA 4% 7.020 337.227,20 ATC 10B (insuline) 6.136 DM IVA 21% 130 5.203,38 2.002 52.212,84 Totale 149.250,00 375.000,00 AFIR Totale n. ricette spesa lorda 394.643,32 L. Cecco. Servizio farmaceutico, ASS n° 3 «Alto Friuli»
Scaricare