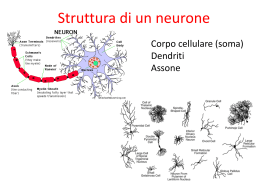
REGOLAZIONE DELL’APPETITO DALLO STOMACO AL SNC Lamorte Sara Omeostasi delle riserve energetiche Esistono meccanismi fisiologici per mantenere costanti le riserve energetiche in risposta alla disponibilità di cibo e alle spese energetiche.Se questi meccanismi non funzionano correttamente si instaurano condizioni patologiche quali l’anoressia e l’obesità. Regolazione dell’omeostasi energetica ( slide 3) L’omeostasi è regolata da segnali efferenti, rappresentati da fame, attività fisiche, livelli ormonali, riproduzione e crescita; e da segnali afferenti. Quest’ultimi si suddividono in segnali a corto termine, prodotti durante i pasti e segnali a lungo termine prodotti dalle riserve energetiche. Zona del SNC coinvolta in regolazione dell’appetito (slide 4) La zona del SNC coinvolta nell’omeostasi energetica è l’ipotalamo, regione situata sotto il talamo, nella parte centrale dell’encefalo. Esso è costituito da diversi nuclei, ognuno di essi svolge un funzione diversa, ma tutti sono coinvolti nei riflessi omeostatici. L’ipotalamo mette in comunicazione il corpo con il cervello. Come il SNC integra i diversi segnali afferenti ( slide 5) Il nucleo arcuato, uno dei nuclei in cui è suddiviso l’ipotalamo, rappresenta il centro di elaborazione primaria dell’informazione. Qui ,infatti, arrivavo ,attraversando la barriera emato-encefalica tramite carries specifici, i diversi segali afferenti, i quali vengono integrati tra loro originando una risposta che sarà poi inviata ai neuroni secondari. Il nucleo arcuato è costituito da due diversi set di neuroni: AgRP/Npy e Pomc/Cart. Tra di essi esiste una relazione di inibizione reciproca, quando uno è attivo inibisce l’altro e viceversa. I segnali afferenti possono essere classificati in segnali di sazietà e segnali di appetito. SEGNALI DI APPETITO: tra i segnali di appetito troviamo la grelina, ormone prodotto dallo stomaco prima dei pasti. La grelina si lega ai recettori presenti sui neuroni AgRP/Npy attivandoli, antagonizzando così l’azione della leptina e dell’insulina. SEGNALI DI SAZIETA’: sono la leptina e l’insulina prodotti rispettivamente dal tessuto adiposo e dal pancreas, in quantità proporzionali alle riserve energetiche.Questi si legano ai recettori presenti sui due set di neuroni, inibendo i neuroni AgRP/Npy e stimolando quelli Pomc/Cart. PYY3-36 è, invece, prodotto dalle cellule della mucosa intestinale dopo i pasti e in proporzione alla loro quantità. Si lega al recettore Y2R espresso sui neuroni AgRP/Npy. Infine vi sono altri due ormoni (slide 6) CCK, colicistochenina, e GLP-1, glucagone like petpide 1, entrambi prodotti dall’intestino e dal duodeno. Questi stimolano il nervo vago a livello locale, il nervo vago è una fibra nervosa che parte dal cervello e arriva a innervare l’intestino, lo stimolo viene inviato al SNC nel nucleo del tratto solitario, che fa sinapsi con i nuclei LHA e PVN, determinando una diminuzione dell’assunzione di cibo. Peptidi prodotti da neuroni primari ( slide 7) I neuroni primari producono due classi di neuropeptidi, che hanno come terget i neuroni secondari : Neuropeptidi anoressigenici: prodotti dai neuroni Pomc/Cart, in seguito a segnali di sazietà, inibiscono l’assunzione di cibo;sono rappresentati da: Cart (cocaina and anphetamine ragulated transcript) chiamato così perché i suoi livelli aumentano in seguito ad assunzione di cocaina e anfetamine e da α- MSH (melanocyte stimulating hormone) deriva dal precursore Pomc in seguito al suo clivaggio post-traduzionale. Neuropeptidi oressigenici: prodotti dai neuroni Npy/AgRP, in seguito a segnali di fame, stimolano l’assunzione di cibo; sono rappresentati da AgRP (agouti related protein)antagonista di α- MSH e da Npy (neuropeptide y). Modello “Dual center” (slide 8) Stellar nel 1954, ipotizzò che nell’ipotalamo vi fossero due centri distinti che regolano la fame e la sazietà e li chiamò: “Feeding center”, costituito dal nucleo dell’ipotalamo laterale LHA, la sua eliminazione causa l’anoressia e “Saziety center”, costituito dal nucleo ventromediale VMN e dal nucleo paraventricolare PVN, la sua eliminazione determina obesità. Il modello è tuttora valido. Saziety center (slide 9) Il centro della sazietà è rappresentato dai nuclei VMN e PVN, i quali esprimono due tipi di recettori, il recettore della melanocortina di tipo 4, MC4R, e il recettore per il neuropeptide Y, Y1R. Al primo si lega il neuropeptide α- MSH con funzione inibitoria e il neuropetide AgRP, antagonista che si lega al recettore occupando il sito di legame per α- MSH, impedendo così l’inibizione di questi neuroni. Questi due neuropeptidi fanno parte del pathway della melanocortina. Il legame di Npy al recettore Y1R disinibisce questi neuroni. Feeding center (slide 10) Il centro che controlla l’appetito è rappresentato dall’ipotalamo laterale, costituito da due gruppi di neuroni, quelli esprimenti orexina e quelli esprimenti MCH (melanin concentratine hormone),si tratta di ormoni ad azione oressigenica. Entrambi i neuroni sono espressi in modo uniforme all’interno di LHA e fanno sinapsi con diverse zone del cervello in cui si trovano i recettori per i rispettivi ormoni. L’azione su questi target determina salivazione, motilità gastrica, secrezione di insulina e glucagone (ormoni pancreatici), aumentando la possibilità che l’animale selvatico si metta alla ricerca di cibo. I neuroni orexina e MCH ricevono diversi imput: i primi sono attivati dal nucleo del tratto solitario con cui fanno sinapsi (slide 6) e dai neuroni Npy del nucleo arcuato, quest’ultimi attivano anche i neuroni MCH. Esiste un crosstalk tra i due gruppi di neuroni e in particolare, sembra che i neuroni orexina siano in grado di influenzare,attraverso meccanismi diretti e indiretti, l’espressione di MCH. Relazione tra omeostasi energetica e meccanismo edonico (slide 11) Nell’uomo i pathway omeostatici interagiscono con i circuiti del piacere e della ricompensa, ciò offre una possibile spiegazione sui fattori che ci spingono a mangiare. Questa relazione è stata dimostrata sia a livello molecolare che a livello comportamentale. A livello molecolare si è visto che uno dei siti in cui l’ormone MCH agisce è il nucleo accumbens, che si sa essere coinvolto nei meccanismi edonici. Il nucleo accumbens integra i segnali inviati dall’ipotalamo laterale con informazioni sensoriali e comportamentali e origina un pathway GABAergico, che disinibisce i neuroni LHA, favorendo così l’assunzione di cibo. Si tratta di un meccanismo di feed-back positivo. A livello comportamentale ,invece, si è visto che cibi piacevoli, quando si è affamati, diventano spiacevoli, quando si è sazi. Regolazione dell’appetito: dallo stomaco al SNC Lamorte Sara & Longo Angela Omeostasi delle riserve energetiche Esistono meccanismi fisiologici per mantenere costanti i depositi energetici in risposta a: ¾ possibilità di accesso al cibo ¾ richieste di spese energetiche Lamorte Sara Regolazione dell’omeostasi energetica Cell, Obesity Wars.. Area del SNC coinvolta nella regolazione dell’appetito Ipotalamo Clinical Endocronology, Appetite regulation.. Come il SNC integra i diversi segnali afferenti Insulina Leptina CCK GLP-1 PYY3-36 Ghrelina SAZIETA’ FAME Nature, Genetics.. CCK e GLP-1 CCK GLP-1 Nervo vago Nucleo del tratto solitario Nucleo paraventricolare Ipotalamo laterale Assunzione di cibo Clinical Endocronology, Appetite regulation.. Neuropeptidi prodotti dai neuroni primari Neuropeptidi anoressigenici: prodotti dai neuroni Pomc/Cart in seguito a segnali di sazietà, inibiscono l’assunzione di cibo α-MSH: melanocyte stimulating hormone Cart: cocaine and amphetamine regulated transcript Neuropeptidi oressigenici: prodotti dai neuroni Npy/AgRP in seguito a segnali di fame, stimolano l’assunzione di cibo AgRP: agouti related protein Npy: neuropeptide y MCH: melanin concentrating hormone Orexina Modello “DUAL CENTER” (Stellar,1954) ANORESSIA OBESITA’ Nature, Genetics.. “ Saziety Center ” Nature, Genetics.. “ Feeding Center ” Cell, Obesity Wars.. Relazione tra omeostasi energetica e meccanismo edonico A livello molecolare: Neuron, The need to feed.. A livello comportamentale
Scaricare