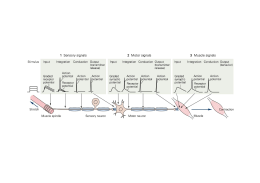
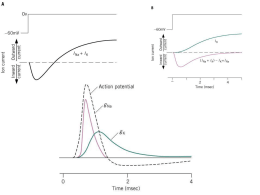
4. Generale Le Sinapsi e Integrazione Neuronale Prof. Carlo Capelli Fisiologia Generale e dell’Esercizio Facoltà di Scienze Motorie Università degli Studi di Verona Obiettivi • Definizione e struttura della sinapsi chimica • Sinapsi chimiche rapide e lente, diffuse e discrete • Sinapsi colinergiche (placca neuromuscolare) e adrenergiche • Meccanismi pre e post sinaptici (EPSP; IPSP) • Principali neurotrasmettitori centrali e periferici • Sinapsi elettriche Definizione 1. E’ una giunzione cellulare attraverso la quale si trasmettono in segnali da una cellula all’altra (neuroni, neuroni cellule tessuti eccitabili) 2. Componenti principali: membrana presinaptica, membrana postsinaptica 3. Due tipi di sinapsi: chimiche ed elettriche Sinapsi elettriche 1. 2. 3. 4. 5. 6. L’informazione si trasmette mediante uno scambio di ioni tra le cellule attraverso canali di membrana di congiunzione a bassa resistenza Le membrane pre e post-sinaptiche sono congiunte per mezzo di proteine che danno origine alle cosiddette giunzioni strette (gap junctions) Ogni semicanale, o connessone, è formato da sei sub unità proteiche (connessine) Nell’uomo sono frequenti nel tessuto muscolare miocardico e liscio permettendo una rapida diffusione dell’onda di depolarizzazione La trasmissione elettrica può avvenire nelle due direzioni I canali consentono anche il passaggio di molecole più grandi (AMPc). Servono anche a trasmettere segnali metabolici e di crescita Il Connessone Connessina (26 - 70kDa) Giunzioni strette Proprietà dell gap junctions Sinapsi Chimiche 1. 2. 3. 4. 5. 6. Una sostanza rilasciata dal neurone presinaptico (neurotrasmettore) per esocitosi è rilasciata nella fessura sinaptica e passa il segnale alla cellula postsinaptica Sinapsi assosomatiche, assodendritiche, assoassoniche, en passant Sinapsi colinergiche, adrenergiche, etc, etc Trasmissione sinaptica chimica rapida: il neurotrasmettitore (basso peso molecolare) rilasciato per esocitosi da vescicole poste in prossimità della membrana presinaptica si accoppia rapidamente ai recettori postsinaptici Trasmissione sinaptica lenta: rilascio di neurotrasmettitore (alto peso molecolare) da vescicole di maggiori dimensioni che si legano a recettori postsinaptici associati ad una proteina G membranaria Il legame del neurotrasmettitore altera la conduttanza di membrana ed il potenziale post sinaptico Struttura generale della sinapsi chimica Trasmissione rapida e lenta Rapida Lenta Meccanismi presinaptici 1 • Sintesi ed accumulo di neurotrasmettitore • Nel bottone terminale si accumulano le vescicole che contengono quantità fisse (quanti) di neurotrasmettitore • Le vescicole sono sequestrate in questa zona congiunte all’actina del citoscheletro tramite la sinapsina I • La congiunzione è controllata da un meccanismo di fosforilazione dipendente dal sistema calmodulina-Ca++ • la fosforilazione della sinapsina I svincola la vescicola dal legame e le permette la liberazione del neurotrasmettitore in risposta all’arrivo del PA Meccanismi presinaptici 2 • Liberazione del neurotrasmettitore • L’arrivo del PA nel bottone sinaptico attiva canali del Ca++ voltaggio dipendenti • Ca++ entra transitoriamente nel bottone terminale • Il breve aumento della concentrazione intracellulare locale di Ca++ provoca la fusione delle vescicole in zone attive della m. presinaptica ed il rilascio del neurotrasmettitore mediante esocitosi • La quantità di neurotrasmettitore liberate dipende dalla concentrazione di Ca++ nel bottone terminale e dal numero di vescicole disponibili. Riutilizzazione dei neurotrasmettitori-ACh • Reuptake del neurotrasmettitore, riutilizzazione o degradazione locale • Riutilizzo del neurotrasmettitore • Es.: ACh è formata da acetato e colina • Dopo liberazione, ACh è idrolizzata nei due componenti dall’enzima acetilcolinesterasi • La colina ricaptata riforma ACh unendosi all’acetil-CoA durante una reazione catalizzata dall’enzima colina acetiltransferasi (ChAT) Riutilizzazione dei neurotrasmettitori-NE • Reuptake di NE nel terminale presinaptico • Riutilizzo o degradazione del neurotrasmettitore • NE è immagazzinata di nuovo o degradata dalla monoammino ossidasi (MAO) o dalla catecol-Ometil transferasi (COMT) presente nel bottone terminale Meccanismi postsinapici 1 1. 2. 3. 4. 5. Accoppiamento nel neurotrasmettitore con canali specifici Apertura di canali controllati chimicamente Il flusso ionico procura variazioni graduali di voltaggio: potenziale postsinaptico (PP) PP: variazioni di voltaggio del PMR postsinaptico localizzate e non propagate che provocano correnti ioniche determinate da variazioni di conduttanza ionica Queste varazioni possono favorire (depolarizzazione) o inibire (iperpolarizzazione) la probablilità di generare un PA Meccanismi postsinaptici 2 - EPSP 1. 2. 3. 4. 5. Sinapsi eccitatorie: aumento di flusso di ioni positivi all’interno con conseguente depolarizzazione Potenziale postinaptico eccitatorio (EPSP) Aumento di gNa e/o di gK Il flusso di corrente causato dalla liberazione di un singolo quanto di neurotrasmettitore genere il cosiddetto potenziale postsinaptico unitario Nelle sinapsi eccitatorie si sommano per dare origine all’EPSP Meccanismi postsinaptici 3 - IPSP 1. 2. Sinapsi inibitorie: aumento di flusso di ioni positivi all’esterno o di ioni negativi (Cl-) all’interno con conseguente iperpolarizzazione Potenziale postinaptico inibitorio (IPSP) • I canali rimangono aperti sino a quando il neurotrasmettitore rimane legato al recetttore • I meccanismi di chiusura sono solitamente legati su sistemi di secondo messaggero Sinapsi chimiche diffuse e discrete • Sinapsi discrete: il neurotrasmettitore è rilasciato in punti specifici e discreti del terminale presinaptico chiamati zone attive • Sinapsi diffuse: la liberazione non è limitata alle zone attive • Hanno la forma di varicosità (sinapsi en passant) • Tipiche della componente simpatiche del SNA Neurotrasmettitori • Neurotrasmettitori a basso peso molecolare Basso peso molecolare Sintetizzati nei terminali presinaptici • Trasmettitori peptidici (neuropetidi) Fabbricati nel soma e convogliati mediante trasporto assonico al terminale sinaptico Neurotrasmettitori a basso peso molecolare-ACh • Acetilcolina SNC Placca neuromuscolare SNA: pre e post gangliari parasimpatico, pregangliari simpatico • Due recettori • Nicotinici • Muscarinici Recettori nicotinici • Recettori nicotinici 5 sub-unità β,γ ,δ e (2) α siti attivi) ACh si lega alle sub unità α Il canale si apre e permette il passaggio contemporaneo di sodio (interno) e potassio (esterno) Il risultato è una depolarizzazione di membrana Il canale ionico rimane aperto sino al distacco dell’ACh l’ACh è in seguito idrolizzata nella fessura sinaptica in colina e acetato dalla acetilcolinesterasi Questo è il recettore presente nella placca neuromuscolare Placca neuromuscolare Organizzazione e struttura • L’apertura dei canali genera localmente un potenziale di placca eccitatorio • Le correnti locali ioniche, se sufficienti, possono portare il PM a superare il potenziale soglia e indurre un PA Placca neuromuscolareRiassunto degli eventi Recettori muscarinici • Due tipi (M1 e M2) con 7 domini • Agiscono tramite una proteina G • M1: diminuzione gK, mediante fosfolipasi C, depolarizzazione • M2: aumenta gK per inibizione dell’adenilciclasi, iperpolarizzazione • Recettore M2 Neurotrasmettitori a basso peso molecolare-Ammine biogene • • • Ammine biogene: caratterizzate dalla presenza di un gruppo NH2 Un sottogruppo, le catecolammine, presenta un anello catecol Le catecolammine comprendono i trasmettitori noradrenalina (NE), adrenalina, dopammina (DA) Ammine biogene - Noradrenalina • • • • • ∀ ∀ La sintesi di NE è un processo labile epuò essere aumentata da meccanismi a breve e lungo termine (stress, p.e.) 80% ricaptato, 20% degradato da COMT Due gruppi di recettori: α (SNC e SNP) e β (SNP) a loro volta divisi in α1, α2, β1, ε β2 α1: β1: - SNC: aumenta gK, IPSP - SNP: i) α1 -A, corrente verso l’interno di Ca++ (nel muscolo liscio si ha contrazione); ii) α1 -B, DAG, innesco di una lunga serie di reazioni cellulari - tachicardia (cuore) - secrezione renina (rene) - tessuto adiposo (lipolisi) β2: - rilassamento muscolo liscio Recettori adrenergici e meccanismi a feedback Inibizione a feedback: autorecettori α2 • Autorecettori α2 • Quando aumenta la concentrazione di NE nella fessura sinaptica, sono attivati e la liberazione di NE è inibita Recettori adrenergici e meccanismi a feedback Eccitazione a feedback: autorecettori β2 • Autorecettori β2 • L’attivazione di questi recettori stimola la liberazione di NE Ammine biogene-Dopammina • • • • • • Tre sottotipi di recettori D1: accoppiati a proteina Gs attivano l’adenilciclasi D2 e D3: accoppiati a proteina Gp inibiscono l’adenilciclasi D2 iperpolarizza L’80% di DA è riutilizzato, il rimanente è degradato da COMT La trasmisione sinaptica della DA è influenzata da sostanza stupefacenti: - cocaina: inibisce il riassorbimento di DA nel terminale presinaptico - amfetamine: aumentano la liberazione nella fessura sinaptica Ammine biogene - Serotonina • • Serotinina o 5-idrossitriptamina (5HT), soprattutto nel tronco Diversi recettori: • 5-HT1A: aumenta gK, IPSP, tramite AMPc • 5-HT1C: aumenta kCl, IPSP, tramite IP3 • 5-HT2: diminuisce gK, EPSP, tramite IP3 • 5-HT3: aumento gK e gNa, EPSP Amminoacidi-GABA • • 1. 2. • Acido gamma ammino butirrico (GABA), potente inibitore Due sottotipi di recettori: GABAA: aumento gCl, IPSP. L’aumento di gCl è facilitato dalle benzodiazepine GABAb: aumento gK, IPSP, AMPc La trasmissione sinaptica tramite GABA è terminata dal riassorbimento e trasporto del GABA nelle cellule gliali Amminoacidi-Glutammato • • • • Tre sottotipi di recettori: Cainato: aumento gk e gNA, EPSP Quisqualato: aumento gK e e gNA, EPSP N-metil-D-aspartato (NMDA) : aumento gCa, recettore è bloccato da Mg++ quando la membrana è a riposo ed è sbloccato dalla depolarizzazione di membrana Quindi è regolato sia chimicamente sia dal voltaggio Neurotrasmettitori e recettori-Sinossi Neurotrasmettitore Recettore Conduttanza di membrana Potenziale di membrana Secondo messaggero Acetilcolina (ACh) Nicotinico Muscarinico M1 Muscarinico M2 Aumenta gNa, gK Diminuisce gK Aumenta gK EPSP EPSP IPSP IP3 e DAG AMPc EPSP (?) IPSP AMPc AMPc Dopammina (DA) D1 D2 Noradrenalina α1 α2 β1 β2 Serotonina Aumenta gK Diminuisce gCa IPSP (SNC) Contrazione (SNP) [tachicardia] [dilatazione] IP3/DAG AMPc AMPc AMPc 5-HT1A 5-HT1B 5-HT1C 5-HT1D 5-HT2 5-HT3 Aumenta gK IPSP AMPc Aumenta gCl IPSP IP3 Diminuisce gK Aumenta gK/gNa EPSP EPSP IP3 Glutammato Cainato Quisqualato NMDA Aumenta gNa, gK Aumenta gNa, gK Aumenta gCa EPSP EPSP EPSP GABA GABA-A GABA-B Aumenta gCl Aumenta gK IPSP IPSP AMPc (?) Neuropetidi ad alto peso molecolare Colocalizzazione di trasmettitori a basso peso molecolare e di neuropetidi Trasmettitori a basso peso mollecolare Neuropeptide ACh Peptide vasoattivo intestinale NE Somatostatina Encefalina Neurotensina DOPA Colecistochinina Encefalina Adrenalina (E) Encefalina 5-HT Sostanza P Ormone rilasciante la tirotropina • Neurotrasmettitori formati da catene aminoacidiche • Sono formati nel soma e derivano come prodotti di grosse poliproteine • I peptidi sono poi trasportati nella zona terminale dove, una volta secreti, modulano l’attirvità dei neurotrasmettitori: colocalizzazione • Oppiacei • met-encefalina, leu-encefalina, dinorfina, beta endorfinaDerivano da tre polipeptidi: proencefalina, prooppiomelanocortina, prodinorfina • Recettori oppioidi: recettori mu (betaendorfina), recettore delta (leu-encefalina, met-encefalina), recettore kappa (dinorfina) • Regolazione percezione dolore • Ossido nitrico (NO) • Oltre all’attività vasodilatatrice, ha diverse funzioni regolatorie Integrazione neuronale • Ogni Neurone deve ricevere un input (eccitatorio, inibitorio), integrarlo e trasformare il risultato modulando la propria frequenza di generazione dei PA • Decodificazione dell’informazione: Integrazione dei segnali in arrivo • Codificazione dell’informazione: modulazione della frequenza di generazione dei PA l’informazione trasmessa consiste nel numero di impulsi nell’unità di tempo: codice in frequenza Decodificazione dell’informazione – Sommazione temporale • La somma (spaziale e temporale) dell’attività delle sinapsi eccitatorie ed inibitorie determina se un neurone genera PA o no e a quale frequenza 1. Sommazione temporale di EPSP • Se due EPSP generati dalla stessa sinapsi si succedono in tempi ravvicinati, si raggiunge PS e si genera PA Decodificazione dell’informazione – Sommazione spaziale 1. Sommazione spaziale di EPSP • Vari EPSP generati da diverse sinapsi si sovrappongono in tempi ravvicinati, si raggiunge PS e si genera PA Bibliografia • Fisiologia Generale ed umana, IV edizione, Rhoades R e Pflanzer R, Piccin editore, Padova • Capitolo 7- Organizzazione funzionale del sistema nervoso - Le sinapsi • Fisiologia dell’Uomo, autori vari, Edi.Ermes, Milano • Capitolo : Neurofisiologia generale (Capitolo 1.5)
Scaricare