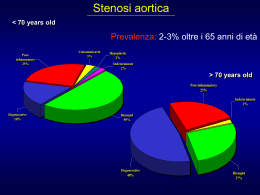
Stenosi valvolare aortica È caratterizzata dalla presenza di un’ostruzione al passaggio del flusso sanguigno dal ventricolo sinistro all’aorta Eziologia della stenosi aortica Congenita (con valvola tricuspide, bicuspide unicuspide) Acquisita A. Reumatica B. Calcifica (o degenerativa) C. Cause rare 1. Vegetazioni infettive ostruttive 2. Iperlipoproteinemia omozigote tipo II 3. Malattia di Paget dell’osso 4. Lupus eritematoso sistemico 5. Coinvolgimento reumatoide 6. Radiazioni o Stenosi aortica congenita Nei pazienti tra 15 e 65 anni, nel 60% dei casi si presenta con valvole bicuspidi, nel 10% unicuspidi (ostruzione molto grave nei neonati) e nel 25-30% tricuspidi (le cuspidi però sono in genere di diversa misura e presentano un certo grado di fusione) Stenosi aortica reumatica È caratterizzata dall’adesione e dalla fusione delle commissure e delle cuspidi. Interviene poi la calcificazione e l’orifizio aortico si riduce ad una piccola apertura triangolare o rotonda. Il cuore mostra spesso lesioni della valvola mitrale e la presenza di noduli di Aschoff nel miocardio Stenosi aortica calcifica (c. d. degenerativa) Si osserva sulle cuspidi la presenza di un infiltrato cellulare infiammatorio, depositi lipidici nella sede della lesione e nell’adiacenza della zona fibrotica. Questi pazienti presentano un’alta incidenza di fattori di rischio per coronaropatia aterosclerotica Cenni di fisiopatologia Con la riduzione dell’area valvolare aortica viene dispersa energia durante il passaggio del sangue dal ventricolo sinistro all’aorta. Il cuore compensa l’aumentato stress di parete ipertrofizzandosi Ipertrofia del ventricolo sinistro Poiché la stenosi aortica evolve lentamente, l’ipertrofia ventricolare rappresenta il principale meccanismo compensatorio del cuore per far fronte all’ostruzione dell’efflusso del ventricolo sinistro Disfunzione diastolica del V S È data dalla combinazione tra l’alterato rilasciamento miocardico con ridotta compliance e l’aumento della rigidità miocardica causato da alterazioni strutturali. Questa condizione determina un incremento della pressione telediastolica del ventricolo sinistro. La maggiore contrazione atriale sinistra determina una gittata sistolica adeguata Importanza della contrazione atriale La perdita di una contrazione atriale efficace, per la comparsa di fibrillazione atriale o di disturbi della conduzione atrio-ventricolare, determina un aumento della pressione media atriale, una riduzione della gittata cardiaca e può portare ad insufficienza cardiaca con edema polmonare Ulteriori meccanismi di compenso Quando l’ipertrofia del ventricolo sinistro non riesce a compensare da sola l’ostruzione all’efflusso ventricolare, il cuore fa ricorso al meccanismo di Frank-Starling (riserva di precarico) per mantenere la funzione sistolica Insufficienza cardiaca Si manifesta quando la stenosi aortica diventa progressivamente più grave, la gittata cardiaca rimane normale a riposo, ma non aumenta in proporzioni adeguate durante lo sforzo o non aumenta affatto (gittata cardiaca fissa). Con l’evoluzione verso l’insufficienza cardiaca si ha una riduzione della gittata cardiaca a riposo e tachicardia. Manifestazioni cliniche All’anamnesi i pazienti con stenosi congenita possono riferire il riscontro di un soffio fin dall’infanzia, i pazienti con stenosi reumatica riportano storia di febbre reumatica. La maggior parte dei pazienti, anche con stenosi severa, sono asintomatici. I sintomi maggiormente lamentati sono: angina pectoris, sincope, dispnea (da sforzo, ortopnea, parossistica notturna) e i sintomi relati all’insufficienza cardiaca. Sintomi L’angina pectoris è determinata da uno squilibrio tra la richiesta e l’apporto di ossigeno al miocardio, dovuto all’aumento della massa muscolare (ipertrofia) e delle pressioni ventricolari sinistre. La sincope si manifesta quando si crea una condizione tale da provocare una ridotta perfusione cerebrale. Quando compare a riposo è in genere dovuta ad una tachiaritmia ventricolare transitoria, a remissione spontanea. Quella che si presenta dopo sforzo può essere dovuta sia a vasodilatazione sistemica, in presenza di una gittata cardiaca inadeguata, sia alla comparsa di aritmie, o per entrambe le cause. Sintomi 2 La dispnea da sforzo, l’ortopnea, la dispnea parossistica notturna e l’edema polmonare acuto sono dovuti a diversi gradi di ipertensione venosa polmonare. La congestione venosa sistemica, con epatomegalia ed edema periferico, è dovuta all’aumentata pressione venosa sistemica e a ritenzione idrosalina. Auscultazione Nell’80-90% dei pazienti adulti con stenosi aortica severa è presente un IV tono di galoppo, un soffio eiettivo mesosistolico con rinforzo in telesistole spesso con uno sdoppiamento paradosso del II tono Ecocardiogramma L’ecocardiogramma con valutazione Doppler, quando correttamente eseguito, è molto utile per stimare non invasivamente il gradiente transvalvolare e l’area valvolare aortica. Quando non è possibile ottenere dati attendibili con l’eco transtoracico, può essere utile il ricorso all’ecocardiografia transesofagea Cateterismo cardiaco/angiografia È la tecnica migliore per uno studio accurato della stenosi aortica. Con tale metodica vengono misurate simultaneamente le pressioni del VS, dell’aorta ascendente e la gittata cardiaca. Si può inoltre calcolare l’area valvolare aortica. Con l’angiografia è possibile osservare la presenza ed il grado di estensione delle lesioni coronariche. Tale valutazione deve essere eseguita in tutti i pazienti >35 anni candidati alla correzione chirurgica. Prognosi Una volta manifestati i sintomi, la prognosi dei pazienti con stenosi aortica è molto infausta se non si interviene chirurgicamente. Il 5% dei pazienti con stenosi aortica grave muore per morte improvvisa Terapia Tutti i pazienti con stenosi aortica devono essere sottoposti a profilassi antibiotica contro l’endocardite batterica Se la valvulopatia è reumatica, occorre un’ulteriore profilassi contro la febbre reumatica ricorrente Terapia 2 I pazienti con stenosi aortica lieve o moderata raramente manifestano sintomi o complicanze e, in genere, non necessitano di alcuna terapia specifica. L’intervento chirurgico è indicato per i pazienti sintomatici con stenosi aortica grave. La sostituzione valvolare determina un miglioramento della sopravvivenza. L’ipertrofia del VS tende a regredire dopo l’intervento chirurgico Insufficienza aortica Condizione patologica in cui vi è un rigurgito di sangue dall’aorta al ventricolo sinistro durante la fase diastolica del ciclo cardiaco. Può essere acuta e cronica Eziologia dell’insufficienza aortica cronica Dilatazione della radice aortica Valvola bicuspide congenita Endocardite infettiva pregressa Reumatica In associazione ad altre malattie: Lesioni congenite (stenosi aortica sotto- o sopravavolare, DIV) Malattie del connettivo (S. di Marfan) Malattie autoimmuni (spondilite anchilosante, LES, artrite reumatoide) Aortiti ed arteriti Sifilide Patologia A seconda delle cause, le cuspidi valvolari possono mostrare ispessimento, accorciamento, lesioni commissurali o calcificazione. Indipendentemente dalle cause, il ventricolo sinistro è dilatato ed ipertrofico Fisiopatologia Se l’insufficienza aortica è lieve o moderata, il volume telediastolico del ventricolo sinistro è moderatamente aumentato e la pressione diastolica è di solito normale L’aumento del volume telediastolico è proporzionale all’entità del rigurgito e dipende dall’alterazione sistolica del VS Fisiopatologia 2 Infatti in presenza di alterata funzione sistolica, ogni aumento della quantità di sangue rigurgitato determina un incremento del volume telediastolico nel tentativo di mantenere la gittata sistolica adeguata Fisiopatologia 3 Nell’insufficienza aortica grave il volume rigurgitato è elevato ed il VS risponde dilatandosi. La dilatazione è proporzionale al volume rigurgitato. Ne consegue un aumento della gittata sistolica che determina ipertensione sistolica del VS che, a sua volta, comporta un aumento dello stress di parete (post-carico) il quale, come vedremo, può arrivare a determinare scompenso cardiaco Fisiopatologia 4 Infatti, continuando ad aumentare il postcarico (per la combinazione tra dilatazione ventricolare, ipertrofia e ipertensione sistolica) il ventricolo sinistro tenta di compensare utilizzando due meccanesmi: l’aumento del pre-carico e l’aumento della contrattilità miocardica Fisiopatologia 5 Quando viene raggiunto il limite della riserva di pre-carico (afterload mismatch) e/o la contrattilità miocardica si riduce, inizia il deterioramento della funzione sistolica, con progressione verso l’insufficienza cardiaca Sintomi All’anamnesi i pazienti con IA lieve o moderata non presentano in genere nessun sintomo specifico. Anche i soggetti con IA grave all’anamnesi possono essere asintomatici o lamentare soltanto pulsazioni al capo e palpitazioni Sintomi 2 I principali sintomi dell’IA grave derivano dall’aumentata pressione venosa polmonare e comprendono: dispnea da sforzo, ortopnea e dispnea parossistica notturna. Nel 20% dei pazienti si riscontra angina pectoris, anche se le coronarie sono normali Esame obiettivo Il polso arterioso è molto caratteristico e consiste in una brusca distensione con rapida salita e veloce discesa (polso di Corrigan) La pressione arteriosa sistolica aumenta, la pressione diastolica si riduce e i toni di Korotkoff possono essere udibili fino a 0 mmHg Auscultazione È udibile un soffio diastolico precoce ad alta frequenza È meglio apprezzato in regione parasternale sinistra, mettendo il paziente seduto con il busto inclinato davanti e in espirazione forzata Ecocardiogramma Nei pazienti che presentano anche un soffio diastolico di Austin-Flint l’ecocradiogramma può escludere la presenza di una insufficienza mitralica associata. Le dimensioni del VS sono aumentate e molto spesso si riscontra dilatazione dell’aorta ascendente e dell’atrio sinistro. Qualora non si ottengano dati soddisfacenti con l’ecocardiogramma transtoracico, si può utilizzare quello tarnsesofageo Cateterismo cardiaco/angiografia Anche se sia l’esame obiettivo che l’ecocardiogramma permettono di arrivare ad una diagnosi sicura, questa indagine permette di misurare le pressioni intracavitarie e intravascolari e la gittata cardiaca. Con l’angiografia è possibile osservare l’eventuale presenza ed il grado di estensione delle lesioni coronariche. Tale valutazione deve essere eseguita in tutti i pazienti >35 anni candidati alla correzione chirurgica Prognosi I pazienti con IA lieve che non progredisce verso stadi più avanzati della malattia hanno buona prognosi ed una aspettativa di vita normale. Per questi pazienti il rischio maggiore è l’endocardite infettiva che comporta un ulteriore danno valvolare. Anche i pazienti con IA moderata hanno buona prognosi. Se tuttavia la malattia progredisce la mortalità a 10 anni è del 15% Prognosi 2 I pazienti con IA grave possono rimanere asintomatici per un periodo di tempo molto lungo. La comparsa dei sintomi è in genere legata alla disfunzione del VS a riposo. Una volta che compaiono i sintomi, le condizioni del paziente si aggravano velocemente. La morte improvvisa, in pazienti asintomatici, può aversi quando il VS è molto dilatato (dimensioni telediastoliche del VS > di 80 mm). Terapia Tutti i pazienti con IA necessitano di profilassi antibiotica per prevenire l’endocardite infettiva. Nell’IA di origine reumatica è necessaria anche la profilassi antibiotica per prevenire la cardite reumatica. L’IA lieve e quella moderata non richiedono alcuna terapia, anche se nella forma moderata i pazienti dovrebbero evitare sforzi fisici intensi Terapia 2 I pazienti con IA grave, anche se asintomatici e con normale funzione del VS, dovrebbero essere trattati con calcio-antagonisti a meno che non sussistano controindicazioni specifiche. I pazienti sintomatici con IA grave necessitano di trattamento medico e chirurgico. La terapia medica prevede l’uso di digitale, diuretici e vasodilatatori. Se il paziente è in classe NYHA III o IV va aggiunto anche l’ACE-inibitore. Terapia 3 I pazienti con IA cronica grave devono essere sottoposti ad intervento chirurgico di sostituzione valvolare. Il momento più corretto per intervenire chirurgicamente è prima che intervenga un’alterazione del VS irreversibile. Valori molto bassi di frazione d’eiezione potrebbero rendere l’intervento chirurgico inadatto! Dopo l’intervento i pazienti presentano un miglioramento della sintomatologia, un aumento della frazione d’eiezione e una riduzione del volume ventricolare
Scaricare