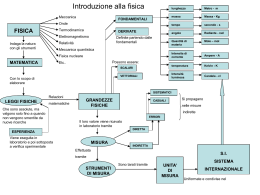
Grandezze colligative Ebullioscopia Crioscopia Pressione osmotica Innalzamento del punto di ebollizione di una soluzione rispetto a quello del solvente puro; abbassamento del punto di congelamento della soluzione rispetto a quello del solvente puro; pressione osmotica: la variazione dipende dal numero di particelle del soluto (in genere non dalla loro natura) e dalla natura del solvente (effetto aumenta se soluto ionico,dissociabile…) T°C 100°C 70°C 0°C -5°C S1 S1 S1 S1 S2 La temperatura di ebollizione della soluzione supera quella del solvente puro in funzione della quantità di soluto presente (non della natura):varia con solvente T°C 100°C 70°C 0°C -5°C S1 S1 S1 S1 S2 temperatura di congelamento della soluzione è inferiore a quella del solvente puro in funzione della quantità di soluto presente (non della natura):varia con solvente A parità di numero di particelle le temperature variano in funzione del solvente 82 S1 -1 71 82 84 86 S1 S1 S1 -1 80°C S1 0°C -2 70°C S2 10°C S2 7 -3 A parità di solvente, la variazione di temperatura di ebollizione e di solidificazione varia con il numero di particelle di soluto (non con la natura) A parità di numero di particelle le temperature variano in funzione del solvente 82 S1 -1 82 84 86 S1 S1 S1 -1 80°C S1 0°C -2 70°C S2 10°C 71 S2 7 -3 A parità di solvente, la variazione di temperatura di ebollizione e di solidificazione varia con il numero di particelle di soluto (non con la natura) T°C S1 S2 Numero particelle Applicazioni-conseguenze relative alle proprietà colligative Liquido anticongelante:soluzione che abbassa il punto di congelamento in proporzione alla concentrazione in particelle del soluto e innalza il punto di ebollizione:usato per evitare congelamento dell’acqua del radiatore in inverno e rendere più difficile ebollizione durante l’estate Per ritardare la formazione di ghiaccio sulle strade in inverno si sparge sale L’acqua dolce (laghi,corsi d’acqua) gela più facilmente dell’acqua salata dei mari Le piante che possono concentrare la loro linfa possono resistere meglio alle basse temperature che con il congelamento farebbero aumentare il volume del liquido nei vasi , tessuti , della pianta favorendone la disgregazione: per questo si genera una selezione latitudinale e altitudinale Verifica della concentrazione denunciata di liquidi vari, ricerca natura soluto mediante calcolo del peso molecolare Dt = Km = K * g.soluto * 1000 / peso molecolare * g.solvente Misurando la variazione di temperatura di ebollizione o congelamento di una soluzione rispetto al solvente puro si può determinare la concentrazione del soluto, la sua natura, con le formule inverse Se soluzione denunciata al 50% bolle a 95° significa che in realtà è solo 25% circa m = Dt / K pm = K * g.soluto*1000 / Dt * g.S 100% 50% 100% t°C 100°C 90°C 80°C S2 S1 100°C 90°C 80°C % 0 50 100 pila pila Sostanze solubili in acqua( zucchero, alcool..) non rendono conduttrice la soluzione (lampada spenta..):si definiscono non elettrolitiche Sostanze solubili in acqua( acidi, sali, basi.) rendono conduttrice la soluzione (lampada accesa..):si definiscono elettrolitiche soluto Due recipienti separati da membrana permeabile a soluto e solvente mantengono il medesimo livello:principio vasi comunicanti Il soluto introdotto nella soluzione diffonde attraverso i pori della membrana e dopo un certo tempo la concentrazione è uguale in entrambi i recipienti soluto Pressione idrostatica Pressione osmotica Due recipienti separati da membrana semipermeabile,cioè permeabile solo alle piccole molecole del solvente,portano il livello del liquido a valori diversi nei due rami se viene introdotto in uno del soluto La pressione che si oppone alla pressione idrostatica del ramo con soluto si definisce pressione osmotica Soluzioni con concentrazioni uguali o diverse Emazia e plasma isotoniche ipertonica plasma ipotonica emazia L’acqua esce dalla emazia che si riduce di volume Ipertonica emazia ipotonica plasma L’acqua entra nella emazia che si rigonfia e può disgregarsi Animali che vivono in ambiente acquatico devono essere in equilibrio osmotico con ambiente esterno:se questo varia anche gli animali devono variarlo o cercare altro ambiente:es.migrazioni dei salmoni dalla sorgente al mare e ritorno alla sorgente Le piante assorbono acqua dall’ambiente:se la concentrazione interna è superiore a quella del liquido esterno l’assorbimento può avvenire; in caso contrario è impedito: conseguenza diretta:solo certe piante (es.alghe) possono vivere nell’acqua salata e altre in terreni ricchi di sali (selezione)
Scaricare