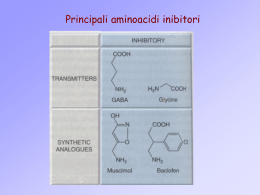
Farmaci antiepilettici Epilessie Epilessie • Manifestazioni accessuali ricorrenti, clinicamente polimorfe, dovute ad una scarica simultanea ed eccessiva di neuroni cerebrali. In base all’eziopatogenesi si distinguono: - epilessie idiopatiche - epilessie secondarie o sintomatiche Classificazione • Crisi parziali - semplici - complesse - secondariamente generalizzate • Crisi generalizzate - convulsive, tonico-cloniche o del tipo Grande Male - assenze semplici o del tipo Piccolo Male - miocloniche Farmaci antiepilettici Antiepilettici tradizionali Nuovi antiepilettici • • • • • • • • • • • • • Fenobarbital Fenitoina Carbamazepina Acido valproico Etosuccimide Benzodiazepine Vigabatrin Gabapentina Lamotrigina Felbamato Oxcarbazepina Tiagabina Topiramato Farmaci antiepilettici Meccanismo generale d’azione • riducono la diffusione dell’eccitamento da un focus epilettogeno che scarica in modo anormale ai tessuti cerebrali adiacenti. Dal punto di vista neurochimico: • stabilizzano le membrane neuronali, bloccando i canali del sodio e del calcio • possono potenziare la neurotrasmissione inibitoria mediata dal GABA • possono ridurre la neurotramissione eccitatoria mediata dagli aminoacidi eccitatori Modelli di studio dei farmaci antiepilettici Modelli di epilessia generalizzata primaria • Elettroshock • Convulsioni indotte da pentilentetrazolo • Convulsioni indotte da antagonisti del recettore GABAA (bicucullina e picrotossina) • Convulsioni indotte da antagonisti del recettore della glicina (stricnina) • Convulsioni indotte da agonisti dei recettori degli aminoacidi eccitatori (N-metil-D-aspartato o acido cainico) Modelli di epilessia parziale (focale) con secondaria generalizzazione • Kindling elettrico • Iniezione focale di agenti chimici FENOBARBITAL Meccanismo d’azione • aumenta l’attività inibitoria del GABA legandosi ad un sito recettoriale collegato al complesso del GABA-A e determinando l’apertura dei canali del cloro Farmacocinetica • assorbimento lento ma completo, poco legato alle proteine plasmatiche (4060%) • metabolizzato per via ossidativa; lunga emivita (60-180 ore) • potente ed aspecifico induttore degli enzimi microsomiali epatici implicati nel metabolismo di numerosi farmaci FENOBARBITAL Effetti indesiderati • ACUTI: sedazione, nistagmo, atassia, disartria, irritabilità ed iperattività nei bambini, agitazione e confusione nell’anziano • CRONICI: anemia megaloblastica, osteomalacia Uso clinico • crisi parziali e crisi generalizzate tonico-cloniche • efficace nella profilassi e terapia delle convulsioni febbrili nei bambini • livelli ematici terapeutici: 15-40 g/ml FENITOINA Meccanismo d’azione • blocca i canali del sodio voltaggio-dipendenti (prolunga l’inattivazione dei canali del sodio, limitando la scarica neuronale ripetitiva o ad alta frequenza), stabilizzando la membrana neuronale Farmacocinetica • assorbimento lento, non sempre completo • elevato grado di legame alle proteine plasmatiche • metabolizzata mediante para-idrossilazione; questa via metabolica è saturabile ed il farmaco ha una cinetica dose-dipendente; emivita plasmatica di circa 20-30 ore • induce gli enzimi microsomiali responsabili del metabolismo di numerosi farmaci Fenitoina: cinetica di saturazione FENITOINA Effetti indesiderati • ACUTI: nistagmo, disartria, atassia, diplopia, vertigini • CRONICI: disturbi gastrointestinali, acne, iperplasia gengivale, irsutismo, osteomalacia, anemia megaloblastica, neuropatia periferica • IDIOSINCRASICI: eritemi cutanei (sindrome di Stevens-Johnson), agranulocitosi Uso clinico • crisi parziali e crisi generalizzate tonico-cloniche • livelli ematici terapeutici: 10-20 g/ml CARBAMAZEPINA Meccanismo d’azione • blocca i canali del sodio voltaggio-dipendenti (prolunga l’inattivazione dei canali del sodio, limitando la scarica neuronale ripetitiva o ad ad alta frequenza), stabilizzando la membrana neuronale Farmacocinetica • assorbimento lento, non sempre completo • poco legato alle proteine plasmatiche (75%) • metabolizzato a 10,11-epossido, attivo • emivita tra 15 e 20 ore • induce gli enzimi microsomiali coinvolti nel metabolismo di numerosi farmaci, incluso il proprio (autoinduzione) CARBAMAZEPINA Effetti indesiderati • ACUTI: diplopia, vertigine, atassia, disartria • CRONICI: turbe gastrointestinali, ritenzione idrica con iponatremia • IDIOSINCRASICI: eritemi cutanei, discrasie ematiche (leucopenia, trombocitopenia, anemia aplastica) Uso clinico • crisi parziali (soprattutto quelle complesse) e crisi generalizzate tonicocloniche • efficace anche nella nevralgia del trigemino e nei disturbi bipolari, come alternativa al litio • livelli ematici terapeutici: 4-12 g/ml ACIDO VALPROICO Meccanismo d’azione • riduce le correnti del calcio a bassa soglia (correnti T) nei neuroni talamici • blocca i canali del sodio voltaggio-dipendenti (prolunga l’inattivazione dei canali del sodio, limitando la scarica neuronale ripetitiva o ad ad alta frequenza), stabilizzando la membrana neuronale • inibisce la GABA-transaminasi e la semialdeide succinico-deidrogenasi, innalzando i livelli di GABA Farmacocinetica • assorbimento rapido, esteso metabolismo, emivita breve (10 ore) ACIDO VALPROICO Effetti indesiderati • ACUTI: disturbi gastrointestinali, sedazione, atassia, tremore • CRONICI: epatotossicità, iperammoniemia Uso clinico • assenze semplici tipo Piccolo Male • in associazione o in alternativa agli altri antiepilettici nelle crisi parziali e nelle crisi convulsive generalizzate • nei disturbi bipolari, come alternativa al litio • livelli ematici terapeutici: 50-100 g/ml ETOSUCCIMIDE Meccanismo d’azione • riduce le correnti del calcio a bassa soglia (correnti T) nei neuroni talamici Effetti indesiderati • disturbi gastrointestinali e sul SNC Uso clinico • assenze semplici tipo Piccolo Male • dosaggio: 500-1500 mg/die • livelli ematici terapeutici: 40-80 g/ml BENZODIAZEPINE Meccanismo d’azione • potenziano la trasmissione GABAergica Uso clinico • Clonazepam: assenze e crisi miocloniche • Diazepam: stato di male epilettico • Lorazepam: stato di male epilettico NUOVI ANTIEPILETTICI Vigabatrin • inibisce la GABA-transaminasi Gabapentina • aumenta il rilascio del GABA Lamotrigina • blocca i canali per il sodio Felbamato • blocca i recettori NMDA del glutammato Oxcarbazepina • blocca i canali per il sodio Tiagabina • inibisce la captazione del GABA Topiramato • blocca i canali per il sodio, potenzia la trasmissione GABA-ergica ed antagonizza i recettori per il glutammato Criteri generali di terapia antiepilettica (1) INIZIO DELLA TERAPIA • La terapia deve iniziare subito dopo la prima crisi riconosciuta come epilettica SCELTA DEL FARMACO • Crisi parziali e generalizzate tonico-cloniche - carbamazepina, fenitoina, acido valproico o fenobarbital - nelle forme resistenti si possono associare i nuovi antiepilettici vigabatrin, gabapentin, lamotrigina o felbamato • Assenze semplici - acido valproico, etosuccimide • Trattamento di forme particolari - Assenze atipiche, miocloniche ed atoniche: acido valproico o clonazepam - Spasmi infantili o Sindrome di West: ACTH - Sindrome di Lennox-Gastaut: felbamato - Stato di male: diazepam o lorazepam e.v. fenitoina o fenobarbital e.v. anestesia generale con barbiturici ad azione rapida - Convulsioni febbrili: fenobarbital o acido valproico Criteri generali di terapia antiepilettica (2) MONOTERAPIA O POLITERAPIA • Il trattamento si inizia con un solo farmaco; in caso di mancata risposta si prova un altro farmaco; in caso di ulteriore insuccesso si ricorre alla politerapia TERAPIA IN GRAVIDANZA • La terapia deve essere continuata durante la gravidanza, ma deve essere considerata la potenziale teratogenicità dei farmaci antiepilettici, in particolare fenitoina (sindrome fetale da idantoina), acido valproico e carbamazepina SOSPENSIONE DELLA TERAPIA • Se il paziente non ha presentato crisi per parecchi anni (almeno 2-5 anni) si può gradualmente (2-3 mesi) sospendere il trattamento PROFILASSI FARMACOLOGICA • Prevenzione dell’epilessia post-traumatica con basse dosi di fenobarbital o fenitoina Criteri generali di terapia antiepilettica (3) UTILITA’ E LIMITI DEL MONITORAGGIO PLASMATICO • La misurazione dei livelli ematici di equilibrio dei farmaci antiepilettici può essere utile per individualizzare lo schema di dosaggio: - all’inizio del trattamento, quando si sia raggiunto lo “steady-state” - in caso di inefficacia della terapia - in caso di effetti indesiderati - in caso di politerapia - in tutte quelle condizioni che possono modificare l’eliminazione dei farmaci antiepilettici (associazioni con altri farmaci, malattie epatiche e renali, ecc.) • La misurazione è inutile: - in caso di efficacia della terapia - nei giorni immediatamente successivi all’inizio del trattamento
Scaricare