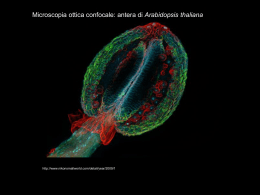
Il controllo di qualità in Micobatteriologia Dr. Claudio Piersimoni Gruppo di Lavoro Micobatteri AMCLI Firenze, 19-22 gennaio 2009 Concetti generali • Il Controllo di Qualità (CQ) valuta la performance di un prodotto correlandola all’obbiettivo atteso. In caso di discrepanze, promuove azioni per individuare le cause e porre rimedio al deficit riscontrato. Il Controllo di Qualità in Microbiologia • Metodi e procedure diagnostiche – Adozione – Formalizzazione (manuali) • Verifica e validazione dei test – Controllo di qualità interno • • • • Refertazione (tracciabilità ed archiviazione) Formazione del personale Valutazione esterna di qualità (Proficiency) Individuazione degli errori di laboratorio – Contaminazioni crociate Metodi e procedure diagnostiche Campioni Reagenti Strumenti Refertazione Selezione dei pazienti Criteri di adozione Manutenzione Compatibilità clinica Raccolta Stoccaggio Verifiche periodiche Tempi Trasporto Scadenza Numero Growth tests Quantità Qualità Errori di segreteria Decontaminazione • Monitorare regolarmente la percentuale di campioni inquinati. Valori fra il 2 ed il 5% sono accettabili, mentre percentuali inferiori o superiori indicano rispettivamente una decontaminazione troppo energica o troppo blanda ovvero una incompleta fluidificazione. Cernoch et al. Cumitech 16A, ASM 1994. Microscopia • Le variazioni di positivià vanno analizzate e correlate con la tipologia dei pazienti (extracomunitari in particolare) • Aumento di casi microscopicamente positivi e negativi alla coltura (se non provenienti da pazienti in terapia) • Presenza di casi microscopicamente positivi per presenza di AFB contaminanti (acqua, liquidi di lavaggio di endoscopi) senza un corrispettivo clinico • Rischi di cross-contaminazione usando coloratori automatici dotati di cestelli portavetrini Microscopia • Ogni nuovo lotto di coloranti deve essere controllato con vetrini negativi e positivi. • Vetrini positivi devono essere verificati da un secondo operatore. Questo è fortemente raccomandato se si utilizza la colorazione in fluorescenza o, in alternativa, eseguire un sovrastain con Z-N. Terreni di coltura e test di sensibilità • Ogni nuovo lotto di terreni va sottoposto a growth test con i seguenti ceppi di riferimento: – Myc. tuberculosis H37Rv ATCC 27294 – Myc. kansasii ATCC 12478 – Myc. avium ATCC 15769 – Myc. fortuitum ATCC 6841 • Il test di sensibilità per MTB prevede l’uso di ceppi di controllo: – Myc. tuberculosis H37Rv ATCC 27294 – I ceppi di Myc. tuberculosis monoresistenti (ATCC 35820, 35822, 35838, 35837, 35828) non sono raccomandati Formazione del personale • • • • • Addestramento Formazione continua Assegnazione stabile (rotazione lunga) Motivazione (job satisfaction) Competenza Proficiency Coinvolge tutte le attività diagnostiche erogate – Microscopia – Decontaminazione/coltura – Identificazione – DST – Amplificazione VEQ disponibili in Italia • NEQAS del Centre Public Health Laboratory di Colindale, UK (distribuito in Italia da Oxoid) – 4 campioni x 3 invii annui • Quality Control for Molecular Diagnostics, Glasgow, UK (consociata ESCMID) – 10-12 campioni una volta all’anno • INSTAND,Frankfurt, D. Controllo di Qualità Nazionale Tedesco diffuso a tutti i paesi di lingua tedesca – 4-8 campioni x 2 invii annui • Biodev VEQ Regionale – 1 campione x 3 invii annui Il programma “Tuberkulosediagnostik“ INSTAND 8 slides for detection of AFB 5 specimens for cultural detection of AFB 6 specimens for detection of MTB-bacilli by DAT 5 specimens for DST of MTB-bacilli to first-line drugs 4 suspensions of atypical mycobacteria for identification VEQ disponibili in Italia Campo di applicazione NEQAS INSTAND QCMD BIODEV Microscopia Sì Sì No Sì Coltura Sì Sì No No No Sì No No No Sì No No Sì Sì Sì No Identificazione DST Amplificazione Contaminazioni crociate È un aspetto che trova sempre maggior spazio in letteratura. Raccomandazioni di carattere generale: J. Clin. Microbiol. 2003; 41: 2269-2270 – Operatori ordinati e metodici – Seminare i campioni microscopico-positivi da ultimi – Separare le aree di lavoro dedicate al trattamento dei campioni da quelle dedicate alle colture – Risultati di microscopia ed amplificazione – Tempo di detection – Correlazione clinica – Valutazione ceppi con spoligotyping Contaminazioni crociate Diagn. Microbiol. Infect. Dis. 1991; 14: 33-35 Raccomandazioni relative all’uso del Bactec 460 TB i. Cambiare spesso gli aghi e relativi tubi ii. Rimuovere i flaconi positivi iii. Non agitare o rovesciare i flaconi iv. Alternare i flaconi positivi con flaconi non inoculati v. Ruotare i flaconi al fine di far penetrare l’ago in punti diversi del setto di gomma vi. L’ultimo flacone di ogni serie deve essere un flacone non inoculato Contaminazioni crociate • Studio condotto dal 1993 al 2000 in 44 laboratori periferici mediante DNA fingerprinting (IS6110-based RFLP) • Prevalenza di falsi-positivi del 2.4 % • Incidenza dal 3.9% del 1993 all’1.1% del 2000. Contaminazioni crociate No.(%) of laboratories Characteristic w/o false-positive cultures with false-positive cultures <3,000 samples per yr. 0 (0) 9 (41) >3,000 samples per yr. 12 (100) 13 (59) Class II BSB 11 (92) 21 (91) BSB >5 years in use 6 (50) 12 (55) 70% alcohol disinfect. 3 (25) 13 (59) Bactec 460 TB in use 0 (0) 4 (18) Room size < 30 m2 3 (50) 7 (70) Contaminated buffer 0 (0) 8 (36) Contaminated equip. 0 (0) 7 (32) Conclusioni • Il laboratorio di micobatteriologia deve poter disporre di un controllo interno di qualità riguardante i più importanti aspetti della attività diagnostica: • Microscopia/amplificazione • Coltura • DST • Deve partecipare ad uno o più programmi di VEQ per tutti i livelli diagnostici praticati in laboratorio • Si sente la mancanza di un laboratorio di Riferimento Nazionale che organizzi e gestisca un programma completo di VEQ per l’intero paese
Scaricare