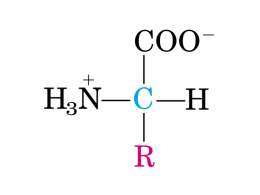
Scuola estiva Borsisti PLS Perugia 26 agosto-1 settembre 2007 Mariano Venanzi [email protected] Centro di Nanoscienze, Nanotecnologie e Strumentazione Motori molecolari Conversione di energia luminosa Catalizzatori chimici Canali ionici Mimicking the capability of biological systems to convert and transduce energy, synthesise specialist organic chemistry, create biomass, store information, recognise sense, signal, move, self-assemble and reproduce represents a significant challenge for the future. Christopher R. Lowe In ‘Nanobiotechnology: the fabrication and application of chemical and biological nanostructures’ • E’ un filamento di amminoacidi 1. Le attuali metodologie di sintesi peptidica permettono di sintetizzare facilmente una sequenza qualsiasi tra 5 e 50 amminoacidi. 2. Peptidi possono essere progettati in modo da assumere specifiche strutture secondarie (-eliche, -sheets, -hairpins,..) 3. Peptidi possono essere progettati in modo da avere specifiche proprietà di autoassemblaggio (regioni idrofiliche e idrofobiche) 4. Peptidi sono oggetti intrinsecamente chirali, che danno luogo a strutture supramolecolari chirali! 5. Peptidi possono essere facilmente funzionalizzati con gruppi intelligenti (adding smartness) - elica - sheet -elica Legame a Idrogeno ii+4 13 atomi per ciclo 3.5 residui per spira L’ -elica è stabilizzata da favorevoli interazioni dipolari. Tutti i legami peptidici puntano nella stessa direzione, dando a luogo a favorevoli interazioni dipolo-dipolo. Gli angoli di rotazione interna caratteristici di strutture elicoidali corrispondono a minimi dell’energia potenziale ma… la formazione di strutture ordinate congela molti gradi di libertà -elica Eliche formate da pochi amminoacidi non sono stabili in soluzione, allorchè vengano estratte dalla struttura proteica nativa J. Biochem. Vol. 129, pp. 971-977 (2001) ‘Foldamers are molecules that have well-defined and predictable folding properties in solution.’ S. H. Gellman, Accounts of Chemical Research 1998, 31, 173. Amminoacidi disostituiti C, Amminoacidi disostituiti C, Elica 310 -elica Eth 1 2 R 1 2 3k R0 6 R = interchromophoric distance Eexp 1 0 peptidi peptidi 1. Sintetizzare building-bloks molecolari funzionalizzati 2. Costruire per autoassemblaggio strutture nanometriche a 2- o 3- dimensioni sensibili a stimoli esterni 3. Deposizione ordinata in architetture molecolari indirizzabili (Patterning) Costruzione di strutture terziarie • forma complementare • interazioni deboli, non covalenti 16 amminoacidi con un pattern alternato di residui polari e non polari. Formano -sheet e -strand che per autoassemblaggio danno luogo alla formazione di nanofibre anfifiliche (idrofobiche all’interno, idrofiliche all’esterno). In opportune condizioni si ottengono idrogel ad alto contenuto di acqua. Hanno una testa polare (carica positivamente o negativamente) e una coda idrofobica (peptide surfactant). Per autoassemblaggio formano nanotubi e nanovescicole con un diametro di 30-50 nm, dando luogo a superstrutture reticolate. Peptidi ciclici in configurazione alternata D,L possono assemblarsi in strutture nanometriche cilindriche capaci di permeare membrane biologiche. 1. Una testa funzionalizzata per il riconoscimento di cellule o di biomolecole; 2. uno spaziatore per la separazione fisica dalla superficie; 3. una coda funzionalizzata per l’attacco covalente sulla superficie. • vettori terapeutici • rilascio di farmaci • sensori di proteine K. A. Williams, P. T. M. Veenhuizen, B. G. de la Torre, R. Eritja and C. Dekker Nature 420, 761(2002) Controllo programmato dell’espressione genica: Nanoparticelle d’oro funzionalizzate con un peptide (S18), che si lega su una proteina S per formare un complesso funzionale S- RNasi [Park et al., 2004; Audin et al., 2005]. Microarrays di fibrille peptidiche depositate su un substrato piano attraverso soft-litografia. a: Un elastomero (polidimetil silossano, PDMS) è usato per creare canali micrometrici che servono come guida per una soluzione peptidica che scorre per capillarità sul substrato di vetro. b: array lineari di argento ottenuti per incubazione sul peptide depositato su vetro di una soluzione 0.1 mM di AgNO3 per 48h a temperatura ambiente. c: Fluorescenza delle particelle di argento hexc Elettroni or energia D A hem D* (D+····A-) Dem Donore Stato a trasferimento di carica Accettore Elettronica Molecolare: unità logica di AND habs e- Input ottico D A Input chimico habs D A Off hem And Input ottico Input chimico Output 0 0 0 1 0 0 0 1 0 1 1 1 On Eliche peptidiche generano un campo elettrostatico direzionale (3.5 D per residuo)! Eliche peptidiche controllano la direzione del trasferimento elettronico = 40 D + A- D+ in 310-helix: k1 ≈ 30 k2 M.A. Fox, JACS (1997) - D+ Ain random coil: k1 ≈ k2 Il peptide assume una rigida struttura in elica 310 S Au S Aib-Aib-Aib-Aib-Trp-Aib-OtBu O Ha in sequenza un amminoacido fluorescente (Trp) e un gruppo disolfuro per legarlo covalentemente alla superficie d’oro (acido lipoico) Buche di diametro di 20-50 Å sono la struttura predominante. La profondità delle buche (2.4 Å) corrisponde allo step monoatomico di Au(111) Buche (holes) fasci peptidici regolarmente depositati sulla superficie (stripes). Ogni filare è separato di 7 nm. Stripes Il SAM peptidico inibisce la scarica agli elettrodi! Elettrodo nudo SAM peptidico SAM di undecatiolo La risposta corrente vs. potenziale applicato dipende dalle interazioni tra il SAM peptidico e la superficie elettrodica. SAM peptidico SAM di undecatiolo Elettrodo nudo SAM peptidico misto SAM a singolo peptide Uno switch molecolare fotoattivato! Emanuela Gatto, Ph.D. Thesis Premio Semerano 2007 Where Nature ends, there begins the man, that using the substances and the methods that Nature used, creates infinite species. Jean-Marie Lehn Supramolecular Chemistry. Concepts Perspective, VCH, Weinheim 1995 and
Scaricare