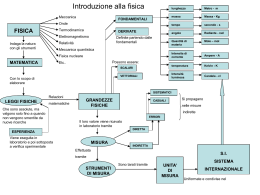
LE SOLUZIONI • Le soluzioni sono miscele uniformi, in cui la fase dispersa (soluto) è costituita da atomi, ioni o molecole di piccole dimensioni (>1nm). A seconda della fase disperdente (solvente) le soluzioni possono essere: 1) gassose (miscele) 2) liquide: il soluto può essere solido, liquido o gassoso 3) solide (leghe) • Durante il processo di solubilizzazione le molecole di soluto vanno ad occupare gli interstizi esistenti tra le molecole del solvente: si rompono i legami soluto-soluto e solvente-solvente e si formano interazioni nuove tra soluto e solvente. • Una regola per prevedere la solubilità di un soluto è: il simile scioglie il simile, dove simile si riferisce alle polarità relative. Similia similibus solvuntur olio glicole etilenico (CH2OHCH2OH) in acqua liquida Solubilità* degli alcoli in H2O a 20°C sostanza formula gsoluto 100g H2O metanolo CH3OH c. sol. etanolo CH3CH2OH c. sol. propanolo CH3CH2CH2OH c. sol. butanolo CH3(CH2)2CH2OH 7.4 pentanolo CH3(CH2)3CH2OH 2.7 pentano CH3(CH2)4CH3 insol. *massima concentrazione di soluto che si scioglie nel solvente ad una data T • l’acqua liquida solubilizza i composti ionici e polari mediante l’idratazione: gli ioni (o poli) positivi e negativi sono circondati da molecole di acqua attratte dalle cariche di segno opposto dei loro dipoli. ioni in soluzione acquosa soluto g/100g H O a 0°C g/100g H O a 20°C g/100g H O a 50°C g/100g H O a 100°C NaCl 35.7 36.0 37.0 39.8 NaOH 42 109 145 347 BaSO4 0.000115 0.00024 0.00034 0.00041 Ca(OH)2 0.185 0.165 0.128 0.077 2 2 2 2 Il processo di solubilizzazione può essere: - esotermico e quindi spontaneo (DH negativo) quando la differenza tra l’energia liberata dalla formazione dei legami soluto-solvente e quella consumata per la rottura dei legami soluto-soluto e solvente-solvente è positiva. Un innalzamento della T diminuisce la solubilità. - endotermico (DH positivo) quando tale differenza è negativa. Un innalzamento della T aumenta la solubilità. ossigeno saccarosio • in soluzione acquosa le molecole e i gruppi apolari tendono a raggrupparsi insieme (interazioni idrofobiche, micelle, proteine). formazione di micelle formazione enzima-substrato CONCENTRAZIONE DELLE SOLUZIONI Concentrazione (C)=quantità di soluto/quantità di soluzione Molarità (M)=moli soluto/V soluzione Molalità (m)=moli soluto/Kg solvente Frazione molare (X)=moli soluto/moli totali Percento in peso(p%)=(g soluto/g soluzione).100 Percento in volume(v%)=(ml soluto/ml soluzione).100 SOLUZIONI ACQUOSE DI GAS gas + solvente soluzione + calore (DH negativo) La solubilità di un gas in un liquido: • diminuisce all’aumentare della T; • a T=cost aumenta all’aumentare della pressione del gas sul liquido (legge di Henry dal nome del suo scopritore W.Henry 1775-1836): C=k.P k = coefficiente di solubilità k indica la solubilità del gas a P=1atm ed è specifico del sistema gas/solvente. Se il liquido è in equilibrio con una miscela gassosa la solubilità di ogni componente dipende da k e dalla pressione parziale di quel componente ed è indipendente da quella degli altri. applicazione medica: camera iperbarica, maschera di O2; • diviene molto alta se le interazioni gas-liquido danno origine a composti chimici: NH3g + H2O NH3 + H2O NH4+ + OH- Soluzioni acquose di gas soluto g/100g H O a 0°C g/100g H O a20°C g/100g H O a 50°C g/100g H O a100°C O2 0.0069 0.0043 0.0027 0 CO2 0.335 0.169 0.076 0 N2 0.0029 0.0019 0.0012 0 SO2 22.8 10.6 4.3 1.8 (a 90°C) NH3 89.9 51.8 28.4 7,4 (a 95°C) 2 2 2 2 Soluzioni acquose di gas Solubilità O2 a 25°C Solubilità O2 a 1 atm SOLUZIONI ACQUOSE DI SOLIDI E LIQUIDI Si distinguono in: 1) soluzioni di elettroliti: il soluto si dissocia in ioni parzialmente (elettrolita debole acidi e basi deboli) o totalmente (elettrolita forte – acidi e basi forti, sali). CaCO3 Ca2+ + CO32CaCl2 Ca2+ + 2ClCH3COOH CH3COO- + H+ La presenza di ioni aumenta enormemente la conducibilità della soluzione di elettroliti rispetto al solvente puro: H2O a 25°C x=5.483.10-8 ohm/cm HCl 0.25M a 25°C x=0.213 ohm/cm La concentrazione effettiva delle particelle (ioni+molecole) è: Ceff=C . (1+a(n-1)) (1+a(n-1))=binomio di Van’t Hoff a= grado di dissociazione=n dissociate/ n totali n= numero di particelle originate dalla dissociazione a=1 se la dissociazione è completa 0<a<1 se la dissociazione è incompleta AnBn nA + mB all’equilibrio in soluzione sono presenti: AnBn non dissociate C(1-a) A nCa B mCa -------------------------------TOTALE C(1-a) + nCa + mCa C(1 + a(m+n-1)) C(1 + a(n -1)) 2) soluzioni di non elettroliti: le molecole di soluto sono inalterate, percui non vi sono particelle cariche (saccarosio, glucosio, etanolo). Ceff= C poiché a=0 LE PROPRIETA’ COLLIGATIVE DELLE SOLUZIONI Sono indipendenti dalla natura del soluto e dipendono solo dalla concentrazione effettiva del soluto, cioè dal numero di particelle presenti in soluzione. 1 ) LEGGE DI RAOULT La tensione di vapore di una soluzione è pari alla somma delle tensioni di vapore dei componenti puri, ciascuna moltiplicata per la rispettiva frazione molare: P=P0X0 + P1X1 Se il soluto è liquido, la P della soluzione può essere minore o maggiore di quella del solvente puro a seconda che il soluto sia più o meno volatile del solvente (P non è una proprietà colligativa). Se il soluto è solido, la P della soluzione è sempre minore di quella del solvente puro, poiché la P del soluto è nulla. La legge di Raoult diviene: P=P0X0 dove X0=frazione molare del solvente<1 P=P0. (1-X1)= P0-P0X1 dove X1=frazione molare del soluto P0 - P=DP=P0X1 In queste condizioni, P0 subisce una variazione proporzionale alla quantità di soluto, ma identica, a parità di concentrazione, per tutti i soluti solidi (P è una proprietà colligativa). Poiché per soluzioni diluite molalità e frazione molare sono direttamente proporzionali: DP=k0.m.(1 + a(n -1)) dove ko è caratteristica del solvente e della T molecole di soluto molecole di solvente molecole di solvente allo stato di vapore La tensione di vapore (o pressione di vapore all’equilibrio) di un liquido è la pressione esercitata dal vapore in equilibrio con il suo liquido. E’ indipendente dalla quantità di liquido e dalla forma del recipiente. Dipende dalle interazioni intermolecolari che stabilizzano il liquido e aumenta all’aumentare della T. solvente puro L’aggiunta di un soluto solido abbassa la concentrazione di solvente nella fase liquida. Per mantenere l’equilibrio, diminuiscono anche le molecole di solvente nella fase gassosa, diminuendo la tensione di vapore. soluzione 2) INNALZAMENTO EBULLIOSCOPICO (DTeb) E’ una caratteristica delle soluzioni costituite da soluti solidi, in cui la P della soluzione è minore rispetto a quella del solvente puro. DTeb=keb.m.(1 + a(n -1)) dove keb=costante caratteristica del solvente e m=molalità del soluto. La temperatura di ebollizione del solvente puro subisce una variazione proporzionale alla quantità di soluto, ma identica, a parità di concentrazione effettiva, per tutti i soluti. Si usa la m, in quanto il suo valore è indipendente dalla T. 3) ABBASSAMENTO CRIOSCOPICO (DTcr) E’ una caratteristica delle soluzioni costituite da soluti sia liquidi che solidi: la presenza delle molecole di soluto rende più difficile l’assemblamento delle molecole di solvente nel cristallo. DTcr=kcr.m.(1 + a(n -1)) dove kcr=costante caratteristica del solvente. La temperatura di congelamento del solvente puro subisce una variazione proporzionale alla quantità di soluto, ma identica, a parità di concentrazione effettiva, per tutti i soluti. Si usa la m, in quanto il suo valore è indipendente dalla T. Applicazione: liquidi anticongelanti (glicole etilenico p.e. 198°C) Abbassamento della tensione di vapore dell’acqua. a parità di Ceff tutti i soluti inducono lo stesso Dteb e DTcr. solvente kcr (°C/m) keb (°C/m) acqua 1.86 0.52 Ac. acetico 3.90 2.53 benzene 5.10 2.53 cicloesano 20.2 2.75 naftalina 6.94 5.80 4) PRESSIONE OSMOTICA Se una soluzione è separata dal solvente puro da una membrana semipermeabile o osmotica che lascia passare solo le molecole del solvente, vi è passaggio di solvente attraverso detta membrana dal solvente alla soluzione finchè la pressione esterna eguaglia la pressione idrostatica prodotta dal sistema, detta PRESSIONE OSMOTICA p. Il fenomeno è detto osmosi. E’ stato trovato che la p è la stessa di quella che il soluto eserciterebbe se fosse un gas ideale ed occupasse lo stesso volume, cioè pV=nRT da cui p=RTC.(1 + a(n -1)) per C=1M T=273K a=0 p=22,4atm C=molarità M Il valore di p è proporzionale alla quantità di soluto, ma identica, a parità di concentrazione effettiva, per tutti i soluti. Osmosi e misura della pressione osmotica stato iniziale stato finale pressione osmotica p: è la forza che bisogna applicare per far ritornare l’acqua nel tubo al livello di partenza. Quando una miscela è separata da una membrana semipermeabile e contiene sia particelle di soluto (sali, acidi, basi) che particelle colloidali (proteine), la p è: ptot=psoluto + pcolloidale fenomeni di osmosi
Scaricare