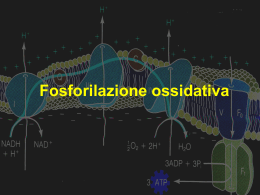
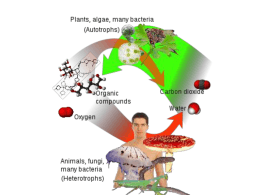
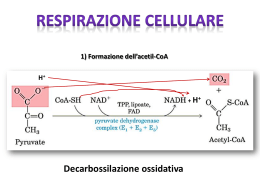
Pre-Test 2013 Davide Loizzo È la “centrale energetica” della cellula EUCARIOTICA Più mitocondri = Più capacità di produrre energia Dispone di: •MEMBRANA ESTERNA (molto permeabile alle macromolecole, ioni e soluti in genere = PORINE) •MEMBRANA INTERNA (altamente selettiva, impermeabile agli ioni H+). La membrana interna si dispone con classiche invaginazioni dette CRESTE, delimitando all’interno la MATRICE MITOCONDRIALE. Tra le due membrane è presente lo SPAZIO INTERMEMBRANA (ha caratteristiche assimilabili al citosol) CATABOLISMO: Insieme delle reazioni di degradazione delle molecole complesse in sostanze più semplici. Si tratta di reazioni esoergoniche. ANABOLISMO: Insieme delle reazioni di sintesi dei costituenti a partire da composti semplici. Si tratta di reazioni endoergoniche. CATABOLISMO + ANABOLISMO = METABOLISMO È un ribonucleotide trifosfato con la capacità di interconnettere CATABOLISMO e ANABOLISMO cellulare (“moneta di scambio”). Utilizziamo circa 1 quintale di ATP AL GIORNO. Ogni mole di ATP sottoposta ad idrolisi (perdita di un gruppo fosfato) rilascia energia pari a 7,3 ATP + H2O kcal ADP + P(fosfato) + 7,3kcal Sono poche le reazioni dove l'ATP dona energia a una molecola tramite idrolisi, principalmente fornisce energia alle altre molecole per trasferimento di gruppi fosfato. (L'idrolisi in se produce solo la liberazione di calore che non può essere utilizzato) Scissione fosforica: ATP + X X-Pi + ADP Scissione pirofosforica: ATP + X X-P-Pi + AMP Scissione pirofosforica: ATP + X X-AMP + P-Pi Per produrre una mole di ATP è necessario fornire ai reagenti una quantità di energia pari a quella liberata dall’idrolisi. Da dove ricavare l’energia? I vari sistemi biologici hanno messo a punto una serie di reazioni e meccanismi in grado di TRASFORMARE l’energia chimica contenuta nei nutrienti (carboidrati, lipidi, amminoacidi) in ATP PROCARIOTI: Fermentazione lattica-alcolica EUCARIOTI: Fermetazione lattica + respirazione cellulare Molte delle reazioni implicate nella produzione di energia sono di tipo REDOX (è necessario il trasferimento di elettroni). I cofattori hanno la capacità di intervenire nella reazione fungendo da ossidanti (accettare elettroni) o riducenti (donare elettroni). Nelle reazioni CATABOLICHE essi fungono da ossidanti, accettando elettroni. Uno dei principali ruoli dei cofattori è quello di trasportare equivalenti di riduzione alla catena respiratoria. EQUIVALENTE DI RIDUZIONE: •Elettroni liberi •Atomi di H •Ioni idruro (H-) IDRURO: È 1 atomo di H che porta 2 elettroni e che deriva da una scissione ASIMMETRICA di una molecola biatomica di idrogeno (H2). NORMALMENTE una molecola H2 si dissocia in 2H ciascuno con 1 protone e 1 elettrone. NAD (NICOTINAMMIDE ADENINA DINUCLEOTIDE) Derivato vitamina B3 o Niacina o PP (Pellagra preventing) 1) Il NAD+ svolge il suo ruolo essenziale di trasportatore in numerosissime reazioni chimiche, quali alcune tappe della glicolisi o del ciclo di Krebs 2) Il NAD+, così come tutti i coenzimi, non viene né prodotto né consumato nelle cellule: queste utilizzano dunque, effettivamente, sempre le stesse molecole, che di volta in volta si ossidano o riducono TRASPORTA 2 EQUIVALENTI PER VOLTA! Esiste inoltre la forma fosforilata del coenzima (NADP+) che si differenzia solo per la presenza di un radicale fosforico esterificato in posizione 3’ della struttura del NAD+. La fx resta la stessa solo che la forma non fosforilata prende parte soprattutto a reazioni di ossidazione mentre la forma fosforilata interviene nelle reazioni di riduzione (ANABOLISMO). FAD (FLAVINA ADENINA DINUCLEOTIDE) Derivato vitamina B2 La molecola è costituita da 3 anelli condensati, che costituiscono il gruppo isoalloazinico della flavina Contrariamente al NAD un coenzima flavinico può trasportare elettroni uno per volta oppure a coppie: dalla forma ossidata (FAD) attraverso l’ingresso di 1 elettrone si passa ad un intermedio radicalico (cioè con 1 elettrone spaiato) detto SEMICHINONE. Successivamente si avrà una protonazione dell’intermedio accettando anche un secondo elettrone. Dunque un coenzima flavinico può trasportare 2 oppure un solo equivalente. FAD + 2H FADH2 Il FAD è un GRUPPO PROSTETICO: non è un solubile ma è un componente intrinseco di alcune proteine a funzione redox: FLAVOPROTEINE È presente in TUTTE le cellule e avviene nel CITOSOL. Un suo sinonimo è FERMENTAZIONE. Nei batteri e nei lieviti essa è l’unica fonte di ATP e quindi di energia attraverso reazioni chimiche a carico del GLUCOSIO. Nelle cellule eucariotiche dotate di mitocondri la principale funzione non è la produzione di ATP, ma la produzione di NADH per la catena respiratoria e piruvato che avrà altri destini, seguendo diversi pathway metabolici. C6H12O6 + 2Pi + 2ADP + 2 NAD+ 2C3H4O3 (Piruvato) + 2ATP + 2 NADH + 2 H+ + 2 H2O La resa energetica netta sarà di 2 molecole di ATP per ogni molecola di glucosio degradata. Negli organismi superiori il 90% dell’ATP sarà prodotto dalla catena respiratoria (che necessita di O2), salvo alcune eccezioni. Per questo motivo il piruvato proseguirà il suo processo di ossidazione per produrre NADH. Nelle cellule procariotiche (e in quelle eucariotiche in scarsa presenza di O2) il piruvato non sarà degradato (ossidato), ma ridotto. Si compie in 10 tappe suddivise in 3 fasi principali: 1. ATTIVAZIONE: Necessaria per portare il glucosio ad uno stato “attivato”, a più alta energia libera. Glucosio + 2ATP Fruttosio 1,6 BisFosfato + 2 ADP 2. SCISSIONE: Glucosio e fruttosio sono esosi (zuccheri a 6 C). Poiché il prodotto finale sarà piruvato a 3 C è necessaria una scissione che darà vita a 2 catene di reazioni parallele. Fruttosio 1,6 Bisfosfato 2 Gliceraldeide 3-P 3. OSSIDAZIONE – PRODUZIONE: In questa fase vengono prodotti ATP e NADH. L’intera fase è moltiplicata per 2 (data la presenza di 2 catene di reazioni, ognuna costituita da molecole a 3 atomi di C via via più ossidate). Gliceraldeide 3-P + 2ATP + 2P + 2NAD+ Piruvato + 2NADH + 2ATP + 2H+ Le singole reazioni che producono ATP sono reazioni altamente favorite dal pdv energetico, tanto da poter sostenere la sintesi di una molecola di ATP (la liberazione di energia libera DEVE essere maggiore a 7,3 kcal/mol). Le molecole “cariche” di energia sono l’1,3 Bisfosfoglicerato e il Fosfoenolpiruvato (PEP) Il processo di ossidazione del glucosio non potrebbe durare all’infinito per eccessiva produzione e accumulo di NADH e continuo utilizzo e scomparsa di NAD+. È necessario infatti rifornire la cellula continuamente di NAD+ e per la farlo la via più semplice è ritrasformare il NADH in NAD+ (ossidare il NADH). In cellule dotate di mitocondri questo avviene grazie alla respirazione cellulare. In cellule senza mitocondri l’agente ossidante è proprio il piruvato, che accetta equivalenti di riduzione permettendo al NADH di ritornare NAD+, fornendo continuo substrato alla glicolisi. La riduzione del piruvato genera lattato = fermentazione lattica. La fermentazione alcolica è leggermente più complessa ma ha lo stesso fine! N.B. : gli eritrociti produrranno energia solo tramite fermentazione lattica perché non posseggono mitocondri. CULTURA GENERALE: i lieviti che producono alcol etilico sono Saccaromyces cerevisiae, elipsoideus e apiculatus. FIBRE MUSCOLARI ROSSE: Necessitano di molta O2, Producono ATP con respirazione - Esplosività + Durata FIBRE MUSCOLARI BIANCHE: Necessitano di poca O2, Producono ATP con glicolisi +Esplosività – Durata (acido lattico!) È la fase più produttiva e avviene solo in cellule dotate di mitocondri. L’intera sequenza di reazioni avviene infatti nel mitocondrio tra MATRICE e SPAZIO INTERMEMBRANA ed ha assoluta necessità di OSSIGENO. Si costituisce in tre fasi: 1. Decarbossilazion e ossidativa del piruvato 2. Ciclo di Krebs 3. Catena di trasporto degli elettroni N.B. : Si parla di respirazione solo considerano le 3 reazioni nell’insieme: ognuna non avrebbe senso senza la presenza dell’altra. Costituisce la prima tappa della respirazione ed interessa il PIRUVATO prodotto dalla glicolisi. Questo è infatti il destino più comune del piruvato: proseguire la via ossidativa per produrre NADH e CO2 (che rappresenta lo stato più ossidato del carbonio). La reazione avviene all’interno della MATRICE mitocondriale: il piruvato di origine glicolitica è citosolico e deve raggiungere la matrice tramite la membrana mitocondriale interna (impermeabile e selettiva). Lo fa attraverso un simporto con H+ La reazione è catalizzata dall’enzima piruvato deidrogenasi, complesso multienzimatico (è composto da 3 proteine diverse). L’enzima per funzionare necessita di tiamina (vit. B1), alla cui carenza è associato il Beriberi Piruvato + HSCoA + NAD+ CO2 + NADH + H+ + AcetilCoA I prodotti sono la CO2 espulsa con la respirazione, NADH substrato della Catena.T.E. e AcetilCoA. Esso è costituito da una molecola di Acido Acetico (a 2 C) legato tramite legame estere ad una molecola di Coenzima A (derivato dell’acido pantotenico, o vit. B5). N.B. : è stata liberata la prima molecola di CO2, indice di inizio ossidativo del piruvato. O ciclo degli acidi tricarbossilici o ciclo dell’acido citrico È costituito da 10 reazioni in serie col fine di ossidare i substrati per produrre NADH da inviare alla catena respiratoria. Proprio dal ciclo ne proverrà la quota maggiore. Quella di fornire NADH per produrre energia è solo una delle tante funzioni del ciclo: le reazioni che lo compongono servono anche per produrre intermedi che saranno utilizzati in altre vie metaboliche (sintetizzare amminoacidi, neurotrasmettitori, eme, glucosio e soprattutto acidi grassi) Solo 3 delle 10 reazioni produrranno NADH ed una FADH2. Reazione complessiva: AcetilCoA + 3H2O + 3 NAD+ + GDP + Pi 3NADH SHCoA + GTP + 2CO2 + FADH2 + Chiamiamo l’insieme delle reazioni “ciclo” perché esso ripropone come prodotto uno dei reagenti. L’inizio del ciclo si configura con una condensazione tra AcetilCoA e Ossalacetato a dare Acido Citrico (da cui il nome del ciclo). Al termine delle reazioni ritroveremo tra i prodotti proprio l’Ossalacetato, che potrà ricondensarsi con un’altra molecola di AcetilCoA e dare via ad un altro ciclo di reazioni. Nella prima reazione il gruppo acetile (a 2C) si lega all’acido ossalacetico (a 4c), formando l’ac.Citrico (a 6C). Successivamente l’ac. Citrico subisce una serie di ossidazioni che portano alla formazione di : - 2 molecole di CO2 - 3 molecole di NADH -1 molecola di GTP a livello della sesta reazione -1 FADH2 O catena di trasporto degli elettroni FOSFORILAZIONE: processo che permette la formazione di ATP a partire da ADP e Pi OSSIDATIVA: ossidazione di substrati (NADH eFADH2) da cui ricavare elettroni, i quali forniranno l’energia necessaria per formare ATP. In cosa consiste? Il fine è creare un gradiente di concentrazione protonico di ioni H+ tra matrice mitocondriale e spazio intermembrana. Sarà proprio l’energia di questo gradiente a permettere la sintesi di ATP, operazione sfavorita da pdv energetico (richiede energia!). Come si crea questo gradiente? È permesso dalla presenza nella membrana mitocondriale interna di POMPE PROTONICHE che spingendo ioni H+ nello spazio intermembrana creano una differenza di concentrazione (H+ > nello spazio i.m.). Queste “pompe” sono enzimi multimerici (formati da tante proteine) dette complessi. I complessi attraverso reazioni di ossido-riduzione, in serie, vanno incontro a modifiche conformazionali che “pompano” fisicamente protoni all’esterno. N.B. : le reazioni redox tra i complessi avvengono grazie alla presenza in essi di veri e propri “centri” redox, grazie alla presenza nei complessi di atomi metallici che vanno incontro ad ossido-riduzione (centri Fe-S, centri Cu), di Ubichinone o Coenzima Q, flavoproteine, e di proteine, facenti sempre parte dei complessi, chiamate Citocromi. I Citocromi sono proteine contenenti al loro interno il gruppo eme, con al centro legato uno ione Fe. Il Fe può essere ossidato 2+ (forma ridotta) o 3+ (forma ossidata). Il continuo passaggio del Fe dalla forma ridotta alla forma ossidata, e viceversa, permette il trasferimento di elettroni dal donatore all’accettore. Le Flavoproteine hanno la stessa funzione dei citocromi, solo che anziché l’eme troviamo un FMN (Flavina mononucleotide) con la presenza dell’anello isoallosazinico. Idem le proteine Fe-S dove troviamo insieme Fe e S che cambiano il loro numero di ossidazione per trasferire elettroni. L’Ubichinone è un molecola presente all’interno delle membrane capace di ridursi a Ubichinolo e viceversa, con funzione di trasporto di elettroni. I complessi della catena di trasporto sono 5, ognuno con una determinata funzione • Complesso I I complessi (I-IV) sono dotati di potenziale redox. I potenziali sono • Complesso II via via crescenti, questo significa che ogni complesso tende a • Complesso III ridursi più velocemente rispetto al precedente. L’ossidante • Complesso IV terminale sarà l’O2, con potenziale maggiore di tutti, che si • Complesso V ridurrà ad H2O. Il trasporto degli elettroni tra i complessi permetterà di non dissipare l’energia di reazione tra NADH e O2. Complesso I o NADH-Ubichinone ossido-reduttasi Lega il NADH (ridotto) per ossidarlo e trasferire gli elettroni all’Ubichinone, che a sua volta si riduce ad ubichinolo. Gli elettroni vengono trasferiti grazie alla presenza di proteine Fe-S e Flavoproteine. Col passaggio degli elettroni vengono pompati 4 H+ nello spazio intermembrana. Complesso II o Succinato deidrogenasi È uno degli enzimi che interviene nel Ciclo di Krebs, con la produzione di FADH2. Poiché il FADH2 è un gruppo prostetico, e quindi fa parte della proteina stessa, gli elettroni vengono trasferiti direttamente da questo enzima all’Ubichinone, riducendolo. Il complesso II non pompa protoni nello spazio intermembrana: per questo motivo, se la catena respiratoria inizia dal complesso II, la resa energetica in termini di produzione di ATP è minore Complesso III o Ubichinolo-Citocromo C ossido-reduttasi È una ossido-reduttasi, il substrato da ossidare è l’Ubichinolo (precedentemente ridotto), riducendo così il Citocromo C. All’interno del complesso sono presenti proteine citocromiche e proteine Fe-S. Il passaggio di una coppia di elettroni attraverso il complesso permette di trasferire 2 H+ nello spazio intermembrana, attraverso il “ciclo dell’ubichinone”. Complesso IV o Citocromo C ossidasi È l’enzima finale del processo di ossidazione. In questo caso viene ossidato il Citocromo C (proteina di membrana del MT, non fa parte di alcun complesso) per ridurre l’O2 ad H2O; il passaggio di elettroni attraverso il complesso IV (grazie a proteine citocromiche e centri Cu) pompa 4 H+ nello spazio intermembrana. L’enzima può essere inibito dal CN- (cianuro), sostanza letale a piccolissime concentrazioni. Poiché gli elettroni lungo la catena sono trasferiti uno per volta, nel processo di riduzione dell’O2 si può formare l’anione superossido, facente parte della famiglia dei “radicali liberi”, specie altamente reattive e dannose per la cellula invecchiamento fisiologico. Complesso V o ATP sintasi È l’enzima che sintetizza ATP a partire da ADP e Pi sfruttando il gradiente di H+. Dobbiamo immaginarlo come un canale protonico rotante, alla cui estremità è posta la subunità catalitica, tutto a forma di fiore stilizzato, con: -1 porzione idrofobica transmembrana (F0), attraverso cui passano i protoni -1 collo -1 porzione idrofilica (F1) che sporge nella matrice mitocondriale. F1 è costituito da 3 dimeri αβ che si trovano in 3 stati conformazionali diversi: -STATO O (OPEN) non lega nulla - STATO L (LOOSE) lega debolmente ADP -STATO T (TIGHT) lega saldamente ATP. Gli stati conformazionali sono determinati dalla rotazione di F0. La rotazione è data dal passaggio di protoni! = ENERGIA Resa energetica Per produrre una molecola di ATP sono ncessari 4H+. Questo vuol dire che a partire dal NADH, con il trasferimento di 2 elettroni, si producono 10H+, equivalenti a 2,5 ATP. Al passaggio di ogni 3 protoni attraverso il complesso V, grazie a modifiche conformazionali, si verifica una rotazione di 120° di F0, più un H+ per portare il Pi nella matrice. Ciò corrisponde alla sintesi di un ATP. A partire dal FADH2 del complesso II vengono pompati 6 protoni = 1,5 ATP. Per ogni molecola di glucosio si producono 36 ATP di cui: -2 di origine glicolitica - 34 di origine respiratoria di cui: -2 GTP (ATP) per ogni AcetilCoA 4 ATP -10 ATP provenienti dall’ossidazione di 4 NADH di glicolisi e decarbossilazione ossidativa del piruvato -20 ATP provenienti dall’ossidazione di 3 NADH e 1 FADH2 del ciclo di Krebs C6H12O6 + 6O2 6 CO2 + 6 H2O + 686 Kcal/mol (36 ATP + 423 Kcal) Per superare il test servono… Ma soprattutto… QUESTO!
Scaricare