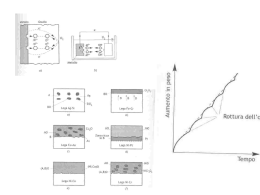
CONTROLLO DELLA CORROSIONE NEGLI IMPIANTI AMMINICI R. B. Nielsen, K R. Lewis Fluor Daniel, Inc. 3333 Michelson Drive Irvine, CA 92730 John G. McCullough Proton Technology, Ltd. 186 Amsterdam Ave. Hawthorne, NY-10532 D. A. Hansen Fluor Daniel, Inc. One Fluor Daniel Drive Sugar Land, IX 77478-3899 Traduzione inglese/italiano a cura World Image s.r.l. Italia SINTESI In questo articolo sono esaminate le cause e la prevenzione della corrosione dell’acciaio al carbonio negli impianti amminici. Gli agenti corrosivi, negli impianti in generale, sono i gas acidi, l’ossigeno, i sali termostabili, i prodotti della degradazione delle ammine e, particolarmente negli impianti di raffinazione, gli inquinanti presenti nel gas da lavare, come l’ammoniaca e l’acido cianidrico. Corrosioni possibili dell’acciaio al carbonio sono previste nelle sezioni esposte alle soluzioni amminiche e nelle sezioni di testa delle colonne rigeneratrici a contatto con il condensato di testa colonna. La corrosione può essere evitata nei seguenti modi: - additivando inibitori di corrosione utilizzando, in determinate aree, materiali resistenti alla corrosione purificando le ammine e/o i gas di alimentazione modificando opportunamente le variabili di processo Affronteremo le varie tipologie di cricche nell’acciaio al carbonio e le misure per la loro riduzione. Parole chiave: ammine, alcanolammina, trattamento gas, corrosione, erosione, cianuro, lavaggio con acqua, polisolfuro di ammonio, gas acidi, cricche, SSC, HIC, SOHIC, ASCC, bisolfuro di ammonio, cloruro, sali termostabili. 1 INTRODUZIONE Gli impianti amminici sono soggetti alla corrosione causata dall’anidride carbonica e dall’idrogeno solforato ove è presente la fase vapore, nelle parti ove circola la soluzione amminica, nel circuito del riflusso di testa colonna rigeneratrice. Nelle raffinerie, gli impianti amminici sono soggetti a corrosione da parte di numerosi agenti che solitamente non si trovano nei processi di gas di sintesi e naturali, quali ammoniaca, acido cianidrico e acidi organici. Alcuni di questi formano dei sali che tendono ad accumularsi in alcune colonne degli impianti amminici di raffineria. Gli impianti amminici devono essere progettati per superare questi problemi specifici. Il presente documento, basato su una revisione dei documenti pubblicati, spiega le cause di questi problemi e la loro soluzione. Descrive le aree all’interno dell’impianto dove i vari contaminanti causano corrosione, illustra i meccanismi della corrosione in tali aree, rivede le pratiche di progettazione e le misure preventive richieste per risolvere la corrosione. Queste misure includono il controllo della velocità e della erosione per attriti dovuti a turbolenze, le variazioni di configurazione del processo, le strategie di controllo del processo, l’uso selettivo di materiali resistenti alla corrosione, la purificazione della soluzione amminica e la scelta dell’ammina. CORROSIONE NEGLI IMPIANTI AMMINICI La Figura 1 illustra un impianto tipico di trattamento con alcanolammina. Il gas di alimentazione contenente CO2 o H2S o una miscela di entrambi i gas acidi entra nel fondo di una colonna a piatti o a riempimento dove entra in contatto con la soluzione amminica. I componenti acidi del gas vengono rimossi dal gas tramite reazione chimica con l’ammina. Il gas purificato esce dalla testa colonna, mentre la soluzione di ammina ricca esce dal fondo della colonna di assorbimento ed attraverso il controllo del livello va al flash drum dell’ammina ricca. Il flash drum si trova ad una pressione tanto bassa da consentire la rimozione degli idrocarburi disciolti o trascinati. Successivamente l’ammina ricca va in carica alla colonna di rigenerazione, sotto il controllo di livello del flash drum quindi attraversa lo scambiatore di calore di ammina povera/ricca e va alla colonna di rigenerazione di ammina. Nella rigeneratrice, i componenti acidi rimossi del gas vengono eliminati dalla soluzione amminica per mezzo del calore fornito dal ribollitore del fondo colonna della rigeneratrice. Il gas acido esce dalla testa della colonna di rigenerazione dell’ ammina, mentre l’ammina povera o rigenerata esce dal fondo colonna. L’ammina povera calda proveniente dal fondo colonna di rigenerazione scambia il calore con l’ammina ricca fredda, dopodiché ritorna alla colonna di assorbimento. Come indica la Figura 1, la maggior parte delle apparecchiature e delle tubazioni di un impianto di alcanolammina sono costruite in acciaio al carbonio. Infatti è possibile, nella maggior parte dei casi costruire un impianto utilizzando solo acciaio al carbonio ma mantenendo basse le temperature di esercizio della colonna di rigenerazione di ammina, riducendo la concentrazione della soluzione di ammina e il suo carico molare acido (mole gas acido/mole di ammina). Tuttavia, come mostra la Figura 1, è pratica comune costruire certe parti del circuito amminico con acciaio inossidabile od altre leghe. L’uso selezionato di acciaio inossidabile permette il funzionamento a più alte concentrazioni di ammina e carico molare acido, permette uno strippaggio migliore della soluzione amminica, riduce la corrosione nelle zone suscettibili e migliora i costi di processo. Le posizioni segnate in grassetto sulla Figura 1 mostrano dove l’acciaio al carbonio viene sostituito dall’acciaio inossidabile. Le zone circoscritte con linee tratteggiate mostrano dove possono essere richieste modifiche alla progettazione meccanica o del processo o l’utilizzo di materiali resistenti 2 alla corrosione in base soprattutto alla composizione del gas trattato. Per comprendere queste scelte, è necessario capire perché l’acciaio al carbonio è soggetto a corrosione negli impianti amminici. In assenza di inibitori, l’acciaio al carbonio è corroso nelle soluzioni acquose da un meccanismo elettrochimico. La semi-reazione anodica è l’ossidazione del ferro in ione ferroso: Fe=Fe2+ + 2e- (1) La semi-reazione catodica è la riduzione di una forma di idrogeno dallo stato di ossidazione +1 all’elemento. 2H+ + 2e- = H2 (2) La reazione chimica netta è la somma delle due semi-reazioni: Fe + 2H+ = H2 + Fe2+ (3) Questa è una reazione irreversibile e di conseguenza, la sua entità è influenzata solo dalla concentrazione delle specie nella parte a sinistra dell’equazione. Perciò l’entità della reazione (3) aumenta con l’aumento della concentrazione degli ioni di idrogeno (diminuzione del pH) con l’aumento della temperatura e poiché la reazione è elettrochimica, con l’aumento della conduttività della soluzione. La Figura 1 indica le zone principali dove la corrosione può avvenire negli impianti amminici. Come indicato in questa figura, la corrosione negli impianti amminici può essere suddivisa in due categorie: 1. Corrosione da Gas Acido Umido La corrosione dell’acciaio al carbonio è causata dalla reazione di CO2 e H2S con il ferro attraverso una pellicola liquida sottile. 2. Corrosione causata dalla qualità della Soluzione Amminica E’ la corrosione dell’acciaio al carbonio in presenza di soluzione amminica qualitativamente degradata.. MECCANISMO DELLA CORROSIONE DELL’ACCIAIO AL CARBONIO DA GAS ACIDO UMIDO Il gas acido umido si trova nella sezione di testa della colonna di rigenerazione amminica e sul fondo della colonna di lavaggio amminico se il gas da lavare è saturo di acqua. Le superfici di metallo di queste zone di impianto possono perciò entrare in contatto con soluzioni acquose di gas acido contenenti poca o niente ammina. Vedere figura 1. 3 Corrosione di CO 2 umido Se sussiste una fase acquosa e se l’unico gas acido è l’anidride carbonica, la CO2 si scioglierà in acqua per formare l’acido carbonico H2 CO3. La corrosione predominante dell’acciaio al carbonio in presenza di CO2 umida è determinata dalla ridotta capacità dell’acido non dissociato a formare carbonato ferroso, che è solo leggermente solubile e non forma uno strato protettivo reale (1) . Fe + H2CO3 = FeCO3 + H2 (4) La Figura 2 mostra l’effetto della temperatura sulla corrosione dell’acciaio al carbonio da parte dell’anidride carbonica acquosa. Questa figura mostra che il tasso di corrosione raggiunge un massimo ad una data pressione di CO2. Si pensa che la riduzione del tasso di corrosione sia dovuta alla formazione di un film protettivo, di FeCO3 o Fe3O4, a temperature più alte (1) . De Waard e Lotz hanno sviluppato un grafico che può essere usato per prevedere la corrosione dell’acciaio al carbonio da parte delle soluzioni acquose di anidride carbonica (1) . Corrosione da H2S umido Se il gas acido contiene idrogeno solforato, il prodotto principale di corrosione è il solfuro ferroso, che è insolubile e forma uno strato di solfuro di ferro, debolmente aderente alle pareti, che è in un certo qual modo protettivo: Fe+H2S=FeS+H2 Il solfuro di ferro è più protettivo del carbonato di ferro e soltanto se il gas acido contiene sufficiente H2S, si può formare uno strato protettivo di solfuro. Se gli agenti contaminanti che distruggono questo strato di solfuro di ferro non sono presenti e la progettazione meccanica è ben dimensionata per ridurre l’erosione-corrosione, la corrosione dell’ acciaio al carbonio sarà limitata. D’altra parte, se il gas predominante è la CO2, si verificherà una corrosione da gas acido umido e saranno necessarie misure protettive. Ci sono discrepanze per quale rapporto CO2/H2S sono richieste misure protettive. Le API 945 suggeriscono che la corrosione da CO2 umido avviene quando il gas acido contiene il 95% o più di CO2.(2) Corrosione di gas acido umido dovuta a NH3 e HCN Nelle raffinerie, il sistema di testa della colonna di rigenerazione dell’ ammina è spesso soggetto a corrosione da gas acido umido dovuta dalla presenza combinata di ammoniaca con CO2 e H2S. La corrosione è accelerata se l’HCN è anche presente. In queste circostanze, la corrosione dovuta ad H2S e CO2 può sopraggiungere quando il contenuto di CO2 nel gas acido è inferiore al 90%. Infatti, si può verificare una corrosione di una certa importanza in assenza totale di CO2 se sono presenti quantità sufficienti di HCN e ammoniaca. L’ammoniaca e l’HCN sono presenti nei flussi di gas provenienti dall’Unità di Delayed Coker, dal Visbreaker e dall’impianto di Cracking Fluido Catalitico (FCC). L’ammoniaca, l’HCN e l’H2S vengono anche prodotti negli impianti di Hydrotreating e di Hydrocracking. Quando il gas proveniente da questi impianti è lavato in un impianto amminico, l’ammoniaca viene subito assorbita dalle soluzioni acquose di alcanolammina. L’HCN che è un acido debole e altamente 4 solubile in acqua, è assorbito chimicamente dalle soluzioni di alcanolammina nelle colonne di lavaggio ed è rilasciato, insieme all’ammoniaca assorbita, nella colonna di rigenerazione di ammina. Nel condensatore di testa della colonna di rigenerazione, l’ammoniaca gassosa e l’HCN sono riassorbiti dall’acqua condensata che costituisce il riflusso di testa. L’ammoniaca disciolta nell’acqua di riflusso reagisce con l’H2S per formare bisolfuro di ammonio. NH3 + H2S = NH4+ + HS- (6) Senza uno spurgo dell’acqua di riflusso, l’HCN e il bisolfuro di ammonio sono intrappolati nel circuito di testa della colonna di rigenerazione. La CO2 può essere intrappolato nel circuito di testa in modo simile al bicarbonato di ammonio. Se sono presenti entrambi l’ammoniaca e l’HCN, l’effetto risultante è un aumento sostanziale delle concentrazioni di HCN, H2S e H2CO3 nel circuito di testa della colonna di rigenerazione dell’ammina. L’H2S nel circuito di testa, causa corrosione secondo la seguente reazione: Fe + H2S = FeS + 2H0 (7) Come notato da Ehmke,(3,4) il film del solfuro di ferro fornisce una protezione ad un pH di 7 o 8, ma è poroso ad un pH di 8 o 9. Inoltre se sono presenti ioni di cianuro, il film protettivo di solfuro di ferro sarà rimosso secondo la reazione: (3,4,5) FeS + 6CN- = Fe(CN)6 4- + S2- (8) La rimozione del film protettivo di solfuro di ferro secondo la reazione (8) dipende dal pH, la velocità di rimozione aumenta all’aumentare del pH. (3,4) Come indicano le reazioni (7) e (8), più alte sono le concentrazioni di H2S e CN, maggiore è il tasso di corrosione. Se la CO2 è intrappolata dall’ammoniaca nel circuito di testa della colonna di rigenerazione ammina dall’ammoniaca, si può verificare la corrosione secondo la seguente reazione: Fe + 2H2CO3 = Fe2+ + 2HCO3 + 2H0 (9) Le reazioni (7) e (9) producono idrogeno atomico, H0. In condizioni normali, l’idrogeno atomico si combinerebbe con la superficie metallica per formare idrogeno molecolare. Tuttavia, gli agenti inquinanti delle superfici di acciaio come il solfuro e gli anioni di cianuro ostacolano questa ricombinazione, ed una parte significativa dell’idrogeno atomico migra nel reticolo metallico. (6) La maggior parte dell’idrogeno atomico passa completamente nell’acciaio e forma idrogeno molecolare sulla superficie opposta. Tuttavia, se l’idrogeno atomico incontra una discontinuità della superficie o un’inclusione nel metallo di base, rimane intrappolato e si ricombina per formare idrogeno molecolare. Poiché sempre più idrogeno molecolare è intrappolato in questi punti, la pressione cresce fino a superare il carico di snervamento dell’acciaio. Le alte concentrazioni di idrogeno molecolare in questi punti possono portare a corrosione da idrogeno o rottura provocata da idrogeno (HIC). Nei punti con maggiore sollecitazioni, come le zone termicamente alterate dal calore delle saldature, l’(HIC) si può propagare in modo planare, attraverso lo spessore. Questo tipo di rottura si chiamerà rottura provocata da idrogeno con sollecitazione (SOHIC). Inoltre l’idrogeno atomico disciolto nel reticolo 5 di acciaio può rendere fragili le zone delle microstrutture dure nell’acciaio al carbonio o nelle saldature. Le alte concentrazioni di idrogeno atomico nell’acciaio al carbonio possono portare alla rottura da sollecitazione di solfuro (SSC) di questi punti duri. Gli impianti amminici che trattano gas provenienti da FCCU sono particolarmente suscettibili all’attacco dell’idrogeno a bassa temperatura perché il gas proveniente da questi impianti può avere un alto contenuto di cianuro. Secondo Neuemaier e Schillmoller, l’attacco dell’idrogeno si può verificare ogni qualvolta i composti di azoto organico nell’alimentazione al FCCU sono maggiori di 0,05 wt%. (7 ) L’acqua di lavaggio o di riflusso con colore blu (blu di Prussia) dopo l’ossidazione con l’aria indica che si sta verificando una corrosione indotta da cianuro. (3,4) Neumaier, Schillmoller e Ehmke hanno descritto una prova per individuare il cianuro che utilizza una soluzione diluita di cloruro ferrico (3,4,7) . PREVENZIONE DELLA CORROSIONE DELL’ ACCIAIO AL CARBONIO DA GAS ACIDO UMIDO Prevenzione della corrosione da CO 2 e H2S umido Come mostrato alla Figura 1, la corrosione da CO2 umido si può verificare sul fondo della colonna di assorbimento o nel circuito di testa della colonna di rigenerazione di ammina. Se la soluzione di ammina bagna completamente tutta la superficie esposta di acciaio al carbonio, il pH della condensa si alzerà di molto e la sua corrosività sarà ridotta. Nei casi in cui il gas acido contiene il 95% di CO2 o maggiore, una spruzzata di ammina in testa alla colonna di rigenerazione è stata raccomandata per ridurre la corrosione. (2,8) L’ammina dovrebbe essere iniettata in modo che il riflusso contenga lo 0,5 wt% di ammina. (8,9) In molti impianti di raffineria, la corrosione dovuta a CO2 umido sulla testa delle colonna di rigenerazione non è un problema perché è predominante il contenuto di H2S sulla CO2. Tuttavia, si consiglia una spruzzata di ammina nei rigeneratori di ammina associati ad impianti idrogeno che utilizzano ammina per la rimozione di CO2 . La corrosione da CO2 umida può anche rappresentare un problema nelle colonne di assorbimento degli impianti idrogeno. Sul fondo dell’assorbitore, la corrosione dovuta ad alto contenuto di CO2 nel gas acido, può essere evitata introducendo il gas attraverso un distributore immerso nell’ammina (10) . Il distributore dovrebbe essere immerso nella soluzione di ammina ricca in modo che il gas che fuoriesce porti la soluzione di ammina a schizzare e bagnare la superficie di acciaio al carbonio. Se il distributore si rompe o è installato sopra il livello della soluzione, il CO2 umido può attaccare rapidamente le pareti dell’assorbitore e i suoi elementi interni. Se l’assorbitore è provvisto di piatti, la parte sottostante il piatto di fondo viene attaccata dal gas acido fino a quando il piatto non crolla, poi viene attaccato il secondo piatto il quale cade anche lui. Come mostrato in Figura 1, tutti i piatti possono essere risparmiati se il piatto di fondo è in acciaio inossidabile. Se il progetto meccanico relativo al fondo dell’assorbitore o al sistema di testa del rigeneratore di ammina prevede che l’ammina non bagni le superfici in acciaio al carbonio, allora le tubazioni e le apparecchiature dovrebbero essere in acciaio inox o rivestite con acciaio inox. Un altro fattore che dovrebbe essere considerato per quanto riguarda i gas ad alto contenuto di CO2 è quello di ridurre la velocità del gas sulle superfici in acciaio al carbonio. 6 Dupart ed altri riportano un’osservazione in cui l’alta velocità di un gas ricco di CO2 portava alla corrosione sul fondo di una colonna di assorbimento (10). Questo problema fu corretto modificando il distributore del gas per ridurre la velocità del gas acido sulla parete dell’assorbitore. Prevenzione della corrosione da NH3 e HCN Sono state adottate diverse soluzioni per ridurre la corrosione prodotta dall’ammoniaca e dal cianuro nel circuito di testa del rigeneratore di ammina. Questi metodi includono: Uno spurgo dell’acqua di riflusso per ridurre la concentrazione di bisolfuro di cianuro e di ammonio nella testa della colonna di rigenerazione. Vedere Figura 1. Un lavaggio con acqua a monte della colonna di assorbimento con ammina, per rimuovere l’ammoniaca e l’HCN. Iniezione di polisolfuro di sodio o di ammonio a monte del rigeneratore di ammina o nel circuito di testa del rigeneratore. Lo strippaggio dei componenti corrosivi contenuti nell’acqua di riflusso testa rigeneratrice. L’uso di materiali resistenti alla corrosione nel circuito di testa del rigeneratore di ammina. La combinazione dei punti sopra detti. In genere, la soluzione più economica è quella di modificare le condizioni del processo per permettere l’uso dell’acciaio al carbonio. L’eliminazione dell’HCN e dell’ammoniaca a monte dell’impianto di trattamento dell’ammina è solitamente la soluzione più efficace. Segue una breve descrizione dei metodi di prevenzione della corrosione: Spurgo continuo del riflusso testa colonna rigeneratrice. L’ammoniaca e il cianuro accumulati nel circuito di testa del rigeneratore di ammina possono essere ridotti e la corrosione può essere controllata se si mantiene uno spurgo continuo dell’acqua di riflusso. Vedere Figura 1. Lo spurgo è efficace se le concentrazioni di cianuro e ammoniaca nel gas da lavare sono basse (7). Infatti, se il contenuto di cianuro dell’acqua di riflusso o l’acqua di lavaggio posta a monte dell’assorbitore sono inferiori a 100 ppmw, la corrosione prodotta dal cianuro (HIC) dell’acciaio al carbonio sarà minima. (7) Per ridurre i problemi di corrosione di H2S umido (SSC, HIC, SOHIC), il contenuto di cianuro dell’acqua di lavaggio dovrebbero essere sotto i 20 ppm. (11) Seguendo le linee guida sviluppate per le raffinerie, i refrigeranti ad aria possono usare l’acciaio al carbonio nel condensatore di testa del rigeneratore e nelle tubazioni a valle se la concentrazione di bisolfuro di ammonio nell’acqua di riflusso è inferiore a 2-3 wt% e le velocità nel fascio tubero e nelle tubazioni sono tenute al di sotto dei 20 piedi al secondo (12). L’iniezione di un inibitore (polisolfuro di ammonio) può essere richiesta per il circuito di testa del rigeneratore di ammina se la concentrazione di cianuro è troppo alta. Nelle raffinerie è spesso previsto un sistema di iniezione di inibitore in standby . (7) Se uno spurgo di riflusso è utilizzato per controllare il contenuto di cianuro e di NH3 dell’acqua di riflusso, si consiglia di evitare l’uso di doppie curve a 180° nei condensatori di testa per il raffreddamento dell’aria o dell’acqua. (12) 7 Lo svantaggio dello spurgo del riflusso rigeneratore è che si hanno perdite di ammina perché la concentrazione dell’ ammina nell’acqua di riflusso può essere tra 0.5 e 2.0 wt% in funzione del trascinamento dell’ammina, del tipo di ammina, e del numero di piatti nel rigeneratore di ammina. (13) Inoltre, il tasso di spurgo richiesto per ridurre le concentrazioni di ammoniaca e di cianuro al di sotto dei livelli di corrosione è difficile sia da determinare che da controllare. Mentre le perdite di ammina possono essere ridotte probabilmente installando un demister nel rigeneratore di ammina, le condizioni di corrosione possono esistere anche con uno spurgo continuo del riflusso. Per questa ragione, quando sono presenti entrambi l’ammoniaca e il cianuro, gli impianti di ammina sono progettati appositamente con materiali anticorrosivi del tipo mostrato alla Figura 1. Il rigeneratore di ammina è rivestito con placcatura integrale tipo 304L o con sovrapposizione di lamiera saldata a partire dai due piatti sotto il piatto di alimentazione fino e incluso il piatto di testa. Le tubazioni di testa sono solitamente 304L SS. Tubi in titanio sono stati usati di frequente nel condensatore di testa. Ehmke nota che l’alluminio è stato usato con successo nel condensatore di testa se il pH, il contenuto di ioni cloro, l’erosione e la velocità sono sotto controllo. (14) L’acciaio al carbonio è utilizzato di frequente nell’accumulatore di riflusso, tuttavia un sovraspessore per corrosione è necessario e qualche volta è utilizzato materiale resistente all’(HIC). Il rivestimento della pompa di riflusso e le giranti dovrebbero essere 316 SS. Tutte le tubazioni di riflusso sono in 304L SS. Lavaggio con acqua a monte o lavaggio caustico. Il lavaggio caustico fu raccomandato da Polderman e Steele e usato da Norris e Clegg per la rimozione di acidi formici e acetici contenuti nei gas che entrano negli impianti amminici. (14,15) Poiché entrambi gli acidi acetici e formici sono più forti dell’H2S e del CO2, questi sostituiscono i sali di solfuri o carbonati. Tuttavia, come notato da Polderman, Steele ed Ehmke, il lavaggio caustico non può rimuovere l’HCN dal gas perché l’HCN è un acido più debole dell’H2S o CO2 e sarà eliminato dalla soluzione caustica da uno di questi due gas acidi. (14,3,4) Poiché l’HCN è più solubile in acqua dell’H2S o del CO2, il lavaggio con acqua è utilizzato per rimuovere il acido cianidrico dal gas (7,14,16). La tabella 1 indica che una singola fase di lavaggio con acqua da sola non basta per rimuovere l’ammoniaca e il cianuro. (3,4,7) Ciò vuol dire che sono richieste misure protettive aggiuntive per esempio un sistema di back-up per iniezione di polisolfuro di ammonio nel circuito di testa del rigeneratore ed uno spurgo del riflusso del rigeneratore. (7) Lavaggio con polisolfuro di ammonio. La corrosione dovuta al cianuro e al bisolfuro di ammonio può essere eliminata lavando il gas a monte dell’assorbitore di ammina con soluzione di polisolfuro di ammonio. (3,4) Nel lavaggio con acqua a monte, l’ammoniaca è disciolta nell’acqua di lavaggio mentre il polisolfuro di ammonio reagisce con il CN per formare ioni di tiocianato, SCN. L’acido tiocianico, l’HSCN, è un acido forte ed è più solubile in acqua dell’HCN. Ehmke (3,4) presenta dati che mostrano che l’iniezione di polisolfuro di ammonio può ridurre le concentrazioni di CN a meno di 10 ppmw, il che è al di sotto della soglia richiesta per prevenire l’HIC e l’SSC (7,11) Sx-2 + CN- = Sx-1 -2 + SCN (10) Il polisolfuro di ammonio è preferito al polisolfuro di sodio perché reagisce più velocemente con il CN e non alza il pH dell’acqua di lavaggio. (3,4) Linee guida di progettazione e funzionamento per i sistemi di lavaggio con polisolfuro di ammonio sono forniti da Ehmke. (3,4) Utilizzando un lavaggio con acqua e polisolfuro di ammonio si rimuove l’ammoniaca e l’HCN. Ciò permette di avere il sistema di testa del rigeneratore di ammina in acciaio al carbonio. I principi di progettazione di un sistema di lavaggio con polisolfuro di ammonio sono stati rivisti da Bucklin e Mackey i quali 8 hanno raccomandato l’uso di un lavatore multistadio in contro corrente con 8÷10 piatti effettivi (13). Il sistema di lavaggio con acqua qui descritto utilizza acqua acida contenente 50 ppm NH3 per ridurre l’ammoniaca nel gas lavato a 0.1 ppm. Il polisolfuro di ammonio è aggiunto all’acqua di lavaggio per convertire il cianuro in tiocianato. Strippaggio di componenti corrosivi dal riflusso del rigeneratore di ammina Neumaier e Schillmoller descrivono un altro metodo per eliminare la corrosione in presenza di l’ammoniaca e cianuro nel sistema di testa del rigeneratore di ammina.(7) In questo metodo il riflusso del rigeneratore di ammina è inviato ad un apposito separatore di acqua acida. L’ammoniaca e l’HCN sono separati dall’acqua di riflusso in questo separatore. Così facendo l’acqua di riflusso può ritornare al rigeneratore di ammina. Poiché il cianuro e l’ammoniaca non ritornano al rigeneratore di ammina, non c’è formazione di questi componenti nel circuito di testa del rigeneratore e quindi il circuito di testa potrà essere in acciaio al carbonio. 9 CORROSIONE DA PARTE DELLA SOLUZIONE DI AMMINA DELL’ACCIAIO AL CARBONIO La corrosione da parte della soluzione di ammina sull’acciaio al carbonio può essere causata da numerosi fattori, tra i quali: - Alte temperature di funzionamento Alti carichi molari di ammina ricca e povera (moli di gas acido/moli di ammina) Il rapporto tra CO2 e H2S nel gas acido Contaminanti della soluzione di ammina inclusi prodotti di degradazione dell’ammina e sali termostabili Concentrazione della soluzione amminica Tipo di ammina Come mostrato nella figura 1, la corrosione della soluzione amminica è più significativa nella parte calda del fondo del rigeneratore. La corrosione può avvenire nella linea che inizia dalla valvola di controllo del livello del contattore fino al flash drum dell’ammina ricca, nello scambiatore di ammina povera/ricca, e nelle tubazioni che vanno dalla valvola di controllo livello della flash drum dell’ammina ricca al rigeneratore. La corrosione della soluzione amminica in queste zone può essere minimizzata scegliendo idonei parametri di processo e materiali in AISI adeguati. Meccanismi della corrosione nell’acciaio al carbonio da parte del gas acido e dalla ammina Le ammine pure e le miscele di sola acqua e ammina non sono corrosive perché hanno o una bassa conduttività o un alto pH. (10,17) Tuttavia, le soluzioni di ammina ricca, che hanno un’alta conduttività ed un pH molto più basso rispetto alle soluzioni di ammina povera, possono essere abbastanza corrosive. Numerose soluzioni sono state proposte per questo tipo di corrosione. Riesenfeld e Blohm furono i primi a notare che una corrosione significativa dell’ammina era associata di solito con lo sviluppo dei gas acidi provenienti dalla soluzione di ammina ricca (18,19,20).Sulla base di questa osservazione Riesenfeld e Blohm affermavano che la corrosione nell’acciaio al carbonio da parte della soluzione di ammina era dovuta alla presenza dei gas acidi stessi. Ad esempio, il gas acido si sviluppa dalle soluzioni di ammina ricca secondo le reazioni (11) e (12): R3NH+ + HCO3 = R3N + H2O + CO2 R2NH2+ + R2NCO2 = CO2 + 2R2NH (11) (12) I gas acidi possono reagire direttamente con l’acciaio al carbonio esposto per formare carbonato di ferro secondo la reazione (13): Fe + H2O + CO2 = FeCO3 + H2 (13) Il carbonato di ferro è leggermente solubile e forma una pellicola sopra la superficie di metallo attivo che offre una protezione limitata alla corrosione. Reazioni di corrosione simile si verificano con l’H2S; tuttavia, la pellicola di solfuro di ferro che copre la superficie di metallo attivo è molto più protettiva del carbonato di ferro, e resiste molto bene alla corrosione. Questo meccanismo spiega numerosi fenomeni di corrosione. Ad esempio, le ammine primarie come la MEA e la DGA sono più corrosive delle ammine secondarie e terziarie per via delle alte 10 temperature che sono necessarie per strippare. Perciò negli impianti amminici che impiegano le ammine primarie sono presenti alte concentrazioni di gas acidi nelle zone più calde del processo. Al contrario la MDEA, ammina terziaria, viene facilmente separata sia dalla CO2 che dall’H2S, perciò è meno corrosiva perché i gas acidi si separano dalla soluzione ad una temperatura più bassa. Sebbene si pensi che i gas acidi siano responsabili della corrosione dell’acciaio al carbonio, il vero meccanismo che causa la corrosione non è ben chiaro. Come indica la Reazione (13), non è certo quale elemento, l’H2CO3 o l’HCO3-, contribuisce con i relativi ioni idrogeno alla reazione di corrosione. Non sono state fatte ricerche che definiscano questo problema e chiaramente è necessario del lavoro ulteriore per stabilire l’esatto meccanismo per cui alcune specie di anidride carbonica sono responsabili della corrosione. Sebbene è improbabile che l’anidride carbonica e gli ioni di bicarbonato siano presenti nelle soluzioni amminiche alle condizioni operative del rigeneratore; i siti di nucleazione (fessure, pits e zone intergranulari) dove le bolle di CO2 si formano dalla soluzione amminica, sono soggetti all’attacco della corrosione e la pressione parziale del CO2 in questi siti di nucleazione può essere considerevolmente più alta che nella soluzione normale. Quindi è possibile che il bicarbonato e probabilmente anche l’anidride carbonica possano essere presenti in queste zone. Inoltre è possibile che la corrosione dell’acciaio al carbonio possa essere dovuta in parte al CO2 liberato dall’ammina che forma soluzioni corrosive acquose di CO2 quando il CO2 libero entra in contatto con la condensa di acqua nelle zone non bagnate dalla soluzione amminica come ad esempio i passi d’uomo non isolati del rigeneratore. Kosseim e altri forniscono un’altra spiegazione sulla corrosione di gas ammino-acidi attribuibile agli ioni di idrogeno necessari per spiegare la corrosione dell’acciaio al carbonio (21) . Gli autori notano che i gas acidi reagiscono con le ammine per formare gli ioni di alcanolammonio e gli anioni dei gas acidi: H2S + R 3N = R3NH + HS (14) CO2 + R3N + H2O = R3NH+ + HCO3 (15) CO2 + 2R2NH = R 2NH 2+ + R 2 NCO 1 Gli ioni di alcanolammonio sono acidi perché possono fornire gli ioni di idrogeno per una reazione di corrosione. Il metallo corrosivo (ferro in questo caso) reagirà con l’acido più forte o più concentrato nella soluzione. Nelle soluzioni amminiche, lo ione di alcanolammonio è l’acido più forte e (eccetto l’acqua) il più concentrato. Perciò la reazione (3) può essere riscritta nella seguente forma: Fe + 2R 3NH+ = Fe2+ + H2 + 2R3N (17) La reazione (17) implica che i tassi di corrosione dovrebbero aumentare proporzionalmente alla concentrazione degli ioni di alcanolammonio e generalmente questo è vero. Le soluzioni più ricche sono più corrosive di quelle più povere. Lo ione di idrogeno non appare nella reazione (17); quindi il pH non influenza direttamente il tasso di reazione. Di conseguenza le soluzioni di MEA non degradate sono più corrosive della DEA non degradata, perché la MEA, la base più forte, scarica meno nello stripper e trattiene una maggiore concentrazione di ioni di alcanolammonio per cui la base più forte trattiene più acido (ioni di alcanolammonio) e forma una soluzione più corrosiva. 11 La reazione (17), come la reazione (3), è irreversibile; perciò il suo rateo non può essere influenzato dalle concentrazioni dei suoi prodotti. In particolare, gli anioni acidi termostabili e i prodotti di degradazione dell’ammina che formano complessi con ioni ferrosi, non dovrebbero influenzare il proprio rateo anche se l’esperienza mostra che questi contaminanti spesso aggravano la corrosione. La ragione probabilmente è che la reazione (16) è una reazione totale caratterizzata da numerose fasi. La fase che determina il rateo può essere costituita dall’attacco degli atomi di ferro sulla superficie di acciaio al carbonio da parte degli agenti complessi. Inoltre, questi agenti complessi che si associano agli ioni ferrici e ferrosi probabilmente inibiscono il passaggio da attivo a passivo evitando la formazione di uno strato passivo di ossido ferrico insolubile. Per queste ragioni, i sali termostabili e i prodotti di degradazione dell’ammina possono fortemente influenzare i tassi di corrosione, sebbene possono non comparire nelle reazioni di corrosione totale. Le soluzioni incontaminate delle ammine terziarie come la MDEA generalmente non sono corrosive indipendentemente dal gas acido lavato. Secondo l’API 945, le soluzioni della maggior parte delle ammine non sono corrosive se il rapporto tra idrogeno solforato e anidride carbonica è sopra 1/20, perché la reazione di corrosione porta alla formazione di uno strato protettivo di solfuro (2). Le combinazioni più corrosive sono quelle delle ammine primarie o secondarie con l’anidride carbonica, o perché gli ioni di carbonato formano complessi con lo ione ferroso o perché gli ioni di carbonato sono difficili a rigenerarsi. Di conseguenza, con ammine come la MEA, gli ioni di alcanolammonio o in alternativa i gas acidi corrosivi, sono presenti nella sezione più calda del rigeneratore di ammina. Effetto dei carichi molari acidi di ammina e della temperatura sulla corrosione dell’acciaio al carbonio La Figura 3 mostra l’effetto dei carichi di CO2 sulla corrosione dell’acciaio al carbonio. (22) Ad una data concentrazione dell’ammina, la corrosione aumenta quando aumenta il carico di CO2. Attraverso l’esperienza, le linee guida generali si sono ampliate riguardo ai carichi massimi accettabili dell’ammina povera e ricca. La Tabella 2 riassume i carichi raccomandati della soluzione povera e ricca ottenuti dalle varie fonti. Come ci si può aspettare, ci sono variazioni considerevoli su queste raccomandazioni. Una delle ragioni per queste differenze è che i carichi massimi ignorano l’effetto passivante dell’H2S sul carico molare massimo ammissibile della ammina. Di conseguenza queste raccomandazioni sono da considerarsi conservative. La corrosione dell’acciaio al carbonio dovuta agli alti carichi molari di ammina povera può essere limitata controllando le operazioni di strippaggio nel rigeneratore di ammina. Il grado di strippaggio dei rigeneratori di ammina è in funzione di due variabili: 1. Quantità di vapore di strippaggio per unità di volume della soluzione di ammina ricca oppure, 2. Rapporto di mole di acqua di riflusso rispetto al gas acido che esce dalla testa del rigeneratore dell’ammina. Sono di uso comune due metodi per controllare il grado di strippaggio dell’ammina povera. Il primo usa il controllo del rapporto di flusso per settare il flusso medio di calore del ribollitore ad un valore fisso rispetto al flusso di ammina ricca (kg di vapore per mc di soluzione o lb di vapore per gallone di soluzione di ammina ricca). L’ammina ricca può essere adeguatamente strippata usando tra i 110 e 133 kg di vapore per mc di soluzione di ammina ricca (da 0,9 a 1,1 lb di vapore per gallone). (23) Il secondo metodo di controllo utilizza la temperatura tra il piatto superiore del rigeneratore ed il condensatore di testa per resettare il flusso medio di calore al ribollitore. Questo controlla le mole di acqua di riflusso per mole di gas acido che lascia il rigeneratore, perché ad una 12 pressione operativa di servizio del rigeneratore, la temperatura sopra il piatto superiore è direttamente correlata alla % mol. di acqua nel gas acido che lascia il piatto superiore. Solitamente, un rapporto di riflusso di 1,0-2,0 mole di acqua per mole di gas acido è adeguato per strippare la maggior parte delle ammine. (9,10) Fitzgerald e Richardson forniscono una guida per lo strippaggio della MEA in funzione del rapporto H2S/CO2 nel gas di alimentazione (24,25) . Secondo Smith e Younger queste linee guida possono essere usate per la DEA.(26) Come mostra la figura 3, gli alti carichi molari di ammina ricca possono portare ad una corrosione eccessiva. La Figura 6 descrive una strategia di controllo usata per limitare i carichi molari di ammina ricca e controllare la corrosione. (27) Come mostrato nella Figura 6, in un assorbitore di ammina tipico, la maggior parte del calore di reazione è dato sul fondo della colonna. Se c’è troppo poca ammina in relazione alla quantità di gas acido, la temperatura aumenta nella parte superiore della colonna. Se c’è troppa ammina, la temperatura aumenta verso il fondo della colonna ed i carichi di gas acido sono bassi. Utilizzando la temperatura sul fondo dell’assorbitore di ammina per settare il flusso di ammina, come illustrato nella Figura 6, si mantiene relativamente costante il carico molare di ammina ricca. Ciò riduce la possibilità di corrosione rilevante dovuta a sovraccarico temporaneo della soluzione ricca di ammina e riduce anche il pompaggio di ammina povera e i costi di strippaggio dell’ammina ricca. Butwell raccomanda l’aumento delle concentrazioni di ammina piuttosto che l’aumento dei carichi di ammina. (28) Sebbene le soluzioni di ammina concentrata sono più difficili da strippare, le soluzioni più concentrate sono preferite specie se il ribollitore ha abbastanza capacità per rigenerare la soluzione. Anche la figura 5 mostra che per un carico molare acido costante, la corrosione dell’acciaio al carbonio aumenta quando aumenta la temperatura. Per ridurre la corrosione, le temperature di esercizio del ribollitore sono generalmente contenute entro i valori massimi. La Tabella 3 riassume varie raccomandazioni. Nella maggior parte dei casi, è auspicabile limitare la temperatura di vapore del ribollitore a circa 150°C (300°F). Effetto del rapporto H2S/CO2 sulla corrosione dell’acciaio al carbonio Secondo le istruzioni API 945 si concorda che la maggior parte delle soluzioni amminiche non sono corrosive se il rapporto tra il solfuro di idrogeno e l’anidride carbonica è sopra 1/19, perché quando è presente sufficiente H2S si forma uno strato protettivo di solfuro di ferro come avviene nella reazione (18) (2). Fe + H2S = H2 + FeS (18) Lo strato di solfuro ferroso è sufficientemente aderente per prevenire ulteriore corrosione, a condizione che l’azione di erosione-corrosione sia prevenuta da una buona progettazione meccanica e non siano presenti impurità di gas come il cianuro, che rimuovono lo strato di solfuro protettivo. La mancanza di corrosione con alti rapporti H2S/CO2 è stata sfruttata nel processo SNPA-DEA in cui sono stati raggiunti carichi molari acidi da 0,77 a 1,0 mole di gas acido per mole di ammina (23). Alti carichi molari acidi potranno essere raggiunti anche con altre ammine in condizioni di un alto rapporto H2S/CO2; tuttavia non sono stati pubblicati dati di conferma. Senza dati di conferma, i carichi molari acidi di soluzione ricca riportati da Dupart e riassunti nella Tabella 2, dovrebbero essere osservati, sebbene ignorino l’effetto del rapporto H2S/CO2 (10) Numerosi studi sono stati pubblicati sull’effetto del rapporto H2S/CO2 sulla corrosione dell’acciaio al carbonio da parte delle soluzioni di ammina. (29, 30, 31, 32) I risultati di Froning e Jones sono riassunti nelle Figure 4 e 5. La Figura 4, che riassume i test in ambienti di N2/H2S/H2O/MEA, 13 suggerisce che una pressione minima parziale di H2S è richiesta per prevenire la corrosione dell’acciaio al carbonio. La Figura 5, che riassume le prove in ambiente N2/H2S/CO2/H2O/MEA, mostra che la corrosione dell’acciaio al carbonio è minima ed indipendente dal rapporto H2S/CO2 fino a che il gas acido contiene almeno 5 vol% di H2S. Poichè le prove furono condotte a pressione atmosferica, 5 vol% di H2S corrisponde alla pressione parziale di H2 di 5,1 kPa (0,74 psia). Ciò suggerisce tre possibili interpretazioni dei risultati di Froning e Jones: 1. La corrosione dell’acciaio al carbonio sarà minima finchè la pressione parziale di H2S è maggiore di 5,1 kPa (0,74 psia). 2. Per ridurre la corrosione dell’acciaio al carbonio il rapporto H2S/CO2 dovrebbe essere maggiore di 1:19 (il gas acido dovrebbe contenere almeno 5 vol% di H2S). 3. Per la corrosione minima di acciaio al carbonio il rapporto H2S/CO2 dovrebbe essere maggiore di 1:19 (il gas acido dovrebbe contenere almeno 5 vol% di H2S) e la pressione parziale di H2S dovrebbe essere maggiore di 5,1 kPa (0,74 psia). L’alternativa 2 costituisce la base delle linee guida previste nelle norme API 945 . (33) Tuttavia, l’alternativa 3 è l’interpretazione più conservatrice dei test di Froning e Jones ed è più conforme ai dati dei test. In ogni caso, i risultati delle Figure 4 e 5 dovrebbero essere usati con cautela perché Froning e Jones riportano che si verifica pitting quando la concentrazione di solfuro di idrogeno ed il rapporto di H2S/CO2 sono bassi. (29) I test di corrosione riportati da Riesenfeld e Blohm confermano la conclusione di Froning e Jones che non c’è correlazione tra il tasso di corrosione dell’acciaio al carbonio ed il rapporto H2S/CO2 finchè c’è sufficiente H2S presente per formare uno strato protettivo ed inibire la corrosione dell’acciaio al carbonio. (18,19,20) McNab e Treseder hanno anche fatto ricerche sull’effetto del rapporto H2S/CO2 sulla corrosione dell’acciaio al carbonio nella soluzione amminica . (30) I loro risultati, che sono basati sulle prove con soluzioni di disopropanolammina (DIPA o ADIP) non supportano le conclusioni di Froning e Jones. E’ possibile che questa discrepanza sia dovuta all’uso da parte di McNab e Treseder di contenitori di vetro sigillati per le prove di corrosione. Si sa che il silicio inibisce la corrosione della soluzione di ammina, ed il silicio dei contenitori di vetro potrebbe influenzare i risultati delle prove. (29) Effetto dei sali termostabili e dei prodotti di degradazione delle ammine L’anidride carbonica e il solfuro di idrogeno sono acidi abbastanza deboli e le loro reazioni con le ammine sono termicamente reversibili. Gli acidi sufficientemente forti, tali che le loro reazioni con le ammine non sono reversibili termicamente, sono chiamati acidi termostabili. E cioè, prodotti che reagiscono con le ammine formando sali termostabili. Se gli acidi termostabili entrano in un impianto di ammina o sono generati per reazione con tracce di ossigeno o per degradazione termica dell’ammina, i sali termostabili restano nella soluzione e ivi si accumulano. I sali termostabili hanno varie origini. Nelle raffinerie, i gas FCCU possono contenere tracce di acidi formici e acetici. Le tracce di ossigeno nei vari gas di raffineria (FCCU, Delayed Coker, Unità Vuoto, Sistema recupero Vapore), le entrate di aria nei sistemi di assorbimento del gas funzionanti sotto vuoto, l’ossigeno presente nei serbatoi di stoccaggio ammina non pressurizzati e nei serbatoi di raccolta drenaggi possono reagire con l’ammina per formare acidi carbossilici e con l’H2S per formare zolfo elementare e tiosolfato. Nelle raffinerie, lo zolfo elementare può reagire con il cianuro per formare tiocianato. I sali termostabili riducono la capacità di rimozione dei gas acidi della soluzione amminica perché reagiscono irreversibilmente con l’ammina. Le soluzioni di ammina possono essere corrosive se 14 sono contaminate da sali termostabili. (10) I sali temostabili sono corrosivi perché abbassano il pH della soluzione amminica aumentano la conduttività della soluzione e possono agire come agenti chelanti, dissolvendo lo strato protettivo che copre il metallo di base. E’ anche possibile che alcuni acidi termostabili più leggeri, come l’acido formico, si ricombinino nel rigeneratore di ammina per formare l’acido libero, che può poi reagire con l’acciaio al carbonio esposto. I prodotti di degradazione dell’ammina-CO2, alcuni dei quali sono forti agenti chelanti, possono anche contribuire alla corrosività della soluzione amminica rimuovendo gli strati protettivi di ossido o solfuro. (34,35) Mentre si concorda che i sali termostabili e i prodotti di degradazione dell’ammina contribuiscono alla corrosione della soluzione amminica, non esiste una spiegazione definitiva del processo di corrosione. Infatti è probabile che numerosi fattori, incluso l’abbassamento del pH della soluzione amminica e gli effetti chelanti, contribuiscono alla corrosione dell’acciaio al carbonio da parte dei sali termostabili e dei prodotti di degradazione dell’ammina. Rigenerazione dell’ammina. Il funzionamento in slip stream degli impianti di purificazione (reclaimers) rende possibile mantenere costante la concentrazione della soluzione amminica circolante e prevenire l’accumulo di sali termostabili corrosivi e dei prodotti di degradazione dell’ammina. Le tecniche commerciali usate per rigenerare le soluzioni amminiche includono: la distillazione a batch sotto vuoto; distillazione atmosferica o ad alta pressione (rigenerazione termica); rigenerazione con resine a scambio ionico ed elettrodialisi. La distillazione semplice ad alta pressione o quella atmosferica può essere utilizzata solo per la MEA e il DGA che sono ammine primarie. Le ammine secondarie (DEA e DIPA) e l’MDEA, un’ammina terziaria, devono essere rigenerate con distillazione sotto vuoto, con resine a scambio ionico o elettrodialisi perché queste ammine si decompongono a temperature atmosferiche di distillazione. In numerosi riferimenti sono fornite le istruzioni sul reclaming termico della MEA . (9,36,37,32,38) La rigenerazione del DGA è stata studiata da Kenney, le resine a scambio ionico da Keller e l’elettrodialisi dalla Dow Union Carbide. (39,40,41) La rigenerazione delle ammine secondarie e terziarie è di solito eseguita su base contrattuale quando necessaria, mentre le ammine primarie sono rigenerate durante il normale ciclo operativo. La rigenerazione delle ammine dovrebbe essere presa in considerazione quando il contenuto dei sali termostabili è maggiore del 10% della concentrazione amminica attiva. (10) Neutralizzazione sali termostabili . Soda caustica è spesso aggiunta alle soluzioni di DEA e MDEA per neutralizzare i sali termostabili. Questo metodo è efficace per ridurre la corrosione. (26,42,43) L’aggiunta di soda caustica riduce la corrosività della soluzione amminica ed alza il pH della soluzione. Inoltre riduce la corrosione prevenendo la ricombinazione di acidi più leggeri come l’acido formico in forma molecolare durante la rigenerazione dell’ammina. Sebbene l’aggiunta di soda caustica può limitare la corrosione, la quantità che può essere aggiunta è limitata, perché alla fine i sali solidi formatisi precipiteranno creando occlusioni sugli scambiatori e sulle tubazioni. Tuttavia la precipitazione dei solidi può essere evitata se l’aggiunta di soda caustica si combina con la rigenerazione della soluzione amminica utilizzando la distillazione semplice, lo scambio ionico o l’elettrodialisi. L’aggiunta di soda caustica è ottima per le ammine secondarie e terziarie come la DEA e l’MDEA. Quindi per queste ammine, l’aggiunta di soda caustica può essere effettuata per controllare la corrosione fino a quando non è previsto in loco il loro reclaiming. Secondo Scheirman, la soda caustica dovrebbe essere aggiunta prima nelle soluzioni di DEA quando la concentrazione di sali termostabili raggiunge lo 0,5 wt.%. (44) Circa il 20 wt.% dei sali di sodio può essere tollerato prima che i solidi iniziano a precipitare. Il carbonato di potassio può essere anche usato per neutralizzare i sali termostabili ed ha il vantaggio di essere circa il 25% wt più solubile dei componenti di sodio. (44) 15 Per le soluzioni di MDEA, Liu e Gregory raccomandano che la soda caustica venga aggiunta per mantenere il contenuto dei sali termostabili di ammina sotto i 2 wt.% (43) La soluzione di MDEA dovrebbe essere rigenerata quando il contenuto anionico totale dei sali termostabili raggiunge i 40.000 ppm (43). Effetto del tipo di ammina sulla corrosione della soluzione amminica E’ ormai noto che la scelta dell’ammina influenza la corrosione. (10, 17) Le ammine primarie come la MEA e la DGA sono più corrosive delle ammine secondarie come la DEA e la DIPA. A loro volta la DIPA e la DEA sono più corrosive delle ammine terziarie come la MDEA. Esattamente non si sa il perché di tutto questo. Come notato da Dupart e altri, (10,17) numerosi ricercatori hanno dimostrato che tutte le ammine sono allo stesso modo non corrosive quando non contengono contaminanti acidi. (29,30,31,45,46) Perciò le differenze nel tipo di corrosione non sono dovute alla sola ammina. La MDEA è diversa dalla MEA, dalla DEA, dalla DIPA e dalla DGA per il fatto che non forma prodotti di degradazione di ammina-CO2. Tuttavia, ricerche da parte di Polderman e altri riguardo la MEA e da parte di Chakma e Meisen per la DEA suggeriscono che mentre i prodotti di degradazione di ammina-CO2 contribuiscono alla corrosione, non costituiscono la causa primaria .(34,35) Come notato da Dupart e altri, è possibile che la capacità delle ammine primarie e secondarie a formare carbamati secondo la reazione (16) può determinare la differenza tra i vari tipi di corrosione. (10,17) Forse le ammine più basiche come la MEA sono più corrosive per la presenza di ioni di alanolammonio nella parte più calda del rigeneratore di ammina. Fe + 2R3NH + = Fe2+ + H2 + 2R 3N (19) Le ammine meno basiche come la DEA sono più facili da rigenerare, e poiché le concentrazioni di ioni di alkanolammonio sono basse sul fondo colonna del rigeneratore di ammina, le ammine meno basiche sono meno corrosive. Erosione-corrosione L’erosione e la corrosione sono causate dalle alte velocità delle soluzioni di ammina, dalla turbolenza e dall’urto del gas e dell’ammina contro le superfici metalliche. L’erosione-corrosione rimuove lo strato protettivo di solfuro o ossido di ferro che protegge le tubazioni e le apparecchiature dalla corrosione. Le zone soggette ad erosione-corrosione includono le tubazioni che vanno dalla valvola di riduzione della pressione dal contattore al flash drum della ammina ricca, le tubazioni che vanno dalla valvola di controllo del livello del flash drum di ammina ricca al rigeneratore di ammina, e alla pompa di ammina povera. Altre zone interessate includono il fascio tubiero dello scambiatore di calore vicino il bocchello di entrata, il contattore di ammina vicino l’ingresso del gas acido, e l’ingresso di ammina ricca nella colonna di rigenerazione. L’erosionecorrosione è aggravata dalla soluzione di ammina “sporca” contenenti solidi sospesi. L’erosionecorrosione può essere ridotta scegliendo materiali giusti di costruzione ed una buona progettazione meccanica che riduca gli urti, la turbolenza e la velocità della soluzione amminica. La filtrazione meccanica della soluzione amminica rimuove i solidi sospesi e riduce anche l’erosione-corrosione. Erosione-corrosione delle tubazioni La norma API 945 raccomanda la progettazione delle tubazioni in acciaio al carbonio per entrambe le ammine ricche e povere per velocità inferiori a 1,8 m/sec (6 piedi/sec).(2) La Tabella 2 riassume altri tipi di raccomandazioni riguardo alle velocità. Come notato, le velocità raccomandate vanno da 0,9 a 1,8 m/sec (da 3 a 6 piedi/sec.). Mentre non esistono ricerche pubblicate che supportano queste raccomandazioni, si pensa che la norma API 945 rappresenti una buona pratica perché è un 16 documento accettato dall’industria. Sheilan, Smith, Dingman e altri raccomandano l’uso di tubi senza saldatura e curve a lungo raggio per ridurre l’erosione-corrosione dei tubi di ammina. (47,48) Sheilan e Smith suggeriscono anche di evitare gli attacchi filettati o le raccorderia a tasca da saldare (47) Erosione-corrosione di scambiatori e ribollitori Ballard e Dingman raccomandano l’uso di entrate e uscite multiple per ridurre la corrosione nei ribollitori kettle e in quelli orizzontali a termosifoni.(9,48) Sheilan e Smith raccomandano degli schermi perforati all’ingresso degli scambiatori di calore per evitare la corrosione dovuta ad urto .(47) Ballard e Connors suggeriscono dei ribollitori con spazio di disimpegno per ridurre la turbolenza della ebollizione e la risultante erosione-corrosione.(9,49) Entrambi raccomandano la rimozione delle file di tubi per formare una “V” o “X” negli impianti esistenti in cui la ebollizione violenta costituisce un problema. Ballard raccomanda la progettazione di scambiatori e ribollitori con i fasci tuberi posizionati in modo che sia facilitata la pulizia e ridotta l’erosione-corrosione, mentre Connors, Dingman , Smith e Younger consigliano di mantenere le velocità dell’ammina negli scambiatori di calore in acciaio al carbonio sotto lo 0,9 m/sec (3 piedi/sec). (9,49,48,26) Tuttavia, questa raccomandazione può essere troppo conservativa come le raccomandazioni sulla velocità (1,8 m/sec o 6 piedi/sec) riassunte in Tabella 4, perciò queste possono essere applicate anche agli scambiatori di calore. Ballard consiglia anche che il fascio tubiero del ribollitore venga coperto con 15 – 20 cm (6-8 pollici) di liquido per evitare essiccamento localizzato e surriscaldamento.(9) Raccomanda anche di posizionare il fascio tubero del ribollitore circa 15 cm (6 pollici) sopra il fondo del ribollitore per permettere la circolazione libera dell’ammina nel fascio tubiero.(9) La valvola di controllo vapore del ribollitore dovrebbe essere ubicata all’ingresso del ribollitore (non all’uscita della condensa) per evitare alte temperature localizzate dovute ad eccesso di vapore del ribollitore e conseguente corrosione. (9) Come mostrato nella Figura 1, gli scambiatori di ammina povera/ricca dovrebbero essere posizionati a monte della valvola di controllo livello del flash drum ammina ricca, per ridurre il flashing all’interno degli scambiatori, e l’ammina ricca dovrebbe essere sul lato tubo. Se gli scambiatori di ammina povera/ricca sono sovrapposti, l’ammina ricca dovrebbe salire attraverso lo scambiatore di fondo verso lo scambiatore superiore. Erosione-corrosione delle pompe di ammina povera. Per ridurre la turbolenza e l’erosionecorrosione delle giranti delle pompe di ammina povera e del corpo pompe, Sheilan e Smith raccomandano di posizionare a monte della pompa di aspirazione un tratto rettilineo di tubazione di un minimo di 8-9 diametri del tubo. Come mostrato nella Figura 1, le pompe di ammina povera dovrebbero essere posizionate a valle dello scambiatore di ammina povera/ricca perché la soluzione calda di ammina povera che lascia il rigeneratore è spesso vicina alla saturazione alla quota corrispondente l’aspirazione della pompa di ammina povera. Il posizionamento delle pompe di ammina povera a valle dello scambiatore di ammina povera/ricca assicura che l’ammina povera sia raffreddata prima di entrare nella pompa. Erosione-corrosione delle valvole di riduzione della pressione. Per ridurre l’erosione-corrosione delle valvole di riduzione della pressione a valle degli assorbitori, Graff raccomanda l’uso di corpi in acciaio al carbonio con interni in 316 SS con sede ed otturatore in stellite quando il ? p sulla valvola è superiore a 7÷14 barg (da 100 a 200 psig). (50) Scheirman raccomanda valvole a globo con interni 316 SS in stellite, ma suggerisce anche di scegliere valvole aventi corpo di dimensioni massime possibili per ridurre la velocità dell’ammina nel corpo della valvola. (51) 17 CRICCHE NELL’ACCIAIO AL CARBONIO SUGLI IMPIANTI AMMINICI Sono stati identificate quattro tipologie di cricche dell’acciaio al carbonio negli impianti di lavaggio del gas con alcanolammina. Osservazioni relative a queste tipologie sono state fornite da Merrick, Buchheim, Gutzeit e nelle norme API 945. (52,53,54,2) I primi tre tipi di cricche sono collegati all’ingresso dell’idrogeno atomico nel reticolo dell’acciaio al carbonio. Questi tre processi sono conosciuti come cricche da stress per presenza di solfuri (SSC – Sulfide Stress Cracking), cricche provocate da idrogeno (HIC – Hydrogen Induced Cracking), e cricche da stress provocate da idrogeno (SOHIC – Stress Oriented Hydrogen Induced Cracking). Questi tre processi richiedono la produzione di idrogeno atomico in soluzione acquosa-H2S. Mentre non esiste alcun limite di concentrazione dell’H2S, la pratica nell’industria ha portato ad assumere che le soluzioni acquose contenenti più di 50 ppmw di H2S possono provocare cricche. (11) Nella fase vapore, una soglia comunemente usata per l’SSC è una pressione parziale di H2S di 0,34 kPa (0,5 psia). Ciò che distingue questi tre meccanismi l’uno dall’altro è il modo in cui si imprigiona l’idrogeno atomico all’interno del reticolo del metallo, se si ricombina per formare idrogeno molecolare, l’orientamento e le caratteristiche delle cricche provocate, e le misure correttive necessarie per ridurre ogni tipo di cricca. La quarta tipologia di cricca è quella delle cricche da stress per corrosione alcalina (ASCC – Alcaline Stress Corrosion Cracking). Si pensa che questo processo sia causato dalla rottura del film protettivo. Le zone stressate, come quelle delle saldature, rompendo il film protettivo espongono l’acciaio nudo, che si corrode formando le cricche. Il film protettivo si riforma, ma il restante stress causa una nuova rottura del film provocando ulteriore corrosione. La ripetizione di questo processo causa le cricche. Segue una sintesi su ogni tipologia di cricche. Nelle norme API 945, Allegato A sono forniti gli esempi di ogni tipologia di cricche. (2) SSC (cricche da stress per presenza di solfuri – Sulfide Stress Cracking) L’acciaio al carbonio è indebolito dall’idrogeno atomico penetrato nel reticolo del metallo. Nelle zone intaccate dal calore delle saldature ci sono spesso piccole zone con alta durezza associate a zone con alta sollecitazione residua che vengono indebolite dall’idrogeno atomico penetrato in maniera così forte da causare la rottura. Questi tipi di cricche sono collegate direttamente alla quantità di idrogeno atomico disciolto nel reticolo del metallo e solitamente si verificano a temperature sotto i 90°C (194°F). (54) L’SSC dipende anche dalla composizione, microstruttura, sforzo, livelli di stress residui e applicati sull’acciaio. (53) Cricche da stress per presenza di solfuri sono state trovate nelle saldature continue nel circuito di testa del rigeneratore di ammina, sul fondo dell’assorbitore di ammina, sopra la colonna del rigeneratore di ammina, e sul lato ammina ricca dello scambiatore di ammina povera/ricca. (54) Queste zone suggeriscono che le cricche sono dovute soprattutto alla corrosione da gas acido umido. Vedere Figura 1. Questa forma di cricche può essere generalmente evitata limitando la durezza delle saldature dell’acciaio al carbonio a meno di 200 Brinell (BHN) e riducendo la tensione di sollecitazione dell’acciaio a meno di 621 Mpa (90 ksi). (55,56) Il trattamento termico dopo la saldatura è ottimo per eliminare le cricche, perché riduce la durezza e gli stress. (52,53) 18 HIC (Cricche provocate da idrogeno) Quando gli atomi di idrogeno penetrati nell’acciaio al carbonio incontrano una inclusione non metallica come i solfuri o una ossidazione, una scoria, una laminazione o altre discontinuità, spesso si combinano irreversibilmente per formare idrogeno molecolare. L’idrogeno molecolare, a differenza dell’idrogeno atomico, non può disperdersi perciò si accumula e crea alta pressione all’interno del metallo. Infine la pressione fa separare l’inclusione metallica dando luogo a cricche o blistering. Il blistering è parallelo alla superficie dell’acciaio perché la laminazione dell’acciaio al carbonio o le inclusioni sono formate in modo parallelo alla superficie dell’acciaio al carbonio quando l’acciaio è laminato durante la costruzione. Questo tipo di cricche raramente si verificano nelle forme di prodotti che non siano piatti o prodotti da piatti. HIC è chiamato anche “cricche da corrosione di idrogeno” (Hydrogen Blistering Cracking) o “cricche graduali” (Stepwise Cracking) e dipende dalla composizione e dalla pulizia dell’acciaio. Si verifica generalmente soprattutto sul fondo delle colonne dell’assorbitore, nel circuito di testa del rigeneratore di ammina, e nella parte superiore della colonna rigeneratrice di ammina. (54) Queste zone evidenziano che la causa principale dell’HIC è la corrosione del gas acido umido. L’HIC può essere evitato utilizzando piatti in “acciaio pulito” prodotti in modo speciale e più resistenti all’HIC rispetto all’acciaio al carbonio convenzionale. L’acciaio al carbonio resistente all’HIC è soggetto a trattamento a caldo con calcio o metallo raro per il controllo delle forme delle inclusioni residue dei solfuri. Un Rapporto del Comitato Tecnico Internazione della NACE pubblicato recentemente descrive la costruzione e i test dell’acciaio resistente all’HIC. Poiché le cricche provocate da idrogeno dipendono dalla purezza dell’acciaio al carbonio e dal suo metodo di costruzione, l’HIC non può essere evitata con il trattamento a caldo post saldatura.. (53) SOHIC (Cricche da stress provocate da idrogeno – Stress Oriented Hydrogen Induced Cracking) Come l’HIC, il SOHIC è causato da idrogeno atomico penetrato nell’acciaio al carbonio che si combina irreversibilmente per formare idrogeno molecolare. L’idrogeno molecolare si accumula con le imperfezioni nel reticolo del metallo proprio come nell’HIC. Tuttavia, a causa degli stress residui o applicati, l’idrogeno molecolare intrappolato produce delle microfessure che si allineano e si collegano in direzione della parete. Il SOHIC può propagarsi dal blistering causato dall’HIC e dall’SSC, e dalle imperfezioni delle saldature. (53,54) Tuttavia, né l’HIC né l’SSC sono precursori dell’SOHIC.(53) Negli impianti amminici, l’SOHIC è stato osservato principalmente nella sezione superiore della colonna rigeneratrice di ammina, nel circuito di testa del rigeneratore di ammina e nella parte inferiore dell’assorbitore sotto il piatto di fondo. (54) Come per l’HIC, queste zone suggeriscono che la causa primaria dell’SOHIC è probabilmente l’idrogeno atomico prodotto dalla corrosione del gas acido umido. Vedere figura 1. Il trattamento a caldo post saldatura (PWHT) migliora la resistenza dell’acciaio al carbonio all’SOHIC, ma non lo elimina totalmente (Buchheim, 1990). Negli anni recenti, molti utenti hanno utilizzato acciai al carbonio resistenti all’HIC, con PWHT, per resistenza all’SOHIC. Tuttavia, in condizioni di laboratorio molto corrosive persino gli acciaio resistenti all’HIC hanno dimostrato di essere suscettibili all’SOHIC. (55) Perciò è stata effettuata una placcatura dei piatti in acciaio al carbonio con acciaio inossidabile austenitico per eliminare il rischio di SOHIC. Poiché l’SOHIC è prevalente nella zona di testa del rigeneratore di ammina, la placcatura di questa zona, come mostrato in Figura 1, può prevenire sia l’SOHIC che l’HIC. 19 ASCC (Cricche da stress per corrosione alcalina – Alcaline Stress Corrosion Cracking) Come notato in precedenza, si pensa che l’ASCC sia causata da un processo di rottura del film protettivo. In zone ad alto stress residuo, come le zone calde delle saldature, lo slipping provoca la rottura del film, e l’acciaio che resta nudo si corrode per formare cricche. Se il tasso di corrosione è superiore al tasso di formazione del film, non si riformerà il film protettivo, e si verificherà pitting o altra forma di corrosione localizzata. Tuttavia, se la pellicola si forma più velocemente rispetto alla corrosione del metallo, lo strato protettivo sarà recuperato. La ripetizione di questo processo provoca l’aumento delle cricche da tensione di corrosione alcalina. L’ASCC è il processo di criccatura più comune negli impianti di trattamento del gas con alcanolammina. Si può verificare negli impianti che trattano CO2, H2S, o miscele di entrambi i gas acidi. (56,57) L’ASCC negli impianti di trattamento dei gas con ammina è stata riscontrata per la prima volta nel 1951 dal Comitato della NACE. (58) Nel 1953, Garwood osservò l’ASCC negli impianti MEA che trattavano gas naturale. (59) Furono scoperte cricche negli scambiatori di calore di testa, negli assorbitori di ammina, tubazioni e rigeneratori di ammina. Le cricche erano intergranulari e piene di ossido. Poiché si verificavano cricche solo nelle aree soggette a forte stress termico, fu raccomandato il PWHT per eliminare l’ASCC. Il risultato di questo lavoro iniziale, fu quello che nell’industria fu adottata la politica generale del PWHT per tutte le apparecchiature e le tubazioni (eccetto i serbatoi di stoccaggio) a contatto con l’ammina sopra una certa temperatura. In base alle compagnie e all’ammina usata, la temperatura scelta variava tra i 38° e i 93°C (100 e 200°F;) con 66°C (150°F) che costituiva una scelta comune. (56,57) Nel 1982, Hughes osservò delle ASCC nell’acciaio al carbonio non trattato con PWHT di un impianto di raffineria utilizzante MEA. (60) Le ASCC si erano verificate nelle saldature a contatto con l’ammina a temperature tra i 53 e i 93°C (127 e 200°F) mentre non erano apparse cricche nelle saldature PWHT che lavorano con temperature fino a 155°C (311°F). Hughes concluse che il PWHT eliminava le ASCC in tutte le tubazioni e apparecchiature in acciaio al carbonio in servizio con l’ammina. (60) Nel 1984, una colonna di lavaggio GPL con ammina di una raffineria degli Stati Uniti ebbe dei problemi che causarono una esplosione che uccise 17 persone. (61,62) Sebbene il disastro fu causato apparentemente da una combinazione di HIC e SOHIC, il disastro stesso e la rilevazione di cricche estese in altri impianti di ammina avviò le ricerche sulle criccature dell’acciaio al carbonio negli impianti di ammina. (63,64) Queste ricerche, che rivelavano molti tipi di ASCC, furono intraprese dal gruppo T-8 del Comitato della NACE in cooperazione con l’API. I risultati delle ricerche eseguite dal gruppo furono riportati nel 1989 da Richert e altri (56). La ricerca comprendeva 294 impianti di ammina, 272 dei quali erano di raffineria, e la maggior parte di essi erano impianti MEA e DEA. La ricerca indicava che le cricche si verificavano principalmente nei servizi con MEA. Quasi ogni cricca era associata con una saldatura che non aveva ricevuto trattamento a caldo post saldatura. Cricche si verificavano in ogni tipo di apparecchiatura, finanche a temperature ambiente. Tuttavia non fu trovata nessuna correlazione conclusiva tra le cricche e le variabili del processo, compreso il tipo di gas, la concentrazione dell’ ammina o il carico molare acido, l’uso di filtri o reclaimer, l’uso di inibitori di corrosione, tipo di acciaio al carbonio o aggiunta di soda caustica per neutralizzare i sali termostabili. Si scoprì che le ASCC erano indipendenti dal rapporto H2S/CO2. Tuttavia tutti gli impianti di ammina con meno di 1% mol. di H2S presente nel gas trattato furono soggetti a formazione di cricche. Ciò suggerisce che almeno 1 20 mol. % di H2S in un flusso con predominanza di CO2 ha la tendenza ad inibire l’ASCC. Questa conclusione fu confermata da successive ricerche di laboratorio. (65,66,67) I dati delle ricerche non potevano essere utilizzati per dimostrare che l’ASCC dipendeva dalla temperatura poiché la maggior parte delle apparecchiature funzionanti ad alte temperature erano trattate a caldo dopo la saldatura. Tuttavia, l’esperienza documentata da Garwood suggerisce che l’ASCC aumenta con l’aumento della temperatura quando le apparecchiature e le tubazioni non sono soggetti a PWHT. (59) Poiché il 98% delle cricche riportate nella ricerca si verificavano nelle saldature dell’acciaio al carbonio non trattate a caldo o sui bocchelli dove il PWHT è difficile, il PWHT di tutte le apparecchiature e tubazioni in acciaio al carbonio nei servizi di ammina fu considerato l’unica misura efficace preventiva per ASCC . Ulteriori dati successivi sugli impianti di trattamento gas DEA e DIPA, che riportavano ASCC sotto i 66°C (150°C) sia per la DEA che per la DIPA, evidenziavano la necessità del PWHT per prevenire le ASCC. (68) Un rapporto del Southwest Institute ed un conseguente articolo evidenziano che la ricerca della NACE comprende dati relativi solo a 16 impianti di trattamento di gas naturale su u totale di 294 impianti di ogni genere. (67,69) Questi riferimenti indicano che fu fatta una ricerca più completa sugli impianti di trattamento del gas naturale, ma i risultati della ricerca sono forniti solo in breve sintesi e non dicono quanti impianti sono stati esaminati. Entrambi i rapporti tuttavia forniscono i particolari relativi allo studio di laboratorio, che conclude che l’ASCC nell’acciaio al carbonio è inibita dalla presenza di H2S. Inoltre, secondo i due rapporti, l’ASCC nelle raffinerie si verifica principalmente nelle soluzioni di ammina povera mentre le cricche da ASCC negli impianti di gas naturale si verificano principalmente nelle soluzioni di ammina ricca. ATTACCO DA CLORURI SULL’ACCIAIO INOSSIDABILE NEI SERVIZI AMMINICI Negli impianti amminici si accumulano gradualmente delle impurità come i cloruri, fino a che non si raggiunge una concentrazione costante. Poiché la maggior parte degli impianti di ammina contengono acciaio inossidabile, è interessante sapere quali livelli di cloruro possono causare le pittino sull’acciaio inossidabile. Sono disponibili scarse informazioni su questo argomento. Gli esperimenti riportati da Seubert e Fallace indicano poca tendenza o l’assenza di tendenza da parte dell’SS 304 esposto a soluzioni di DGA contenenti fino a 4000 ppm di cloruri. (70) Sulla base di questi esperimenti il livello di cloruro massimo accettabile negli impianti DGA contenenti SS 304 fu stabilito a 1000 ppm. INIBITORI DI CORROSIONE Gli inibitori di corrosione sono spesso classificati come inibitori catodici, che inibiscono la reazione (2), inibitori anodici, che inibiscono la reazione (1), e inibitori di ossidazione che sono di seguito discussi. Gli inibitori catodici e anodici, come pure i film di ammine, sono spesso assorbiti dal metallo che viene corroso. Lo stesso avviene anche per l’arsenico e l’antimonio. Gli inibitori di corrosione sono stati raccomandati e brevettati molte volte, ma nessuno di essi ha avuto molto successo commerciale nel trattamento degli impianti amminici. (2) Gli inibitori di ossidazione sono agenti ossidanti molto più forti rispetto agli ioni di idrogeno, e funzionano portando il potenziale dell’acciaio ad un valore più positivo con il quale non avvengono le reazioni (1) e (2). Invece un inibitore ossida il ferro sulla superficie allo stato trivalente per formare un ossido ferrico che è molto aderente e protettivo. Questo ossido è chiamato film passivante. Tali inibitori funzionano bene negli impianti che rimuovono soltanto l’anidride 21 carbonica, riducendo a zero il tasso di corrosione e costituiscono gli unici inibitori efficaci per la MEA in assenza di idrogeno solforato. (2) Al contrario, essi sono distrutti dall’ idrogeno solforato. Gli inibitori di ossidazione lavorano bene quando vengono conservati adeguatamente, ma hanno molti inconvenienti. Prima di tutto devono essere analizzati e la loro concentrazione deve essere mantenuta. Secondo, devono essere protetti contro le impurità che li distruggono, inclusi il solfuro di idrogeno e grandi quantità di prodotti di corrosione del ferro, entrambi solubili e insolubili. Terzo, quando non funzionano, permettono spesso l’attacco localizzato se non anche un incremento della corrosione. Infine, molti di loro contengono metalli tossici e sono dispendiosi. CONCLUSIONI Negli ultimi 40 anni sono stati pubblicati numerosi documenti relativi alla corrosione degli impianti amminici. Lo studio di questi documenti costituisce un punto di partenza utile per avere una visione completa della corrosione negli impianti amminici e delle relative misure preventive. Come indica questo documento, la corrosione degli impianti amminici è causata da molti fattori inclusi i gas acidi, i sali termostabili, l’ossigeno, i prodotti di degradazione dell’ammina e, nelle raffinerie, le impurità dei gas come gli acidi organici, l’ammoniaca e il acido cianidrico. La corrosione può essere evitata grazie a numerose combinazioni tra scelte progettuali e scelta di materiali resistenti alla corrosione, lavaggio a monte dei gas da trattare, purga del riflusso del rigeneratore, purificazione dell’ammina (reclaiming) e PWHT. Seguono così come sono in inglese le referenze, le tavole e le figure. REFERENCES 1. de Waard, C. and Lotz, U, 1993, "Prediction of CO 2 Corrosion of Carbon Steel," Paper No. 69 presented at Corrosion/93. 2. API (American Petroleum Institute), 1990, "Avoiding Environmental Cracking in Amine Units," API Recommended Practice 945, 1st Edition, Aug, American Petroleum Institute, Washington, D.C. 3. Ehmke, E. F., 1981, "Polysulfide Stops FCCU Corrosion," Hydro. Proc., July, pg. 149-15S. 4. Ehmke, E. F., 1981, "Use Ammonium Polysulfide to Stop Corrosion and Hydrogen Blistering," paper #59, NACE, Corrosion/81, Ontario, Canada, April 6-10. 5. Ehmke, E. F., 1960, "Hydrogen Diffusion Corrosion Problems In a Fluid Catalytic Cracker and Gas Plant," Corrosion, May, pg. 116-122. 6. Fontana, M. G. and Greene, N. D., 1967, Corrosion Engineering. McGraw-Hill, NY, NY. 7. Neumaier, B. W. and Schillmoller, C. M., 1955, "Deterrence of Hydrogen Blistering at a Fluid Catalytic Cracking Unit," Proceedings of the API Division of Refining, Vol. 35, No. 3, pg. 92-109. 22 8. Gutzeit, J., 1986, "Refinery Corrosion Overview,. in Process Industries Corrosion - The Theory and Practice, Moniz, B. J. and Pollock, W. 1, editors, National Assoc. of Corrosion Engineers, Houston, TX, pg. 184. 9. Ballard, D., 1966, "How to Operate an Amine Plant," Hydro. Proc., Vol. 45, No. 4, pg. 137-144. 10. Dupan, M. S., Bacon, T. R., and Edwards, D. J., 1993, "Part 2 - Understanding corrosion in alkanolamine gas treating plants,", Hydrocarbon Processing, May, pg. 89- 94. 11. NACE International Publication 8x194, 1994, "Materials and Fabrication Practices for New Pressure Vessels Used in Wet H 2 S Refinery Service," NACE, Houston, TX, June. 12. Piehl, R. L., 1975, "Survey of Corrosion in Hydrocracker Effluent Air Coolers," Paper No. 5, presented at Corrosion/75, Ontario, Canada, April 14-18. 13. Bucklin, R. W. and Mackey, J. D., 1983, "Sulfur, Pollution and Corrosion Management in a Modern Refinery," paper presented at the 1983 AIChE Summer National Meeting in Denver, CO. 14. Polderman, L D. and Steele, A. B., 1956, "Why Diethanolamine Breaks Down ... in gas treating service," Oil and Gas J., July 30, pg. 206-214. 15. Norris, W. E. and Clegg, F. R., 1947, "Investigation of a Girbotol Unit Charging Cracked Refinery Gases Containing Organic Acids," Petroleum Refiner, Nov., pg. 107-109. 16. Kelley, A. E. and Poll, H. F., 1953, "Double-duty Gas Plant," Petrol Proc., Jan., pg. 55-59. 17. Dupan, M. S., Bacon, T. R., and Edwards, D. J., 1993, "Part 1 - Understanding corrosion in alkanolamine gas treating plants,", Hydrocarbon Processing, April, pg. 75- 80. 18. Riesenfeld, F. C and Blohm, C C, 1950, "Corrosion Problems in Gas Purification Units Employing MEA Solutions," Pet. ReL, Vol. 29, No. 4. pg. 141-150. 19. Riesenfeld, F. C and Blohm, C L 1951A, "Corrosion in Amine Gas Treating Plants," Pet. Ref., Vol. 30, No. 2. pg. 97-106. 20. Riesenfeld, F. C and Blohm, C ~, 1951B, "Corrosion Resistance of Alloys in Amine Gas Treating Systems," Pet. Ref., Vol. 30, Oct. pg. 107-115. 21. Kosseim, A. J., McCullough, J. G., and Butwell, K F., 1984, "Treating Acid & Sour Gas: Corrosion Inhibited Amine Guard ST Process," Chem. Eng. Prog., Oct., pg. 64-71. 22. Fochtman, E. G., Langdon, W. M., and Howard, D. R., 1963, "Continuous Corrosion Measurements," Chem. Eng., Vol. 7Q No. 2, pg. 140-142. 23. Wendt, C J. and Dailey, L. W., 1967, "Gas Treating: The SNPA Process," Hydrocarbon Processing, Vol. 46, No. 10, pg. 155-157. 23 24. Fitzgerald, K J. and Richardson, J. A., 1966, "How Gas Composition Affects Treating Process Selection," Hydro. Proc., Vol. 45, No. 7, pg. 125-129. 25. Fitzgerald, K J. and Richardson, J. A., 1966, "New correlation’s enhance value of monoethanolamine process," Oil and Gas J., Oct. 24, pg. 110-118. 26. Smith, R. F. and Younger, ~ M., 1972, "Tips on DEA Treating," Hydro. Proc., July, pg. 98-100. 27. Dingman, J. C. and Moore, T. F., 1968, "Gas Sweetening With Diglycolaminεâ," Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK 28. Butwell, K F., 1968, "How to Maintain Effective MEA Solutions," Hydro. Proc., Vol. 47, No. 4, pg. 111-113. 29. Froning, H. R. and Jones, J. H., 1958, "Corrosion of Mild Steel in Aqueous Monoethanolamine," Ind. & EnB. Chem., Vol. 50, No. 12, Dec., pg. 1737-1738. 30. MacNab, A. J. and Treseder, R. S., 1971, "Materials requirements for a gas treating process," Materials Performance, Vol. 10, No. 1, pg. 21-26. 31. Lang, F. S. and Mason, J. F., 1958, "Corrosion in Amine Gas Treating Solutions," Corrosion, Vol. 14, No. 2, pg. 105t-108t (Feb.). 32. Dow, 1962, Gas Conditioning Fact Book, The Dow Chemical Co., Midland, Michigan. 33. Gutzeit, J., 1994, Consultant, Personal Communication. 34. Polderman, L D., Dillon, C. P., and Steele, A. B., 1955, "Why MEA Solution Breaks Down in Gas Treating Service," Oil and Gas J., Vol. 54, No. 2, pg. 180-183. 35. Chakma, A. and Meisen, A., 1986, "Corrosivity of Diethanolamine Solutions and Their Degradation Products," Ind. Eng. Chem. Prod. Res. Dev., Vol. 25, No. 4, pg. 627-630. 36. Blake, R. J. and Rothert, K C., 1962, "Reclaiming Monoethanolamine Solutions," Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK 37. Blake, R. J., 1963, "Why Reclaim Monoethanolamine Solutions?" Oil and Gas J., Sept. 9, pg. 130134. 38. Jefferson Chemicals, 1963, "Monoethanolamine Reclaiming Part II, Design Considerations," Hydro. Proc. and Pet. Re£, Vol. 42, No. 10, pg 225. 39. Kenney, T. J., Khan, A. R., Holub, P. E., and Street, D. E., 1994, "DGA Agent Shows Promise for Trace Sulfur Compound Removal from Hydrocarbon Streams," paper presented at the 1994 GRI Sulfur Recovery Conference, May 15-17, Austin, TX. 40. Keller, A. E., Kammiller, R. M., Veatch, F. C., Cummings, A. L, and Thompsen, J. C., 1992, "HeatStable Salt Removal from Amines by the HSSX process Using lon Exchange," Laurance Reid Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK 24 41. Union Carbide, 1994, Sales Brochure, "The Union Carbide Corporation UCARSEP Process." 42. Butwell, K F., Kubek, D. J., and Sigmund, P. W., 1982, "AIkanolamine Treating," Hydro. Proc., March, pg. 108-116. 43. Liu, H. J. and Gregory, R. A., 1994, "Union Carbide Amine Management Program," paper presented at NACE Corrosion/94, March 3, Baltimore, MD. 44. Scheirman, W. L., 1973, "Diethanolamine Solution Filtering and Reclaiming in Gas Treating Plants," Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK. 45. Blanc C., Grall, M., and Demarais, G., 1982, "The Part Played by Degradation Products in the Corrosion of Gas Sweetening Plants Using DEA and MDEA," Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK 46. Blanc C, Grall, M., and Demarais, G., 1982, "Amine-degradation products play no part in corrosion at gas sweetening plants," Oil Gas J., Nov. 15, pg. 128-129. 47. Sheilan, M. and Smith, R. F., 1984, "Hydraulic-flow effect on amine plant corrosion," Oil and Gas J., Nov. 19, pg. 138-140. 48. Dingman, J. C, Allen, D. ~, and Moore, T. F., 1966, "Minimize Corrosion in MEA Units," Hydro. Proc, Vol. 45, No. 9, pg. 285-290. 49. Connors, J. S., 1958, "Aqueous-amine acid-removal process needn't be corrosive," Oil and Gas J., March 3, pg. 100-110. 50. Graff, R. A., 1959, "Corrosion in Amine Type Gas Processing Units," Ref. Eng., March, pg. C-12 -C14. 51. Scheirman, W. L., 1976, "Operating Experience With Amine Absorber Level Control Valves," Gas Conditioning Conference Proceedings, University of Oklahoma, Norman, OK 52. Merrick, R. D., 1989, "An Overview of Hydrogen Damage to Steels at Low Temperatures," Materials Performance, Feb. pg. 53-55. 53. Buchheim, G. M., 1990, "Ways to deal with wet H 2 S sacking revealed by study," Oil and Gas J., July 9, 1990, pg. 92-96. 54. Gutzeit, J., 1990, "Cracking of Carbon Steel Components in Amine Service," Materials Performance, September, pg. 54-57. 55. NACE International, Material Requirement MR0175-94, 1994, Standard Material Requirements, "Sulfide Stress Cracking Resistant Metallic Materials for Oilfield Equipment," NACE, Houston, TX. 55. Cayard, M. S., Kane, R. D., Horvath, R. J., and Prager, M., 1994, "Large-Scale Wet H 2 S Performance: Evaluation of Mechanical, Metallurgical and Welding Variables," Second 25 International Conference on Interaction of Steels with Hydrogen in Petroleum Industry Pressure Vessel and Pipeline Service, Vienna, Austria, October 1994. 56. NACE International, Refinery Practice RP0472-87, 1987, Standard Recommended Practice, "Methods and Controls to Prevent In-Service Cracking of Carbon Steel (P-1) Welds in Corrosive Petroleum Refining Environments," NACE, Houston, TX. 56. Richert, J. P., Bagdasarian, A. J., and Shargay, C. A., 1989, "Extent of stress corrosion cracking in amine plants revealed by survey," Oil and Gas J., June 5, 1989, pg. 45-52. 57. Richert, J. P., Bagdasarian, A. J., and Shargay, C. A., 1987, "Stress corrosion cracking of carbon steel in amine systems," Materials Performance, Jan., 1988, pg. 9-18. 58. Schmidt, H. W., Gegner, P. J., Heinemann, G., Pogacar, C F., and Wyche, E. H., 1951, Corrosion, Vol. 7, No. 9, pg. 295. 59. Ganvood, G. L., 1953, "What to do about Amine Stress Corrosion," Oil and Gas J., July 27, 1953, pg. 334-340. 60. Hughes, P. G., 1982, "Stress Corrosion Cracking in an M.E.A. Unit," Proceedings U.K National Corrosion Conference, Nov. pg 87-91. 61. McHenry, H. I., Shives, T. R., Read, D. T., McColskey, J. D., Brady, C. H., and Purtscher, P. T., 1986, "Examination of a Pressure Vessel that Ruptured at the Chicago Refinery of the Union Oil Company on July 23, 1984," National Bureau of Standards Report NBSIR 86-3049, March. 62. McHenry, H. I., Read, D. T., and Shives, T. R., 1987, "Failure analysis of an amine-absorber pressure vessel," Materials Performance, August, pg. 18-24. 63. Gutzeit, J. and Johnson, J. M, 1986, "Stress corrosion cracking of carbon steel welds in amine service," Materials Performance, Vol. 25, No. 7, July, pg. 18-26. 64. Anon., 1985, Minutes of NACE Group Committee Group T-8, March 27. 65. Schutt, H. U., 1988, "New Aspects of Stress Corrosion Cracking in Monoethanolamine Solutions," Materials Performance, Dec., 1988, pg. 53-58. 66. Parkins, R. N., and Foroulis, Z A, 1988, "Stress corrosion cracking of mild steel in monoethanolamine solutions," Materials Performance, Vol. 27, No. 1, Jan., pg. 19-29. 67. Lyle, F. F., Jr., 1988, "Stress Corrosion Cracking of Steels in Amine Solutions Used in Natural Gas Treatment Plants," Paper No. 158, Corrosion/88, NACE, St Louis, March 21-25. 68. Bagdasarian, A J., Shargay, C. A, and Coombs, J. W., 1991, "Stress Corrosion Cracking of Carbon Steel in DEA and 'ADIP' Solutions," Materials Performance, May, pg. 63-67. 26 69. SwRI, 1989 "An Investigation of Amine-Induced Stress Corrosion Cracking of Steels in Natural Gas Treatment Plants," Final Report SwRI Project No. 06-1202, prepared by the Southwest Research Institute, San Antonio, TX 70. Seubert, M. K and Wallace, G. D., Jr., 1985, "Corrosion in DGA Treating Plants," paper #159, Corrosion/85, NACE, Boston, Mass., March 25-29. 71. Montrone, E. D. and Long, W. P., 1971, "Choosing Materials for CO 2 Absorption Systems," Chem. Eng. Vol. 78, Jan., pg. 94-97. 72. Hall, G. D. and Polderman, L D., 1960, "Design and operating tips for ethanolamine gas scrubbing systems," Chem. Eng. Prog., Vol. 56, No. 10, pg. 52-58. 73. Ballard, D., 1986, "Cut Energy/Chemical/Corrosion Costs in Amine Units," Proc. of the Sixty-Fifth Annual Convention (Gas Processors Assoc.), Tulsa, OK, pg. 223-236. 74. Carlson, E. C., Davis, G. R., and Huysak, K L, 1952, "Corrosion in CO 2 -H 2 S-Amine System," Chem. Eng. Prog., Vol. 48, No. 7, pg. 333-336. 75. Campbell, J. M., 1981, Gas Conditioning and Processing, 4th Edition, Campbell Petroleum Series, Inc., Norman, O.K 27 28 29 30 31 32 33
Scarica