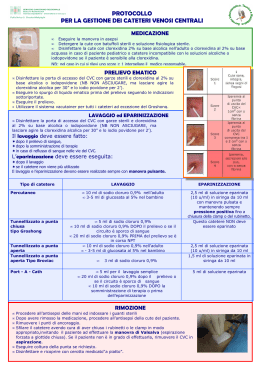
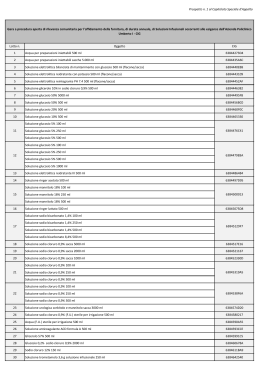
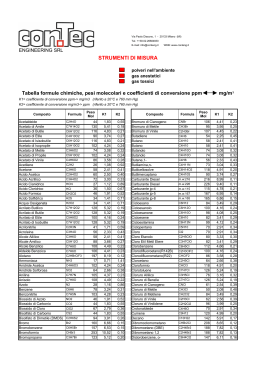
Il saggio alla fiamma è una tecnica utilizzata per scoprire l’identità degli elementi. BECCO BUNSEN FILO DI PLATINO BARIO POTASSIO SODIO CLORURO DI CALCIO RAME ACIDO CLORIDRICO 1. Accendiamo il becco Bunsen ; 2. Immergiamo il filo di platino nel cloruro di cui vogliamo analizzare la colorazione ; 3. Osserviamo il colore del cloruro analizzato; 4. Dopo aver eseguito l’esperimento dobbiamo pulire il filo di platino con l’acido cloridrico; 5. Ripetiamo l’esperimento per i tipi di cloruri che vogliamo analizzare. CLORURO DI BARIO Bario A contatto con una fonte di calore il cloruro di bario assume il colore arancione. Simbolo: Ba (Barys,“pesante”) N° atomico: 56 N° massa: 137,34 Gruppo: 2 A Periodo: VI Il bario è un elemento abbondante in natura. Il bario è un metallo argenteo, tenero, duttile, malleabile e volatile. E’ un elemento molto reattivo, elettropositivo e quindi riducente: reagisce con l'acqua e con l'ammoniaca, con l'ossigeno, lo zolfo, l'azoto, il carbonio, l'idrogeno e con quasi tutti i nonmetalli. CLORURO DI POTASSIO Potassio A contatto con una fonte di calore il cloruro di potassio assume il colore violetto. Simbolo: K (Kalium/Potassium,”alcalino,potassa’’) N° atomico: 19 N° massa: 39,09 Gruppo: 1A (metalli alcalini) Periodo: IV Il potassio è un metallo tenero, biancoargenteo, che si trova in natura combinato con altri elementi sia nell'acqua di mare che in molti minerali. Si ossida rapidamente all'aria, ed è molto reattivo, specie con l'acqua. È facilmente infiammabile e corrosivo. CLORURO DI CALCIO Calcio A contatto con una fonte di calore il cloruro di calcio assume il colore rosso acceso. Simbolo: Ca (Calx,”calce”) N° atomico: 20 N° massa: 40,08 Gruppo: 2 A Periodo: IV Il cloruro di calcio è il sale di calcio dell'acido cloridrico; la sua formula chimica è CaCl2. A temperatura ambiente si presenta come polvere cristallina bianca, molto igroscopica, molto solubile in acqua e abbastanza solubile in etanolo. CLORURO DI RAME A contatto con una fonte di calore il cloruro di rame assume il colore verde/blu. Simbolo: Cu (Cuprum,”Cipro”) N° atomico: 29 N° massa: 63,55 Gruppo: 11 B Periodo: IV Con ogni probabilità il rame è il metallo che l'umanità usa da più tempo,sono stati ritrovati oggetti in rame datati 8700 a.C. CLORURO DI SODIO Sodio A contatto con una fonte di calore il cloruro di sodio assume il colore giallo. Simbolo: Na (Natrium,”soda”) N° atomico: 11 N° massa: 22,98 Gruppo: 1 A (metalli alcalini) Periodo: III È un metallo soffice, ceroso, argenteo e altamente reattivo, brucia con una fiamma gialla, si ossida a contatto con l'aria e reagisce violentemente con l'acqua. Notiamo che la fiamma di volta in volta cambierà colore a seconda del cloruro di cui abbiamo verificato l’identità dell’elemento. Potassio Calcio Bario Sodio In un elemento gli elettroni sono suddivisi su vari livelli e sottolivelli. Alcuni elettroni, eccitati da una fonte di calore, saltano al livello successivo, ma non riuscendo a mantenere la loro nuova posizione ritornano al livello iniziale. Ciò causa un emissione di energia sottoforma di radiazione che, a seconda della lunghezza d’onda, influenza il colore della fiamma. Gli spettri di emissione Le radiazioni elettromagnetiche generate dagli elettroni costituiscono lo spettro di emissione di ogni elemento. A seconda della lunghezza d’onda, possiamo notare sia onde visibili (i colori) che onde invisibili, oggi molto utilizzate nelle moderne tecnologie (ultravioletti, infrarossi, onde radio, microonde, raggi X, ecc...).
Scaricare