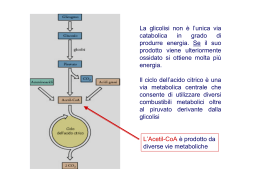
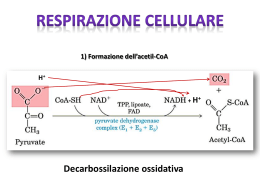
Ciclo dell’acido citrico 1 Il metabolismo ossidativo dei carburanti metabolici I gruppi acetili derivati da carboidrati, amminoacidi e acidi grassi entrano nel ciclo dell’acido citrico dove vengono ossidati a CO2 2 3 Il piruvato, derivato dal glucosio ad opera della glicolisi, viene ossidato formando acetil CoA e CO2 per azione di 3 enzimi organizzati nel complesso della piruvato deidrogenasi, localizzato nei mitocondri delle cellule eucariotiche. 4 Reazione complessiva catalizzata dal complesso della piruvato deidrogenasi. In questa reazione sono coinvolti cinque coenzimi e tre enzimi. 5 Reazione complessiva catalizzata dal complesso della piruvato deidrogenasi: La decarbossilazione ossidativa processo di ossidazione irreversibile: il gruppo carbossilico viene rimosso dal piruvato sotto forma di una molecola di CO2, e i 2 atomi di carbonio che restano diventano il gruppo acetilico legato al CoA. 6 La deidrogenazione e la decarbossilazione del piruvato ad Acetil CoA coinvolgono l’azione sequenziale di 3 enzimi diversi: piruvato deidrogenasi (E1), diidrolipoil transacetilasi (E2) diidrolipoil deidrogenasi (E3). e di 5 gruppi prostetici o coenzimi: tiamina pirofosfato (TPP) FAD CoA NAD lipoato. Ben 4 vitamine sono elementi essenziali di questo sistema: la tiamina per la TPP, la riboflavina per il FAD, la niacina per il NAD il pantotenato per il CoA 7 8 E2= diidrolipoil transacetilasi (24) E1= piruvato deidrogenasi (24) Intero complesso (60 subunità) E3= diidrolipoil Deidrogenasi (12) Organizzazione strutturale del complesso multienzimatico della piruvato deidrogenasi 9 10 11 Regolazione del complesso multienzimatico • l’attivazione avviene ad opera di una fosfoproteina fosfatasi che defosforila il cmplesso attraverso una reazione Mg2+ e Ca 2+ dipendente •L’inattivazione del complesso si realizza per azione di una proteina chinasi Mg 2+ATP-dipendente strettamente legata al complesso multienzimatico • l’acetil CoA e il NADH prodotti nella reazione inibiscono la forma defosforilata (attiva) dell’enzima, ma stimolano la proteina chinasi, promuovendo l’interconversione del complesso nella sua forma inattiva 12 • il CoA libero inibisce la proteina chinasi e il NAD • quando aumenta il rapporto NADH/NAD+mitocondriale o il rapporto acetil-CoA/CoA come avviene durante la ossidazione degli acidi grassi, il complesso della piruvato deidrogenasi è inattivato per azione della chinasi • il piruvato è un potente inibitore della proteina chinasi, quindi alti livelli di piruvato inibiscono la chinasi e attivano il complesso 13 Modificazione covalente della piruvato deidrogenasi negli eucarioti. 14 15 16 Funzione principale del Ciclo è quella di generare equivalenti riducenti che sono utilizzati per produrre energia, cioè ATP, nel processo di trasporto degli elettroni-fosforilazione ossidativa 17 CICLO DELL’ACIDO CITRICO Il ciclo dell’acido citirco ossida l’acetil CoA, il prodotto comune della degradazione di: • glucosio • acidi grassi • amminoacidi chetogenici a CO2 e H2O con produzione di NADH e FADH2 • molti amminoacidi glucogenici possono essere ossidati attraverso il ciclo dell’acido citrico grazie alla loro demolizione in uno dei suoi intermedi 18 L’attività degli enzimi dell’acido citrico: • citrato sintasi • isocitrato deidrogenasi • -chetoglutarato • è controllata dalla disponibilità di substrato e dall’inibizione a feedback da parte degli intermedi del ciclo 19 20 1a reazione: formazione di citrato • l’enzima citrato sintasi è inibito da elevate concentrazioni di NADH(H), ATP di succinil CoA e di acil-CoA che agiscono come effettori negativi • il citrato a sua volta agisce come effettore negativo della fosfofruttochinasi-1 21 L’intermedio citril-CoA non viene rilasciato dall’enzima durante la reazionee si ritiene che rimanga legato al sito catalitico della citrato sintasi • la citrato sintasi è presente nella matrice mitocondriale ed ha un peso molecolare di 100.000 22 23 2a reazione: formazione di isocitrato • la reazione aconitasica è fortemente inibita da fluoroacetato ( CH2-FCOO- ) un composto presente in certe piante del Sud Africa 24 Centro ferro-zolfo dell’aconotasi La reazione dell’aconitasi non richiede cofattori , essa richiede la partecipazione di ioni ferroso che gli vengono forniti dal centro ferrozolfo che è un componente essenziale dell ’attività idratasica dell’enzima 25 3a reazione: decarbossilazione ssidativa dell’isocitrato per formare achetoglutarato. Isocitrato deidrogenasi: NAD+ dip. (matrice mitocondriale, ciclo di Krebs) NADP+ dip.(citosol, reazioni anaboliche) • peso molecolare di 380.000 • è costituita da 8 sub unità identiche • è stimolata da ADP e in alcuni casi da AMP • è inibita da ATPe NADH+ 26 4a reazione: decarbossilazione ossidativa dell’ a-chetoglutarato in succinil-CoA e CO2 • questo complesso è identico a quello della piruvato deidrogenasi ma non è regolato da reazioni di fosforilazione e defosforilazione • il complesso è inibito da ATP, GTP da NADH e succinil CoA • sembra attivato da ioni calcio 27 La formazione di ATP o GTP a spese dell’energia rilasciata dalla decarbossilazione ossidativa dell’ achetoglutarato è un esempio di fosforilazione a livello del substrato Il GTP formato dalla succinil-CoA sintetasi può donare il suo gruppo fosforico terminale all’ADP per formare ATP, mediante l’azione reversibile della nucleoside difosfato chinasi. 28 29 5a reazione: Conversione del succinil-CoA a succinato • fase intermedia in cui la molecola dell’enzima diventa fosforilata a livello di un suo residuo di His presente nel sito attivo • Il gruppo fosforico viene quindi trasferito all’ADP o al GTP per formare ATP e GTP E ‘ questa l’unica reazione metabolica in cui il GTP è preferito all’ ATP • le cellule animali hanno 2 isozimi, uno per l’ADP e un altro per il GDP. 30 Reazione della succinil CoA sintetasi Un gruppo fosforico sostituisce il CoA legato all’enzima formando un fosfato ad alta energia Il succinil fosfato dona il gruppo fosforico a un residuodi His dell’enzima formando un fosfoenzima ad alta energia Il gruppo fosforico viene trasferito dal residuo di His al gruppo fosforico terminale del GDP 31 6a reazione: sintesi di fumarato • la succinato deidrogenasi è fortementa inibita da malonato e ossalacetato • è attivata da ATP, fosfato inorganico e succinato • il malonato inibisce l’enzima in modo competitivo, dovuto alla notevole somiglianza strutturale col succinato 32 La succinato deidrogenasi • è una flavoproteina che è inserita a differenza degli altri enzimi, nelle membrana mitocondriale interna favorendo il trasferimento diretto degli elettroni alla catena respiratoria • è’ costituito da due subunità di 70.000 e 30.000 m.w. rispettivamente • la prima contiene il sito di legame per il substrato, il FAD legato alla lisina e 4 atomi di ferro + 4 atomi di zolfo • la seconda contiene solo ferro e zolfo 33 7a reazione: idratazione del fumarato per produrre malato • la fumarasi è un tetramero con M.W. Di 200.000 34 Ultima reazione: ossidazione del malato a ossalacetato • in questa reazione con l’ossidazione del malato ad ossalacetato si rigenera il prodotto di partenza che così può riprendere il ciclo • l’ossalacetato può essere convertito anche in fosfoenol-piruvato o transaminato ad aspartato 35 36 37 38 Le reazioni anaplerotiche riforniscono il ciclo di Krebs di intermedi. In condizioni normali, esiste un bilanciamento quasi perfetto tra le reazioni che rimuovono intermedi dal ciclo e quelle che invece lo riforniscono, e quindi la concentrazione di questi composti resta costante. 39 CARENZA DI PIRUVATO DEIDROGENASI • Deficienze dei differenti componenti catalitici o subunità regolatrici • I bambini con questo deficit presentano alti livelli di lattato, piruvato e alanina che causano acidosi lattica cronica . . Presentano inoltre gravi danni neurologici. In molti casi questa carenza comporta la morte dell’individuo • La diagnosi viene fatta saggiando il complesso enzimatico e/o le sue subunità enzimatiche in colture di fibroblasti di pelle prelevata dal paziente •In alcuni casi i pazienti rispondono a un regime dietetico di tipo chetogenico con bassi livelli di carboidrati 40 DEFICIT DI FUMARASI • Il deficit di enzimi del ciclo degli acidi ticarbossilici è raro, tuttavia sono stati riportati alcuni casi in cui è presente un grave deficit di fumarasi sia a livello mitocondriale che citosolico • È presente un grave danno neurologico con encefalopatia e distonia che si manifestano precocementa dopo la nascita • Le urine contengono quantità anomale di fumarato e di una o più delle seguenti sostanze : succinato, -chetoglutarato, citrato e malato • Entrambi i genitori presentano livelli di attività enzimatica dimezzati rispetto al normale come si verifica nei disordini su base autosomica recessiva 41 Una molecola di glucosio può potenzialmente promuovere la sintesi di circa 38 ATP in condizioni di aerobiosi, cioè quando funziona il ciclo dell' acido citrico. 42 L’energia liberata dalle ossidazioni viene efficacemente conservata nel ciclo L’energia liberata dalle reazioni dell’intero processo viene conservata sotto forma di energia chimica mediante la formazione di un ATP o di un GTP e per riduzione di 3 NAD+ e di un FAD+. 43 Il ciclo dell’acido citrico produce di per sé una sola molecola di ATP per giro (nella conversione del succinil-CoA a succinato). Nelle 4 reazioni di ossidazione presenti nel ciclo viene prodotto un grande flusso di elettroni che entrano nella catena respiratoria, portando alla formazione di un gran numero di molecole di ATP nella fosforilazione ossidativa 44 45 Nella fosforilazione ossidativa il passaggio di 2 elettroni dal NADH all’ossigeno porta alla formazione di circa 2.5 molecole di ATP Il passaggio di 2 elettroni dal FADH2 all’ossigeno ne forma circa 1.5. Questa stechiometria ci permette di calcolare il numero totale di ATP dalla ossidazione completa del glucosio. 46 Quando le 2 molecole di piruvato sono ossidate completamente a 6 molecole di CO2 dalle reazioni del complesso della piruvato deidrogenasi e del ciclo dell’acido citrico e gli elettroni vengono trasferiti all’O2 dalla catena respiratoria, si ottengono tramite la fosforilazione ossidativa ben 32 molecole di ATP per molecola di glucosio 47 48 Questo processo ciclico a 8 tappe necessario per ossidare a CO2 il semplice gruppo acetilico a 2 atomi di carbonio può sembrare una complicazione inutile e soprattutto non in linea con il principio della massima economia della logica molecolare delle cellule. La funzione del ciclo di Krebs non è però esclusivamente quella di ossidare l’acetato; questa via infatti è il cuore del metabolismo intermedio. 49 I prodotti finali a 4 o 5 atomi di carbonio di molti processi catabolici entrano nel ciclo e possono servire come sostanze nutrienti. Per esempio, l’ossalacetato e l’a-chetoglutarato si formano rispettivamente dall’aspartato e dal glutammato quando vengono degradate le proteine introdotte nell’organismo con la dieta. In alcune situazioni, dal ciclo possono essere prelevati intermedi per usarli come precursori in una varietà di vie biosintetiche. 50 51 Negli organismi aerobici, il ciclo dell’acido citrico è una via anfibolica (serve sia ai processi anabolici sia a quelli catabolici). Non soltanto agisce nel catabolismo dei carboidrati, degli acidi grassi e degli aminoacidi, ma produce anche precursori per molte vie biosintetiche a-chetoglutarato = aspartato (prodotto per transamminazione) ossalacetato = glutammato per transamminazione). (prodotto 52 Attraverso l’aspartato e il glutammato, gli atomi di carbonio dell’ossalacetato e dell’a-chetoglutarato vengono usati per costruire altri aminoacidi, come pure i nucleotidi purinici e pirimidinici. L’ossalacetato viene convertito in glucosio nel processo della gluconeogenesi. Il succinil-CoA è biosintesi dell’eme. un intermedio fondamentale nella 53 54 Le reazioni anaplerotiche riforniscono il ciclo di Krebs di intermedi. In condizioni normali, esiste un bilanciamento quasi perfetto tra le reazioni che rimuovono intermedi dal ciclo e quelle che invece lo riforniscono, e quindi la concentrazione di questi composti resta costante. 55 La più importante reazione anaplerotica che avviene nel rene e nel fegato è la carbossilazione reversibile del piruvato per formare ossalacetato, catalizzata dalla piruvato carbossilasi. Quando il ciclo dell’acido citrico è povero ossalacetato o di qualsiasi altro intermedio, di il piruvato viene carbossilato a ossalacetato. L’aggiunta enzimatica di un gruppo carbossilico alla molecola del piruvato richiede energia, che viene fornita dall’ATP; l’energia libera necessaria a legare un gruppo carbossilico è quasi uguale a quella ricavabile da una molecola di ATP. 56 La piruvato carbossilasi è un enzima regolatorio ed è praticamente inattivo in assenza di Ac-CoA (modulatore positivo). Ogni qualvolta l’Ac-CoA è presente in eccesso stimola la reazione della piruvato carbossilasi a produrre più ossalacetato, consentendo quindi al ciclo di utilizzare più Ac-CoA nella reazione della citrato sintasi. 57 La reazione della piruvato carbossilasi richiede la biotina; questa vitamina è un trasportatore specializzato di gruppi a un atomo di carbonio nella loro forma più ossidata: la CO2 I gruppi carbossilici sono attivati in una reazione che idrolizza ATP e lega CO2 all’enzima a cui è legata la biotina. Questa CO2 “attivata” viene quindi donata a un accettore in una reazione di carbossilazione 58 La piruvato carbossilasi è composta da 4 subunità identiche, contenenti ognuna una molecola di biotina legata covalentemente mediante un legame amidico con il gruppo aminico e di uno specifico residuo di lisina. La reazione procede in 2 fasi; • prima il gruppo carbossilico derivato dall’HCO3- viene legato alla biotina, •poi il gruppo è trasferito al piruvato per formare ossalacetato 59 60 REGOLAZIONE DEL CICLO DELL’ACIDO CITRICO 61 Il ciclo dell’acido citrico è regolato a livello delle sue tre tappe esoergoniche Il flusso dei metaboliti attraverso il ciclo dell’acido citrico è sotto stretto controllo. Tre fattori governano la velocità del flusso attraverso il ciclo: 1.la disponibilità di substrato, 2.l’inibizione da accumulo di prodotti 3.l’inibizione allosterica retroattiva (a feedback) dei primi enzimi del ciclo da parte degli ultimi intermedi. Vi sono 3 tappe fortemente esoergoniche nel ciclo: 1. reaz. catalizzata dalla citrato sintasi 2. reaz. catalizzata dalla isocitrato deidrogenasi 3. reaz. catalizzata dalla a-chetoglutarato deidrogenasi 62 In condizioni normali la velocità della citrico glicolisi e del acido sono coordinate in modo che la quantità di glucosio metabolizzato a piruvato sia soltanto quella che poi entra nel ciclo dell’acido citrico sotto forma di Acetil-CoA. Piruvato, lattato e Acetil-CoA sono mantenuti a concentrazioni stazionarie. La velocità della glicolisi viene quindi adeguata a quella del ciclo dell’acido citrico non soltanto dai livelli di ATP e di NADH, che sono fase sia glicolitica sia respiratoria dell’ossidazione del glucosio, ma anche dal citrato. componenti della Quest’ultimo, cioè il prodotto della prima tappa del ciclo, è anche un inibitore allosterico della fosforilazione del fruttosio 6-fosfato da parte della fosfofrutto chinasi-1 della via glicolitica. 63 Il ciclo del citrato come piattaforma girevole del metabolismo. 64 L‘ aconitasi funziona in condizioni vicine all' equilibrio, per cui la velocità di consumo del citrato dipende dall'attività: 1.dell'isocitrato deidrogenasi NAD+-dipendente, che in vitro viene fortemente inibita dal suo prodotto NADH. 2. La citrato sintasi viene anche inibita dal NADH, ma è meno sensibile dell'isocitrato deidrogenasi alle variazioni della [NADH]. La citrato sintasi è anche inibita e dal citrato che compete con l'ossalacetato) 3. l'inibizione dell‘a-chetoglurarato deidrogenasi da parte del NADH e del succinil-CoA. Il succinil-CoA compete anche con l'acetil-CoA nella reazione della citrato sintasi (inibizione retroattiva competitiva). Questo sistema di inibizioni combinate aiuta a mantenere regolato il ciclo dell' acido citrico in modo coordinato. 65 Altri meccanismi regolatori Studi in vitro riguardanti gli enzimi del ciclo dell'acido citrico hanno permesso di identificare alcuni inibitori e attivatori allosterici. L’ADP è un attivatore allosterico dell'isocitrato deidrogenasi, mentre l'ATP inibisce questo enzima. Il Ca2+ oltre alle sue altre numerose funzioni cellulari, regola il ciclo dell' acido citrico in diversi punti: attiva la piruvato deidrogenasi fosfatasi, che a sua volta attiva il complesso della piruvato deidrogenasi per la produzione di acetilCoA. Il Ca2+, attiva anche l'isocitrato deidrogenasi e l‘a chetoglutarato deidrogenasi 66 Regolazione dell’acido del ciclo citrico. Questo schema del ciclo dell’acido citrico, che comprende anche la reazione della piruvato deidrogenasi, indica i punti di inibizione (ottagoni rossi) e gli intermedi della via che agiscono da inibitori (frecce rosse tratteggiate). ADP e Ca++ (sfere verdi) sono invece attivatori. 67 Così il Ca2+, il segnale che stimola la contrazione muscolare, stimola anche la produzione dell'ATP che andrà a supportarla Nel muscolo cardiaco, dove il ciclo dell' acido citrico è attivo, il flusso dei metaboliti lungo il ciclo è proporzionale alla velocità del consumo cellulare di ossigeno Poiché il consumo di ossigeno, la riossidazione del NADH e la produzione di ATP sono saldamente accoppiati, il ciclo dell'acido citrico deve essere regolato da meccanismi retroattivi che coordinino la produzione di NADH con il consumo di energia. 68 I più importanti regolatori del ciclo dell'acido citrico sono i suoi substrati, l'acetil-CoA e l'ossalacetato, e il suo prodotto, NADH. 69 Sia l'acetil-CoA sia l'ossalacetato sono presenti nei mitocondri a una concentrazione che non è in grado di saturare la citrato sintasi. l flusso metabolico lungo questo enzima varia quindi in funzione della concentrazione di substrato e viene controllato dalla disponibilità di quest'ultimo. Si è già visto che la produzione di acetil-CoA a partire da piruvato viene regolata dall' attività della piruvato deidrogenasi. 70 . La concentrazione di ossalacetato, che è in equilibrio con il malato, fluttua a seconda del rapporto [NADH]/[NAD+] seguendo l'espressione all'equilibrio K = [ossalacetato][NADH] [malato] [NAD+] Se, per esempio, aumenta il carico di lavoro del muscolo e la respirazione, nei mitocondri la [NADH] diminuisce. Il conseguente aumento della [ossalacetato] stimola l'attività della citrato sintasi, che controlla la velocità di formazione del citrato. 71 Diversamente da quanto accade agli enzimi che limitano la velocità della glicolisi e del metabolismo del glicogeno, i quali regolano il flusso mediante • elaborati sistemi di controllo allosterico • cicli del substrato • modificazioni covalenti gli enzimi regolatori del ciclo dell' acido citrico sembrano controllare il flusso principalmente mediante tre semplici meccanismi: 72 (1) disponibilità di substrato (2) inibizione da prodotto (3) inibizione retroattiva competitiva da parte di intermedi prodotti più avanti lungo il ciclo 73 74 fine 75
Scaricare