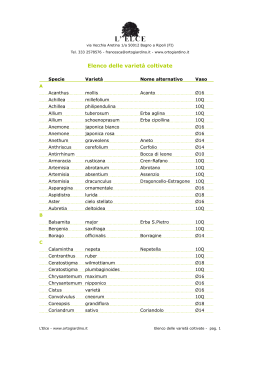
Le distrofie muscolari Lezione8 By NA Le distrofie muscolari Con questo termine vengono definite le miopatie di origine genetica la cui evoluzione è progressiva. Sul piano clinico la compromissione muscolare si traduce in una diminuzione di forza, a volte con una modifica del volume, della consistenza, dell’estensibilità e della contrattilità del muscolo (amiotrofia o al contrario ipertrofia). Le conseguenze funzionali variano a seconda della gravità, della topografia e dell’evoluzione della malattia. Il tipo di deficit motorio è specifico per ogni distrofia. Alcune toccano in maniera diffusa l’insieme della muscolatura, altre ne colpiscono selettivamente determinate aree. So tto questa definizione sono raggruppate malattie che si trasmettono sia come autosomiche dominanti e recessive che X linked recessive Distretti muscolari coinvolti nelle distrofie A Duchenne-Becker; B Emery-Dreifuss; C distrofia dei cingoli; D Distrofia facio-scapolo-omerale; E distale; F distrofia oculofaringea By NA Le distrofie muscolari By NA Distrofie dei cingoli (Limb-Girdle Muscular Distrophy-LGMD) In questo gruppo vengono raggruppate numerose patologie a trasmissione autosomica sia dominante LGMD1 che recessiva LGMD2. Non di tutte si conosce il gene coinvolto e/o la proteina interessata solo 16 (6 LGMD1 e 10 LGMD2) sono identificabili con il test molecolare. By NA La prevalenza non e’ nota, soprattutto per l’eterogeneita’ che caratterizza questo gruppo di malattie e la mancanza di una specificita’ diagnostica clinica fra le diverse forme. Una stima e’ stata fatta nel 2005 per le sarcoglicanopatie (LGMD2 C>F) da cui risulta una prevalenza di circa 1/170.000 con un frequenza dei portatori di circa 1/200 (non pochi). Solo la diagnosi molecolare consente di distinguere fra le diverse forme anche se non e’ semplice. Distrofie dei cingoli LGMD In questo gruppo vengono raggruppate numerose patologie a trasmissione autosomica sia dominante LGMD1 che recessiva LGMD2. Non di tutte si conosce il gene coinvolto e/o la proteina interessata solo 16 (6 LGMD1 e 10 LGMD2) sono identificabili con il test molecolare. By NA La prevalenza non e’ nota, soprattutto per l’eterogeneita’ che caratterizza questo gruppo di malattie e la mancanza di una specificita’ diagnostica clinica fra le diverse forme. Una stima e’ stata fatta nel 2005 per le sarcoglicanopatie (LGMD2 C>F) da cui risulta una prevalenza di circa 1/170.000 con un frequenza dei portatori di circa 1/200 (non pochi). Solo la diagnosi molecolare consente di distinguere fra le diverse forme anche se non e’ semplice. Distrofie dei cingoli recessive LGMD2 By NA La proteina titina LGMD2J By NA Il gene TTN, lungo circa 281 kb e composto da 313 esoni, codifica per la titina, una proteina del peso di 4.200 kDa e composta da 38138 aa Distrofie dei cingoli dominanti LGMD1 Le forme dominanti sono state descritte in singole famiglie anche se estese e sono considerate rare. By NA Emery-Dreifuss EDMD By NA Emery-Dreifuss EDMD Tre forme cliniche a ereditarieta’ diversa: due forme autosomiche, dominante e recessiva originate da mutazioni nel gene che codifica per la Lamina A/C , e una X linked recessiva originata dal gene della emerina. La forma recessiva e’ stata descritta in una sola famiglia. La prevalenza nel loro insieme non e’ nota, si ritiene che la X-linked sia 1/100.000, e che costituiscano nell’abito delle distrofie muscolari la terza categoria in termine di numero di affetti, seconde solo alle due distrofinopatie (Duchenne e Becker). By NA EDMD autosomica Genetica di AD/AR EDMD Il 76% degli affetti della forma dominante sono nuove mutazioni, pertanto il rischio per i fratelli e’ basso, anche se sono stati descritti casi di mosaicismo germinale: piu’ di un figlio affetto e mancanza di mutazioni nel DNA dei genitori. U na storia famigliare negativa potrebbe essere dovuta alla variazione di espressivita’ all’interno della famiglia, per cui un genitore non risulta affetto perche’ l’insorgenza potrebbe essere piu’ tardiva, o perche’ deceduto prima dell’inzio dei segni. Naturalmente il test molecolare puo’ fugare i dubbi. By NA EDMD autosomica By NA EDMD autosomica By NA EDMD autosomica By NA Sono state descritte oltre 237 mutazioni, l’85% sono missenso, che per la maggior parte delle missenso portano ad una proteina normalmente espressa. Relazione genotipo fenotipo Non e’ stata stabilita una relazione fra particolari mutazioni e fenotipo, i motivi risiedono nell’accentuata variabilita’ fra le famiglie e all’interno delle famiglie anche fra i portatori della stessa mutazione. Per esempio all’interno della stessa famiglia la stessa mutazione puo’ esprimersi provocando la ADEDMD, LGMD1B o DCM-CD cioe’ una delle laminapatie a carico del musculo striato EDMD autosomica By NA Diagnosi La presenza di emerina identificata con immuno fluorescenza o Western blot (dal momento che ubiquitaria, si puo’ fare su qualunque tessuto) indirizza verso le laminapatie, come pure la storia famigliare nei casi che lo sono. Gli stessi test non si possono fare direttamente per la lamina A/C perche’ quest’ultima e’ comunque presente anche negli affetti. La diagnosi molecolare ricercando le mutazioni nel gene LMNA e’ diagnostica, permette di identificare i portatori che non manifestano (utile per tenere sotto controllo i problemi cardiaci), per una eventuale diagnosi prenatale. Si esegue l’analisi della sequenza con lo scanning delle mutazioni che permette di identificare il 100% delle mutazioni puntiformi, per identificare le mutazioni di splicing e’, invece, necessario sequenziare il c-DNA. EDMD X-linked Cen 11.3Kb Filamina 26Kb Emerina 2Kb 11.3Kb Tel 48Kb Inversione in ~ 20% delle X By NA Tel EDMD X-linked By NA Il suo prodotto e’ l’emerina, proteina del peso di 29 kDa e composta da 254 aa, ricca di serine, espressa in molti tessuti. La sua localizzazione e’ nucleare, ancorata alla membrana interna per mezzo delle sua estremita’ idrofobica, mentre il resto della proteina idrofillica sporge nel nucleo dove interagisce con la lamina nucleare legandosi alla lamina A/C e a BAF, un’altra proteina coinvolta nell’assemblaggio del nucleo, nell’organizzazione della cromatina e nell’espressione genica, funzioni condivise anche dall’emerina e dalla lamina A/C. L’emerina e’ specificatamente coinvolta nell’espressione genica nella muscolatura striata. Relazione genotipo fenotipo La maggior parte delle mutazioni sono nulle e portano ad assenza dell’emerina ci si aspetterebbe un fenotipo con manifestazioni costanti sia fra le famiglie che al loro interno, ma e’ presente una variabilita’ nella gravita’ della malattia anche all’interno della stessa famiglia in cui la mutazione e’ la stessa. patogenesi molecolare delle distrofie di Emery- Dreifuss By NA Distrofia facio-scapolo-omerale FSHD D4Z4 cen ANT1 FRG1 FRG2 (TTAGGG)n -sat 4qB cen cen cen By NA 4qA -sat -sat 10q 10q Distrofia facio-scapolo-omerale FSHD La prevalenza e’ stimata essere compresa fra 4 e 10/100.000, la forbice ampia e’ legata alla presenza di affetti asintomatici ed e’ la terza distrofia in termini di frequenza dopo Duchenne e la distrofia miotonica considerando tutte le distrofie indipendentemente dalle modalita’ di trasmissione. Viene ereditata come autosomica dominante a penetranza ridotta con differenze fra i due sessi e nelle fasce di eta’: circa 83% considerando gli affetti intorno ai 30 anni, cioe’ se considero tutti i portatori della mutazione entro i 30 anni 83/100 manifestano i segni. Se suddivido questi portatori trentenni per sesso risultano affetti il 95% dei maschi e il 69% delle femmine il motivo di questa differenza e’ ignoto. Dopo i 50 anni la penetranza e’ ridotta al 2%. By NA Distrofia facio-scapolo-omerale FSHD By NA Genetica di FSHD La maggioranza degli affetti (70-90%) hanno un genitore che manifesta la malattia e/o presenta la mutazione. Il 10-30% sono de novo perche’ non ha ereditato ha la mutazione, il fatto che i genitori siano asintomatici non e’ significativo vista la penetranza ridotta, infatti prima di dire che ci si trova di fronte ad una nuova mutazione bisogna fare il test molecolare. Il gene FSHD Questo gene non esiste o meglio non l’hanno ancora trovato e forse non esiste proprio, inteso come singolo gene molecolare infatti praticamente tutti gli affetti hanno una delezione all’interno di una sequenza composta di unita’ di 3,3kb (D4Z4) ripetute in tandem in 4q35 , ma anche se sono stati individuati un certo numero di geni a valle del repeat non e’ stato ancora chiarito come e perche’ la delezione di D4Z4 provochi la malattia Distrofia facio-scapolo-omerale FSHD By NA Distrofia facio-scapolo-omerale FSHD D4Z4 cen ANT1 FRG1 FRG2 (TTAGGG)n -sat 4qB cen cen cen -sat -sat D4Z4 cen ANT1 FRG1 FRG2 10q 10q (TTAGGG)n -sat 4qA 4qB cen cen cen By NA 4qA -sat -sat sito di riconoscimento DRC 10q 10q Facio-scapolo-omerale D4Z4 cen ANT1 FRG1 FRG2 (TTAGGG)n -sat 4qB cen cen cen -sat -sat sito di riconoscimento DRC By NA 4qA 10q 10q meccanismo molecolare By NA PLOS GENETICS By NA PLOS GENETICS By NA PLOS GENETICS By NA Il materiale didattico e’ presente in rete : http://www.biologia.uniba.it/DIGEMI/Didattica.html sono presenti anche i file PDF degli articoli necessari per la preparazione By NA
Scaricare