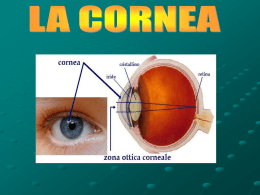
a cura di Claudio Macaluso e Lucio Buratto Mi opero di CORNEA CAMO CENTRO AMBROSIANO OFTALMICO © Copyright gennaio 2014 Camo S.p.A. Piazza Repubblica, 21 - 20124 Milano http://www.camospa.it - e-mail: [email protected] Tutti i diritti sono riservati È vietata ogni riproduzione totale e parziale. I N T R O D U Z I O Questa pubblicazione è dedicata a tutti quei pazienti che soffrono di problemi che coinvolgono la cornea, e che possono essere migliorati o risolti chirurgicamente. La chirurgia della cornea ha visto straordinari sviluppi negli ultimi anni. Grazie anche a grandi avanzamenti tecnologici, specie nel campo dei laser, il chirurgo oculista ha oggi a disposizione molteplici tecniche chirurgiche per intervenire sulla cornea. Tali tecniche vanno da procedure minimamente invasive fino a interventi chirurgici maggiori. Il caso del singolo paziente merita uno studio attento e una valutazione “su misura” della strategia chirurgica da adottare. L’avere a disposizione molte “armi” consentirà quindi al chirurgo oculista di scegliere la modalità meno invasiva e più adatta alla soluzione del singolo caso, tenendo conto di numerosi elementi, fra i quali non ultime le esigenze lavorative e di vita del paziente. Claudio Macaluso Lucio Buratto N E Per consultare gratuitamente altre pubblicazioni sui problemi dell’occhio andare sul sito www.camospa.it Il presente libretto viene stampato ad uso esclusivo dei pazienti in cura presso il Centro Ambrosiano Oftalmico 5 ANATOMIA DELL’OCCHIO L’occhio si compone di varie strutture anatomiche ognuna delle quali deve avere caratteristiche ben precise per consentire una visione corretta. La parte anteriore è costituita dalla cornea, una struttura di forma convessa formata da tessuto trasparente; proprio sulla cornea viene eseguita la maggior parte degli interventi Anatomia del bulbo oculare: si evidenziano le varie strutture che compongono l’occhio 6 “rifrattivi” che consentono cioè la correzione dei difetti di rifrazione (miopia, astigmatismo, ipermetropia). La cornea per consentire una buona vista deve essere trasparente e di forma regolare; in caso contrario, la vista ne viene compromessa in modo più o meno rilevante in relazione all’entità dell’anomalia. Ai lati la cornea si continua alla periferia con un tessuto quasi bianco, la sclera. Appena dietro la cornea c’è l’iride; quando si dice che una persona ha gli occhi azzurri ecc. ci si riferisce appunto al colore dell’iride. L’iride ha al centro un foro che è la pupilla, il diametro della quale varia con l’intensità della luce ambiente regolando così la quantità di luce idonea all’occhio per vedere correttamente. Dietro la pupilla e l’iride c’è il cristallino; si tratta di una lente trasparente, un po’ più grande di una lenticchia. Il cristallino ha lo scopo di filtrare e convergere la luce che entra nell’occhio in modo da convogliarla sulla retina; il cristallino ha la proprietà di cambiare la sua forma e quindi la distanza focale della luce che entra nell’occhio (processo di accomodazione); in tale maniera l’occhio è in grado di mettere a fuoco un oggetto situato a varie distanze, sia esso lontano o vicino. Dopo i 40 anni il cristallino perde pro- La cornea e il cristallino sono le lenti dell’occhio: la cornea è la piccola calotta trasparente che chiude la parte anteriore del bulbo oculare, mentre il cristallino è una piccola lente situata internamente. 7 gressivamente la sua capacità di mettere a fuoco gli oggetti vicini (ad esempio i caratteri della scrittura); è l’inizio della presbiopia, un fenomeno naturale di senescenza del cristallino. Se il cristallino diviene opaco in parte o completamente si ha la cataratta; in una tale evenienza occorre procedere chirurgicamente; per creare delle condizioni visive il più possibile vicine a quelle di un occhio normale, è importante inserire un cristallino artificiale al posto di quello opaco che è stato rimosso. Dietro il cristallino, c’è il vitreo, una sostanza gelatinosa e trasparente che riempie tutta la parte centrale posteriore dell’occhio. Sulla superficie posteriore dell’occhio, internamente, è situata la retina che è la membrana visiva dell’occhio; paragonando l’occhio ad una macchina fotografica essa ha le stesse funzioni della pellicola. La parte più importante, dal punto di vista visivo, della retina è la sua porzione centrale, la macula; è con la macula che uno legge, lavora al pc, guida la macchina. Se la macula subisce alterazioni (ad es. DMLE Degenerazione Maculare Legata all’Età) si ha una riduzione, anche consistente, della capacità visiva. La luce dopo esser passata attraverso la cornea, la pupilla, il cristallino, il vitreo raggiunge la retina; qui stimola alcune speciali cellule chiamate fotorecettori; esse trasmettono lo stimolo ad altre cellule che attraverso dei prolungamenti vanno a formare il nervo ottico. Il nervo ottico è costituito da prolungamenti delle cellule retiniche e trasporta gli impulsi nervosi dalla retina al cervello. Il cervello in una sua area chiamata corteccia visiva riceve gli impulsi nervosi dall’occhio, li elabora e ne permette la loro identificazione. Solo a questo punto si può parlare di visione e perché ciò avvenga correttamente è necessario che tutte le strutture fino ad ora menzionate siano integre e funzionanti. Da un punto di vista strettamente rifrattivo, cioè ottico, le due strutture più importanti sono la cornea ed il cristallino; ed è su queste che si può agire chirurgicamente per modificare la rifrazione di un occhio e quindi correggere i cosiddetti difetti di vista (miopia, astigmatismo, ipermetropia) e talora anche la presbiopia. 8 LA CORNEA: UNA LENTE DELL’OCCHIO La cornea, oltre a costituire il completamento più anteriore della parete dell’occhio, ne è anche la lente più “importante”. Ovviamente anche il cristallino è importante, anzi indispensabile per una perfetta visione. Ma in termini puramente di quanto “forti” o, tecnicamente, “potenti” sono queste lenti, risulta che la cornea ha un potere circa doppio rispetto a quello del cristallino. L’efficienza ottica della cornea dipende da due sue caratteristiche, straordinarie per un tessuto biologico (si pensi ad esempio all’assenza di vasi sanguigni), per le quali la possiamo considerare una vera lente: una perfetta trasparenza e una curvatura regolare. Una cornea trasparente e con curvatuVisione nell’occhio emmetrope, ra regolare, lavorando “insieme” ad un cioè privo di difetti rifrattivi: l’immacristallino trasparente, consente a un gine viene focalizzata esattamente occhio normale di vedere nitidamente sulla retina. (a condizione che anche le altre strutture dell’occhio siano normali). Nell’occhio emmetrope (cioè privo di difetti rifrattivi quali miopia, astigmatismo e ipermetropia) i raggi della luce, che entrano nell’occhio in modo parallelo vengono focalizzati dalla cornea e dal cristallino esattamente sulla retina in un singolo punto e producono una visione chiara e normale. Visione nell’occhio miope: l’immagi- Quando invece l’immagine non va a fuone viene focalizzata davanti alla reti- co sulla retina può cadere dietro (ipermena, arrivando così sfuocata sulla reti- tropia) o davanti ad essa (miopia) o in più na stessa (l’occhio miope è in genere di una zona (astigmatismo); in tali casi più lungo di un occhio emmetrope) si ha un “difetto di rifrazione”; nella gran 9 parte dei casi essi possono essere risolti facilmente con lenti da occhiale o con lenti a contatto; meglio ancora, possono essere corretti con chirurgia rifrattiva, mediante una procedura laser o chirurgica. Le procedure laser (LASIK, PRK) vengono eseguite proprio a livello della cornea; il laser modifica la curvatura Visione nell’occhio ipermetrope: corneale per renderla più adatta a quel l’immagine viene focalizzata oltre particolare occhio e quindi, eliminando la retina, rendendola così sfocata il difetto presente, migliorare la vista. (l’occhio ipermetrope è in genere Le procedure chirurgiche con impianto più corto di un occhio emmetrope di cristallino artificiale, prevedono invece l’inserimento di una piccola lente all’interno dell’occhio e sono utilizzate prevalentemente per difetti di una certa entità. In altre situazioni diverse dai semplici difetti di refrazione (miopia, ipermetropia, astigmatismo), la cornea può mostrare alterazioni della sua trasparenza o della sua forma, o anche un’associazione Visione nell’occhio astigmatico: dei due problemi. si formano due immagini, una per • Perdita di trasparenza. I raggi luogni asse dell’astigmatismo, ren- minosi, che per entrare nell’occhio, dendo l’immagine confusa e “allun- incontrano la zona dove la traspagata” (la superficie anteriore dell’oc- renza è perduta possono essere ferchio è più simile ad un pallone da mati e soprattutto diffusi in tutte le direzioni. Questa situazione porterà i rugby che ad un pallone da calcio) raggi luminosi provenienti dall’ esterno a diffondersi caoticamente sulla retina: l’immagine nel suo complesso ne risulterà sfocata, spesso molto gravemente. Situazioni che comportano tali problemi sono lo scompenso corneale/distrofia di Fuchs che riduce nel suo complesso la trasparenza, o una cicatrice corneale, che può essere di varie estensioni e densità. • Curvatura non regolare. In tal caso, i raggi luminosi vengono fatti convergere sulla retina in maniera irregolare. Non riescono quindi a formare un’immagine nitida, ma un’immagine così irregolare che risulterà inevitabilmente sfocata, a volte in modo intol- 10 Visione nell’occhio emmetrope senza malattie corneali (cornea trasparente e di curvatura regolare): l’immagine viene focalizzata esattamente sulla retina Visione nell’occhio con opacità della cornea: I raggi luminosi vengono intercettati dalle opacità, che li diffondono in tutte le direzioni, impedendo la formazione di un’immagine nitida sulla retina Visione dell’occhio con un’alterazione della curvatura corneale (come nel cheratocono): nonostante I raggi luminosi possano attraversare indenni la cornea, che è trasparente, vengono deviati in modo irregolare, non consentendo la messa a fuoco di un’immagine nitida sulla retina. lerabile. La situazione patologica che più comunemente induce alterazioni irregolari della curvatura corneale è il cheratocono. In casi fortunatamente molto più rari la cornea può anche assottigliarsi molto o addirittura perforarsi (in tale evenienza bisogna intervenire con urgenza) 11 LA CORNEA: COME E’ FATTA Vediamo ora più nel dettaglio come è fatta la cornea. Si tratta di una calotta trasparente spessa circa mezzo millimetro al centro (andando verso la periferia lo spessore aumenta progressivamente), con un diametro di circa 12 mm. Gli strati della cornea. I più importanti sono tre: l’epitelio, che la protegge e si rigenera in continuazione; lo stroma, che ne costituisce la struttura principale, l’endotelio, indispensabile a mantenere la trasparenza degli altri strati. Esistono inoltre altri due sottili strati: la membrana di Bowman, che costituisce un supporto per la crescita dell’epitelio corneale, e la membrana di Descemet. Quest’ultima è particolarmente robusta, ha una consistenza elastica e sostiene le cellule dello strato endoteliale. 12 Ha una struttura a lamelle saldamente adese, con vari strati dall’esterno all’interno. Epitelio corneale: E’ costituito da vari strati di cellule che si rinnovano continuamente. In seguito ad una abrasione corneale o anche dopo alcune procedure chirurgiche le cellule proliferano rapidamente per andare a riparare la zona che è rimasta scoperta. Per mantenere la sua integrità e trasparenza, la cornea non può rimanere a lungo scoperta dall’epitelio. Negli stati profondi dell’ epitelio corneale vi è una ricchissima innervazione, più densa che in ogni altra parte del corpo umano. Cio’ spiega la grandissima Quando lo strato più interno della cornea, l’endotelio, è danneggiato, la cornea perde trasparenza, con effetti sulla nitidezza dell’immagine simili a quelli di un vetro smerigliato. 13 sensibilità della cornea (basta una piccolissima abrasione della cornea per scatenare un dolore molto intenso) ed è fondamentale per la stessa integrità del tessuto (funzione detta “trofica”). Membrana di Bowman, confine fra stroma ed epitelio. Stroma: costituisce più del 90% dello spessore della cornea ed è composto prevalentemente da fibre collagene impacchettate molto strettamente in modo ordinato. Tale disposizione delle fibre garantisce la trasparenza. Membrana di Descemet, sottile ma robusta ed elastica. Endotelio corneale: è un singolo strato di cellule piatte di forma esagonale che tappezza completamente l’interno della cornea. Purtroppo queste cellule non sono in grado di moltiplicarsi se per traumi o malattie una parte di esse viene perduta. Anche se sottilissimo l’endotelio è indispensabile perché la cornea rimanga trasparente: le sue cellule infatti lavorano in continuazione “togliendo” acqua allo stroma corneale e indirizzandola all’interno dell’occhio. Senza questa azione di pompa le molecole di acqua in eccesso si incuneano fra le fibre collagene dello stroma e la trasparenza della cornea viene progressivamente perduta (si parla di scompenso corneale o scompenso endoteliale). Per esemplificare basta pensare alla differenza di trasparenza fra un vetro normale e uno smerigliato: il secondo lascia passare la luce ma diffonde i raggi luminosi in tutte le direzioni impedendo la trasmissione di immagini nitide. 14 GLI ESAMI PREOPERATORI Oltre a quelli che normalmente vengono eseguiti durante una visita oculistica, per stabilire l’idoneità dell’occhio ad un determinato intervento e alla pianificazione dell’intervento stesso, occorrono altri esami più specifici. Abbiamo visto come la cornea sia la lente più potente dell’occhio: non stupisce quindi come molti di questi strumenti ne analizzino le proprietà ottiche. La topografia corneale: serve a fare una precisa mappatura della curvatura della cornea: le eventuali irregolarità possono essere analizzate nel dettaglio per studiare la procedura chirurgica più adatta a correggerle. Gli strumenti più moderni permettono di analizzare le curvature sia della faccia anteriore che di quella posteriore della cornea. La pachimetria: serve a misurare lo spessore della cornea: in alcune patologie si possono riscontrare zone troppo sottili, in altre, come lo scompenso corneale, la cornea risulta ispessita. Gli strumenti più moderni non misurano lo spessore solo nel punto centrale della cornea, ma forniscono una mappa pachimetrica di tutta la cornea. L’OCT (Tomografia a Coerenza Ottica): serve a visualizzare nel dettaglio alcune caratteristiche dell’anatomia oculare in modo completamente non invasivo, come ad esempio la profondità esatta di eventuali opacità nello spessore della cornea, ma anche le condizioni della retina e del nervo ottico. La pupillometria: serve a misurare il diametro della pupilla: è fondamentale soprattutto se viene pianificato un intervento con il laser per correggere un difetto rifrattivo. L’aberrometria: serve ad identificare e quantificare alcune anomalie rifrattive della cornea e dell’occhio in generale; in tal caso esse possono essere eliminate o ridotte con un trattamento laser “personalizzato”, che può dare ottimi risultati in modo poco invasivo. 15 Curvatura corneale anteriore Curvatura corneale anteriore Curvatura corneale posteriore Curvatura corneale posteriore Topografia corneale. Gli strumenti più moderni non si limitano a fornire una mappa della curvatura anteriore della cornea (in alto), ma riescono ad analizzare la cornea anche “in sezione” (al centro), misurando quindi anche la sua curvatura posteriore, della quale ricavano un’ulteriore mappa (in basso). Si noti la differenza fra le curvature regolari della colonna di sinistra (caso normale), e l’aumento focalizzato della curvatura (zona “rossa”), tipica del cheratocono, nella colonna destra. 16 Spessore corneale (pachimetria) Spessore corneale (pachimetria) Pachimetria corneale. Mentre in passato ci si poteva accontentare di misurare lo spessore corneale solo al centro, oggi è possibile ricavare la misura dello spessore corneale in tutti i suoi punti analizzandone la sezione (in alto), ricavando delle vere e proprie “mappe” dello spessore corneale, o “mappe pachimetriche” (in basso). Si noti l’assottigliamento localizzato della cornea nel cheratocono (zona “rossa”, colonna destra) rispetto ad un caso normale (colonna sinistra). OCT della cornea. La tomografia a coerenza ottica della cornea permette di analizzarne con precisione le caratteristiche morfologiche anche in casi di ridotta trasparenza. In questo esempio si osservano nello spessore corneale varie zone opache (quelle più chiare), localizzandone esattamente estensione e profondità. Tali informazioni sono preziose per pianificare la migliore soluzione laser o chirurgica. 17 La microscopia endoteliale: serve a visualizzare e a misurare le cellule dell’endotelio corneale. Microscopia endoteliale. E’ possibile, in modo completamente non invasivo, fotografare le singole cellule dell’endotelio corneale, lo strato più profondo della cornea, indispensabile a garantirne la trasparenza. A sinistra un caso con un numero adeguato di cellule endoteliali. Mentre al centro si nota come le cellule siano in numero ridotto e di dimensioni aumentate, a destra si osservano delle macchie scure, dette guttae, tipiche della distrofia endoteliale: in queste situazioni la cornea si può scompensare e perdere trasparenza, ma è possibile risolvere il problema con il trapianto di endotelio. L’aberrometro consente, proiettando una serie di fasci luminosi dentro l’occhio ed esaminando il loro comportamento all’uscita, di ottenere importanti informazioni sulla qualità visiva dell’occhio. 18 LA CORNEA: QUALI PATOLOGIE Le patologie della cornea possono condurre alla necessità di intervenire chirurgicamente; sostanzialmente ciò avviene per riduzione della trasparenza, alterazione della curvatura, dolore, raramente per estremo assottigliamento o perforazione (in tali casi bisogna intervenire tempestivamente). Riduzione della trasparenza La cornea, la più potente lente dell’occhio, quanto meno è trasparente, tanto meno consentirà di vedere nitidamente. In casi lievi la conseguenza sarà un annebbiamento visivo, ma in casi avanzati la capacità visiva potrà essere ridotta alla percezione di forme indistinte. In casi così gravi la cornea ha in genere un aspetto biancastro. Quali sono le principali patologie che possono alterare la trasparenza della cornea? La formazione di cicatrici, in risposta a infezioni, a infiammazioni o in seguito a traumi, anche da agenti chimici. La guarigione mediante cicatrizzazione è una caratteristica comune di tutti i tessuti dell’organismo. Mentre però una piccola cicatrice sulla pelle al massimo può essere brutta da vedere, sulla cornea può compromettere seriamente la vista. Fra le infezioni sono comuni quelle batteriche che spesso insorgono secondariamente a microtraumatismi della superficie corneale da molteplici cause (ad es. lavori domestici, attività all’aria aperta, trauma da lenti a contatto), e quelle virali, soprattutto erpetiche (il Virus Herpes più comune, il Simplex o HSV, può recidivare e via via compromettere la trasparenza corneale). Anche altre patologie corneali che inizialmente alterano solo la forma della cornea, come il cheratocono, possono portare alla formazione di cicatrici Malattie specifiche della cornea, spesso con una componente ereditaria, dette distrofie corneali: nella maggior parte di queste 19 patologie si formano opacità nello spessore della cornea, a volte limitatamente agli strati superficiali, a volte coinvolgenti tutto lo spessore corneale. Le opacità tendono ad aumentare nel corso di alcuni anni e quindi portare alla necessità di intervenire chirurgicamente. La formazione delle opacità spesso dipende dall’accumulo di sostanze non trasparenti a causa di un errore metabolico determinato geneticamente: questo spiega perché le opacità nel tempo possono talvolta riformarsi anche nella cornea trapiantata. Lo scompenso corneale o endoteliale: l’eccessiva diminuzione del numero di cellule endoteliali conduce ad una eccessiva imbibizione dello stroma corneale che si gonfia e perde progressivamente trasparenza. Spesso nelle fasi iniziali della patologia l’annebbiamento è maggiore al risveglio con un miglioramento visivo dopo le prime ore della giornata. Questo fenomeno avviene perché le cellule endoteliali “superstiti” riescono a lavorare in modo più efficace quando l’occhio è aperto che quando la cornea è coperta dalle palpebre chiuse. Le cause più comuni di perdita endoteliale sono la “cornea guttata” o distrofia di Fuchs, le malattie infiammatorie dell’occhio, e i pregressi interventi chirurgici sul segmento anteriore dell’occhio, come quelli per cataratta o glaucoma, specie se si sono verificate complicanze. Altre cause di riduzione della trasparenza corneale sono dovute alla crescita al di sopra della cornea di membrane vascolarizzate come nello pterigio avanzato o agli esiti di gravi causticazioni. La gravità di compromissione della capacità visiva e il tipo di chirurgia che potrà essere effettuata dipendono soprattutto da due fattori, oltre che dalla presenza o meno di scompenso corneale: Dove tali opacità sono localizzate: centrali? Periferiche? se sono nella periferia corneale possono interessare poco la vista poiché la pupilla, unico passaggio “ottico” per arrivare a formare l’immagine sulla retina, è in genere nettamente più piccola della cornea ed è posizionata centralmente. In tali casi anche opacità dense non necessitano di terapia chirurgica. Una opacità anche piccola che invece interessi il centro della cornea ha conseguenze importanti sulla vista e spesso porta alla necessità di intervenire con la chirurgia. La profondità: le opacità sono superficiali? Profonde? A tutto spessore? Nei casi più favorevoli di opacità molto superficiali può essere sufficiente asportarle con il laser a eccimeri (vedi avanti 20 PRK/PTK) lo stesso che si usa per trattare i difetti di refrazione come la miopia, senza dover ricorrere a un trapianto. Negli altri casi sarà necessario asportare in parte o completamente la cornea opacizzata e sostituirla con tessuto sano da donatore (trapianto di cornea o cheratoplastica, che può essere superficiale o a tutto spessore). Scompenso corneale: se invece la perdita di trasparenza a tutto spessore è causata dalla scarsità di cellule endoteliali, si può oggi procedere a un trapianto selettivo particolare, detto appunto “endoteliale”: la cornea malata non viene asportata, ma viene rimosso solo lo strato di cellule alterate; poi, al suo posto, viene trapiantata solamente una sottile lamina ricca di cellule endoteliali sane che renderà la cornea di nuovo trasparente. Opacità corneali: che fare? Le opacizzazioni della cornea, dovute in genere a cicatrici o a distrofie, ne compromettono la funzione di lente e possono ridurre seriamente la capacità visiva. Non è detto che il problema sia risolvibile solo con un trapianto di cornea “tradizionale”, cioè la cheratoplastica perforante: tutto dipende in primo luogo dalla profondità con cui le opacità sono localizzate nello spessore corneale. Opacità superficiali - ablazione con laser a eccimeri (PTK) o anteriori - cheratoplastica lamellare anteriore superficiale Opacità profonde - cheratoplastica lamellare anteriore profonda (DALK) Opacità totali - cheratoplastica perforante (trapianto “tradizionale”, a tutto spessore) Scompenso corneale, cheratopatia bollosa, cornea guttata, distrofia endoteliale di Fuchs: che fare? I termini riportati nel titolo vengono spesso usati nello stesso contesto in modo anche intercambiabile: sono effettivamente strettamente imparentati ma non sono tutti sinonimi. Lo scompenso corneale si ha quando le cellule endoteliali di una cornea non sono più in numero sufficiente a mantenerla trasparente; nei casi più avanzati la cornea si riempie di troppa acqua che ne solleva lo strato più superficiale, l’epitelio, forman- 21 do delle bolle (oltre che ridurre gravemente la capacità visiva, possono provocare dolore e facilitare infezioni in caso di rottura): è la cheratopatia bollosa. La cornea guttata o distrofia endoteliale di Fuchs (medico viennese che descrisse la patologia all’inizio del ‘900) è la patologia che più comunemente conduce allo scompenso corneale e quindi alla cheratopatia bollosa. Si chiama “guttata” perché si formano dei depositi microscopici in forma di goccioline a livello dell’endotelio corneale. Esse provocano una rugosità che di per sé riduce la trasparenza corneale, ma soprattutto fanno soffrire le cellule endoteliali riducendone il numero e provocando quindi lo scompenso. In linea di massima è possibile schematizzare in questo modo il tipo di intervento necessario in base alla situazione clinica: Cornea guttata o distrofia endoteliale di Fuchs senza scompenso cor- osservazione (controlli oculistineale, buona trasparen- ci regolari) za senza scompenso cor- trapianto corneale endoteliale neale, trasparenza molto alterata (raro) Altre patologie che provocano perdita di cellule endoteliali scompenso corneale ini- osservazione e terapia con ziale, trasparenza accet- colliri (controlli oculistici regotabile lari) scompenso corneale, trapianto endoteliale trasparenza alterata scompenso corneale, trasparenza molto alterata, cheratopatia bollosa - trapianto corneale endoteliale - in attesa del trapianto terapia della cheratopatia bollosa (ad es. colliri, lente a contatto terapeutica, etc) scompenso corneale, cheratoplastica perforante trasparenza molto al- (trapianto corneale a tutto terata, con presenza di spessore) cicatrici corneali presenza di cataratta programmare asportazione (l’eventuale combinazione di interventi va valutata dal chirurgo) 22 Visione dell’occhio con un’alterazione della curvatura corneale (come nel cheratocono): nonostante I raggi luminosi possano attraversare indenni la cornea, che è trasparente, vengono deviati in modo irregolare, non consentendo la messa a fuoco di un’immagine nitida sulla retina. Alterazione della curvatura Anche a causa di modificazioni della sua forma o curvatura la cornea non funzionerà adeguatamente come lente. I raggi luminosi che colpiscono una cornea perfettamente trasparente, ma di curvatura non regolare, non potranno essere focalizzati correttamente sulla retina e ne risulterà un’immagine sfuocata. Le malattie che più comunemente determinano irregolarità della curvatura corneale sono le “ectasie” corneali, cioè situazioni nelle quali la struttura corneale si sfianca in un punto, assottigliandosi. La patologia ectasica più comune è il cheratocono ma esistono altre patologie meno frequenti come la degenerazione marginale pellucida e l’ectasia post-chirurgica Altre condizioni che portano a irregolarità della curvatura corneale dipendono solitamente da deformazioni causate da cicatrizzazione irregolare, in seguito a traumi ma anche in seguito a chirurgia. Dolore La cornea è la struttura più densamente innervata dell’organismo. Questo si traduce in una sensibilità spiccatissima. E’ sufficiente una piccola lesione dello strato più superficiale, l’epitelio corneale, per “scoprire” le terminazioni nervose e provocare dolore molto intenso accompagnato da fotofobia (fastidio alla luce). La ricrescita dell’epitelio in genere avviene in alcune ore o giorni e, se non sopravvengono complicanze come infezioni, vi è una guarigione completa e il dolore scompare. Una comune causa di interruzione dello strato dell’epitelio corneale (“abrasioni” corneali) sono i piccoli traumi, ma esistono anche vere patologie nelle quali lo strato dell’epitelio corneale continua a rompersi spontaneamente, creando situazioni di disagio intollerabile: Le erosioni corneali recidivanti possono essere dovute a rare 23 forme di distrofia corneale, a volte possono essere fatte risalire a pregressi traumi, foglie di pianta o unghiata o da foglio di carta (lesioni “lineari”), ma in altri casi non si individua una causa di questa aderenza imperfetta dell’epitelio corneale agli strati sottostanti. Tipicamente il dolore intenso compare al mattino, aprendo gli occhi per la prima volta dopo aver dormito. Se le misure di terapia medica non risolvono il problema, la terapia più efficace è il trattamento con laser a eccimeri (vedi avanti PRK/PTK), lo stesso utilizzato per correggere i difetti di refrazione come la miopia. In questo caso il laser viene usato per asportare un piccolo strato di cornea al di sotto dell’epitelio, scoprendone un altro più sano sul quale l’epitelio possa aderire meglio. La cheratopatia bollosa è invece un’altra conseguenza dello scompenso corneale (dovuto a mal funzionamento dell’endotelio): l’eccesso di liquido che conduce ad un ispessimento delle cornea e le fa perdere trasparenza, spinge anche verso l’esterno l’epitelio facendolo sollevare. A volte si tratta di piccole bolle, ma a volte queste confluiscono ed è facile che l’epitelio così sollevato si rompa provocando dolore intenso e sottoponendo la cornea al rischio di infezione. La terapia chirurgica in questi casi mira a curare la malattia alla base del problema (trapianto di endotelio). 24 CHIRURGIA DELLA CORNEA I trattamenti chirurgici che possono essere eseguiti sulla cornea sono molteplici. Si va da procedure per nulla invasive dette parachirurgiche come il Cross Linking Corneale (CXL), che si limita a irrigidire la struttura corneale, a trattamenti laser come PRK, Lasik, PTK, che agiscono solo sulla superficie della cornea, e ad altri nei quali la cornea viene rinforzata con l’impianto di inserti intrastomali, oppure anche sostituita in parte o per tutto il suo spessore (trapianti di cornea lamellari e perforanti). Le indicazioni ad eseguire un trattamento specifico vengono attentamente valutate dal chirurgo oculista e scelte per adattarsi al meglio a risolvere il singolo caso. PRINCIPALI CATEGORIE DI CHIRURGIA DELLA CORNEA Cross linking corneale (CXL) - aumenta la rigidità e la stabilità biomeccanica della cornea - previene la progressione e può ridurre miopia e astigmatismo nelle malattie ectasiche (cheratocono) Trattamenti laser a eccimeri (PRK customizzata, Lasik) - con la PRK si può ridurre l’astigmatismo irregolare in casi selezionati (spesso associata a CXL) - la Lasik viene spesso usata per correggere astigmatismi post-trapianto (oltre al laser a eccimeri si utilizza il laser a femtosecondi) Anelli intrastromali o ICR (intracorneal rings) - rinforzano la cornea con malattie ectasiche regolarizzandone la curvatura (minore astigmatismo) - meglio se impiantati con laser a femtosecondi Cheratoplastica perforante o a tutto spessore - viene sostituita la cornea per tutto il suo spessore - indicata quando la patologia corneale è molto avanzata Cheratoplastica lamellare anteriore - viene sostituita la cornea ad eccezione degli strati più profondi - indicata quando la sola parte anteriore della cornea è alterata (es. molti cheratoconi ed opacità) Cheratoplastica endote- viene sostituito solo lo strato endoteliale: la cornea del liale o lamellare posteriore ricevente è conservata quasi completamente - indicata quando c’è uno scompenso corneale (cornea guttata, cheratopatia bollosa) 25 RINFORZARE LA STRUTTURA CORNEALE: IL CROSS LINKING CORNEALE (CXL) Il cross linking corneale (CXL) è un trattamento fondamentale nella cura del cheratocono e delle altre ectasie corneali. Non è un intervento chirurgico, nel senso che non vengono effettuate incisioni, suture o altre manovre invasive; è un intervento chiamato “parachirurgico”. Il cross linking del cheratocono E’ una procedura non chirurgica che viene applicata per la terapia del cheratocono iniziale, cioè quando ancora lo spessore e le curvature della cornea sono discretamente o completamente conservate; è possibile applicare questo trattamento anche a pazienti affetti da cheratocono in uno stadio evolutivo più avanzato al fine soprattutto di limitare la velocità di progressione. Questo metodo chiamato cross linking del collagene corneale consiste nell’applicazione sulla cornea di un prodotto chiamato Riboflavina; esso viene poi attivato da una luce ultravioletta della famiglia dei raggi UVA. L’azione della luce associata al farmaco, stimola la cornea a rinforzare i legami tra le molecole che la compongono, determinando un arresto o quanto meno un rallentamento dell’evoluzione della malattia. Lo scopo è sostanzialmente quello di aumentare la rigidità e la resistenza della cornea. I risultati ottenuti fino ad ora sono molto favorevoli, in quanto i pazienti trattati presentano un rallentamento del processo di assottigliamento della cornea con una conseguente stabilizzazione del difetto visivo dovuto alla deformazione della cornea affetta da cheratocono. In alcuni casi si è anche assistito ad una lieve riduzione del difetto refrattivo con conseguente miglioramento della qualità visiva. Alla terapia consegue una stabilizzazione della malattia, una migliore tolleranza delle lenti a contatto, un beneficio della qualità della vista ed un allontanamento dell’ eventuale intervento di trapianto. Ci sono varie modalità di esecuzione del crosslinking; tutte comun- 26 que vengono fatte in anestesia con colliri, sono indolori ed eseguibili ambulatoriamente; la tecnica di esecuzione è semplice e poco invasiva rispetto alle altre proposte terapeutiche del cheratocono. Tecnica standard di esecuzione del crosslinking EPI-OFF Il paziente viene anestetizzato con alcune gocce di collirio. Vengono poi instillate alcune gocce di antibiotico e di disinfettante oculare. Viene applicato un telino sterile intorno all’occhio e le palpebre vengono aperte mediante due piccoli divaricatori. Il medico oculista rimuove l’epitelio, cioè lo strato di cellule che ricopre la cornea (tecnica EPI-OFF) e poi instilla ripetutamente la Riboflavina in gocce per un tempo di circa 15’ Avvicina poi all’occhio uno strumento che emette una luce della famiglia degli U-V e irradia la cornea per circa 30’, continuando di tanto in tanto ad instillare delle gocce di Riboflavina. Il medico applica poi una lente a contatto terapeutica per facilitare il processo di guarigione e ridurre i fastidi al paziente nel periodo che segue il trattamento; applica poi qualche goccia di collirio antibiotico e invia il paziente in sala d’attesa. Egli potrà quindi andare a casa dopo 15’-20’. Tecnica di crosslinking EPI-ON Nel 2009 un’azienda italiana leader del settore ha introdotto una Riboflavina modificata rendendola capace di superare lo strato superficiale della cornea (epitelio); in tal modo si può effettuare il trattamento di Cross-linking corneale senza togliere l’epitelio (EPI-ON) e di conseguenza in modo meno fastidioso per il paziente. Utilizzando questa modalità la tecnica di crosslinking diviene più semplice e meno invasiva. Il crosslinking in una delle sue modalità di esecuzione, oltre che per curare il cheratocono, può essere effettuato anche in pazienti che presentano un assottigliamento post-chirurgico della cornea ed in altre patologie. Un esempio è rappresentato dai pazienti operati di trapianto di cornea che presentano una riduzione dello spessore del lembo trapiantato o un aspetto irregolare della superficie della cornea; il trattamento di cross linking può essere utile sia per ripristinare una superficie corneale più omogenea, ma anche per rafforzare gli strati interni della cornea. 27 Anche nei rari pazienti che presentano un assottigliamento patologico (ectasia) dopo correzione refrattiva con Laser ad Eccimeri il cross linking rappresenta una possibilità di trattamento. Recentemente, l’impiego del CXL è stato esteso anche ad alcune forme di cheratiti infettive non responsive alla terapia standard e alle erosioni corneali recidivanti. Il CXL trova inoltre utilizzo in combinazione con tecniche refrattive come la PRK o gli ICRs (anelli intracorneali). Ad oggi la tecnica standard EPI-OFF (cioè con rimozione dell’epitelio) può vantare un follow-up di 10 anni. La tecnica del CXL viene eseguita in Italia dal 2007; essa ha dimostrato negli anni di essere una tecnica sicura ed efficace per il trattamento del cheratocono e delle ectasie corneali. Si calcola che dall’avvio della tecnica ad oggi siano stati praticati oltre 300.000 interventi negli oltre 1.500 centri diffusi in tutto il mondo. Il CXL, come è stato inizialmente eseguito e come tutt’ora viene fatto nella grande maggioranza dei casi, ha durata complessiva di quasi un’ora (30’ per preparazione dell’occhio e rimozione dell’epitelio e imbibizione della cornea con Riboflavina + 30 minuti di irraggiamento). La durata del trattamento transepiteliale (EPION) è pure di circa un’ora (30 minuti di imbibizione + 30 minuti di irraggiamento). Però, questa tecnica consente per il paziente un decorso post-operatorio con minori disagi. Ad oggi la tecnica EPI-ON ha un follow-up di 4 anni. Entrambe le tecniche EPI-OFF ed EPI-ON hanno il limite di essere ritenute tediose e fastidiose dai pazienti a causa dei lunghi tempi di esecuzione, circa un’ora per ogni paziente. La recente ricerca scientifica si è pertanto indirizzata verso un’ulteriore ottimizzazione della procedura, per poter coniugare l’efficacia e la sicurezza della tecnica transepiteliale ad una maggiore facilità e rapidità di trattamento, tramite una nuova procedura di imbibizione rapida chiamata IONTOFORESI. La iontoforesi corneale, sviluppata in Italia e brevettata nel 2010 da una importante azienda nazionale, consente una drastica riduzione dei tempi di trattamento del CXL dagli attuali 60 minuti della tecnica EPI-OFF e EPI- ON ai 15 minuti con la nuova procedura. Grazie alla iontoforesi, si raggiunge nello stroma corneale una concentrazione di riboflavina equivalente alla imbibizione della tecnica standard. La iontoforesi oculare risulta estremamente semplice nell’esecuzione ed è ottimamente tollerata dal paziente, oltre che dai tessuti oculari. 28 Tecnica del Crosslinking mediante Iontoforesi La iontoforesi (da iòntos=ione e phòresis = trasporto, trasporto di ioni) consiste nel trasferimento unidirezionale di molecole, fornite di carica ionica, all’interno dei tessuti da trattare, grazie ad un campo elettrico a bassa intensità. Ecco come si svolge l’intervento. Il trattamento viene effettuato mediante l’applicazione sul paziente dei due elettrodi collegati ad un delicato generatore di corrente continua. Per primo, viene posizionato l’elettrodo positivo a forma di cerotto al centro della fronte del paziente, e, successivamente, l’altro sull’occhio del paziente. Poi, viene riempito l’elettrodo negativo, situato nell’occhio, con un’apposita formulazione di riboflavina specifica per iontoforesi corneale. Viene applicata la corrente elettrica a bassissima intensità, ottimamente tollerata dal paziente per cinque minuti. Il flusso di corrente (a bassa intensità) tra i due elettrodi permette alla formulazione di riboflavina di penetrare rapidamente nello stroma corneale, attraverso l’epitelio integro (quindi senza disepitelizzazione). Contemporaneamente alla iontoforesi è stata introdotta un’altra innovazione; la riduzione dei tempi di irraggiamento da 30’ a 9’ grazie ad un nuovo strumento che emette irradiazione necessaria in un tempo molto più breve. I dati ottenuti fino ad ora hanno dimostrato l’efficacia e la sicurezza della nuova tecnica. La tecnica del crosslinking mediante iontoforesi unisce i benefici della tecnica transepiteliale EPION (assenza di haze, di infezioni e di dolore; nessuna riduzione del visus nel periodo post-intervento) ai vantaggi della tecnica standard EPI-OFF (maggiore penetrazione stromale). Il tutto con un intervento più rapido e più confortevole Strumento che emette raggi UV per trat- sia per gli oculisti che per il patare la cornea durante il procedimento di ziente, in quanto dura soltanto un quarto d’ora. cross linking 29 L’ultima novità nel trattamento del cheratocono mediante cross-linking è la iontoforesi che consente un intervento più veloce ed una guarigione più rapida Conclusioni Con il crosslinking in ognuna delle sue modalità di esecuzione si è aperta una strada nuova nella cura del cheratocono (e di altre patologie che indeboliscono la cornea); questa nuova modalità certamente consentirà anche tutta una serie di studi e di ricerche che condurranno nel prossimo futuro ad un ulteriore maggior controllo di questa difficile patologia. Ma è il concetto di cross linking che è veramente innovativo e che apre la strada al trattamento di molte altre malattie dell’occhio e con ogni probabilità anche della miopia. 30 LASER SULLA CORNEA: PRK, LASIK E PTK La cornea è la più potente lente dell’occhio, oltre che la più accessibile. Non stupisce quindi il fatto che la cornea sia il “bersaglio” principale e meno invasivo per correggere i difetti “ottici” (o refrattivi) della visione, come miopia, ipermetropia, astigmatismo. La chirurgia rifrattiva corneale con PRK o LASIK agisce infatti modificando la curvatura della “lente” cornea in modo che i raggi luminosi possano andare a focalizzare correttamente le immagini sulla retina. La chirurgia refrattiva corneale ha raggiunto un grado di affidabilità molto alto e oggi utilizza in pratica solo sistemi laser di alta precisione: il laser a eccimeri e il laser a femtosecondi. PRK e Lasik vengono spiegate in modo esteso nella pubblicazione della stessa serie “MI OPERO DI … MIOPIA, IPERMETROPIA, ASTIGMATISMO”, cui si rimanda. In casi selezionati di cheratocono è possibile correggere le più marcate irregolarità della curvatura corneale mediante trattamenti laser PRK su misura o “customizzata”, cioe personalizzata, consentendo un consistente miglioramento visivo mediante un trattamento pochissimo invasivo. Per ridurre al minimo la possibilità di una successiva evoluzione del cheratocono, la PRK è bene venga associata in questi casi a trattamento di cross linking corneale (CXL). LASIK: Il laser a femtosecondi emette Le irregolarità di curvatura (astigmamigliaia di microscopici spot (= punti tismo e aberrazioni) che possono laser) uno vicino all’altro creando un insorgere a distanza di tempo dopo “taglio” perfetto, creando una lamella trapianto di cornea, vengono invedi spessore perfettamente uniforme ce meglio trattate con la Lasik. 31 Lasik: dopo aver sollevato la lamella, si esegue il trattamento con il laser ad eccimeri per correggere il difetto Lasik: a fine intervento non servono punti di sutura, ma la lamella si riattacca in pochi istanti: questo permette un recupero visivo molto rapido PRK: l’epitelio corneale viene rimosso con una spatolina smussa, ricrescerà nell’arco di qualche giorno PRK: dopo aver rimosso l’epitelio corneale lo specialista attiva il laser ed esegue l’ablazione con il laser ad eccimeri per correggere il difetto PRK: a fine intervento si applica una lente a contatto terapeutica che serve ad attutire i disturbi conseguenti al trattamento laser ed accelerare la ricrescita dell’epitelio corneale 32 Lievi opacità superficiali della cornea o modeste irregolarità di superficie possono trovare una buona soluzione in un trattamento chiamato PTK. La PTK è in sostanza un trattamento laser molto simile alla PRK, vale a dire che consiste nell’effettuare una precisa asportazione di tessuto dalla superficie della cornea con laser a eccimeri. Cambia la finalità: invece che per motivi refrattivi (la “R” di PRK, sta per Rifrattiva) viene eseguita per motivi terapeutici (la “T” di PTK sta per Terapeutici). Perché si può rendere necessaria una PTK? Se la cornea presenta delle opacità o delle irregolarità superficiali si può ridurle o eliminarle con una ablazione mirata, eliminando e lisciando con il laser la parte alterata, “scoprendo” così la parte sottostante di cornea trasparente e sana, invece di procedere a interventi più invasivi come il trapianto di cornea. PTK: il laser a eccimeri permette di asportare tramite ablazione gli strati più superficiali della cornea se sono irregolari o opacizzati, lasciando una superficie perfetta. L’epitelio, rimosso all’inizio del trattamento, ricrescerà in pochi giorni con la protezione di una lente a contatto. Un altro campo di applicazione è quello delle erosioni epiteliali recidivanti, nelle quali una ablazione superficiale della cornea “rigenera” lo strato di ancoraggio dell’epitelio corneale evitando che si possa sollevare rompendosi e provocando dolore. Con la corretta indicazione, la PTK può brillantemente risolvere gravi problemi sia di riduzione della capacità visiva che di dolore in modo minimamente invasivo. Si tratta di interventi ambulatoriali in tutto sovrapponibili a quelli di PRK, per i quali è sufficiente solo l’anestesia con gocce di collirio (anestesia “topica”). Al termine del trattamento viene applicata sull’occhio una lente a contatto terapeutica per proteggere la cornea durante la ricrescita dell’epitelio corneale, che viene sorvegliata con controlli oculistici nei giorni successivi all’intervento. 33 IMPIANTI INTRASTROMALI COME RINFORZI ED ELEMENTI OTTICI NELLA CORNEA Abbiamo visto come la gran parte dello spessore della cornea sia rappresentato dallo stroma, costituito soprattutto da fibre collagene ordinate e densamente impacchettate. Si è visto che alcuni materiali inerti e biocompatibili possono essere inseriti nello spessore dello stroma corneale senza che provochino alcuna reazione infiammatoria. Gli anelli intrastromali sono impianti utilizzati per il cheratocono e la degenerazione marginale pellucida (ectasie o “sfiancamenti” della cornea). Si tratta più frequentemente di segmenti semicircolari di materiale plastico biocompatibile che hanno una funzione di sostegno e rinforzo. Impiantati opportunamente contrastano lo sfiancamento della cornea correggendone la curvatura. La loro applicazione non riesce in genere a risolvere completamente il difetto refrattivo irregolare indotto dal cheratocono, ma lo riduce e lo regolarizza, rendendolo correggibile con occhiali o anche con laser a eccimeri. Nei casi indicati si possono ottenere significativi miglioramenti della qualità visiva evitando di affrontare interventi più invasivi come il trapianto di cornea. Per ridurre al minimo la possibilità di una successiva evoluzione del cheratocono, l’impianto di anelli intrastromali viene spesso associato in questi casi a trattamento di cross linking corICR o Intra Corneal Ring: sono in geneale (CXL). nere dei semianelli di materiale plastico Gli impianti per presbiopia sono biocompatibile che, inseriti nello speselementi ottici veri e propri (microsore della cornea, ne irrobustiscono la lenti o piccoli diaframmi) in matestruttura e regolarizzano la curvatura. 34 riale sintetico biocompatibile che vengono posizionati nel centro della cornea per consentire la visione per vicino. Si tratta di interventi di norma eseguiti solo su un occhio. Un aspetto positivo di questo tipo di chirurgia oltre alla minima invasività è la reversibilità: in caso di problemi o risultati non soddisfacenti gli impianti possono essere rimossi senza che la cornea rimanga danneggiata. Anche questi interventi sono effettuati in modo ambulatoriale, con la sola anestesia topica. TECNICA DI ESECUZIONE DEGLI IMPIANTI INTRASTROMALI L’operazione di impianti intrastromali corneali, siano essi anelli per cheratocono o impianti per presbiopia, consta di due parti. La prima consiste nell’incidere all’interno della cornea delle piccole tasche. Se si pensa allo spessore della cornea, di circa mezzo millimetro, e che l’accuratezza desiderata per il posizionamento di questi impianti è di pochi micrometri (o micron = 1/1000 di millimetro), ci si rende conto che è necessario uno strumento di grande precisione. Si preferisce infatti utilizzare il laser a femtosecondi, che consente una operazione “bladeless” cioè senza lame, e quindi più sicura ma anche in grado di eseguire un atto chirurgico più accurato: il laser a femtosecondi ricava all’interno della cornea delle piccole tasche delle dimensioni, forma e profondità esattamente come programmato dal chirurgo oculista. La seconda parte dell’intervento consiste nel posizionare gli impianti all’interno delle tasche ricavate con il laser. Il taglio senza lama eseguito con il laser a femtosecondi consente di ottenere delle piccole tasche posizionate all’interno della cornea con assoluta precisione. In queste tasche il chirurgo oculista inserisce gli impianti intrastromali, in questo caso Intra Corneal Ring 35 La successione delle fasi operatorie è la seguente: • il chirurgo Oculista assistito dal tecnico laser inserisce i dati del paziente sul laser a femtosecondi e imposta il trattamento; • il paziente viene fatto sdraiare sotto al laser e vengono applicate alcune gocce di collirio anestetico; • viene poi applicato un divaricatore per tenere le palpebre moderatamente aperte e instillato collirio disinfettante (Iodopovidone 5%); • viene quindi applicato un anello a suzione, una specie di ventosa che poi viene coniugata al laser a femtosecondi; • il chirurgo Oculista assistito dal tecnico laser in 30” circa esegue l’incisione delle tasche all’interno dello spessore corneale; • la prima fase dell’intervento è terminata: Il paziente viene poi spostato sotto al microscopio operatorio; • il chirurgo oculista verifica la perfetta apertura delle tasche create dal laser e con l’ausilio di strumenti microchirurgici dedicati vi fa scivolare delicatamente gli impianti intrastromali; • per alcuni tipi di impianto è necessario apporre un punto di sutura che potrà essere asportato ambulatorialmente senza alcun dolore entro poche settimane; • La procedura è terminata e il chirurgo rimuove il divaricatore; applica qualche goccia di collirio antibiotico e fa accomodare il paziente in una sala d’attesa. Lente intracorneale: il laser a femtosecondi crea una tasca di lunghezza, diametro e profondità adeguate per ricevere la lente 36 Delicatamente con un apposito posizionatore per la lente si entra nel tunnel. La lente viene posizionata al centro della pupilla. Il posizionatore viene delicatamente rimosso per non decentrare la lente. Lente trasparente che aiuta il presbite nella visione da vicino Lente opaca con un foro centrale e tanti microforellini che aiuta il presbite nella visione da vicino 37 IL LASER A ECCIMERI Il laser ad eccimeri è uno strumento che emette una luce ultravioletta tale da esercitare sui tessuti un particolare effetto chiamato ablazione; il risultato è che la parte più superficiale del materiale colpito viene disintegrata, trasformata in vapore. L’ablazione oltre ad avvenire con precisione inferiore al millesimo di millimetro è “selettiva” cioè avviene solo nella zona di cornea prescelta per il trattamento, ad una profondità e su una estensione di ampiezza prestabilita ciò grazie anche al fatto che il laser è controllato da un computer (che, a sua volta, è programmato dal medico oculista). Il risultato di tutto ciò è che la superficie corneale viene rimodellata in modo tale da ottenere la correzione del difetto di vista (miopia, astigmatismo ed ipermetropia). L’applicazione clinica del laser ad eccimeri è stata preceduta da lunghe e attente valutazioni che hanno evidenziato come esso agisca senza conseguenze per i tessuti circostanti e senza determinare alcun indebolimento per il bulbo oculare (sono già passati venticinque anni dal primo intervento con laser ad eccimeri). Inoltre il trattamento è ripetibile; ciò vuol dire che il laser può ripetere un trattamento sempre nella stessa maniera senza variazioni, cosa non possibile in un intervento chirurgico il cui risultato dipende parecchio dalla mano del chirurgo (che è diversa di volta in volta). Il laser ad eccimeri può essere utilizzato Il chirurgo con il tecnico laser al con due modalità diverse: sulla superlaser ad eccimeri durante un inficie della cornea con una procedura tervento Lasik chiamata PRK o all’interno della cornea 38 con una procedura chiamata LASIK. Ambedue queste procedure possono correggere con ottimi risultati la miopia ma anche l’astigmatismo e l’ipermetropia. Altre informazioni sul laser ad eccimeri I laser ad eccimeri per correggere la miopia sono stati utilizzati per la prima volta nel 1987. Da allora in tutto il mondo sono stati trattati con grande successo oltre 50 milioni di persone affette da miopia ma anche da astigmatismo e da ipermetropia. Con i laser di oggi, si ottengono trattamenti di qualità pressoché perfetta e quindi risultati refrattivi molto precisi, anche perché i laser di quinta-sesta generazione sono in grado di evitare i problemi legati ai possibili movimenti dell’occhio durante il trattamento; ciò grazie ad un sofisticato sistema di “eye tracker”; questo dispositivo consente al laser di “seguire” l’occhio durante anche i più lievi movimenti favorendo così la perfetta esecuzione della procedura. Altra innovazione tecnica importante per ottenere un risultato ottimale è il “riconoscimento dell’iride”; esso consente al laser di lavorare con estrema precisione. Un’altra importante innovazione riguarda la possibilità di fare dei trattamenti laser personalizzati; questa è una modalità che consente notevoli vantaggi visivi per il paziente. In pratica prima dell’intervento con un dispositivo computerizzato si esegue una mappatura dell’occhio da trattare (aberrometria); le informazioni ottenute da questo esame vengono inserite nel computer del laser; questo esegue il trattamento in base alle informazioni ricevute. Tutto ciò è un importante elemento di precisione e di perfezionamento che comporta un’ulteriore ottimizzazione dei risultati, specialmente in situazioni particolari come nel cheratocono. Un laser ad eccimeri di quinta-sesta generazione è uno strumento di prezzo elevato e necessita di manutenzione continua e costosa; per questi interventi inoltre occorrono numerose altre strumentazioni costose; questo spiega i costi relativamente elevati della PRK, della LASIK e della PTK. 39 IL LASER A FEMTOSECONDI Il laser a femtosecondi è uno strumento in grado di emettere raggi di luce coerente in tempi incredibilmente brevi (inferiori al millesimo di miliardesimo di secondo) in aree estremamente piccole; in base a questa particolarità è dotato di energia molto grande, in grado cioè di distruggere tessuto e di trasformarlo in gas. Il laser a femtosecondi è sostanzialmente un raggio di luce, che taglia al posto di una lama metallica, e soprattutto taglia con maggior precisione e in completa sicurezza; tutto ciò creando superfici di taglio estremamente liscie. Il laser a femtosecondi, che in chirurgia refrattiva e corneale è ampiamente utilizzato da oltre quindici anni, trova oggi un importante ruolo anche nella chirurgia della cataratta. Il laser a femtosecondi trova la sua applicazione principale in chirurgia rifrattiva, nella Lasik, ma ha altre importanti applicazioni nel campo della chirurgia corneale e della cataratta. I benefici del taglio con questo laser sono: 1) Taglio senza lama scompare l’uso delle lame metalliche; il paziente può avere una procedura completamente laser 2) La chirurgia è programmabile e ripetibile in quanto non chirurgo dipendente; 3) Massimo controllo e accuratezza nella esecuzione dell’intervento Laser a femtosecondi per la chirurgia corneale e particolare dell’interfaccia paziente-laser: permette la precisa focalizzazione del laser sulla cornea 40 I TRAPIANTI DI CORNEA Purtroppo molte malattie, degenerazioni, cicatrici possono opacizzare e/o deformare la cornea a un punto tale che la capacità visiva non è migliorabile con procedure conservative, redendo necessaria la sostituzione del tessuto corneale, cioè effettuando un trapianto di cornea o “cheratoplastica”. I trapianti di cornea hanno una percentuale di successo anatomico molto alta, circa del 95%. Una delle ragioni principali che spiegano questi eccellenti risultati è che la cornea è uno dei pochi tessuti umani che può essere trapiantato con un rischio molto basso di rigetto, venendo quindi “accettata” dall’organismo ricevente. Inoltre lo sviluppo di nuove tecniche mini-invasive ha ulteriormente ridotto questo rischio. Il tessuto corneale Per effettuare un trapianto di cornea è necessario sostituire la cornea malata del ricevente con una trasparente da donatore. Purtroppo non esiste ancora una cornea artificiale con caratteristiche così valide da poter fare a meno del tessuto vivente e quindi della donazione. Il tessuto corneale proviene da persone che hanno deciso di essere donatori perchè altri possano averne un beneficio. A queste persone va il ringraziamento di tutti noi, sia pazienti che medici. Tutti i tessuti di donatori vengono sottoposti a screening per escludere la possibilità di infezioni, quali epatite, sifilide, AIDS. Esiste una rete nazionale che si occupa delle donazioni, che afferiscono alle cosiddette Banche degli Occhi. Si tratta di un network nazionale e sovranazionale regolato da criteri estremamente rigorosi che garantiscono il rispetto e la segretezza dei donatori oltre alla sicurezza dei pazienti. Il titolo al plurale “trapianti di cornea” di questo capitolo non è una svista: esistono oggi diversi tipi di trapianto di cornea, che presentano aspetti molto diversi fra loro. 41 L’esigenza di sviluppare diversi tipi di trapianto è stata condizionata dalla volontà di effettuare interventi sempre meno invasivi e focalizzati a trattare patologie specifiche con modalità altrettanto specifiche. Abbiamo infatti visto come la cornea sia fatta di diversi strati e che molte patologie non li interessano tutti. Perché quindi non trapiantare solo lo strato malato? E’ proprio questa la direzione che la chirurgia dei trapianti corneali ha intrapreso nell’ultimo decennio e che negli ultimi anni ha rivoluzionato le tecniche chirurgiche. Oltre infatti alla possibilità più tradizionale di effettuare un trapianto a tutto spessore (cheratoplastica perforante), si sono aggiunte tecniche cosiddette “lamellari”, nelle quali è solo una lamella, cioè uno strato della cornea ad essere trapiantato. Nei casi in cui è possibile oggi si preferisce impiegare le tecniche “lamellari”. Queste tecniche sono meno invasive, riducono i rischi operatori, e, non essendo perforanti, lasciano il bulbo oculare più resistente ai traumi. Si distinguono cheratoplastica lamellare anteriore, nella quale sono gli strati più esterni della cornea ad essere trapiantati, e cheratoplastica lamellare posteriore o endoteliale, nella quale è lo strato più interno, quello che supporta le cellule endoteliali, ad essere sostituito. Nella pagina seguente è riportata una tabella che schematizza le caratteristiche più importanti delle principali categorie di trapianto di cornea. Risulta evidente come vi siano differenze molto significative, che si traducono in aspetti tecnici, di indicazione, di rischi, e anche di terapia postoperatoria non sovrapponibili. Tutte queste diverse caratteristiche vengono esaminate più dettagliatamente nei capitoli successivi. 42 Cheratoplastica perforante o a tutto spessore Cheratoplastica lamellare anteriore Cheratoplastica endoteliale o lamellare posteriore indispensabile quando la malattia corneale è estesa a tutti gli strati (es. cheratocono molto avanzato) indicata quando la sola parte anteriore della cornea è alterata (es. cheratocono meno avanzato) indicata solo quando c’è uno scompenso corneale (cornea guttata, cheratopatia bollosa) viene sostituito un disco centrale di cornea per tutto il suo spessore viene sostituito un disco centrale di cornea ad eccezione degli strati più profondi viene sostituito solo lo strato endoteliale più profondo: la cornea del ricevente è conservata quasi completamente necessita di sutura a 360° necessita di sutura a 360° sono sufficienti uno o pochi punti di sutura sul bordo della cornea l’occhio è meno robusto (evitare sempre possibili traumi) l’occhio è più robusto rispetto al trapianto a tutto spessore l’occhio ha una robustezza quasi invariata rispetto a prima dell’intervento la visione può subire variazioni nel tempo la visione è in genere più stabile rispetto al trapianto a tutto spessore visione molto stabile la sutura non può essere asportata prima di un anno la sutura può essere asportata prima di un anno le suture possono essere asportate dopo settimane vi è possibilità di rigetto la possibilità di rigetto viene quasi completamente evitata rigetto meno frequente che nel trapianto perforante. 43 CHERATOPLASTICA PERFORANTE Cheratoplastica perforante E’ il nome tecnico del trapianto di cornea “tradizionale”, o “a tutto spessore”. nel quale un disco centrale di tessuto corneale viene asportato in toto, e sostituito con un disco corneale preparato dalla cornea del donatore. Il tessuto trapiantato viene suturato in periferia a 360°. Si tratta di una procedura delicata, che fornisce ottimi risultati, ma richiede un follow-up di anni durante il quale la visione può non risultare sempre stabile, e che inevitabilmente implica un indebolimento strutturale del bulbo oculare (ridotta resistenza ai traumi). Tecnica di esecuzione della cheratoplastica perforante L’operazione di cheratoplastica perforante consiste nel sostituire un disco centrale a tutto spessore della cornea malata del paziente con un disco uguale ricavato dalla cornea sana di un donatore. Il diametro di questo disco è in genere vicino agli 8 mm. E’ infatti necessario lasciare un anello di cornea residua (ricordiamo che il diametro totale della cornea è in genere di 11-12 mm) soprattutto per poter “agganciare” il trapianto mediante la sutura a 360°. Il taglio viene comunemente eseguito con lame di precisione circolari, dette “trapani” corneali. Cheratoplastica perforante o trapianto corneale “a tutto spessore”: tecnica manuale. Il trapano incide un disco di cornea centrale, che viene asportato; viene quindi inserito un lembo di cornea sana, che viene suturato alla periferia della cornea del paziente. 44 Da qualche anno questa chirurgia si avvale del laser a femtosecondi, sfruttandone la capacità di effettuare tagli “bladeless”, cioè senza lama. Il femtolaser consente infatti di ottimizzare la precisione del taglio e soprattutto di creare dei margini sagomati sia sulla cornea ricevente che sul lembo corneale da trapiantare, in modo da migliorare il rapporto tessuto di donatore-tessuto ricevente. In questo modo si ottiene un vero e proprio “incastro” che favorisce la regolarità della curvatura corneale (riducendo il rischio di astigmatismo elevato postoperatorio) e aumenta la superficie di contatto (migliorando, almeno in teoria, la resistenza dell’occhio operato ad eventuali traumi). Cheratoplastica perforante o trapianto corneale “a tutto spessore”: tecnica con laser a femtosecondi. Il laser permette di incidere la cornea con grande precisione, creando una struttura a “incastro”, che consente una perfetta corrispondenza fra la cornea donatrice e quella del paziente. Anche con il laser a femtosecondi è necessaria la sutura, che però tende ad essere asportata in tempi più brevi. La successione delle fasi operatorie è la seguente: • prima di iniziare l’intervento sul paziente, il lembo corneale da impiantare viene sagomato dalla cornea donata inviata dalla banca delle cornee. Questa preparazione può essere effettuata mediante taglio con laser a femtosecondi; • il paziente viene anestetizzato mediante anestesia generale o locale. In caso di anestesia locale viene esguita un’infiltrazione di anestetico intorno all’occhio e si aspettano alcuni minuti per ottenere un effetto ottimale; • viene poi applicato un divaricatore per tenere le palpebre moderatamente aperte e instillato collirio disinfettante (Iodopovidone 5%); • in caso di intervento con laser a femtosecondi il paziente viene fatto sdraiare sotto al laser; viene quindi applicato un anello a 45 suzione, una specie di ventosa che poi viene coniugata al laser a femtosecondi; il chirurgo Oculista assistito dal tecnico laser in 30”- 60” esegue i tagli di precisione nello spessore corneale; • il paziente viene fatto sdraiare sotto al microscopio operatorio; • se i tagli nello spessore della cornea non sono stati eseguiti prima con il laser, il chirurgo oculista procede mediante apposito trapano di precisione (una lama circolare); • il disco centrale di cornea malata viene asportato e subito sostituito con quello preparato in precedenza dalla cornea sana da donatore; • viene applicata a 360° una sutura sottilissima che ancora il bordo del disco corneale impiantato alla parte periferica che rimane della cornea ricevente; • l’intervento è terminato, il chirurgo applica una medicazione antibiotica e il divaricatore palpebrale viene rimosso; l’occhio viene normalmente chiuso e rimarrà bendato per alcune ore o fino al giorno successivo; • se l’intervento è in anestesia generale, l’anestesista procede al risveglio del paziente; • il paziente viene quindi accompagnato in una stanza di osservazione, dove può essere assistito da un familiare. Quale anestesia? E’ doloroso? Il ricovero è necessario? L’anestesia per il trapianto di cornea può essere sia generale che locale. La scelta dipende da numerosi fattori, che devono essere valutati insieme al medico anestesista al momento di pianificare l’intervento. In ogni caso l’intervento non è di norma doloroso. Possono verificarsi modesto fastidio e fotofobia dopo l’intervento, che scompaiono dopo alcuni giorni. L’intervento si può tranquillamente effettuare in day hospital, tornando presso la propria abitazione a dormire. In casi selezionati la presenza di patologie sistemiche potrà invece suggerire di prolungare l’osservazione in un ambiente protetto anche durante la notte. Da un punto di vista della chirurgia oculare raramente vi è la necessità di un ricovero notturno. La decisione riguarda quindi il medico anestesista il quale, valutate le condizioni di salute generale del paziente, deciderà per la soluzione più sicura. 46 Quali complicanze? Nessun intervento chirurgico è privo di rischi e la cheratoplastica perforante non sfugge alla regola, anche se i risultati sono anatomicamente ottimi nella grande maggioranza dei casi. Nella documentazione informativa consegnata e discussa con il paziente prima dell’intervento vengono spiegati in dettaglio i possibili rischi e problemi legati all’intervento. In questa sede vediamo le complicanze principali. La complicanza intraoperatoria più temuta del trapianto di cornea è una improvvisa emorragia intraoculare che avviene nel breve momento in cui il bulbo oculare rimane aperto per sostituire la cornea. Può comportare la perdita della vista, ma bisogna dire che si tratta di un’evenienza eccezionale.. Nel postoperatorio la complicanza più grave, così come per qualunque altro intervento intraoculare (anche il comune intervento per cataratta), è l’insorgenza di un’infezione. Un’estensione dell’infezione all’interno del bulbo oculare (“endoftalmite”) può portare alla perdita della vista. Grazie però alle misure di prevenzione pre-, intra- e post-operatorie oggi utilizzate, tali infezioni sono divenute eccezionalmente rare (una ogni migliaio di interventi di trapianto perforante). Inoltre anche la capacità di intervenire rapidamente e contrastare l’infezione è notevolmente migliorata, per cui l’endoftalmite può essere curata con buon successo in molti casi. Le altre complicanze possibili sono di gran lunga meno gravi. Si può dire in generale che possono portare ad una riduzione della capacità visiva o a un ritardo nel recupero della stessa. Cosa aspettarsi dopo? Sono normali una iniziale difficoltá a tenere l’occhio aperto, un certo fastidio alla luce e una certa lacrimazione: tutto questo migliora gradualmente nell’arco di alcuni giorni. A volte il bulbo operato è dolente o arrossato. Una volta fatto il trapianto si possono riprendere le normali attivitá quotidiane, come leggere (con l’occhio non operato), guardare la televisione, uscire di casa, occuparsi delle piccole faccende domestiche. Particolare attenzione deve essere rivolta a evitare pressioni sull’occhio operato, in quanto la ferita è ancora in via di cicatrizzazione. Per le prime settimane è consigliato tenere una protezione di plastica (conchiglia) durante la notte, mentre si dorme, per evitare traumi accidentali o strofinamenti involontari. In questo periodo è consigliabile proteggere l’occhio anche durante 47 il giorno con occhiali avvolgenti per evitare l’irritazione da agenti atmosferici (luce, vento, polvere). L’attività lavorativa, la guida, le attività sportive potranno essere riprese dopo un breve periodo di sospensione, da definire caso per caso. E’ fondamentale seguire scrupolosamente le istruzioni del chirurgo oculista su farmaci, precauzioni, regolarità dei controlli postoperatori. L’asportazione della sutura non viene effettuata prima di un anno dall’intervento, e spesso viene lasciata molto più a lungo senza che il paziente avverta alcun fastidio. Come recupera la vista? Il recupero visivo dopo cheratoplastica perforante è graduale e richiede alcuni mesi. In genere si ottiene una buona stabilizzazione entro 10-12 mesi dall’intervento, con risultati visivi che possono essere ottimi, con un completo recupero o quasi dell’acuità visiva. Questo dipenderà naturalmente dalle “potenzialità” dell’occhio operato, e quindi dalla eventuale presenza di patologie concomitanti su altre strutture dell’occhio come cristallino, retina, nervo ottico, che possono limitarne la capacità visiva anche se il trapianto ha avuto un risultato anatomico ottimale. L’altro motivo per il quale è possibile che ad un successo anatomico non corrisponda un successo visivo è la cicatrizzazione del punto di contatto fra la cornea trapiantata e quella ricevente: è un fenomeno fisiologico di guarigione sul quale il chirurgo non sempre può intervenire. Questo si può tradurre in irregolarità di tensione che agiscono sulla curvatura corneale, provocando quindi astigmatismo. Un certo grado di astigmatismo è quasi sempre presente dopo un trapianto. Se si osserva un astigmatismo elevato nei primissimi mesi dopo l’intervento è possibile per il chirurgo intervenire agendo ambulatoriamente sulla tensione della sutura. Una volta invece avvenuta una stabilizzazione del quadro, sarà possibile prendere in considerazione un intervento laser per correggere, in parte o in toto, l’astigmatismo presente . Il rigetto: significa che si “perde” la cornea trapiantata? No, il rigetto non “espelle” né distrugge la cornea impiantata, ma può farle perdere trasparenza. Si tratta di una reazione infiammatoria che il sistema immunitario attiva se “si accorge” che ci sono cellule non proprie. 48 Iniziando prontamente una terapia adeguata, nella maggior parte dei casi si riesce a “spegnere” la reazione di rigetto e ridare trasparenza alla cornea. La comparsa di un sintomo come l’arrossamento dell’occhio associato ad annebbiamento della vista ed ad una certa dolenzia, è sempre sospetto dopo trapianto di cornea e richiede per prudenza una visita oculistica da effettuare in tempi brevi dall’insorgere della sintomatologia (1-2 giorni). Il rigetto è molto più probabile a uno-due anni dal trapianto, ma è sempre possibile, anche a distanza di molti anni. In alcuni casi il rigetto può essere particolarmente intenso e la cornea nonostante la terapia può non riprendere trasparenza. In questi casi nulla è perduto, è quasi sempre possibile ripetere il trapianto, spesso anche con una modalità meno invasiva, il trapianto endoteliale. La conseguenza principale del rigetto è infatti la perdita delle cellule endoteliali, che come abbiamo visto non sono in grado di rigenerarsi. SINTOMI CHE POSSONO FAR SOSPETTARE UN RIGETTO Che fare? Annebbiamento visivo - verificare che i sintomi non siano passeggeri Arrossamento dell’occhio (partico- - non allarmarsi, non è necessario correre al pronto soccorso nel cuore larmente intorno alla cornea) della notte… Dolenzia all’occhio, fotofobia - … ma effettuare al più presto una visita oculistica: solo così si può chiarire l’origine dei sintomi e instaurare la terapia eventualmente necessaria 49 CHERATOPLASTICA LAMELLARE ANTERIORE Cheratoplastica lamellare anteriore E’ indicata quando l’opacità coinvolge la parte anteriore della cornea, o quando la struttura corneale si è assottigliata e sfiancata per rinforzarla e correggerne la curvatura (ad esempio nel cheratocono). Servendosi del laser e di altri strumenti, la parte anteriore “malata” viene rimossa e viene sostituita con una lamella sana ricavata dalla cornea donatrice, e suturata a 360°. Il trapianto lamellare anteriore è meno invasivo rispetto al trapianto perforante e l’occhio operato sarà più resistente. La possibilità di rigetto è quasi annullata. Uno svantaggio delle tecniche lamellari è che si possono allungare i tempi di recupero per via della non perfetta trasparenza che può svilupparsi nel punto di contatto fra la cornea residua del ricevente e la lamella corneale del donatore, ma gli altri importanti vantaggi fanno in genere propendere per la soluzione lamellare se perseguibile ed indicata. Tecnica di esecuzione della cheratoplastica lamellare anteriore L’operazione di cheratoplastica lamellare anteriore consiste nel sostituire un disco centrale della parte anteriore della cornea malata del paziente con un disco uguale ricavato dalla cornea sana di un donatore. Il diametro di questo disco è in genere vicino agli Cheratoplastica lamellare anteriore. Solo la parte anteriore, malata della cornea (evidenziata in colore più scuro) viene asportata. Viene quindi applicata e suturata una lamella di cornea sana preparata da un lembo di donatore. 50 8 mm. E’ infatti necessario lasciare un anello di cornea residua (ricordiamo che il diametro totale della cornea è in genere di 1112 mm) soprattutto per poter “agganciare” il trapianto mediante la sutura a 360°. Trattandosi di un campo in continua evoluzione che ha trovato applicazione frequente solo negli ultimi anni, non deve stupire come esistano diverse metodiche per asportare la lamella anteriore di cornea. La scelta della metodica dipende da diversi fattori, primo fra i quali la natura (le più frequenti sono il cheratocono e le opacità corneali) e la gravità della patologia (ad esempio, quanto è profonda nello spessore corneale l’opacità). Il chirurgo oculista studierà attentamente il singolo caso e sceglierà la soluzione migliore parlandone con il paziente. Possiamo suddividere le metodiche di separazione e asportazione della lamella corneale anteriore in quattro possibilità principali. • Manuale. Nel senso che non vengono usate lame automatizzate o laser, ma solo fini strumenti chirurgici e mezzi fluidi che permettono di separare (“slamellare”) la parte di cornea anteriore dagli strati profondi. Fra i mezzi fluidi uno dei più frequentemente utilizzati oggi è l’aria. Si parla infatti di tecnica “big bubble” (letteralmente “grande bolla”, anche se il suo diametro non supera in genere il centimetro). L’obiettivo degli interventi manuali è quello di lasciare uno strato di cornea il più sottile possibile a sostegno delle cellule endoteliali, in quanto si è osservato che questa situazione si accompagna a un recupero visivo più rapido. La sottigliezza però di questo strato residuo (anche pochi millesimi di millimetro, o “micron”) fa sì che sia estremamente delicato e possa rompersi, anche a causa dell’indebolimento causato dalla patologia. In questi casi si rende necessario modificare il programma chirurgico ed effettuare contestualmente il trapianto a tutto spessore, o cheratoplastica perforante. Con gli altri tipi di separazione automatizzata descritti più avanti, sia meccanici che laser, non è al momento possibile raggiungere la stessa profondità che si ottiene con la metodica “big bubble”. Nonostante la capacità di creare superfici di taglio estremamente lisce, in certe situazioni cliniche (si pensi ad un’opacità molto profonda), le tecniche “manuali” sono ancora utilizzate. • Con microcheratomo. Questo strumento (agisce sostanzialmente come una “pialla” chirurgica) è dotato di una lama che per 51 effetto di un piccolo motore elettrico vibra ad alta velocità e che può asportare lamelle di spessore definito lasciando eccellenti superfici di taglio. Come per la chirurgia refrattiva Lasik, anche per la chirurgia dei trapianti lamellari il microcheratomo tende ad essere sostituito dal laser a femtosecondi, ancora più preciso. Esistono però alcuni casi in cui si dimostra ancora molto utile, come le opacità superficiali dense al centro della cornea al di sotto delle quali il laser fatica a penetrare. • Con laser a eccimeri. Le caratteristiche di velocità e precisione degli strumenti di ultima generazione permettono di eseguire un’ablazione laser del tessuto corneale malato, creando uno “scavo” conformato su misura per la cornea del singolo paziente. • Con laser a femtosecondi. Il laser a femtosecondi può eseguire tagli “senza lama” all’interno della cornea virtualmente in tutte le direzioni. Può quindi essere utilizzato anche per separare la lamella anteriore dagli strati più posteriori, oltre che per la creazione del taglio circolare periferico. Il laser a femtosecondi può anche essere usato in combinazione con la tecnica di dissezione con aria per eseguire la DALK (Deep Anterior Lamellar Keratoplasty, cioè la Cheratoplastica Lamellare Anteriore). Indipendentemente dalla tecnica usata per asportare la lamella anteriore di cornea malata, viene poi apposta una lamella di spessore uguale o leggermente superiore e suturata a 360°. Tale sutura è estremamente sottile e viene eseguita manualmente dal chirurgo al microscopio operatorio con l’aiuto di punti di riferimento, per ottenere una perfetta corrispondenza del lembo corneale trapiantato con il letto ricevente. I materiali utilizzati per la sutura non sono riassorbibili, ma tengono a degradarsi dopo anni. Si tende però ad asportare tali suture prima che si degradino, comunque in genere non prima di sei mesi dall’intervento. 52 Un intervento con molte “declinazioni” Le varie metodiche con le quali è possibile effettuare la cheratoplastica lamellare anteriore sono spesso abbreviate in acronimi più o meno complessi. Ecco i più comuni: DALK o DLK Deep Anterior Lamellar Keratoplasty, cheratoplastica lamellare anteriore di tipo “profondo” SALK Superficial Anterior Lamellar Keratoplasty, cheratoplastica lamellare anteriore di tipo “superficiale” ALTK Automated Lamellar Therapeutic Keratoplasty, cheratoplastica lamellare anteriore “automatizzata” con utilizzo di microcheratomo FALK Femtosecond Laser Assisted Lamellar Keratoplasty IEK Intralase Enhanced Keratoplasty, cheratoplastica lamellare anteriore con utilizzo di laser a femtosecondi ELALK o ELLK Excimer Laser Assisted Lamellar Keratoplasty, cheratoplastica lamellare anteriore con utilizzo di laser a eccimeri. ELLKAT Excimer Laser Lamellar Keratoplasty of Augmented Thickness. Cheratoplastica Lamellare Anteriore: Tecnica personale di Buratto Nella chirurgia lamellare della cornea il risultato visivo e funzionale dipende in grande parte dalla qualità delle superfici di contatto dei due tessuti; naturalmente entrano in gioco altri fattori…la qualità del materiale ricevuto dalla Banca delle Cornee, l’atto chirurgico in sè, l’azione esercitata dai numerosi punti di sutura e la buona accettazione del materiale donato da parte della cornea del paziente ricevente . Il materiale che proviene dalla banca delle cornee può essere “fresco” o “disidratato” in quanto trattandosi di una lamella di tessuto superficiale non sono presenti le cellule endoteliali così importanti invece quando si effettua un trapianto perforante, cioè a tutto spessore. Questo materiale solitamente viene prelevato dalla cornea del donatore mediante uno strumento chiamato microcheratomo, che funziona in maniera molto similare ad una piccola pialla da falegname, con la differenza che ha una lama molto affilata che funziona per effetto di un motore elettrico che la fa funzionare ad altissima velocità. Si ottiene così una lamella che ha un’ottima superficie di taglio… ma che è pur sempre fatta con una lama metallica. 53 Egualmente il prelievo sul paziente della lamella di tessuto malato o danneggiato (da ferite, corpi estranei, cheratiti o interventi chirurgici) viene quasi sempre effettuato usando lo stesso strumento. E quindi si ottengono due superfici di contatto di ottima qualità, ma pur sempre con le microscopiche irregolarità tipiche di un taglio effettuato con uno strumento meccanico quale è una lama. Ebbene, nei centri di eccellenza, già da una decina di anni nella chirurgia refrattiva lamellare della cornea, si adoperano i laser … Perché ? Perché i laser sono più precisi, più riproducibili nella loro azione … ma soprattutto perché riescono a ottenere superfici più lisce ed omogenee di quelle ottenibili con mezzi meccanici (lame ed altro) e quindi in grado di ottimizzare la trasmissione delle luce all’interno dell’occhio e quindi la funzione visiva. Nella tecnica di cheratoplastica lamellare di Buratto vengono adoperati due laser, per l’esattezza i due che vengono usati per la Lasik ed altra chirurgia refrattiva della cornea e cioè il laser a femtosecondi ed il laser ad eccimeri. Il laser a femtosecondi è noto per la sua capacità di tagliare lamelle di tessuto con estrema precisione per profondità e diametro creando superfici di taglio estremamente lisce; questo laser viene adoperato per il prelievo della lamella dalla cornea del paziente. Si ottiene così nel paziente ricevente una superfice molto liscia. Il laser ad eccimeri, noto per asportare tessuto corneale con grande precisione, è invece adoperato per eseguire una PTK cioè un trattamento di lisciatura sul tessuto di donatore proveniente dalla Banca delle Cornee per ottimizzare ulteriormente la già ottima qualità della superficie che poi entrerà in contatto con quella del paziente. Quando il tessuto di donatore e il tessuto ricevente entrano in contatto hanno quindi due superfici estremamente lisce e ciò può solo migliorare il risultato anatomico e funzionale e quindi visivo per il paziente. Naturalmente poi, come detto sopra, per un buon risultato globale entrano in gioco anche altri fattori, ma ottimizzando le superfici di contatto sicuramente le probabilità di ottenere un buon risultato aumentano. 54 La successione delle fasi operatorie è la seguente: • prima di iniziare l’intervento sul paziente, il lembo corneale da impiantare viene sagomato dalla cornea donata inviata dalla banca delle cornee. Questa preparazione può essere effettuata mediante taglio con una delle tecniche, manuale, automatizzata, laser, descritte sopra; • il paziente viene anestetizzato mediante anestesia locale, e cioè viene eseguita un’infiltrazione di anestetico intorno all’occhio e si aspettano alcuni minuti per ottenere un effetto ottimale; in alcuni casi può essere preferibile effettuare un’anestesia generale; • viene poi applicato un divaricatore per tenere le palpebre moderatamente aperte e instillato collirio disinfettante (Iodopovidone 5%); • in caso di intervento con laser (a femtosecondi o a eccimeri) il paziente viene fatto sdraiare sotto al laser; il chirurgo Oculista assistito dal tecnico laser esegue il trattamento onde rimuovere il tessuto corneale programmato; • il paziente viene poi fatto sdraiare sotto al microscopio operatorio; • se non si è proceduto mediante laser, il chirurgo oculista procede mediante apposito trapano di precisione, che si limita ad incidere la parte anteriore della cornea risparmiando la parte più profonda (endoteliale); mediante sistemi manuali (come l’iniezione di aria) o automatizzati (microcheratomo) la parte di cornea anteriore viene separata dagli strati profondi e asportata; • il disco centrale anteriore di cornea malata viene subito sostituito con quello preparato in precedenza dalla cornea sana da donatore; • viene applicata a 360° una sutura sottilissima che ancora il bordo del disco corneale impiantato alla parte periferica che rimane della cornea ricevente; • l’intervento è terminato, il chirurgo applica una medicazione antibiotica e il divaricatore palpebrale viene rimosso; l’occhio viene normalmente chiuso e rimarrà bendato per alcune ore e poi viene protetto con un paio di occhiali scuri; • il paziente viene quindi accompagnato in una stanza di osservazione, dove può essere assistito da un familiare. 55 Quali le principali differenze della cheratoplastica lamellare rispetto alla cheratoplastica perforante? Dipendono tutte dal fatto che viene evitata l’asportazione della parte più profonda della cornea e quindi anche dell’endotelio corneale. L’occhio non viene quindi “aperto” come nella cheratoplastica perforante, riducendo il rischio di complicanze intraoperatorie anche molto gravi. Per questo motivo viene praticamente sempre eseguito in anestesia locale mentre la cheratoplastica perforante può richiedere l’anestesia generale . Abbiamo visto come nel trapianto perforante il rigetto comporta primariamente il danneggiamento dell’endotelio corneale. Con la cheratoplastica lamellare anteriore il paziente conserva il proprio endotelio e quindi non corre questo rischio. Tale caratteristica permette anche di ridurre di molto i tempi della terapia antiinfiammatoria dopo l’intervento, riducendone i possibili effetti indesiderati (soprattutto possibile aumento della pressione oculare e cataratta). Esistono però degli svantaggi legati anch’essi al fatto che viene lasciata una parte di tessuto corneale del paziente: la velocità di recupero visivo è spesso più lenta rispetto al trapianto a tutto spessore, ma i risultati finali sono sovrapponibili nella gran parte dei casi. La tendenza attuale è quella di eseguire una cheratoplastica lamellare anteriore quando ve ne sia la possibilità, ricordando comunque che anche la cheratoplastica perforante fornisce ottimi risultati nella grande maggioranza dei casi, sebbene sia più invasiva. 56 CHERATOPLASTICA ENDOTELIALE O LAMELLARE POSTERIORE Cheratoplastica lamellare posteriore Viene eseguita quando lo strato più interno della cornea, l’endotelio, perde la sua funzionalità, che è quella di mantenere la trasparenza. In questi casi si parla di scompenso corneale o endoteliale, le cui cause più frequenti sono la distrofia endoteliale di Fuchs (cornea “guttata”) e gli esiti di interventi di cataratta complicati. Nella cheratoplastica endoteliale la cornea del ricevente non viene incisa nella sua parte anteriore, ma viene effettuata una piccola incisione laterale, simile a quella che si esegue per l’intervento di cataratta. Attraverso questa apertura l’endotelio malato viene asportato, e una lamella sottilissima di tessuto sano viene introdotta e fatta aderire grazie ad una bolla d’aria che la solleva. E’ spesso sufficiente un solo o pochissimi punti di sutura lateralmente alla cornea per chiudere l’incisione. La capacità visiva tende a recuperare molto più rapidamente con questa tecnica che con la cheratoplastica perforante, e l’occhio Cheratoplastica endoteliale o lamellare posteriore. Solo la parte più posteriore della cornea, alla quale sono adese le cellule endoteliali (membrana di Descemet), viene asportata. Attraverso una piccola incisione laterale viene inserita al di sotto della cornea malata del paziente una sottilissima lamina di tessuto ricco di cellule endoteliali sane, ricavata da una cornea di donatore. Una piccola bolla d’aria spinge poi la lamina trapiantata verso l’alto, in modo che aderisca alla cornea del paziente. Questa recupererà gradualmente la trasparenza grazie alle cellule endoteliali trapiantate. 57 mantiene un’integrità strutturale quasi normale, riducendo grandemente il rischio di gravi danni in caso di urti accidentali. Il rischio di rigetto è presente, ma meno frequente rispetto al trapianto a tutto spessore. TECNICA DI ESECUZIONE DELLA CHERATOPLASTICA ENDOTELIALE L’operazione di cheratoplastica endoteliale consiste nell’asportare la membrana di Descemet e l’endotelio malati dalla cornea del paziente e inserire una lamella corneale sottilissima con endotelio sano ricavata dalla cornea sana di un donatore. Si tratta di una lamella corneale in genere di 8-9 mm di diametro costituita solo dall’endotelio corneale, dalla membrana di Descemet che lo sostiene e spesso anche da un sottile strato di stroma. La preparazione viene effettuata mediante dissezione manuale, taglio con microcheratomo, o laser a femtosecondi; più frequentemente oggi questa preparazione viene effettuata già presso la banca delle cornee; il chirurgo oculista dovrà però ricavare da questa cornea “pretagliata” il disco del diametro necessario (in genere 8-9mm) utilizzando una lama circolare apposita. Sarà la presenza di cellule endoteliali sane a far tornare trasparente la cornea malata. A differenza degli altri tipi di trapianto, le manovre che vengono eseguite sul paziente non richiedono strumenti sofisticati come il microcheratomo o il laser a femtosecondi. Questi sono però indispensabili per “costruire” la sottile lamella di cornea che poi verrà inserita al momento del trapianto. Esistono alcuni tipi di trapianto endoteliale con vari acronimi piuttosto complicati che fanno riferimento ad aspetti molto specialistici, dei quali citiamo i principali essendo di uso comune: DSAEK (Descemet Stripping Automated Endotelial Keratoplasty) e DMEK (Descemet Membrane Endothelial Keratoplasty) 58 La successione delle fasi operatorie è la seguente: • prima di iniziare l’intervento sul paziente, il lembo corneale endoteliale da impiantare viene preparato dal tessuto corneale sano donato, proveniente dalla banca delle cornee; • il paziente viene di norma anestetizzato mediante anestesia locale: viene eseguita un’infiltrazione di anestetico intorno all’occhio e si aspettano alcuni minuti per ottenere un effetto ottimale; • il paziente viene fatto sdraiare sotto al microscopio operatorio; • viene poi applicato un divaricatore per tenere le palpebre moderatamente aperte e instillato collirio disinfettante (Iodopovidone 5%); • il chirurgo oculista esegue un piccolo taglio laterale nella cornea, simile a quello che si esegue per l’intervento di cataratta; • attraverso questa incisione il chirurgo rimuove dalla faccia interna della cornea solo la parte “malata”, cioè l’endotelio e la membrana di Descemet che lo sostiene. Questo “scollamento” normalmente lascia una superficie estremamente liscia, quindi ottimale da un punto di vista di trasparenza; • Viene quindi inserito il trapianto endoteliale. Questa sottile lamina viene in genere introdotta arrotolata all’interno dell’occhio del paziente, in modo da non dover effettuare un’apertura troppo grande, che rallenterebbe la guarigione e il recupero visivo; • Il trapianto endoteliale viene quindi sollevato da una bolla d’aria e fatto aderire alla faccia interna della cornea ricevente; • Uno o pochi punti di sutura chiudono le incisioni eseguite sulla periferia della cornea; • l’intervento è terminato, il chirurgo applica una medicazione antibiotica e una lente a contatto terapeutica; • il divaricatore palpebrale viene rimosso; l’occhio viene normalmente chiuso e rimarrà bendato per alcune ore; • il paziente viene quindi accompagnato in una stanza di osservazione, dove può essere assistito da un familiare; dovrà rimanere sdraiato per almeno un paio di ore al fine di favorire l’adesione del trapianto endoteliale, che verrà verificata dal chirurgo oculista prima di dimettere il paziente. Quali le principali differenze rispetto alla cheratoplastica perforante? Le grandi differenze rispetto alla cheratoplastica perforante (ma anche alla lamellare anteriore) scaturiscono fondamentalmente dal fatto che a parte un sottilissimo strato interno (l’endotelio e la membrana di Descemet), il paziente mantiene la propria cornea, che viene solo incisa per pochi mm in periferia. 59 Grazie alla piccola incisione, l’anestesia per il trapianto endoteliale è di norma locale. La presenza di una piccola bolla d’aria nell’occhio a fine intervento comporta alcune accortezze particolari (il paziente deve rimanere sdraiato per qualche tempo dopo l’intervento per favorire l’adesione della lamella trapiantata) e deve essere sorvegliato e valutato prima della dimissione per scongiurare aumenti eccessivi di pressione intraoculare (per lo stesso motivo non è possibile effettuare viaggi aerei finchè l’aria non si è riassorbita - in genere uno o due giorni). L’intervento può essere eseguito in day hospital, ma in casi selezionati potrà essere consigliabile prolungare l’osservazione in un ambiente protetto anche durante la notte. In modo simile alla cheratoplastica lamellare anteriore, i rischi legati all’ampia apertura dell’occhio, caratteristici della cheratoplastica perforante, sono assenti. La complicanza intraoperatoria più comune del trapianto endoteliale è in realtà un inconveniente risolvibile, la cui natura dipende direttamente dal tipo di trapianto: la lamella endoteliale, non suturata, può distaccarsi. Per riattaccarla è in genere necessario reinserire un po’ di aria al di sotto del trapianto. La presenza della piccola bolla d’aria nell’occhio determina nell’immediato periodo postoperatorio una visione molto annebbiata perché la luce non può focalizzarsi sulla retina. Il recupero visivo successivo è molto variabile in quanto bisogna aspettare che la cornea malata, grazie all’azione del nuovo endotelio, riprenda trasparenza. La rapidità con cui questo avviene è in genere proporzionale a quanto la cornea malata ha “sofferto” prima. Vi sono casi che raggiungono una capacità visiva molto buona dopo unadue settimane. Questo è possibile perché il piccolo taglio laterale di questo trapianto non porta a cicatrizzazioni poco prevedibili con possibilità di astigmatismi elevati, come avviene per gli altri trapianti, che hanno una sutura su tutta la cornea a 360°: una volta ripristinata la trasparenza, il difetto refrattivo risulta in genere molto contenuto e stabile. In casi di pregressa sofferenza corneale più grave il progressivo miglioramento della trasparenza corneale può durare anche un anno. Può sembrare un fenomeno lento rispetto alla sostituzione a tutto spessore della cornea della cheratoplastica perforante, che dà trasparenza quasi subito, ma è preferibile in genere eseguire la chirurgia meno invasiva quando se ne ravvisa la possibilità. Vale comunque sempre la regola che il recupero dell’acuità visiva dell’occhio operato sarà limitato in presenza di patologie conco- 60 mitanti su altre strutture dell’occhio come cristallino, retina, nervo ottico. Le piccole dimensione del taglio periferico fanno anche sì che un’altra caratteristica positiva di questo tipo di trapianto sia il mantenimento della “resistenza” del bulbo oculare, che risulta quasi uguale a quella di un occhio non operato. Ricordando come il rigetto danneggi primariamente l’endotelio corneale, non sorprende che nella cheratoplastica endoteliale, nella quale viene sostituito proprio l’endotelio, il rigetto possa verificarsi. Si è osservato però che la probabilità di andare incontro a rigetto è più bassa rispetto al trapianto a tutto spessore. Anche il paziente operato di cheratoplastica endoteliale, oltre ad attenersi scrupolosamente alle terapie prescritte, deve quindi insospettirsi e farsi visitare rapidamente in caso noti arrossamento dell’occhio associato ad annebbiamento della vista. Cheratoplastica lamellare endoteliale: per una tecnica più “dolce”. Nella chirurgia lamellare endoteliale, cioè dello strato posteriore della cornea, rivestito appunto dalle cellule endoteliali, è fondamentale che queste vengano preservate il più possibile durante la chirurgia: una loro eccessiva perdita potrebbe compromettere il risultato dell’intervento, cioè il ripristino della trasparenza della cornea del paziente, che dipende appunto dall’apporto di cellule endoteliali “in salute”. All’inizio di questa chirurgia rivoluzionaria, alcuni anni fa, spesso troppe cellule venivano danneggiate in quanto la lamella da trapiantare veniva piegata e compressa. Tale manovra inevitabilmente determinava la morte di moltissime cellule. Un considerevole passo avanti è stato quello di trovare un modo di “arrotolare” la lamella in modo che le cellule endoteliali si trovino all’interno: non venendo in contatto con strumenti chirurgici il danno viene evitato. Il primo sistema chirurgico che ha permesso di ottenere tale risultato è stato messo in atto da Macaluso (uno degli autori di questo opuscolo) fin dal 2005, sui primi trapianti di endotelio eseguiti in Italia. Successivamente sono stati sviluppati strumenti sempre più perfezionati che consentono di ottenere eccellenti risultati in modo affidabile, e che vengono utilizzati da chirurghi della cornea in tutto il mondo. 61 CHERATOCONO Il cheratocono è una malattia progressiva della cornea che può provocare una riduzione anche molto grave della capacità visiva. Consiste in un assottigliamento e deformazione della cornea stessa, che tende a sfiancarsi protudendo in avanti, a volte in modo così evidente da assumere una forma conica. La causa non è nota. Si verifica una alterazione del collagene nello stroma corneale, le cui molecole perdono compattezza e il tessuto diventa più debole e deformabile. Vi è un certo grado di familiarità ma non si può considerare il cheratocono una malattia ereditaria. In pratica è da sospettare maggiormente se in famiglia vi è un’altra o più persone affette. Si è osservata anche una associazione con allergie durante la crescita. Alcuni medici pensano che sia lo sfregamento degli occhi indotto dall’allergia a danneggiare la cornea: a scopo preventivo è consigliabile evitarlo il più possibile. Deve inoltre sempre insospettire un difetto rifrattivo con astigmatismo che aumenta nel tempo. Può comparire a partire dai 10-14 anni di età, ma, il più delle volte, viene diagnosticato più avanti negli anni. La velocità e l’entità della progressione della deformazione corneale da cheratocono sono estremamente variabili. Come regola generale la velocità di evoluzione è maggiore nei giovanissimi e diminuisce sensibilmente con l’età. Il motivo è il naturale “irrigidimento” della struttura corneale nel corso degli anni. Il cheratocono è da considerarsi una patologia bilaterale, che coinvolge entrambi gli occhi, ma il più delle volte questo avviene in modo anche marcatamente asimmetrico. Quali sintomi avverte il paziente? Non vi sono di norma disturbi come dolore o infiammazione oculare. I problemi avvertiti dal paziente consistono in un peggioramento della capacità visiva indotto dall’alterazione, spesso progressiva, della cornea. Spesso l’occhio affetto da cheratocono diventa miope, ma è l’astigmatismo irregolare a disturbare maggiormente 62 la visione, inducendo la percezione di un’immagine sfocata e deformata (soprattutto le fonti luminose tendono ad essere allungate come se avessero una coda luminosa). Questo sfuocamento in casi medi e avanzati può essere tale da ostacolare seriamente le attività quotidiane del paziente. Come viene fatta la diagnosi? E’ necessaria una visita oculistica accurata. In particolare, la topografia corneale con analisi delle curvature corneali sia anteriore che posteriore e la mappa pachimetrica permettono uno studio completo della geometria corneale. Il paragone di esami effettuati regolarmente nel tempo può confermare o escludere un’evoluzione del quadro. A B C D Peggioramento della visione nel cheratocono: mentre in A una cornea normale consente una perfetta messa a fuoco dell’immagine sulla retina, nel cheratocono la progressiva alterazione di curvatura (B, C, D) determina un progressivo deterioramento della capacità visiva 63 E’ possibile rallentare la progressione del cheratocono? L’unico trattamento che ha dimostrato efficacia nel rallentare e in molti casi a fermare l’evoluzione del cheratocono è il cross linking corneale o CXL (vedi capitolo apposito), che induce un aumento della rigidità della cornea. E’ indicato praticamente sempre nei giovani e giovanissimi vista la quasi ineluttabile tendenza a peggiorare, e comunque ogni qualvolta si riscontrino segni di evolutività. Sebbene la funzione del CXL sia quella di irrobustire la cornea e non di correggere difetti refrattivi o modificare la vista, in diversi casi si è osservato un miglioramento visivo a distanza di tempo dal trattamento CXL, in genere dopo diversi mesi. Il CXL è anche indicato in associazione a trattamenti conservativi come la PRK customizzata o l’impianto di anelli intrastromali. Come migliorare la capacità visiva? A secondo dell’entità dello sfiancamento, la curvatura irregolare provoca alterazioni dell’acuità e della qualità visiva fino a una perdita quasi completa. In casi molto rari l’assottigliamento della cornea può essere così marcato da mettere a rischio l’integrità del globo oculare: in tali casi bisogna intervenire tempestivamente con un trapianto di cornea. Solo in casi lievi, in cui le curvature corneali sono ancora abbastanza ben conservate, è possibile una correzione ottimale con lenti da occhiale. Un’eccessiva irregolarità della curvatura corneale non permette invece una focalizzazione adeguata sulla retina da parte delle lenti degli occhiali. Le lenti a contatto o LAC (rigide, ma anche semirigide o morbide) in molti casi permettono, se tollerate, di ottenere eccellenti risultati visivi. E’ spesso necessaria una certa dose di pazienza sia al contattologo che al paziente per trovare la giusta lente che fornisca un buon risultato visivo. Un concetto che a volte genera confusione e aspettative errate è quello che la lente a contatto rigida sia in grado di contrastare lo sfiancamento e rallentare l’evoluzione del cheratocono. Purtroppo la lente a contatto è solo appoggiata sulla cornea e non è in grado di “contenerla” e quindi evitare la progressione della malattia. Permette invece di correggere molto efficacemente il difetto rifrattivo irregolare tipico del cheratocono. Ciò viene ottenuto perché lo strato di lacrime che si viene a trovare 64 tra cornea e lente a contatto “ammortizza” le irregolarità corneali e ciò consente di migliorare la qualità visiva; inoltre, la correzione ottica fornita dalla LAC fornisce un aumento dell’acuità visiva. Se il cheratocono è troppo avanzato, la lente a contatto può non essere tollerata e debbono essere prese in considerazione le possibilità chirurgiche, più o meno conservative, a seconda della gravità del quadro. L’impianto di anelli intrastromali in casi selezionati permette di contrastare lo sfiancamento e regolarizzare la curvatura centrale della cornea (l’assottigliamento della cornea non deve essere troppo marcato). La regolarizzazione di curvatura consente una più facile correzione con occhiale o lente a contatto e un miglioramento della capacità visiva. Vengono impiantati con una procedura ambulatoriale in sottili canalini creati nello spessore corneale grazie all’azione estremamente precisa del laser a femtosecondi. E’ quindi una procedura chirurgica minimamante invasiva (vedi descrizione), nella quale non viene asportato tessuto corneale ed è anche completamente reversibile. Anche la PRK può essere utile in casi di cheratocono stabile e in forma leggera, cioè senza eccessivo sfiancamento e senza troppo assottigliamento corneale. Un trattamento su misura o “customizzato” permette di ridurre le irregolarità di curvatura più marcate o anche di eliminare alcune opacità superficiali che a volte insorgono anche dopo uso prolungato di lenti a contatto. La maggiore regolarità ottica ottenuta sul centro della cornea può portare a benefici visivi con una procedura minimamante invasiva. La PRK in tali casi deve essere accompagnata anche dal CXL. In alcuni casi un difetto rifrattivo molto elevato associato al cheratocono – di regola di tipo miopico e astigmatico – può essere parzialmente corretto anche grazie alla tecnica dell’impianto di un cristallino artificiale aggiuntivo o “IOL fachica” (cosiddetta tecnica del “doppio cristallino”) in modo del tutto analogo a quanto viene effettuato in casi di miopia elevata, con o senza astigmatismo. In casi di cheratocono più avanzato è necessario ripristinare la struttura corneale mediante un trapianto di cornea o cheratoplastica. 65 Quando le condizioni anatomiche lo consentono il chirurgo oculista cercherà di preservare gli strati più profondi della cornea e l’endotelio corneale eseguendo una cheratoplastica lamellare anteriore (DALK è la modalità più comune). Questo intervento, molto conservativo, consente di ridurre alcuni rischi intra e postoperatori, compreso il rigetto, ma in alcuni casi non è possibile eseguirlo e si può rendere necessario trapiantare la cornea in tutto il suo spessore eseguendo la cheratoplastica perforante. Con entrambi i tipi di trapianto si possono ottenere ottimi risultati nel recupero della capacità visiva. Cheratocono: che fare? Il cheratocono può presentarsi in stadi estremamente diversi, che richiedono soluzioni “su misura” che verranno valutate dal chirurgo oculista caso per caso. La scelta dipende da numerose variabili, ma cerchiamo di elencare gli interventi possibili e il loro razionale, partendo dalle soluzioni meno invasive: Correzione con occhiali un difetto rifrattivo lieve può essere correggibile con occhiali Lenti a contatto le lenti a contatto permettono di correggere difetti molto più elevati: ne esistono di vari tipi (morbide, morbide customizzate, ibride, rigide, etc.) Cross linking corneale (CXL) - - - Trattamento con laser a eccimeri (PRK customizzata) - - Anelli intrastromali o ICR (intracorneal rings) - - aumenta la rigidità e la stabilità biomeccanica della cornea previene la progressione della malattia può ridurre miopia e astigmatismo riduce l’astigmatismo irregolare al centro della cornea è molto utile associare CXL rinforzano la cornea regolarizzandone la curvatura (minore astigmatismo) meglio se impiantati con laser a femtosecondi Impianto di IOL fachiche (tecnica può correggere difetti residui di miopia e/o astigmadel “doppio” cristallino) tismo elevati Cheratoplastica lamellare anterio- Sostituisce gran parte della cornea deformata lare (DALK, etc.) sciando lo strato endoteliale (minor rischio di rigetto) Cheratoplastica perforante Sostituisce la cornea a tutto spessore (quando la patologia è molto avanzata) 66 PTERIGIO Lo pterigio è la crescita benigna di un tessuto vascolarizzato a livello della congiuntiva che invade la cornea, quasi sempre dal lato del naso. La sua comparsa è più frequente in persone che si espongono molto al sole, all’aria, alla polvere. Si pensa che i raggi ultravioletti siano implicati nella genesi dello pterigio. E’ sicuramente raccomandabile proteggersi con adeguati occhiali da vento, sole, polvere. I disturbi legati alla presenza dello pterigio sono soprattutto l’arrossamento dell’occhio, spesso associato a bruciore e fastidio. Anche l’inestetismo legato alla presenza di uno pterigio è un fattore non trascurabile nella decisione di intervenire. Inoltre in casi avanzati la crescita dello pterigio sulla cornea si può estendere fino alla pupilla o addirittura ricoprirla, con riduzioni visive anche gravi. Si cerca di intervenire chirurgicamente prima che lo pterigio invada così estesamente la cornea. Non è infatti possibile arrestarne la progressione o farlo regredire con terapia medica. I colliri lubrificanti (lacrime artificiali) e antiinfiammatori possono però alleviare il fastidio che spesso viene avvertito negli occhi affetti da questa patologia. Chirurgia dello pterigio: asportazione e autotrapianto di congiuntiva. Lo pterigio viene isolato dalla cornea e dalle strutture oculari, e quindi completamente rimosso. Un lembo di congiuntiva sana viene isolato nella parte superiore dell’occhio e trasportato a ricoprire la zona di congiuntiva mancante: costituisce un’efficace barriera alla ricrescita dello pterigio. La zona dove è stato prelevato il lembo per l’autotrapianto di congiuntiva guarisce senza problemi in pochi giorni. 67 Tecnica di esecuzione dell’asportazione di pterigio con autotrapianto congiuntivale L’intervento chirurgico sullo pterigio consiste nella sua asportazione. Si raccomanda di eseguire inoltre nello stesso intervento anche l’autotrapianto congiuntivale. Tale intervento combinato è infatti la procedura chirurgica maggiormente raccomandata per lo pterigio progressivo ed aggressivo e quella che dà le maggiori garanzie possibili in termini di prevenzione delle recidive. Le recidive, e quindi la necessità di reintervenire, sono purtroppo sempre possibili, dopo mesi o anche anni, ma si è visto che la tecnica chirurgica qui descritta ne riduce enormemente la probabilità. L’intervento viene eseguito ambulatorialmente in anestesia locale. La successione delle fasi operatorie è la seguente: • il paziente viene di norma anestetizzato mediante anestesia locale: viene eseguita un’infiltrazione di anestetico solo in corrispondenza dello pterigio, o intorno all’occhio nei casi di maggiore estensione della patologia; • il paziente viene fatto sdraiare sotto al microscopio operatorio; • viene poi applicato un divaricatore per tenere le palpebre moderatamente aperte e instillato collirio disinfettante (Iodopovidone 5%); • il chirurgo oculista effettua un accurato isolamento dello pterigio dalle strutture ad esso aderenti: oltre alla cornea che ricopre parzialmente, va isolato dalla congiuntiva, dalla sclera, e a volte, in caso di crescita marcata, anche dai muscoli che muovono l’occhio. In casi rari di recidiva si possono osservare erosioni corneali così gravi da necessitare di trapianto corneale lamellare, per ripristinare l’integrità della zona alterata; • tutto il tessuto dello pterigio viene quindi rimosso e si può procedere all’autotrapianto di congiuntiva; • nello stesso occhio viene prelevato un sottile foglietto di congiuntiva nel settore superiore. Questo foglietto viene quindi sollevato e portato a ricoprire la zona di congiuntiva malata dove era situato lo pterigio, fino al limite della cornea, dove viene fissato con fini suture riassorbibili o con colla biologica; • l’intervento è terminato, il chirurgo applica una medicazione antibiotica; • il divaricatore palpebrale viene rimosso; l’occhio viene normalmente chiuso e rimarrà bendato per alcune ore; • il paziente viene quindi accompagnato in una sala di attesa. 68 LE CELLULE STAMINALI Una forma molto particolare di trapianto, che nella stragrande maggioranza dei casi è in effetti un autotrapianto, è quella che riguarda le cellule staminali dell’epitelio corneale, o cellule staminali corneali limbari. Tutti i media (giornali, televisione, ecc.) tendono ad esporci a innumerevoli notizie che riguardano le cellule staminali, il più delle volte però senza spiegare di quali cellule si sta parlando e per curare cosa. Nel caso dell’occhio esiste una terapia, consolidata da alcuni anni, che ha superato la fase sperimentale e ha consentito di risolvere situazioni molto gravi non altrimenti trattabili. L’epitelio corneale è lo strato più esterno della cornea, costituito da cellule specializzate che (similmente a quanto avviene per la pelle) continuano a rinnovarsi. Questo rinnovarsi è possibile perché esistono delle cellule “staminali” specifiche dell’epitelio corneale: in pratica ognuna di queste cellule si divide in due: una si dirige lentamente verso il centro della cornea e dopo un certo tempo (molti mesi) verrà eliminata in superficie, mentre l’altra rimane uguale a se stessa, pronta per ricominciare il ciclo e dividersi nuovamente. Le cellule staminali dell’epitelio corneale sono localizzate alla periferia della cornea, in una regione detta limbus (sono infatti dette anche cellule staminali limbari). Soprattutto in seguito a causticazioni, queste cellule staminali specializzate possono danneggiarsi irreparabilmente. La cornea, senza le sue cellule epiteliali specifiche, tenderà ad essere rivestita da vasi (neovascolarizzazione) e perderà trasparenza. Anche se viene eseguito un trapianto di cornea, la mancanza di cellule staminali limbari condanna il trapianto a perdere trasparenza come è accaduto alla cornea che è stata sostituita. Una possibilità recentemente messa a punto è quella di effettuare una piccola biopsia, di soli 1-2 mm, dall’occhio sano o meno danneggiato del paziente, fare crescere in laboratorio (“ex-vivo”) le 69 cellule “staminali”, e reimpiantare uno strato ricco di queste cellule sull’occhio malato, dopo aver liberato la cornea dai vasi anomali che la rivestono. Questa metodica richiede la collaborazione con un centro di medicina rigenerativa (“Cell Factory”, letteralmente fabbrica delle cellule) che esegue in speciali laboratori l’isolamento, la coltura e l’espansione delle cellule prelevate. Si tratta di una terapia che presenta un elevato grado di complessità e costi elevati, ma in alcuni casi, fortunatamente rari, costituisce l’unica possibilità terapeutica. In conclusione è opportuno ricordare che: - le cellule staminali non sono una terapia in grado di curare qualunque malattia dell’occhio o anche solo della cornea. - l’unica terapia con cellule staminali di utilizzo clinico convalidato è quella per ricostruire l’epitelio corneale (cellule staminali corneali limbari). Tale terapia si applica solo in gravi casi, fortunatamente rari, di “panno corneale” (una membrana vascolare che ricopre la cornea), spesso conseguenza di un incidente con agenti chimici (causticazione). - è allo studio una interessante evoluzione di autotrapianto di cellule staminali corneali limbari che si spera permetterà di risolvere alcuni rari casi di distrofia corneale. In questi casi il laboratorio non solo farà “crescere” le cellule del paziente, ma ne correggerà con una terapia genica specifica l’errore metabolico che porta alla formazione delle opacità. Le cellule staminali che verranno impiantate saranno quindi si quelle proprie del paziente (trapianto autologo), ma private del difetto genetico che porta alla distrofia e spesso conduce al trapianto di cornea. - esistono altre terapie con cellule staminali per curare patologie oculari, ad esempio per la terapia di gravi malattie retiniche, ma si tratta ancora di studi sperimentali. I primissimi casi trattati nell’uomo sono stati di quelli di impianto di cellule di epitelio pigmentato retinico in maculopatie molto avanzate con risultati abbastanza incoraggianti: saranno necessari ancora numerosissimi esperimenti prima di poter ipotizzare una vera e propria applicazione clinica. 70 DISAGI, RISCHI, COMPLICANZE Gli interventi sull’occhio sono interventi chirurgici delicati ma generalmente sicuri. Comunque, come qualsiasi altro intervento, non sono privi di rischi e il loro successo non può essere garantito in quanto possono intervenire condizioni che potrebbero avere ripercussioni negative sulle condizioni finali della vista. Alcuni possibili inconvenienti o complicanze successivi agli interventi oculari sono: • Sensazione di fastidio o dolore più o meno accentuati • Arrossamento dell’occhio. • Ematoma alla congiuntiva o alla palpebra. • Abbassamento della palpebra superiore. • Incompleta chiusura della ferita chirurgica. • Deficit ad uno dei muscoli dell’occhio. • Innalzamento della pressione intraoculare. • Infiammazione della parte anteriore o posteriore dell’occhio. • Emorragie, che generalmente vengono riassorbite spontaneamente senza conseguenze visive; altre volte le emorragie sono più gravi e possono comportare riduzione permanente della vista. • Alterazioni temporanee o permanenti di uno o tutti gli strati della cornea con possibilità di opacità corneale. • Irregolarità della pupilla. • Distacco di retina o peggioramento delle alterazioni retiniche preesistenti. • Infezione: è un rischio estremamente raro ma possibile; nei casi più gravi esse possono condurre anche a gravi ripercussioni sulla vista. • Talvolta anche nel caso sia già stato programmato l’intervento, si possono verificare condizioni intraoperatorie che rendono non indicata o non possibile la sua esecuzione, che, quindi, deve essere rinviata. • L’operazione talvolta comporta l’insorgenza di astigmatismo; • In alcuni casi, nell’immediato periodo postoperatorio o dopo mesi 71 o anni, potrà essere necessario dover rimuovere e sostituire il tessuto trapiantato Gli interventi in occhi già sottoposti ad interventi di glaucoma, retina o cataratta aumentano di difficoltà e sono maggiormente soggetti ad imprecisioni. La difficoltà aumenta anche in caso di patologie oculari preesistenti (come miopia elevata, glaucoma). Fra le complicazioni postoperatorie alcune sono controllabili con terapie mediche; altre possono essere permanenti o rendere necessario un successivo intervento. Il recupero visivo è legato, oltre che alla corretta conduzione dell’intervento, alle condizioni anatomiche e funzionali preoperatorie del nervo ottico e della retina, oltre che allo stato della pressione intraoculare ed alle condizioni generali dell’occhio. Quindi se esistono danni alla retina o al nervo ottico o altrove, la visione potrà essere imperfetta malgrado la corretta esecuzione dell’intervento. Per ulteriori e maggiori informazioni, vedere il consenso informato specifico per ogni intervento oculare. 72 PRECAUZIONI E PRESCRIZIONI DOPO L’INTERVENTO Le cure Prima di lasciare il centro chirurgico viene consegnato un foglio con le istruzioni dei farmaci da utilizzare. Il paziente deve iniziare le cure dopo un paio d’ore dall’intervento, deve cioè iniziare a prendere le pillole e i colliri prescritti dal chirurgo. Il paziente non deve mai sospendere le cure (colliri o pillole) a meno che sia il chirurgo a dirlo; esse aiutano l’occhio operato a guarire meglio ed a prevenire complicazioni. Per applicare i colliri (per le pomate la procedura è uguale) nell’occhio operato, il paziente deve sedersi su una sedia (in alternativa può stare sdraiato a letto), deve aprire bene ambedue gli occhi e guardare verso il soffitto; poi deve abbassare con l’indice della mano sinistra la palpebra inferiore; in tal maniera fra l’occhio e la palpebra si forma una specie di coppa che serve a ricevere le gocce di collirio medicinale; qui con la mano destra vanno instillate 1-2 gocce del prodotto. Il paziente deve poi chiudere le palpebre (senza stringerle) e attendere per qualche secondo l’assorbimento del prodotto. Quando i colliri prescritti sono più di uno essi vanno applicati uno di seguito all’altro a distanza di qualche minuto. E’ bene che almeno nei primi 2-3 giorni sia un familiare ad instillare i colliri. Durante l’applicazione del collirio occorre prestare attenzione a non esercitare pressioni nell’occhio appena operato. Modalità di applicazione del collirio: Le precauzioni con le dita di una mano si abbassa L’occhio operato viene raramente benla palpebra e con l’altra mano si indato; il più delle volte viene protetto con stilla una goccia di collirio 73 un paio di occhiali da sole che hanno lo scopo di riparare l’occhio dalla luce, dall’aria, dalla polvere e soprattutto da eventuali traumi; gli occhiali da sole non occorre che siano molto scuri, ma vanno tenuti durante tutta la giornata, quindi anche in casa, per almeno una settimana; in casa, possono anche essere chiari (il paziente che si appresta ad affrontare l’intervento di cataratta si munisca di un occhiale appropriato). Durante la notte invece l’occhio, per la prima settimana, va protetto con una “conchiglia” in plastica che in genere viene fornita alla dimissione; la conchiglia va tenuta in sede con due o tre cerotti; essa serve ad evitare involontari traumi all’occhio ed a proteggere contro strofinamenti, sempre possibili nel sonno. Una o due volte al giorno le palpebre dell’occhio operato vanno delicatamente pulite con un fazzolettino detergente o con un po’ di cotone bollito; chi esegue tale manovra deve evitare pressioni sul bulbo oculare e comunque sulla parte operata. Nel periodo successivo all’intervento il paziente deve inoltre usare alcune altre attenzioni: • non si deve assolutamente strofinare l’occhio operato (per almeno un mese); è opportuno evitare gli strofinamenti, soprattutto se pesanti, anche nei mesi successivi. • Non si devono inoltre fare sforzi fisici eccessivi (per i primi 2-3 giorni); per esempio non si devono sollevare pesi superiori ai dieci chilogrammi, non prendere in braccio bambini ecc. • L’uso di macchinari o di strumenti pericolosi è sconsigliato per un periodo di almeno una settimana. • Non dormire con la faccia rivolta verso il cuscino (per almeno due settimane); si può però dormire dal lato dell’occhio operato purché questo sia adeguatamente protetto con la conchiglia di plastica che viene fornita. • Da evitare sono pure gli ambienti con prodotti irritanti (ambienti con gas chimici, locali fumosi, posti polverosi ecc.); per qualche giorno evitare pure che shampoo e sapone entrino nell’occhio operato (la doccia può essere fatta fin dal giorno dopo, tenendo gli occhi chiusi quando si usa lo shampoo). • Nelle prime due-tre settimane seguenti all’intervento non fare bagni in piscina o al mare (a meno che non si usi una maschera), non truccare gli occhi, non esporsi a prodotti spruzzati da bombolette spray, etc.. • L’attività sportiva leggera (corsa, ginnastica, ecc.) può essere ripresa anche dopo 3-4 giorni; per fare sport più pesanti attendere 74 4-6 settimane (chiedere maggiori dettagli al chirurgo perché ciò non vale per tutti i tipi di interventi). • Nelle prime settimane è preferibile non esporsi a lungo alla luce intensa del sole specialmente in alta montagna o al mare senza un’adeguata protezione con occhiali scuri dotati di filtro contro i raggi ultravioletti; un occhiale da sole di buona marca è sufficiente a tale scopo. Cosa si puo’ fare dopo l’intervento Il decorso postoperatorio non è fatto però solo di divieti; il paziente fin dai primi giorni può fare molte cose, per esempio: • fin dal giorno dell’operazione può, con l’occhio non operato, leggere, scrivere, guardare la televisione ecc.. (in tal caso la visione dell’occhio operato è preferibile che sia esclusa applicando un pezzo di nastro adesivo sulla superficie posteriore della lente dell’occhiale). • già il giorno dopo l’intervento può lavarsi regolarmente il viso, fare la doccia, la barba, facendo però attenzione a non strofinare l’occhio operato ed a non esercitare pressioni; è preferibile se durante la doccia l’occhio operato viene tenuto chiuso. • L’asciugacapelli può essere adoperato purché il getto di aria calda non venga diretto verso l’occhio operato; le signore possono andare dal parrucchiere già 2-3 giorni dopo l’operazione. • La barba può essere fatta fin dal giorno seguente all’operazione. • Rapporti sessuali sono permessi già 2-3 giorni dopo l’intervento (in caso di trapianto perforante occorre attendere di più). • L’uso del computer, della televisione può iniziare unodue giorni dopo l’intervento se il paziente si sente di farlo; la guida 3-4 giorni dopo, a condizione che l’occhio operato abbia un’acuità visiva tale da consentirla. In caso di dubbi sulle modalità della terapia da seguire o sull’andamento del decorso postoperatorio il paziente deve contattare uno dei componenti dell’èquipe chirurgica. Ciò anche perché le suddette precauzioni possono non essere sufficienti per alcuni pazienti ed, in particolare, per alcuni interventi eseguiti. Altre informazioni Nei giorni seguenti all’operazione l’occhio appare più o meno “rosso” e moderatamente dolente; c’è inoltre una certa sensazione di corpo estraneo (dovuta ad eventuali punti ed al taglio praticato) ed un certo fastidio alla luce; tutti questi sintomi sono normali e non devono preoccupare il paziente. 75 L’occhio operato percepisce i colori in maniera diversa da un occhio sano; talvolta inoltre vede le luci un po’ allungate e con degli aloni intorno. Nei primi giorni successivi all’intervento la visione dell’occhio operato è molto offuscata e occorre attendere giorni o settimane perché raggiunga livelli migliori; in questo periodo occorre avere un po’ di pazienza; la guarigione avviene di norma entro qualche settimana o mese (dipende dal tipo di intervento eseguito). Ricordare che l’entità di visione recuperabile con l’intervento, oltre che dalla corretta esecuzione dell’operazione, dipende molto dalle preesistenti condizioni dell’occhio, in particolare della retina e del nervo ottico. La prescrizione dell’occhiale per l’occhio operato, se richiesta e necessaria, viene fatta dopo qualche settimana dall’intervento o qualche mese; ciò dipende dal tipo di intervento eseguito. Per concludere il paziente deve ricordarsi che anche a guarigione avvenuta l’occhio va periodicamente controllato dall’oculista; nei mesi e negli anni successivi all’intervento egli deve quindi sottoporsi ad alcuni periodici controlli che vengono progressivamente diradati; l’insorgenza di problemi è rara e nella gran parte dei casi essi, quando vengono diagnosticati in tempo, possono essere risolti facilmente. 76 CONCLUSIONI La chirurgia della cornea presenta molteplici sfaccettature, e permette di intervenire con procedure anche molto diverse fra loro e che presentano gradi diversi di invasività. In molti casi è oggi possibile ottenere significativi miglioramenti intervenendo in modo minimamente invasivo, grazie soprattutto all’utilizzo dei laser. Alle numerose patologie che possono interessare la cornea non corrisponde sempre in modo univoco una terapia specifica, ma possono essere applicabili trattamenti differenti a secondo della gravità della evoluzione. In certi casi più trattamenti possono essere combinati, come accade quando il cross linking corneale viene associato ad altre procedure conservative come l’impianto di anelli intrastromali nel cheratocono. Dopo la lettura di questa pubblicazione il lettore non sarà autonomamente in grado di individuare esattamente quale terapia può essere utile al suo caso, ma avrà sicuramente acquisito elementi per ascoltare e discutere in modo informato le possibilità terapeutiche che il chirurgo oftalmologo gli proporrà per la soluzione del suo problema specifico. Attualmente i chirurghi oculisti hanno a disposizione alcune tecniche semplici e non invasive (crosslinking, impianto di anelli corneali, PTK) o altre più complesse (cheratoplastica lamellare o perforante) che consentono di sostituire porzioni alterate e più o meno estese di cornea, di spessore parziale o totale, con lembi corneali sani e trasparenti. In tutte le procedure il mantenimento, nel decorso postoperatorio, della trasparenza della cornea e della regolarità della sua superficie anteriore sono il presupposto indispensabile per una riuscita dell’intervento anche a lungo termine. Occorre comunque sempre tener presente che, in qualche caso particolare, è necessario ricorrere a più di un intervento per poter assicurare una buona funzione visiva. Ciò è vero soprattutto nella cheratoplastica perforante, ove talvolta non è possibile anche con tutte le risorse mediche, mantenere per sempre la trasparenza del 77 lembo trapiantato; nella cheratoplastica lamellare invece le probabilità di rigetto o di perdita di trasparenza sono minori. Le malattie della cornea sono di difficile trattamento e la chirurgia non riesce sempre a fornire risultati altamente soddisfacenti, come ad esempio si ottengono nella chirurgia della cataratta ma i risultati delle tecniche di cheratoplastica vengono continuamente migliorati dall’utilizzo dei laser (a femtosecondi e ad eccimeri) dall’esperienza del chirurgo, dalla tecnica chirurgica adottata, da tutte le precauzioni messe in atto per il prelievo e la conservazione del lembo da trapiantare e forniscono risultati visivi sempre migliori. Il chirurgo e la sua equipe preparano il paziente al trapianto di cornea in sala operatoria sterile, dopo aver eseguito l’ablazione con il laser a femtosecondi 78 RISPOSTE ALLE DOMANDE CHE PIU’ FREQUENTEMENTE IL PAZIENTE PONE ALL’OCULISTA… …SUI TRAPIANTI DI CORNEA Come vengono reperite le cornee da trapianto? Il tessuto corneale proviene da persone che hanno deciso di effettuare la donazione perchè altri possano averne un beneficio. Per tanti anni il problema maggiore del trapianto di cornea è stato quello di reperire un numero sufficiente di donatori. Esiste una rete nazionale che si occupa delle donazioni, che afferiscono alle cosiddette Banche degli Occhi. Oggi, grazie a una maggiore sensibilizzazione della popolazione e ad una efficiente organizzazione dei prelievi e della selezione dei tessuti, la disponibilitá di cornee è maggiore e quindi il trapianto di cornea non deve più essere visto come un evento eccezionale. Tutte le persone sono potenziali donatori di cornea? In caso di decesso di una persona, è necessario che i parenti tramite i medici o il personale infermieristico del reparto ospedaliero, manifestino la volontà di donare le cornee e firmino un’autorizzazione scritta. E’ compito del personale sanitario avviare le procedure per il prelievo. I tessuti prelevati vengono inviati alla più vicina Banca degli occhi, che, dopo averne valutato l’idoneitá, li distribuisce alle strutture, dove i chirurghi oftalmologi eseguono i trapianti. Si tratta di un network nazionale e sovranazionale regolato da criteri estremamente rigorosi che garantiscono il rispetto e la segretezza dei donatori oltre alla sicurezza dei pazienti. Le cornee per il trapianto possono trasmettere malattie? A differenza degli organi, come per esempio il cuore o i reni, la cornea è un tessuto, e non contiene vasi sanguigni: per questo motivo è difficile che i germi responsabili di malattie infettive possano contaminare il tessuto corneale. In ogni caso, vengono esclusi i donatori positivi per epatite B, epatite C, AIDS e i tessuti 79 vengono sottoposti ad accurati controlli microbiologici. Si tratta di un intervento doloroso? No. L’intervento non comporta dolore. Se si esegue in anestesia generale il paziente viene completamente addormentato, se si esegue in anestesia locale, tutta la zona intorno al bulbo oculare ed il bulbo oculare vengono anestetizzati. Quali sono i disturbi dopo l’intervento? Sono normali una iniziale difficoltá a tenere l’occhio aperto, un certo fastidio alla luce e una certa lacrimazione: tutto questo migliora gradualmente nell’arco di alcuni giorni. A volte il bulbo operato è dolente o arrossato. Tomati a casa, come ci si deve regolare? Una volta fatto il trapianto si possono riprendere le normali attivitá quotidiane, come leggere (con l’occhio non operato), guardare la televisione, uscire di casa, occuparsi delle piccole faccende domestiche. Particolare attenzione deve essere rivolta a evitare pressioni sull’occhio operato, in quanto la ferita è ancora in via di cicatrizzazione. Dopo l’intervento è necessario tenere l’occhio bendato? No. Per le prime settimane è consigliato tenere una protezione di plastica (conchiglia) durante la notte, mentre si dorme, per evitare traumi accidentali o strofinamenti involontari. E’ pure necessario proteggere l’occhio durante il giorno con occhiali avvolgenti per evitare traumi e l’irritazione da agenti atmosferici (luce, vento, polvere). E l’igiene del viso e del corpo? E’ possibile lavarsi il viso, i capelli o fare la doccia avendo l’accortezza di non far entrare l’acqua nell’occhio operato durante le prime due tre settimane perché l’acqua può contenere germi e causare infezioni. A tale scopo puó essere sufficiente tenere l’occhio chiuso durante le suddette procedure oppure mettere una benda autoadesiva. Quanto tempo impiega l’occhio a recuperare la vista? I tempi per un pieno recupero visivo variano da persona a persona e da occhio a occhio. Per ottimizzare la visione puó essere indicato l’uso di occhiali o di lenti a contatto o la rimozione di uno o più punti di sutura. In generale, comunque occorrono alcune settimane o mesi affinchè la visione sia discretamente buona. 80 Quando si può guidare la macchina? Tutto dipende dalla vista dell’occhio non operato; occorre comunque ricordare che la visione con un solo occhio riduce la capacitá di percezione della profonditá e può quindi ridurne la capacitá di prevenire o evitare ostacoli. E’ necessario quindi attenersi ai requisiti di legge e comunque rimettersi alla guida con prudenza. Quando si può riprendere a lavorare? Ogni attivitá che richieda sforzi fisici o l’uso dell’occhio operato va eseguita con prudenza. La ripresa del lavoro è condizionata dal tipo di attivitá che si svolge: ad esempio, il lavoro in un ufficio può essere iniziato anche pochi giorni dopo; un lavoro che comporta sforzi fisici, rischi di traumi oppure polvere o sporcizia va ripreso dopo alcune settimane. In linea di massima, si consigliano da uno a due mesi di convalescenza, ma molto dipende da come l’occhio guarisce; ai controlli postoperatori chiedere al medico quando poter riprendere l’attivitá. E’ possibile fare attivitá sportiva dopo il trapianto? L’attivitá sportiva può essere gradualmente ripresa dopo il primo mese, facendo molta attenzione negli sport che comportano rischi di traumi all’occhio come il tennis, il calcio, la pallavolo, la pallacanestro ed altri. Non ci sono invece problemi per una moderata attivitá di palestra, la corsa e la bicicletta. La piscina è controindicata per i primi sei mesi ed è in ogni caso a rischio per la possibilitá di contrarre congiuntiviti e per l’effetto irritante del cloro. Bisogna ricordare sempre che l’infiammazione dell’occhio in seguito all’esposizione all’aria, il sudore, gli sforzi eccessivi, può aumentare il rischio di rigetto. Il rigetto della cornea è possibile? La maggior parte dei casi clinici che necessitano di trapianto di cornea perforante o endoteliale (forme gravi di cheratocono, opacità corneali non vascolarizzate, cheratopatia bollosa) sono interventi a basso rischio di rigetto. Se si manifesta il rigetto, puó essere fatto regredire con una pronta ed efficace terapia. ll rischio di rigetto si verifica per lo più dopo circa un mese e si riduce gradualmente con il passare del tempo; raramente si possono verificare episodi di rigetto anche a distanza di molti anni dal trapianto. Nei casi in cui il rigetto abbia comportato l’opacamento della cornea trapiantata, l’intervento puó essere ripetuto, instaurando però una adeguata terapia preventiva. 81 Nel caso del trapianto lamellare anteriore, il rischio di un rigetto grave è virtualmente assente. Quali sono i sintomi del rigetto? Il rigetto si manifesta all’inizio con lievi disturbi quali l’appannamento della vista, fastidio alla luce, arrossamento dell’occhio e talvolta dolore oculare. Quindi, se questi sintomi compaiono è importante recarsi immediatamente dall’oculista perché è fondamentale, per evitare danni al trapianto, iniziare la terapia il più presto possibile. Il rischio di rigetto aumenta quando l’occhio è irritato o quando vengono fatti interventi o tolti punti alla cornea. E’ necessario quindi fare molta attenzione a tutte quelle situazioni che possono determinare infiammazioni dell’occhio operato: vento, polvere, sostanze irritanti, ecc. Dopo l’intervento quali sono le cure dell’occhio? Le terapie prescritte dal chirurgo oculista devono essere seguite con precisione e scrupolo perché ogni dimenticanza può aumentare il rischio di rigetto e di infezioni. Di solito la terapia viene protratta per diversi mesi e ridotta gradualmente col passare del tempo. Prima di instillare le gocce di collirio bisogna sempre lavarsi le mani e fare attenzione a non toccare le palpebre con l’erogatore del collirio. E’ buona norma conservare i colliri in frigo o quanto meno lontano da fonti di calore. Quando viene tolta la sutura? La sutura viene rimossa se i punti inducono astigmatismo o irritazione o comunque una reazione non desiderata; oppure quando, a giudizio del medico, la cicatrice corneale è stabilizzata. La rimozione richiede pochi minuti e viene fatta per lo più in ambulatorio; l’occhio viene anestetizzato con alcune gocce di collirio e la procedura non comporta dolore. L’occhio viene poi medicato e dopo qualche giorno si possono riprendere tutte le comuni attivitá quotidiane, ricordando sempre che la ferita è fragile. Fa eccezione a questo proposito il trapianto endoteliale, nel quale il bulbo oculare è molto robusto, in quanto vi è solo una piccola incisione periferica e non una a 360° gradi come nel trapianto perforante o lamellare anteriore. Non è questo in ogni caso un buon motivo per correre rischi: anche un occhio normale mai operato è una struttura delicata! 82 DOMANDE E RISPOSTE SUL CROSS-LINKING CORNEALE (CXL) Il cross-linking corneale (CXL) è un intervento chirurgico? No, è considerato un intervento “para-chirurgico”. La cornea non viene sottoposta a manovre chirurgiche vere e proprie, come incisioni o suture. In cosa consiste? In sostanza la cornea viene irraggiata da una sorgente a raggi ultravioletti dopo essere stata imbibita di una sostanza, la riboflavina. A cosa serve il CXL? Induce la formazione di legami chimici fra le molecole di collagene della cornea, aumentandone la rigidità e la resistenza. Per questo motivo permette di rallentare o arrestare la tendenza allo sfiancamento in alcune patologie della cornea, prima fra tutte il cheratocono. Può essere utilizzato in altre situazioni? Sì, è stato utilizzato con successo nel trattamento di infezioni corneali resistenti, sfruttando l’azione sterilizzante dei raggi UV. Può inoltre essere associato alla chirurgia refrattiva corneale a scopo preventivo in alcuni casi complessi. Dove e come viene eseguito il CXL? Il trattamento viene eseguito ambulatorialmente, con il paziente sdraiato su un lettino in un ambiente protetto come un ambulatorio chirurgico. Sia l’imbibizione che l’irraggiamento possono essere eseguiti con modalità e tempi diversi. In particolare, vi è una tendenza nell’evoluzione della tecnica a utilizzare modalità che accellerano l’imbibizione della cornea da parte delle riboflavina e irraggiamenti di maggiore intensità, che permettono di abbreviare notevolmente i tempi dell’intervento. Cosa significano i termini epi-on, epi-off e iontoforesi applicati al CXL? Epi-off è la prima tecnica, nella quale l’epitelio corneale viene 83 asportato all’inizio del trattamento per far sì che la riboflavina penetri con facilità nella cornea: consente di ottenere un buon irrigidimento della cornea, ma è un po’ invasivo e fastidioso per il paziente, e il recupero visivo è piuttosto lento. Epi-on significa che l’epitelio corneale non viene toccato, e si utilizza una apposita formulazione di riboflavina che riesce ad attraversarlo per penetrare all’interno della cornea: questa modalità consente al paziente di avere meno disturbi ma l’effetto di irrigidimento sulla cornea è meno marcato rispetto alla tecnica classica. La iontoforesi applicata al CXL consente di “forzare” il passaggio della riboflavina attraverso l’epitelio corneale grazie all’utilizzo di un campo elettrico fornito da due piccole batterie. In questo modo si ottiene lo stesso effetto di irrigidimento della cornea della tecnica epi-off, ma senza gli inconvenienti ed i fastidi legati all’asportazione dell’epitelio. Si tratta di un intervento doloroso? No. L’intervento non comporta dolore. Vengono utilizzate delle gocce di anestetico e al termine dell’intervento viene applicata una lente a contatto terapeutica. Quali sono i disturbi dopo l’intervento? Con la tecnica epi-off sono normali una iniziale difficoltá a tenere l’occhio aperto, un certo fastidio specie alla luce e una certa lacrimazione ed, a volte, dolore: tutto questo migliora rapidamente nell’arco di uno-due giorni. Con la tecnica di iontoforesi i disturbi sono minori rispetto alla tecnica epi-off. In pratica quasi nessun fastidio con la tecnica epi-on. Quanto tempo impiega l’occhio a recuperare la vista? Il recupero della vista può richiedere alcune settimane per la tecnica epi-off, mentre è più rapido per la tecnica con iontoforesi e con la tecnica epi-on. Il difetto visivo preesistente può ridursi con il trattamento di CXL? E’ possibile. In alcuni casi si assiste ad una lieve riduzione del difetto visivo con conseguente miglioramento della qualità visiva. Si tratta in genere di un miglioramento che si avverte nel giro di mesi e spesso tende a migliorare ulteriormente a 1-2 anni dal trattamento. In conclusione, cosa si vuole ottenere con il CXL? La tecnica, irrobustendo la cornea, si propone di stabilizzare la malattia. Se eseguito precocemente può evitare la necessità di fare il trapianto di cornea. 84 DOMANDE E RISPOSTE SULLA CHIRURGIA DELLO PTERIGIO E’ sempre necessario asportare lo pterigio? No. L’intervento è consigliabile nel caso lo pterigio crei problemi (arrossamento, fastidio, inestetismo marcato). La necessità assoluta di asportare lo pterigio si ha quando la sua crescita avanza verso il centro della cornea e quindi rischia di compromettere seriamente la capacità visiva. In cosa consiste l’intervento? Lo pterigio viene isolato dalla cornea e dalle altre strutture della superficie oculare cui è adeso. Viene inoltre il più delle volte eseguito anche un autotrapianto di congiuntiva sana, prelevato dallo stesso occhio, per ridurre al minimo il rischio di recidive. Si tratta di un intervento doloroso? No. L’intervento non comporta dolore: viene effettuato in anestesia locale in ambulatorio chirurgico ed è di breve durata. Quali sono i disturbi dopo l’intervento? Sono normali una iniziale difficoltá a tenere l’occhio aperto, un certo fastidio specie alla luce e una certa lacrimazione: tutto questo migliora rapidamente nell’arco di alcuni giorni. Solitamente nei primi giorni, l’occhio è molto rosso. Quanto tempo impiega l’occhio a recuperare la vista? A parte rari casi in cui lo pterigio ha coinvolto il centro della cornea, la vista non viene influenzata dall’intervento. Può esservi un transitorio annebbiamento dovuto al trattamento con gel o pomate oftalmiche nel periodo postoperatorio. Lo pterigio può recidivare? Sì, è possibile, ma l’esecuzione dell’intervento con la tecnica corretta rende tale evento molto improbabile. È comunque possibile intervenire con successo anche su pterigi recidivanti. 85 INTERVENTO IN DAY SURGERY Il Day Surgery del Centro Ambrosiano Oftalmico è nato e quindi organizzato ed attrezzato per eseguire la chirurgia dell’occhio senza ricovero notturno; il paziente si reca al Centro il mattino dell’operazione, riceve la necessaria preparazione, viene operato e poi va a casa a fine mattina o nel pomeriggio. Quasi tutti gli interventi sull’occhio non richiedono ricovero in quanto sono interventi che riguardano un piccolo organo quasi indipendente dal resto dell’organismo; inoltre sono interventi che non alterano le condizioni fisiche generali del paziente anche perché sono di breve durata e spesso non richiedono anestesie profonde. L’intervento avviene con l’assistenza di un anestesista e l’ambiente è dotato degli strumenti necessari ad assistere il paziente sia durante che dopo l’intervento; inoltre la sala operatoria è attrezzata con le più recenti apparecchiature per la moderna chirurgia oftalmica. Premesso che le attuali tecniche chirurgiche sono già per conto loro più sicure e più precise di quelle utilizzate fino a pochi anni or sono, la chirurgia oftalmica eseguita in day surgery presenta, rispetto a quella eseguita in ospedale, parecchi vantaggi: • la sala chirurgica e le sale complementari (sale d’attesa, sala postoperatoria) sono attrezzate per le specifiche esigenze dell’oculista e del paziente oftalmico; • il paziente viene assistito da personale specificamente educato e preparato alla chirurgia oftalmica; esso quindi ha una competenza specialistica maggiore e si occupa meglio del paziente; • l’utilizzazione sempre dello stesso personale permette di ottenere una sua migliore conoscenza e familiarità con le strumentazioni e quindi un miglior uso delle stesse; • il paziente evita il ricovero, elemento questo che comporta sempre una certa ansia e preoccupazione (a nessuno piace andare in ospedale... anche perché spesso proprio in ospedale si prendono delle malattie...); 86 • il paziente può essere mobilizzato subito, può cioè alzarsi, camminare etc; • il paziente può avere la compagnia e l’assistenza dei suoi familiari per cui egli si trova in un’atmosfera rilassante prima e dopo l’intervento; ciò riduce il suo stato di ansia e di tensione per cui egli affronta con maggior tranquillità l’operazione con indubbi effetti positivi sul risultato finale; tutto ciò permette anche di utilizzare una minor quantità di farmaci sedativi ed anestetici. Dopo l’operazione il paziente viene trattenuto al centro per una mezz’ora circa e poi, dopo un adeguato controllo sanitario, se abita vicino alla struttura chirurgica, viene inviato a casa (accompagnato da un familiare); egli quindi può contare sull’assistenza di un parente o di un amico e sul proprio ambiente domestico evitando così la fredda ed impersonale struttura ospedaliera. A casa non è richiesta una particolare assistenza generale, solo la compagnia di qualcuno. Se invece abita lontano (a più di un’ora e mezza dalla struttura chirurgica) è bene che rimanga a dormire per la prima notte in un albergo nelle vicinanze dell’ambulatorio chirurgico. Dopo l’intervento il paziente viene trattenuto per il tempo necessario e dopo un adeguato controllo da parte del chirurgo, viene dimesso 87 SERVIZIO URGENZE In orario di ufficio (10.00-12.15/13.15-18.30) chiamare lo studio di Piazza Repubblica 21 al numero 02-6361191 e comunicare il motivo dell’urgenza. Solo per i pazienti operati degli ultimi tre giorni e solo in caso di vera necessità esiste un servizio di reperibilità; esso è operante negli orari di chiusura dell’ufficio (se possibile, evitare le chiamate notturne). Chiamare il numero telefonico indicato nel foglio di terapia che viene dato alla dimissione; è il numero di un telefono cellulare, in caso di difficoltà ripetere la chiamata o inviare un sms o lasciare il messaggio in segreteria telefonica dicendo chiaramente e lentamente nome e cognome e numero di telefono (ripetere due volte il numero telefonico). Per appuntamenti, informazioni o esigenze di normale amministrazione, chiamare in giorni feriali ed in orario di ufficio lo studio di Piazza Repubblica 21, preferibilmente al mattino, al seguente numero: 02-6361191. 88 GLOSSARIO • Afachia: è l’occhio privo di cristallino • Anestesia: procedura per cui si rende indolore l’intervento; può essere topica (a base di gocce), locale (con iniezione) o generale. • Astigmatismo: è un difetto di rifrazione dovuto ad una curvatura ovoidale della cornea; comporta affaticamento visivo, mal di testa e visione ridotta. • Cataratta: opacità del cristallino umano • Chirurgia rifrattiva: ogni tipo di intervento che si propone di correggere un difetto di rifrazione (miopia, astigmatismo, ipermetropia, ecc.). • Cheratocono: malattia della cornea; essa si assottiglia progressivamente, subisce cambiamenti di forma e ciò induce un calo progressivo della vista. • Cornea: struttura trasparente situata nella parte anteriore dell’occhio; serve a concentrare la luce sulla retina. Sulla cornea vengono eseguiti la maggior parte dei trattamenti laser per la correzione dei difetti rifrattivi. • Cristallino umano: lente situata nella porzione interna dell’occhio, dietro al foro pupillare; serve a focalizzare la luce sulla retina (se diventa opaca, si ha la cataratta). • Cristallino artificiale: è una piccola lente, costituita da materiale sintetico trasparente; serve a correggere una miopia elevata o a rimpiazzare il cristallino umano quando questo viene rimosso. • Crosslinking: terapia non chirurgica del cheratocono; se eseguito precocemente è in grado di arrestare la malattia. • Decimi di vista: unità convenzionale di misura per valutare quantitativamente l’acuità visiva di un soggetto; non ha corrispondenza con le diottrie che il paziente usa sull’occhiale o sulla lente a contatto. Una persona ha dieci decimi quando può leggere le lettere più piccole che vengono mostrate durante la visita oculistica; ha 5/10 o 1/10 solo quando legge i caratteri di media grandezza o solo quelli più grandi. • Degenerazione Maculare Legata all’Età (DMLE): alterazione della macula, la parte centrale e più importante della retina; la macu- 89 lopatia è tipica dell’anziano e riduce la capacità di vedere bene. • Diottria: è l’unità di potere rifrattivo; tanto più un difetto di rifrazione è forte tanto più elevato sarà il numero di diottrie; tante più sono le diottrie tanto più spesso è l’occhiale e tanto più esso è necessario. Tante più sono le diottrie del difetto tanto meno il paziente vede senza la correzione. • Emmetropia: condizione per la quale un occhio è privo di difetti di rifrazione. • Errore o difetto di rifrazione: è una anomalia dell’occhio per cui occorre una lente affinché l’occhio veda correttamente (miopia, astigmatismo, ipermetropia). • Facoemulsificazione: tecnica di facoemusificazione per rimuovere la cataratta: con questa metodica la cataratta viene frammentata dentro l’occhio attraverso una piccola incisione (2,0-2,5 mm circa) e poi aspirata con un sistema di lavaggio ed aspirazione. • Glaucoma: è una malattia caratterizzata dalla progressiva riduzione della vista e del campo visivo causata dall’aumento della pressione interna dell’occhio che avviene per accumulo di umore acqueo. • ICL: Intraocular Contact Lens ossia lente a contatto intraoculare; in realtà è un cristallino artificiale che serve a correggere elevati difetti di miopia ed ipermetropia. • Ipermetropia: difetto di rifrazione per cui l’occhio vede male a distanza ravvicinata e meglio per lontano. • Iniezioni intravitreali: consistono nella iniezione dentro l’occhio di farmaci per curare la DMLE (Degenerazione Maculare Legata all’Età) e altre malattie. • Laser ad eccimeri: moderni strumenti in grado di emettere precisi fasci di luce che consentono la correzione di difetti visivi. • Laser a femtosecondi: è un laser che emette raggi di luce in tempi incredibilmente veloci (miliardesimi di secondo) e dotato di notevole energia. Utilizzato in modo adeguato si comporta come un bisturi di luce. • LASIK: intervento e laser per la correzione della miopia lieve, media ed elevata; viene utilizzata anche per l’astigmatismo e l’ipermetropia. • Lente a contatto: sottile disco di materiale plastico che viene applicato sulla parte anteriore dell’occhio cioè sulla cornea per correggere alcuni difetti di rifrazione (miopia, astigmatismo, ipermetropia, afachia). • Lente intraoculare: è stessa cosa di un cristallino artificiale. • Macula: la parte centrale e più importante della retina; è la parte utilizzata per leggere, scrivere, lavorare al computer, vedere la televisione, 90 guidare. Se la macula si ammala (DMLE Degenerazione Maculare Legata all’Età) la vista ne subisce serie conseguenze. • Miopia: difetto di rifrazione per cui un occhio vede bene per vicino e male per lontano. • Oculista: medico specializzato nella cura delle malattie dell’occhio; fra gli oculisti meno del 10% eseguono chirurgia rifrattiva. • Ottico: è un artigiano diplomato che ha il compito di eseguire l’occhiale prescritto dal medico oculista e di consigliare lenti che correggono semplici difetti visivi. • Optometrista: è un diplomato abilitato a prescrivere lenti per la correzione dei difetti di vista e ad applicare lenti a contatto; l’optometrista non può prescrivere medicine, curare malattie, fare operazioni. • Peeling: intervento chirurgico con vitrectomia che serve per la cura della DMLE (Degenerazione Maculare Legata all’Età) • Presbiopia: anomalia per cui un occhio non riesce ad “accomodare”, non riesce cioè a mettere a fuoco a distanza ravvicinata; richiede occhiali per ogni attività svolta nel raggio di 20-50 centimetri o meno. • PRK: consiste nella disintegrazione mediante laser ad eccimeri di uno strato sottilissimo di cornea anteriore; si utilizza prevalentemente per la correzione delle miope lievi e medie, ma anche per l’ipermetropia e l’astigmatismo lieve • Retina: membrana che avvolge l’occhio all’interno; la sua integrità e funzionalità è fondamentale per una vista ottimale • Trapianto di cornea: intervento chirurgico che consiste nella sostituzione di una porzione di cornea malata con un eguale porzione di cornea sana di donatore proveniente da una Banca della Cornea. Esistono vari tipi di trapianto: perforante, lamellare, anteriore, posteriore, ecc. • Visus o acuità visiva: capacità dell’occhio a vedere; un occhio che vede bene ha 10/10 di visus (cioè il 100 per 100 di vista) un occhio che vede poco ha 1-2/10 cioè il 10-20% della visione totale; la minore o maggiore acuità visiva dipende in generale dalle condizioni di salute dell’occhio. • Visione da vicino: quando una persona guarda qualcosa situata ad una distanza inferiore ai 50 cm circa dal suo occhio si dice che utilizza la visione per vicino; è in pratica la visione che serve per leggere, scrivere, ecc. • Visione da lontano: quando una persona guarda qualcosa situata a 3 metri od oltre si dice che usa la visione per lontano; è in pratica la visione che serve per vedere la televisione, per guidare la macchina ecc. Si usa invece la visione intermedia quando si guarda fra i 50 cm ed i 3 metri. 91 P R I N C I PA L I AT T I V I T À D E L C E N T R O A M B R O S I A N O O F TA L M I C O Chirurgia: • Cataratta • Miopia • Astigmatismo • Ipermetropia • Presbiopia • Glaucoma • Chirurgia del vitreo e della retina • Iniezioni intravitreali • Chirurgia palpebrale • Trapianti di cornea Laser: • Miopia, laser ad eccimeri • Cataratta: laser a femtosecondi • Opacità secondaria: laser yag • Malattie della retina: laser argon • Glaucoma: laser yag e argon • Crosslinking per cheratocono Diagnostica: • Aberrometria computerizzata • Autorefrattometria computerizzata • Biometria • Ecografia • Fluorangiografia • OCT del segmento anteriore e posteriore • Ortottica • Perimetria computerizzata • Pachimetria ultrasonica • Topografia corneale • Tonometria ad aria 92 DAY SURGERY DI MICROCHIRURGIA OCULARE È un centro attrezzato per eseguire la chirurgia dell’occhio senza ricovero ed in piena sicurezza. I pregi in questa modalità chirurgica sono: • assenza di ricovero • ambienti specificatamente studiati per la chirurgia oculare • elevata professionalità • assistenza personalizzata • massima sicurezza Nel Day Surgery di Microchirurgia Oculare sono eseguibili, fra gli altri, interventi chirurgici per: • cataratta • glaucoma • miopia • astigmatismo • ipermetropia • presbiopia • chirurgia della retina • vitrectomia • iniezioni intravitreali • trapianti di cornea • cheratocono • chirurgia palpebrale • ed altri Com’è il Day Surgery della CAMO? Il Day Surgery è un insieme di ambienti progettati appositamente per la chirurgia oculare e dotati dei più moderni e sicuri sistemi di assistenza per il paziente: 93 • ha tre modernissime sale chirurgiche realizzate ed attrezzate appositamente per la chirurgia dell’occhio • ha una sala laser dotata dei più recenti ritrovati della tecnologia laser • ha attrezzature per anestesia locale e generale; • dispone di personale altamente specializzato fra cui un medico anestesista. E’ costruito secondo i più avanzati sistemi di sicurezza per il paziente; dispone fra l’altro di: • impianto elettrico ad alta sicurezza dotato di alimentazione autonoma di emergenza • aria condizionata sterile • gas di emergenza • impianto autonomo di sterilizzazione • pavimenti e tappezzerie antistatici e antipolvere. E’ dotato dei più moderni e sofisticati strumenti per chirurgia oculare; dispone fra l’altro di: • due laser a femtosecondi • un laser ad eccimeri • due microscopi operatori • quattro facoemulsificatori • un vitrectomo • due microcheratomi • tanti altri strumenti necessari per la microchirurgia oculare L’ambulatorio è stato ispezionato ed approvato dai competenti Organi Sanitari di Controllo. 94 Biografia di Lucio Buratto Nella chirurgia oculare il Dr. Buratto si occupa della correzione laser e chirurgica di miopia, astigmatismo e ipermetropia così come del trattamento chirurgico della cataratta. In ambedue i settori ha ricevuto numerosi riconoscimenti a livello internazionale. Il Dr. Buratto ha iniziato la sua professione di chirurgo “rifrattivo” nel 1989 quando, primo a livello mondiale, ha iniziato a utilizzare il laser ad eccimeri all’interno della cornea per la correzione della miopia. Fino ad oggi ha eseguito parecchie migliaia di interventi di miopia, astigmatismo ed ipermetropia ed ha acquisito una esperienza ed una competenza unica in Italia. Per le sue ricerche e per i suoi risultati nel campo della miopia ha conseguito numerosi premi e riconoscimenti internazionali: – Al congresso internazionale di San Diego (California) il primo premio per la miglior nuova tecnica chirurgica con laser ad eccimeri. – Al congresso di Barcellona il premio per le sue ricerche ed innovazioni apportate nel campo della chirurgia della miopia. – Al congresso internazionale dell’American Academy of Opthalmology di New Orleans è stato nominato “Chirurgo Rifrattivo dell’Anno” – È stato insignito dalla Società Oftalmologia Italiana del riconoscimento di “Maestro dell’Oftalmologia Italiana”. – Al congresso Europeo di Nizza della Società Europea di Chirurgia della Cataratta e Rifrattiva ha ricevuto il riconoscimento “Pioniere in Chirurgia Rifrattiva”. – Al congresso della Società Inglese UKISCRS per i suoi studi nella Lasik è stato insignito della medaglia d’oro “Peter Choyce”. – Al congresso Internazionale di Dallas dell’American Academy of Ophthalmology ha ricevuto il massimo riconoscimento internazionale per un chirurgo rifrattivo, il premio “Barraquer” per le 95 sue ricerche ed innovazioni sulla chirurgia refrativa con laser. – Al XXII congresso Europeo dell’ESCRS (European Society of Cataract and Refractive Surgery) a Parigi, per i suoi studi sulla chirurgia della cataratta e chirurgia rifrattiva, ha ricevuto la “Binkhorst Medal”. – Al congresso Annuale dell’HSIOIRS ad Atene per i suoi studi sulla chirurgia rifrattiva ha ricevuto il premio “Fyodorov”. Ogni anno organizza a Milano il più importante congresso italiano della chirurgia refrattiva e della cataratta con la partecipazione dei più famosi chirurghi internazionali. È stato fondatore e Presidente della Associazione Italiana di Chirurgia della Cataratta e Rifrattiva. Ha diretto 55 corsi di aggiornamento sulla chirurgia della cataratta e della miopia ed ha tenuto 70 corsi per l’insegnamento della chirurgia oculare. A tutt’oggi ha pubblicato 11 trattati dedicati alla correzione laser o chirurgica della miopia. Il trattato di chirurgia “LASIK Principles and Techniques” è stato il best seller internazionale; il trattato “Lasik Surgical Techniques and Complications” è stato tradotto in tre lingue diverse. Nel 2013 ha pubblicato una serie di 5 trattati sulla moderna chirurgia della cataratta; i 5 trattati sono stati anche pubblicati in lingua inglese dalla principale casa editrice mondiale in oftalmologia. 1) Introduzione alla chirurgia della cataratta 2) Tecniche di faco e femtofacoemulsificazione in chirurgia della cataratta 3) IOL in chirurgia della cataratta 4) Casi complicati in chirurgia della cataratta 5) Complicanze in chirurgia della cataratta 96 Biografia di Claudio Macaluso Il Dr. Macaluso si occupa di chirurgia del segmento anteriore dell’occhio da subito dopo il conseguimento della specializzazione in oculistica, nel 1991. Da allora ha eseguito alcune migliaia di interventi chirurgici sul cristallino e sulla cornea. Nell’ambito degli interventi sulla cornea ha effettuato tutti i tipi di trapianto o cheratoplastica, sia perforante che lamellare anteriore e posteriore. In particolare, è stato il primo in Italia e fra i primi in Europa ad eseguire il trapianto lamellare posteriore o endoteliale, per il quale ha sviluppato tecniche e strumenti che sono utilizzati da chirurghi in tutto il mondo. Per la sua esperienza in questa chirurgia è stato invitato ad intervenire con relazioni sul tema in congressi internazionali: • Al congresso mondiale sulla cornea a Washington, USA, aprile 2005: Automated Lamellar Keratoplasty in Keratoconus, within the 3rd “Lamellar Keratoplasty for Keratoconus”, Moria user meeting. • Al congresso annuale dell’American Academy of Ophthalmology, Las Vegas, USA, novembre 2006: Tips and Techniques for DSAEK. Moria Speaker Forum. • Al congresso europeo delle banche delle cornee a Bratislava, Slovacchia, gennaio 2007: Descemet Stripping Automated Endothelial Keratoplasty. • Presso l’AMC (Academic Medical Center) dell’Università di Amsterdam, Olanda, novembre 2007: Endothelial Keratoplasty. • Alla European Cornea Conference, Padova, giugno 2008: Observations on Endothelial Keratoplasty. A 3-year Experience. • Al congresso europeo della ESCRS (European Society of Cataract and Refractive Surgeons) a Roma, febbraio 2009: DSAEK Surgery for Fuchs Dystrophy. Cornea Day, • Al congresso internazionale sul Cheratocono a Baiona, Spagna, novembre 2010: DSAEK in failed penetrating keratoplasty. • Al simposio internazionale sulla cheratoplastica endoteliale della SITRAC, Bologna, febbraio 2011: Indications for endothelial keratoplasty: is still there a place for PK? 97 • Al congresso europeo della ESCRS (European Society of Cataract and Refractive Surgeons) a Milano, settembre 2012: How to avoid the mistakes we made in starting Descemet stripping automated endothelial keratoplasty (DSAEK). Instruction Course. • Alla European Cornea Conference, Camogli, giugno 2013: DSAEK surgery 2005-2013. Attempting to standardize DSAEK procedure in average and complex cases. E’ professore associato di Oftalmologia presso l’Università di Parma, dove insegna al corso di laurea in Medicina e Chirurgia, alla scuola di specializzazione in Oftalmologia, e al corso di laurea in Biotecnologie. E’ associato al CNR (Consiglio Nazionale delle Ricerche) per lo sviluppo di nuovi materiali per impianti oculari. Collabora inoltre con laboratori di ricerca per lo sviluppo di terapie avanzate con cellule staminali, e con ditte indipendenti per lo sviluppo di tecniche diagnostiche e chirurgiche innovative. 98 Note 99 Note 100 Note a cura di Mi opero di Lucio Buratto CATARATTA a cura di Mi opero di MIOPIA FORTE CAMO CAMO MI OPERO DI CENTRO AMBROSIANO OFTALMICO a cura di Mi opero di CENTRO AMBROSIANO OFTALMICO a cura di Claudio Macaluso Lucio Buratto Lucio Buratto Miopia astigMatisMo iperMetropia Mi opero di CORNEA CAMO CAMO CENTRO AMBROSIANO OFTALMICO CENTRO AMBROSIANO OFTALMICO a cura di Lucio Buratto Luigi Caretti Mi opero di GlAuCOmA a cura di Matteo Cereda Lucio Buratto Mi opero di RETINA CAMO CAMO CENTRO AMBROSIANO OFTALMICO a cura di Mi opero di Lucio Buratto PREsbIOPIA Lucio Buratto CENTRO AMBROSIANO OFTALMICO a cura di Lucio Buratto OCCHIO E NUTRIZIONE Speciale CAMO CENTRO AMBROSIANO OFTALMICO CAMO CENTRO AMBROSIANO OFTALMICO 102 Indirizzo dello Studio Oculistico presso cui visita il Dr. Lucio Buratto: Centro Ambrosiano Oftalmico Piazza della Repubblica, 21 20124 Milano Contatti: Telefono: 02.6361191 Fax: 02.6598875 Sito internet: www.camospa.it Email: [email protected] La struttura è specializzata nella chirurgia dell’occhio; in particolare nel trattamento delle seguenti patologie: • Cataratta • Miopia • Ipermetropia • Astigmatismo • Presbiopia • Glaucoma • Cheratocono • Retina • Cornea CAMO CENTRO AMBROSIANO OFTALMICO
Scaricare