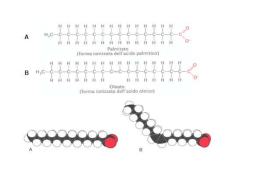
Alogenuri Alchilici Derivati degli idrocarburi in cui uno o più atomi di H sono stati sostituiti da alogeni. R-X (R sta per un qualunque residuo alchilico e X per un alogeno) Nella nomenclatura seguono le regole precedenti in cui l'alogeno (numerato) è il sostituente I H3C CH CH3 CH3 2-iodopropano CH2 I C CH2 CH3 CH3 3-metil-3-iodopentano Nella nomenclatura comune gli alogenuri semplici vengono considerati come derivati alchilici degli acidi alogenidrici: cloruro di metilene, fluoruro di etile, ioduro di isopropile, brouro di ter-butile, cloruro di cicloesile (provate a rappresentarne la formula di struttura). Molti alogenuri sono liquidi con peso specifico >1, hanno punti di ebollizione più elevati dei rispettivi composti in cui l'alogeno è sostituito con H. Sono insolubili in H2O e più densi di questa, sono al contrario solubili negli idrocarburi. Sono ottimi solventi CHCl3 (cloroformio), CH2Cl2 (cloruro di metilene), CCl4 (tetracloruro di carbonio). Cl Cl C Cl H Cl C H H Cl Cl C Cl Cl Cl Analiziamo la nomenclatura dei seguenti composti: Br CH CH3 CH Cl CH H3C CH2 CH3 CH H3C CH2 CH3 2-Bromo-3-cloro-4-metileptano CH3 CH3 I C CH2 3-Iodio-2,3-dimetilesano CH3 Br 3-bromo-2-metilcicloesene CH2 CH3 CH2 CF3 Cl 1-clorometil-2-metil cicloesano trifluorometil benzene (Trifluorotoluene) Composti ossigenati con legami semplici Composti ottenuti per sostituzione di uno o due H dell'H2O con gruppi alchilici (R) o arilici (Ar). Se viene sostituito un H abbiamo gli alcoli R-OH Se si sostituiscono entrambi gli H abbiamo gli eteri R-O-R Se si sostituiscono entrambi gli H con R ed O-R abbiamo perossidi R-O-O-R Se si sostituiscono entrambi gli H con R ed R-OH abbiamo idroperossidi R-O-OH Alcooli R-OH Gli alcoli sono liquidi con p.e. molto alti che aumentano con il peso molecolare e con la ramificazione per la formazione di legami idrogeno intermolecolari. Hanno inoltre alta costante dielettrica che diminuisce con l'aumento del numero di C e sono miscibili in H2O Si comportano da acidi deboli formano sali con metalli alcalini K, Na e Li denominati alcossidi Si trovano ad uno stato di ossidazione più alto rispetto agli alcani corrispondenti e paragonabile agli analoghi alcheni. Vengono denominati sostituendo la -o dell'alcano corrispondente con -olo. La posizione dell'OH viene definita da un numero riferito al carbonio a cui è legato. HO-CH3 HO-CH2CH3 HO-CH2CH2CH3 HO-(CH2)3CH3 H3C H3C alcool metilico, alcool etilico, alcool n-propilico, alcool n-butilico, CH3 HC OH alcool iso-propilico iso-propanolo HO CH2 CH CH3 alcool iso-butilico iso-butanolo metanolo etanolo propanolo butanolo HO H3C C CH3 CH3 alcool ter-butilico ter-butanolo Gli alcooli presentano p.e. molto alti che aumentano con il peso molecolare. Formazione di legami idrogeno intermolecolari!!!
Scarica