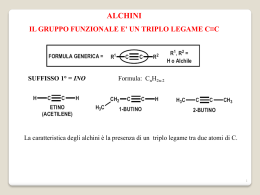
Esercitazione n. 13 - Reazioni sulle reazioni di alcheni, alchini e dieni. 1. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene + HBr b) 2-butene + acqua, in ambiente acido HBr Br CH3 CH CH2 CH3 2-bromobutano CH3 CH CH CH3 OH CH3 CH CH2 CH3 2-butanolo H2O, H+ 2. Scrivere le reazioni del 2-metil-1-pentene con ciascuno dei seguenti reagenti, specificando i nomi dei prodotti che si formano: a) BH3 e poi H2O2, OH-; b) HCl; c) HBr; d) HBr, in presenza di perossidi; e) HI; f) Cl2; g) ICl; h) Br2 + CH3CH2OH. CH3 CH3 CH2 CH2 C BH3 CH2 CH3 (CH CH2 CH2 CH CH2 ) B 3 3 CH3 CH3 CH2 CH2 CH CH2 OH CH3 CH C CH CH2 + HCl CH3 2 2 CH3 CH3CH2 CH2 C CH2 + HBr H2O2, OH- 2-metil-1-pentanolo CH3 CH3CH2 CH2 C CH3 Cl 2-cloro-2-metilpentano CH3 CH3CH2 CH2 C CH3 Br 2-bromo-2-metilpentano CH3 RO-OR CH3CH2 CH2 CH CH2 Br CH3CH2 CH2 C CH2 + HBr CH3 1-bromo-2-metilpentano CH3 CH3CH2 CH2 C CH2 + HI CH3 CH3CH2 CH2 C CH2 + Cl2 CH3 CH3CH2 CH2 C CH3 I 2-iodo-2-metilpentano CH3 CH3CH2 CH2 C CH2Cl Cl 1,2-dicloro-2-metil-pentano 1 CH3 CH3CH2 CH2 C CH2 I Cl CH3 CH3CH2 CH2 C CH2 + I-Cl 2-cloro-1-iodo-2-metilpentano CH3 CH3 CH2OH CH3 CH3CH2 CH2 C CH2 CH3CH2 CH2 C CH2 + Br2 Br + può essereattaccato da qualsiasi Nu presente CH3 CH3 CH3 CH3CH2 CH2 C CH2 Br + CH3 CH2 CH2 C CH2 O CH2 CH3 + CH3CH2 CH2 C CH2 Br Br Br O CH2 CH3 1,2-dibromo-2metilpentano 2-bromo-1-etossi2-metilpentano 1-bromo-2-etossi2-metilpentano 3. Scrivere le equazioni chimiche ed il meccanismo delle seguenti reazioni: a) 1-butene + HI a) I equazione meccanismo CH3 CH2 CH CH3 CH2 CH CH2 CH2 + H+ + CH3 CH2 CH CH3 + HI CH3 CH2 CH CH3 + CH3 CH2 CH CH3 I CH3 CH2 CH CH3 lento + I- b) 1-metilcicloesene + HCl CH3 b) equazione + HCl CH3 meccanismo CH3 Cl CH3 + H+ lento + H H Cl- Cl CH3 2 c) 3-metil-2-pentene + H2SO4 acquoso c) equazione meccanismo :OH2 H2O + CH3 CH2 C CH CH3 + H + OH CH3 2 CH3 CH2 C CH2 CH3 CH3 OH CH3 CH2 C CH2 CH3 H2SO4 CH3 CH2 C CH CH3 CH3 CH3 lento + CH3 CH2 C CH2 CH3 CH3 OH CH3 CH2 C CH2 CH3 CH3 + H+ d) metilpropene con H2SO4 in etanolo d) equazione meccanismo CH3 C CH2 CH3 H2SO4 OCH2CH3 CH3 CH2C CH2CH3 CH3 CH3CH2OH .. CH3CH2OH + lento + CH3 C CH2 + H CH3 C CH3 CH3 CH3 + H OCH2CH3 OCH2CH3 + CH3CH2C CH2CH3 CH3CH2C CH2CH3 + H CH3 CH3 e) 2,2-dimetil-3-esene con acqua in ambiente acido OH CH3 CH3 H+ CH3 C CHCH2CH2CH3 CH3 C CH CH CH2CH3 + H2O CH3 CH3 CH3 + CH3 lento + + H CH3 C CH CH2CH2CH3 CH3 C CH CH CH2CH3 meccanismo CH3 CH3 + OH 2 :OH2 OH CH CH3 CH3 3 + CH3 C CHCH2CH2CH3 CH3 C CH CH2CH2CH3 CH3 C CHCH2CH2CH3 + H+ CH3 CH3 CH3 e) equazione f) 1-butene + HI CI f) equazione meccanismo CH3 CH2 CH CH2 + ICl CH3CH2 CH CH2 + ICl + CH3CH2CH CH2 I + CI- CH3 CH2 CH CH2 I lento + CH3CH2CH CH2 I CI CH3CH2CH CH2 I 3 4. Scrivere la reazione con H2O,H+ dei seguenti alcheni, specificando i nomi dei composti organici che si formano: a) 1-butene; b) metilpropene; c) 2-metil-2-butene; d) 3-metil-1-butene. a) H2O,H+ CH3 CH2 CH CH2 OH CH3 CH2 CH CH3 2-butanolo CH3 b) CH3 C CH3 H2O,H+ CH2 CH3 C CH3 OH 2-metil-2-propanolo c) H2O,H+ CH3 CH3 CH C CH3 CH3 CH3 CH2 C CH3 OH 2-metil-2-butanolo d) CH3 CH3 H O,H+ CH3 CH CH CH3 CH3 CH CH CH2 2 3-metil-2-butanolo OH 5. Scrivere le reazioni del 3-etil-2-pentene con ciascuno dei seguenti reagenti, specificando i nomi dei prodotti organici: a) borano e poi H2O2, OH-; b) HOBr in ambiente acido; c) HBr; d) HBr in presenza di perossidi; e) ICl. CH2 CH3 1. BH3 CH CH3 CH3 CH2 C 2. H2O2,OH- ICl HOBr,H+ CH2 CH3 CH3 CH2 CH CH CH3 OH HBr ROOR HBr CH2 CH3 CH3 CH2 C CH2 CH3 CH3 CH2 C Cl CH2 CH3 CH CH3 I Br 3-etil-2-pentanolo 3-bromo-3-etilpentano CH2 CH3 CH3 CH2 C CH CH3 OH Br CH2 CH3 CH3 CH2 CH CH CH3 Br 2-bromo-3-etilpentano 2-bromo-3-etil-3-pentano 4 6. Completare le seguenti reazioni: BH3 e poi H2O2, OHa) propene + borano e poi H2O2, OH- E+ = B; OH sostituisce B CH3 CH2 CH2 OH ( CH3 CH2 CH2 )3 B CH3 CH CH2 1-propanolo tripropilboro b) 2-metil-2-pentene + borano e poi H2O2, OHCH3 CH3 CH2 CH C CH3 R CH3 CH2 CH B R CH CH3 CH3 OH CH3 CH3 CH2 CH CH CH3 2-metil-3-pentanolo tri(1-isopropil)propilboro c) 1-metilcicloesene + borano e poi H2O2, OH- CH3 CH3 OH 2-metilcicloesanolo 7. Scrivere i prodotti di reazione (specificandone il nome) del bromo con i seguenti alcheni: Br2 addizione elettrofila al doppio legame a) 2-butene Br Br CH3 CH CH CH3 CH3 CH CH CH3 2,3-dibromobutano b) metilpropene CH3 CH3 C CH2 CH3 CH3 C CH2 Br Br 1,2-dibromo-2-metilpropano c) 2-metil-2-butene CH3 c) CH CH C CH 3 3 CH3 CH3 CH C CH3 Br Br 2,3-dibromo-2-metilbutano 5 8. Completare le seguenti reazioni, specificando il nome di tutti i composti organici che si ottengono: a) cicloesene + Br2 Br + Br2 trans-1,2-dibromocicloesano Br b) cicloesene + Br2, in presenza di perossidi (ATTENZIONE!!! Br2 NON dà addizioni radicaliche .....) RO-OR 3-bromocicloesene + Br2 Br c) 2-metil-2-butene + cloro CH3 CH3 CH3 CH C CH3 + Cl2 CH3 CH C CH3 Cl Cl d) 1-butene + bromo CH3 CH2 CH 2,3-dicloro-2-metilbutano Br CH2 + Br2 CH3 CH2 CH CH2 Br 1,2-dibromobutano 9. a) Scrivere il meccanismo della reazione tra 2-metil-2-butene con acetato mercurico in etanolo. b) Scrivere la reazione tra il prodotto ottenuto in (a) e l'idruro di boro e sodio. CH3CO2- + +Hg(OCOCH3) Hg(OCOCH3)2 CH3 CH C CH3 + +Hg(OCOCH3) CH3 OCOCH3 OCOCH3 CH2CH3 δ+ Hg Hg +O H CH3 CH3CH2OH C CH3 C δ+ CH3 CH CH3 CH CH3 CH3 OCOCH3 Hg O CH CH 2 3 CH3 CH C CH3 H+ CH3 NaBH4 CH3 CH2 CH2CH3 O C CH3 CH3 6 10. Completare le seguenti reazioni a) 1-metilcicloesene + acetato mercurico acquoso e poi NaBH4 CH3 H3C OH H3C NaBH4 H H2O + Hg(OCOCH3)2 HgOCOCH3 OH H H b) 4-clorocicloeptene + acetato mercurico in metanolo e poi NaBH4 Cl Cl Cl CH3OH + Hg(OCOCH3)2 Cl Cl + O H3C HgOCOCH3 O CH3 HgOCOCH3 + NaBH4 O O CH 3 CH3 c) 2-metil-2-pentene + acetato mercurico in acido acetico e poi NaBH4. CH3 CH2CH C CH3 + Hg(OCOCH3)2 CH3 NaBH4 CH3CO2H C O H3C CH3 CH3 CH2 CH2 C H3C HgOCOCH3 CH3 CH3 CH2 CH C CH3 O C O O CH3 11. Scrivere le reazioni del 2-metil-1-pentene con ciascuno dei seguenti reagenti, specificando i nomi dei prodotti che si formano: a) H2, PtO2 CH3 H2,PtO2 CH3 CH2 CH2 C CH2 b) D2, Pd-C CH3 CH3 D2, Pd-C CH3 CH2 CH2 C CH2 2-metilpentano CH3 CH2 CH2 CH CH3 CH3 CH3 CH2 CH2 C CH2 D D 1,2-dideutero-2-metilpentano c) acido m-cloroperbenzoico Cl CH3 CH3 CO3H CH3 CH2 CH2 C CH2 CH3 CH2 CH2 C CH2 O1 2-metil-2-propilossaciclopropano d) OsO4 e poi Na2SO3 d’) KMnO4, OHCH3 OsO4 e poi Na2SO3 CH3 CH3 CH2 CH2 C CH2 OH CH3 CH2 CH2 C CH2 KMnO4, OH- OH 2-metil-1,2-pentandiolo 7 e) KMnO4, OH-, a caldo CH3 CH3 KMnO4, OH- CH3 CH2 CH2 C CH2 CH3 CH2 CH2 C O + CO2 Δ 2-pentanone 12. a) Scrivere la reazione del metilene con il cicloesene + :CH2 biciclo[4.1.0]eptano b) scrivere le reazione del cicloesene con cloroformio in ambiente basico acquoso CHCl3 + OHCCl3Cl- + :CCl2 Cl + :CCl2 7,7-dimetilbiciclo[4.1.0]eptano Cl 13. Completare le seguenti reazioni: a) trans-1,2-difeniletene + CHCl3, NaOH in acqua Cl Cl CHCl3 H C C NaOH H2O H b) cicloesene + CH2I2, Zn(Cu); CH2I2 + Zn(Cu) :CH2 + :CH2 c) cis-3-esene + CHBr3, in ambiente basico acquoso Br- + :CBr2 CHBr3 + OHCBr3Br CH3 CH2 C H CH2 CH3 C H Br :CBr2 CH3 CH2 CH2 CH3 8 14. Completare le seguenti reazioni, specificando il nome di tutti i composti organici che si ottengono: a) cicloesene + KMnO4, OH-, a freddo KMnO4,OH- OH cis-1,2-cicloesandio OH b) cicloesene + acido perbenzoico CO3H O 7-ossabiciclo[4.1.0]eptano c) cis-2-esene + KMnO4, in ambiente basico, a caldo CH2 CH2 CH3 CH3 C H CH2 CH2 CH3 CH3 C O + O C O O KMnO4,OH- C Δ H H+ O O CH3 C OH + HO C CH2 CH2 CH3 acido etanoico acido butanoico d) 2-metil-2-pentene + O3 e poi Zn, H2O, H+ CH2 CH3 CH3 C C H CH3 CH2 CH3 CH3 C O + O C H CH3 2) Zn,H+ propanale propanone 1) O3 e) 2-metil-2-pentene + O3 e poi H2O CH3 C CH3 CH2 CH3 C H 1) O3 2) H2O2 CH3 C O CH2 CH3 + CH3 propanone O C OH acido propanoico f) 1-pentene + cloro f) H2C Cl CH2 CH CH2 CH2 CH3 CH CH2 CH2 CH3 + Cl2 Cl 1,2-dicloropentano g) 2-esene + ozono, e poi Zn, H2O, H+ g) CH CH 3 CH CH2 CH2 CH3 1) O3 2) Zn,H+ CH3 CH O + O CH CH2 CH2 CH3 etanale butanale 9 15. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: D Pt a) ciclopentene + D2/Pt + D2 cis-1,2-dideuterociclopentano D b) 1,2-dimetilciclopentene + H2/Pt. CH3 CH3 Pt + H2 CH3 CH3 cis-1,2-dimetilciclopentano c) 2-butino + HBr (un equivalente) CH3 C C CH3 H3 C HBr Br Br CH3 CH2 C CH3 Br HBr C C CH3 H trans-2-bromo-2-butene 2,2-dibromobutano d) 2-butino + Br2 (un equivalente); c) 2-butino + Br2 (due equivalenti) CH3 C C CH3 Br2 H3 C Br C C CH3 Br Br2 Br CH3 C Br trans-2,3-dibromo-2-butene Br C CH3 Br 2,2,3,3-tetrabromobutano e) propino + sodioammide CH3 C CH + CH3 C C (Na+) + NH3 NaNH2 propinuro (di sodio) reazione acido-base 16. Scrivere le reazioni dell'1-pentino con i seguenti reagenti, specificando il nome dei prodotti organici: a) un equivalente di cloro; b) due equivalenti di cloro CH3 CH2 CH2 C CH Cl2 CH3 CH2 CH2 C Cl Cl C Cl2 H trans-1,2-dicloro-1-pentene Cl Cl CH3 CH2 CH2 C CH Cl Cl 1,1,2,2-tetracloropentano 10 c) due equivalenti di HCl Cl CH3 CH2 CH2 C CH3 CH + 2 HCl CH3 CH2 CH2 C Cl 2,2-dicloropentano d) = m) NaNH2 e poi ioduro di metile CH3 CH2 CH2 C CH + NaNH2 CH3 CH2 CH2 C CH3 I CH3 CH2 CH2 C C CH3 C- NH3 I- e) H2/Pt; f) H2/Pd avvelenato CH3 CH2 CH2 CH CH2 H2/Pd avv. H2/Pt CH3 CH2 CH2 C CH CH3 CH2 CH2 CH2 CH3 pentano 1-pentene g) Br2 (un equivalente); h) Br2 (due equivalenti) CH3 CH2 CH2 C CH Br2 CH3 CH2 CH2 C Br Br Br Br Br2 C H CH3 CH2 CH2 C CH Br Br 1,1,2,2-tetrabromopentano trans-1,2-dibromo-1-pentene i) HCl (un equivalente); j) HCl (due equivalenti) CH3 CH2 CH2 C CH HCl Cl CH3 CH2 CH2 H Cl HCl CH3 CH2 CH2 C CH3 H Cl 2-cloro-1-pentene 2,2-dicloropentano k) Na in ammoniaca liquida CH3 CH2 CH2 C CH Na in NH3 CH3 CH2 CH2 C C Na+ pentinuro di sodio l) H2O, H + , Hg 2+ CH3 CH2 CH2 C CH H2O, H+, Hg2+ OH CH3 CH2 CH2 C O CH2 CH3 CH2 CH2 C CH3 2-pentanone 11 17. Scrivere le equazioni chimiche, specificando i nomi dei prodotti organici, delle reazioni che avvengono trattando il 2-pentino con i reagenti dell'Esercizio 62. a) un equivalente di cloro; b) due equivalenti di cloro CH3 CH2 C C CH3 Cl Cl Cl Cl2 CH3 CH2 C Cl2 C CH3 Cl CH3 CH2 C C CH3 Cl Cl trans-2,3-dicloro-2-pentene 2,2,3,3-tetracloropentano c) due equivalenti di HCl CH3 CH2 C Cl Cl 2 HCl CH3 CH2 CH2 C CH3 + CH3 CH2 C CH2CH3 Cl Cl 3,3-dicloropentano 2,2-dicloropentano C CH3 e) H2/Pt; f) H2/Pd avvelenato CH3 CH2 CH CH CH3 H2/Pd avv. CH3 CH2 C C CH3 H2/Pt CH3 CH2 CH2 CH2 CH3 pentano trans-2-pentene g) Br2 (un equivalente); h) Br2 (due equivalenti) CH3 CH2 C C CH3 CH3 CH2 C Br2 Br Br Br Br Br2 CH3 CH2 C C CH3 C CH3 Br Br trans-2,3-dibromo-2-pentene 1,1,2,2-tetrabromopentano i) HBr (un equivalente); j) HBr (due equivalenti) CH3 CH2 C HBr C CH3 CH3 CH2 C Br H C CH3 CH3 CH2 C + H trans-3-bromo-2-pentene Br C CH3 trans-2-bromo-2-pentene HBr Br CH3 CH2 C CH2 CH3 Br 3,3-dibromopentano Br + CH3 CH2 CH2 C CH3 Br 2,2-dibromopentano 12 l) Na in ammoniaca liquida CH3 CH2 C Na in NH3 C CH3 CH3 CH2 C H H C CH3 trans-2-pentene m) H2O, H + , Hg 2+ CH3 CH2 C O OH H2O, H+, Hg2+ CH3 CH2 C C CH3 CH3 CH2 C CH2 CH3 CH CH3 3-pentanone d) = m) NaNH2 e poi ioduro di metile NESSUNA REAZIONE manca H acido! 18. Scrivere il prodotto (o i prodotti) della reazione (se c'è reazione) tra l'1butino ed i seguenti reagenti: a) KMnO4, OHCH3 CH2 C KMnO4, OH- CH b) H2/Pt O CH3 CH2 C O + CO2 CH CH3 CH2 C H2/Pt c) Br2 in eccesso CH3 CH2 C d) NaCl - CH H+ O CH3 CH2 C OH CH3 CH2 CH2 CH3 Non c’à Br Br Br2 CH3 CH2 C CH (eccesso) Br Br NaCl CH3 CH2 C CH NESSUNA REAZIONE e) H2O, H+, Hg2+ CH3 CH2 C CH H2O, H+, Hg2+ OH CH3 CH2 C CH2 f) H2/Pd avvelenato CH3 CH2 C CH H2/Pd avv. CH3 CH2 CH O CH3 CH2 C CH3 CH2 13 19. Scrivere i prodotti (specificandone il nome) che si formano per reazione dell'1-pentino con: a) un equivalente di HBr; b) due equivalenti di HBr HBr CH3 CH2 CH2 C CH Br CH3 CH2 CH2 C CH3 Br 2,2-dibromopentano Br HBr CH3 CH2 CH2 C CH2 2-bromo-1-pentene rivedere c) un equivalente di HBr, in presenza di perossidi Br HBr CH3 CH2 CH2 C CH3 CH2 CH2 CH CH HBr CH RO-OR RO-OR Br CH3 CH2 CH2 CH2 CH Br 1,1-dibromopentano 1-bromo-1-pentene d) bromo, in presenza di perossidi CH3 CH2 CH2 C CH SOSTITUZIONE RADICALICA!! . Br2 CH3 CH2 CH C RO-OR Br e) H2/Pd avvelenato CH CH3 CH2 CH C CH stabilizzato per risonanza H2/Pd avv. CH3 CH2 CH2 C CH3 CH2 CH2 CH CH CH2 1-pentene f) Na in NH3 liquida CH3 CH2 CH2 C CH Na in NH3 CH3 CH2 CH2 C C Na+ 1-pentinuro di sodio g) H2/Pt CH3 CH2 CH2 C CH H2/Pt CH3 CH2 CH2 CH2 CH3 pentano h) KMnO4, OHCH3 CH2 CH2 C CH KMnO4, OH- O CH3 CH2 CH2 C O+ O H+ CO2 CH3 CH2 CH2 C OH acido butanoico i) Ag(NH3)2OH; j) Cu(NH3)2OH. Ag(NH3)2OH CH3 CH2 CH2 C C Ag 1-pentinuro di argento CH3 CH2 CH2 C CH Cu(NH3)2OH CH3 CH2 CH2 C C Cu 1-pentinuro di rame 14 20. Scrivere i prodotti (specificandone il nome) che si formano per reazione del 2-esino con: a) borano, e poi H2O2, OHCH3 CH2 CH2 C BH2 BH2 BH3 CH3 CH2 CH2 CH C CH3 + CH3 CH2 CH2 C C CH3 CH CH3 H2O2, OH- OH OH ENOLO!! C CH3 + CH3 CH2 CH2 CH CH3 CH2 CH2 C CH CH3 O O + CH3 CH2 CH2 CH2 C CH3 CH3 CH2 CH2 C CH2 CH3 3-esanone 2-esanone b) H2/Pd disattivato; c) Na in ammoniaca liquida CH3 CH2 CH2 C C CH3 Na in NH3 liq. H2/Pd disatt. CH3 CH2 CH2 CH3 CH2 CH2 CH3 C C C CH3 H H cis-2-esene H H C trans-2-esene 21. Completare le seguenti reazioni, specificando il nome dei composti organici che si formano: a) ciclopentadiene + HBr (un equivalente) Br = + HBr H add. 1,2 H 3-bromociclopentene Br add. 1,4 b) 2,4-esadiene + Br2 (due equivalenti) CH3 CH CH CH CH CH3 Br2 Br Br Br Br CH3 CH CH CH CH CH3 + CH3 CH CH CH CH CH3 add. 1,4 add. 1,2 Br2 Br 2,3,4,5-tetrabromoesano Br Br Br CH3 CH CH CH CH CH3 c) ciclopentadiene + anidride maleica (=anidride dell'acido cis-butendioico) O + O O O O addotto di Diels-Alder O 15 22. Scrivere le equazioni chimiche e dare il nome al prodotto (o ai prodotti) delle reazioni dell'1,3-pentadiene con: a) H2 (in eccesso)/Pt H2 (ecc.)/Pt CH3 CH2 CH2 CH2 CH3 pentano CH2 CH CH CH CH3 b) Br2 (un equivalente); c) Br2 (due equivalenti) CH2 CH CH CH CH3 Br2 CH2 CH CH CH CH3 + CH2 CH CH CH CH3 + CH2 CH CH CH CH3 Br Br Br Br Br Br 3,4-dibromo-1-pentene 1,4-dibromo-2-pentene 4,5-dibromo-2-pentene Br2 Br2 Br2 CH2 CH CH CH CH3 Br Br Br 1,2,3,4-tetrabromopentano Br d) HCl (un equivalente); e) HCl (due equivalenti) CH2 CH CH CH CH3 HCl H + CH2 CH CH CH CH3 H + CH2 CH CH CH CH3 + H + CH2 CH CH CH CH3 H + CH2 CH CH CH CH3 Cl CH3 CH CH CH CH3 Cl H Cl + CH2 CH CH CH2 CH3 + CH2 CH CH CH CH3 3-cloro-1-pentene 4-cloro-2-pentene 1-cloro-2-pentene HCl HCl HCl Cl + CH3 CH CH CH CH3 + Cl + CH2 CH CH CH2 CH3 + Cl CH2 CH CH CH2 CH3 + H H Cl + CH3 CH CH CH CH3 H Cl + CH2 CH CH CH2 CH3 H H Cl Cl Cl Cl CH3 CH CH2 CH CH3 + CH3 CH CH CH2 CH3 2,4-dicloropentano 2,3-dicloropentano Cl Cl CH2 CH2 CH CH2 CH3 1,3-dicloropentano + Cl Cl CH2 CH CH2 CH2 CH3 1,2-dicloropentano 16 f) H2O, H+ CH2 CH CH CH CH3 H+ H 2O OH OH OH CH2 CH CH CH2 CH3 + CH3 CH CH CH CH3 + CH2 CH CH CH2 CH3 2-penten-1-olo 3-penten-2-olo 1-penten-3-olo H2O H+ OH OH OH OH OH OH OH OH CH3 CH CH2 CH CH3+ CH3 CH2 CH CH CH3 + CH2 CH CH2 CH2 CH3+CH2 CH2 CH CH2 CH3 1,3-pentandiolo 1,2-pentandiolo 2,3-pentandiolo 2,4-pentandiolo 23. Spiegare l'orientamento che si osserva nell'addizione di HCl al 2-metil-2-butene e disegnare il profilo dell'energia della reazione. CH3 - CH3 CH C CH CH CH C CH2 CH3 3 3 CH3 C CH CH3 3 + Cl H si forma il carbocatione terziario, più stabile dell'altro possibile (secondario) + NON si forma CH3 CH CH CH3 CH3 CH3 (2) ΔG# CH3 (1) (4) E Cl + HCl CH3 C CH CH3 + HCl CH3 (3) (2) CH3 C CH CH3 δ+ H δ+ (5) ΔGo (1) CH3 (3) coordinata di reazione CH3 C CH2 CH3 + CH3 (4) δ+ CH3 C CH2 CH3 δ- Cl CH3 (5) CH3 C CH2 CH3 Cl 17 24. Scrivere la struttura ed il nome del composto che si ottiene per addizione di ICl al propene. Quale è il meccanismo? CH3 CH CH2 + ICl CH3 CH CH2 + I+ CH3 CH CH2 I Cl 2-cloro-1-iodopropano Cl+ CH3 CH CH2 I CH3 CH CH2 I Cl lento 25. Mettere i seguenti alcheni in ordine di reattività crescente nei confronti della idratazione acido-catalizzata (= addizione di acqua): propene, etene, vinilbenzene. Spiegare. alchene + H2O, H+ stadio lento: FORMAZIONE DEL CARBOCATIONE reattività maggiore quando si forma un carbocatione più stabile perché è più bassa l'energia dello stato di transizione e quindi è più bassa l'energia di attivazione REATTIVITA' CH CH2 CH2 CH2 < CH3 CH CH2 + CH2 CH3 < + CH3 CH CH3 < < (dell'alchene) STABILITA' (del carbocatione) primario CH CH3 + benzilico secondario 26. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene trattando il propene con HBr; b) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene trattando il propene con HBr, in presenza di perossidi. a) equazione meccanismo CH3 CH CH3 CH Br CH3 CH CH3 + lento Br CH3 CH CH3 CH2 + H+ CH2 + HBr Br CH3 CH CH3 b) equazione meccanismo RO-OR CH3 CH CH2 + HBr INIZIO RO-OR CH3 CH2 CH2 Br Δ . RO + HBr PROPAGAZIONE CH CH 3 . CH2 + Br . lento CH3 CH CH2 Br + HBr ARRESTO . 2 RO ROH + Br . . CH3 CH CH2 Br CH3 CH2 CH2 Br + Br . qualunque urto tra radicali 18 30. Scrivere equazione chimica e meccanismo della reazione che si ha tra metilpropene e HBr a) in assenza di perossidi; b) in presenza di perossidi. equazione CH3 CH3 C CH2 + HBr CH3 CH3 C CH3 Br meccanismo equazione meccanismo CH3 CH3 lento CH3 C CH3 CH3 C CH2 + H+ Br- + CH3 CH3 C CH3 Br CH3 CH3 RO-OR CH3 CH CH2 Br CH3 C CH2 + HBr CH3 CH3 HBr . lento CH3 C CH3 C CH2 + Br . CH2 Br CH3 CH3 CH CH2 Br 32. Scrivere i prodotti per ciascuna delle seguenti reazioni con HCl, tenendo conto del fatto che i carbocationi possono trasporre: a) 3,3-dimetil-1-butene; b) 4,4-dimetil-1-pentene. a) CH3 CH3 C CH CH2 + H+ CH3 CH3 + CH3 C CH CH3 CH3 ClCH3 Cl CH3 C CH CH3 CH3 b) CH3 CH3 C CH2CH CH2 + H+ CH3 CH3 Cl+ CH3 C CH2CH CH3 CH3 CH3 + CH CH3 C CH3 CH3 Cl- Cl CH3 CH3 C CH CH3 CH3 CH3 Cl CH3 C CH2CH CH3 CH3 19 33. Scrivere tutti i passaggi dell'idratazione acido-catalizzata del propene. Spiegare perché il prodotto della reazione è il 2-propanolo e non l'1-propanolo. Come si potrebbe ottenere l'1-propanolo dal propene? + OH2 :OH2 + CH3 CH CH3 CH3 CH CH3 lento CH3 CH CH2 + H+ OH CH3 CH CH3 H+ carbocatione più stabile CH3 CH CH2 1) BH3 CH3 CH2 CH2 OH 2) H2O2, OH- 34. Scrivere il meccanismo della reazione di idroborazione del 2-metil-2-butene, spiegando l'orientamento che si osserva. CH3 CH3 CH C CH3 CH3 δ+ C CH3 CH3 CH + BH3 H2B δ- stato di transizione più stabile, perché la parziale carica + è sul C più sostituito # BH2 CH3 CH3 CH CH CH3 H ( ripetuto due volte con altre due molecole di alchene CH3 CH3 CH CH3 CH B 3 ) 36. a) Scrivere l'equazione chimica ed il meccanismo dell'addizione di bromo all'1-metilcicloesene, commentandone l'andamento stereochimico. b) Che altro si forma, se la reazione con bromo è fatta in presenza di acqua? CH3 CH3 Br 2 equazione Br + enantiomero Br δ- Br δ+ Br CH3 + Br CH3 CH3 + Br2 in presenza di acqua + Br Br- H Br Br CH3 Br CH3+ H Br TUTTI i nucleofili presenti possono attaccare lo ione bromonio Br- CH3 H Br Br CH3 Br CH3 + H Br H + OH 2 Br Br CH3 CH3 + H +OH 2 Br Br CH3 OH CH + 3 H OH H 20 37. Scrivere l'equazione chimica ed il meccanismo della reazione dell'etene con: a) Br2; b) Br2, in presenza di NaCl. In quest'ultimo caso, vi aspettate si possa formare dell'1,2-dicloroetano? Perché? equazione CH2 CH2 + Br2 Br CH2 CH2 Br meccanismo CH2 CH2 + Br2 BrδBr δ+ CH2 CH2 + Br Br- CH2 CH2 Br CH2 CH2 Br ClBr CH2 CH2 Cl c) NO: non c’è Cl+ 38. Scrivere l'equazione chimica ed il meccanismo della reazione del ciclopentene con cloro in acqua, mostrandone l'andamento stereochimico. equazione Cl + Cl 2 trans + cis Cl meccanismo + Cl2 Cl δCl δ+ δ+ Cl δ+ Cl Cl H Cl H Cl H H2O Cl H OH ++ H + H Cl Cl H Cl H H + OH2 H + + H H + H H+ Cl OH Cl + H + Cl OH2 +OH2 Cl OH2 H + H OH H Cl Cl H H H OH Cl + H H 21 39. Scrivere il meccanismo della reazione con bromo dei seguenti alcheni, mettendo in evidenza l'andamento stereochimico: a) trans-2-butene (A) CH3 H H + CH3 Br Br H Br H Br CH3 H = = CH3 H CH3 Br (A) H (A) Br CH3 CH3 H CH3 Br Br2 H H (B) CH3 CH3 Br- (A) Br (B) CH3 H H = Br H Br Br H (B) CH3 CH3 CH3 (B) =H meso Br Br H CH3 CH3 b) cis-2-pentene Br H + CH2CH3 Br 2 (A) CH3 Br- CH2CH3 H Br (B) Br Br H = Br H = CH3 CH2CH3 H CH3 CH3 Br Br H (A) CH3 CH2CH3 H (B) = Br CH2 CH3 CH3 H CH2 CH3 (A) Br (B) CH2CH3 Br H H Br = CH2CH3 H (A) H Br CH3 H (B) H Br CH3 treo (Z)-2-fenil-2-butene Br H Br CH3 + Br H 3C Br CH3 CH3 CH3 Br Br H CH3 (A) C6H5 H CH3 Br- C6H5 H3C Br (A) CH3 CH3 C 6H 5 = (A) C6H5 (B) Br2 H = Br CH3 H (A) (B) H C6H5 Br = CH3 Br Br H enantiomeri H H S T E S S O CH3 = Br CH3 H CH3 Br CH3 (E)-2-metil-2-butenoato di metile Br H Br (A) + Br CO2CH3 H H H CH3 Br CO2CH3 H = CO2CH3 CH3 CO2CH3 H Br2 H H CH3 H CH3 Br- H = Br CO2CH3 Br (B) (A) CH3 Br Br (B) H CO2CH3 H Br CH3 = H H Br CO2CH3 Br (B) = H CO2CH3 H CH3 (B) Br Br CH3 22 42(=46). Scrivere le equazioni chimiche delle seguenti reazioni del ciclopentene, indicando il meccanismo e spiegando il corso stereochimico: O O Mn O O + KMnO4 H2O HO OH cis b) con acido performico, e poi H2O,H+ ; c) con acido performico, e poi H2O, OHH δ+ O δ+ H O+ H C O O O O OH H+ H OH OH- H+ OH2 OH HCO2H trans HO d) con ozono, e poi Zn, H2O, H+ O +O O O- O O δ- O -O δ+ O O O + O O Zn O H2O,H+ 43. Completare le seguenti reazioni del 3-metilbiciclo[4.4.0]-3-decene, specificando (quando possibile) i nomi dei composti organici che si formano: CO3H a) con acido perbenzoico CH3 CH3 O b) con acido perbenzoico, e poi H2O, H+ CO3H CH3 CH3 O CH3 OH H2O H+ OH trans-3-metilbiciclo[4.4.0]-3,4-decandiolo c) con KMnO4 acquoso; d) con KMnO4 acquoso, scaldando; e) con OsO4, e O poi Na2SO3 CH3 KMnO4 1. OsO4 OH CH3 OH CH3 KMnO4 Δ 2. Na2SO3 cis-3-metilbiciclo[4.4.0]-3,4-decandiolo OH O Acido [2-(2-ossopropil)cicloesil]etanoico 23 44. Scrivere i prodotti, specificandone il nome, dell'ozonolisi sia riduttiva che ossidativa per ciascuno dei seguenti alcheni: a) 2.3-dimetil-2-butene CH3 H3C C O3 C H3C H3C 2 C O H3C CH3 b) 3-metilciclopentene O H O O O O oss. 2-metilpentandiale H H H CH3 CH3 H H rid. CH3 OH CH3 OH O O acido 2-metilpentandioico O OH OH CH3 c) α-pinene, un componente della trementina, di nome IUPAC 6,6-dimetil biciclo[3.1.1]-2-eptene H3C H3C H3C rid. H3C O 4-formilmetil-2,2,-dimetilciclobutancarbaldeide O H3C O O H3C oss. H3C H3C H3C OH H3C O OH HO O OH O O acido 4-carbossimetil-2,2-dimetilciclobutancarbossilico d) 2-metil-2-butene rid. H3C C H CH3 O3 C O + H C CH3 CH3 H3C oss. HO C CH3 CH3 H3C C O O + O C CH3 24 O e) cicloesene rid. H esandiale H O O oss. OH OH O acido esandioico O H O f) biciclo[4.4.0]-1-decene rid. 4-(2-ossocicloesil)butanale O HO O oss. acido 4-(2-ossocicloesil)butanoico 50. Dire quale dei seguenti composti reagisce con anidride maleica (=cisbutendioica) e quale no, spiegando e scrivendo l'equazione chimica delle reazioni che avvengono: a) 1,4-pentadiene; b) butadiene; c) ciclopentadiene; d) 1,4-cicloesadiene; e) 1,3-cicloesadiene; f) 1,3-esadiene; g) 1,4-esadiene; h) 1,5-esadiene. O reagisce con i DIENI CONIUGATI (reazione di Diels-Alder) dienofilo O O CH2 CH CH2 CH CH2 CH CH CH2 CH2 O + O O CH CH3 CH CH2 CH CH CH CH CH2 CH3 CH2 CH2 CH CH2 CH2 CH CH2 CH2 O O O O + O O O O O 25 O O O + O O O O O + O O O O 51. Prevedere i prodotti delle seguenti reazioni di Diels-Alder: a) O O Δ O + O O O b) NC CN NC CN + Δ + CN CN CN CN O O c) Δ O O O d) O + Δ O 26 60. Anche gli alchini possono essere usati come dienofili nelle reazioni di Diels-Alder. Scrivere le strutture dei prodotti che si ottengono dalla reazione del butadiene con: a) esafluoro-2-butino; b) propinoato di metile; c) butindioato dimetilico. a) + CF3 C CF3 C CF3 CF3 b) CO2CH3 + C CO2CH3 CH 27 30/05/2011 Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici. 1. Dare la definizione ed un esempio per ciascuno dei seguenti termini: a) complesso σ Intermedio nella sostituzione elettrofila aromatica b) solfonazione Sost. Elettrofila aromatica (E+=SO3) che introduce il gruppo acido solfonico (-SO3H) c) nitrazione Sost. Elettrofila aromatica (E+=NO2+) che introduce il gruppo nitro (-NO2) d) gruppo orto,para orientante Sostituente presente sull’anello benzenico che indirizza l’attacco dell’elettrofilo in o+p, stabilizzando gli addotti corrispondenti Sost. Elettrofila aromatica (E+=R+) che introduce un gruppo alchile (-R) e) alchilazione di Friedel-Crafts f) gruppo meta orientante Sostituente presente sull’anello benzenico che indirizza l’attacco dell’elettrofilo in meta, destabilizzando gli addotti o+p 2. Scrivere quale è e come si forma l'elettrofilo nelle seguenti reazioni aromatiche: a) nitrazione; b) clorurazione; c) solfonazione; d) acilazione con cloruro di acetile; e) alchilazione con cloruro di isobutile. v. lezione 3. Completare le seguenti reazioni del benzene. Scrivere in ogni caso il meccanismo. a) bromuro di terz-butile + AlCl3 CH3 + Cl C CH 3 CH3 AlCl3 C CH3 CH3 CH3 + HCl meccanismo: CH3 CH3 C Cl + AlCl 3 CH3 CH3 CH3 C + + AlCl4CH3 CH3 CH3 CH3 C + CH3 H CH3 C CH3 + CH3 AlCl4- C CH3 CH3 AlCl3 + HCl 1 30/05/2011 b) 1-clorobutano + AlCl3 + Cl CH2 CH2 CH2 CH3 CH3 CH CH2CH3 CH2 CH2 CH2 CH3 + AlCl3 meccanismo: + ......... AlCl4CH3 CH2 CH2 CH2 AlCl3 + Cl CH2 CH2 CH2 CH3 trasposizione + CH3 CH2 CH ......... AlCl4 CH3 + + CH3 CH2 CH2 CH2 + H CH2 CH2 CH2 CH3 AlCl4 CH2 CH2 CH2 CH3 AlCl3 + HCl + + CH3 CH2 CH CH3 CH3 CH CH2CH3 AlCl4- H CH CH2 CH2 + CH 3 AlCl3 + HCl c) bromo + un chiodo (di ferro...non di acciaio!) Br2 + Fe + Br 2 meccanismo: FeBr3 Br + HBr + Br + FeBr4 Br2 + FeBr3 H Br + Br+ FeBr3 FeBr4- + Br FeBr3 + HBr d) acido solforico fumante H H2SO4 + SO3 e) iodio + HNO3 + O- S O O OH S O O Reazione non in programma quest’anno 2 30/05/2011 f) cloruro di benzoile + AlCl3 O O C + AlCl3 Cl C + HCl meccanismo: O C O Cl C+ + AlCl3 + AlCl4- O O O H C+ + + AlCl4- C C AlCl3 + HCl g) acido nitrico + acido solforico + HNO 3 meccanismo: NO2 H2SO4 + H2O + H O NO2 HNO3 + H2SO4 - + HSO4 H + H O NO2 H2O + +NO 2 H catione NITRONIO H3O+ + HSO4= H2O + H2SO4 NO2+ + H3O+ + 2 HSO4= HNO3 + 2 H2SO4 H O + + N O + NO2 NO2 H+ 3 30/05/2011 h) 1-cloro-2,2-dimetilpropano + AlCl3 CH3 CH3 C CH2 CH3 AlCl3 + Cl CH2 C CH3 CH3 CH3 CH3 CH2 C CH3 + CH3 + HCl meccanismo: CH3 -AlCl Cl CH2 C CH3+ AlCl3 4 CH3 + + CH2 C CH3 + CH3 CH2 C CH3 CH3 CH3 CH3 H CH 3 C CH2 CH3 + CH3 + + CH3 CH2 C CH3 CH3 H CH 3 C CH2 CH3 + CH3 -AlCl CH3 C CH2 CH3 4 CH3 + HCl AlCl3 4. Completare le seguenti reazioni dell'isopropilbenzene: a) Br2 alla luce; b) Br2 + FeBr3; c) SO3 in acido solforico; d) cloruro di acetile + AlCl3; e) cloruro di propile + AlCl3. H3C CH3 H3C CH3 CH CH Br SO3, H2SO4 Br2, hν H3C C CH3 + orto Br2, FeBr3 H3C CH CH3 H3C CH + Br H3C CH3COCl, H3C AlCl3 CH3 SO3H CH CH3 AlCl3 Cl CH2 CH2 CH3 Br + orto COCH3 CH CH3 H3C + CH CH3 H3C CH2 CH2 CH3 + CH CH3 H3C CH3 CH + CH3 CH CH3 CH2 CH2 CH3 CH CH3 CH3 4 30/05/2011 5. Completare le seguenti reazioni, catalizzate da AlCl3. Dimostrare in ciascun caso l'orientamento, servendosi degli addotti σ. a) clorocicloesano + benzene a) Cl AlCl3 + + HCl b) cloruro di metile + fenil metil etere O CH3Cl + .. O + H CH3 CH3 O + H3C .. O + O CH3 H CH3 CH3 + CH3+ +O + H CH3 O H H3 C O O CH3 O H CH3 + CH3 O H CH3 + CH3 + O H CH3 CH3 H CH3 CH3 O + H CH3 CH3 O H CH3 CH3 H + H CH3 + CH 3 O CH3 + CH3 O H CH3 CH3 stabile + H CH3 CH3 E+ = CH3+ + O CH3 H3 C stabile O CH3 + CH3 δ+ ........ ... δCH3 Cl AlCl3 CH3 CH3 + H CH3 CH3Cl + AlCl3 O O AlCl3 CH3 CH3 O CH3 + HCl + HCl CH3 5 30/05/2011 c) 3-cloro-2,2-dimetilbutano + isopropilbenzene Cl CH 3 CH3 CH C CH3 CH3 H3C CH CH3 AlCl3 -AlCl 4 H3C CH3 CH3 CH C CH3 + CH3 H3C CH3 CH + H E CH CH3 + CH3 CH C CH3 = E+ CH3 H3C CH3 E H H3C stabile H3C CH CH3 3 CH CH3 CH C CH3 CH3 H3C CH CH3 + + H + CH E E H CH CH3 stabile CH3 CH3 CH CH3 CH3 C CH3 d) 2-cloropropano + nitrobenzene Cl AlCl3 CH3 CH CH3 + + CH3 CH CH3 = E -AlCl 4 NO2 + + CH CH3 CH3 instabile O + ON H CH3 + CH CH3 O + ON O + ON O + ON + H CH H3C CH3 + + H CH H CH H3C CH3 H3C CH3 O + ON instabile CH3 + HCl CH CH3 6 30/05/2011 6. Completare le seguenti reazioni di sostituzione elettrofila aromatica: a) N,N-dimetilanilina + cloruro di acetile e cloruro di alluminio H3C CH3 N H3C CH3 H3C CH3 N N CH3COCl COCH3 + AlCl3 COCH3 b) clorobenzene + bromo e bromuro ferrico Cl Cl Cl FeBr3 Br + + Br2 + HBr Br c) propanoato di fenile e acido nitrico + acido solforico O O O O O CH2CH3 NO2 + O CH2CH3 HNO3 H2SO4 CH2CH3 NO2 d) isopropilbenzene + acido solforico ed anidride solforica SO3 SO3H + H2SO4 SO3H e) nitrobenzene + acido nitrico ed acido solforico NO2 NO2 HNO3 H2SO4 NO2 f) bifenile + anidride acetica e cloruro di alluminio COCH3 AlCl3 + (CH3CO)2O CH3CO2H COCH3 + 7 30/05/2011 7. Completare le seguenti reazioni, specificando i nomi dei composti organici che si formano: a) metilbenzene + cloruro di isobutile + AlCl3 CH3 CH3 CH3 Cl AlCl 3 + + + CH3 CH3 + o-isobutilmetilbenzene + CH2 trasposizione H3C CH CH3 H3 C poco CH3 C CH3 + p-terz-butilmetilbenzene p-isobutilmetilbenzene o-terz-butilmetilbenzene b) benzene + 1-cloro-2-butene e cloruro di alluminio Cl + CH CH 2 CH CH3 CH2 CH AlCl3 CH CH3 + 1-fenil-2-butene Cl CH2 CH CH CH CH3 CH2 -AlCl CH CH3 + AlCl3 4 + 3-fenil-1-butene + CH2 CH CH2 CH CH3 + CH CH CH3 c) benzene + cloruro di butanoile e cloruro di alluminio O + CH3CH2CH2COCl C AlCl3 1-fenil-1-butanone d) benzene + anidride acetica + cloruro di alluminio O O O O AlCl3 + CH3CO2H O C H3C O O C + AlCl3 CH3 + CH3 C O + (CH3CO2)AlCl3 feniletanone acetofenone fenil metil chetone 8 30/05/2011 8. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) isopropilbenzene + permanganato di potassio (KMnO4), a caldo CH3 H3C CH CO2 KMnO4, Δ CO2H H+ 2 CO2 acido benzencarbossilico b) vinilbenzene + acido cloridrico CH Cl CH CH3 CH2 c) metilbenzene + cloro, alla luce ultravioletta 1-cloro-1-feniletano CH3 CH2 Cl Cl2, hν cloruro di benzile d) etilbenzene + cloro e cloruro ferrico CH2 CH3 CH2 CH3 CH2 CH3 Cl Cl2 + FeCl3 Cl o-cloroetilbenzene e) etilbenzene +bromo, a caldo p-cloroetilbenzene Br CH2 CH3 Br2 CH CH3 Δ 1-bromo-1-feniletano f) vinilbenzene + permanganato di potassio, a caldo CH CH2 KMnO4, Δ CO2 CO2 H+ CO2H acido benzencarbossilico 9 30/05/2011 g) metilbenzene + 1-cloropropano e cloruro di alluminio CH3 CH3 CH2 CH2 CH3 Cl CH3 CH2 CH2 CH3 + + CH3 CH3 CH CH3 CH3 + AlCl3 CH CH2 CH2 CH3 CH3 o-isopropilmetilbenzene o-metilpropilbenzene CH3 p-metilpropilbenzene p-isopropilmetilbenzene h) vinilbenzene + H2 (un equivalente) e Pt CH2 CH3 CH CH2 H2 Pt etilbenzene i) vinilbenzene e bromo CH CH2 Br2 Br CH CH2 Br 1,2-dibromo-1-fenilbenzene j) 1,4-diidrossi-2-metossibenzene + ossido di argento OH OCH3 OH O OCH3 Ag2O O 2-metossi-1,4-benzochinone k) benzene + sodio in ammoniaca ed etanolo H H Na in NH3 CH3CH2OH H H 1,4-cicloesadiene 10 30/05/2011 l) vinilbenzene + H2 (in eccesso) e Pt CH CH2 CH2 CH3 H2 (eccesso) Pt etilcicloesano 9. Scrivere l'equazione chimica delle seguenti reazioni: a) benzene + ossigeno e pentossido di vanadio (V2O5), ad elevata temperatura O O2 O V 2O 5 Δ O b) antracene + anidride cromica (CrO3) ed acido solforico O CrO3 H2SO4 O O OH c) p-benzendiolo + ossido di argento (Ag2O) Ag2O O OH d) propilbenzene + permanganato di potassio, a caldo. CH2 CH2 CH3 - CO2 CO2H H+ KMnO4 + 2 CO2 10. Scrivere i prodotti delle seguenti reazioni del cloruro di p-metilbenzen diazonio con: a) KI + N N I b) CuCN + N N C N KI CuCN ClCH3 Cl- CH3 CH3 CH3 11 30/05/2011 c) KOH + N OH N KOH Cl- d) H2O, a caldo + N H2O ClΔ CH3 CH3 OH N CH3 CH3 + N e) CuBr N Br CuBr Cl- + N f) NaNO2, Cu NO2 N CH3 CH3 NaNO2, Cu Cl- CH3 CH3 g) NaBF4 e poi aumentando la temperatura. + N + N N Cl- F N NaBF4 Δ BF4- CH3 CH3 CH3 11. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. Cl Cl2 + FeCl3 + + FeCl4 H + Cl + Cl + H + Cl Cl + FeCl4 - + HCl + FeCl3 12. Il p-dimetilbenzene si nitra molto più facilmente del benzene. Spiegare. H H3 C CH3 H3 C + NO2 CH3 + tutte le posizioni sono identiche; l'addotto σ è stabilizzato dalla presenza del metile in orto H NO2 12 30/05/2011 13. Scrivere il meccanismo della bromurazione aromatica di:a) anilina; b) etossibenzene.Dimostrare l'orientamento, servendosi degli addotti σ. a) anilina (= benzenammina) + Br + FeBr4 Br2 + FeBr3 NH2 NH2 + + Br H Br + Br + NH2 + NH2 Br NH2 + + NH2 NH2 H Br NH2 NH2 FeBr4 H Br + Br NH2 H Br H Br + + H FeBr4 Br FeBr3 HBr + H Br NH2 + NH2 + H Br NH2 H Br +NH2 NH2 + H NH2 NH2 H + H Br H Br FeBr3 HBr H Br Br b) etossibenzene OCH2CH3 H OCH2CH3 + Br Br + + FeBr4 OCH2CH3 H + Br OCH2CH3 OCH2CH3 H H Br Br + + + OCH2CH3 H Br FeBr3 HBr OCH2CH3 Br H Br H Br OCH2CH3 + + + OCH2CH3 OCH2CH3 OCH2CH3 H Br +OCH2CH3 + H Br OCH2CH3 OCH2CH3 OCH2CH3 + + + H Br H Br OCH2CH3 H Br FeBr4 + H Br H Br FeBr3 HBr OCH2CH3 Br 13 30/05/2011 14. Spiegare perché il metilbenzene è orto+para orientante, mentre il triclorometilbenzene è meta orientante. CH3 CH3 + CH3 H CH3 + E H + stabili E E H CCl3 CCl3 + CCl3 H CCl3 + E H + instabili E E H 15. Scrivere le reazioni di bromurazione, solfonazione e nitrazione dei seguenti composti, scrivendo in ciascun caso il prodotto (o i prodotti) di reazione ed indicando se la reazione avviene più velocemente o più lentamente della corrispondente reazione del benzene: -FeBr Bromurazione: Br2 + FeBr3 SO3 E+ Nitrazione: HO NO2 + H2SO4 Solfonazione: H+ O NO2 H a) metossibenzene O CH3 O + + Br+ Br+ 4 + CH3 H + O CH3 H Br Br O + E+ OH2 + CH3 H O +NO 2 E+ CH3 H O CH3 Br + Br Br stabile CH3 O + H Br CH3 O O + CH3 O H + Br CH3 + CH3 O O + Br H Br CH3 O O CH3 + + H CH3 H Br stabileH Br H Br Br 14 30/05/2011 O CH3 CH3 H O SO3 SO3 + + SO 3 + O CH3 H CH3 H O O CH3 O SO3H + SO3 SO3 + CH3 H stabile CH3 O + O + H SO3 CH3 O O CH3 O H SO-3 + CH3 CH3 H SO-3 +O CH3 + H H SO3 3 O CH3 + + SO - CH3 O H SO3 H SO3 SO3H stabile Orientamento: orto + para O CH3 + CH3 H O + NO2+ + O CH3 H O NO2 NO2 CH3 H O CH3 SO3H stabile CH3 O + H O CH3 O CH3 O H + + O CH3 +O CH3 + NO2 H O CH3 O CH3 + + H CH3 NO2 NO2 NO2 H NO2 H NO2 H NO2 stabile Reattività: O + NO2 NO2 + CH3 H +R,-I, con |+R|>|-I| NO2 rilascio elettronico più reattivo di benzene Andrebbe fatto così per tutti I composti seguenti 15 30/05/2011 b) difluorometilbenzene c) etilbenzene CH2 CH3 Orientamento: orto + para rilascio (+I) più reattivo CHF2 Orientamento: meta attrazione (-I) meno reattivo d) clorobenzene Cl e) nitrobenzene NO2 Orientamento: orto + para attrazione (-I > +R) meno reattivo g) benzoato di etile f) acido benzensolfonico SO3H O Orientamento: meta attrazione (-I) meno reattivo i) bifenile C OCH2CH3 Orientamento: meta attrazione (-I) meno reattivo O h) difenil etere Orientamento: orto + para rilascio (+R > -I) più reattivo Orientamento: orto + para rilascio (+R > -I) più reattivo j) terz-butilbenzene k) fluorobenzene F CH3 H3C C CH3 Orientamento: meta attrazione (-I) meno reattivo Orientamento: orto + para attrazione (-I > +R) meno reattivo Orientamento: orto + para rilascio (+I) più reattivo m) acetato di fenile l) metilbenzene O CH3 Orientamento: orto + para rilascio (+I) più reattivo O C CH3 Orientamento: orto + para rilascio (+I) più reattivo 16 30/05/2011 n) acetilbenzene (= acetofenone, oppure fenil metil chetone oppure 1-feniletanone) O C CH3 Orientamento: meta attrazione (-I) meno reattivo o) benzammide p) benzonitrile O C NH2 Orientamento: meta attrazione (-I) meno reattivo C N Orientamento: meta attrazione (-I) meno reattivo q) iodobenzene I Orientamento: orto + para attrazione (-I > +R) meno reattivo 17. Il nitrobenzene viene trattato con la miscela solfonitrica (HNO3 + H2SO4). a) Scrivere l'equazione chimica della reazione, dando il nome del prodotto. b) Scrivere il meccanismo, giustificando l'orientamento. c) Prevedere l'ordine di reattività dei seguenti composti nella nitrazione aromatica: nitrobenzene, fenolo, benzene, metilbenzene (spiegare). NO2 NO2 HNO3 equazione chimica H2SO4 NO2 meccanismo: HNO3 + H2SO4 -O + O N + +NO2 + H2O NO2 H2O + +NO2 Si scrivono gli addotti possibili (sulla carta), relativi all’attacco in orto, meta e para e le rispettive STRUTTURE di RISONANZA Si esaminano le strutture in cui la carica positiva (portata dall’elettrofilo) finisce sul C con il sostituente (addotti orto e para) 17 30/05/2011 -O -O + O N H orto NO2 + O + O N H + O N H + NO2 + NO2 instabile -O -O + O N + meta + H + NO2 -O + O N + O N H NO2 -O -O + O N -O + O N NO2 H NO2 NO2 + O N + para + + H NO2 H H NO2 NO2 instabile Per la REATTIVITA’ si considera la densità elettronica delle posizioni dove viene orientato l’elettrofilo 4° CH3 OH NO2 1° meta 3° orto+para -I 2° orto+para tutte le posizioni -I < +R +I l'elettrofilo reagisce più facilmente con un C ricco di elettroni 18. a) Scrivere l'equazione chimica della reazione che avviene trattando il bromobenzene con acido nitrico + acido solforico, giustificando l'orientamento. b) Spiegare l'ordine di reattività che si osserva se, nelle condizioni di (a), si fanno reagire: benzene, bromobenzene, metilbenzene. Equazione chimica Br Br Br HNO3 H2SO4 NO2 + NO2 18 30/05/2011 Meccanismo e Orientamento: + H 2O HNO3 + H2SO4 Br Br + +NO2 Br Br H + NO2 + + H H NO2 NO2 Br H2O + +NO2 NO2 Br H Br + NO2 + + Br + H H NO2 NO2 H NO2 + Br Br stabili H NO2 H + + Br Br NO2 H NO2 + orto + para Reattività: tutte le posizioni 3° H NO2 -I > +R CH3 Br 2° stabili 1° orto + para -I > +R orto + para +I 19 30/05/2011 24. Il nitrobenzene viene talvolta usato come solvente nelle alchilazioni di FriedelCrafts. Perché il nitrobenzene non interferisce con la reazione desiderata? NO2 poco reattivo con gli elettrofili 25. a) Scrivere l'equazione chimica della reazione che avviene trattando il metilbenzene con cloruro di propanoile e cloruro di alluminio, giustificando l'orientamento. Spiegare l'ordine di reattività che si osserva se, nelle condizioni di (a) si fanno reagire: mdimetilbenzene, metilbenzene, fluorobenzene, benzene. CH3 + CH3CH2COCl orientamento: CH3 + CH3 AlCl3 COCH2CH3 + HCl CH3 H COCH2CH3 + H COCH2CH3 REATTIVITA' CH3 CH3 > > > CH3 +I +I di due CH3 F > -I > +R 26. Quale composto in ciascuna delle seguenti coppie è più reattivo nella bromurazione aromatica? (spiegare): a) acetanilide o benzene NHCOCH3 > orientamento: orto + para +R > -I : rilascio elettronico b) bromobenzene o metilbenzene CH3 Br > orientamento: orto + para per entrambi i sostituenti CH3: +I : rilascio elettronico; Br: -I > + R: attrazione 20 30/05/2011 c) p-dimetilbenzene o acido p-metilbenzoico CH3 CH3 > CO2H CH3 posizioni equivalenti +I(CH3), -I(CO2H) +I (CH3), +I(CH3) d) m-dinitrobenzene o m-metilnitrobenzene NO2 CH3 < NO2 NO2 in 2,4,6: -I(NO2), -R(NO2)-I(NO2), -R(NO2) in 5: -I(NO2), -I(NO2) in 2,4,6: +I(CH3), -I(NO2), -R(NO2) in 5: +I(CH3), -I(NO2) e) clorobenzene o m-diclorobenzene Cl Cl > nelle posizioni reattive del clorobenzene: -I > + R nelle posizioni reattive del m-dicloro benzene: -I > + R per entrambi i Cl Cl maggiore attrazione elettronica minore reattività f) metilbenzene o fenolo CH3 OH > g) fenolo o clorobenzene orto + para orto + para + R > -I +I OH Cl > orto + para + R > -I orto + para -I > + R 21 30/05/2011 27. Il fenolo viene trattato con una soluzione acquosa di bromo; a) scrivere l’equazione chimica della reazione, giustificando l’orientamento, b) Commentare le condizioni in cui la reazione avviene, confrontandole con quelle necessarie perché la reazione avvenga con il benzene. OH OH Br H2O Br + Br2 Br Il gruppo OH è a forte rilascio elettronico (+R > -I) Basta il solvente polare, mentre per bromurare il benzene serve l’acido di Lewis: fenolo più reattivo di benzene 30. Scrivere i prodotti di mononitrazione dei seguenti composti, giustificando l'orientamento: NO2 a) o-metilnitrobenzene CH3 b) m-clorometilbenzene Posizioni favorite da entrambi i sostituenti Cl Posizioni favorite da entrambi i sostituenti CH3 c) acido o-bromobenzoico CO2H Br Posizioni favorite da entrambi i sostituenti 22 30/05/2011 d) acido p-metossibenzoico CO2H O Posizioni favorite da entrambi i sostituenti CH3 e) m-metilbenzenolo OH Posizioni favorite da entrambi i isostituenti CH3 31. L'isopropilbenzene reagisce con il cloro in due modi diversi, a seconda delle condizioni. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene alla luce ultravioletta. b) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene in presenza di cloruro ferrico. CH3 CH3 Cl2, hν H3C H3 C Cl2 + HCl CH H3 C Cl2 SOSTITUZIONE RADICALICA C Cl CH FeCl3 CH3 H3C . 2 Cl ecc. CH3 CH + Cl hν Cl + HCl Cl2 + FeCl3 SOSTITUZIONE ELETTROFILA AROMATICA Cl+ + -FeCl4 23 30/05/2011 33. L'acido salicilico (= acido o-idrossibenzoico) e l'aldeide salicilica (= oidrossibenzencarbaldeide) si preparano dal fenolo. Scrivere le reazioni corrispondenti e spiegare perché gli stessi reagenti non danno reazione con il benzene. OH O C OO O- CO2 CHCl3 Δ, P -OH O C H elettrofili deboli 34. a) Scrivere l'equazione chimica ed il meccanismo della nitrazione aromatica del naftalene, giustificandone l'orientamento. NO2 equazione: HNO3 H2SO4 meccanismo: HNO3 + H2SO4 H NO2 + NO2+ NO2+ + H3O+ + 2 HSO4H NO2 NO2 H NO2 + + + H + H NO2 + H NO2 + NO2 addotto in β meno stabile: orientamento in α 24 30/05/2011 b) Scrivere l'equazione chimica ed il meccanismo della solfonazione a bassa temperatura del naftalene. Spiegare perché a temperature più elevate si ottiene un isomero diverso. equazione: SO3H SO3 H2SO4 a bassa temperatura H SO3 H SO3 H SO3 meccanismo: + + + SO3 SO3H + a bassa temperatura controllo cinetico a temperatura elevata controllo termodinamico H SO3H -SO3H (voluminoso) in β è più stabile H SO3H H 35. A differenza di benzene e naftalene, il fenantrene addiziona una molecola di bromo. Scrivere la reazione e spiegare perché avviene, servendosi delle strutture di risonanza del fenantrene. Br2 H 9,10-dibromo-9,10-diidrofenantrene Br H Br 25 30/05/2011 36. Per ognuno dei seguenti composti indicare un metodo di preparazione a partire dal benzene: a) acido 3-amminobenzensolfonico ? SO3H NH2 -SO3H orienta in meta -NH2 si introduce per riduzione di -NO2 -NO2 orienta in meta SO3 SO3H HNO3 NO2 H2SO4 SO3H [H] H2SO4 H2SO4 oppure: SO3H HNO3 NO2 NH2 SO3H SO3 SO3H [H] H2SO4 NO2 b) m-diamminobenzene NH2 ? NH2 -NH2 si introduce per riduzione di -NO2 -NO2 orienta in meta NO2 NH2 HNO3 HNO3 H2SO4 H2SO4 NO2 [H] NO2 NH2 NH2 c) p-nitroanilina NH2 ? -NH2 si introduce per riduzione di -NO2 -NO2 orienta in meta NO2 -NH2 orienta in orto + para per avere solo para: -NHCOCH3 HNO3 H2SO4 NO2 NHCOCH3 NH2 [H] (CH3CO)2O HNO3 NHCOCH3 NH2 NO2 NO2 H2O,-OH H2SO4 26 30/05/2011 37. Completare le seguenti reazioni di sostituzione nucleofila aromatica, specificando se avvengono con meccanismo di addizione-eliminazione o di eliminazione-addizione (via benzino); spiegare il perché della scelta. a) p-nitrobromobenzene + KOH Br OH Br OH OH Br addizione-eliminazione KOH NO2 NO2 N O + O- NO2 presenza di -NO2 b) m-cloronitrobenzene + KOH OH Cl OH + KOH NO2 + + OH NO2 NO2 NO2 NO2 NO2 eliminazione-addizione -NO2 non è in posizione tale da ospitare la carica negativa c) p-diclorobenzene + KOH (in eccesso) Cl OH HO KOH + Cl Cl eliminazione-addizione non c'è un sostituente in grado di stabilizzare l'addotto anionico Cl Cl OH OH KOH OH + + eliminazione-addizione non c'è un sostituente in grado di stabilizzare l'addotto anionico (eccesso) OH OH + + OH OH OH OH d) 2,4,6-trinitroclorobenzene + KOH Cl OH NO2 O2 N NO2 NO2 KOH O2N NO2 addizione-eliminazione Tutti e tre i gruppo -NO2 sono in grado di stabilizzare la carica negativa dell'anione 27 30/05/2011 Cl OH NO2 O 2N O2N Cl OH NO2 ecc. N O + O- NO2 e) 4-nitroclorobenzene + KOH Cl OH KOH addizione-eliminazione NO2 -NO2 in grado di stabilizzare la carica negativa dell'anione Cl OH Cl OH NO2 NO2 f) m-clorometilbenzene + KOH Cl KOH OH OH + CH3 eliminazione-addizione + OH CH3 CH3 N O + O- CH3 non c'è un sostituente in grado di stabilizzare l'addotto anionico + CH3 CH3 g) p-clorometilbenzene + KOH Cl OH OH KOH eliminazione-addizione + CH3 CH3 CH3 non c'è un sostituente in grado di stabilizzare l'addotto anionico CH3 38. Scrivere equazione chimica e meccanismo delle seguenti reazioni: a) 2,4-dinitroclorobenzene + sodioammide Cl NO2 Na+ -NH2 NO2 Cl NH2 Cl NH2 NO2 NO2 NO2 NH2 NO2 Cl NH2 NO2 N O + O Cl NH2 NO2 NO2 Cl NH2 O N+ O NO2 NO2 NO2 28 30/05/2011 b) 1,2-dicloro-3,5-dinitrobenzene + metossido di sodio (un equivalente) in metanolo Cl Cl Cl CH O-Na+ OCH 3 addizione-eliminazione 3 NO2 O2 N NO2 O 2N c) 1,2-dicloro-3,5-dinitrobenzene + metossido di sodio (due equivalenti) in metanolo; Cl CH3O-Na+ OCH3 NO2 O2 N OCH3 OCH3 Cl Cl CH O-Na+ 3 NO2 O2 N NO2 O2N d) 4-clorometilbenzene + KOH ad elevata temperatura HO H H OH Cl KOH OH OH + Δ eliminazione-addizione CH3 CH3 CH3 CH3 e) 3-bromometilbenzene + dietilammide di litio [= (CH3CH2)2N- Li+] in NR2 dietilammina. H H Cl (CH CH ) N- Li+ 3 22 H H CH3 NR2 H + NR2 CH3 N(CH2CH3)2 CH3 N(CH2CH3)2 + + CH3 NRH2 N(CH2CH3)2 CH3 CH3 40. Il 2,4,6-trinitroclorobenzene reagisce con NaOH in acqua. a) Scrivere equazione chimica e meccanismo della reazione. b) Il nome corrente del prodotto è "acido picrico", pur trattandosi di un fenolo. Come mai? Cl O2 N NO2 NaOH O2N H2O NO2 Cl OH NO2 - NO2 OH O2 N NO2 NO2 è molto acido, per la presenza dei tre gruppi nitro (-I, -R) 29 30/05/2011 41. Il m-clorometilbenzene reagisce con sodioammide in ammoniaca liquida, dando tre prodotti isomeri. Scrivere l'equazione chimica della reazione e spiegare la formazione dei tre isomeri, sulla base del meccanismo. H NH2 Cl NH2 NaNH2 + + + H NH2 CH3 CH3 CH3 CH3 CH3 CH 3 44. Il defoliante Agent Orange, usato nella guerra del Vietnam (e che è ritenuto responsabile della malattia e della morte di molti reduci, anche a distanza di anni), contiene l'acido (2,4,5-triclorofenossi)etanoico, indicato come 2,4,5-T. Questo acido si prepara per reazione parziale dell'1,2,4,5-tetraclorobenzene con NaOH, seguita da reazione con cloroacetato di sodio. a) Scrivere la reazione di sintesi del 2,4,5-T. b) Una delle impurezze contenute nell' Agent Orange (probabilmente il principale componente tossico) era la 2,3,7,8-tetraclorodibenzodiossina, 2,3,7,8-TCDD, spesso chiamata, impropriamente, diossina. Indicare come 2,3,7,8-TCDD si forma nel corso della sintesi di 2,4,5-T. c) Come si può eliminare la contaminazione da TCDD sia dopo il primo passaggio che alla fine della sintesi? Cl Cl O CH2CO2H Cl Cl Cl Cl Cl 2,4,5-T O Cl Cl NaOH Cl OH Cl - Cl CH2 C O Cl Cl Cl Cl Cl Cl Cl O CH2CO2 Cl Cl H+ Cl O CH2CO2H Cl Cl - O 2,4,5-T b) la 2,3,7,8-tetraclorodibenzodiossina viene dalla sostituzione nucleofila tra due molecole di fenossido Cl O Cl Cl Cl O Cl Cl Cl -O Cl Cl O Cl 2,3,7,8-TCDD c) 2,3,7,8-TCDD non è solubile in acqua L’estrazione con una soluzione acquosa moderatamente basica (bicarbonato) purifica il 2,4,5-T 30
Scarica